文档内容
第 28 讲 物质的分离、提纯和检验
第一部分:高考真题感悟
1.(2022·海南·高考真题)《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去
石澄清,慢火熬干,”其中未涉及的操作是
A.洗涤 B.粉碎 C.萃取 D.蒸发
【答案】C
【解析】水洗净是指洗去固体表面的可溶性污渍、泥沙等,涉及的操作方法是洗涤;细研水飞是指将固体
研成粉末后加水溶解,涉及的操作方法是溶解;去石澄清是指倾倒出澄清液,去除未溶解的固体,涉及的
操作方法是倾倒;慢火熬干是指用小火将溶液蒸发至有少量水剩余,涉及的操作方法是蒸发;因此未涉及
的操作方法是萃取,答案选C。
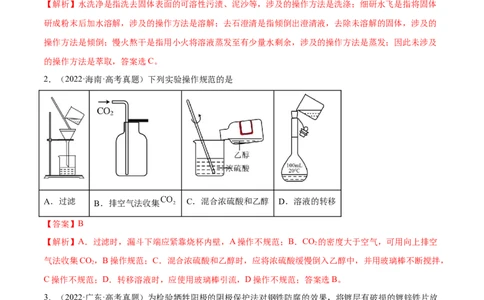
2.(2022·海南·高考真题)下列实验操作规范的是
A.过滤 B.排空气法收集 C.混合浓硫酸和乙醇 D.溶液的转移
【答案】B
【解析】A.过滤时,漏斗下端应紧靠烧杯内壁,A操作不规范;B.CO 的密度大于空气,可用向上排空
2
气法收集CO,B操作规范;C.混合浓硫酸和乙醇时,应将浓硫酸缓慢倒入乙醇中,并用玻璃棒不断搅拌,
2
C操作不规范;D.转移溶液时,应使用玻璃棒引流,D操作不规范;答案选B。
3.(2022·广东·高考真题)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放
入酸化的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是
A.加入 溶液产生沉淀
B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现
D.加入 溶液无蓝色沉淀生成【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于锌比
铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶液反
应产生氢气,溶液中会有亚铁离子生成。A.氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液后,不
管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;B.淀粉碘化钾溶液可检测氧化性物质,但不
论铁片是否被腐蚀,均无氧化性物质与碘化钾发生反应,故B不符合题意;C.KSCN溶液可检测铁离子
的存在,上述现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红色出现,故
C不符合题意;D.K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离子,
3 6
则加入K[Fe(CN) ]溶液就不会出现蓝色沉淀,故D符合题意。综上所述,答案为D。
3 6
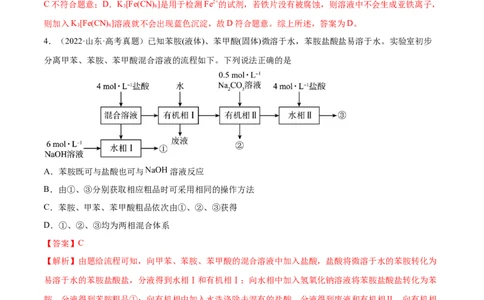
4.(2022·山东·高考真题)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步
分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
【答案】C
【解析】由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为
易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转化为苯
胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有机相
Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向
水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲酸粗品③。A.苯
胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,故A错误;B.由分析可知,得到苯胺
粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过滤、洗涤,获取两者的操作
方法不同,故B错误;C.由分析可知,苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,故C
正确;D.由分析可知,①、②为液相,③为固相,都不是两相混合体系,故D错误;故选C。5.(2020·浙江·高考真题)某固体混合物X,含有Al (SO )、FeCl 、NaCO 和CuSO 中的几种,进行如
2 4 3 3 2 3 4
下实验:
①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;②沉淀Y与NaOH溶液作用,无变化。
下列说法不正确的是
A.混合物X中必定含有NaCO,不含Al (SO )
2 3 2 4 3
B.溶液Z中溶质主要是钠盐,且必含NaHCO
3
C.灼烧沉淀Y,可能得到黑色物质
D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl
3
【答案】D
【解析】由固体混合物X与水作用有气泡冒出可知,X中一定含有NaCO,由得到有色沉淀Y和弱碱性
2 3
溶液Z,沉淀Y与NaOH溶液作用无变化可知,X中一定不含有Al (SO ),至少还有FeCl 和CuSO 中的一
2 4 3 3 4
种或两种,NaCO 在溶液中发生双水解反应生成二氧化碳和碳酸氢钠。A.由分析可知,混合物X中必定
2 3
含有NaCO,不含Al (SO ),A正确;B.由分析可知,NaCO 在溶液中发生双水解反应生成二氧化碳和
2 3 2 4 3 2 3
碳酸氢钠,则溶液Z中溶质主要是钠盐,且必含NaHCO ,B正确;C.沉淀Y可能为氢氧化铜,则灼烧氢
3
氧化铜可以得到黑色氧化铜固体,C正确;D.由分析可知,溶液Z中存在碳酸氢钠溶液,说明铁离子和
铜离子与碳酸钠溶液完全反应,往溶液Z中加入Cu粉,铜粉一定不溶解,则依据铜粉不溶解无法判断X
中是否含有氯化铁,D错误;故答案为:D。
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(共12*5分)
1.(2022·上海杨浦·一模)只用水不能鉴别
A.苯和 B. 晶体和 晶体
C. 和硫粉 D.乙酸乙酯和乙酸丁酯
【答案】D
【解析】A.苯和 都难溶于水,且苯的密度小于水、四氯化碳密度大于水,用水可以鉴别,A不符合
题意;B. 晶体易溶于水形成紫红色溶液, 晶体在水中溶解度较小形成黄色溶液,用水可以鉴别,B不符合题意;C. 和水反应生成氧气逸出有气泡生成,硫粉和水无明显变化,用水可以鉴别,C不
符合题意;D.乙酸乙酯和乙酸丁酯均不溶于水且密度小于水,用水不可以鉴别,D符合题意;故选D。
2.(2022·上海长宁·二模)下列实验用酸性 溶液不能达到预期目的的是
A.鉴别乙烯和乙烷 B.鉴别四氯乙烯和聚四氟乙烯
C.鉴别苯和对二甲苯 D.检验 中含碳碳双键
【答案】D
【解析】A.乙烯中含碳碳双键,能使高锰酸钾溶液褪色;乙烷不含不饱和键,不能使高锰酸钾溶液褪色,
可以鉴别,A错误;B.四氯乙烯含碳碳双键,能使高锰酸钾溶液褪色;聚四氟乙烯不含不饱和键,不能
使高锰酸钾溶液褪色,可以鉴别, B错误;C.苯不能使高锰酸钾溶液褪色;对二甲苯中与苯环直接相连
的甲基上有氢原子,能使高锰酸钾溶液褪色,可以鉴别, C错误;D. 所含的碳碳双键
和醛基均能使高锰酸钾溶液褪色,不能鉴别,D正确;故选D。
3.(2022·山东师范大学附中模拟预测)实验室进行海带提碘实验,萃取后继续分离得到单质碘的主要操
作:用浓氢氧化钠溶液进行反萃取、分液、酸化、过滤及干燥等。下列对应各实验步骤的装置错误的是
A. B. C. D.
【答案】D
【解析】A.用浓氢氧化钠溶液进行反萃取,需要振荡, 是振荡操作,故A正确;B.振荡后需静止后再分液, 是分液操作,故B正确;C.酸化后过滤, 是过滤操作,故C正确;D.
操作中没有蒸发过程, 是蒸发操作,故D错误。综上所述,答案为D。
4.(2022·河南焦作·一模)对下列物质(括号内为杂质)进行检验的方法中,能实现相应目的的是
物质(杂质) 方法
A SO (C H) 通过酸性高锰酸钾溶液后,再通过品红溶液
2 2 4
B NO( NO ) 通过水,再与空气混合
2
C 溶液中的Cl-( ) 滴加过量硝酸银溶液
D 溶液中的 ( ) 滴加过量盐酸,再滴加氯化钡溶液
【答案】D
【解析】A.SO 、C H 均能被酸性高锰酸钾溶液氧化,不能达到实验目的,故A不符合题意;B.NO 能
2 2 4 2
与水反应3NO +H O=2HNO +NO,NO与空气中氧气生成二氧化氮,无法判断原有气体中是否有NO,故B
2 2 3
不符合题意;C.Cl-、SO 均与Ag+产生白色沉淀,故C不符合题意;D.先加入稀盐酸,除去SO 干扰,
再加入氯化钡溶液,有白色沉淀生成,则说明有SO ,反之则没有,故D符合题意;答案为D。
5.(2022·浙江·温州中学模拟预测)下列说法不正确的是
A.鉴别工业盐和食盐:一定条件下,用稀硫酸或酸性 溶液即可鉴别
B.选择分离、提纯方法:结晶、蒸馏、渗析分别适用的是固体、液体、胶体样品的分离
C.电子天平使用:将刚洗净的小烧杯放在秤盘中,按归零键,缓加样品至所需质量,读数
D.提纯阿司匹林:粗品加饱和 溶液、过滤、洗涤,滤液加盐酸、经冰水浴冷却结晶、抽滤、洗涤、干燥得到纯品
【答案】C
【解析】A.工业盐中有亚硝酸钠存在,亚硝酸钠可在酸性条件下可以发生反应产生红棕色气体,可以稀
硫酸或者酸性氯化亚铁溶液鉴别,A项正确;B.结晶是溶液通过降温结晶或者蒸发结晶得到固体物质,
蒸馏是根据沸点分离液体物质,渗析是指胶体和溶液只有溶液可以透过半透膜,通过半透膜可提纯胶体,
B项正确;C.天子天平使用时应用干燥洁净的小烧杯,放在秤盘中,按归零键,缓加样品至所需质量,
读数,C项错误;D.阿司匹林为乙酰水杨酸,结构简式为 ,官能团为酯基和羧基,能
与NaHCO 反应的为羧基,反应生成乙酰基水杨酸钠,易溶于水,在盐酸酸性条件下水解为乙烯基水杨酸,
3
经冰水浴冷却结晶、抽滤、洗涤、干燥得到纯品,D项正确;答案选C。
6.(2022·上海上海·二模)除去下列物质中的杂质(括号内为杂质),可采用加入过量NaOH溶液充分反应
后,再用过滤方法分离的是
A.AlCl 溶液(FeCl ) B.NaCO 溶液(NaHCO )
3 3 2 3 3
C.Fe O 固体(AlO) D.NaCl溶液(MgCl )
2 3 2 3 2
【答案】C
【解析】A.AlCl 溶液(FeCl ),加入过量NaOH溶液充分反应后,AlCl 转化为NaAlO ,杂质FeCl 转化
3 3 3 2 3
为Fe(OH) 沉淀,再用过滤方法分离得不到AlCl ,A错误;B.NaCO 溶液(NaHCO ) ,加入过量NaOH
3 3 2 3 3
溶液充分反应后,NaHCO 转化为NaCO,但过量NaOH依然为杂质,没有除尽,B错误;C. Fe O 固
3 2 3 2 3
体(AlO),Al O 与过量NaOH溶液反应生成可溶性NaAlO ,Fe O 不与NaOH反应,再经过滤可得到纯净
2 3 2 3 2 2 3
的Fe O 固体,C正确;D.NaCl溶液(MgCl ),加入过量NaOH溶液,引入新杂质NaOH,D错误;故选
2 3 2
C。
7.(2022·四川乐山·一模)为提纯下列物质(括号内为杂质),所选用的试剂和除杂方法都正确的是
选项 被提纯物质 除杂试剂 操作
A 乙烯(甲烷) 溴水 洗气
B 溴苯(溴) CCl 萃取
4
C 乙醇(乙酸) 金属钠 蒸馏
D 淀粉溶液(葡萄糖) —— 渗析
【答案】D【解析】A.乙烯与溴水发生加成反应,甲烷与溴水不反应,故用溴水不能除去乙烯中混有的甲烷,A错
误;B.溴苯和溴与CCl 互溶,三者不能分离,B错误;C.乙醇和乙酸均能与金属钠反应,不能用金属钠
4
除去乙醇中的乙酸,C错误;D.淀粉溶液为胶体,不能通过半透膜,葡萄糖溶液能通过半透膜,故可以
通过渗析除去淀粉溶液中的葡萄糖,D正确;故选D。
8.(2022·北京·人大附中三模)根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 实验结论
取久置的 粉末,向其中滴加过量盐酸,产
A 未完全变质
生无色气体
向久置的 溶液中加入足量 溶液,出
B 部分 被氧化
现白色沉淀;再加入足量稀盐酸,部分沉淀溶解
C
向20%蔗糖溶液中加入少量稀 ,加热;再
蔗糖未水解
加入银氨溶液,未出现银镜
D 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 溶液中含
【答案】B
【解析】A.久置的 粉末,在空气中会转化为NaCO ,再加入过量的盐酸,会产生无色气体CO,
3 2
不能确定是否剩余,所以A项错误;B. 溶液中加入足量 溶液,会产生亚硫酸钡白色沉淀,
再加入足量稀盐酸能够全部溶解,而已知实验现象为部分溶解,所以白色沉淀中还有硫酸钡,证明
部分氧化,B正确;C.向20%蔗糖溶液中加入少量稀 ,蔗糖水解生成葡萄糖和果糖,由于硫酸作
为催化剂,体系依然为酸性,再加入的强碱性的银氨溶液会优先于硫酸反应,也可能看不到银镜,所以C
项错误;D.向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色,证明黄色溶液含氧化性的物质,将I-氧化成
I,也可以是Fe3+,D项错误;答案选B。
2
9.(2022·浙江·模拟预测)下列方案设计、现象和结论有正确的是
目的 方案设计 现象和结论
A 鉴定 与溴蒸气 两气体分别通入淀粉KI溶液中 变蓝色的是通入溴蒸气
检验固体混合物是 将固体溶于水,加入足量浓NaOH溶液,加 若试纸不变蓝,说明固体中不
B
否存在铵盐 热,用红色湿润石蕊试纸检验产生的气体 存在铵盐若溶液出现淡黄色沉淀,则说
检验 的氧化
C 在 溶液中加入 溶液
性 明 具有氧化性
检验火柴头中的氯 取用火柴头浸泡过的溶液,加 溶液、稀 若出现白色沉淀,说明有氯元
D
元素 素
硝酸和 溶液
【答案】D
【解析】A. 与溴蒸气均能把碘离子氧化为碘单质,故分别通入淀粉KI溶液中,均能变蓝,A错误;
B.铵根与亚硝酸根离子能在水溶液中发生归中反应产生氮气。则:将固体混合物溶于水,加入足量浓
NaOH溶液,加热,用红色湿润石蕊试纸检验产生的气体,若试纸不变蓝,不能说明固体中不存在铵盐,
B错误;C.在 溶液中加入 溶液不发生反应,在酸性条件下,氢离子、亚硫酸根离子和硫离子
发生反应生成硫和水,溶液出现淡黄色沉淀, C错误;D.氯酸钾、硝酸银和亚硝酸钠反应生成氯化银白
色沉淀,则:取用火柴头浸泡过的溶液,加 溶液、稀硝酸和 溶液,若出现白色沉淀,说明
有氯元素, D正确;答案选D。
10.(2021·山东·济南外国语学校模拟预测)下列说法不正确的是
A.可用新制的 Cu(OH) 检验牙膏中甘油的存在
2
B.可用 AgNO 溶液和稀硝酸鉴别 NaCl 和 NaNO
3 2
C.食醋总酸含量测定的滴定实验中,用酚酞作指示剂
D.用纸层析法分离 Fe3+和 Cu2+,将滤纸上的试样点完全浸入展开剂
【答案】D
【解析】A.甘油为丙三醇,多羟基的醇和新制Cu(OH) 作用得到绛蓝色溶液,所以可用新制的 Cu(OH)
2 2
检验牙膏中甘油的存在,A正确;B.AgNO 溶液和稀硝酸可以和NaCl生成白色难溶于稀硝酸的沉淀,
3
可以鉴别NaCl 和 NaNO ,B正确;C.用已知浓度的氢氧化钠溶液测定食醋总酸含量,滴定终点产物为
2
醋酸钠,溶液呈碱性,可以用酚酞作指示剂,C正确;D.纸上层析法是利用试样中各种离子随展开剂在
滤纸上展开的速率不同而形成不同位置的色斑,如果试样接触展开剂,样点里要分离的离子或者色素就会
进入展开剂,导致实验失败,D错误;答案为:D。
11.(2021·浙江·模拟预测)固体M由Fe (SO )、Fe、KBr、KSO 、AgNO 和BaCl 中的几种或全部物质
2 4 3 2 3 3 2
组成。①取少量M加足量稀HSO 产生气体X、溶液Y和白色固体Z。向溶液Y中加少量稀AgNO 溶液,
2 4 3
产生白色沉淀(Ag SO 是微溶物,浓度较小时不会沉淀);②另取少量Y,加入足量NaOH溶液产生白色沉
2 4
淀,一段时间后颜色变深。下列说法正确的是A.气体X一定是SO 或H
2 2
B.M中一定含有Fe (SO )
2 4 3
C.M中一定不含KBr,一定有BaCl
2
D.Z一定是BaSO
4
【答案】C
【解析】溶液Y中加入少量AgNO 生成白色沉淀,则该沉淀为AgCl,则原固体M中一定含有BaCl ,一
3 2
定不含KBr;溶液Y中加入NaOH溶液,产生白色沉淀,且一段时间后颜色变深,则溶液Y中一定含有
Fe2+,不含Fe3+,原固体M中可能含有Fe,与稀硫酸反应生成Fe2+和H,也可能含有Fe (SO ),被亚硫酸
2 2 4 3
根还原为Fe2+;原固体中可能含有AgNO,酸性条件下的硝酸根具有氧化性,被Fe或亚硫酸根全部还原成
3
NO,银离子则转化成氯化银沉淀,部分可能会转化成硫酸银沉淀。综上可知固体M中一定有BaCl ,Fe
2
和Fe (SO ) 二者至少含有一种,可能有AgNO 和KSO ,一定没有KBr;气体X可能是H,可能是SO ,
2 4 3 3 2 3 2 2
可能是H 和SO 混合,可能是H 和NO混合,可能是SO 和NO混合,可能是H、SO 和NO混合;白色
2 2 2 2 2 2
固体Z可能是BaSO,可能是BaSO 和AgCl,还可能是BaSO、AgCl和Ag SO 。
4 4 4 2 4
A.气体X可能是H,可能是SO ,可能是H 和SO 混合,可能是H 和NO混合,可能是SO 和NO混合,
2 2 2 2 2 2
可能是H、SO 和NO混合,A错误;B.M中一定有Fe和Fe (SO ) 二者至少含有一种,B错误;C.根据
2 2 2 4 3
分析M中一定有BaCl ,一定没有KBr,C正确;D.白色固体Z可能是BaSO,可能是BaSO 和AgCl,
2 4 4
还可能是BaSO、AgCl和Ag SO ,D错误。故选C。
4 2 4
12.(2022·四川眉山·三模)某固体X可能含有 、Fe3+、Na+、Cl-、 、 中的几种离子,将固
体X均分为两份,进行如下实验:
(1)一份固体溶于水得透明溶液,加入足量BaCl 溶液,得白色沉淀6. 63 g,在沉淀中加入过量稀盐酸,仍
2
有4. 66g白色沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0. 672 L(标准
状况)。
下列说法正确的是
A.该固体中一定含有 、 、 、Na+
B.固体X中Na+物质的量至少为0.03mol
C.该固体中一定没有Fe3+和Cl-
D.该固体中只含有 、 、
【答案】AB【解析】根据实验(1)得白色沉淀,加入过量盐酸部分溶解可知,X一定含有 、 ,n(
)=n(BaSO )= ,n( )=n(BaCO )= , 与Fe3+发生双水解反
4 3
应不能大量共存,故一定没有Fe3+;根据实验(2)可知,X一定含有 ,n( )=n(NH )=
3
;根据电荷守恒,X中一定还有Na+,不确定Cl-是否存在,故n(Na+) 0.03mol
(0.02mol×2+0.01mol×2 - 0.03mol=0.03mol);A.根据上述分析,该固体中一定含有 、 、 、
Na+,A项正确;B.X中Na+物质的量至少为0.03mol,B项正确;C.该固体中一定没有Fe3+,可能含有
Cl-,C项错误;D.根据上述分析,该固体中除含有 、 、 ,还含有Na+,D项错误;答案选
AB。
二、主观题(共3小题,共40分)
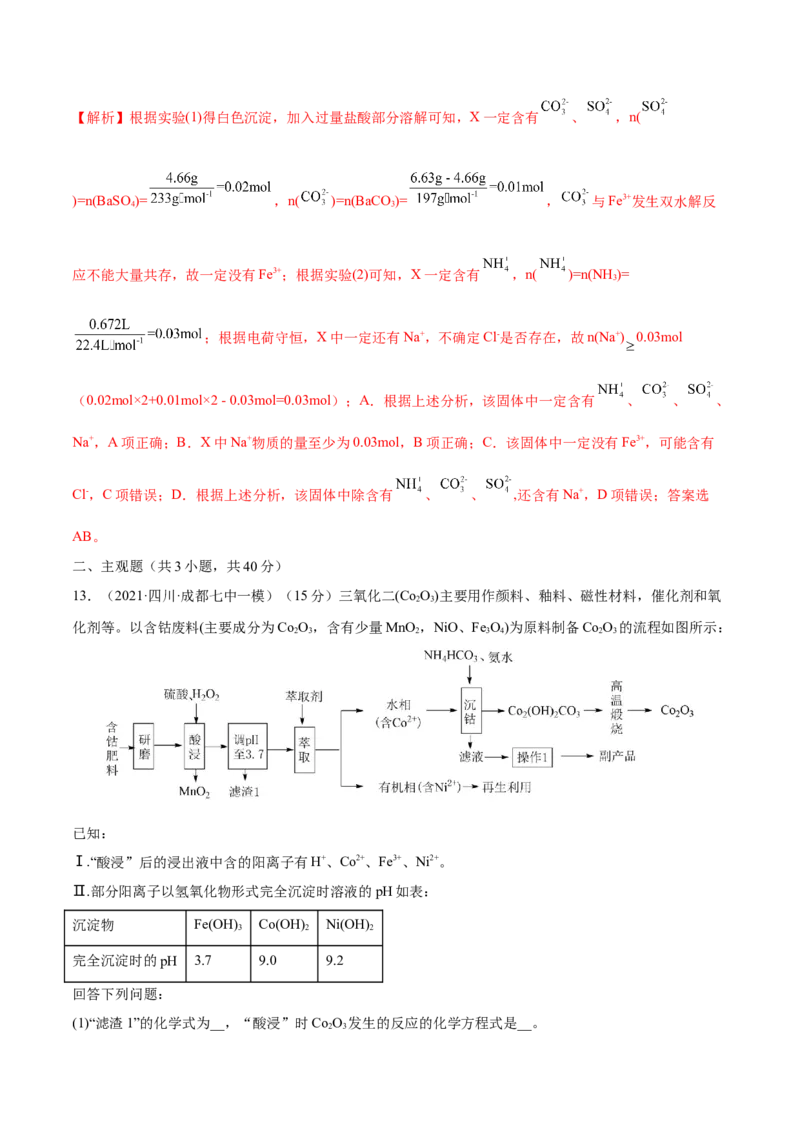
13.(2021·四川·成都七中一模)(15分)三氧化二(Co O)主要用作颜料、釉料、磁性材料,催化剂和氧
2 3
化剂等。以含钴废料(主要成分为Co O,含有少量MnO ,NiO、Fe O)为原料制备Co O 的流程如图所示:
2 3 2 3 4 2 3
已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+。
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表:
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2
完全沉淀时的pH 3.7 9.0 9.2
回答下列问题:
(1)“滤渣1”的化学式为__,“酸浸”时Co O 发生的反应的化学方程式是__。
2 3(2)“酸浸”时加入HO 的目的是__。生产过程中发现实际消耗双氧水的量大于理论值,可能的原因是__。
2 2
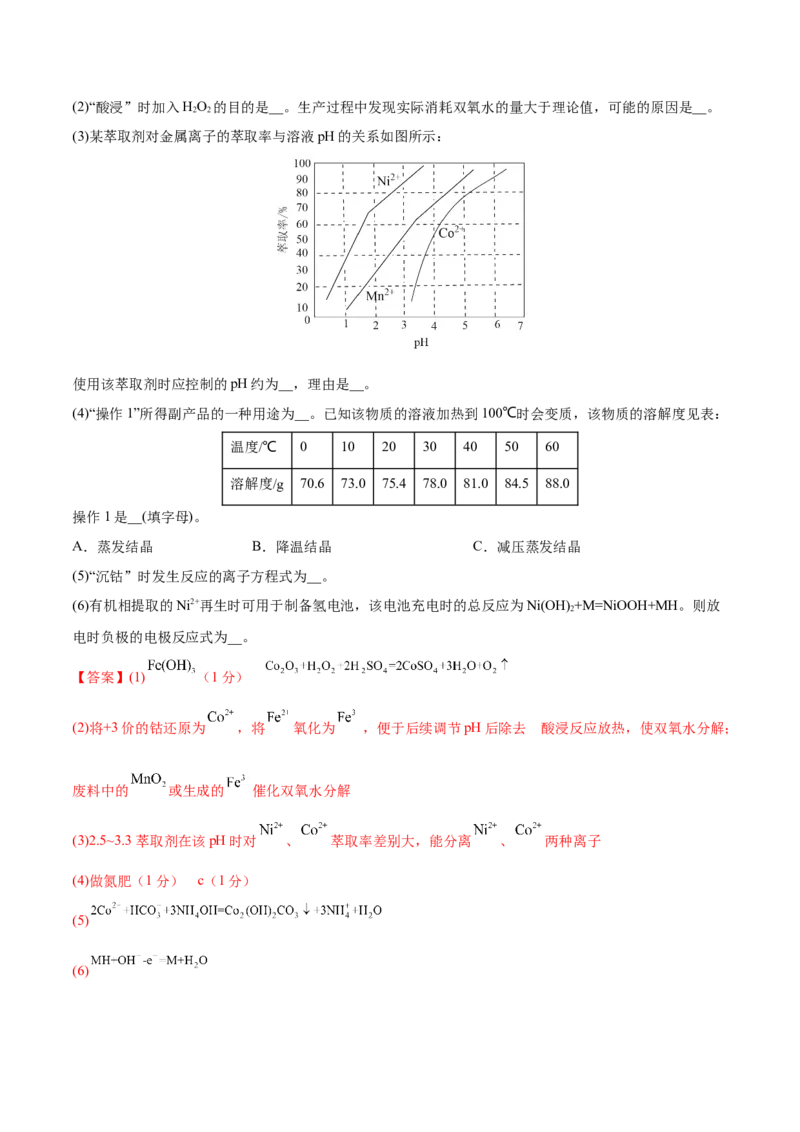
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:
使用该萃取剂时应控制的pH约为__,理由是__。
(4)“操作1”所得副产品的一种用途为__。已知该物质的溶液加热到100℃时会变质,该物质的溶解度见表:
温度/℃ 0 10 20 30 40 50 60
溶解度/g 70.6 73.0 75.4 78.0 81.0 84.5 88.0
操作1是__(填字母)。
A.蒸发结晶 B.降温结晶 C.减压蒸发结晶
(5)“沉钴”时发生反应的离子方程式为__。
(6)有机相提取的Ni2+再生时可用于制备氢电池,该电池充电时的总反应为Ni(OH) +M=NiOOH+MH。则放
2
电时负极的电极反应式为__。
【答案】(1) (1分)
(2)将+3价的钴还原为 ,将 氧化为 ,便于后续调节pH后除去 酸浸反应放热,使双氧水分解;
废料中的 或生成的 催化双氧水分解
(3)2.5~3.3 萃取剂在该pH时对 、 萃取率差别大,能分离 、 两种离子
(4)做氮肥(1分) c(1分)
(5)
(6)【解析】(1)由已知I可知,酸浸后浸出液中含有的阳离子为 、 、 、 ,再由已知II可知,
当调节pH至3.7时, 会先以沉淀的形式析出,所以“滤渣1”的化学式为 ;酸浸时
在酸性条件下与 发生氧化还原反应生成 、氧气和水,依据得失电子守恒、质量守恒,化学方程
式为: 。
(2)由分析可知,加入过氧化氢的目的是酸性条件下,氧化钴与过氧化氢发生氧化还原反应生成 ,四氧
化三铁中的 与过氧化氢发生氧化还原反应生成 ;过氧化氢的稳定性差,酸浸时,反应放热,放出
的热量能使过氧化氢分解,同时,废料中的二氧化锰或溶液中的 也可以做过氧化氢分解的催化剂,加
快过氧化氢的分解,导致实际消耗的过氧化氢的量大于理论值。
(3)使用该萃取剂萃取 ,单纯从萃取率考虑,萃取率越高越好,但同时还要考虑到 尽可能的不被萃
取,两方面综合考虑,pH应控制在2.5~3.3;因为萃取剂在该pH时对 、 萃取率差别大,能分离
、 两种离子。
(4)整个过程中加入的物质有:硫酸、过氧化氢、氨水和碳酸氢铵,过氧化氢和碳酸氢根在反应过程中反应
完全,依据质量守恒,溶液中还有的物质为硫酸铵,可用作氮肥;从溶解度角度看,硫酸铵的溶解度随温
度升高有所增大,但变化量不大,且硫酸铵受热易分解,因此操作1应采取减压蒸发结晶,选c。
(5)沉钴时发生的反应为向水相中加入氨水和碳酸氢铵溶液,亚钴离子转化为 沉淀,钴元素化
合价不变,因此发生非氧化还原反应,离子方程式为: 。
(6)由电池充电时的总反应可知,放电时负极为MH,失电子化合价升高,发生氧化反应生成M,因此放电
时负极电极反应式为: 。
14.(2022·河南河南·三模)(11分)电镀废液中含有Cu2+、Mg2+、Ca2+、Ni2+和Fe3+,某专利申请用下列
方法从该类废液中制备高纯度的铜粉。已知导体和其接触的溶液的界面上会形成一定的电位差,被称作电极电位。如反应Cu2+(氧化态)+2e-=Cu(还
原态)的标准电极电位表示为Cu2+/Cu=0.34,该值越大氧化态的氧化性越强,越小还原态的还原性越强。两
个电对间的电极电位差别越大,二者之间的氧化还原反应越易发生。某些电对的电极电位如下表所示:
Fe3+/Fe2+ Cu2+/Cu+ Cu2+/Cu Fe2+/Fe Ni2+/Ni Mg2+/Mg Ca2+/Ca
/SO
2
0.77 0.52 0.34 0.17 -0.44 -0.23 -2.38 -2.76
回答下列问题:
(1)蒸发浓缩后的溶液中,Cu2+的物质的量浓度≥_______(结果保留两位小数)。分离固液混合物时,需要用
真空抽滤的方法提高过滤的速度和效果,其原因是_______。
(2)溶液的氧化还原电位越高,其氧化能力同样越强。溶液的氧化还原电位,与溶液中离子等微粒的种类及
其浓度相关,实验测得Cu2+与SO 反应体系的氧化还原电位与铜粉的回收率和纯度的关系如下表所示:
2
反应液的电位(mV) 360 340 320 300 280 260
铜粉的回收率(%) 86.5 90.2 95.6 97.2 97.3 97.4
产品的纯度(%) 99.9 99.9 99.9 99.9 99.9 99.9
①由此可知,制备过程中进行电位检测时,要把溶液的氧化还原电位控制在_______mV左右。
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是
Cu2+直接被还原为Cu的原因是_______。反应生成Cu+的离子方程式是_______。
(3)废液2中含有的金属离子除Mg2+、Ca2+外还有_______。为了使这些离子均除去,使水得到进一步的净
化,应该在调节溶液pH使其他杂质离子沉淀后,再使Ca2+转化为_______(填化学式)而除去。
【答案】(1)0.94mol/L(1分) 固液混合物中铜为粉末状,普通过滤速率非常慢
(2)①260 ②Cu2+/Cu+的电极电位为0.52,而Cu2+/Cu的电极电位为0.34,前者大于后者,即Cu2+更容易转化
为Cu+ Cu2++e-=Cu+(1分)
(3)Ni2+和Fe2+ CaSO(1分)
4
【解析】通过题干表格中各组电极电势的数据可知,废液1蒸发浓缩后通入SO ,将Cu2+还原为Cu,
2
Fe3+还原为Fe2+,过滤后得到铜粉和滤液2,滤液2中含有Mg2+、Ca2+、Ni2+和Fe2+,其中Ca2+与 转化为
CaSO 沉淀,而Mg2+和Fe2+、Ni2+可以通过调节pH值的方法转化为氢氧化物的形成除去。
4(1)由题干数据可知,蒸发浓缩后的溶液中Cu2+的浓度不小于60g/L,则Cu2+的物质的量浓度≥
=0.94mol/L,由于分离固液混合物时Cu为粉末状,普通过滤时易造成滤纸堵塞,过滤速率非常慢,则需要
用真空抽滤的方法提高过滤的速度和效果,故答案为:0.94mol/L;固液混合物中铜为粉末状,普通过滤速
率非常慢;
(2)①由表可知,制备过程中进行电位检测时,氧化还原电位在260mV时铜的回收率最高,纯度高,故要
把溶液的氧化还原电位控制在260mV左右,故答案为:260;
②专利申请书指出,反应液的反应历程为Cu2+首先被还原为Cu+,Cu+再歧化为Cu和Cu2+。反应历程不是
Cu2+直接被还原为Cu的原因是由表中数据可知,Cu2+/Cu+的电极电位为0.52,而Cu2+/Cu的电极电位为
0.34,前者大于后者,即Cu2+更容易转化为Cu+,反应生成Cu+的离子方程式是Cu2++e-=Cu+,故答案为:
Cu2+/Cu+的电极电位为0.52,而Cu2+/Cu的电极电位为0.34,前者大于后者,即Cu2+更容易转化为Cu+;
Cu2++e-=Cu+;
(3)由题干数据可知,Fe3+/Fe2+的电极电位为0.77mV,Cu2+/Cu+的电极电位为0.52mV,Cu2+/Cu的电极电位
为0.34mV, /SO 的电极电位为0.17mV,故Cu2+被还原为Cu时,Fe3+被还原为Fe2+,则滤液2中还有
2
的离子为:Mg2+、Ca2+、Ni2+和Fe2+,为了使这些离子均除去,使水得到进一步的净化,应该在调节溶液
pH使其他杂质离子沉淀后,再使Ca2+转化为CaSO 而除去,故答案为:Ni2+和Fe2+;CaSO。
4 4
15.(2022·四川乐山·一模)(14分)某种常见补铁药物的主要成分为琥珀酸亚铁。该药品不溶于水但能
溶于常见稀酸。某学习小组同学分别设计实验检验药片中Fe2+的存在并测定Fe2+的含量(假设杂质不参与反
应)。回答下列问题:
(1)甲同学为了检验药品中的Fe2+ ,将药物碾碎、水溶后过滤。取少量所得滤液于两支试管中,分别加入
K[Fe(CN) ]溶液和KSCN溶液,观察并记录实验现象。
3 6
①甲同学过滤时的下列操作规范的是_______(填编号)。
a.用玻璃棒引流
b.漏斗口未紧靠烧杯内壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高于漏斗边缘
e.用玻璃棒在漏斗中搅动以加快过滤速度
②滤液加入K[Fe(CN) ]溶液或KSCN溶液均未出现明显现象,其主要原因为 _______。
3 6
(2)乙同学设计如下实验测定药片中Fe2+的含量。步骤一:取本品10片,碾碎后加入一定浓度试剂a,在适当的条件下配成100mL溶液。
步骤二:准确量取20.00mL步骤一所得溶液放入烧杯中。
步骤三:向烧杯中加入过量HO 溶液,后加入过量NaOH溶液生成沉淀,将沉淀过滤、洗涤、干燥后灼烧
2 2
至固体质量恒定,得0. 64g固体。
①步骤一中加入的试剂a为 _______ 。
②步骤三中,加入HO 溶液发生反应的离子方程式为 _______,灼烧后 所得固体的颜色为 _______,灼
2 2
烧时需要使用下列仪器中的 _______(填编号)。
a.酒精灯 b.坩埚 c.蒸发皿 d.铁架台(带铁圈) e.三脚架
③若将步骤三中的HO 溶液换为Cl 也能达到目的,但使用HO 溶液的好处是_______。
2 2 2 2 2
④由实验数据计算,每片药片中约含Fe2+ _______mg。
(3)医生建议该药品与维生素C同时服用以增强补铁效果,原因是利用了维生素C的_______ (选填“氧化
性”、“ 还原性”或“碱性”。)
【答案】(1)①ac ②该药品不溶于水(1分)
(2)①稀硫酸/稀盐酸(1分) ②HO+2H++2Fe2+=2Fe3++2H O 红棕色(1分) abe ③无污染/操作方便 ④224
2 2 2
(3)还原性(1分)
【解析】(1)①a.过滤时,用玻璃棒引流,故a正确;b.过滤时,为防止滤液迸溅,漏斗口应紧靠烧
杯内壁,故b错误;c.用少量水润湿滤纸,使滤纸紧贴漏斗,滤纸层与漏斗壁间不留气泡,故c正确;
d.滤纸边缘低于漏斗边缘,故d错误;e.用玻璃棒搅动漏斗里的液体,容易把滤纸弄破,起不到过滤的
作用,故e错误;正确的做法是ac;
②琥珀酸亚铁不溶于水,所以滤液加入K[Fe(CN) ]溶液或KSCN溶液均未出现明显现象。
3 6
(2)①琥珀酸亚铁能溶于常见稀酸,所以步骤一中加入稀硫酸或稀盐酸溶解。
②步骤三中,加入HO 溶液把Fe2+氧化为Fe3+,发生反应的离子方程式为HO+2H++2Fe2+=2Fe3++2H O,灼
2 2 2 2 2
烧后 所得固体为氧化铁,氧化铁的颜色为红棕色,灼烧固体的装置为 ,需要使用仪器有.酒
精灯、坩埚、三脚架等,选abe。
③HO 是绿色氧化剂,使用HO 溶液的好处是无污染/操作方便。
2 2 2 2④灼烧得0. 64g固体Fe O,根据铁元素守恒,每片药片中约含Fe2+
2 3
。
(3)该药品与维生素C同时服用以增强补铁效果,维生素C能防止Fe2+氧化,所以利用维生素C的还原
性。