文档内容
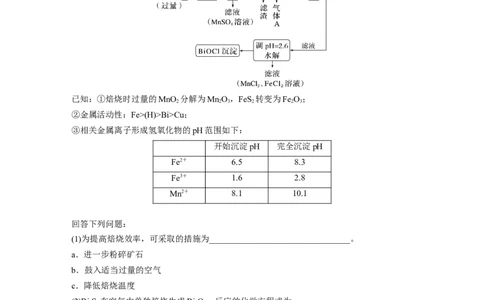
1.(2022·辽宁,16)某工厂采用辉铋矿(主要成分为BiS ,含有FeS 、SiO 杂质)与软锰矿(主
2 3 2 2
要成分为MnO )联合焙烧法制备BiOCl和MnSO ,工艺流程如下:
2 4
已知:①焙烧时过量的MnO 分解为MnO,FeS 转变为Fe O;
2 2 3 2 2 3
②金属活动性:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围如下:
开始沉淀pH 完全沉淀pH
Fe2+ 6.5 8.3
Fe3+ 1.6 2.8
Mn2+ 8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为_________________________________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2)Bi S 在空气中单独焙烧生成BiO,反应的化学方程式为____________________。
2 3 2 3
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出Bi3+和Mn2+;②_______________。
(4)滤渣的主要成分为________________(填化学式)。
(5)生成气体A的离子方程式为_____________________________________________
________________________________________________________________________。
(6)加入金属Bi的目的是___________________________________________________。
2.(2022·全国乙卷,26)废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少
4 2
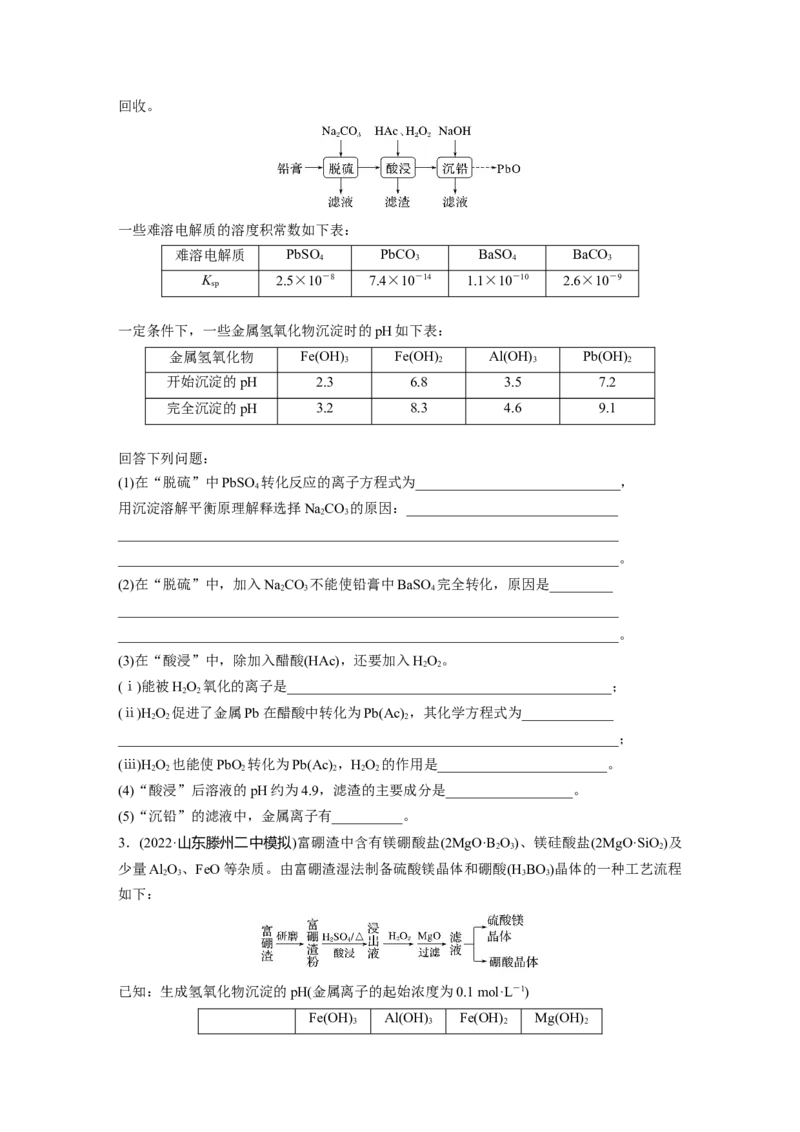
量Ba、Fe、Al的盐或氧化物等,为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
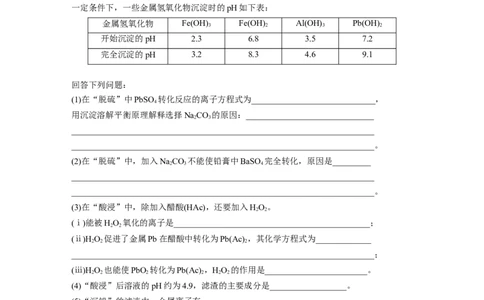
(1)在“脱硫”中PbSO 转化反应的离子方程式为_____________________________,
4
用沉淀溶解平衡原理解释选择NaCO 的原因:______________________________
2 3
_______________________________________________________________________
_______________________________________________________________________。
(2)在“脱硫”中,加入NaCO 不能使铅膏中BaSO 完全转化,原因是_________
2 3 4
_______________________________________________________________________
_______________________________________________________________________。
(3)在“酸浸”中,除加入醋酸(HAc),还要加入HO。
2 2
(ⅰ)能被HO 氧化的离子是______________________________________________;
2 2
(ⅱ)H O 促进了金属Pb在醋酸中转化为Pb(Ac) ,其化学方程式为_____________
2 2 2
_______________________________________________________________________;
(ⅲ)H O 也能使PbO 转化为Pb(Ac) ,HO 的作用是________________________。
2 2 2 2 2 2
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是__________________。
(5)“沉铅”的滤液中,金属离子有__________。
3.(2022·山东滕州二中模拟)富硼渣中含有镁硼酸盐(2MgO·B O)、镁硅酸盐(2MgO·SiO )及
2 3 2
少量Al O 、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H BO)晶体的一种工艺流程
2 3 3 3
如下:
已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol·L-1)
Fe(OH) Al(OH) Fe(OH) Mg(OH)
3 3 2 2开始沉淀时 1.9 3.4 7.0 9.1
完全沉淀时 3.2 4.7 9.0 11.1
(1)酸浸时发生反应:2MgO·SiO +2HSO ===2MgSO +SiO +2HO,2MgO·B O +2HSO +
2 2 4 4 2 2 2 3 2 4
HO===2HBO+2MgSO 。
2 3 3 4
①上述反应体现出酸性强弱:HSO __________(填“>”或“<”)H BO。
2 4 3 3
②已知硼酸与过量NaOH溶液发生的中和反应为HBO +OH-===B(OH)。下列关于硼酸的
3 3
说法正确的是________(填字母)。
A.硼酸是一元酸
B.向NaHCO 固体中滴加饱和硼酸溶液,有气泡产生
3
C.硼酸的电离方程式可表示为HBO+HOB(OH)+H+
3 3 2
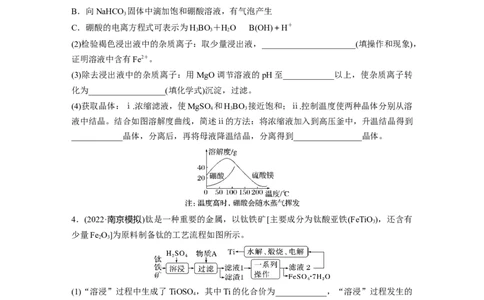
(2)检验褐色浸出液中的杂质离子:取少量浸出液,______________________(填操作和现象),
证明溶液中含有Fe2+。
(3)除去浸出液中的杂质离子:用MgO调节溶液的pH至____________以上,使杂质离子转
化为__________________(填化学式)沉淀,过滤。
(4)获取晶体:ⅰ.浓缩滤液,使MgSO 和HBO 接近饱和;ⅱ.控制温度使两种晶体分别从溶
4 3 3
液中结晶。结合如图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜中,升温结晶得到
____________晶体,分离后,再将母液降温结晶,分离得到________________晶体。
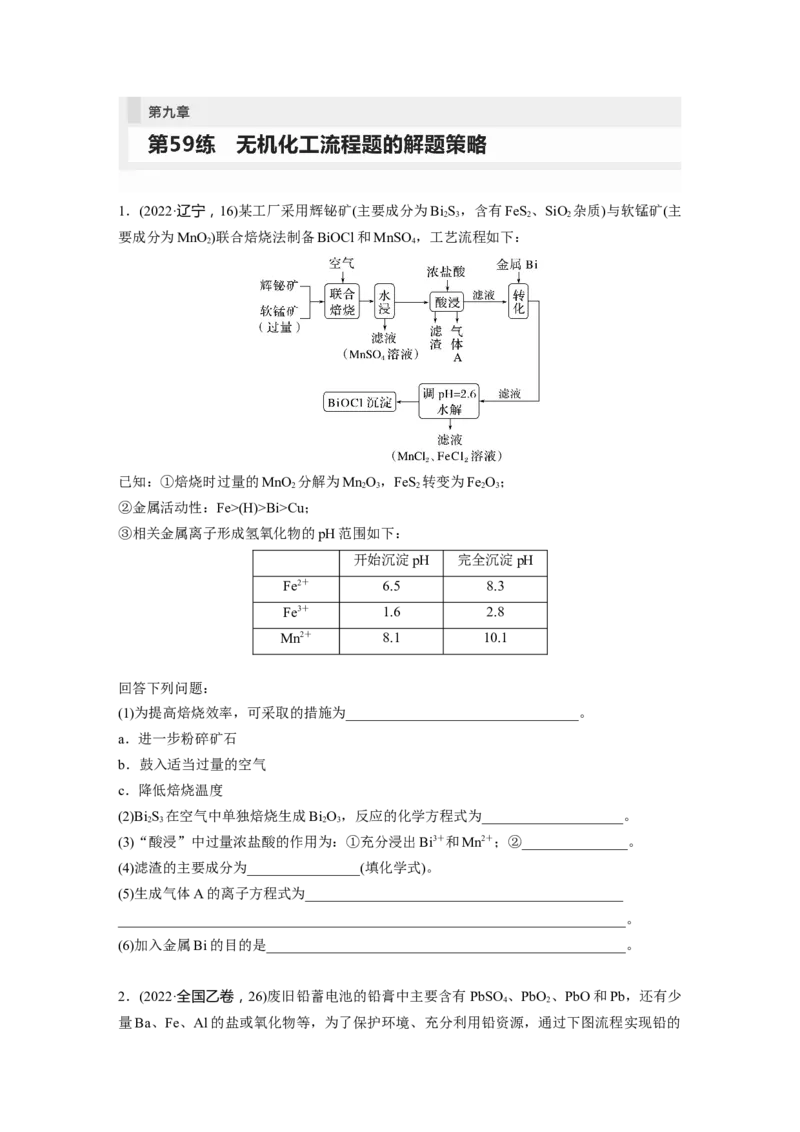
4.(2022·南京模拟)钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO),还含有
3
少量Fe O]为原料制备钛的工艺流程如图所示。
2 3
(1)“溶浸”过程中生成了TiOSO ,其中Ti的化合价为____________,“溶浸”过程发生的
4
主要反应的化学方程式为__________________________________________________
________________________________________________________________________。
(2)物质A为单质,化学式为__________,“一系列操作”为蒸发浓缩、________和过滤。
(3)将少量FeSO ·7H O溶于水,加入一定量的NaHCO 溶液,可制得FeCO ,写出反应的离
4 2 3 3
子方程式为______________________________________________________________
________________________________________________________________________。
(4)若反应后的溶液中c(Fe2+)=2.0×10-6 mol·L-1,则溶液中c(CO)=__________ mol·L-1(已
知:常温下FeCO 饱和溶液浓度为4.5×10-6 mol·L-1)。
3