文档内容
考点 10 硫及其化合物(好题冲关)
【基础过关】
1.(2023·浙江省东阳市高三5月模拟考试)硫酸钙用途广泛,下列说法不正确的是( )
A.CaSO·2H O俗名:熟石膏 B.CaSO 属于强电解质
4 2 4
C.CaSO 中即含离子键又含共价键 D.石膏可用来调节水泥硬化速度
4
【答案】A
【解析】A项,CaSO·2H O俗名:生石膏,A错误;B项,CaSO 是盐,在水溶液中完全电离,属于
4 2 4
强电解质,B正确;C项,CaSO 中Ca2+和SO 2-之间形成离子键,SO 2-内S原子和O原子形成共价键,C
4 4 4
正确; D项,水泥具有水硬性,石膏可用来调节水泥硬化速度,D正确;故选A。
2.(2023·浙江省义乌市高三高考适应性考试)在岩层深处和海底中存在黄铁矿(FeS ),下列说法不正确
2
的是( )
A.Fe元素位于周期表d区
B.Fe和S在加热条件下可制备FeS
2
C.FeS 受氧气和水的长期作用,可转化为硫酸盐
2
D.工业上可用黄铁矿为原料来制备硫酸
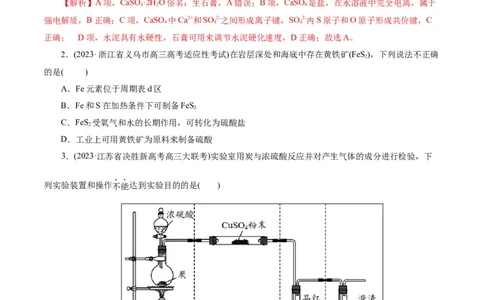
3.(2023·江苏省决胜新高考高三大联考)实验室用炭与浓硫酸反应并对产生气体的成分进行检验,下
列实验装置和操作不能达到实验目的的是( )
A.用装置甲进行反应 B.用装置乙检验HO(g)
2
C.用装置丙检验SO D.用装置丁检验CO
2 2
4.自然界中不同价态硫元素之间的转化如图所示,下列说法正确的是( )
资料收集整理【淘宝店铺:向阳百分百】A.上图中,酸雨的含硫成分只有 ,由SO 溶于水生成
2
B.芒硝在浓硫酸中失水的过程体现了浓硫酸的脱水性
C.黄铁矿燃烧产生的尾气,与空气混合后通入碳酸钙的浆状物,可用来制备石膏
D.凝聚法是将SO 通入HS稀溶液中得到S胶体,该反应中氧化剂:还原剂=2:1
2 2
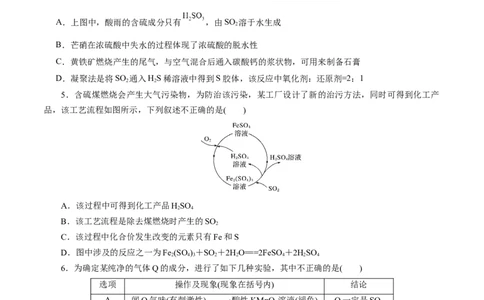
5.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产
品,该工艺流程如图所示,下列叙述不正确的是( )
A.该过程中可得到化工产品HSO
2 4
B.该工艺流程是除去煤燃烧时产生的SO
2
C.该过程中化合价发生改变的元素只有Fe和S
D.图中涉及的反应之一为Fe (SO )+SO +2HO===2FeSO+2HSO
2 4 3 2 2 4 2 4
6.为确定某纯净的气体Q的成分,进行了如下几种实验,其中不正确的是( )
选项 操作及现象(现象在括号内) 结论
A 闻Q气味(有刺激性)――→酸性KMnO 溶液(褪色) Q一定是SO
4 2
B 闻Q气味(有刺激性)――→澄清石灰水(变浑浊) Q可能是SO
2
C Q――→品红溶液(褪色)――→变红色 Q一定是SO
2
D Q――→紫色石蕊溶液(先变红色后褪色) Q一定不是SO
2
7.(2023·河北省衡水市部分重点高中高三二模)金属冶炼时产生的含二氧化硫废气经回收后可用于制
硫酸,实现资源化利用。下列化学反应表示正确的是( )
A.硫酸型酸雨露置于空气中一段时间后溶液酸性增强:HSO +O =H SO
2 3 2 2 4
B.用足量的石灰乳吸收废气中的SO :Ca2++SO+2OH- =CaSO ↓+H O
2 2 3 2
资料收集整理【淘宝店铺:向阳百分百】C.SO 通入足量的硝酸钡溶液中有白色沉淀生成: 3Ba2++3SO+2NO -+2H O=3BaSO ↓+2NO+4H+
2 2 3 2 3
D.向Ca(ClO) 溶液中通入少量SO :Ca2++SO+2ClO-+H O=CaSO ↓+2HClO
2 2 2 2 3
8.(2023·湖北省荆荆宜仙四地高三联考)单质硫与可溶性硫化物溶液作用生成多硫化物,如
(x一般为2~6);多硫化物在酸性溶液中不稳定,易歧化:
。下列说法错误的是( )
A.AsS (其中As显 价)是多硫化物 B.AsS 是氧化产物
2 3 2 5
C.NaS 中阴阳离子个数比为1:2 D.久置NaS洛液遇酸可能变浑浊
2 2 2
9.(2023·河北省石家庄市高三联考)硫及其化合物的“价-类二维图”体现了化学变化之美。下列有关
说法正确的是( )
A.硫在过量的氧气中燃烧直接生成Y
B.将X通入BaCl 溶液中有白色沉淀生成
2
C.M的无水固体粉末显蓝色
D.N与Z反应可生成X
10.(2023·海南省海口市二模)硫及其化合物在工业生产中多有涉及。下列有关说法正确的是( )
A.硫在过量的氧气中燃烧直接生成SO
3
B.将SO 通入BaCl 溶液中有白色沉淀生成
2 2
C.CuSO 的无水固体粉末显蓝色
4
D.HS和SO 反应可生成S
2 2
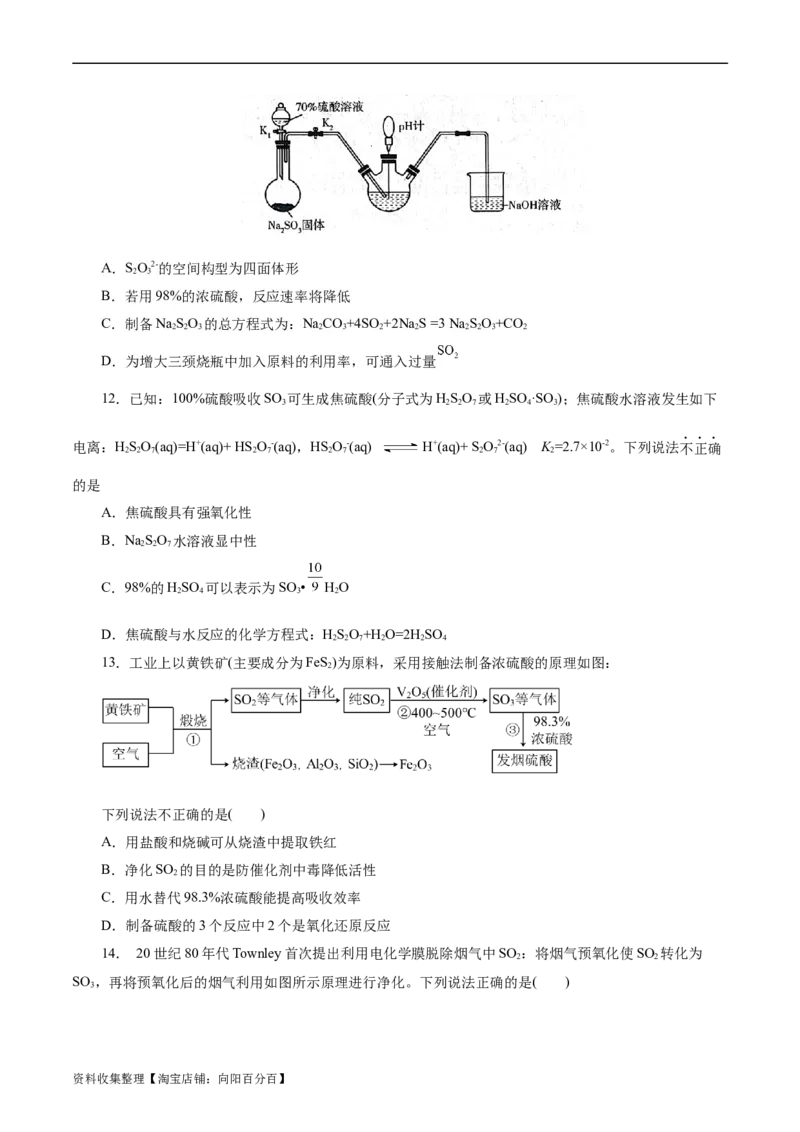
11.(2023·山东省济宁市三模)硫代硫酸钠(Na SO)是一种重要的化工产品,将SO 通入NaCO 和NaS
2 2 3 2 2 3 2
混合溶液中可制得NaSO。其制备装置如图所示,下列说法错误的是( )
2 2 3
资料收集整理【淘宝店铺:向阳百分百】A.SO2-的空间构型为四面体形
2 3
B.若用98%的浓硫酸,反应速率将降低
C.制备NaSO 的总方程式为:NaCO+4SO+2Na S =3 Na SO+CO
2 2 3 2 3 2 2 2 2 3 2
D.为增大三颈烧瓶中加入原料的利用率,可通入过量
12.已知:100%硫酸吸收SO 可生成焦硫酸(分子式为HSO 或HSO ·SO );焦硫酸水溶液发生如下
3 2 2 7 2 4 3
电离:HSO(aq)=H+(aq)+ HS O-(aq),HS O-(aq) H+(aq)+ SO2-(aq) K =2.7×10-2。下列说法不正确
2 2 7 2 7 2 7 2 7 2
的是
A.焦硫酸具有强氧化性
B.NaSO 水溶液显中性
2 2 7
C.98%的HSO 可以表示为SO • HO
2 4 3 2
D.焦硫酸与水反应的化学方程式:HSO+H O=2HSO
2 2 7 2 2 4
13.工业上以黄铁矿(主要成分为FeS)为原料,采用接触法制备浓硫酸的原理如图:
2
下列说法不正确的是( )
A.用盐酸和烧碱可从烧渣中提取铁红
B.净化SO 的目的是防催化剂中毒降低活性
2
C.用水替代98.3%浓硫酸能提高吸收效率
D.制备硫酸的3个反应中2个是氧化还原反应
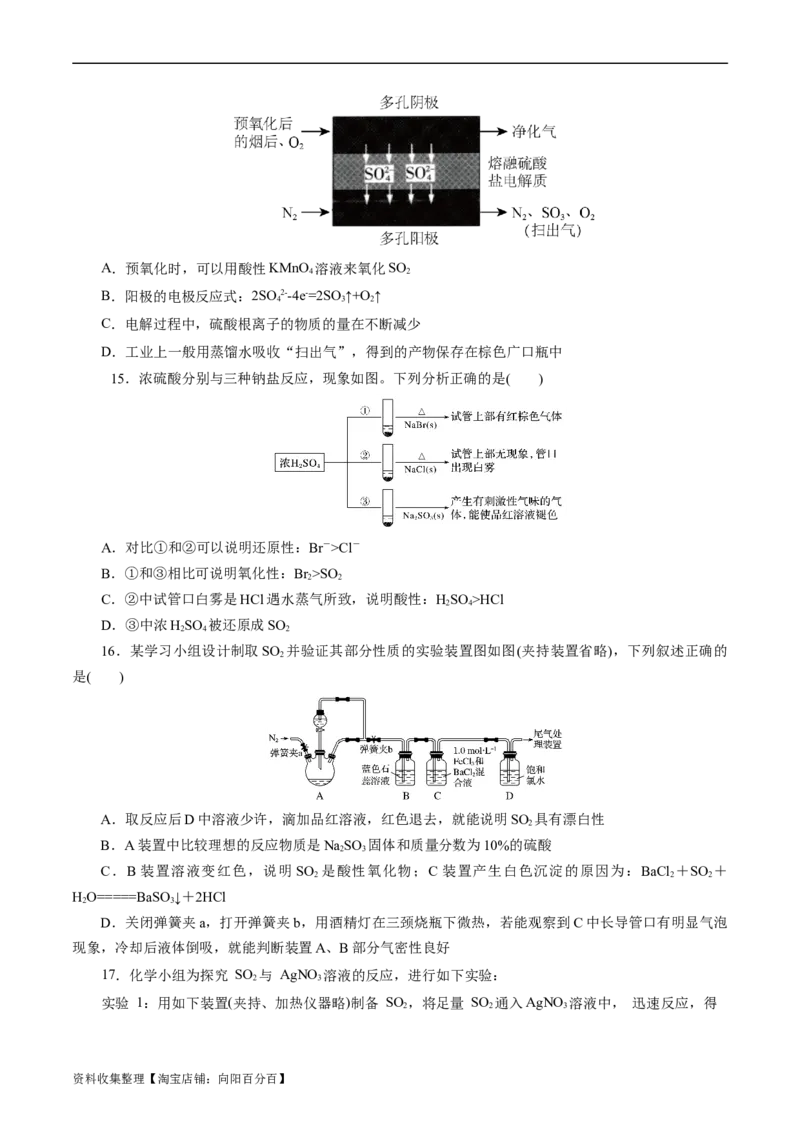
14. 20世纪80年代Townley首次提出利用电化学膜脱除烟气中SO :将烟气预氧化使SO 转化为
2 2
SO ,再将预氧化后的烟气利用如图所示原理进行净化。下列说法正确的是( )
3
资料收集整理【淘宝店铺:向阳百分百】A.预氧化时,可以用酸性KMnO 溶液来氧化SO
4 2
B.阳极的电极反应式:2SO 2--4e-=2SO↑+O ↑
4 3 2
C.电解过程中,硫酸根离子的物质的量在不断减少
D.工业上一般用蒸馏水吸收“扫出气”,得到的产物保存在棕色广口瓶中
15.浓硫酸分别与三种钠盐反应,现象如图。下列分析正确的是( )
A.对比①和②可以说明还原性:Br->Cl-
B.①和③相比可说明氧化性:Br >SO
2 2
C.②中试管口白雾是HCl遇水蒸气所致,说明酸性:HSO >HCl
2 4
D.③中浓HSO 被还原成SO
2 4 2
16.某学习小组设计制取SO 并验证其部分性质的实验装置图如图(夹持装置省略),下列叙述正确的
2
是( )
A.取反应后D中溶液少许,滴加品红溶液,红色退去,就能说明SO 具有漂白性
2
B.A装置中比较理想的反应物质是NaSO 固体和质量分数为10%的硫酸
2 3
C.B 装置溶液变红色,说明SO 是酸性氧化物;C 装置产生白色沉淀的原因为:BaCl +SO +
2 2 2
HO=====BaSO↓+2HCl
2 3
D.关闭弹簧夹a,打开弹簧夹b,用酒精灯在三颈烧瓶下微热,若能观察到C中长导管口有明显气泡
现象,冷却后液体倒吸,就能判断装置A、B部分气密性良好
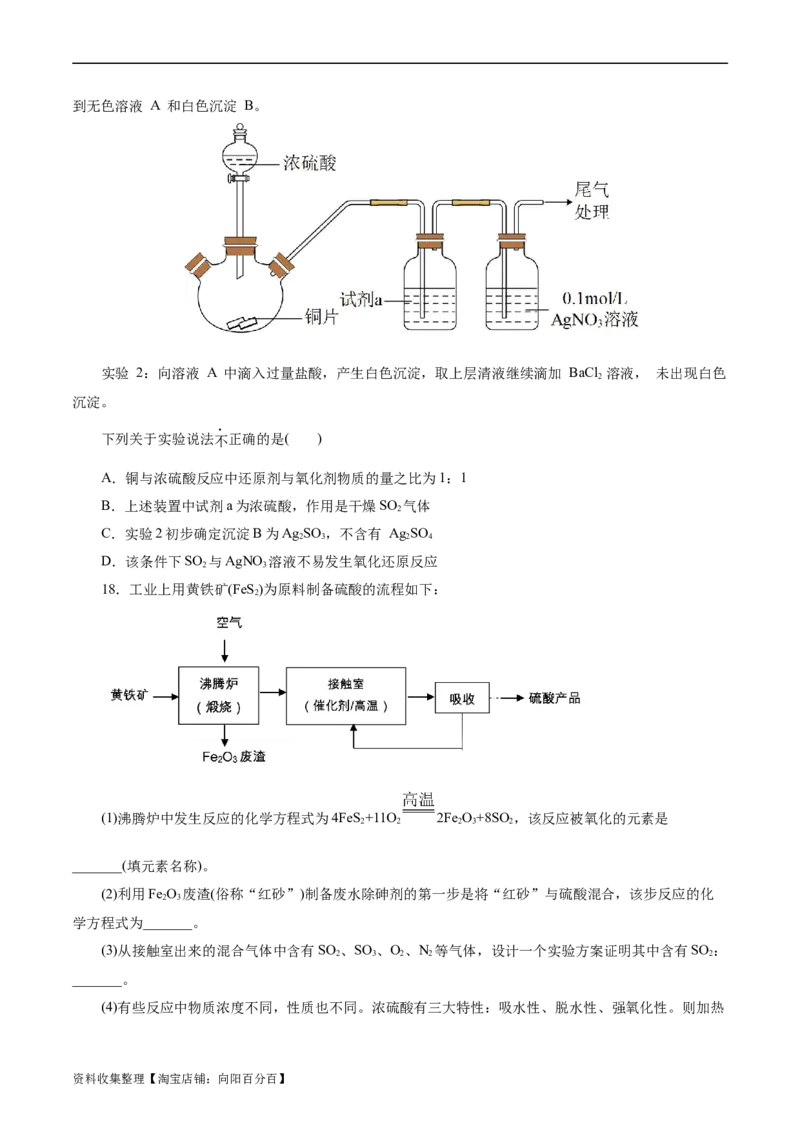
17.化学小组为探究 SO 与 AgNO 溶液的反应,进行如下实验:
2 3
实验 1:用如下装置(夹持、加热仪器略)制备 SO ,将足量 SO 通入AgNO 溶液中, 迅速反应,得
2 2 3
资料收集整理【淘宝店铺:向阳百分百】到无色溶液 A 和白色沉淀 B。
实验 2:向溶液 A 中滴入过量盐酸,产生白色沉淀,取上层清液继续滴加 BaCl 溶液, 未出现白色
2
沉淀。
下列关于实验说法不正确的是( )
A.铜与浓硫酸反应中还原剂与氧化剂物质的量之比为1:1
B.上述装置中试剂a为浓硫酸,作用是干燥SO 气体
2
C.实验2初步确定沉淀B为Ag SO ,不含有 Ag SO
2 3 2 4
D.该条件下SO 与AgNO 溶液不易发生氧化还原反应
2 3
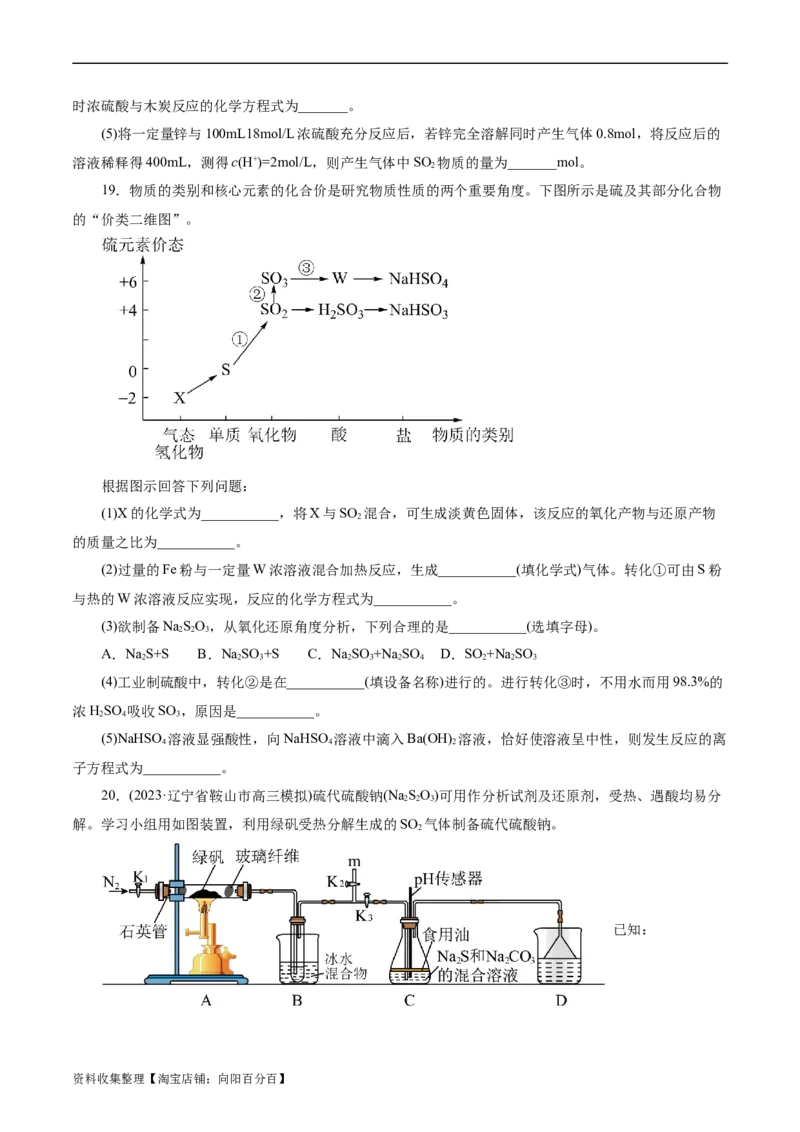
18.工业上用黄铁矿(FeS )为原料制备硫酸的流程如下:
2
(1)沸腾炉中发生反应的化学方程式为4FeS+11O 2Fe O+8SO,该反应被氧化的元素是
2 2 2 3 2
_______(填元素名称)。
(2)利用Fe O 废渣(俗称“红砂”)制备废水除砷剂的第一步是将“红砂”与硫酸混合,该步反应的化
2 3
学方程式为_______。
(3)从接触室出来的混合气体中含有SO 、SO 、O、N 等气体,设计一个实验方案证明其中含有SO :
2 3 2 2 2
_______。
(4)有些反应中物质浓度不同,性质也不同。浓硫酸有三大特性:吸水性、脱水性、强氧化性。则加热
资料收集整理【淘宝店铺:向阳百分百】时浓硫酸与木炭反应的化学方程式为_______。
(5)将一定量锌与100mL18mol/L浓硫酸充分反应后,若锌完全溶解同时产生气体0.8mol,将反应后的
溶液稀释得400mL,测得c(H+)=2mol/L,则产生气体中SO 物质的量为_______mol。
2
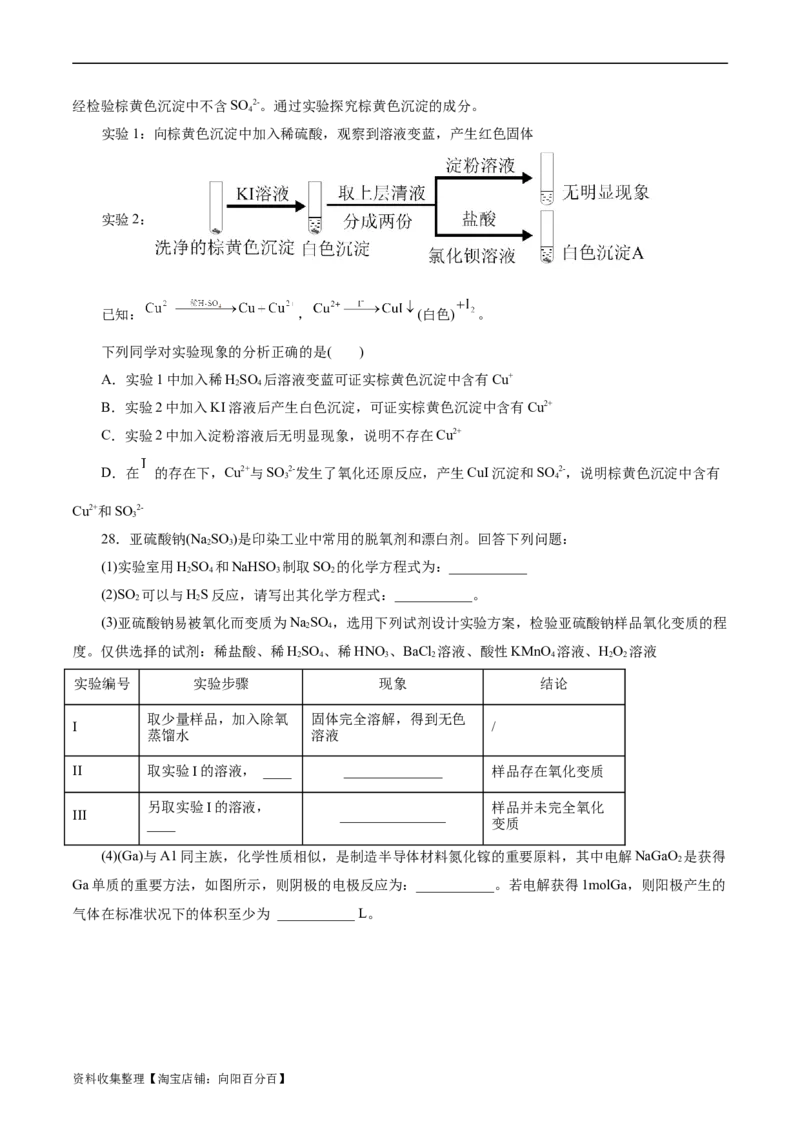
19.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物
的“价类二维图”。
根据图示回答下列问题:
(1)X的化学式为___________,将X与SO 混合,可生成淡黄色固体,该反应的氧化产物与还原产物
2
的质量之比为___________。
(2)过量的Fe粉与一定量W浓溶液混合加热反应,生成___________(填化学式)气体。转化①可由S粉
与热的W浓溶液反应实现,反应的化学方程式为___________。
(3)欲制备NaSO,从氧化还原角度分析,下列合理的是___________(选填字母)。
2 2 3
A.NaS+S B.NaSO +S C.NaSO +Na SO D.SO +Na SO
2 2 3 2 3 2 4 2 2 3
(4)工业制硫酸中,转化②是在___________(填设备名称)进行的。进行转化③时,不用水而用98.3%的
浓HSO 吸收SO ,原因是___________。
2 4 3
(5)NaHSO 溶液显强酸性,向NaHSO 溶液中滴入Ba(OH) 溶液,恰好使溶液呈中性,则发生反应的离
4 4 2
子方程式为___________。
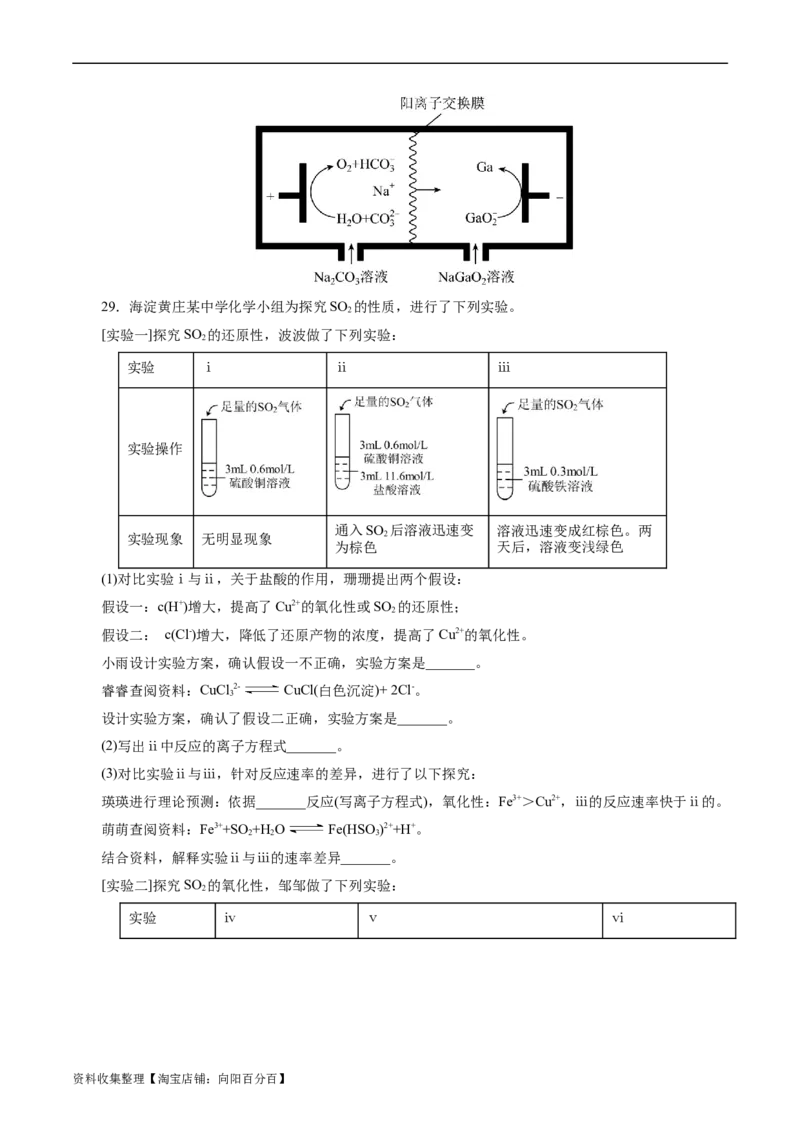
20.(2023·辽宁省鞍山市高三模拟)硫代硫酸钠(NaSO)可用作分析试剂及还原剂,受热、遇酸均易分
2 2 3
解。学习小组用如图装置,利用绿矾受热分解生成的SO 气体制备硫代硫酸钠。
2
已知:
资料收集整理【淘宝店铺:向阳百分百】①绿矾受热分解反应为:FeSO ·7H O Fe O+SO ↑+SO ↑+14H O↑;
4 2 2 3 3 2 2
②SO 的沸点为44.8℃。
3
回答下列问题:
(1)完成实验操作过程:
连接装置,___________,加入药品(NaS和NaCO 混合溶液用煮沸过的蒸馏水配制),使所有活塞处
2 2 3
于关闭状态。开始制备,打开某些活塞,通入一段时间N;关闭活塞___________,打开活塞___________,
2
加热绿矾;使用pH传感器始终观测C处溶液的pH,在pH7~8之间时停止加热,同时关闭活塞K;……
3
将锥形瓶用热水浴浓缩至水层表面出现结晶为止,经过___________、过滤、洗涤、干燥得到NaSO 晶体。
2 2 3
(2)写出锥形瓶中发生反应的离子方程式___________。
(3)装置B的作用为___________。
(4)将锥形瓶中的反应停止在pH传感器的读数为7~8时的原因是___________。
(5)该装置存在一个明显的缺点,请提出改进方法___________。
21.(2023·海南省海口市高三模拟)兴趣实验小组在实验室模拟接触法制硫酸的关键环节。在查资料后
开展了以下制备实验。完成其实验过程中的问题。
Ⅰ.催化剂的准备取 的偏钒酸铵加入到 水中,加热到70℃溶解。放入石棉绒浸透,取出石
棉绒灼烧得到黄色固体。(资料:2NH NO VO+2NH↑+H O)
4 3 2 5 3 2
(1)该步骤中使用到的仪器不包括______(填序号)。
a.玻璃棒 b.温度计 c.烧杯 d.量筒 e.镊子 f.坩埚 g.天平 h.蒸发皿
(2)检验NH 的方法是__________。
3
Ⅱ.连接装置并完成实验
装置连接,检查气密性。加入药品后,点燃酒精灯和硫黄,通入空气。观察。
(3)装置接口连接
的顺序为a→__________。
(4)开始实验后装置C中可看到的现象是__________。
(5)装置B的作用是__________。其中发生反应的离子方程式为__________。
Ⅲ.问题与讨论
(6)小组在装置B后面添加了装置E,当E中品红褪色,说明__________。
资料收集整理【淘宝店铺:向阳百分百】【能力提升】
22.(2023·黑龙江省绥化市第一中学高三期中)图为接触法制硫酸的示意图,已知2SO (g)+CO(g)
2 2
2SO (g) ΔH<0,下列说法不正确的是( )
3
A.黄铁矿的主要成分是FeS,沸腾炉中的化学方程式为4 FeS + 11O 2Fe O + 8SO
2 2 2 2 3 2
B.接触室的热交换器的作用是加热a处气体,冷却c处气体,控制气体接触催化剂时的温度
C.将黄铁矿粉碎有利于增大与空气的接触面积,加快反应速率,提高原料利用率
D.应将98.3%的浓硫酸换成蒸馏水,以便吸收更多的SO
3
23.(2023·浙江省强基联盟高三上学期10月统测)硫的四种含氧酸根离子的结构如图所示,下列有关说
法正确的是( )
A.①②③④中都含有极性键和非极性键
B.①④中硫原子的化合价不同
C.能在酸性溶液中将Mn2+转化为MnO-的只有④
4
D.只考虑硫元素的价态,②只有氧化性
资料收集整理【淘宝店铺:向阳百分百】24.(2023·福建省龙岩市高中毕业班教学质量检测)硫代硫酸钠(Na SO)可用于脱除废水中游离氯。其
2 2 3
工业制备方法为:将一定比例的NaCO 与NaS配成混合溶液,再通入SO ,先有黄色沉淀生成,当黄色
2 3 2 2
沉淀消失时,即生成了NaSO,同时释放CO。下列说法错误的是( )
2 2 3 2
A.制备反应中NaSO 既是氧化产物又是还原产物
2 2 3
B.制备总反应的离子方程式为CO2-+4SO+2S2- =3S O2-+CO
3 2 2 3 2
C.产生黄色沉淀的反应中氧化剂与还原剂物质的量之比为2∶1
D.将NaSO 脱除游离氯反应设计成原电池时,SO2-为负极反应物
2 2 3 2 3
25.玻璃仪器内璧残留的硫单质可用热NaOH溶液洗涤除去,发生如下反应:
①3S+ 6NaOH 2NaS+ Na SO + 3H O
2 2 3 2
②(x-1)S+Na S NaS (x=2~6)
2 2 x
③S+ Na SO NaSO
2 3 2 2 3
下列说法正确的是( )
A.反应①②③中,硫单质的作用相同
B.反应①中,每消耗1 mol硫单质转移4 mol电子
C.0.96g硫单质与amL2mol·L-1热NaOH溶液恰好完全反应,只生成NaS和NaSO ,则a= 60
2 2 3
D.1.28 g硫单质与10 mL 2 mol·L-1热NaOH溶液恰好完全反应,只生成NaS 和NaSO,则x=5
2 x 2 2 3
26.(2023·重庆市万州第二高级中学高三检测) 排放到空气中会引起酸雨等环境问题,严重危害人
类健康。SO 的水溶液中存在下列平衡:
2
已知:K、K、K 为各步反应的平衡常数,且 [ 表示SO 的平衡压强]。下列
1 2 3 2
说法正确的是( )
A.由图平衡可知NaSO 溶液和NaHSO 溶液都可以水解,溶液一定呈碱性
2 3 3
B.氨水也可吸收SO ,防止大气污染,同时通入O 能进一步提高SO 去除率
2 2 2
C.当 的平衡压强为p时,测得c(SO 2-) =a mol/L,则溶液
3
D.用 的 溶液吸收0.2mol的SO ,则溶液中存在关系式: c(Na+) =3c(H+) +
2
3c((HSO -) + 6c(SO ·xH O) -3c(OH-)
3 2 2
27.向2mL0.2mol/LCuSO 溶液中滴加0.2mol/LNa SO 溶液时溶液变绿,继续滴加产生棕黄色沉淀,
4 2 3
资料收集整理【淘宝店铺:向阳百分百】经检验棕黄色沉淀中不含SO 2-。通过实验探究棕黄色沉淀的成分。
4
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2:
已知: , (白色) 。
下列同学对实验现象的分析正确的是( )
A.实验1中加入稀HSO 后溶液变蓝可证实棕黄色沉淀中含有Cu+
2 4
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有Cu2+
C.实验2中加入淀粉溶液后无明显现象,说明不存在Cu2+
D.在 的存在下,Cu2+与SO 2-发生了氧化还原反应,产生CuI沉淀和SO 2-,说明棕黄色沉淀中含有
3 4
Cu2+和SO 2-
3
28.亚硫酸钠(Na SO )是印染工业中常用的脱氧剂和漂白剂。回答下列问题:
2 3
(1)实验室用HSO 和NaHSO 制取SO 的化学方程式为:___________
2 4 3 2
(2)SO 可以与HS反应,请写出其化学方程式:___________。
2 2
(3)亚硫酸钠易被氧化而变质为NaSO ,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程
2 4
度。仅供选择的试剂:稀盐酸、稀HSO 、稀HNO、BaCl 溶液、酸性KMnO 溶液、HO 溶液
2 4 3 2 4 2 2
实验编号 实验步骤 现象 结论
取少量样品,加入除氧 固体完全溶解,得到无色
I /
蒸馏水 溶液
II 取实验I的溶液, ____ ______________ 样品存在氧化变质
另取实验I的溶液, 样品并未完全氧化
III _______________
____ 变质
(4)(Ga)与A1同主族,化学性质相似,是制造半导体材料氮化镓的重要原料,其中电解NaGaO 是获得
2
Ga单质的重要方法,如图所示,则阴极的电极反应为:___________。若电解获得1molGa,则阳极产生的
气体在标准状况下的体积至少为 ___________ L。
资料收集整理【淘宝店铺:向阳百分百】29.海淀黄庄某中学化学小组为探究SO 的性质,进行了下列实验。
2
[实验一]探究SO 的还原性,波波做了下列实验:
2
实验 ⅰ ⅱ ⅲ
实验操作
通入SO 后溶液迅速变 溶液迅速变成红棕色。两
实验现象 无明显现象 2
为棕色 天后,溶液变浅绿色
(1)对比实验ⅰ与ⅱ,关于盐酸的作用,珊珊提出两个假设:
假设一:c(H+)增大,提高了Cu2+的氧化性或SO 的还原性;
2
假设二: c(Cl-)增大,降低了还原产物的浓度,提高了Cu2+的氧化性。
小雨设计实验方案,确认假设一不正确,实验方案是_______。
睿睿查阅资料:CuCl 2- CuCl(白色沉淀)+ 2Cl-。
3
设计实验方案,确认了假设二正确,实验方案是_______。
(2)写出ⅱ中反应的离子方程式_______。
(3)对比实验ⅱ与ⅲ,针对反应速率的差异,进行了以下探究:
瑛瑛进行理论预测:依据_______反应(写离子方程式),氧化性:Fe3+>Cu2+,ⅲ的反应速率快于ⅱ的。
萌萌查阅资料:Fe3++SO+H O Fe(HSO )2++H+。
2 2 3
结合资料,解释实验ⅱ与ⅲ的速率差异_______。
[实验二]探究SO 的氧化性,邹邹做了下列实验:
2
实验 ⅳ ⅴ ⅵ
资料收集整理【淘宝店铺:向阳百分百】