文档内容
【基础知识】离子反应
考点一 电解质及电离
【必备知识】
一、电解质及其分类
1、电解质与非电解质
(1)电解质:在水溶液中或熔融状态下能够导电的化合物。
实例:酸、碱、盐、活泼金属氧化物、水。
(2)非电解质:在水溶液中和熔融状态下都不能导电的化合物。
实例:大多数非金属氧化物、部分非金属氢化物、多数有机物。
【注意】单质、混合物即不是电解质也不是非电解质。
2、强、弱电解质的区别
(1)强电解质:在水溶液中能完全电离的电解质。
实例:强酸、强碱、大多数盐、活泼金属氧化物
(2)弱电解质:在水溶液中部分电离的电解质。
实例:弱酸、弱碱、水、少数盐
例、现有12种物质:①Al ②稀硝酸 ③HNO ④NH ·H O ⑤CO ⑥空气 ⑦NaCl
3 3 2 2
⑧CaCO ⑨NaHCO ⑩乙醇 ⑪Al O ⑫Cu(OH)
3 3 2 3 2
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 电解质,熔融状态下能导电
(2) 非电解质
(3) 强电解质,但熔融状态下并不导电
(4) 强电解质,但难溶于水
(5) 弱电解质
(6) 既不是电解质,也不是非电解质,但本身能导电
【答案】 (1)⑦⑧⑨⑪⑫ (2)⑤ ⑩ (3)③ (4)⑧⑪ (5)④ ⑫ (6)① ②
二、电解质的电离
电离:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
例、按要求书写下列电解质的电离方程式:
①Ba(OH) :___________________________________________________________________;
2
②KAl(SO ):__________________________________________________________________;
4 2
③CH COOH:_________________________________________________________________;
3
④H CO:____________________________________________________________________;
2 3⑤Cu(OH) :___________________________________________________________________;
2
⑥NaHSO 溶于水:______________________________________________________________;
4
⑦NaHSO 熔融:________________________________________________________________;
4
⑧NaHCO :___________________________________________________________________。
3
⑨[Al(OH)] 的 电 离 : 酸 式 电 离 : , 碱 式 电 离 :
3
。
【答案】 ①Ba(OH) ===Ba2++2OH-
2
② KAl(SO )===K++Al3++2SO
4 2
③ CHCOOH CH COO-+H+
3 3
④ H CO H++HCO、HCO H++CO
2 3
⑤ Cu(OH) Cu2++2OH-
2
⑥NaHSO ===Na++H++SO
4
⑦NaHSO (熔融)===Na++HSO
4
⑧NaHCO ===Na++HCO、HCO H++CO
3
⑨Al(OH) +HO [Al(OH) ]- + H+ Al(OH) Al3++3OH-
3 2 4 3
三、导电能力
导电能力与电荷、浓度、温度有关。
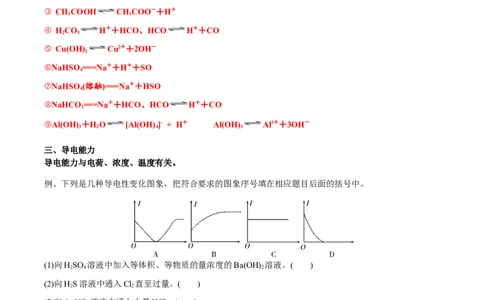
例、下列是几种导电性变化图象,把符合要求的图象序号填在相应题目后面的括号中。
(1)向HSO 溶液中加入等体积、等物质的量浓度的Ba(OH) 溶液。( )
2 4 2
(2)向HS溶液中通入Cl 直至过量。( )
2 2
(3)向AgNO 溶液中通入少量HCl。( )
3
(4)向NaOH溶液中通入少量Cl。( )
2
(5)向氨水中通入HCl直至过量。( )
【答案】(1)D(2)B(3)C(4)C(5)B
【概念辨析】
1、离子化合物都是强电解质,共价化合物部分属于强电解质,部分属于弱电解质( )
2、Cl 、SO 、NH 的水溶液均导电,故Cl 、SO 、NH 均为电解质( )
2 2 3 2 2 3
3、在熔融状态下能导电的物质一定为电解质( )4、BaSO 的水溶液的导电性很弱,故它是弱电解质。( )
4
5、NaCl溶液在电流的作用下电离成钠离子和氯离子( )
6、强电解质溶液的导电性一定比弱电解质的强( )
7、能导电的物质不一定是电解质( )
8、0.1 mol·L-1 NaCl溶液与0.1 mol·L-1 CaCl 溶液的导电性相同( )
2
9、溶解度小的物质的导电性一定比溶解度大的物质的导电性弱( )
10、固态共价化合物不导电,熔融态的共价化合物可以导电( )
【答案】 1.√ 2.× 3.× 4.× 5.× 6.× 7.√ 8.× 9.× 10.×
【跟踪练习】
1、(2022·浙江6月选考,2)下列物质属于强电解质的是( )
A.HCOOH B.Fe C.NaCO D.C H
2 3 2 2
【答案】 C
2、目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的
电解质成分。下列物质可用作该饮料中的电解质的是( )
A.Fe B.葡萄糖 C.MgSO D.CO
4 2
【答案】 C
3、(2022·北京卷)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其中太空
“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是( )
A.醋酸钠是强电解质 B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的 D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
【答案】B
4、下列说法正确的是( )
A.CO 的水溶液能导电,所以CO 是电解质
2 2
B.BaSO 难溶于水,其水溶液的导电能力极弱,所以BaSO 的电离方程式为BaSO Ba2++SO
4 4 4
C.液溴不导电,所以溴是非电解质
D.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
【答案】 D
【解析】 因为CO +HO HCO ,HCO 电离出H+和HCO从而使溶液导电,而不是CO 自身电离,
2 2 2 3 2 3 2
因此HCO 是电解质,CO 是非电解质,A错误;电解质强弱的划分是根据其电离的程度,而不是根据其
2 3 2
溶解度的大小,BaSO 溶解度很小,但溶于水的BaSO 完全电离,所以BaSO 是强电解质,不能用“
4 4 4
”,B错误;电解质和非电解质都是化合物,液溴是单质,C错误;电解质导电能力的强弱与溶液中自由
移动的离子的浓度大小以及所带的电荷多少有关,所以强电解质溶液的导电能力不一定比弱电解质溶液的
导电能力强,D正确。5、某离子化合物MCl(s)在水中溶解并发生电离,该过程的微观示意图如图。已知N 为阿伏加德罗常数的
A
值。下列相关说法正确的是( )
A.1 mol MCl中含有N 个共用电子对 B.MCl为弱电解质,在水中仅部分电离
A
C.M+和Cl-均与水分子中的氧原子结合形成水合离子 D.MCl在水作用下的溶解和电离过程是物理变
化
【答案】 D
【解析】 MCl为离子化合物,通过阴、阳离子之间的静电作用形成化学键,不存在共用电子对,故 A错
误;MCl为离子化合物,故MCl为强电解质,在水中完全电离,故B错误;M+带正电荷,与水分子中显
负电性的氧原子结合形成水合离子,Cl-带负电荷,与水分子中显正电性的氢原子结合形成水合离子,故
C错误;MCl在水作用下的溶解和电离过程中没有新物质生成,是物理变化,故D正确。
6、将等浓度的H SO 、NaHSO 溶液,分别滴入两份相同的Ba(OH) 溶液中,其电导率与滴入溶液体积
2 4 4 2
变化的曲线如图所示。下列分析正确的是( )
A.b→d反应的离子方程式为H++OH-===H O
2
B.d点溶液中,Na+与SO 2-的物质的量之比为1∶1
4
C.c点导电能力相同,所以两溶液中含有相同量的OH-
D.a、b两点Ba2+均沉淀完全,所以对应的溶液均显中性
【答案】A
【解析】Ba(OH) 溶液和HSO 、NaHSO 溶液反应的化学方程式分别为HSO +Ba(OH) ===BaSO ↓+
2 2 4 4 2 4 2 4
2HO,NaHSO +Ba(OH) === BaSO ↓+NaOH+HO、2NaHSO +Ba(OH) ===BaSO ↓+Na SO +
2 4 2 4 2 4 2 4 2 4
2HO,溶液导电能力与离子浓度成正比,根据图知,曲线①在a点溶液电导率接近0,说明该点溶液离子
2
浓度最小,应该为Ba(OH) 和HSO 的反应,则曲线②为Ba(OH) 和NaHSO 的反应。b→d反应为向
2 2 4 2 4
NaOH溶液中继续滴加NaHSO 溶液,实际上是酸碱中和反应,离子方程式为H++OH-===H O,故A项
4 2
正确;d点时溶质为Na SO ,根据化学式知,Na+与SO 2-的物质的量之比为2∶1,故B项错误;c点,①中
2 4 4
稀硫酸过量,溶质为硫酸,②中溶质为NaOH、Na SO ,则该点两种溶液中氢氧根离子浓度不同,故C项
2 4
错误;a点液体为纯水,b点溶质为NaOH,所以a点呈中性,b点呈碱性,故D项错误。
7、电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。如
图是KOH溶液分别滴定HCl溶液和CHCOOH溶液的滴定曲线示意图。下列示意图中,能正确表示用
3
NH ·H O溶液滴定HCl和CHCOOH混合溶液的滴定曲线的是( )
3 2 3【答案】 D
【解析】 HCl为强电解质,CH COOH为弱电解质,滴加NH ·HO,先与HCl反应,生成同样为强电解
3 3 2
质的NH Cl,但溶液体积不断增大,溶液稀释,所以电导率下降;当HCl被中和完后,继续与CH COOH
4 3
反应,生成CH COONH ,为强电解质,所以电导率增大;HCl与CH COOH均反应完后,继续滴加弱电
3 4 3
解质NH ·HO,电导率变化不大,因为溶液被稀释,有下降趋势。
3 2