文档内容
阶段检测卷一 基本概念
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.(2024·陕西安康高新中学高三5月模拟考试最后一卷)生活中处处有化学。下列叙述错误的是
A.农业生产中,氯化铵和草木灰不能一起使用
B.熟石膏常用于古陶瓷修复,熟石膏的主要成分为
C.水果罐头中添加的抗坏血酸、奶粉中添加的硫酸锌都属于营养强化剂
D.《本草纲目》中记载“凡酸坏之酒,皆可蒸烧”,“蒸烧”时发生了物理变化
【答案】C
【解析】氯化铵溶液中的 水解而使其呈酸性,草木灰的主要成分为碳酸钾, 水解而使碳酸钾溶液
呈碱性,二者水解互相促进,生成氨气,会降低肥效,所以农业生产中,氯化铵和草木灰不能一起使用,
A项正确;熟石膏的主要成分为 ,B项正确;水果罐头中添加的抗坏血酸属于抗氧化剂,不
属于营养强化剂,C项错误;文中“酸坏”是指少量乙醇被氧化为乙酸,乙酸和乙醇的沸点不同,用蒸馏
操作进行分离,所以“蒸烧”过程发生了物理变化,D项正确。
2.我国古代曾用反应Cu S+O=====SO +2Cu制铜,并最早发明了青铜器的铸造技术。下列说法不正确
2 2 2
的是( )
A.青铜是铜的一种合金
B.O 和O 是氧元素的同素异形体
2 3
C.Cu S只作还原剂
2
D.该反应属于置换反应
【答案】C
【解析】该反应中Cu S中Cu元素化合价降低,S元素化合价升高,所以既是氧化剂又是还原剂。
2
3.(2024·贵州贵阳清华中学高三5月模拟预测)下列有关方程式错误的是
A.利用 水解制备 :
B.铅蓄电池放电时正极反应:
C. 溶液滴入 溶液中:D.用醋酸和淀粉-KI溶液检验加碘盐中的 :
【答案】D
【解析】TiCl 加入水中发生水解反应可以制备TiO,反应的离子方程式为TiCl +
4 2 4
(x+2)HO=TiO⋅xHO↓+4H++4Cl-,A正确;原电池正极得电子,铅酸电池放电时正极PbO 得电子转化为
2 2 2 2
PbSO ,正极反应式为PbO +2e-+4H++ =PbSO+2H O,B正确;K[Fe(CN) 溶液滴入FeCl 溶液中生成
4 2 4 2 3 6] 2
KFe[Fe(CN) ]蓝色沉淀,反应的离子方程式为K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ],C正确;醋酸是弱酸,书
6 6 6
写离子方程式时不能拆为离子形式,正确的离子方程式为 +5I-+6CH COOH=3I +3H O+6CHCOO-,D错
3 2 2 3
误。
4.磁流体是电子材料的新秀。在一定条件下,将含等物质的量的FeSO 和Fe (SO ) 的溶液混合,再滴入
4 2 4 3
稍过量的NaOH溶液,可得到分散质粒子直径大小在36~55 nm之间的黑色磁流体。下列说法中正确的是(
)
A.所得的分散系属于悬浊液
B.用一束光照射该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe O,不能透过滤纸
2 3
D.分散系为胶体,分散质粒子大小即Fe(OH) 分子直径大小
3
【答案】B
【解析】由题意磁流体分散系分散质粒子直径,知该分散系属于胶体,能产生丁达尔效应。
5.(2024·广东佛山高三普通高中教学质量检测)部分含Mg或含Al物质的类别与化合价关系如图所示。
下列推断不合理的是
A.a不能与 反应生成d或g
B.b和e均可用于制造耐高温材料
C.可存在a→f→g→e→a的循环转化关系D.直接加热蒸干c或f溶液无法得到无水氯化物
【答案】A
【解析】由图知,a为Al或Mg,b为MgO,e为Al O,c为MgCl ,f为AlCl ,d为Mg(OH) ,g为
2 3 2 3 2
Al(OH) 。Mg能与 在加热条件下反应生成Mg(OH) ,A错误;MgO和Al O 均可用于制造耐高温材
3 2 2 3
料,B正确;存在Al→AlCl →Al(OH) →Al O→Al的循环转化关系,C正确;由于MgCl 或AlCl 均会水
3 3 2 3 2 3
解,生成的氯化氢易挥发,直接加热蒸干MgCl 或AlCl 溶液无法得到无水氯化物,D正确。
2 3
6.下列说法正确的是( )
A.煤的气化、液化是物理变化,煤的干馏是化学变化
B.C 、液氯是单质,HD、干冰是化合物,NO 是酸性氧化物
60 2
C.烟、雾属于胶体,能产生丁达尔效应
D.可用热的饱和碳酸钠溶液除去金属表面的石蜡
【答案】C
【解析】A项,煤的气化、液化和干馏都是化学变化;B项,C 、液氯、HD都是单质,NO 不是酸性氧
60 2
化物;D项,石蜡是多种烃的混合物,与热的饱和碳酸钠溶液不反应,故不能用热的饱和碳酸钠溶液除去
金属表面的石蜡。
7.(2024·陕西铜川王益中学高三模拟)设 为阿伏加德罗常数的值。下列说法正确的是
A.16.9g过氧化钡 固体中阴、阳离子总数为
B. 个氢氧化铁胶体粒子的质量是107g
C. 的烃分子中含有 共价键的数目一定为
D.常温下, 的醋酸溶液中含有的氢离子数为
【答案】A
【解析】16.9g过氧化钡物质的是为0.1mol,固体中阴、阳离子共0.2mol,总数为 ,A项正确;一个
氢氧化铁胶粒是多个氢氧化铁的聚集体,则N 个氢氧化铁胶粒中含有的氢氧化铁的物质的量多于1mol,
A
质量也大于107g,B项错误;不确定该物质为环烷烃还是不饱和烃,不能计算其 共价键的数目,C
项错误;没有给出醋酸溶液的体积,无法计算出氢离子数目,D项错误。
8.(2023·辽宁大连一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是( )
选 离子组 加(或 判断和分析项 通)入
试剂
A NH+ 、Ba2+、Cl−、NO− 足量 能大量共存
4 3
CO
2
B Na+、Mg2+、Cl−、HCO− 足量 不 能 大 量 共 存 , 只 发 生 下 列 反 应 :
3
NaOH Mg2++HCO−+OH− MgCO ↓+H O
溶液 3 3 2
C Na+、K+、Cl−、 足量 不能大量共存,因[Al(OH) ] − 和HCO− 之间会发
4 3
[Al(OH) ] − NaHCO 3生相互促进的水解反应生成CO 气体和Al(OH)
4 2 3
溶液
沉淀
D Na+、K+、ClO−、SO2− 少量SO 不能大量共存,只发生下列氧化还原反应:
4 2
ClO−+H O+SO Cl−+SO2−+2H+
2 2 4
【答案】A
【解析】 、 、 、 之间不反应,能够大量共存,通入足量 也不反应,能够大量共
NH+ Ba2+ Cl− NO− CO
4 3 2
存, 正确;生成的碳酸镁与氢氧化钠溶液反应生成更难溶的氢氧化镁, 错误; 和
A B [Al(OH) ] − HCO−
4 3
之间反应生成氢氧化铝沉淀和碳酸根离子, 和 发生的不是相互促进的水解反应, 错
[Al(OH) ] − HCO− C
4 3
误; 、 、 、 之间不反应能够共存,通入少量 后先发生氧化还原反应
Na+ K+ ClO− SO2− SO
4 2
ClO−+H O+SO Cl−+SO2−+2H+,然后H+ 与ClO− 结合生成HClO,D错误。
2 2 4
9.(2023·广东佛山期末)现有两等份含有酚酞的Ba(OH) 溶液,分别滴加稀硫酸、Na SO 溶液,滴加
2 2 4
速率始终相同,测得溶液的电导率随时间变化如图所示。下列说法正确的是( )
A. b曲线对应Ba(OH) 溶液与Na SO 溶液的反应
2 2 4
B. 稀硫酸和Na SO 溶液的浓度相同
2 4C. a曲线电导率减小过程中,溶液由红色变为无色
D. a曲线对应的反应中OH−数目一直在减少
【答案】B
【解析】H SO 和Ba(OH) 反应生成H O 和BaSO ,溶液中离子浓度减小,导电率减小,恰好反应
2 4 2 2 4
时溶液中几乎不存在自由移动的离子,导电率几乎为零;继续滴加稀硫酸,稀硫酸过量又存在自由移动的
、 ,溶液的导电率增大;滴加 溶液过程中生成 ,溶液一直能导电,故 、 分别为
H+ SO2− Na SO NaOH b a
4 2 4
滴加稀硫酸、Na SO 溶液的曲线。由分析可知,A错误;由题图可知,曲线的突变点时间相同,则稀硫
2 4
酸和Na SO 溶液的浓度相同,B正确;a曲线对应Ba(OH) 溶液与Na SO 溶液的反应,反应生成的
2 4 2 2 4
NaOH 为强碱,溶液一直为红色,C错误;a曲线对应的反应中OH− 不参与反应,OH−数目一直不变,
D错误。
10.(2024·重庆万州第二高级中学高三高考适应性考试)一定条件下,下列各项中的物质按如图所示的箭
头不能实现一步转化的是
甲 丙 乙
选
甲 乙 丙 丁
项
A NaOH溶液 CO NaCO 溶液 NaHSO 溶液
2 2 3 4
B SiO C CO Fe
2 2
C HS SO S O
2 2 2
D 氨水 AlCl Al(OH) 盐酸
3 3
【答案】B
【解析】氢氧化钠与少量二氧化碳反应生成碳酸钠和水,碳酸钠与硫酸氢钠反应生成硫酸钠、二氧化碳和
水,均能一步实现,A不符合题意;二氧化硅与碳在高温条件下反应生成硅和CO,且CO 和铁也不反
2
应,不能实现一步转化,B符合题意;氢硫酸与二氧化硫反应生成硫和水,S与O 反应生成SO ,均能实
2 2
现一步转化,C不符合题意;氨水与氯化铝反应生成氢氧化铝沉淀和氯化铵,氢氧化铝与盐酸反应生成氯
化铝,均能实现一步转化,D不符合题意。
11.(2024·浙江五校联盟高三3月联考)在溶液中能大量共存的离子组是
A. 的 溶液:B. 的 溶液:
C. 的 溶液:
D. 的 溶液:
【答案】D
【解析】 和 因发生彻底的双水解而不能大量共存,A错误; 三种离子会发生氧
化还原反应而不能大量共存,B错误; 与 反应生成Fe [Fe(CN) ] 蓝色沉淀,C错误;各种离
4 6 3
子之间均不反应,可大量共存,D正确。
12.(2024·重庆荣昌永荣中学校高三模拟)黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所
示。下列说法错误的是
A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为
C.反应Ⅱ的离子方程式为
D.该过程的总反应为
【答案】A
【解析】反应I的离子方程式为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,反应Ⅲ的离子方程式为Fe2+
2 2
+NO=Fe(NO)2+,反应Ⅱ的离子方程式为FeS+14Fe3++8H O=15Fe2++2 +16H+。反应I、Ⅱ是氧化还原反
2 2
应;反应Ⅲ,无元素化合价变化,为非氧化还原反应,A错误;反应I的离子方程式为4Fe(NO)2++O +4H+=4Fe3++4NO+2HO,氧化剂与还原剂的物质的量之比为 ,B正确;反应Ⅱ的离子方程式为
2 2
,C正确;该过程的总反应为
,D正确。
13.(2024·江西南昌高三5月模拟)已知皓矾的化学式可表示为ZnSO·7H O,受热易分解。取28.70 g
4 2
ZnSO·7H O晶体,加热过程中所得固体质量与温度的变化关系如图所示。则下列说法不正确的是( )
4 2
A.A点时物质成分为ZnSO·H O
4 2
B.B点时ZnSO·7H O中的结晶水全部失去
4 2
C.C点时物质成分为ZnO(SO )
3 4 2
D.从B点到D点,总反应方程式一定为ZnSO=====ZnO+SO ↑
4 3
【答案】D
【解析】28.70 g ZnSO ·7H O的物质的量为0.1 mol,根据图示可知,A点时,质量变为17.90 g,质量损失
4 2
10.80 g,A点温度为100 ℃,损失的可能为结晶水,物质的量为 0.6 mol,则A点物质的化学式应为
ZnSO·H O,A项正确;随着温度继续升高,当晶体中的结晶水全部失去时,剩余固体的质量为17.90 g-
4 2
0.1 mol×18 g·mol-1=16.10 g,即B点,B项正确;随着温度升高,ZnSO 开始分解,分解过程中,Zn元素
4
的质量保持不变,最终全部转化为ZnO,质量应为0.1 mol×81 g·mol-1=8.10 g,即D点,可见C点时物质
成分既有ZnO又有ZnSO ,设ZnO为x mol,则ZnSO 为(0.1-x)mol,81x+161×(0.1-x)=13.43,解得
4 4
x≈0.033,则n(ZnO)∶n(ZnSO)≈1∶2,C点物质的化学式为ZnO·2ZnSO ,也可写作ZnO(SO ),C项正确;从
4 4 3 4 2
B点到D点,发生的反应为ZnSO 分解产生ZnO,既可能发生反应ZnSO=====ZnO+SO ↑,还可能发生
4 4 3
反应2ZnSO=====2ZnO+2SO ↑+O↑,D项错误。
4 2 2
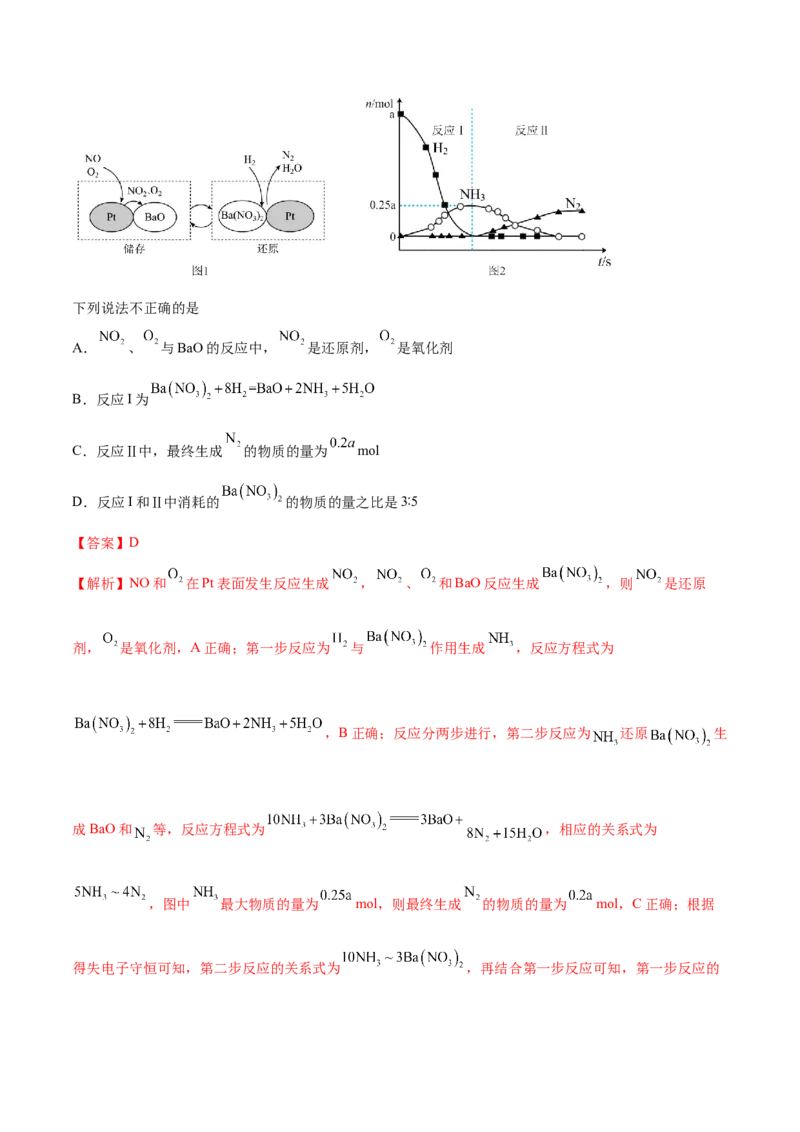
14.(2024·湖南长沙雅礼中学高三模拟)在Pt-BaO催化下,NO的“储存-还原”过程如图1所示。其中
“还原”过程依次发生反应I和反应Ⅱ,各气体的物质的量变化如图2所示。下列说法不正确的是
A. 、 与BaO的反应中, 是还原剂, 是氧化剂
B.反应I为
C.反应Ⅱ中,最终生成 的物质的量为 mol
D.反应I和Ⅱ中消耗的 的物质的量之比是3∶5
【答案】D
【解析】NO和 在Pt表面发生反应生成 , 、 和BaO反应生成 ,则 是还原
剂, 是氧化剂,A正确;第一步反应为 与 作用生成 ,反应方程式为
,B正确;反应分两步进行,第二步反应为 还原 生
成BaO和 等,反应方程式为 ,相应的关系式为
,图中 最大物质的量为 mol,则最终生成 的物质的量为 mol,C正确;根据
得失电子守恒可知,第二步反应的关系式为 ,再结合第一步反应可知,第一步反应的关系式为 ,则反应Ⅰ和Ⅱ中消耗的 的物质的量之比是5∶3,D错误。
15.(2024·湖南天壹名校联盟高三4月大联考)锡在材料、医药、化工等方面有广泛的应用,锡精矿
(SnO )中主要有Fe、S、As、Sb、Pb等杂质元素。下图为锡的冶炼工艺流程:
2
已知:SnO 性质稳定,难溶于酸。下列说法错误的是
2
A.焙烧产生的烟尘、烟气中主要杂质元素是S、As、Sb
B.酸浸时,PbO生成 ,为了提高铅的浸出率,可添加适量NaCl固体
C. 的反应2中S元素化合价全部升高
D.电解精炼时,电源的正极与粗锡相连
【答案】C
【解析】锡精矿 中主要有Fe、S、As、Sb、Pb等杂质元素,焙烧时Fe、S、As、Sb、Pb杂质元素
转化为氧化物,焙烧后加入稀盐酸溶解,由于 性质稳定,难溶于酸,过滤得到 ,再使用焦炭还
原 得到粗锡,最后电解精炼得到精锡。焙烧时Fe、S、As、Sb、Pb杂质元素转化为氧化物,由题可
知,加入稀盐酸后的滤液经过处理得到Fe和Pb,所以烟尘、烟气中的主要杂质元素是S、As、Sb,A正
确;酸浸时,PbO生成 ,离子方程式为 ,浸出过程中添加氯化
钠,可促使氯化铅转化成可溶性的离子,提高其浸出效果,B正确;PbS与熔融NaOH反应的化学方程式
为 ,S元素化合价只有部分升高,C错误;电解精炼时,
与电源的正极相连的是粗锡,D正确。
二、非选择题(本题包括4小题,共55分)
16.(10分)(1)1 mol NO 与HO充分反应,转移________ mol e-。
2 2(2)2Na O+2HO===4NaOH+O↑,每产生1 mol 氧气转移________ mol e-。
2 2 2 2
(3)已知将过氧化钠加入硫酸亚铁盐溶液中发生反应:4Fe2++4NaO +6HO===4Fe(OH) ↓+O↑+8Na+,
2 2 2 3 2
每4 mol Na O 发生反应转移______mol e-。
2 2
(4)向0.2 L 1 mol·L-1的FeBr 溶液中通入0.2 mol Cl 充分反应,被氧化的Br-为______mol。
2 2
【答案】(1)(2分)
(2)2(2分)
(3)6(3分)
(4)0.2(3分)
【解析】(1)根据3NO +HO===2HNO +NO反应,1 mol NO 反应转移电子为1××2 mol e-。(2)中NaO 中
2 2 3 2 2 2
的氧由-1到-2、0价,故每生成1 mol O 转移2 mol e-。(3)化合价升高总数:4Fe2+―→4Fe3+,化合价升
2
高4,对于4 mol Na O ,其中1 mol Na O 中的氧由-1到0价,化合价升高2,总数为6;化合价降低总
2 2 2 2
数:3 mol Na O 中的氧由-1到-2价,降低总数为6,所以每4 mol Na O 发生反应转移6 mol电子。
2 2 2 2
(4)Cl 先氧化Fe2+再氧化Br-,根据电子守恒,被氧化的Br-为0.2×2 mol-0.2×1 mol=0.2 mol。
2
17.(10分)标准状况下,在乙室中充入1.2 mol HCl,甲室中充入NH 、H 的混合气体,静止时活塞如
3 2
图。已知甲室中气体的质量比乙室中气体的质量少33.8 g。
请回答下列问题:
(1)甲室中气体的物质的量为________ mol。
(2)甲室中气体的质量为________ g。
(3)甲室中NH 、H 的物质的量之比为________,质量之比为________。
3 2
(4)如果将活塞a去掉,当HCl与NH 完全反应后,活塞b将静止于刻度“________”(填数字)处。
3
【答案】(1)2(2分)
(2)10(2分)
(3)1∶4(2分)17∶8(2分)
(4)6(2分)
【解析】(1)由题图可知甲、乙两室气体的体积之比为5∶3,故其物质的量之比也为5∶3,所以甲室中气体为
2 mol。(2)HCl气体的质量为1.2 mol×36.5 g·mol-1=43.8 g,则甲室中气体的质量为43.8 g-33.8 g=10 g。
(3)设氨气的物质的量为x,氢气的物质的量为y,根据其物质的量、质量列方程组为
解得x=0.4 mol,y=1.6 mol,所以氨气和氢气的物质的量之比=0.4 mol∶1.6 mol=1∶4,其质量之比=(0.4
mol×17 g·mol-1)∶(1.6 mol×2 g·mol-1)=17∶8。(4)甲室中NH 的物质的量为0.4 mol,能与0.4 mol HCl反应,
3
剩余气体为2.4 mol,相同条件下,气体的体积之比等于其物质的量之比,所以活塞b会移至“6”处。
18.(18分)(2024·北京首都师范大学附属中学高三考前热身)探究溶液中Ag+与单质S的反应。
资料:Ag S不溶于6mol/L盐酸,Ag SO 和Ag SO 在6mol/L盐酸中均发生沉淀的转化
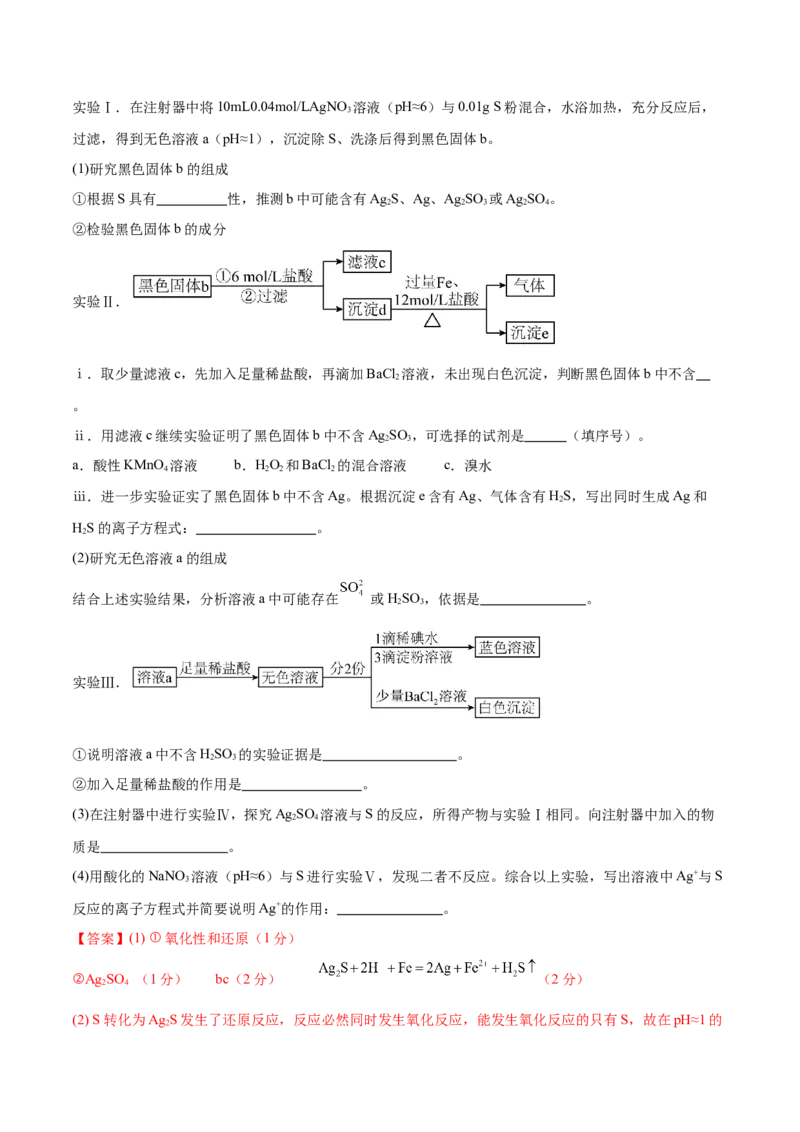
2 2 3 2 4实验Ⅰ.在注射器中将10mL0.04mol/LAgNO 溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,
3
过滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。
(1)研究黑色固体b的组成
①根据S具有 性,推测b中可能含有Ag S、Ag、Ag SO 或Ag SO 。
2 2 3 2 4
②检验黑色固体b的成分
实验Ⅱ.
ⅰ.取少量滤液c,先加入足量稀盐酸,再滴加BaCl 溶液,未出现白色沉淀,判断黑色固体b中不含
2
。
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag SO ,可选择的试剂是 (填序号)。
2 3
a.酸性KMnO 溶液 b.HO 和BaCl 的混合溶液 c.溴水
4 2 2 2
ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有HS,写出同时生成Ag和
2
HS的离子方程式: 。
2
(2)研究无色溶液a的组成
结合上述实验结果,分析溶液a中可能存在 或HSO ,依据是 。
2 3
实验Ⅲ.
①说明溶液a中不含HSO 的实验证据是 。
2 3
②加入足量稀盐酸的作用是 。
(3)在注射器中进行实验Ⅳ,探究Ag SO 溶液与S的反应,所得产物与实验Ⅰ相同。向注射器中加入的物
2 4
质是 。
(4)用酸化的NaNO 溶液(pH≈6)与S进行实验Ⅴ,发现二者不反应。综合以上实验,写出溶液中Ag+与S
3
反应的离子方程式并简要说明Ag+的作用: 。
【答案】(1) ①氧化性和还原(1分)
②Ag SO (1分) bc(2分) (2分)
2 4
(2) S转化为Ag S发生了还原反应,反应必然同时发生氧化反应,能发生氧化反应的只有S,故在pH≈1的
2溶液中可能存在 或HSO (3分)
2 3
①向溶液a中加入足量稀盐酸后,再加入碘水和淀粉溶液,蓝色不褪去 (2分)
②排除Ag+对 和HSO 检验的干扰(2分)
2 3
(3)10mL0.02mol/L Ag SO 溶液与0.01g S粉(2分)
2 4
(4) ,形成Ag S难溶物,降低c(S2-),提高S的氧化性,利于反应发
2
生(3分)
【解析】在注射器中将10mL0.04mol/LAgNO 溶液(pH≈6)与0.01g S粉混合,水浴加热,充分反应后,过
3
滤,得到无色溶液a(pH≈1),沉淀除S、洗涤后得到黑色固体b。探究无色溶液a的成分时,通过碘的淀粉
溶液的蓝色不褪去,确定不含有HSO ,通过加入BaCl 后产生白色沉淀,确定含有 ;探究沉淀b的
2 3 2
成分时,加入6mol/L盐酸,实验证实滤液c中不含有HSO 、不含有 ,表明沉淀b中不含有Ag SO 、
2 3 2 3
Ag SO ,沉淀d中加入Fe、12mol/L盐酸,有Ag和HS生成,确定b为Ag S,从而确定在AgNO 的作用
2 4 2 2 3
下,S发生歧化反应,生成Ag S、Ag SO 等。(1)①S为0价,化合价既能升高也能降低,则S具有氧
2 2 4
化性和还原性,推测b中可能含有Ag S、Ag、Ag SO 或Ag SO 。②ⅰ.取少量滤液c,先加入足量稀盐
2 2 3 2 4
酸,再滴加BaCl 溶液,未出现白色沉淀,表明未生成BaSO 沉淀,从而确定黑色固体b中不含Ag SO 。
2 4 2 4
ⅱ.用滤液c继续实验证明了黑色固体b中不含Ag SO ,也就是检验不存在HSO ,但需排除Cl-产生的干
2 3 2 3
扰,所以不能选择a.酸性KMnO 溶液(能被Cl-还原),可选择b.HO 和BaCl 的混合溶液(H SO 被HO
4 2 2 2 2 3 2 2
氧化为HSO ,再与Ba2+反应生成BaSO 沉淀)、c.溴水(H SO 还原Br ,使溴水褪色),可选择的试剂是
2 4 4 2 3 2
bc。ⅲ.进一步实验证实了黑色固体b中不含Ag。根据沉淀e含有Ag、气体含有HS,则Fe作还原剂,
2
在HCl的帮助下,将Ag S还原为Ag,同时生成HS气体,离子方程式:
2 2
。(2)S与AgNO 溶液反应后,生成Ag S,S元素的价态降低,则S
3 2
元素的价态也应升高,所以溶液a中可能存在 或HSO ,依据是:S转化为Ag S发生了还原反应,反
2 3 2
应必然同时发生氧化反应,能发生氧化反应的只有S,故在pH≈1的溶液中可能存在 或HSO 。①碘
2 3
的淀粉溶液的蓝色不褪去,确定溶液a中不含有HSO ,实验证据是:向溶液a中加入足量稀盐酸后,再
2 3加入碘水和淀粉溶液,蓝色不褪去。②Ag+能与I-、 发生反应,从而干扰后续实验,所以加入足量稀
盐酸的作用是:排除Ag+对 和HSO 检验的干扰。(3)在注射器中进行实验Ⅳ,探究Ag SO 溶液与
2 3 2 4
S的反应,所得产物与实验Ⅰ相同,此时是与实验Ⅰ做对比实验,所以S的物质的量、Ag+的浓度都应相
同,从而得出向注射器中加入的物质是10mL0.02mol/L Ag SO 溶液与0.01g S粉。(4)用酸化的NaNO 溶
2 4 3
液(pH≈6)与S进行实验Ⅴ,发现二者不反应,说明Ag+对S的歧化反应提供了帮助,由此得出溶液中Ag+与
S反应的离子方程式并简要说明Ag+的作用: ,形成Ag S难溶物,
2
降低c(S2-),提高S的氧化性,利于反应发生。
19.(17分)(2024·安徽名校教研联盟高三3月月考)某科研小组模拟在实验室条件下,用硫铁矿制备硫
酸并测定其浓度,其实验过程如图所示。
回答下列问题:
(1)硫铁矿主要成分为 (写化学式);“操作1”和“操作2” (填“相同”或“不同”)。
(2)“浸取”过程中,主要发生的反应的离子方程式为 。
(3)“氧化”过程所需的氯气,可用漂白液和浓盐酸反应制取,该制取氯气的反应中氧化剂和还原剂的物质
的量之比为 。
(4)量取上述制备的硫酸溶液 ,煮沸一段时间,冷却后,加水稀释到250mL,量取25mL配制的硫酸
溶液于锥形瓶,滴几滴 溶液,用 溶液滴定到终点,消耗 溶液 。该硫酸溶液
的浓度为 ,经过3次平行实验,发现测得的结果高于实际浓度,其原因可能是 (操作都正
确)。
【答案】(1) (2分) 不同(2分)
(2) (3分)
(3) (3分)(4)酚酞(2分) (3分) 硫酸溶液中含有盐酸(2分)
【解析】硫铁矿的主要成分为二硫化亚铁,加入饱和氯化铁溶液,三价铁离子具有强氧化性,可以将硫元
素从-1价氧化为0价,加入四氯化碳后,硫单质溶于有机相中,操作1萃取、分液后得到硫的四氯化碳溶
液,再通入氯气氧化硫单质,促使硫元素进入到水溶液的体系中,经过操作2分液后得到硫酸溶液。(1)
硫铁矿的主要成分为二硫化亚铁 ;“操作1”包含萃取和分液,“操作2”为分液操作。(2)“浸
取”过程中,饱和的 溶液和硫铁矿粉发生的主要反应的离子方程式为 。
(3)氧化过程的反应方程式为: ,参加反应的 只有一半做还原剂,
因此氧化剂和还原剂的物质的量之比为 。(4)用氢氧化钠标准溶液滴定强酸溶液,指示剂可选用酚䣭
或甲基橙;量取的 配制的硫酸溶液,其溶质的物质的量为 , 配制的硫酸溶液中
溶质的物质的量为 ,则该硫酸溶液的浓度为 。经过3次平行实
验,发现测得的结果高于实际浓度,其原因可能是硫酸溶液中含有未除净的盐酸。