文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷03
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.化学与生产、生活密切相关。下列说法错误的是
A.氯化钠、蔗糖、维生素C等物质可用于食品防腐 B.铁罐可用于储运浓硫酸
C.用热的纯碱溶液可清洗衣物上的汽油污渍 D.氢氟酸可用于雕刻石英艺术品
2.下列说法不正确的是
A.实验室宜用饱和食盐水代替水与电石反应制取乙炔
B.牺牲阳极法是利用原电池原理保护设备
C.可用 溶液鉴别苯、乙醇、乙酸
D.红外光谱可以测定有机物的元素组成及含量
3.用铜锌合金制成的黄铜制品常被误认为黄金。下列关于黄铜的说法错误的是
A.有金属光泽 B.熔点比锌高
C.硬度比铜大 D.可用稀盐酸鉴别黄铜与黄金
4.下列有关物质的性质和用途说法不正确的是
A.利用高纯单质硅的半导体性能,可以制成光电池
B.国庆节天安门广场燃放烟花,色彩绚丽,利用了某些金属元素的焰色试验
C.NaO 与CO 反应放出氧气,可用于制作呼吸面具
2 2 2
D.用氯化铁溶液刻蚀覆铜板制作印刷电路板,铜与FeCl 发生置换反应
3
5.S与Cl为同一周期元素,下列事实正确且能比较两者非金属性强弱的是
A.热稳定性: B.酸性:
C.氢化物的沸点: D.将氯气通入 溶液中,观察到有淡黄色沉淀产生6.下列有关说法正确的是
A.HCl与NaCl的晶体类型相同
B. 与 中的O—Cl—O夹角都为109°28'
C.CuCl 中Cu2+核外电子排布式为[Ar]3d9
2
D.ClO与HClO都是由极性键构成的非极性分子
2
7.我国科研人员研制了 双温区催化剂( 区域和 区域的温度差可超过 )。 双
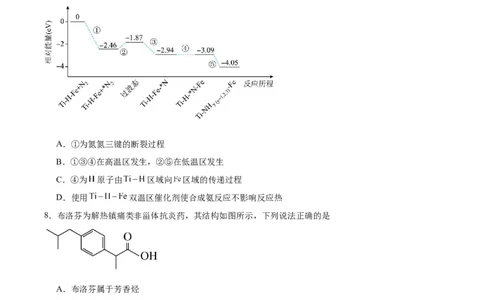
温区催化合成氨的反应历程如图所示,其中吸附在催化剂表面上的物种用*标注。下列说法正确的是
A.①为氮氮三键的断裂过程
B.①③④在高温区发生,②⑤在低温区发生
C.④为 原子由 区域向 区域的传递过程
D.使用 双温区催化剂使合成氨反应不影响反应热
8.布洛芬为解热镇痛类非甾体抗炎药,其结构如图所示,下列说法正确的是
A.布洛芬属于芳香烃
B.1mol布洛芬最多可与 加成
C.布洛芬分子中最多有12个碳原子共平面
D.布洛芬能使酸性高锰酸钾溶液褪色
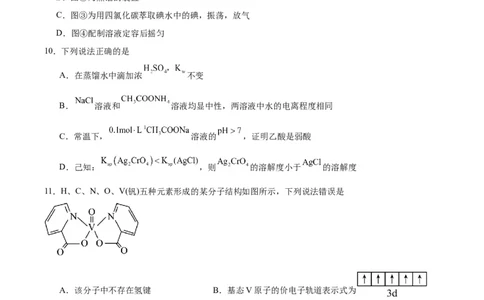
9.化学是以实验为基础的科学,下列有关仪器的使用和操作方法正确的是A.图①为实验室收集氯气的操作
B.图②为蒸馏的装置
C.图③为用四氯化碳萃取碘水中的碘,振荡,放气
D.图④配制溶液定容后摇匀
10.下列说法正确的是
A.在蒸馏水中滴加浓 不变
B. 溶液和 溶液均显中性,两溶液中水的电离程度相同
C.常温下, 溶液的 ,证明乙酸是弱酸
D.己知: ,则 的溶解度小于 的溶解度
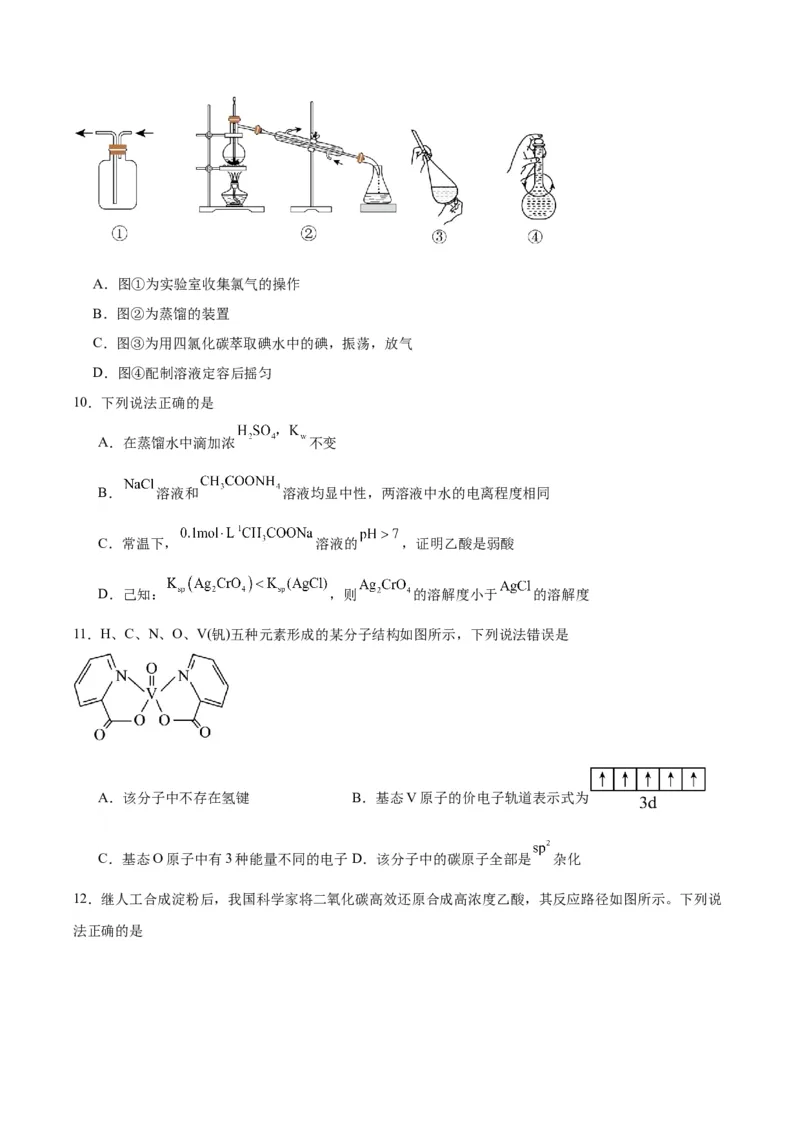
11.H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错误是
A.该分子中不存在氢键 B.基态V原子的价电子轨道表示式为
C.基态O原子中有3种能量不同的电子 D.该分子中的碳原子全部是 杂化
12.继人工合成淀粉后,我国科学家将二氧化碳高效还原合成高浓度乙酸,其反应路径如图所示。下列说
法正确的是A. 为反应的中间产物
B.第4步反应的氧化剂是
C.反应过程中碳元素的化合价始终不变
D.催化循环的总反应为
二、非选择题:本题共4小题,共64分。
13.(16分)利用光催化技术可将太阳能转化为化学能。
(1)光催化可实现 的净化
①比较N、O元素第一电离能:N O(填“>”或“小于”)。
②光催化还原 可得到 ,从结构角度分析 性质稳定的原因 。
③光催化氧化 最终产物为硝酸盐, 的空间结构是 形。
(2)光催化 和 合成甲醇是 转化利用最有前景的途径之一。比较甲醇分子中H-C-H与C-O-H的
键角大小并解释原因 。
(3)光催化可降解苯酚( )。在紫外光的作用下催化剂表面有 (羟基自由基)生成, 可将苯酚氧
化为 和 ,该反应的方程式为 。
(4)某含钛的复合型物质可作光催化剂,晶胞结构如图所示,边长均为 。①基态钛原子的价层电子轨道表示式为 。
②晶体中每个钛原子周围与其距离最近且相等的氧原子的个数是 。
③ 表示阿伏加德罗常数的值,则该晶体的密度为 。
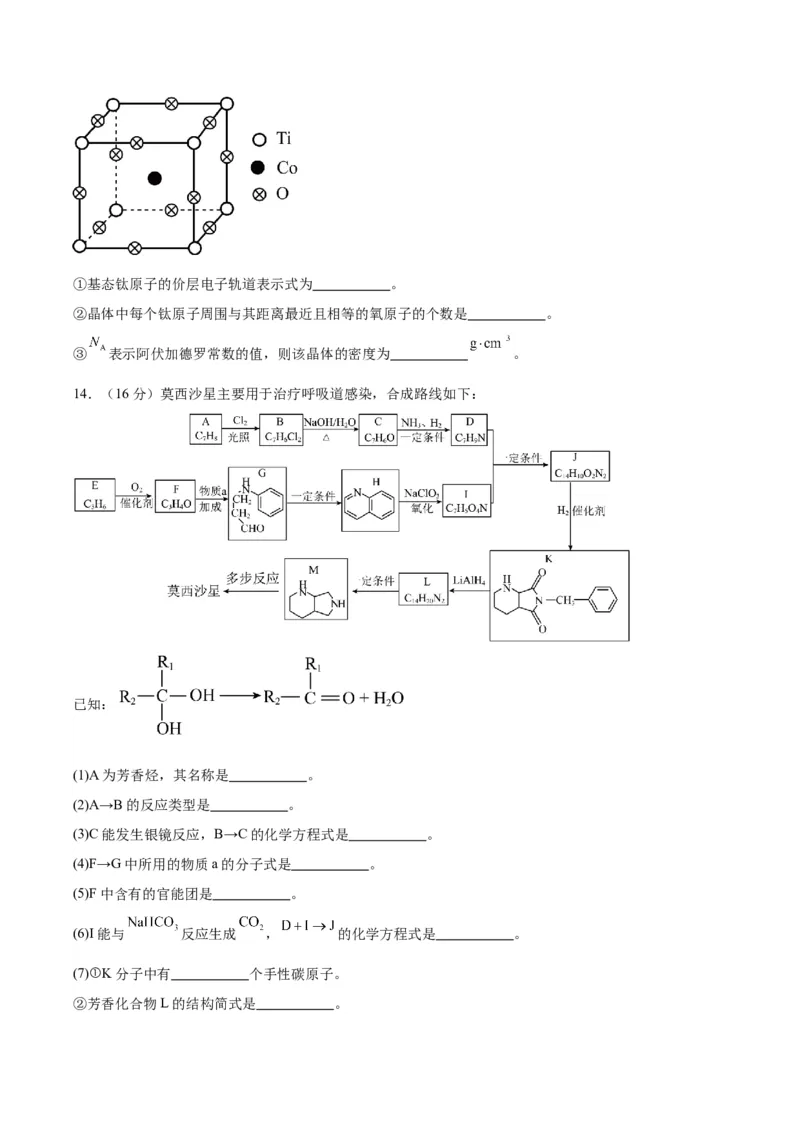
14.(16分)莫西沙星主要用于治疗呼吸道感染,合成路线如下:
已知:
(1)A为芳香烃,其名称是 。
(2)A→B的反应类型是 。
(3)C能发生银镜反应,B→C的化学方程式是 。
(4)F→G中所用的物质a的分子式是 。
(5)F中含有的官能团是 。
(6)I能与 反应生成 , 的化学方程式是 。
(7)①K分子中有 个手性碳原子。
②芳香化合物L的结构简式是 。(8)还可用A为原料,经如下“电化学氧化工艺流程”合成C,反应器中由A生成C的离子方程式是
。
15.(16分)完成下列问题。
(1) 为紫色固体,易溶于水,微溶于KOH溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶
液中较稳定,在酸性或中性溶液中快速产生 。
①A中发生反应的离子反应方程式是 。
②下列试剂中,装置B的X溶液可以选用的是 。
A.饱和食盐水 B.浓盐酸 C.饱和氯水 D. 溶液
③C中得到紫色固体和溶液,生成 的化学方程式是 ;若要从反应后的装置C中尽可能
得到更多的 固体,可以采取的一种措施是 。
(2)高铁酸钾与水反应的离子方程式是 。则其作为水处理
剂的原理是① ,② 。
(3)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。①X不能是硝酸,原因是 ,装置4的作用是 。
②实验开始时,开关 应 (填“打开”成“关闭”);这样操作的目的是 。
16.(16分)工业上以铬铁矿[主要成分为 ,杂质主要为硅和铝的氧化物]制备重铬酸钾的工艺
流程如下图所示:
已知:焙烧时 转化为 和 ,硅和铝的氧化物分别转化为 和 。
(1)写出焙烧过程中发生主要反应的化学方程式: 。
(2)“水浸”后滤渣的主要成分是 ,“中和”后滤渣的主要成分是 (填化学式)。
(3)测定 产品的纯度:称取重铬酸钾试样 配成 溶液,取出 于锥形瓶中,加
和足量碘化钾(铬的还原产物为 ),置于暗处 ,然后加入 水,加入淀粉
溶液做指示剂,用 标准溶液滴定( ),消耗标准溶液 。
①滴定终点的判断方法是 。
②该样品的纯度为 (写出计算过程)
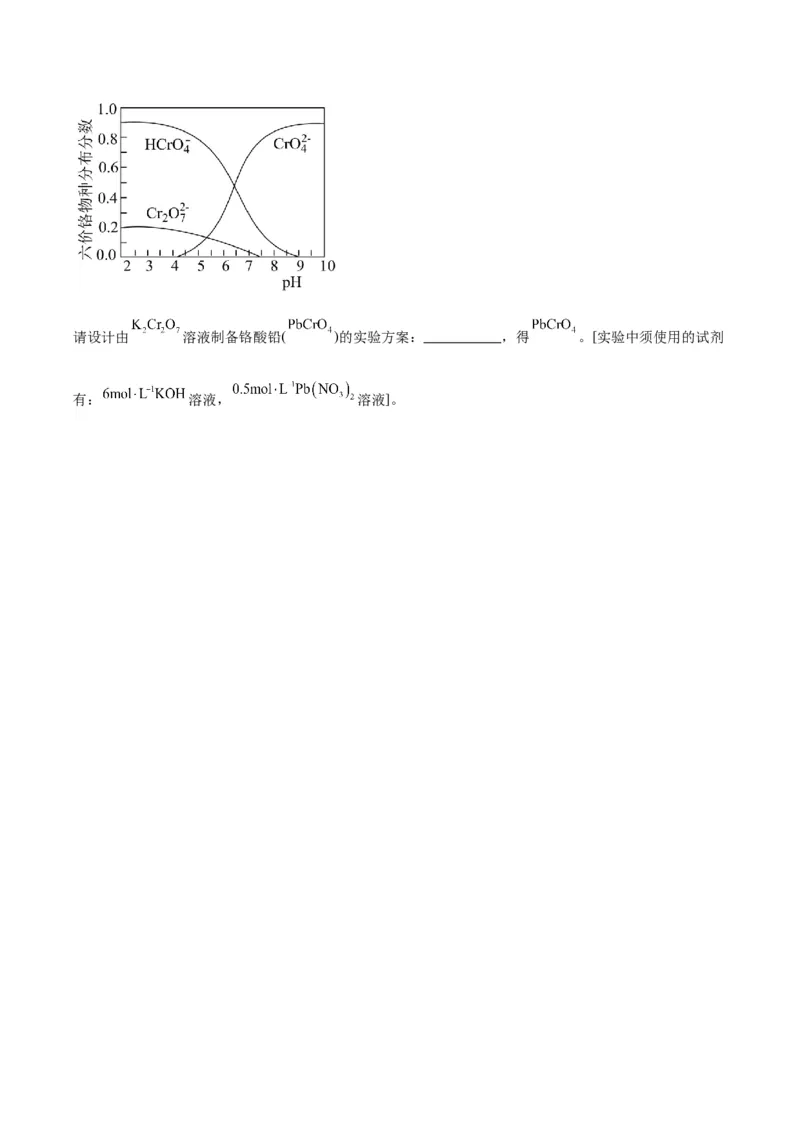
(4)铬酸铅( )是一种黄色颜料,难溶于水,可由沸腾的铬酸盐溶液与铅盐溶液反应制得。
已知:① 开始沉淀时 为7.2,完全沉淀时 为8.7。
②六价铬在溶液中物种分布分数与 关系如图所示。请设计由 溶液制备铬酸铅( )的实验方案: ,得 。[实验中须使用的试剂
有: 溶液, 溶液]。