文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷04
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、铁盐及铁的氧化物的在生活中的应用(本题共21分)
自公元前2000年开始,铁及其化合物在人类生活中有着极其重要的作用。
1. 完成下列填空:
(1)铁的原子结构示意图为 。由此可知,铁是第 周期元素,
铁原子核外3d轨道上共填充了 个电子。
(2)古代中国四大发明之一的司南是由天然的磁石制成的,其主要成分是 (选填编号)。
a.Fe b.FeO c.Fe O d.Fe O
2 3 3 4
(3)FeSO 可以用来净水、治疗缺铁性贫血等,实验室在配制FeSO 溶液时,为了防止FeSO
4 4 4
变质,经常向溶液中加入铁粉,其原因是 (用离子方程式表示)。
(4)向新配制的FeSO 溶液中,加入一定量的稀硝酸,发生如下反应:
4
_______Fe2++_______H++_______NO =_______Fe3++_______NO↑+_______HO
− 2
❑
3
①配平上述反应 。
②每生成0.5molNO气体,转移的电子数为 。
③要检验该反应后的溶液中是否还含有Fe2+,实验方案是 。
现在可以利用铁氧化物循环裂解水制备氢气,其过程如图所示:
(5)写出反应Ⅲ的平衡常数表达式 。
(6)写出铁氧化物循环裂解水制氢的总反应的化学方程式: 。
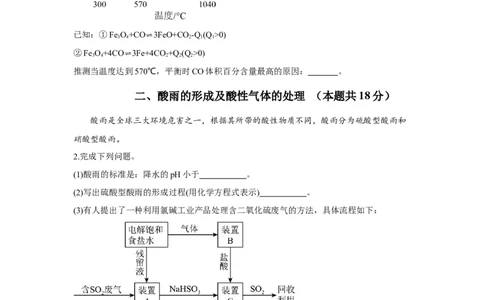
(7)Fe O 和CO的反应过程与温度密切相关。向某容器中加入Fe O 与CO,当其它条件一定
3 4 3 4
时,达到平衡时CO的体积百分含量随温度的变化关系如图所示。已知:①Fe
3
O
4
+CO⇌3FeO+CO
2
-Q
1
(Q
1
>0)
②Fe
3
O
4
+4CO⇌3Fe+4CO
2
+Q
2
(Q
2
>0)
推测当温度达到570℃,平衡时CO体积百分含量最高的原因: 。
二、酸雨的形成及酸性气体的处理 (本题共18分)
酸雨是全球三大环境危害之一,根据其所带的酸性物质不同,酸雨分为硫酸型酸雨和
硝酸型酸雨。
2.完成下列问题。
(1)酸雨的标准是:降水的pH小于 。
(2)写出硫酸型酸雨的形成过程(用化学方程式表示) 。
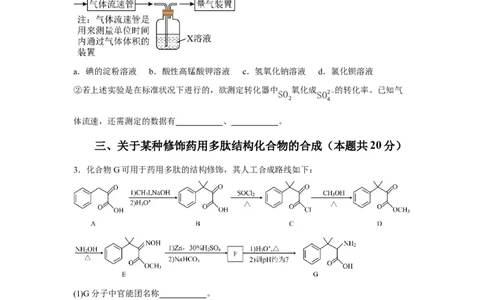
(3)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,具体流程如下:
①写出装置C中反应的离子方程式 。
②该流程中可以循环利用的物质是 (填写化学式)。
(4)还有学者提出利用 、 等离子的催化作用,常温下将 氧化成 而实现 的
Fe2+ Fe3+ SO SO2− SO
2 4 2
回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO 氧化
2
成 的转化率。
SO2−
4①该小组采用下图装置在实验室测定模拟烟气中SO 的体积分数,X溶液可以是
2
(选填字母)。
a.碘的淀粉溶液 b.酸性高锰酸钾溶液 c.氢氧化钠溶液 d.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中 氧化成 的转化率。已知气
SO SO2−
2 4
体流速,还需测定的数据有 、 。
三、关于某种修饰药用多肽结构化合物的合成(本题共20分)
3.化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)G分子中官能团名称 。
(2)A→B的反应类型为 ,E→F过程1)的反应类型为
(3)D中碳原子的杂化类型有 。
(4)写出C→D的化学方程式 。
(5)F的分子式为C H NO ,其结构简式为 。
12 17 2
(6)A的同分异构体中满足下列条件的有 种。
①遇FeCl 溶液呈紫色 ②能发生水解 ③苯环上含两个取代基,且不含其它环
3
写出其中核磁共振氢谱有6个峰,且峰面积之比为2:2:1:1:1:1的分子的结构简式。
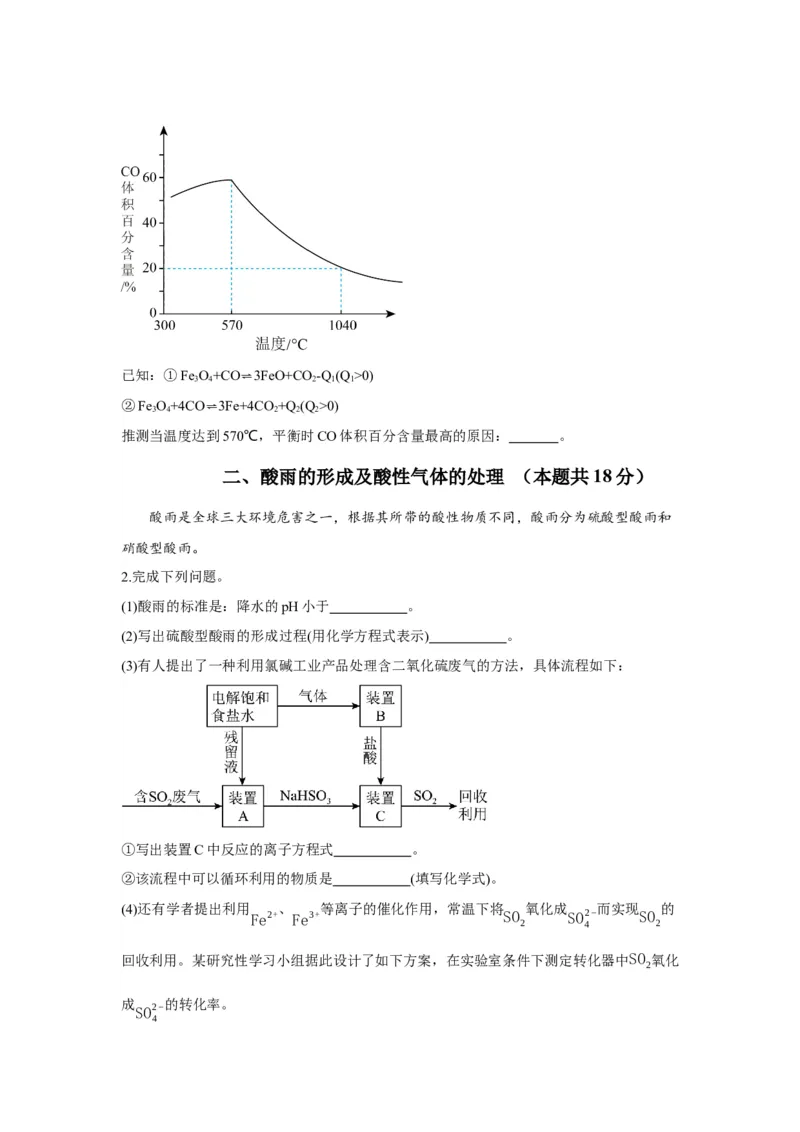
(7)药物结构的修饰有助于新药的开发与利用。青蒿素可以获得双氢青蒿素,其变化过程示
意图如下。下列说法不正确的是
A.若试剂①为NaH,其还原产物为H O
2
B.青蒿素中存在过氧键,具有强氧化性
C.该过程若有1mol青蒿素完全转化,则转移2mol电子
D.羟基的引入使得双氢青蒿素分子拥有更多修饰与改造的可能
四、金属钠及其化合物(本题共22分)
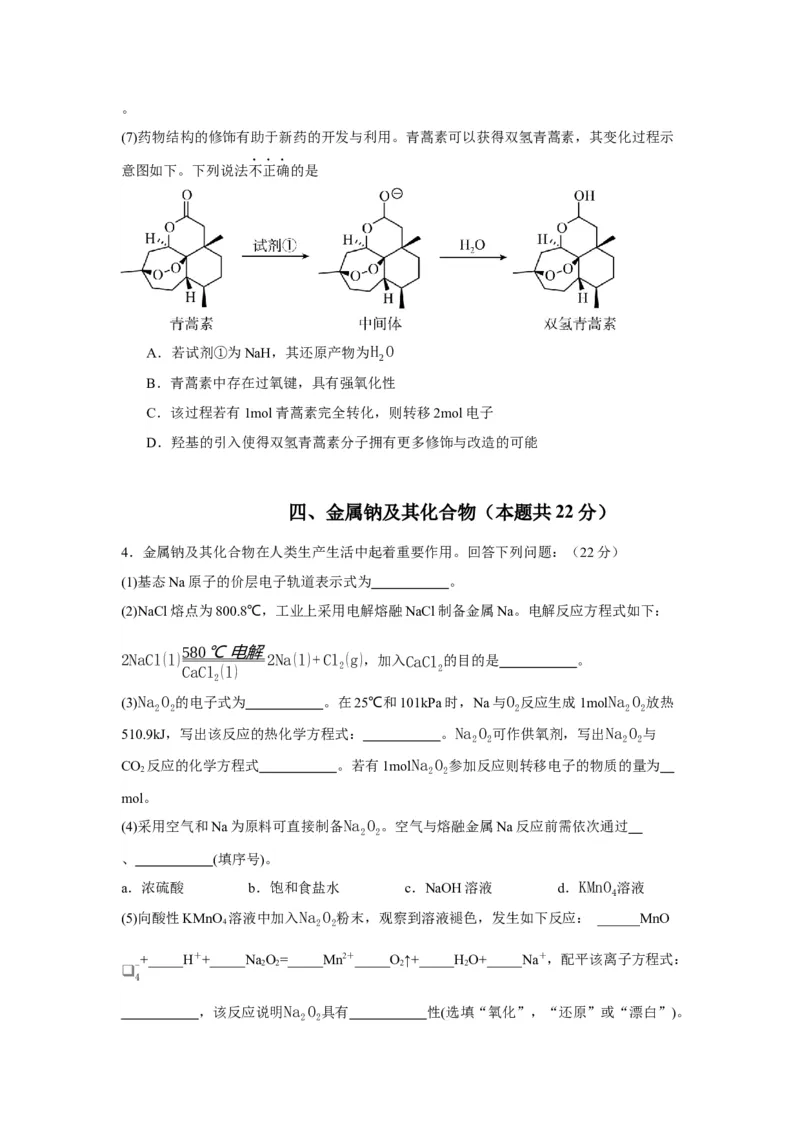
4.金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:(22分)
(1)基态Na原子的价层电子轨道表示式为 。
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:
580℃电解
2NaCl(l) 2Na(l)+Cl (g),加入CaCl 的目的是 。
CaCl (l) 2 2
2
(3)Na O 的电子式为 。在25℃和101kPa时,Na与O 反应生成1molNa O 放热
2 2 2 2 2
510.9kJ,写出该反应的热化学方程式: 。Na O 可作供氧剂,写出Na O 与
2 2 2 2
CO 反应的化学方程式 。若有1molNa O 参加反应则转移电子的物质的量为
2 2 2
mol。
(4)采用空气和Na为原料可直接制备Na O 。空气与熔融金属Na反应前需依次通过
2 2
、 (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO 溶液
4
(5)向酸性KMnO 溶液中加入Na O 粉末,观察到溶液褪色,发生如下反应: ______MnO
4 2 2
+_____H++_____Na O=_____Mn2+_____O↑+_____H O+_____Na+,配平该离子方程式:
- 2 2 2 2
❑
4
,该反应说明Na O 具有 性(选填“氧化”,“还原”或“漂白”)。
2 2(6)钠的某氧化物晶胞如下图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的
化学式为 。
(7)天然碱的主要成分为Na CO ⋅NaHCO ⋅2H O,1molNa CO ⋅NaHCO ⋅2H O经充分加
2 3 3 2 2 3 3 2
热得到Na CO 的质量为 g。
2 3
五、叠氮化纳的合成(本题共19分)
叠氮化钠(NaN )是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要应用。学
习小组对叠氮化钠₃的制备和产品纯度测定进行相关探究。(19分)
5. 查阅资料:
I.氨基钠(NaNH₂)熔点为208°C,易潮解和氧化;N₂O有强氧化性,不与酸、碱反应;
NaN₃易溶于水,叠氮酸(HN₃)不稳定,易分解爆炸;+2价锡具有较强的还原性。
II.
2HNO +8HCl+4SnCl =4SnCl +5H O+N O↑,2NaN H +N O≜NaN +NaOH+N H
3 2 4 2 2 2 2 3 3
回答下列问题:
(1)制备NaN₃
② 按气流方向,上述装置合理的连接顺序为 (填仪
器接口字母)。
②D的作用为 。
③C处充分反应后,停止加热,为防止倒吸,需继续进行的操作为
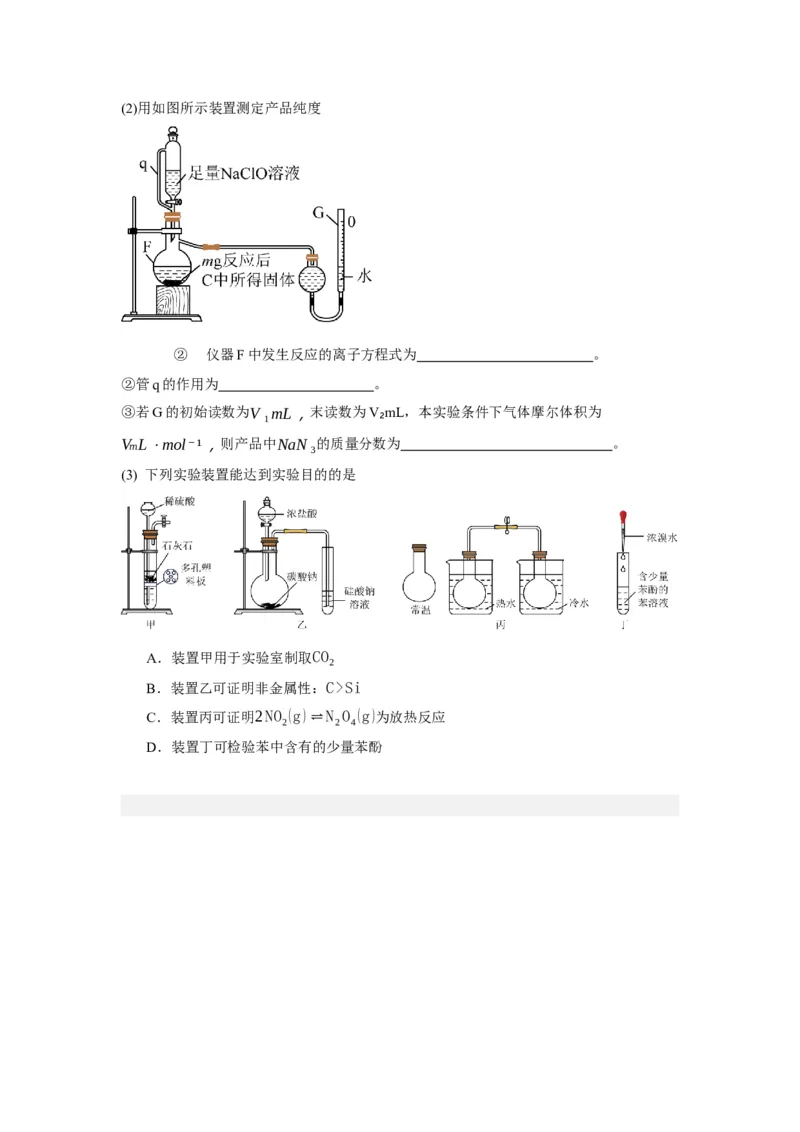
;E中SnCl₂溶液的作用是 。(2)用如图所示装置测定产品纯度
② 仪器F中发生反应的离子方程式为 。
②管q的作用为 。
③若G的初始读数为V ₁mL,末读数为V₂mL,本实验条件下气体摩尔体积为
VₘL⋅mol⁻¹,则产品中NaN₃的质量分数为 。
(3) 下列实验装置能达到实验目的的是
A.装置甲用于实验室制取CO
2
B.装置乙可证明非金属性:C>Si
C.装置丙可证明2NO (g)⇌ N O (g)为放热反应
2 2 4
D.装置丁可检验苯中含有的少量苯酚