文档内容
大题突破练(三) 化学反应原理综合题
1.(2024·广东大亚湾区1月联合模拟)某课题组研究CO 加氢制甲醇。涉及的主要反应有:
2
反应Ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-48.3 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
反应Ⅲ:CO (g)+4H(g) CH(g)+2HO(g)
2 2 4 2
ΔH=-154.8 kJ·mol-1
3
反应Ⅳ:CO(g)+2H (g) CHOH(g) ΔH
2 3 4
回答下列有关问题:
(1)反应Ⅳ的ΔH= 。
4
(2)下列有关说法正确的是 。
A.增压时,CO的物质的量分数一定增大
B.当甲醇的分压不再改变时,体系达到平衡
C.在恒容密闭容器中充入Ar,反应Ⅲ速率不变
D.升温时,反应Ⅱ逆反应速率加快的程度大于正反应速率
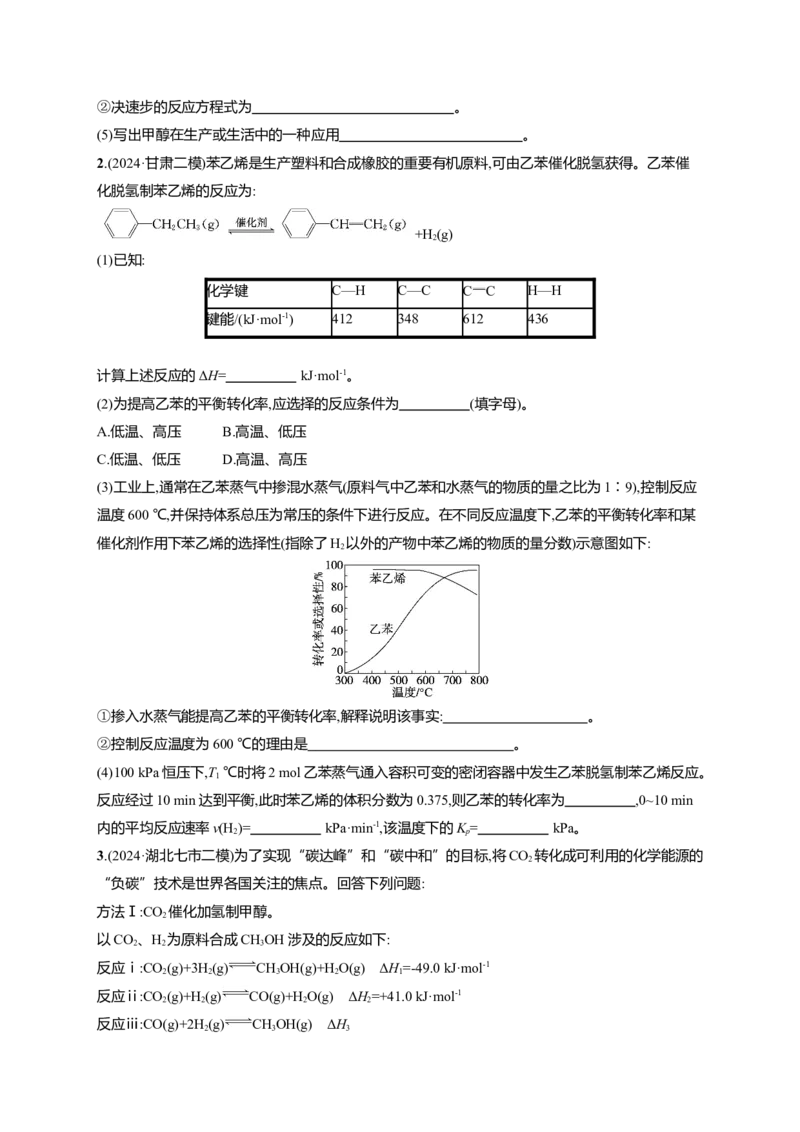
(3)研究发现,在3 MPa条件下,当起始n(CO)∶n(H )=1∶3,平衡时CO 的转化率、含碳产物的选择性
2 2 2
生成CH OH的量
3
(转化的CO 中生成CHOH、CH 或CO的百分比,如甲醇的选择性= ×100%)与
2 3 4 消耗CO 的量
2
温度关系如图所示。
①随着温度升高,甲醇选择性降低而CO 的转化率却升高的原因可能是
2
。
②在T温度下,若CH 的选择性为10%,计算此温度下反应Ⅱ的平衡常数K= 。
4
(4)一种在铜基催化剂上CO 加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用
2
“*”标注。
①基态铜原子的价电子排布式为 。②决速步的反应方程式为 。
(5)写出甲醇在生产或生活中的一种应用 。
2.(2024·甘肃二模)苯乙烯是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。乙苯催
化脱氢制苯乙烯的反应为:
+H (g)
2
(1)已知:
化学键 C—H C—C C C H—H
键能/(kJ·mol-1) 412 348 612 436
计算上述反应的ΔH= kJ·mol-1。
(2)为提高乙苯的平衡转化率,应选择的反应条件为 (填字母)。
A.低温、高压 B.高温、低压
C.低温、低压 D.高温、高压
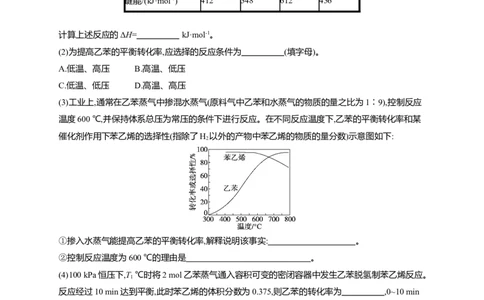
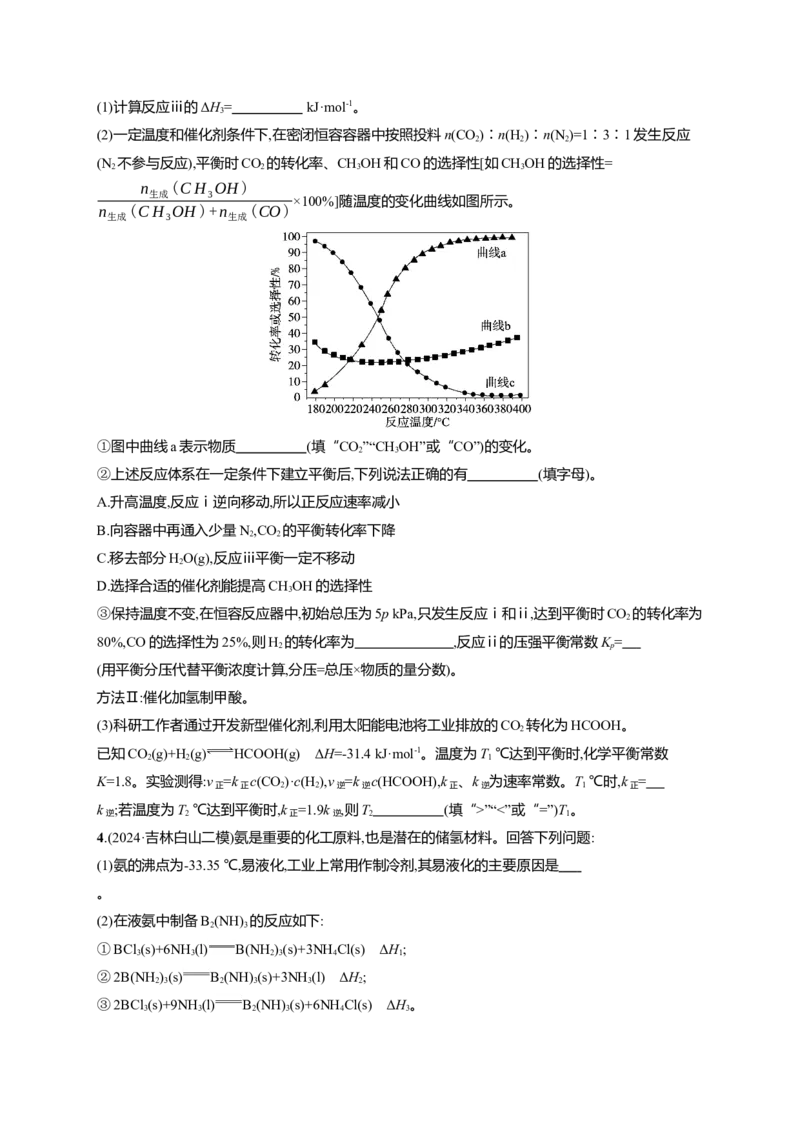
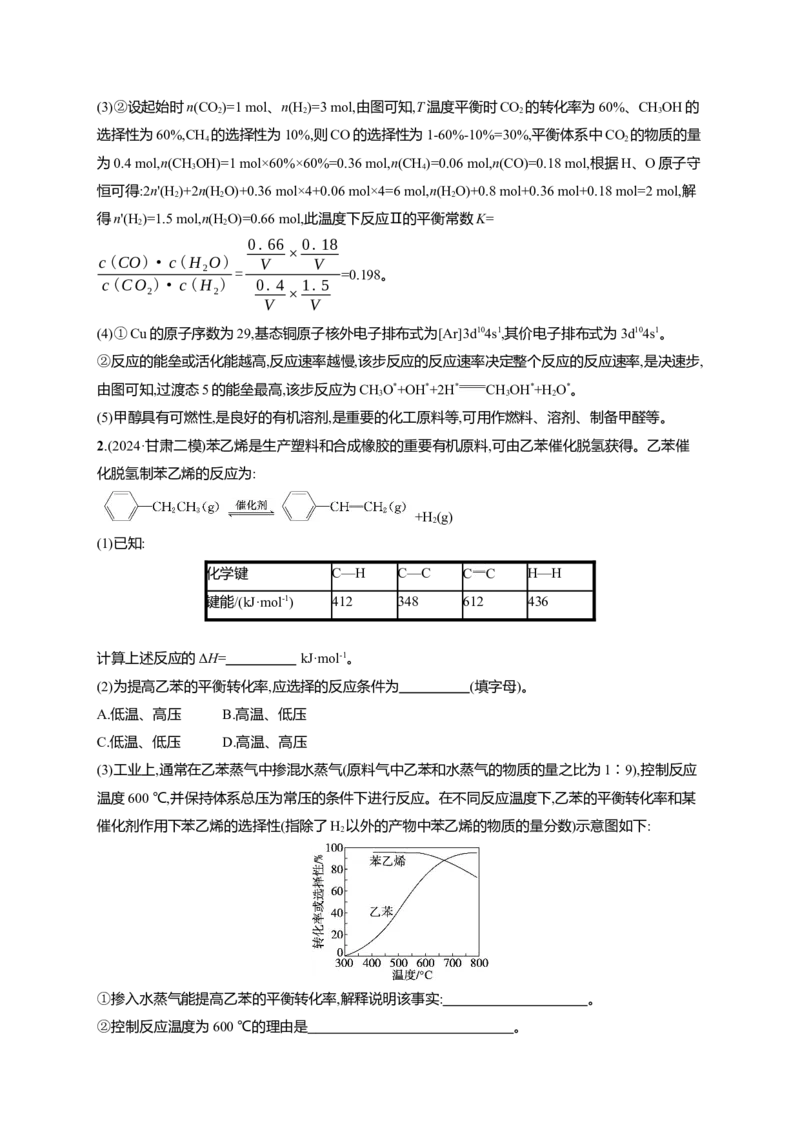
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应
温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某
催化剂作用下苯乙烯的选择性(指除了H 以外的产物中苯乙烯的物质的量分数)示意图如下:
2
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实: 。
②控制反应温度为600 ℃的理由是 。
(4)100 kPa恒压下,T ℃时将2 mol乙苯蒸气通入容积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
1
反应经过10 min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为 ,0~10 min
内的平均反应速率v(H )= kPa·min-1,该温度下的K = kPa。
2 p
3.(2024·湖北七市二模)为了实现“碳达峰”和“碳中和”的目标,将CO 转化成可利用的化学能源的
2
“负碳”技术是世界各国关注的焦点。回答下列问题:
方法Ⅰ:CO 催化加氢制甲醇。
2
以CO、H 为原料合成CHOH涉及的反应如下:
2 2 3
反应ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.0 kJ·mol-1
2 2 3 2 1
反应ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.0 kJ·mol-1
2 2 2 2
反应ⅲ:CO(g)+2H (g) CHOH(g) ΔH
2 3 3(1)计算反应ⅲ的ΔH= kJ·mol-1。
3
(2)一定温度和催化剂条件下,在密闭恒容容器中按照投料n(CO)∶n(H )∶n(N )=1∶3∶1发生反应
2 2 2
(N 不参与反应),平衡时CO 的转化率、CHOH和CO的选择性[如CHOH的选择性=
2 2 3 3
n (CH OH)
生成 3
×100%]随温度的变化曲线如图所示。
n (CH OH)+n (CO)
生成 3 生成
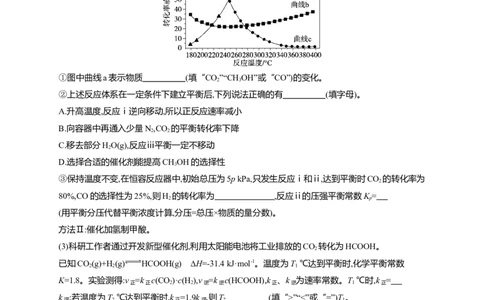
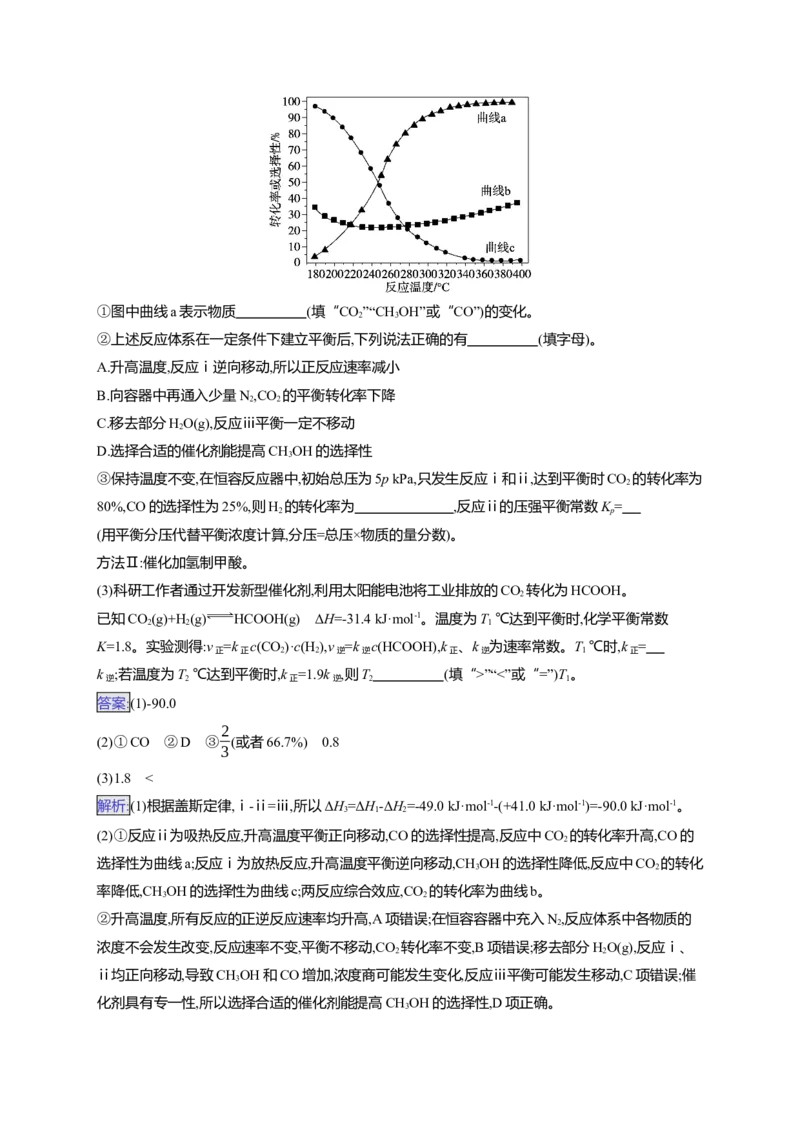
①图中曲线a表示物质 (填“CO”“CH OH”或“CO”)的变化。
2 3
②上述反应体系在一定条件下建立平衡后,下列说法正确的有 (填字母)。
A.升高温度,反应ⅰ逆向移动,所以正反应速率减小
B.向容器中再通入少量N,CO 的平衡转化率下降
2 2
C.移去部分HO(g),反应ⅲ平衡一定不移动
2
D.选择合适的催化剂能提高CHOH的选择性
3
③保持温度不变,在恒容反应器中,初始总压为5p kPa,只发生反应ⅰ和ⅱ,达到平衡时CO 的转化率为
2
80%,CO的选择性为25%,则H 的转化率为 ,反应ⅱ的压强平衡常数K =
2 p
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
方法Ⅱ:催化加氢制甲酸。
(3)科研工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为HCOOH。
2
已知CO(g)+H(g) HCOOH(g) ΔH=-31.4 kJ·mol-1。温度为T ℃达到平衡时,化学平衡常数
2 2 1
K=1.8。实验测得:v =k c(CO)·c(H ),v =k c(HCOOH),k 、k 为速率常数。T ℃时,k =
正 正 2 2 逆 逆 正 逆 1 正
k ;若温度为T ℃达到平衡时,k =1.9k ,则T (填“>”“<”或“=”)T。
逆 2 正 逆 2 1
4.(2024·吉林白山二模)氨是重要的化工原料,也是潜在的储氢材料。回答下列问题:
(1)氨的沸点为-33.35 ℃,易液化,工业上常用作制冷剂,其易液化的主要原因是
。
(2)在液氨中制备B (NH) 的反应如下:
2 3
①BCl (s)+6NH (l) B(NH )(s)+3NH Cl(s) ΔH;
3 3 2 3 4 1
②2B(NH )(s) B (NH) (s)+3NH (l) ΔH;
2 3 2 3 3 2
③2BCl (s)+9NH (l) B (NH) (s)+6NH Cl(s) ΔH。
3 3 2 3 4 3上述反应中,ΔH、ΔH、ΔH 之间等式关系为 。
1 2 3
(3)氨分解制备氢气,反应历程如图所示。
①N(g)的键能为 kJ·mol-1。
2
②写出NH 分解总反应的热化学方程式: 。
3
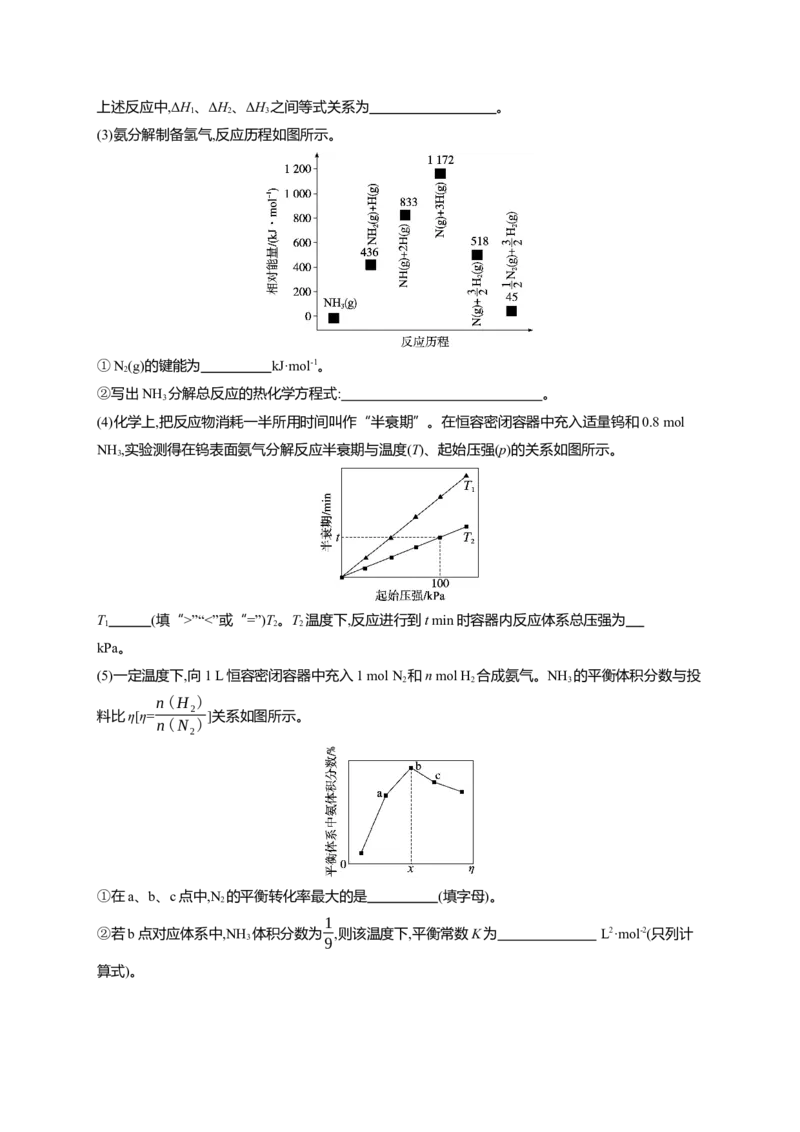
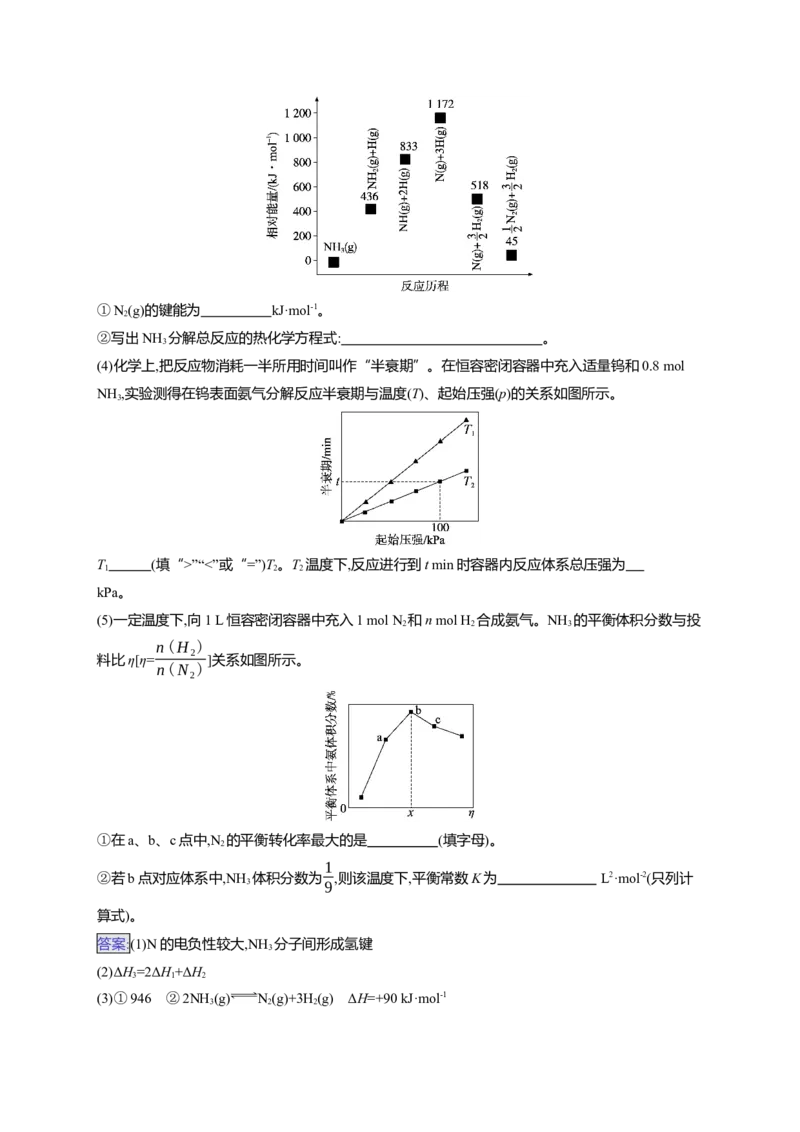
(4)化学上,把反应物消耗一半所用时间叫作“半衰期”。在恒容密闭容器中充入适量钨和0.8 mol
NH ,实验测得在钨表面氨气分解反应半衰期与温度(T)、起始压强(p)的关系如图所示。
3
T (填“>”“<”或“=”)T。T 温度下,反应进行到t min时容器内反应体系总压强为
1 2 2
kPa。
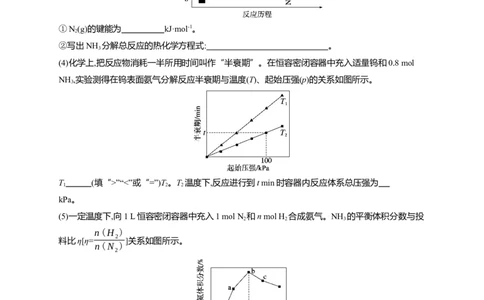
(5)一定温度下,向1 L恒容密闭容器中充入1 mol N 和n mol H 合成氨气。NH 的平衡体积分数与投
2 2 3
n(H )
2
料比η[η= ]关系如图所示。
n(N )
2
①在a、b、c点中,N 的平衡转化率最大的是 (填字母)。
2
1
②若b点对应体系中,NH 体积分数为 ,则该温度下,平衡常数K为 L2·mol-2(只列计
3 9
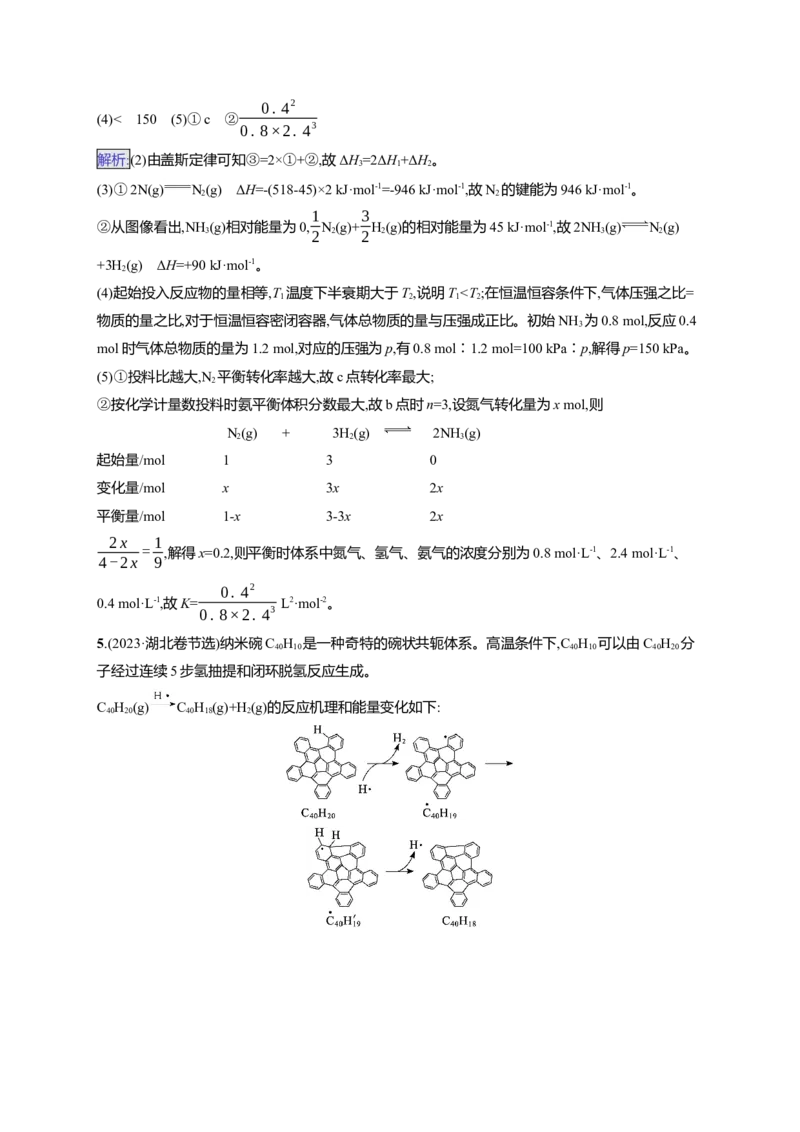
算式)。5.(2023·湖北卷节选)纳米碗C H 是一种奇特的碗状共轭体系。高温条件下,C H 可以由C H 分
40 10 40 10 40 20
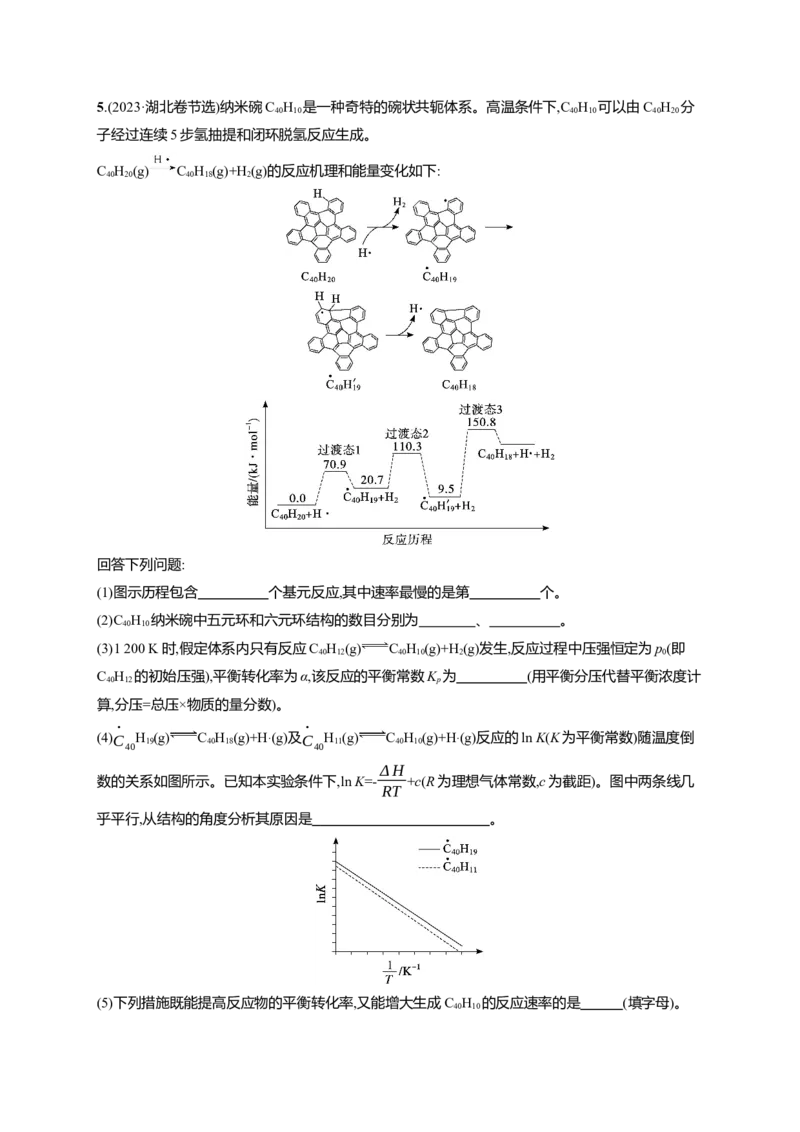
子经过连续5步氢抽提和闭环脱氢反应生成。
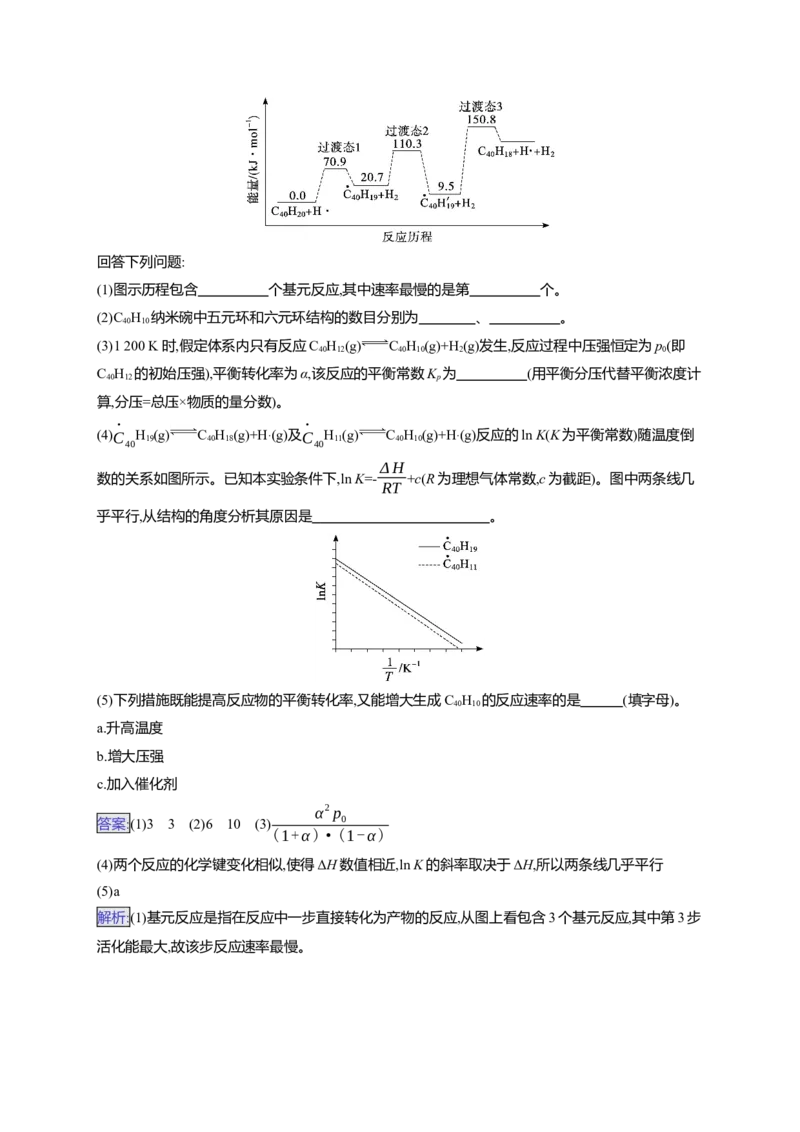
C H (g) C H (g)+H(g)的反应机理和能量变化如下:
40 20 40 18 2
回答下列问题:
(1)图示历程包含 个基元反应,其中速率最慢的是第 个。
(2)C H 纳米碗中五元环和六元环结构的数目分别为 、 。
40 10
(3)1 200 K时,假定体系内只有反应C H (g) C H (g)+H(g)发生,反应过程中压强恒定为p(即
40 12 40 10 2 0
C H 的初始压强),平衡转化率为α,该反应的平衡常数K 为 (用平衡分压代替平衡浓度计
40 12 p
算,分压=总压×物质的量分数)。
· ·
(4)C H
19
(g) C
40
H
18
(g)+H·(g)及C H
11
(g) C
40
H
10
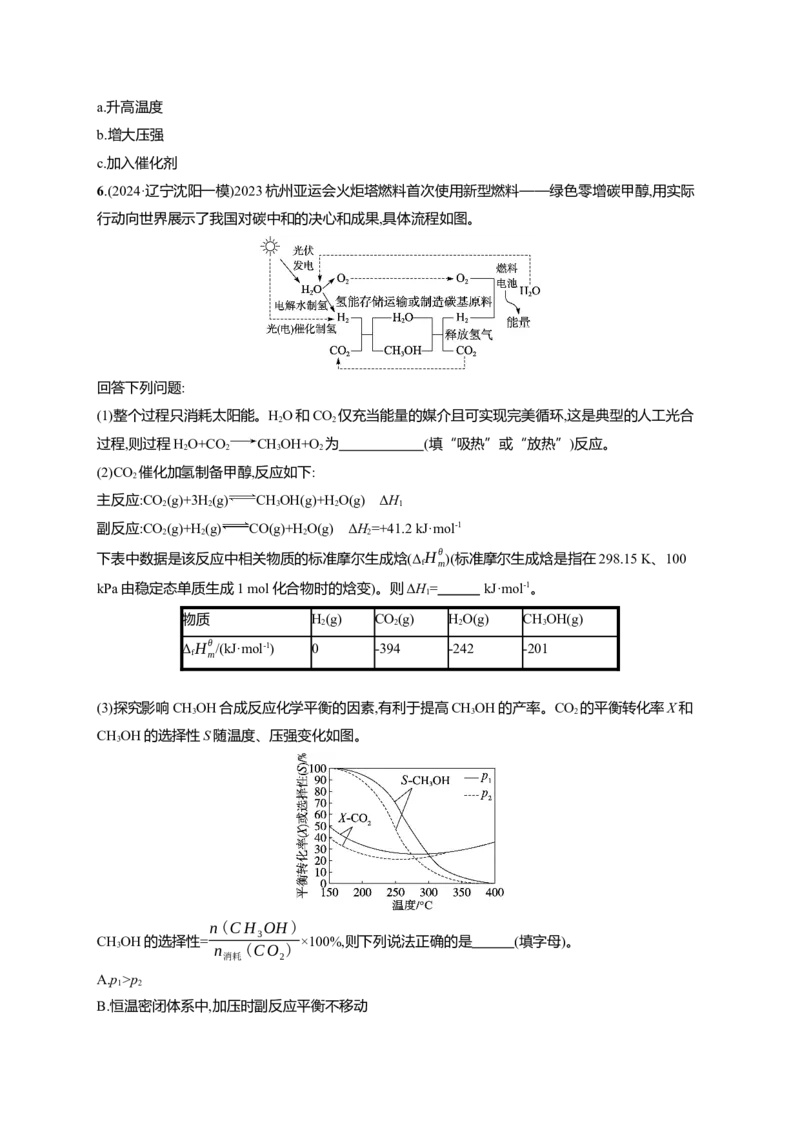
(g)+H·(g)反应的ln K(K为平衡常数)随温度倒
40 40
ΔH
数的关系如图所示。已知本实验条件下,ln K=- +c(R为理想气体常数,c为截距)。图中两条线几
RT
乎平行,从结构的角度分析其原因是 。
(5)下列措施既能提高反应物的平衡转化率,又能增大生成C H 的反应速率的是 (填字母)。
40 10a.升高温度
b.增大压强
c.加入催化剂
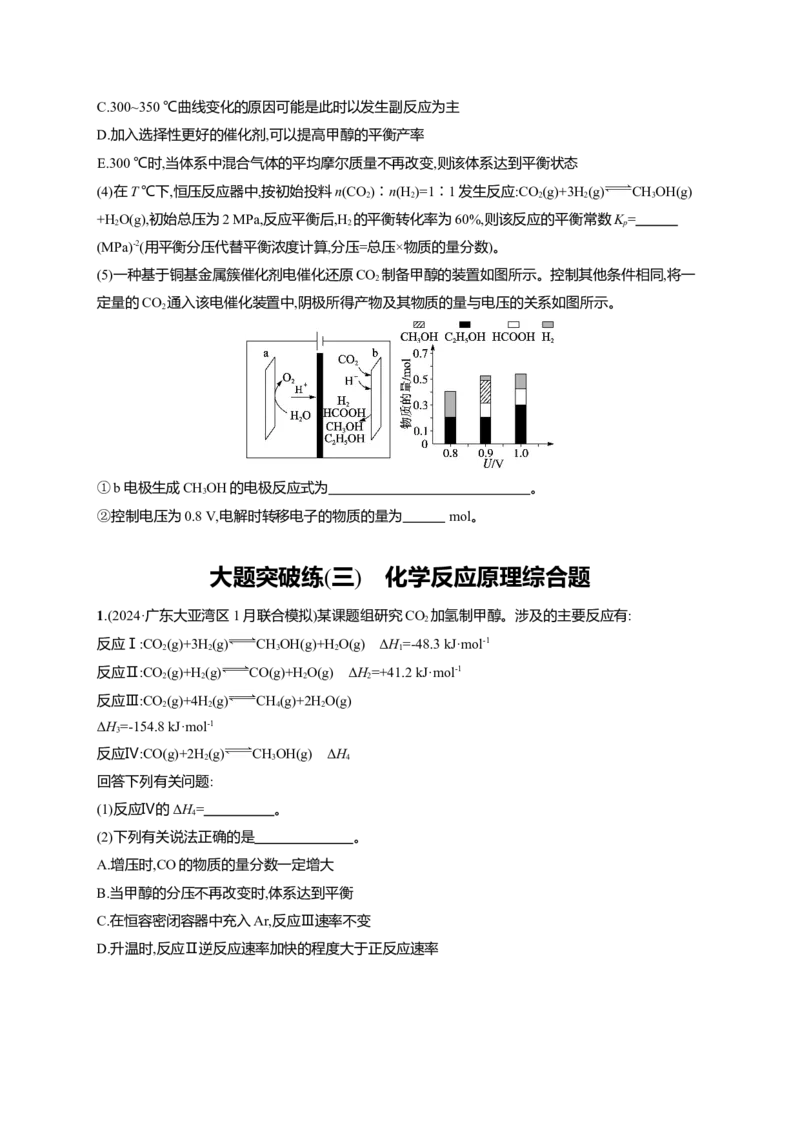
6.(2024·辽宁沈阳一模)2023杭州亚运会火炬塔燃料首次使用新型燃料——绿色零增碳甲醇,用实际
行动向世界展示了我国对碳中和的决心和成果,具体流程如图。
回答下列问题:
(1)整个过程只消耗太阳能。HO和CO 仅充当能量的媒介且可实现完美循环,这是典型的人工光合
2 2
过程,则过程HO+CO CHOH+O 为 (填“吸热”或“放热”)反应。
2 2 3 2
(2)CO 催化加氢制备甲醇,反应如下:
2
主反应:CO (g)+3H(g) CHOH(g)+H O(g) ΔH
2 2 3 2 1
副反应:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
下表中数据是该反应中相关物质的标准摩尔生成焓(ΔHθ
)(标准摩尔生成焓是指在298.15 K、100
f m
kPa由稳定态单质生成1 mol化合物时的焓变)。则ΔH= kJ·mol-1。
1
物质 H(g) CO(g) HO(g) CHOH(g)
2 2 2 3
ΔHθ /(kJ·mol-1) 0 -394 -242 -201
f m
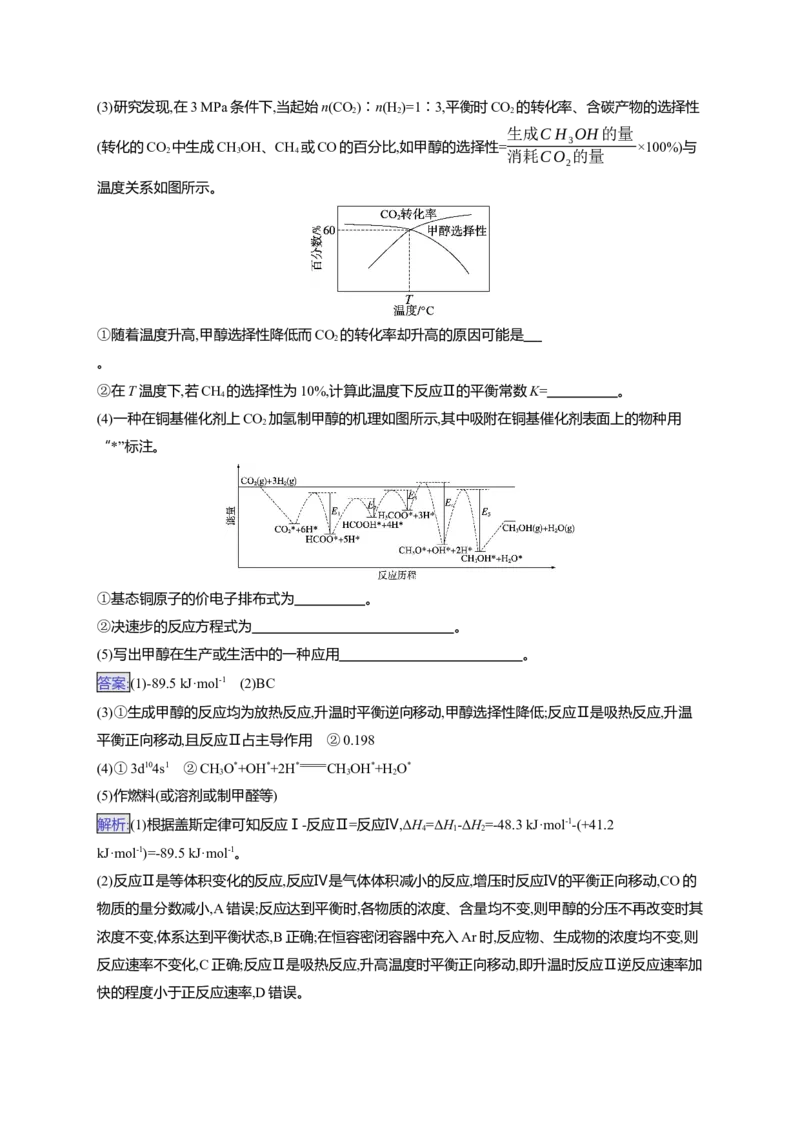
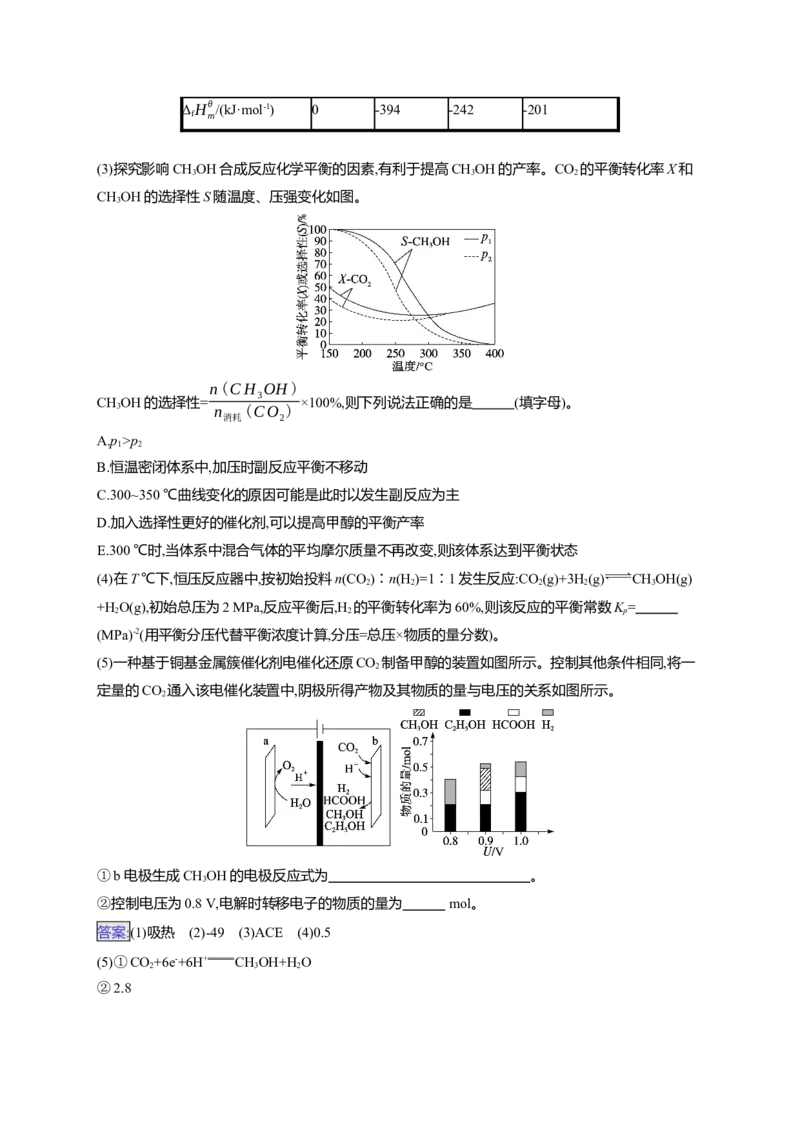
(3)探究影响CHOH合成反应化学平衡的因素,有利于提高CHOH的产率。CO 的平衡转化率X和
3 3 2
CHOH的选择性S随温度、压强变化如图。
3
n(CH OH)
3
CHOH的选择性= ×100%,则下列说法正确的是 (填字母)。
3 n (CO )
消耗 2
A.p>p
1 2
B.恒温密闭体系中,加压时副反应平衡不移动C.300~350 ℃曲线变化的原因可能是此时以发生副反应为主
D.加入选择性更好的催化剂,可以提高甲醇的平衡产率
E.300 ℃时,当体系中混合气体的平均摩尔质量不再改变,则该体系达到平衡状态
(4)在T ℃下,恒压反应器中,按初始投料n(CO)∶n(H )=1∶1发生反应:CO (g)+3H(g) CHOH(g)
2 2 2 2 3
+H O(g),初始总压为2 MPa,反应平衡后,H 的平衡转化率为60%,则该反应的平衡常数K =
2 2 p
(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)一种基于铜基金属簇催化剂电催化还原CO 制备甲醇的装置如图所示。控制其他条件相同,将一
2
定量的CO 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图所示。
2
①b电极生成CHOH的电极反应式为 。
3
②控制电压为0.8 V,电解时转移电子的物质的量为 mol。
大题突破练(三) 化学反应原理综合题
1.(2024·广东大亚湾区1月联合模拟)某课题组研究CO 加氢制甲醇。涉及的主要反应有:
2
反应Ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-48.3 kJ·mol-1
2 2 3 2 1
反应Ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2 2
反应Ⅲ:CO (g)+4H(g) CH(g)+2HO(g)
2 2 4 2
ΔH=-154.8 kJ·mol-1
3
反应Ⅳ:CO(g)+2H (g) CHOH(g) ΔH
2 3 4
回答下列有关问题:
(1)反应Ⅳ的ΔH= 。
4
(2)下列有关说法正确的是 。
A.增压时,CO的物质的量分数一定增大
B.当甲醇的分压不再改变时,体系达到平衡
C.在恒容密闭容器中充入Ar,反应Ⅲ速率不变
D.升温时,反应Ⅱ逆反应速率加快的程度大于正反应速率(3)研究发现,在3 MPa条件下,当起始n(CO)∶n(H )=1∶3,平衡时CO 的转化率、含碳产物的选择性
2 2 2
生成CH OH的量
3
(转化的CO 中生成CHOH、CH 或CO的百分比,如甲醇的选择性= ×100%)与
2 3 4 消耗CO 的量
2
温度关系如图所示。
①随着温度升高,甲醇选择性降低而CO 的转化率却升高的原因可能是
2
。
②在T温度下,若CH 的选择性为10%,计算此温度下反应Ⅱ的平衡常数K= 。
4
(4)一种在铜基催化剂上CO 加氢制甲醇的机理如图所示,其中吸附在铜基催化剂表面上的物种用
2
“*”标注。
①基态铜原子的价电子排布式为 。
②决速步的反应方程式为 。
(5)写出甲醇在生产或生活中的一种应用 。
答案:(1)-89.5 kJ·mol-1 (2)BC
(3)①生成甲醇的反应均为放热反应,升温时平衡逆向移动,甲醇选择性降低;反应Ⅱ是吸热反应,升温
平衡正向移动,且反应Ⅱ占主导作用 ②0.198
(4)①3d104s1 ②CHO*+OH*+2H* CHOH*+H O*
3 3 2
(5)作燃料(或溶剂或制甲醛等)
解析:(1)根据盖斯定律可知反应Ⅰ-反应Ⅱ=反应Ⅳ,ΔH=ΔH-ΔH=-48.3 kJ·mol-1-(+41.2
4 1 2
kJ·mol-1)=-89.5 kJ·mol-1。
(2)反应Ⅱ是等体积变化的反应,反应Ⅳ是气体体积减小的反应,增压时反应Ⅳ的平衡正向移动,CO的
物质的量分数减小,A错误;反应达到平衡时,各物质的浓度、含量均不变,则甲醇的分压不再改变时其
浓度不变,体系达到平衡状态,B正确;在恒容密闭容器中充入Ar时,反应物、生成物的浓度均不变,则
反应速率不变化,C正确;反应Ⅱ是吸热反应,升高温度时平衡正向移动,即升温时反应Ⅱ逆反应速率加
快的程度小于正反应速率,D错误。(3)②设起始时n(CO)=1 mol、n(H )=3 mol,由图可知,T温度平衡时CO 的转化率为60%、CHOH的
2 2 2 3
选择性为60%,CH 的选择性为10%,则CO的选择性为1-60%-10%=30%,平衡体系中CO 的物质的量
4 2
为0.4 mol,n(CHOH)=1 mol×60%×60%=0.36 mol,n(CH)=0.06 mol,n(CO)=0.18 mol,根据H、O原子守
3 4
恒可得:2n'(H )+2n(H O)+0.36 mol×4+0.06 mol×4=6 mol,n(H O)+0.8 mol+0.36 mol+0.18 mol=2 mol,解
2 2 2
得n'(H )=1.5 mol,n(H O)=0.66 mol,此温度下反应Ⅱ的平衡常数K=
2 2
0.66 0.18
×
c(CO)·c(H O) V V
2 = =0.198。
c(CO )·c(H ) 0.4 1.5
2 2 ×
V V
(4)①Cu的原子序数为29,基态铜原子核外电子排布式为[Ar]3d104s1,其价电子排布式为3d104s1。
②反应的能垒或活化能越高,反应速率越慢,该步反应的反应速率决定整个反应的反应速率,是决速步,
由图可知,过渡态5的能垒最高,该步反应为CHO*+OH*+2H* CHOH*+H O*。
3 3 2
(5)甲醇具有可燃性,是良好的有机溶剂,是重要的化工原料等,可用作燃料、溶剂、制备甲醛等。
2.(2024·甘肃二模)苯乙烯是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。乙苯催
化脱氢制苯乙烯的反应为:
+H (g)
2
(1)已知:
化学键 C—H C—C C C H—H
键能/(kJ·mol-1) 412 348 612 436
计算上述反应的ΔH= kJ·mol-1。
(2)为提高乙苯的平衡转化率,应选择的反应条件为 (填字母)。
A.低温、高压 B.高温、低压
C.低温、低压 D.高温、高压
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1∶9),控制反应
温度600 ℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某
催化剂作用下苯乙烯的选择性(指除了H 以外的产物中苯乙烯的物质的量分数)示意图如下:
2
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实: 。
②控制反应温度为600 ℃的理由是 。(4)100 kPa恒压下,T ℃时将2 mol乙苯蒸气通入容积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
1
反应经过10 min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为 ,0~10 min
内的平均反应速率v(H )= kPa·min-1,该温度下的K = kPa。
2 p
答案:(1)+124 (2)B
(3)①正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器容积增大,等效为降低压强,平
衡向正反应方向移动 ②600 ℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,
转化率较低,温度过高,选择性下降,高温下可能使催化剂失去活性,且消耗能量较大
(4)60% 3.75 56.25
解析:(1)反应热=反应物断键所吸收的热量-生成物成键放出能量,ΔH=2×412 kJ· mol-1+348 kJ· mol-1-
612 kJ· mol-1-436 kJ· mol-1=+124 kJ· mol-1。
(2)正反应为气体分子数增大的反应,减小压强,有利于平衡正向移动;正反应为吸热反应,升高温度,有
利于平衡正向移动,所以选择高温、低压。
(3)①正反应方向气体分子数增加,加入水蒸气起稀释作用,相当于起减压的效果,减压的条件下,平衡
正向移动,乙苯的平衡转化率增大。
(4)根据方程式 +H (g),反应经过10 min达到平
2
衡,设反应消耗的乙苯的物质的量为x mol,则剩下的乙苯为(2-x) mol,苯乙烯的体积分数为0.375=
x 1.2mol
×100%,解得x=1.2,则乙苯的转化率为 ×100%=60%;0~10 min内的平均反应
(2-x)+x+x 2mol
Δp 0.375×100 kPa p(H )·p(苯乙烯)
速率v(H )= = =3.75 kPa·min-1;该温度下的K = 2 =
2 Δt 10min p p(苯乙烷)
0.375×100 kPa×0.375×100 kPa
=56.25 kPa。
0.25×100 kPa
3.(2024·湖北七市二模)为了实现“碳达峰”和“碳中和”的目标,将CO 转化成可利用的化学能源的
2
“负碳”技术是世界各国关注的焦点。回答下列问题:
方法Ⅰ:CO 催化加氢制甲醇。
2
以CO、H 为原料合成CHOH涉及的反应如下:
2 2 3
反应ⅰ:CO (g)+3H(g) CHOH(g)+H O(g) ΔH=-49.0 kJ·mol-1
2 2 3 2 1
反应ⅱ:CO (g)+H(g) CO(g)+HO(g) ΔH=+41.0 kJ·mol-1
2 2 2 2
反应ⅲ:CO(g)+2H (g) CHOH(g) ΔH
2 3 3
(1)计算反应ⅲ的ΔH= kJ·mol-1。
3
(2)一定温度和催化剂条件下,在密闭恒容容器中按照投料n(CO)∶n(H )∶n(N )=1∶3∶1发生反应
2 2 2
(N 不参与反应),平衡时CO 的转化率、CHOH和CO的选择性[如CHOH的选择性=
2 2 3 3
n (CH OH)
生成 3
×100%]随温度的变化曲线如图所示。
n (CH OH)+n (CO)
生成 3 生成①图中曲线a表示物质 (填“CO”“CH OH”或“CO”)的变化。
2 3
②上述反应体系在一定条件下建立平衡后,下列说法正确的有 (填字母)。
A.升高温度,反应ⅰ逆向移动,所以正反应速率减小
B.向容器中再通入少量N,CO 的平衡转化率下降
2 2
C.移去部分HO(g),反应ⅲ平衡一定不移动
2
D.选择合适的催化剂能提高CHOH的选择性
3
③保持温度不变,在恒容反应器中,初始总压为5p kPa,只发生反应ⅰ和ⅱ,达到平衡时CO 的转化率为
2
80%,CO的选择性为25%,则H 的转化率为 ,反应ⅱ的压强平衡常数K =
2 p
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
方法Ⅱ:催化加氢制甲酸。
(3)科研工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO 转化为HCOOH。
2
已知CO(g)+H(g) HCOOH(g) ΔH=-31.4 kJ·mol-1。温度为T ℃达到平衡时,化学平衡常数
2 2 1
K=1.8。实验测得:v =k c(CO)·c(H ),v =k c(HCOOH),k 、k 为速率常数。T ℃时,k =
正 正 2 2 逆 逆 正 逆 1 正
k ;若温度为T ℃达到平衡时,k =1.9k ,则T (填“>”“<”或“=”)T。
逆 2 正 逆 2 1
答案:(1)-90.0
2
(2)①CO ②D ③ (或者66.7%) 0.8
3
(3)1.8 <
解析:(1)根据盖斯定律,ⅰ-ⅱ=ⅲ,所以ΔH=ΔH-ΔH=-49.0 kJ·mol-1-(+41.0 kJ·mol-1)=-90.0 kJ·mol-1。
3 1 2
(2)①反应ⅱ为吸热反应,升高温度平衡正向移动,CO的选择性提高,反应中CO 的转化率升高,CO的
2
选择性为曲线a;反应ⅰ为放热反应,升高温度平衡逆向移动,CH OH的选择性降低,反应中CO 的转化
3 2
率降低,CH OH的选择性为曲线c;两反应综合效应,CO 的转化率为曲线b。
3 2
②升高温度,所有反应的正逆反应速率均升高,A项错误;在恒容容器中充入N,反应体系中各物质的
2
浓度不会发生改变,反应速率不变,平衡不移动,CO 转化率不变,B项错误;移去部分HO(g),反应ⅰ、
2 2
ⅱ均正向移动,导致CHOH和CO增加,浓度商可能发生变化,反应ⅲ平衡可能发生移动,C项错误;催
3
化剂具有专一性,所以选择合适的催化剂能提高CHOH的选择性,D项正确。
3③投料n(CO)∶n(H )∶n(N )=1∶3∶1,假设初始物质的量分别为1 mol、3 mol、1 mol,因为发生反
2 2 2
应ⅰ和ⅱ,达到平衡时CO 的转化率为80%,CO的选择性为25%,所以共反应掉CO 的物质的量为0.8
2 2
mol,生成CO物质的量为0.8 mol×25%=0.2 mol,根据C守恒,生成CHOH物质的量为0.6 mol。列三
3
段式:
CO(g) + 3H (g) CHOH(g) + H O(g)
2 2 3 2
起始/mol 1 3 0 0
转化/mol 0.6 1.8 0.6 0.6
平衡/mol 0.2 1 0.6 0.8
CO(g) + H (g) CO(g) + H O(g)
2 2 2
起始/mol 1 3 0 0
转化/mol 0.2 0.2 0.2 0.2
平衡/mol 0.2 1 0.2 0.8
1.8mol+0.2mol 2
则H 的转化率为 = ;平衡时气体(包括N)的总物质的量为0.2 mol+1 mol+0.6
2 3mol 3 2
mol+0.8 mol+0.2 mol+1 mol=3.8 mol,平衡时总压强p =3.8p kPa,CO、H、CO、HO的分压分别为
平 2 2 2
0.2pkPa×0.8pkPa
0.2p kPa、p kPa、0.2p kPa、0.8p kPa,反应ⅱ的K = =0.8。
p 0.2pkPa×pkPa
c(HCOOH)
(3)反应CO(g)+H(g) HCOOH(g)的化学平衡常数表达式K= ;而v =k
2 2 c(CO )·c(H ) 正 正
2 2
c(CO)·c(H ),v =k c(HCOOH),k 、k 为速率常数,平衡时v =v ,即k c(CO)·c(H )=k
2 2 逆 逆 正 逆 正 逆 正 2 2 逆
c(HCOOH) k
= 正
c(HCOOH),则K= ,所以k =1.8k ;温度为T ℃时,k =1.9k ,则K=1.9,即平
c(CO )·c(H ) k 正 逆 2 正 逆
2 2 逆
衡常数K增大,反应正向移动,该反应为放热反应,所以T”“<”或“=”)T。T 温度下,反应进行到t min时容器内反应体系总压强为
1 2 2
kPa。
(5)一定温度下,向1 L恒容密闭容器中充入1 mol N 和n mol H 合成氨气。NH 的平衡体积分数与投
2 2 3
n(H )
2
料比η[η= ]关系如图所示。
n(N )
2
①在a、b、c点中,N 的平衡转化率最大的是 (填字母)。
2
1
②若b点对应体系中,NH 体积分数为 ,则该温度下,平衡常数K为 L2·mol-2(只列计
3 9
算式)。
答案:(1)N的电负性较大,NH 分子间形成氢键
3
(2)ΔH=2ΔH+ΔH
3 1 2
(3)①946 ②2NH (g) N(g)+3H(g) ΔH=+90 kJ·mol-1
3 2 20.42
(4)< 150 (5)①c ②
0.8×2.43
解析:(2)由盖斯定律可知③=2×①+②,故ΔH=2ΔH+ΔH。
3 1 2
(3)①2N(g) N(g) ΔH=-(518-45)×2 kJ·mol-1=-946 kJ·mol-1,故N 的键能为946 kJ·mol-1。
2 2
1 3
②从图像看出,NH(g)相对能量为0, N(g)+ H(g)的相对能量为45 kJ·mol-1,故2NH (g) N(g)
3 2 2 2 2 3 2
+3H (g) ΔH=+90 kJ·mol-1。
2
(4)起始投入反应物的量相等,T 温度下半衰期大于T,说明Tp
1 2
B.恒温密闭体系中,加压时副反应平衡不移动
C.300~350 ℃曲线变化的原因可能是此时以发生副反应为主
D.加入选择性更好的催化剂,可以提高甲醇的平衡产率
E.300 ℃时,当体系中混合气体的平均摩尔质量不再改变,则该体系达到平衡状态
(4)在T ℃下,恒压反应器中,按初始投料n(CO)∶n(H )=1∶1发生反应:CO (g)+3H(g) CHOH(g)
2 2 2 2 3
+H O(g),初始总压为2 MPa,反应平衡后,H 的平衡转化率为60%,则该反应的平衡常数K =
2 2 p
(MPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)一种基于铜基金属簇催化剂电催化还原CO 制备甲醇的装置如图所示。控制其他条件相同,将一
2
定量的CO 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图所示。
2
①b电极生成CHOH的电极反应式为 。
3
②控制电压为0.8 V,电解时转移电子的物质的量为 mol。
答案:(1)吸热 (2)-49 (3)ACE (4)0.5
(5)①CO+6e-+6H+ CHOH+H O
2 3 2
②2.8解析:(1)整个过程只消耗太阳能,H O和CO 仅充当能量的媒介且可实现完美循环,这是典型的人工光
2 2
合过程,光合过程中太阳能转化为化学能(或CHOH+O CO+H O为放热反应),则过程HO+CO
3 2 2 2 2 2
CHOH+O 为吸热反应。(2)CO (g)+3H(g) CHOH(g)+H O(g) ΔH=[(-201 kJ·mol-1)+(-242
3 2 2 2 3 2 1
kJ·mol-1)]-(-394 kJ·mol-1)=-49 kJ·mol-1。(3)主反应的正反应气体分子数减小,副反应反应前后气体分
子数不变,其他条件相同时,增大压强,主反应平衡正向移动、CO 的平衡转化率增大,CH OH的选择
2 3
性增大,则p>p ,A项正确;恒温密闭体系中,加压时主反应平衡正向移动,CO 、H 物质的量减小,副反
1 2 2 2
应平衡逆向移动,B项错误;300~350 ℃在不同的压强下CO 的平衡转化率趋于重合、升高温度CO
2 2
的平衡转化率增大,说明压强影响不大、升温平衡正向移动为主,说明此时以发生副反应为主,C项正
确;催化剂不能使平衡发生移动,不能提高甲醇的平衡产率,D项错误;该体系中所有物质都呈气态,建
立平衡的过程中混合气体的总质量始终不变,混合气体的总物质的量是变量,混合气体的平均摩尔质
量是变量,故当体系中混合气体的平均摩尔质量不再改变,则该体系达到平衡状态,E项正确。
(4)设CO、H 的初始物质的量均为a mol。列三段式
2 2
CO(g) + 3H (g) CH OH(g) + H O(g)
2 2 3 2
n(起始)/mol a a 0 0
n(转化)/mol 0.2a 0.6a 0.2a 0.2a
n(平衡)/mol 0.8a 0.4a 0.2a 0.2a
平衡时总物质的量为1.6a mol,平衡时CO、H、CHOH、HO的分压依次为1 MPa、0.5 MPa、0.25
2 2 3 2
0.25 MPa×0.25 MPa
MPa、0.25 MPa,则该反应的平衡常数K = =0.5(MPa)-2。
p 1 MPa×(0.5 MPa)3
(5)①根据图示,a电极为阳极,b电极为阴极,b极上生成CHOH的电极反应式为CO+6e-+6H+
3 2
CHOH+H O。②由图知,控制电压为0.8 V时,阴极生成0.2 mol C HOH和0.2 mol H,阴极的电极反
3 2 2 5 2
应式为2CO+12e-+12H+ C HOH+3H O、2H++2e- H↑,电解时转移电子物质的量为0.2
2 2 5 2 2
mol×12+0.2 mol×2=2.8 mol。