文档内容
九年级化学练习
相对原子质量:C-12 H-1 O-16 Ca-40
一、选择题(本大题共17题,共20分,1~14每题只有1个正确选项,每题1分,共14分。
15~17每题有1~2个正确选项,每题2分,共6分)
1. 幼儿及青少年缺钙会患佝偻病。因此,每日必须摄入足够量的钙。这里的“钙”指的是
A. 原子 B. 分子 C. 元素 D. 单质
【答案】C
【解析】
【详解】这里的“钙”不是以分子、原子、单质的形式存在,而是强调存在的元素,与具体形态无关。
故选C。
2. 空气中含量最多的气体是
A. 氧气 B. 氮气 C. 二氧化碳 D. 水蒸气
【答案】B
【解析】
【详解】空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳:0.03%、
水蒸气和杂质:0.03%,所以空气中含量最多的气体是氮气。故选B。
3. 生活中常见的物质属于纯净物的是
A. 蒸馏水 B. 肥皂水 C. 食盐水 D. 矿泉水
【答案】A
【解析】
【详解】A、蒸馏水中只有水一种物质,属于纯净物,选项正确;
B、肥皂水中含有肥皂和水等物质,属于混合物,选项错误;
C、食盐水是由食盐溶于水而成的,属于混合物,选项错误;
D、矿泉水中含有水和某些矿物质,属于混合物,选项错误。
故选A。
4. 放入水中能形成溶液的物质是
A. 面粉 B. 麻油 C. 牛奶 D. 蔗糖
【答案】D
【解析】
【详解】A、面粉不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,A不符合题意;
B、麻油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,B不符合题意;
C、牛奶是不溶性的小液滴等分散到液体中形成的,不能和水形成均一、稳定的混合物,即不能够形成溶
第1页/共14页
学科网(北京)股份有限公司液,C不符合题意;
D、蔗糖糖易溶于水,形成均一、稳定的混合物,属于溶液,D符合题意。
综上所述:选择D。
5. 和C 互称为同素异形体的是
60
A. 石墨 B. 活性炭 C. 木炭 D. 炭黑
【答案】A
【解析】
【详解】A、石墨和C 都是由碳元素形成的不同物质,都是单质,互为同素异形体,故A正确;
60
B、活性炭主要成分是碳,含有其它杂质,属于混合物,与 C 不互为同素异形体,故B不正确;
60
C、木炭主要成分是碳,含有其它杂质,属于混合物,与 C 不互为同素异形体,故C不正确;
60
D、炭黑主要成分是石墨,含有其它杂质,属于混合物,与 C 不互为同素异形体,故D不正确。
60
故选A。
6. 能引起酸雨的气体是
.
A 二氧化碳 B. 二氧化硫 C. 臭氧 D. 一氧化碳
【答案】B
【解析】
【详解】酸雨产生的主要原因:空气中的二氧化硫、二氧化氮等溶于水会形成酸雨,故选B。
7. 不会影响气体物质溶解度的因素是
A. 温度的高低 B. 溶质的质量 C. 压强的大小 D. 溶剂的性质
【答案】B
【解析】
【详解】A、温度会影响气体物质的溶解度,温度越高,气体溶解度越小,不符合题意;
的
B、溶质质量不会影响气体物质 溶解度,符合题意;
C、压强会影响气体物质的溶解度,压强越大,气体溶解度越大,不符合题意;
D、溶剂的性质影响气体物质的溶解度,不符合题意。
故选B。
8. 配制100g质量分数为5%的氯化钠溶液,操作顺序正确的是
A. 计算→称取、量取→溶解 B. 计算→溶解→称取、量取
C. 称取、量取→计算→溶解 D. 溶解→计算→称取、量取
【答案】A
第2页/共14页
学科网(北京)股份有限公司【解析】
【详解】配制100g质量分数为5%的氯化钠溶液,操作顺序正确的是计算→称取、量取→溶解。
故选A。
9. 氢能是未来国家能源体系的重要组成部分。有关“氢气”说法错误的是
A. 属于非金属单质 B. 点燃前需要检验其纯度
C. 氢元素以化合态存在 D. 保持氢气化学性质的微粒是氢分子
【答案】C
【解析】
【详解】A、氢气是由氢元素组成的纯净物,属于非金属单质,故A不符合题意;
B、氢气具有可燃性,氢气不纯时,燃烧易发生爆炸,所以点燃前需要检验其纯度,故B不符合题意;
C、氢气属于单质,元素以单质形态存在时称为游离态,故C符合题意;
D、氢气是由氢分子构成的,则保持氢气化学性质的微粒是氢分子,故D不符合题意;
故选C。
10. 物质的性质与用途没有对应关系的是
A. 金刚石硬度大,可用于切割玻璃 B. 点燃前需要检验其纯度
C. 氧气供给呼吸,可用于医疗急救 D. 活性炭有吸附性,可作口罩滤芯
【答案】B
【解析】
【详解】A、金刚石硬度大,可用于切割玻璃,故A正确;
B、可燃性气体点燃前需要检验纯度,防止爆炸,这不是物质的性质和用途对应,故B错误;
C、氧气可以供给呼吸,所以可用于医疗急救,故C正确;
D、活性炭具有吸附性可以吸附异味粒子,所以可以作口罩滤芯,故D正确。
故选B。
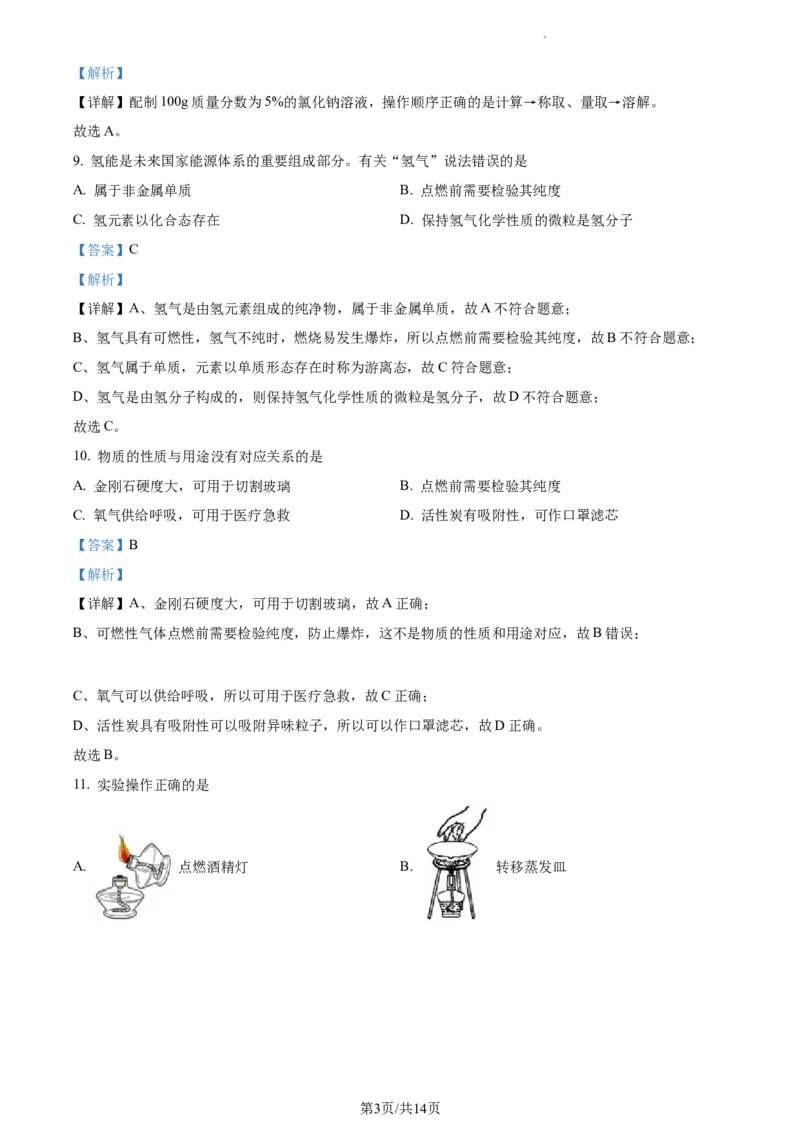
11. 实验操作正确的是
A. 点燃酒精灯 B. 转移蒸发皿
第3页/共14页
学科网(北京)股份有限公司C. 取用稀盐酸 D. 装固体粉末
【答案】D
【解析】
【详解】A、点燃酒精灯时要用火柴点燃,禁止用一燃着的酒精灯去引燃另一酒精灯,以防引起火灾,操
作错误;
B、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,应用坩埚钳夹取,操作错
误;
C、使用胶头滴管时,为防止液体腐蚀橡胶胶帽,滴管不能平放或倒放,操作错误;
D、向试管中加入粉末状固体药品时,应先将试管横放,用纸槽或药匙把药品送到试管底部,再慢慢将试
管竖立起来,操作正确。
故选D。
12. 化学用语的表述错误的是
A. 胆矾:CuSO ·5HO B. 氦气:He
4 2
C. 硫酸根:SO D. 汞元素:Hg
4
【答案】C
【解析】
【详解】A、胆矾为五水硫酸铜,化学式为CuSO ·5H O,该选项表述正确;
4 2
B、氦气为稀有气体,化学式为He,该选项表述正确;
C、元素符号右上角的数字表示离子所带电荷数,硫酸根的符号为 ,该选项表述错误;
D、汞元素的符号为Hg,该选项表述正确。
故选C。
13. 乳酸(化学式为C HO)可作饮料中的酸味剂。有关“乳酸”说法正确的是
3 6 3
A. 氢元素的质量分数最大
B. 碳、氢、氧元素质量比为1:2:1
C. 乳酸由碳原子、氢原子、氧原子构成
D. 式量计算式为(12×3+1×6+16×3)
【答案】D
【解析】
【详解】A、乳酸中碳、氢、氧元素的质量比为(12×3):(1×6):(16×3)=6:1:8,乳酸中氧元素的质
第4页/共14页
学科网(北京)股份有限公司量分数最大,故选项说法错误;
B、乳酸中碳、氢、氧元素的质量比为6:1:8,故选项说法错误;
C、乳酸由乳酸分子构成,一个乳酸分子由3个碳原子、6个氢原子、3个氧原子构成,故选项说法错误;
D、乳酸式量计算式为(12×3+1×6+16×3),故选项说法正确。
故选:D。
14. 取一定质量的碳酸钙固体高温灼烧一段时间后,冷却,测得剩余固体的质量为8.0g,其中钙元素质量
分数为50.0%。下列判断正确的是
A. 剩余固体中可能含有CaO
B. 生成2.0gCO 气体
2
C. 灼烧前后固体中钙元素的质量分数不变
D. 剩余固体中滴加足量盐酸无明显现象
【答案】B
【解析】
【详解】A、碳酸钙中钙元素质量分数= ,但剩余固体中钙元素质量分数为
50.0%,氧化钙中钙元素质量分数= ,碳酸钙受热分解为氧化钙和二氧化碳,所以
剩余固体中一定含有CaO,判断错误;
B、根据题意可以知道钙元素的质量为:8.0g×50.0%=4.0g,所以反应前碳酸钙的质量=
, 碳酸钙受热分解为氧化钙和二氧化碳,根据质量守恒定律可以知
道生成二氧化碳的质量为:10.0g-8.0g=2.0g,判断正确;
为
C、因 碳酸钙受热分解为氧化钙和二氧化碳,固体质量降低,钙元素质量不变,所以灼烧前后固体中钙
元素质量分数变大,判断错误;
D、因为氧化钙中钙元素质量分数= ,剩余固体中钙元素质量分数为50.0%,所以
剩余固体中一定有未完全反应的碳酸钙,剩余固体中滴加足量盐酸会产生气泡,判断错误。
故选B。
15. 常温下,四种水果及两种饮料的pH如下。下列说法正确的是
第5页/共14页
学科网(北京)股份有限公司A. 纯净水显中性 B. 苏打水中滴入酚酞试液,溶液变红
C. 番茄汁显碱性 D. 水果中酸性最强的物质是西瓜汁
【答案】AB
【解析】
【详解】A、纯净水pH=7,显中性,正确;
B、苏打水的pH大于7,显碱性,酚酞遇碱性物质变红色,苏打水中滴入酚酞试液,溶液变红,正确;
C、番茄汁的pH小于7,显酸性,错误;
D、pH越小,酸性越强,显酸性,水果中柠檬pH最小,其酸性最强,错误。
故选AB。
16. 相关叙述错误的是
A. 分子种类发生改变的变化一定是化学变化
B. 物质跟氧气发生的反应一定是氧化反应
C. 只含两种元素,其中一种为氧元素的物质一定是氧化物
D. 燃烧生成水的可燃物中一定含有氢元素
【答案】C
【解析】
【详解】A、分子的种类发生改变,说明生成了新物质,有新物质生成的变化是化学变化,叙述正确;
B、物质跟氧气发生的反应,属于氧化反应,叙述正确;
C、只含两种元素,其中一种为氧元素的纯净物,一定是氧化物,必须强调是纯净物,叙述错误;
D、根据质量守恒定律,化学反应前后,元素的种类不变,故含氢元素的可燃物燃烧一定生成水,所以燃
烧生成水的可燃物中一定含有氢元素,叙述正确。
故选C。
17. t℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量关系绘制成下图所示斜线。有
关说法错误的是
第6页/共14页
学科网(北京)股份有限公司A. T℃时该物质的溶解度是20g/100g水
B. 该物质的溶解度随温度的升高而增大
C. N点所示的溶液中溶质质量分数为10%
D. Q点与G点所示的溶液均为t℃时该物质的饱和溶液
【答案】BC
【解析】
【详解】A、由图可知,t℃时,100g水中溶解该物质20g达到饱和状态,则该物质的溶解度是20g/100g水,
故A不符合题意;
B、图中信息不能确定该物质溶解度与温度的变化关系,故B符合题意;
C、N点所示的溶液中溶质质量分数为 ×100%≈9.1%,故C符合题意;
D、由图可知,t℃时,该物质的溶解度是20g,Q点的水为80g,最多溶解固体16g,所以Q点为饱和溶液,
G点的水为100g,固体质量为20g,恰好为饱和溶液,故D不符合题意;
故选BC。
二、简答题(本大题共4题,共30分)
18. 化学与生活、科技、科学实验息息相关。
(1)自来水厂在净化水的过程中加入明矾的作用是______(填“杀菌消毒”或“使悬浮物沉淀”)。
(2)2022年12月4日,航天员陈冬、刘洋、蔡旭哲结束了为期6个月的太空之旅,安全返回地球。
Ⅰ.航天员呼吸所需的O 来自水的电解,其反应的化学方程式是____,该反应属于____(选填“化合”或
2
“分解”)反应。
Ⅱ.在飞船的火箭推进器中装有肼(化学式为NH,常温下呈液态)和过氧化氢,它们混合时的反应图示
2 4
如下。
0.5mol N H 中约含有_____个氮原子;该反应的化学方程式为________。
2 4
(3)根据图示实验,回答下列问题。
第7页/共14页
学科网(北京)股份有限公司Ⅰ.实验一是验证燃烧的条件,铜片上的白磷燃烧而红磷不燃烧说明可燃物燃烧需要的条件之一是____。
Ⅱ.实验二是粗盐提纯实验中的过滤操作。仪器a的名称是________;若过滤后所得滤液仍然浑浊,可能的
原因是________(任写一种)。
Ⅲ.实验三是检查装置气密性,用微观的角度解释该操作中产生的现象________。
【答案】(1)使悬浮物沉淀
(2) ①.
②. 分解 ③. 6.02×1023 ④.
(3) ①. 温度达到可燃物的着火点 ②. 漏斗 ③. 滤纸破损(或液面高于滤纸边缘或盛接滤液
的烧杯不干净) ④. 用手握住大试管,温度升高,装置内气体微粒间(或气体分子间)的间隔增大
【解析】
【小问1详解】
明矾能使水中不溶性固体小颗粒凝聚而沉降到水底,自来水厂在净化水的过程中加入明矾的作用是使悬浮
物沉淀;
【小问2详解】
Ⅰ.水电解生成氢气和氧气,反应的化学方程式为: ,该反应是由一种物质分解
生成两种物质,属于分解反应;
Ⅱ.1个NH 含有2个N原子和4个H原子,0.5mol N H 中约含有6.02×1023个氮原子;根据微观示意图可
2 4 2 4
知,该反应的化学方程式为: ;
【小问3详解】
Ⅰ.铜片上的白磷燃烧而红磷不燃烧说明可燃物燃烧需要的条件之一是温度达到可燃物的着火点;
Ⅱ.仪器a的名称是漏斗;若过滤后所得滤液仍然浑浊,可能的原因是滤纸破损或液面高于滤纸边缘或盛接
第8页/共14页
学科网(北京)股份有限公司滤液的烧杯不干净;
Ⅲ.检查装置气密性时,用手握住大试管,温度升高,装置内气体微粒间(或气体分子间)的间隔增大。
19. 硝酸钾(KNO)和氯化钾(KCl)的部分溶解度数据如下表:
3
温度/℃ 0 10 20 40 100
KNO 13.3 20.9 31.6 63.9 246
3
溶解度(g/100g水)
KC1 27.6 31.0 34.0 40.0 56.7
(1)20℃时,硝酸钾的溶解度_____(填“大于”“小于”或“等于”)氯化钾的溶解度。
(2)溶解度受温度的影响较大的物质是_____(选填“KNO”或“KCl”)。
3
(3)40℃时,_____(填“可以”或“不可以”)配制溶质质量分数为30%的KCl溶液。
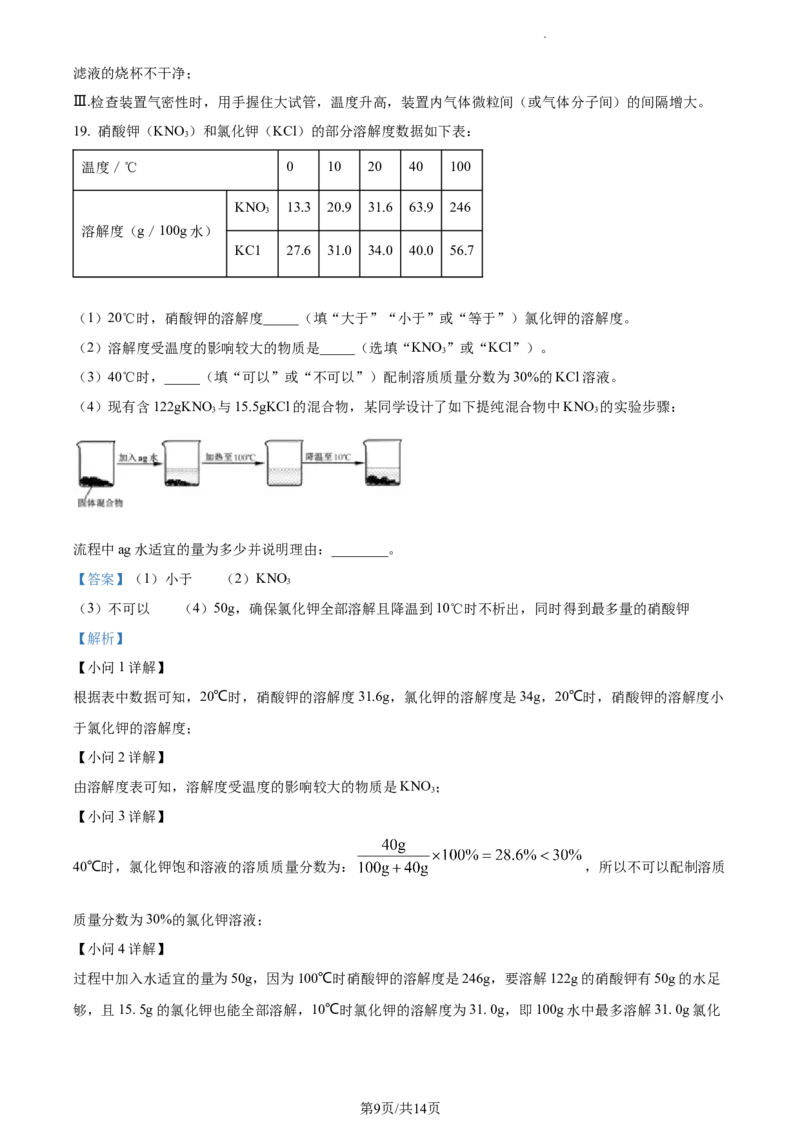
(4)现有含122gKNO 与15.5gKCl的混合物,某同学设计了如下提纯混合物中KNO 的实验步骤:
3 3
流程中ag水适宜的量为多少并说明理由:________。
【答案】(1)小于 (2)KNO
3
(3)不可以 (4)50g,确保氯化钾全部溶解且降温到10℃时不析出,同时得到最多量的硝酸钾
【解析】
【小问1详解】
根据表中数据可知,20℃时,硝酸钾的溶解度31.6g,氯化钾的溶解度是34g,20℃时,硝酸钾的溶解度小
于氯化钾的溶解度;
【小问2详解】
由溶解度表可知,溶解度受温度的影响较大的物质是KNO;
3
【小问3详解】
40℃时,氯化钾饱和溶液的溶质质量分数为: ,所以不可以配制溶质
质量分数为30%的氯化钾溶液;
【小问4详解】
过程中加入水适宜的量为50g,因为100℃时硝酸钾的溶解度是246g,要溶解122g的硝酸钾有50g的水足
够,且15. 5g的氯化钾也能全部溶解,10℃时氯化钾的溶解度为31. 0g,即100g水中最多溶解31. 0g氯化
第9页/共14页
学科网(北京)股份有限公司钾,50g水中最多溶解15. 5g氯化钾,确保氯化钾全部溶解且降温到10℃时不析出,同时得到最多量的硝
酸钾。
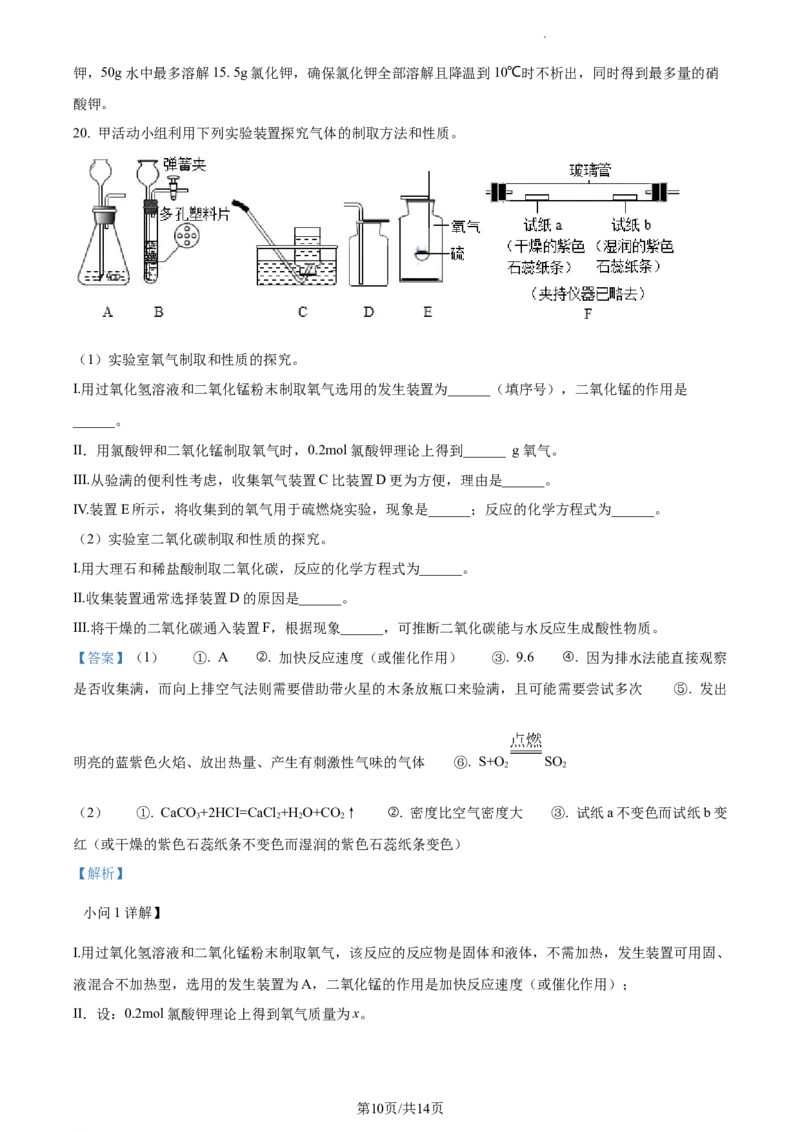
20. 甲活动小组利用下列实验装置探究气体的制取方法和性质。
(1)实验室氧气制取和性质的探究。
I.用过氧化氢溶液和二氧化锰粉末制取氧气选用的发生装置为______(填序号),二氧化锰的作用是
______。
II.用氯酸钾和二氧化锰制取氧气时,0.2mol氯酸钾理论上得到______ g氧气。
III.从验满的便利性考虑,收集氧气装置C比装置D更为方便,理由是______。
IV.装置E所示,将收集到的氧气用于硫燃烧实验,现象是______;反应的化学方程式为______。
(2)实验室二氧化碳制取和性质的探究。
I.用大理石和稀盐酸制取二氧化碳,反应的化学方程式为______。
II.收集装置通常选择装置D的原因是______。
III.将干燥的二氧化碳通入装置F,根据现象______,可推断二氧化碳能与水反应生成酸性物质。
【答案】(1) ①. A ②. 加快反应速度(或催化作用) ③. 9.6 ④. 因为排水法能直接观察
是否收集满,而向上排空气法则需要借助带火星的木条放瓶口来验满,且可能需要尝试多次 ⑤. 发出
明亮的蓝紫色火焰、放出热量、产生有刺激性气味的气体 ⑥. S+O SO
2 2
(2) ①. CaCO +2HCI=CaCl +H O+CO↑ ②. 密度比空气密度大 ③. 试纸a不变色而试纸b变
3 2 2 2
红(或干燥的紫色石蕊纸条不变色而湿润的紫色石蕊纸条变色)
【解析】
【
小问1详解】
I.用过氧化氢溶液和二氧化锰粉末制取氧气,该反应的反应物是固体和液体,不需加热,发生装置可用固、
液混合不加热型,选用的发生装置为A,二氧化锰的作用是加快反应速度(或催化作用);
II.设:0.2mol氯酸钾理论上得到氧气质量为x。
第10页/共14页
学科网(北京)股份有限公司x=9.6g。
III.从验满的便利性考虑,收集氧气装置C比装置D更为方便,理由是因为排水法能直接观察是否收集满,
而向上排空气法则需要借助带火星的木条放瓶口来验满,且可能需要尝试多次;
IV.装置E所示,将收集到的氧气用于硫燃烧实验,现象是发出明亮的蓝紫色火焰、放出热量、产生有刺激
性气味的气体;硫在氧气中燃烧生成二氧化硫,反应的化学方程式为S+O SO ;
2 2
【小问2详解】
I. 实验室制取二氧化碳,常用大理石或石灰石与盐酸反应,大理石或石灰石的主要成分是碳酸钙,碳酸钙
与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO +2HCl=CaCl +H O+CO↑;
3 2 2 2
II.收集装置通常选择装置D的原因是密度比空气密度大;
III.将干燥的二氧化碳通入装置F,根据现象试纸a不变色而试纸b变红(或干燥的紫色石蕊纸条不变色而
湿润的紫色石蕊纸条变色),可推断二氧化碳能与水反应生成酸性物质。
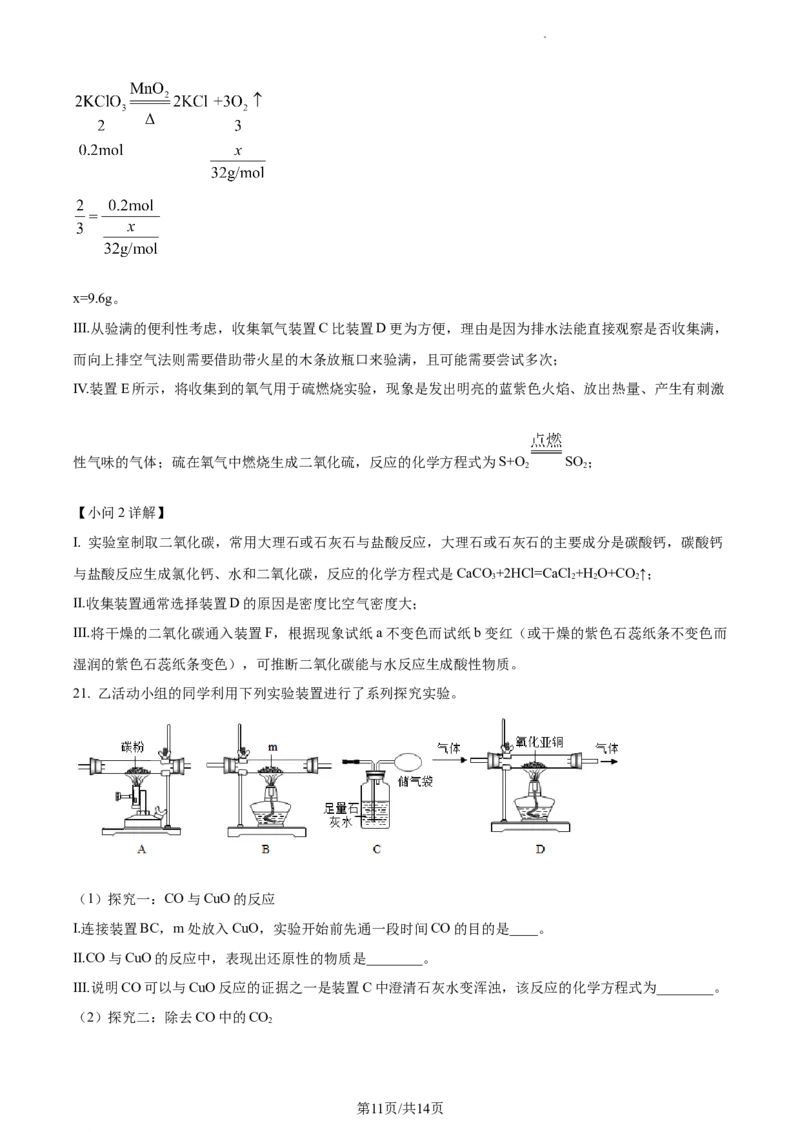
21. 乙活动小组的同学利用下列实验装置进行了系列探究实验。
(1)探究一:CO与CuO的反应
I.连接装置BC,m处放入CuO,实验开始前先通一段时间CO的目的是____。
II.CO与CuO的反应中,表现出还原性的物质是________。
III.说明CO可以与CuO反应的证据之一是装置C中澄清石灰水变浑浊,该反应的化学方程式为________。
(2)探究二:除去CO中的CO
2
第11页/共14页
学科网(北京)股份有限公司方案1:在装置C中,缓缓通入混合气体。
方案2:连接装置AC,缓缓通入混合气体。
I.装置C中储气袋的作用是:_____。
II.比较方案1和方案2,写出各自的一条优点:_____。
(3)探究三:检验N 中的O
2 2
Cu可形成化合价为+1和+2的化合物,其中+1价化合物称为亚铜化合物。
I.氧化亚铜的化学式为_____。
II.氧化亚铜是一种红色粉末,加热时氧化亚铜能与氧气发生化合反应。利用该性质可检验氮气中是否含有
氧气,装置D所示,判断氮气中含有氧气的现象是:____。
【答案】(1) ①. 排尽装置内的空气防止一氧化碳不纯发生爆炸 ②. CO##氧化铜 ③.
CO+Ca(OH) =CaCO ↓+H O
2 2 3 2
(2) ①. 收集一氧化碳 ②. 方案1操作简单(或能得到较纯的一氧化碳),方案2可以增加一氧
化碳的量
(3) ①. Cu O ②. 红色粉末变成黑色
2
【解析】
【小问1详解】
I. 当可燃性气体中混有氧气时,在加热或点燃时可燃发生爆炸连接装置BC,m处放入CuO,实验开始前
先通一段时间CO的目的是排尽装置内的空气防止一氧化碳不纯发生爆炸;可燃性气体中混有氧气在加热
或点燃时可燃发生爆炸
II.CO与CuO的反应中,氧化铜失去氧元素,表现出氧化性,一氧化碳得到氧元素,表现为还原性,表现
出还原性的物质是一氧化碳(CO)。
的
III.说明CO可以与CuO反应 证据之一是装置C中澄清石灰水变浑浊,二氧化碳能与澄清石灰水中的氢氧
化钙反应生成碳酸钙沉淀和水,该反应的化学方程式为CO+Ca(OH) =CaCO ↓+H O;
2 2 3 2
【小问2详解】
I. 二氧化碳能与澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,澄清石灰水能吸收二氧化碳,装置C
中储气袋的作用是:收集一氧化碳;
II.比较方案1和方案2,优点:方案1操作简单(或能得到较纯的一氧化碳),
方案2可以增加一氧化碳的量,二氧化碳与碳在高温条件下生成一氧化碳;
【小问3详解】
I.氧化亚铜中铜元素显+1价,氧元素显-2价,书写化学式时,一般正价的写在左边,负价的写在右边,根
据化合物中各元素化合价代数和为零,其化学式为Cu O;
2
II.根据“氧化亚铜是一种红色粉末,加热时氧化亚铜能与氧气发生化合反应”可知,加热时氧化亚铜能与
第12页/共14页
学科网(北京)股份有限公司氧气发生化合反应能生成氧化铜。氧化铜是一种黑色粉末。利用该性质可检验氮气中是否含有氧气,装置
D所示,判断氮气中含有氧气的现象是:红色粉末变成黑色。
第13页/共14页
学科网(北京)股份有限公司第14页/共14页
学科网(北京)股份有限公司