文档内容
2021 年重庆市新高考化学试卷
参考答案与试题解析
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.(3分)“垃圾分类记心上,魅力山城新时尚”,下列可回收物中,主要成分为无机非金属
材料的是( )
A. 普通玻璃 B. 不锈钢锅
C. 矿泉水瓶 D. 棉麻织物
【分析】A.玻璃是三大无机非金属材料之一;
B.不锈钢锅属于合金材料;
C.矿泉水瓶属于有机合成材料;
D.棉麻织物属于有机高分子材料。
【解答】解:A.玻璃主要成分是硅酸盐材料,属于三大无机非金属材料之一,故A正
确;
B.不锈钢锅属于合金材料,不是无机非金属材料,故B错误;
C.矿泉水瓶属于有机合成材料,不是无机非金属材料,故C错误;
D.棉麻织物属于有机高分子材料,不是无机非金属材料,故D错误;
故选:A。
【点评】本题考查了化学知识在生产生活中的应用,侧重于生产生活中化学材料的考查,
题目难度不大,明确复合材料、有机合成材料、无机非金属材料和金属材料的组成是解
题的关键。
2.(3分)葡萄酒中含有CH CH OH、CH COOH、SO 和CO 等多种成分。若N 代表阿
3 2 3 2 2 A
伏伽德罗常数的值,下列说法正确的是( )
A.46gCH CH OH中含有C﹣H键数为5N
3 2 A
第1页 | 共27页B.1L1mol•L﹣1CH COOH溶液中含有氢离子数为N
3 A
C.1molSO 与1molO 完全反应转移的电子数为4N
2 2 A
D.11.2L(标准状况)CO 完全溶于水后溶液中H CO 分子数为0.5N
2 2 3 A
【分析】A.一个CH CH OH分子中含有5条C﹣H键;
3 2
B.醋酸为弱酸;
C.可逆反应不能反应完全;
D.二氧化碳与水的反应为可逆反应,碳酸为弱酸,部分电离。
【解答】解:A.46gCH CH OH中含有C﹣H键数为 ×5×N /mol=5N ,故A
3 2 A A
正确;
B.醋酸为弱酸,在水中部分电离,1L1mol•L﹣1CH COOH溶液中含有氢离子数小于N ,
3 A
故B错误;
C.二氧化硫与氧气生成三氧化硫的反应为可逆反应,反应不能完全,故 1molSO 与
2
1molO 完全反应转移的电子数小于2N ,故C错误;
2 A
D.二氧化碳与水的反应为可逆反应,碳酸为弱酸,部分电离,11.2L(标准状况)即
0.5molCO 完全于水后溶液中H CO 分子数小于0.5N ,故D错误;
2 2 3 A
故选:A。
【点评】本题考查阿伏伽德罗常数的有关计算和判断,题目难度中等,阿伏伽德罗常数
是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏伽德罗常
数关系的理解,又可以涵盖多角度的化学知识内容,掌握好以物质的量为中心的各化学
量与阿伏伽德罗常数的关系是解题的关键。
3.(3分)25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0mol•L﹣1氯化钡溶液中:Mg2+、K+、Br﹣、SO
B.1.0mol•L﹣1 硫酸中:A13+、Na+、Cl﹣、NO
C.pH=11的氨水中:Fe2+、Na+、NO ﹣、ClO﹣
3
D.pH=1的硝酸中:Fe3+、K+、I﹣、SO
【分析】A.该溶液有钡离子,与硫酸根离子不能共存;
B.四种离子之间不反应,都不与氢离子反应;
C.该溶液呈碱性,铁离子与氢氧根离子反应;
第2页 | 共27页D.铁离子和碘离子不能共存。
【解答】解:A.该溶液中有钡离子,与硫酸根离子发生反应生成沉淀,不能大量共存,
故A错误;
B.A13+、Na+、Cl﹣、NO 之间不反应,能够在酸性溶液中大量共存,故B正确;
C.铁离子在碱性溶液中不能大量共存,故C错误;
D.铁离子和碘离子发生氧化还原反应不能大量共存,在酸性溶液中不能大量共存,故D
错误;
故选:B。
【点评】本题考查离子共存的判断,为高频考点,明确题干暗含信息、常见离子的性质
及离子反应发生条件为解答关键,注意掌握常见离子不能共存的情况,试题侧重考查学
生的分析与应用能力,题目难度不大。
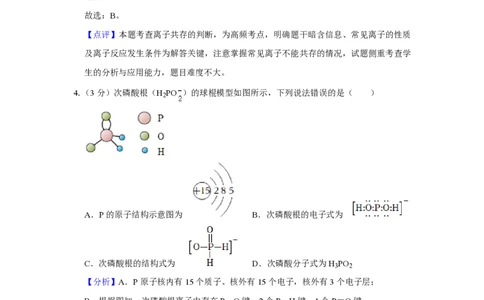
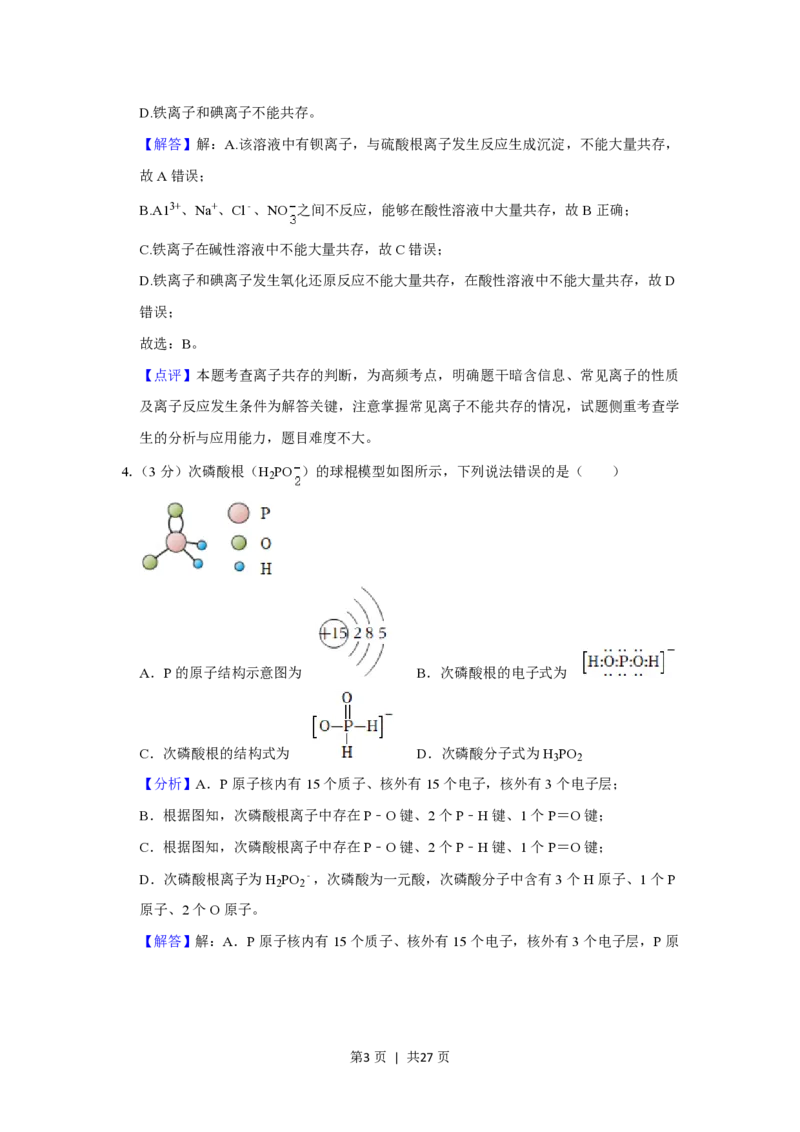
4.(3分)次磷酸根(H PO )的球棍模型如图所示,下列说法错误的是( )
2
A.P的原子结构示意图为 B.次磷酸根的电子式为
C.次磷酸根的结构式为 D.次磷酸分子式为H PO
3 2
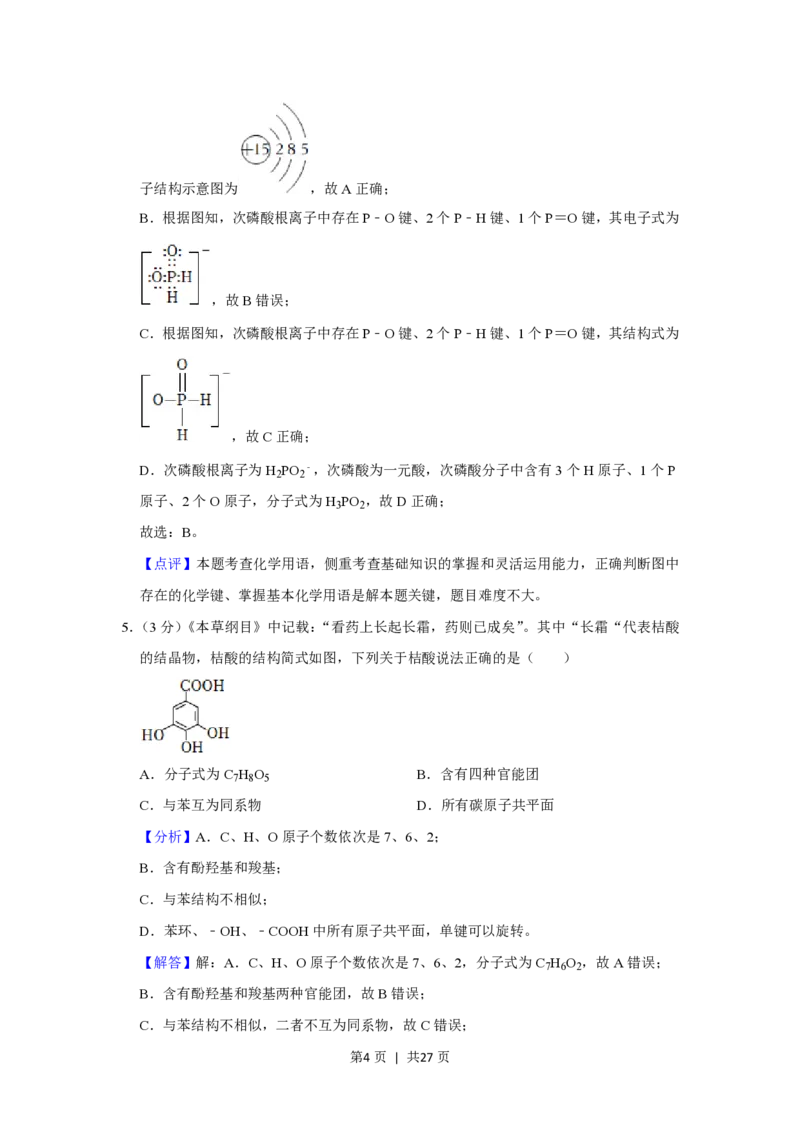
【分析】A.P原子核内有15个质子、核外有15个电子,核外有3个电子层;
B.根据图知,次磷酸根离子中存在P﹣O键、2个P﹣H键、1个P=O键;
C.根据图知,次磷酸根离子中存在P﹣O键、2个P﹣H键、1个P=O键;
D.次磷酸根离子为H PO ﹣,次磷酸为一元酸,次磷酸分子中含有3个H原子、1个P
2 2
原子、2个O原子。
【解答】解:A.P原子核内有15个质子、核外有15个电子,核外有3个电子层,P原
第3页 | 共27页子结构示意图为 ,故A正确;
B.根据图知,次磷酸根离子中存在P﹣O键、2个P﹣H键、1个P=O键,其电子式为
,故B错误;
C.根据图知,次磷酸根离子中存在P﹣O键、2个P﹣H键、1个P=O键,其结构式为
,故C正确;
D.次磷酸根离子为H PO ﹣,次磷酸为一元酸,次磷酸分子中含有3个H原子、1个P
2 2
原子、2个O原子,分子式为H PO ,故D正确;
3 2
故选:B。
【点评】本题考查化学用语,侧重考查基础知识的掌握和灵活运用能力,正确判断图中
存在的化学键、掌握基本化学用语是解本题关键,题目难度不大。
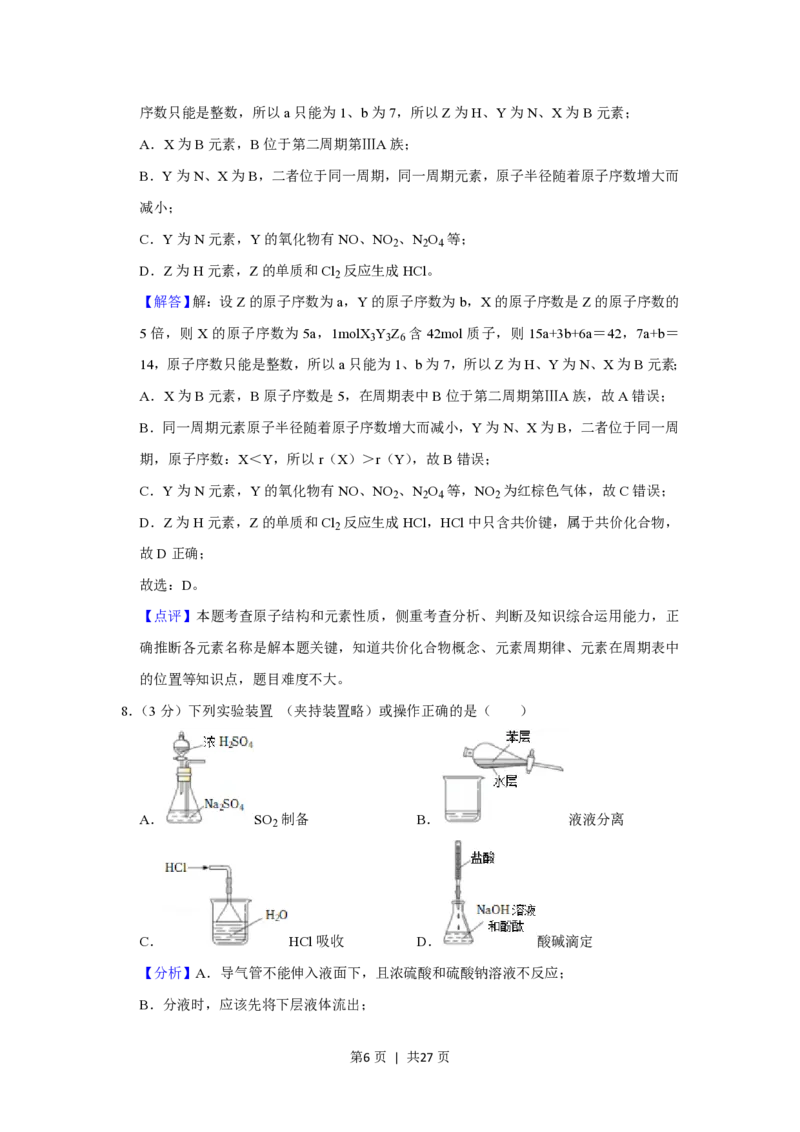
5.(3分)《本草纲目》中记载:“看药上长起长霜,药则已成矣”。其中“长霜“代表桔酸
的结晶物,桔酸的结构简式如图,下列关于桔酸说法正确的是( )
A.分子式为C H O B.含有四种官能团
7 8 5
C.与苯互为同系物 D.所有碳原子共平面
【分析】A.C、H、O原子个数依次是7、6、2;
B.含有酚羟基和羧基;
C.与苯结构不相似;
D.苯环、﹣OH、﹣COOH中所有原子共平面,单键可以旋转。
【解答】解:A.C、H、O原子个数依次是7、6、2,分子式为C H O ,故A错误;
7 6 2
B.含有酚羟基和羧基两种官能团,故B错误;
C.与苯结构不相似,二者不互为同系物,故C错误;
第4页 | 共27页D.苯环、﹣OH、﹣COOH中所有原子共平面,单键可以旋转,则该分子中所有碳原子
一定共平面,故D正确;
故选:D。
【点评】本题考查有机物的结构和性质,侧重考查基础知识的掌握和灵活运用能力,明
确原子共平面判断方法、官能团的名称、同系物概念是解本题关键,题目难度不大。
6.(3分)下列叙述错误的是( )
A.Mg在空气中燃烧可生成MgO
B.Fe O 与Al发生铝热反应可生成Fe
2 3
C.BaCl 溶液与CO 反应可生成BaCO
2 2 3
D.Ca(OH) 溶液与Cl 反应可生成Ca(ClO)
2 2 2
【分析】A.Mg是活泼金属;
B.Al比Fe活泼;
C.BaCl 溶液与CO 不反应;
2 2
D.Ca(OH) 与 Cl 发生反应的总化学方程式为 2Ca(OH) +2Cl =Ca(ClO)
2 2 2 2
+CaCl +2H O。
2 2 2
【解答】解:A.Mg是活泼金属,Mg在空气中燃烧生成MgO,故A正确;
B.Al比Fe活泼,Fe O 与Al发生铝热反应可生成Fe,故B正确;
2 3
C.碳酸的酸性比盐酸弱,所以BaCl 溶液与CO 不反应,故C错误;
2 2
D.Ca(OH) 与 Cl 发生反应的总化学方程式为 2Ca(OH) +2Cl =Ca(ClO)
2 2 2 2
+CaCl +2H O,即Ca(OH) 溶液与Cl 反应可生成Ca(ClO) ,故D正确;
2 2 2 2 2 2
故选:C。
【点评】本题考查常见的物质间的反应,熟悉物质的性质是解答的关键,题目较简单。
7.(3分)元素X、Y和Z可形成化合物X Y Z ,X的原子序数是Z的原子序数的5倍,
3 3 6
1molX Y Z 含42mol质子,下列叙述正确的是( )
3 3 6
A.X位于周期表的第二周期第VA族
B.Y的原子半径大于X的原子半径
C.Y的氧化物为无色气体
D.Z的单质与Cl 反应可生成共价化合物
2
【分析】设Z的原子序数为a,Y的原子序数为b,X的原子序数是Z的原子序数的5倍,
则X的原子序数为5a,1molX Y Z 含42mol质子,则15a+3b+6a=42,7a+b=14,原子
3 3 6
第5页 | 共27页序数只能是整数,所以a只能为1、b为7,所以Z为H、Y为N、X为B元素;
A.X为B元素,B位于第二周期第ⅢA族;
B.Y为N、X为B,二者位于同一周期,同一周期元素,原子半径随着原子序数增大而
减小;
C.Y为N元素,Y的氧化物有NO、NO 、N O 等;
2 2 4
D.Z为H元素,Z的单质和Cl 反应生成HCl。
2
【解答】解:设Z的原子序数为a,Y的原子序数为b,X的原子序数是Z的原子序数的
5倍,则X的原子序数为5a,1molX Y Z 含42mol质子,则15a+3b+6a=42,7a+b=
3 3 6
14,原子序数只能是整数,所以a只能为1、b为7,所以Z为H、Y为N、X为B元素;
A.X为B元素,B原子序数是5,在周期表中B位于第二周期第ⅢA族,故A错误;
B.同一周期元素原子半径随着原子序数增大而减小,Y为N、X为B,二者位于同一周
期,原子序数:X<Y,所以r(X)>r(Y),故B错误;
C.Y为N元素,Y的氧化物有NO、NO 、N O 等,NO 为红棕色气体,故C错误;
2 2 4 2
D.Z为H元素,Z的单质和Cl 反应生成HCl,HCl中只含共价键,属于共价化合物,
2
故D正确;
故选:D。
【点评】本题考查原子结构和元素性质,侧重考查分析、判断及知识综合运用能力,正
确推断各元素名称是解本题关键,知道共价化合物概念、元素周期律、元素在周期表中
的位置等知识点,题目难度不大。
8.(3分)下列实验装置 (夹持装置略)或操作正确的是( )
A. SO 制备 B. 液液分离
2
C. HCl吸收 D. 酸碱滴定
【分析】A.导气管不能伸入液面下,且浓硫酸和硫酸钠溶液不反应;
B.分液时,应该先将下层液体流出;
第6页 | 共27页C.倒置的漏斗能防止倒吸;
D.酸溶液应该用酸式滴定管盛放。
【解答】解:A.导气管不能伸入液面下,且浓硫酸和硫酸钠溶液不反应,所以得不到二
氧化硫气体,应该将硫酸钠溶液换为Na SO 溶液,故A错误;
2 3
B.分液时,应该先将下层液体流出,然后将上层液体从上口流出,故B错误;
C.HCl极易溶于水,倒置的漏斗能防止倒吸,所以该操作正确,故C正确;
D.酸溶液应该用酸式滴定管盛放,所以盐酸应该盛放在酸式滴定管中,图中滴定管为碱
式滴定管,故D错误;
故选:C。
【点评】本题考查实验装置综合,侧重考查分析、判断及知识综合运用能力,明确实验
原理、元素化合物的性质、实验操作规范性是解本题关键,题目难度不大。
9.(3分)下列实验操作及其现象与对应结论不匹配的是( )
选项 实验操作及其现象 结论
A 将CO与水蒸气通过炽热的催化剂,所得气体通入澄清石 水蒸气有氧化性
灰水,溶液变浑浊
B 将新制Cu(OH) 加入葡萄糖溶液中,加热至沸腾,有 葡萄糖具有还原性
2
砖红色沉淀产生
C 将NaBiO 固体加入酸性MnSO 溶液中,充分振荡,溶液 NaBiO 有氧化性
3 4 3
变为紫红色
D 有FeCl 溶液和KSCN溶液混合后,滴加H O 溶液,溶 H O 有还原性
3 2 2 2 2
液变为红色
A.A B.B C.C D.D
【分析】A.将CO与水蒸气通过炽热的催化剂,所得气体通入澄清石灰水,溶液变浑浊,
说明有CO 生成,则CO和H O反应生成CO ,该反应中C元素化合价由+2价变为+4
2 2 2
价、H O中H元素化合价由+1价变为0价,H O作氧化剂;
2 2
B.﹣CHO能和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀Cu O,反应中Cu元
2
素化合价由+2价变为+1价,葡萄糖作还原剂、Cu(OH) 作氧化剂;
2
C.将NaBiO 固体加入酸性MnSO 溶液中,充分振荡,溶液变为紫红色,说明有KMnO
3 4 4
生成,Mn元素化合价由+2价变为+7价,则MnSO 作还原剂,NaBiO 作氧化剂;
4 3
第7页 | 共27页D.FeCl 和KSCN反应生成络合物Fe(SCN) 而使溶液变为红色,且FeCl 能促进H O
3 3 3 2 2
分解。
【解答】解:A.将CO与水蒸气通过炽热的催化剂,所得气体通入澄清石灰水,溶液变
浑浊,说明有CO 生成,则CO和H O反应生成CO ,该反应中C元素化合价由+2价
2 2 2
变为+4价、H O中H元素化合价由+1价变为0价,H O作氧化剂,H O体现氧化性,
2 2 2
故A正确;
B.﹣CHO能和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀Cu O,反应中Cu元
2
素化合价由+2价变为+1价,葡萄糖作还原剂、Cu(OH) 作氧化剂,葡萄糖体现还原
2
性,故B正确;
C.将NaBiO 固体加入酸性MnSO 溶液中,充分振荡,溶液变为紫红色,说明有KMnO
3 4 4
生成,Mn元素化合价由+2价变为+7价,则MnSO 作还原剂,NaBiO 作氧化剂,NaBiO
4 3 3
体现氧化性,故C正确;
D.FeCl 和KSCN反应生成络合物Fe(SCN)而使溶液变为红色,且FeCl 能促进H O
3 3 3 2 2
分解,现象和结论不匹配,故D错误;
故选:D。
【点评】本题考查化学实验方案评价,侧重考查分析、判断及知识综合运用能力,明确
元素化合物的性质、物质之间的反应、氧化性和还原性判断方法是解本题关键,题目难
度不大。
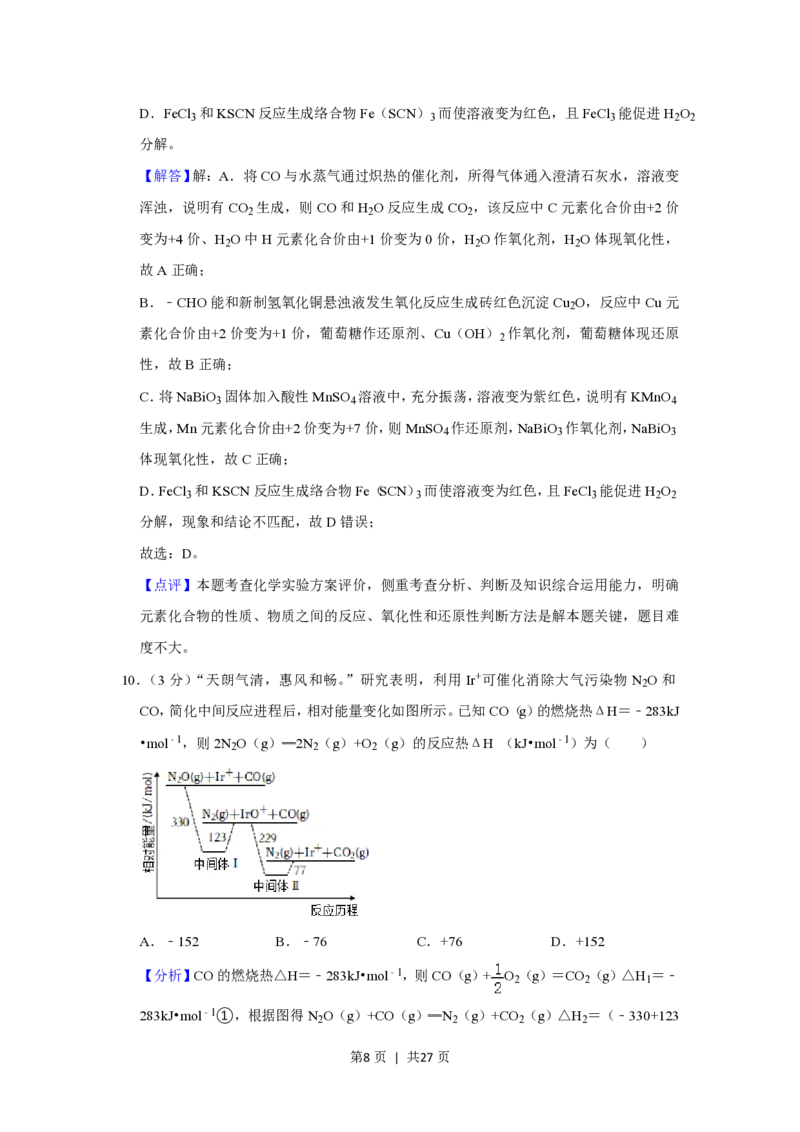
10.(3 分)“天朗气清,惠风和畅。”研究表明,利用 Ir+可催化消除大气污染物 N O 和
2
CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热ΔH=﹣283kJ
•mol﹣1,则2N O(g)═2N (g)+O (g)的反应热ΔH (kJ•mol﹣1)为( )
2 2 2
A.﹣152 B.﹣76 C.+76 D.+152
【分析】CO的燃烧热△H=﹣283kJ•mol﹣1,则CO(g)+ O (g)=CO (g)△H =﹣
2 2 1
283kJ•mol﹣1①,根据图得N O(g)+CO(g)═N (g)+CO (g)△H =(﹣330+123
2 2 2 2
第8页 | 共27页﹣229+77)kJ/mol=﹣359kJ/mol②,根据盖斯定律得,反应(②﹣①)×2得2N O
2
(g)═2N (g)+O (g),ΔH=(△H ﹣△H )×2。
2 2 2 1
【解答】解:CO的燃烧热△H=﹣283kJ•mol﹣1,则CO(g)+ O (g)=CO (g)△
2 2
H =﹣283kJ•mol﹣1①,根据图得N O(g)+CO(g)═N (g)+CO (g)△H =(﹣
1 2 2 2 2
330+123﹣229+77)kJ/mol=﹣359kJ/mol②,根据盖斯定律得,反应(②﹣①)×2得
2N O(g)═2N (g)+O (g),ΔH=(△H ﹣△H )×2=[(﹣359+283)×2]kJ/mol
2 2 2 2 1
=﹣152kJ/mol,
故选:A。
【点评】本题考查盖斯定律的计算,侧重考查阅读、分析、判断及计算能力,明确盖斯
定律含义、图中方程式的焓变计算方法是解本题关键,题目难度不大。
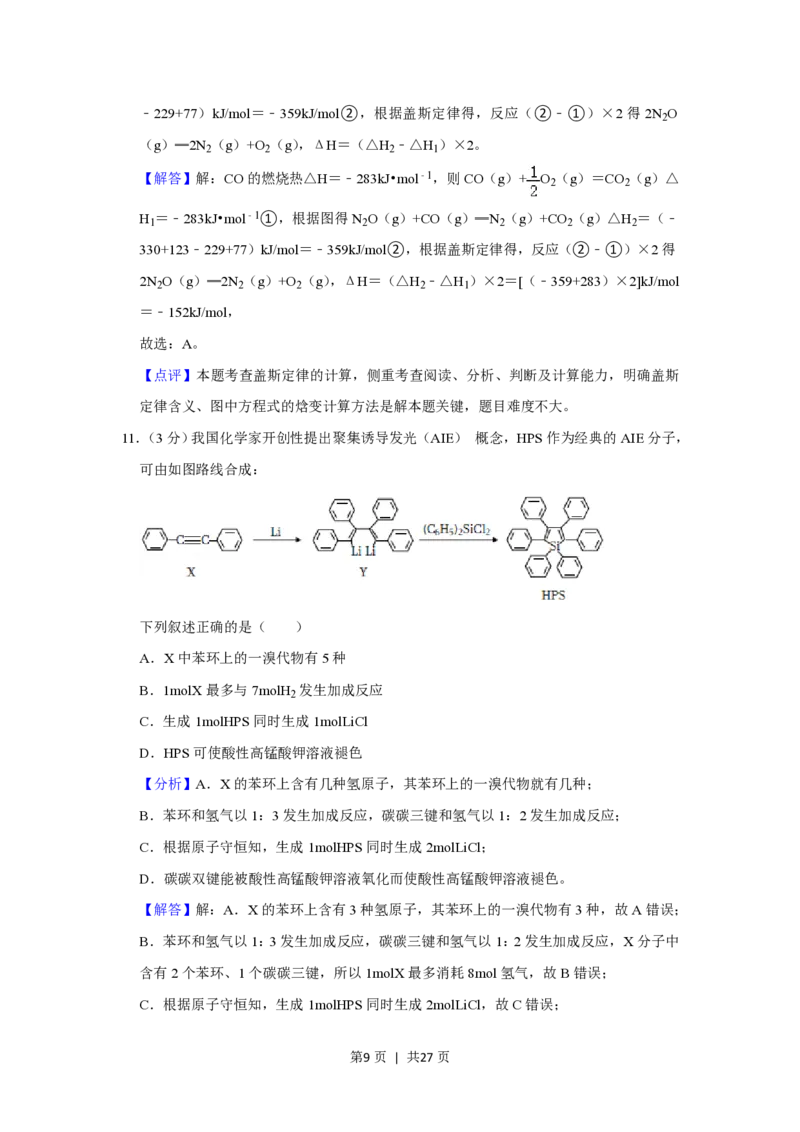
11.(3分)我国化学家开创性提出聚集诱导发光(AIE) 概念,HPS作为经典的AIE分子,
可由如图路线合成:
下列叙述正确的是( )
A.X中苯环上的一溴代物有5种
B.1molX最多与7molH 发生加成反应
2
C.生成1molHPS同时生成1molLiCl
D.HPS可使酸性高锰酸钾溶液褪色
【分析】A.X的苯环上含有几种氢原子,其苯环上的一溴代物就有几种;
B.苯环和氢气以1:3发生加成反应,碳碳三键和氢气以1:2发生加成反应;
C.根据原子守恒知,生成1molHPS同时生成2molLiCl;
D.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色。
【解答】解:A.X的苯环上含有3种氢原子,其苯环上的一溴代物有3种,故A错误;
B.苯环和氢气以1:3发生加成反应,碳碳三键和氢气以1:2发生加成反应,X分子中
含有2个苯环、1个碳碳三键,所以1molX最多消耗8mol氢气,故B错误;
C.根据原子守恒知,生成1molHPS同时生成2molLiCl,故C错误;
第9页 | 共27页D.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,HPS中含有碳碳
双键,所以HPS能使酸性高锰酸钾溶液褪色,故D正确;
故选:D。
【点评】本题考查有机物的结构和性质,侧重考查基础知识的掌握和灵活运用能力,明
确官能团及其性质的关系是解本题关键,题目难度不大。
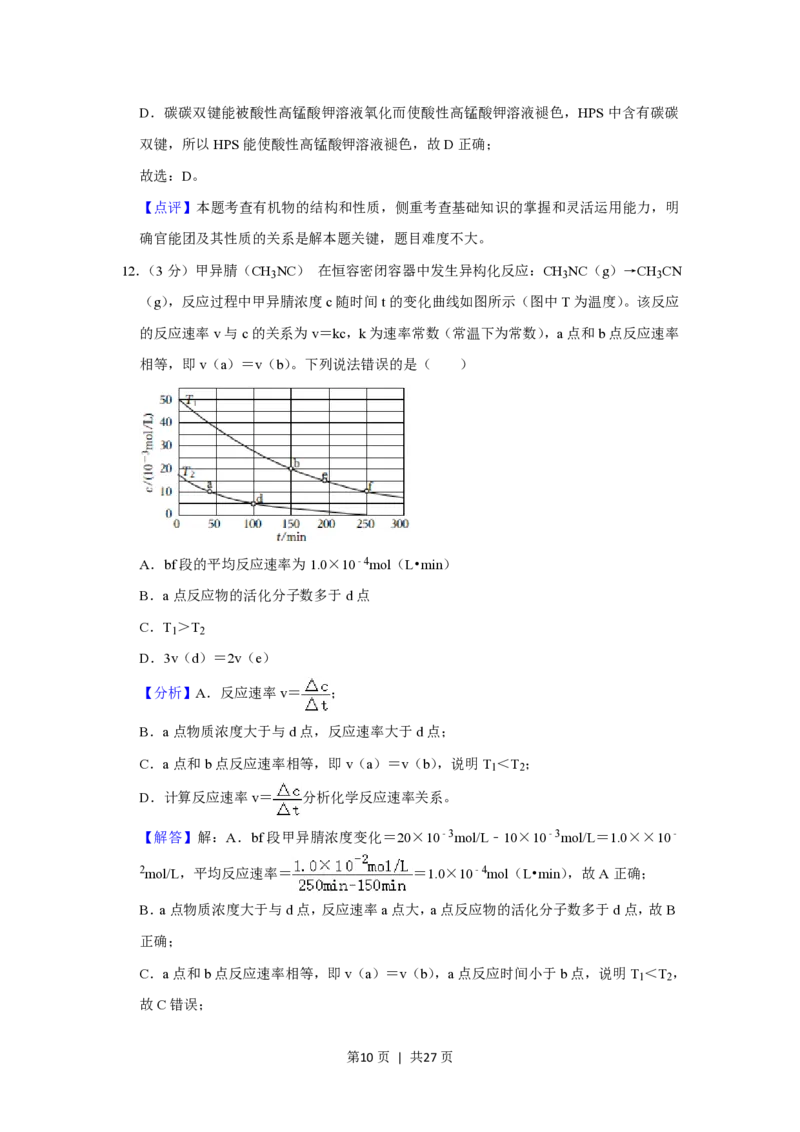
12.(3分)甲异腈(CH NC) 在恒容密闭容器中发生异构化反应:CH NC(g)→CH CN
3 3 3
(g),反应过程中甲异腈浓度c随时间t的变化曲线如图所示(图中T为温度)。该反应
的反应速率v与c的关系为v=kc,k为速率常数(常温下为常数),a点和b点反应速率
相等,即v(a)=v(b)。下列说法错误的是( )
A.bf段的平均反应速率为1.0×10﹣4mol(L•min)
B.a点反应物的活化分子数多于d点
C.T >T
1 2
D.3v(d)=2v(e)
【分析】A.反应速率v= ;
B.a点物质浓度大于与d点,反应速率大于d点;
C.a点和b点反应速率相等,即v(a)=v(b),说明T <T ;
1 2
D.计算反应速率v= 分析化学反应速率关系。
【解答】解:A.bf段甲异腈浓度变化=20×10﹣3mol/L﹣10×10﹣3mol/L=1.0××10﹣
2mol/L,平均反应速率= =1.0×10﹣4mol(L•min),故A正确;
B.a点物质浓度大于与d点,反应速率a点大,a点反应物的活化分子数多于d点,故B
正确;
C.a点和b点反应速率相等,即v(a)=v(b),a点反应时间小于b点,说明T <T ,
1 2
故C错误;
第10页 | 共27页D.v(d)= =5×10﹣5mol(L/min),v(e)= =7.5
×10﹣5mol(L/min), = = ,3v(d)=2v(e),故D正确;
故选:C。
【点评】本题考查了化学反应速率的影响因素分析、反应速率的计算应用,注意图象变
化的理解应用,题目难度不大。
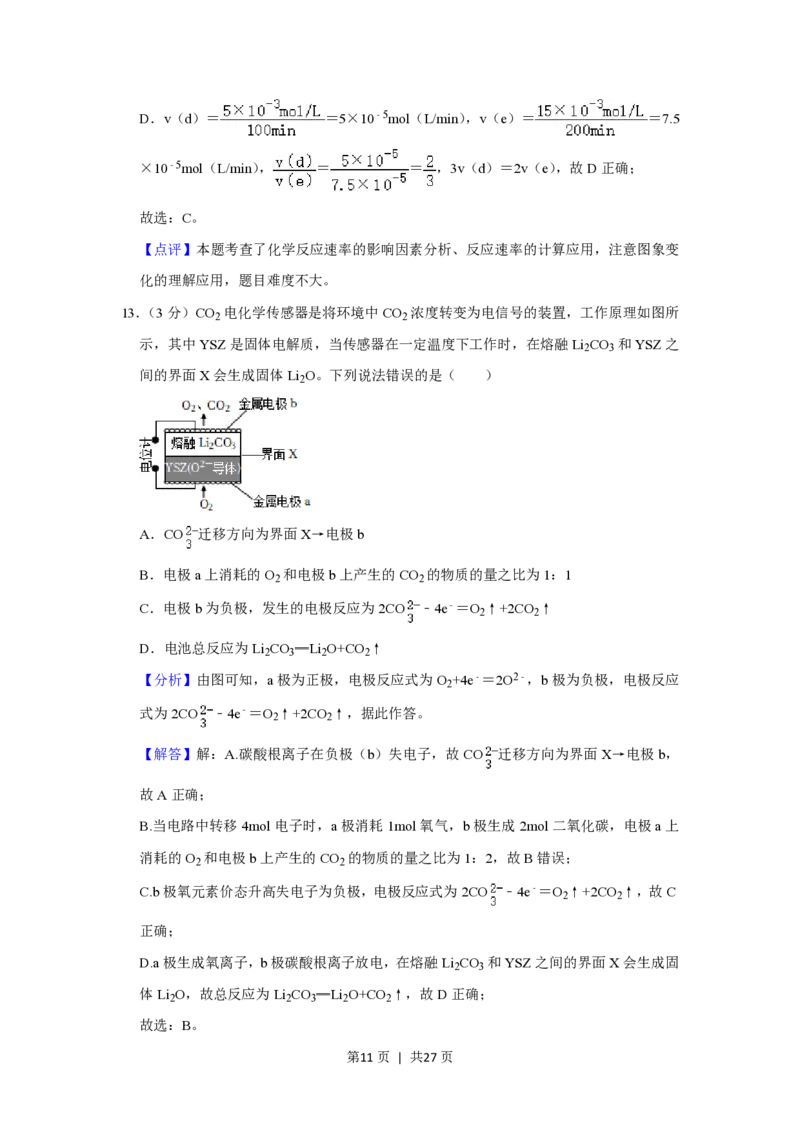
13.(3分)CO 电化学传感器是将环境中CO 浓度转变为电信号的装置,工作原理如图所
2 2
示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融Li CO 和YSZ之
2 3
间的界面X会生成固体Li O。下列说法错误的是( )
2
A.CO 迁移方向为界面X→电极b
B.电极a上消耗的O 和电极b上产生的CO 的物质的量之比为1:1
2 2
C.电极b为负极,发生的电极反应为2CO ﹣4e﹣=O ↑+2CO ↑
2 2
D.电池总反应为Li CO ═Li O+CO ↑
2 3 2 2
【分析】由图可知,a极为正极,电极反应式为O +4e﹣=2O2﹣,b极为负极,电极反应
2
式为2CO ﹣4e﹣=O ↑+2CO ↑,据此作答。
2 2
【解答】解:A.碳酸根离子在负极(b)失电子,故CO 迁移方向为界面X→电极b,
故A正确;
B.当电路中转移4mol电子时,a极消耗1mol氧气,b极生成2mol二氧化碳,电极a上
消耗的O 和电极b上产生的CO 的物质的量之比为1:2,故B错误;
2 2
C.b极氧元素价态升高失电子为负极,电极反应式为2CO ﹣4e﹣=O ↑+2CO ↑,故C
2 2
正确;
D.a极生成氧离子,b极碳酸根离子放电,在熔融Li CO 和YSZ之间的界面X会生成固
2 3
体Li O,故总反应为Li CO ═Li O+CO ↑,故D正确;
2 2 3 2 2
故选:B。
第11页 | 共27页【点评】本题考查原电池原理,题目难度中等,能依据图象和题目信息准确判断正负极
是解题的关键,难点是电极反应式的书写。
14.(3分)下列叙述正确的是( )
A.向氨水中加入醋酸使溶液呈酸性,则c(NH +)>c(CH COO﹣ )
4 3
B.向NH Cl溶液中加入少量Al (SO ) 固体、则水的电离程度减小
4 2 4 3
C.向Na CO 溶液中滴加盐酸至c(Na+)=2c(Cl﹣),则c(HCO )>c(H CO )
2 3 2 3
D.向0.2mol•L﹣1磷酸中加水至原体积的两倍,则c(H+)>0.1mol•L﹣1
【分析】A.溶液呈酸性,则c(H+)>c(OH﹣),结合电荷守恒判断;
B.Al (SO ) 中铝离子在溶液中会发生水解反应,水解过程是对水的电离的促进;
2 4 3
C.根据钠离子和氯离子之间量的关系确定发生的反应,找到碳酸的来源进行判断即可;
D.磷酸是弱酸,不能完全电离,据此回答。
【解答】解:A.向氨水中加入醋酸使溶液呈酸性,c(H+)>c(OH﹣),根据电荷守恒:
c(H+)+c(NH +)=c(OH﹣)+c(CH COO﹣ ),得到c(NH +)<c(CH COO﹣ ),
4 3 4 3
故A错误;
B.溶液中加入少量Al (SO ) 固体,Al (SO ) 中铝离子在溶液中会发生水解反应,
2 4 3 2 4 3
对水的电离起到促进作用,水的电离程度增大,故B错误;
C.向Na CO 溶液中滴加盐酸至c(Na+)=2c(Cl﹣ ),即n(Na+)=2n(Cl﹣ ),得
2 3
到 n(Na CO )= n(Na+)=n(Cl﹣ )=n(HCl),发生反应:Na CO +HCl=
2 3 2 3
NaCl+NaHCO ,H CO 来自于HCO ﹣的微弱水解,所以c(HCO ﹣)>c(H CO ),故
3 2 3 3 3 2 3
C正确;
D.向0.2mol•L﹣1磷酸中加水至原体积的两倍,稀释后c(H PO )=0.1mol/L,磷酸是
3 4
弱酸,电离程度很小,所以c(H+)<0.1mol•L﹣1,故D错误;
故选:C。
【点评】本题考查盐的水解原理以及应用知识,题目难度中等,注意掌握电荷守恒、物
料守恒及盐的水解原理在判断离子浓度大小中的应用方法,试题培养了学生的灵活应用
能力。
二、非选择题:本题包含必考题和选考题,共58分。(一)必考题(共43分)
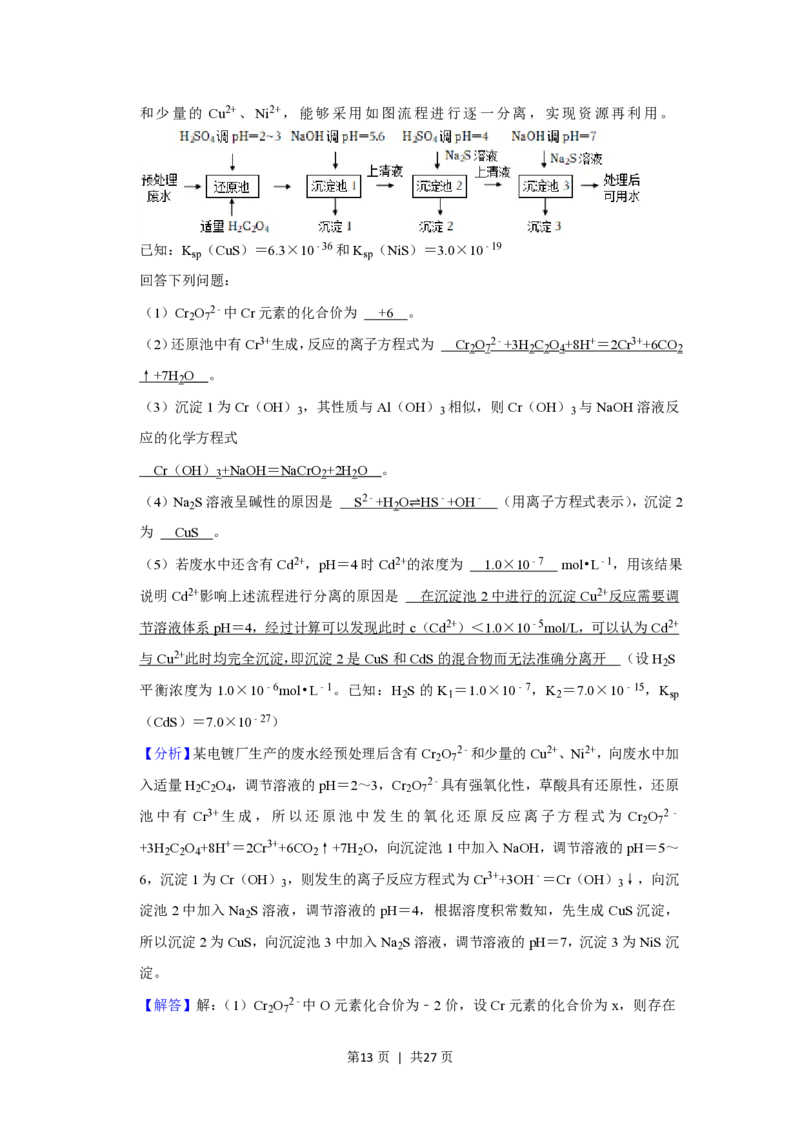
15.(14分)电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有Cr O
2
第12页 | 共27页和少量的 Cu2+、Ni2+,能够采用如图流程进行逐一分离,实现资源再利用。
已知:K (CuS)=6.3×10﹣36和K (NiS)=3.0×10﹣19
sp sp
回答下列问题:
(1)Cr O 2﹣中Cr元素的化合价为 +6 。
2 7
(2)还原池中有Cr3+生成,反应的离子方程式为 Cr O 2﹣+3H C O +8H+=2Cr3++6CO
2 7 2 2 4 2
↑+7H O 。
2
(3)沉淀1为Cr(OH) ,其性质与Al(OH) 相似,则Cr(OH) 与NaOH溶液反
3 3 3
应的化学方程式
Cr(OH) +NaOH=NaCrO +2H O 。
3 2 2
(4)Na S溶液呈碱性的原因是 S2﹣+H O⇌HS﹣+OH﹣ (用离子方程式表示),沉淀2
2 2
为 CuS 。
(5)若废水中还含有Cd2+,pH=4时Cd2+的浓度为 1.0×10﹣7 mol•L﹣1,用该结果
说明Cd2+影响上述流程进行分离的原因是 在沉淀池2中进行的沉淀Cu2+反应需要调
节溶液体系pH=4,经过计算可以发现此时c(Cd2+)<1.0×10﹣5mol/L,可以认为Cd2+
与Cu2+此时均完全沉淀,即沉淀2是CuS和CdS的混合物而无法准确分离开 (设H S
2
平衡浓度为 1.0×10﹣6mol•L﹣1。已知:H S 的 K =1.0×10﹣7,K =7.0×10﹣15,K
2 1 2 sp
(CdS)=7.0×10﹣27)
【分析】某电镀厂生产的废水经预处理后含有Cr O 2﹣和少量的Cu2+、Ni2+,向废水中加
2 7
入适量H C O ,调节溶液的pH=2~3,Cr O 2﹣具有强氧化性,草酸具有还原性,还原
2 2 4 2 7
池中有 Cr3+生成,所以还原池中发生的氧化还原反应离子方程式为 Cr O 2﹣
2 7
+3H C O +8H+=2Cr3++6CO ↑+7H O,向沉淀池1中加入NaOH,调节溶液的pH=5~
2 2 4 2 2
6,沉淀1为Cr(OH) ,则发生的离子反应方程式为Cr3++3OH﹣=Cr(OH) ↓,向沉
3 3
淀池2中加入Na S溶液,调节溶液的pH=4,根据溶度积常数知,先生成CuS沉淀,
2
所以沉淀2为CuS,向沉淀池3中加入Na S溶液,调节溶液的pH=7,沉淀3为NiS沉
2
淀。
【解答】解:(1)Cr O 2﹣中O元素化合价为﹣2价,设Cr元素的化合价为x,则存在
2 7
第13页 | 共27页2x+(﹣2)×7=﹣2,则Cr元素的化合价为+6,
故答案为:+6;
(2)通过以上分析知,还原池中有 Cr3+生成,反应的离子方程式为 Cr O 2﹣
2 7
+3H C O +8H+=2Cr3++6CO ↑+7H O,
2 2 4 2 2
故答案为:Cr O 2﹣+3H C O +8H+=2Cr3++6CO ↑+7H O;
2 7 2 2 4 2 2
(3)沉淀1为Cr(OH) ,其性质与Al(OH) 相似,根据Al(OH) 和NaOH反应
3 3 3
方程式书写 Cr(OH) 与 NaOH 溶液反应的化学方程式为 Cr(OH) +NaOH=
3 3
NaCrO +2H O,
2 2
故答案为:Cr(OH) +NaOH=NaCrO +2H O;
3 2 2
(4)Na S 为强碱弱酸盐,S2﹣水解导致溶液呈碱性,Na S 溶液呈碱性的原因是 S2﹣
2 2
+H O⇌HS﹣+OH﹣,通过以上分析知,沉淀2为CuS,
2
故答案为:S2﹣+H O⇌HS﹣+OH﹣;CuS;
2
( 5 ) H S 的 K = 、 K = , K × K =
2 1 2 1 2
× = , 则 c ( S2 ﹣ ) =
= mol/L=7.0×10﹣
20mol/L,c(Cd2+)= = mol/L=1.0×10﹣7mol/L,在沉淀池2
中进行的沉淀Cu2+反应需要调节溶液体系pH=4,此时c(Cd2+)=1.0×10﹣7mol/L<
1.0×10﹣5mol/L,可以认为Cd2+与Cu2+此时均完全沉淀,则沉淀2为CuS和CdS的混合
物,无法准确分离开,
故答案为:1.0×10﹣7mol/L;在沉淀池2中进行的沉淀Cu2+反应需要调节溶液体系pH=
4,经过计算可以发现此时c(Cd2+)<1.0×10﹣5mol/L,可以认为Cd2+与Cu2+此时均完
全沉淀,即沉淀2是CuS和CdS的混合物而无法准确分离开。
【点评】本题考查物质分离提纯和物质制备,侧重考查阅读、分析、判断及计算能力,
明确流程图中各物质成分及其性质、可能发生的反应是解本题关键,难点是(5)题有关
计算,题目难度中等。
16.(15分)立方体形的三氧化二铟(In O ),具有良好的气体传感性能。研究小组用水热
2 3
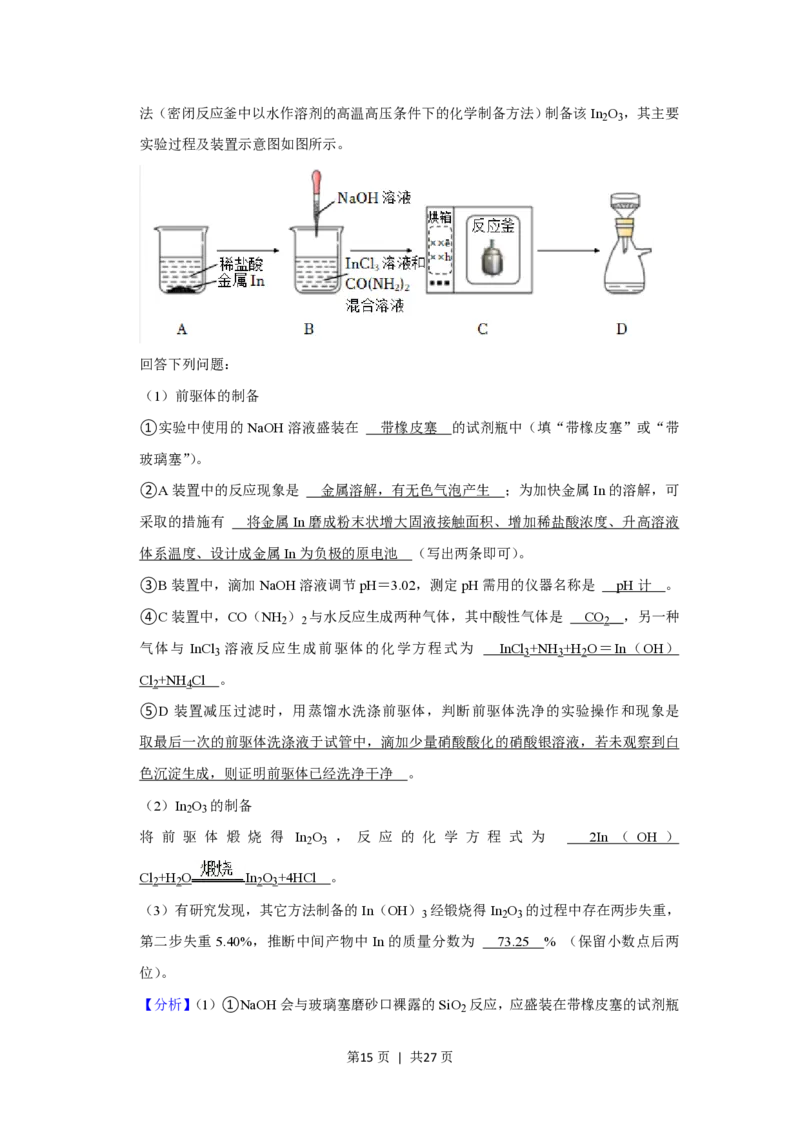
第14页 | 共27页法(密闭反应釜中以水作溶剂的高温高压条件下的化学制备方法)制备该In O ,其主要
2 3
实验过程及装置示意图如图所示。
回答下列问题:
(1)前驱体的制备
①实验中使用的NaOH溶液盛装在 带橡皮塞 的试剂瓶中(填“带橡皮塞”或“带
玻璃塞”)。
②A装置中的反应现象是 金属溶解,有无色气泡产生 ;为加快金属In的溶解,可
采取的措施有 将金属In磨成粉末状增大固液接触面积、增加稀盐酸浓度、升高溶液
体系温度、设计成金属In为负极的原电池 (写出两条即可)。
③B装置中,滴加NaOH溶液调节pH=3.02,测定pH需用的仪器名称是 pH计 。
④C装置中,CO(NH ) 与水反应生成两种气体,其中酸性气体是 CO ,另一种
2 2 2
气体与 InCl 溶液反应生成前驱体的化学方程式为 InCl +NH +H O=In(OH)
3 3 3 2
Cl +NH Cl 。
2 4
⑤D 装置减压过滤时,用蒸馏水洗涤前驱体,判断前驱体洗净的实验操作和现象是
取最后一次的前驱体洗涤液于试管中,滴加少量硝酸酸化的硝酸银溶液,若未观察到白
色沉淀生成,则证明前驱体已经洗净干净 。
(2)In O 的制备
2 3
将 前 驱 体 煅 烧 得 In O , 反 应 的 化 学 方 程 式 为 2In ( OH )
2 3
Cl +H O In O +4HCl 。
2 2 2 3
(3)有研究发现,其它方法制备的In(OH) 经锻烧得In O 的过程中存在两步失重,
3 2 3
第二步失重5.40%,推断中间产物中In的质量分数为 73.25 % (保留小数点后两
位)。
【分析】(1)①NaOH会与玻璃塞磨砂口裸露的SiO 反应,应盛装在带橡皮塞的试剂瓶
2
第15页 | 共27页中;
②根据B中生成了InCl 可知,A中In与盐酸反应置换出了氢气,会溶解;将金属In磨
3
成粉末状增大固液接触面积、增加稀盐酸浓度、升高溶液体系温度、设计成金属In为负
极的原电池等,都可以加快反应速率;
③测得pH=3.02,精确到了0.01,需用的仪器为:pH计;
④根据 CO(NH ) 与水所含元素分析,其中酸性气体应为 CO ;另一种气体应为
2 2 2
NH ;
3
⑤判断前驱体洗净看是否有NH Cl残留,可通过检验Cl﹣验证,滴加少量硝酸酸化的硝
4
酸银溶液检验;
(2)将前驱体煅烧得In O 、HCl;
2 3
(3)制备的In(OH) 经锻烧得In O 的过程中存在两步失重,第二步失重5.40%,质
3 2 3
量分数为 ×100%=73.25%。
【解答】解:(1)①NaOH会与玻璃塞磨砂口裸露的SiO 反应,故实验中使用的NaOH
2
溶液应盛装在带橡皮塞的试剂瓶中,
故答案为:带橡皮塞;
②根据B中生成了InCl 可知,A中In与盐酸反应置换出了氢气,故A装置中的反应现
3
象是金属溶解,有无色气泡产生;将金属In磨成粉末状增大固液接触面积、增加稀盐酸
浓度、升高溶液体系温度、设计成金属In为负极的原电池等,都可以加快反应速率,
故答案为:金属溶解,有无色气泡产生;将金属In磨成粉末状增大固液接触面积、增加
稀盐酸浓度、升高溶液体系温度、设计成金属In为负极的原电池;
③测得pH=3.02,精确到了0.01,故测定pH需用的仪器为:pH计,
故答案为:pH计;
④根据 CO(NH ) 与水所含元素分析,其中酸性气体应为 CO ;另一种气体应为
2 2 2
NH ,前驱体是获得目标产物前的一种存在形式,NH 与InCl 溶液反应生成前驱体的化
3 3 3
学方程式为:InCl +3NH +3H O=In(OH) ↓+3NH Cl,
3 3 2 3 4
故答案为:CO ;InCl +NH +H O=In(OH)Cl +NH Cl;
2 3 3 2 2 4
⑤判断前驱体洗净看是否有NH Cl残留,可通过检验Cl﹣验证,故实验操作和现象是:
4
取最后一次的前驱体洗涤液于试管中,滴加少量硝酸酸化的硝酸银溶液,若未观察到白
色沉淀生成,则证明前驱体已经洗净,
第16页 | 共27页故答案为:取最后一次的前驱体洗涤液于试管中,滴加少量硝酸酸化的硝酸银溶液,若
未观察到白色沉淀生成,则证明前驱体已经洗净干净;
( 2 ) 将 前 驱 体 煅 烧 得 In O , 反 应 的 化 学 方 程 式 为 2In ( OH )
2 3
Cl +H O In O +4HCl,
2 2 2 3
故答案为:2In(OH)Cl +H O In O +4HCl;
2 2 2 3
(3)中间产物中In的质量分数为 ×100%=
73.25%,
故答案为:73.25%。
【点评】本题考查物质的制备实验方案设计,为高考常见题型和高频考点,侧重考查学
生知识综合应用、根据实验目的及物质的性质进行分析、实验基本操作能力及实验方案
设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等。
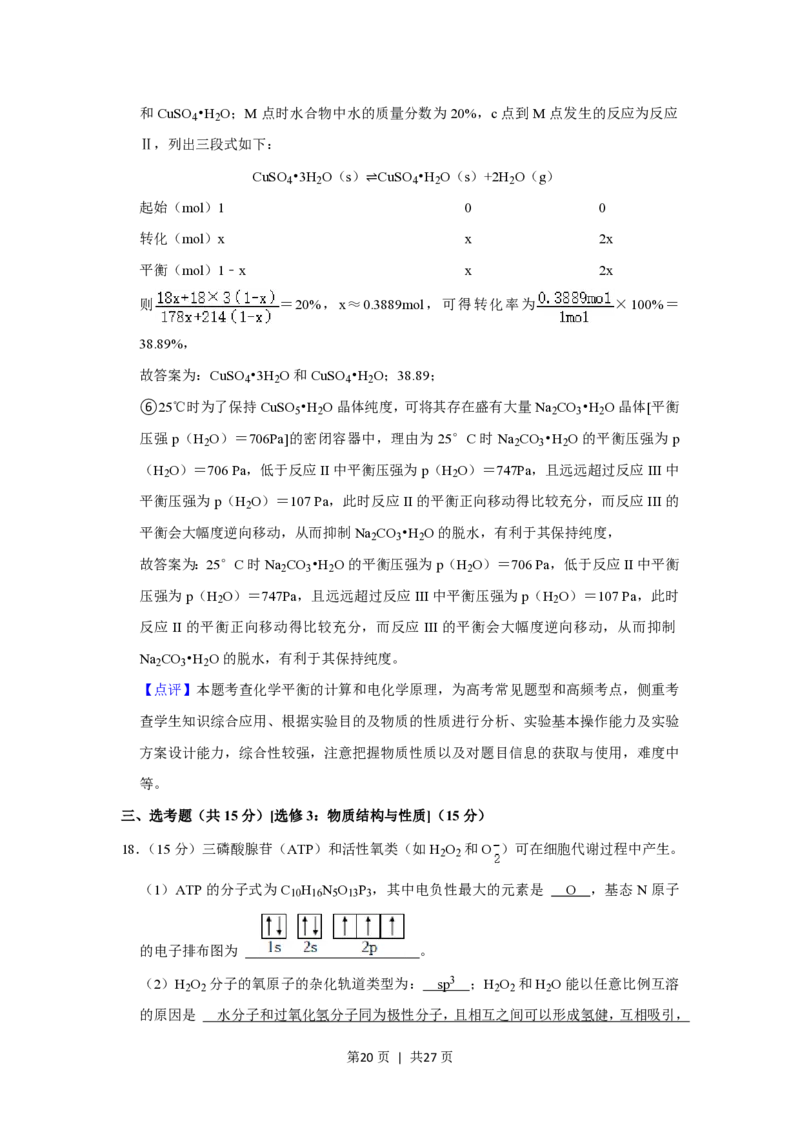
17.(14分)含结晶水的无机物可应用在吸波材料、电极材料和相变储能材料等领域。胆矾
(CaSO •5H O)是一种重要的结晶水合物。
4 2
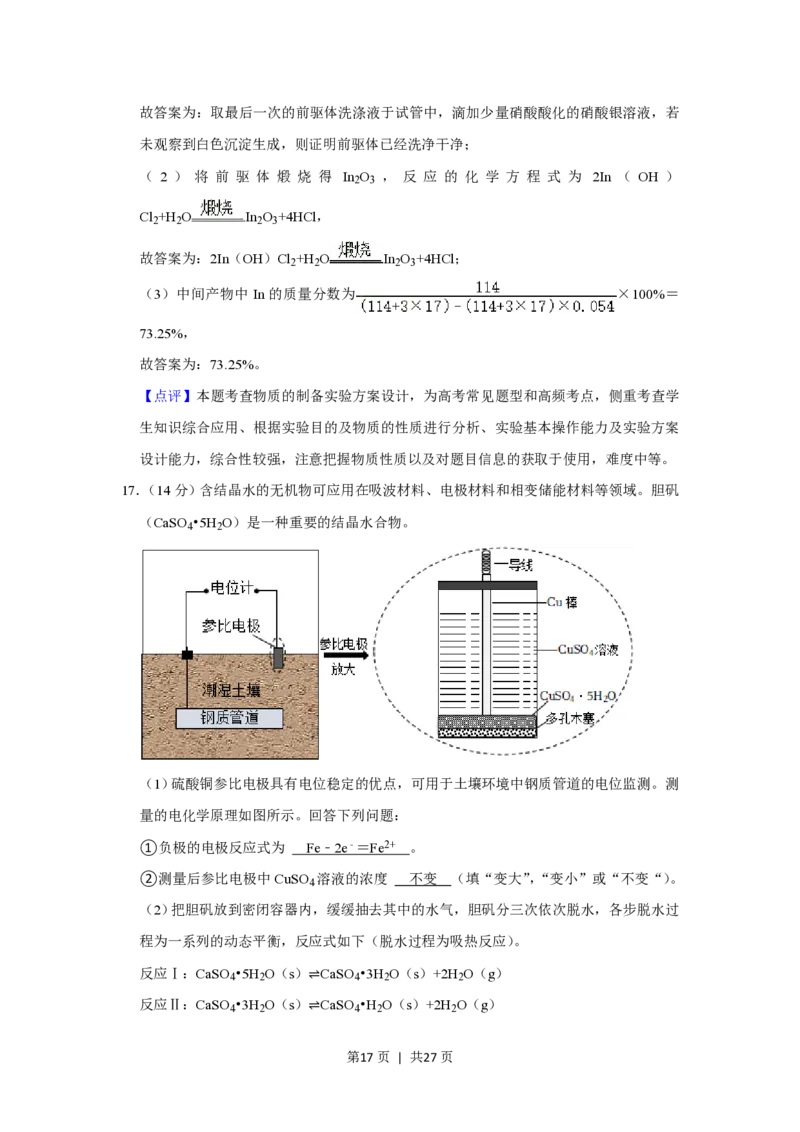
(1)硫酸铜参比电极具有电位稳定的优点,可用于土壤环境中钢质管道的电位监测。测
量的电化学原理如图所示。回答下列问题:
①负极的电极反应式为 Fe﹣2e﹣=Fe2+ 。
②测量后参比电极中CuSO 溶液的浓度 不变 (填“变大”,“变小”或“不变“)。
4
(2)把胆矾放到密闭容器内,缓缓抽去其中的水气,胆矾分三次依次脱水,各步脱水过
程为一系列的动态平衡,反应式如下(脱水过程为吸热反应)。
反应Ⅰ:CaSO •5H O(s)⇌CaSO •3H O(s)+2H O(g)
4 2 4 2 2
反应Ⅱ:CaSO •3H O(s)⇌CaSO •H O(s)+2H O(g)
4 2 4 2 2
第17页 | 共27页反应Ⅲ:CaSO •H O(s)⇌CuSO (s)+H O(g)
4 2 4 2
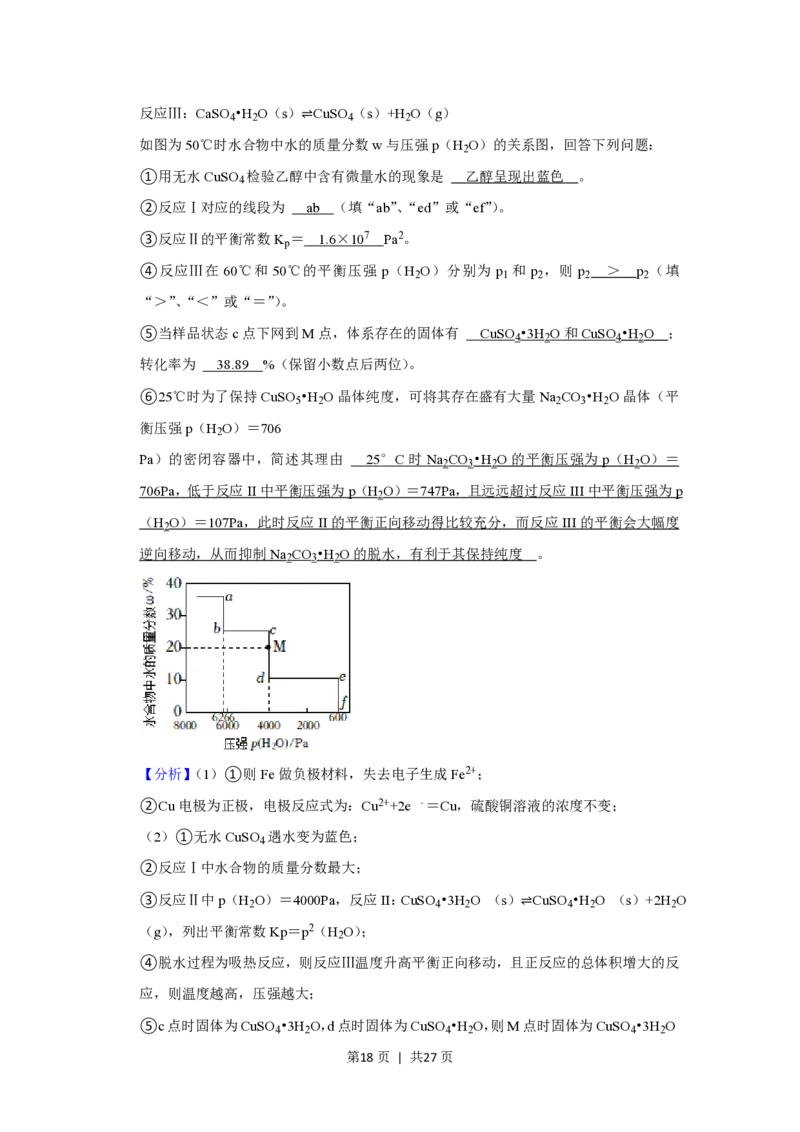
如图为50℃时水合物中水的质量分数w与压强p(H O)的关系图,回答下列问题:
2
①用无水CuSO 检验乙醇中含有微量水的现象是 乙醇呈现出蓝色 。
4
②反应Ⅰ对应的线段为 ab (填“ab”、“ed”或“ef”)。
③反应Ⅱ的平衡常数K = 1.6×107 Pa2。
p
④反应Ⅲ在 60℃和 50℃的平衡压强 p(H O)分别为 p 和 p ,则 p > p (填
2 1 2 2 2
“>”、“<”或“=”)。
⑤当样品状态c点下网到M点,体系存在的固体有 CuSO •3H O和CuSO •H O ;
4 2 4 2
转化率为 38.89 %(保留小数点后两位)。
⑥25℃时为了保持CuSO •H O晶体纯度,可将其存在盛有大量Na CO •H O晶体(平
5 2 2 3 2
衡压强p(H O)=706
2
Pa)的密闭容器中,简述其理由 25°C时Na CO •H O的平衡压强为p(H O)=
2 3 2 2
706Pa,低于反应II中平衡压强为p(H O)=747Pa,且远远超过反应III中平衡压强为p
2
(H O)=107Pa,此时反应II的平衡正向移动得比较充分,而反应III的平衡会大幅度
2
逆向移动,从而抑制Na CO •H O的脱水,有利于其保持纯度 。
2 3 2
【分析】(1)①则Fe做负极材料,失去电子生成Fe2+;
②Cu电极为正极,电极反应式为:Cu2++2e ﹣=Cu,硫酸铜溶液的浓度不变;
(2)①无水CuSO 遇水变为蓝色;
4
②反应Ⅰ中水合物的质量分数最大;
③反应Ⅱ中p(H O)=4000Pa,反应II:CuSO •3H O (s)⇌CuSO •H O (s)+2H O
2 4 2 4 2 2
(g),列出平衡常数Kp=p2(H O);
2
④脱水过程为吸热反应,则反应Ⅲ温度升高平衡正向移动,且正反应的总体积增大的反
应,则温度越高,压强越大;
⑤c点时固体为CuSO •3H O,d点时固体为CuSO •H O,则M点时固体为CuSO •3H O
4 2 4 2 4 2
第18页 | 共27页和CuSO •H O;M点时水合物中水的质量分数为20%,c点到M点发生的反应为反应
4 2
Ⅱ,列出三段式如下:
CuSO •3H O(s)⇌CuSO •H O(s)+2H O(g)
4 2 4 2 2
起始(mol)1 0 0
转化(mol)x x 2x
平衡(mol)1﹣x x 2x
则 =20%,x≈0.3889mol;
⑥25°C时Na CO •H O的平衡压强为p(H O)=706 Pa,低于反应II中平衡压强为p
2 3 2 2
(H O)=747Pa,此时反应II的平衡正向移动得比较充分,而反应III的平衡会大幅度
2
逆向移动,有利于其保持纯度。
【解答】解:(1)①钢制管道、参比电极、潮湿土壤构成原电池,参比电极为Cu电极,
钢制管道为铁电极,金属性Fe>Cu,则Fe做负极材料,负极的电极反应式为:Fe﹣2e ﹣=
Fe2+,
故答案为:Fe﹣2e ﹣=Fe2+;
②Cu电极为正极,电极反应式为:Cu2++2e ﹣=Cu;,CuSO •5H O溶解与电解质溶液
4 2
中,此时硫酸铜溶液的浓度不变,
故答案为:不变;
(2)①无水CuSO 遇水变为蓝色,则用无水CuSO 检验乙醇中含有微量水的现象是:
4 4
乙醇变为蓝色,
故答案为:乙醇呈现出蓝色;
②反应Ⅰ中水合物的质量分数最大,符合条件的线段为ab,
故答案为:ab;
③反应Ⅱ中p(H O)=4000Pa,反应II:CuSO •3H O (s)⇌CuSO •H O (s)+2H O
2 4 2 4 2 2
(g),列出平衡常数Kp=p2(H O)=(4000pa)2=1.6×107,
2
故答案为:1.6×107;
④脱水过程为吸热反应,则反应Ⅲ温度升高平衡正向移动,且正反应的总体积增大的反
应,则温度越高,压强越大,则p >p ,
1 2
故答案为:>;
⑤c点时固体为CuSO •3H O,d点时固体为CuSO •H O,则M点时固体为CuSO •3H O
4 2 4 2 4 2
第19页 | 共27页和CuSO •H O;M点时水合物中水的质量分数为20%,c点到M点发生的反应为反应
4 2
Ⅱ,列出三段式如下:
CuSO •3H O(s)⇌CuSO •H O(s)+2H O(g)
4 2 4 2 2
起始(mol)1 0 0
转化(mol)x x 2x
平衡(mol)1﹣x x 2x
则 =20%,x≈0.3889mol,可得转化率为 ×100%=
38.89%,
故答案为:CuSO •3H O和CuSO •H O;38.89;
4 2 4 2
⑥25℃时为了保持CuSO •H O晶体纯度,可将其存在盛有大量Na CO •H O晶体[平衡
5 2 2 3 2
压强p(H O)=706Pa]的密闭容器中,理由为25°C时Na CO •H O的平衡压强为p
2 2 3 2
(H O)=706 Pa,低于反应II中平衡压强为p(H O)=747Pa,且远远超过反应III中
2 2
平衡压强为p(H O)=107 Pa,此时反应II的平衡正向移动得比较充分,而反应III的
2
平衡会大幅度逆向移动,从而抑制Na CO •H O的脱水,有利于其保持纯度,
2 3 2
故答案为:25°C时Na CO •H O的平衡压强为p(H O)=706 Pa,低于反应II中平衡
2 3 2 2
压强为p(H O)=747Pa,且远远超过反应III中平衡压强为p(H O)=107 Pa,此时
2 2
反应 II 的平衡正向移动得比较充分,而反应 III 的平衡会大幅度逆向移动,从而抑制
Na CO •H O的脱水,有利于其保持纯度。
2 3 2
【点评】本题考查化学平衡的计算和电化学原理,为高考常见题型和高频考点,侧重考
查学生知识综合应用、根据实验目的及物质的性质进行分析、实验基本操作能力及实验
方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取与使用,难度中
等。
三、选考题(共15分)[选修3:物质结构与性质](15分)
18.(15分)三磷酸腺苷(ATP)和活性氧类(如H O 和O )可在细胞代谢过程中产生。
2 2
(1)ATP的分子式为C H N O P ,其中电负性最大的元素是 O ,基态N原子
10 16 5 13 3
的电子排布图为 。
(2)H O 分子的氧原子的杂化轨道类型为: sp3 ;H O 和H O能以任意比例互溶
2 2 2 2 2
的原因是 水分子和过氧化氢分子同为极性分子,且相互之间可以形成氢健,互相吸引,
第20页 | 共27页并且它们的结构相似,相似相溶,所以可以任意比例互溶 。
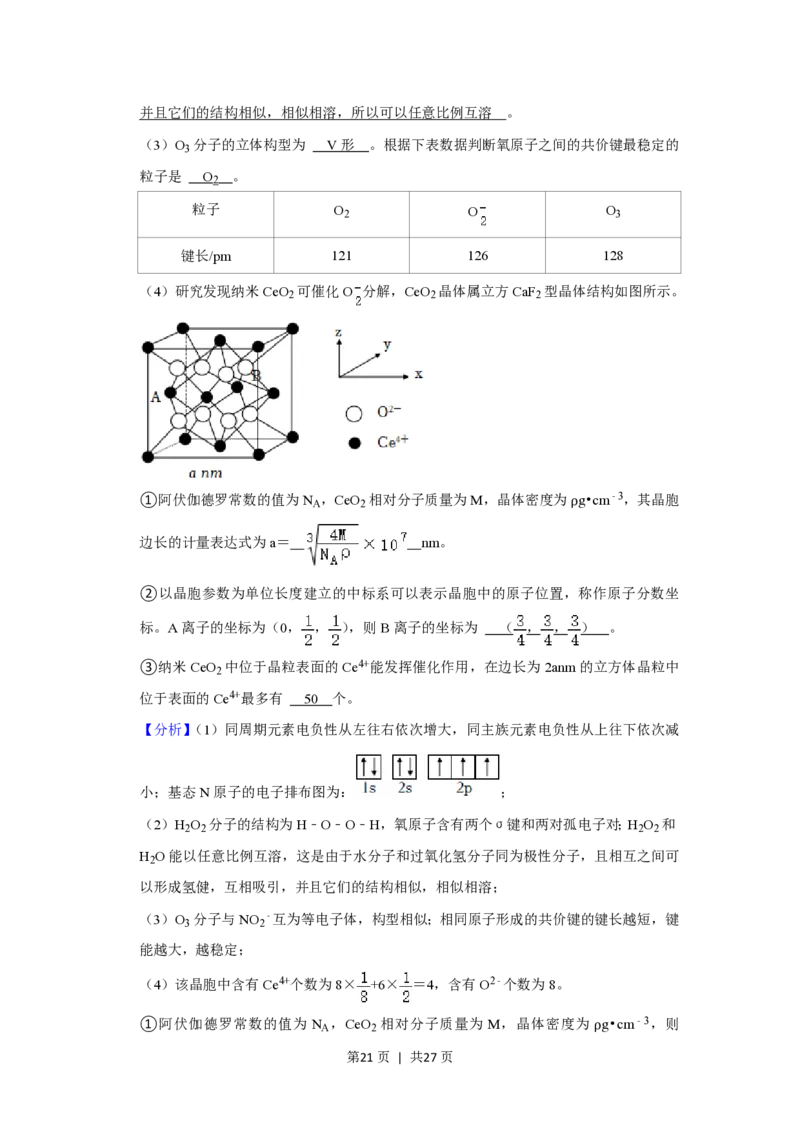
(3)O 分子的立体构型为 V形 。根据下表数据判断氧原子之间的共价键最稳定的
3
粒子是 O 。
2
粒子 O 2 O O 3
键长/pm 121 126 128
(4)研究发现纳米CeO 可催化O 分解,CeO 晶体属立方CaF 型晶体结构如图所示。
2 2 2
①阿伏伽德罗常数的值为N ,CeO 相对分子质量为M,晶体密度为ρg•cm﹣3,其晶胞
A 2
边长的计量表达式为a= nm。
②以晶胞参数为单位长度建立的中标系可以表示晶胞中的原子位置,称作原子分数坐
标。A离子的坐标为(0, , ),则B离子的坐标为 ( , , ) 。
③纳米CeO 中位于晶粒表面的Ce4+能发挥催化作用,在边长为2anm的立方体晶粒中
2
位于表面的Ce4+最多有 50 个。
【分析】(1)同周期元素电负性从左往右依次增大,同主族元素电负性从上往下依次减
小;基态N原子的电子排布图为: ;
(2)H O 分子的结构为H﹣O﹣O﹣H,氧原子含有两个σ键和两对孤电子对;H O 和
2 2 2 2
H O能以任意比例互溶,这是由于水分子和过氧化氢分子同为极性分子,且相互之间可
2
以形成氢健,互相吸引,并且它们的结构相似,相似相溶;
(3)O 分子与NO ﹣互为等电子体,构型相似;相同原子形成的共价键的键长越短,键
3 2
能越大,越稳定;
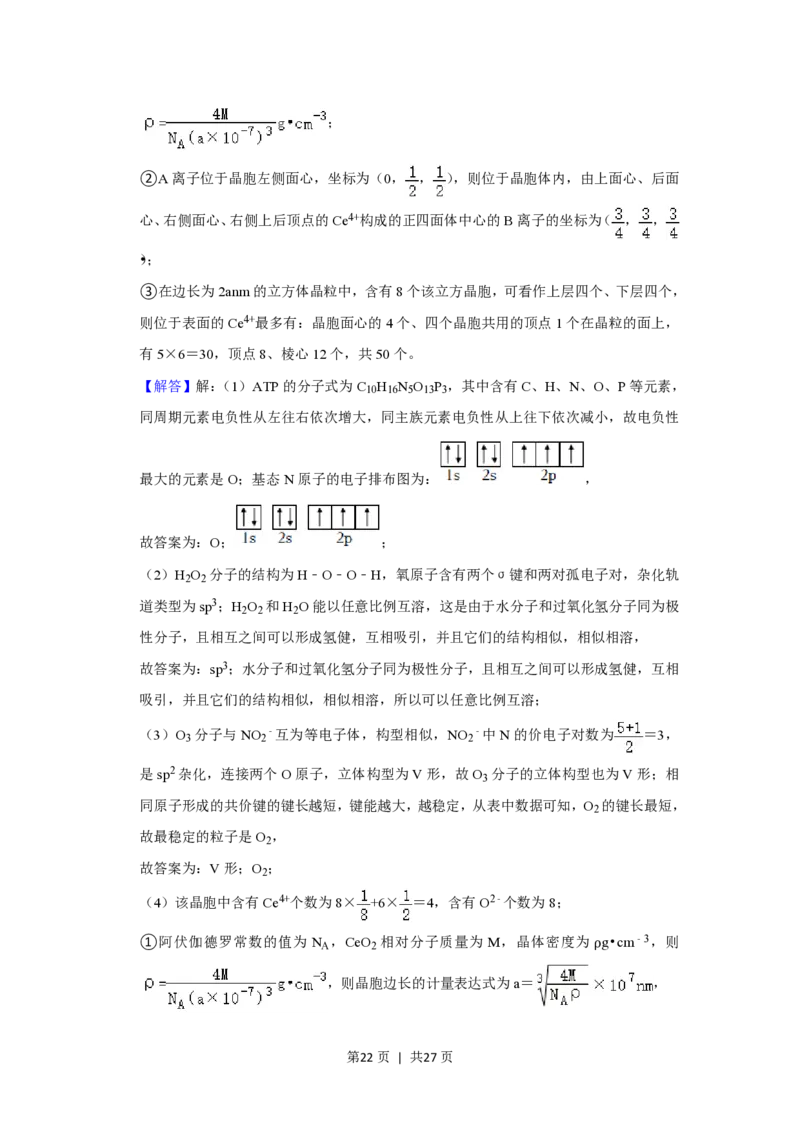
(4)该晶胞中含有Ce4+个数为8× +6× =4,含有O2﹣个数为8。
①阿伏伽德罗常数的值为 N ,CeO 相对分子质量为 M,晶体密度为 ρg•cm﹣3,则
A 2
第21页 | 共27页;
②A离子位于晶胞左侧面心,坐标为(0, , ),则位于晶胞体内,由上面心、后面
心、右侧面心、右侧上后顶点的Ce4+构成的正四面体中心的B离子的坐标为( , ,
•);
③在边长为2anm的立方体晶粒中,含有8个该立方晶胞,可看作上层四个、下层四个,
则位于表面的Ce4+最多有:晶胞面心的4个、四个晶胞共用的顶点1个在晶粒的面上,
有5×6=30,顶点8、棱心12个,共50个。
【解答】解:(1)ATP的分子式为C H N O P ,其中含有C、H、N、O、P等元素,
10 16 5 13 3
同周期元素电负性从左往右依次增大,同主族元素电负性从上往下依次减小,故电负性
最大的元素是O;基态N原子的电子排布图为: ,
故答案为:O; ;
(2)H O 分子的结构为H﹣O﹣O﹣H,氧原子含有两个σ键和两对孤电子对,杂化轨
2 2
道类型为sp3;H O 和H O能以任意比例互溶,这是由于水分子和过氧化氢分子同为极
2 2 2
性分子,且相互之间可以形成氢健,互相吸引,并且它们的结构相似,相似相溶,
故答案为:sp3;水分子和过氧化氢分子同为极性分子,且相互之间可以形成氢健,互相
吸引,并且它们的结构相似,相似相溶,所以可以任意比例互溶;
(3)O 分子与NO ﹣互为等电子体,构型相似,NO ﹣中N的价电子对数为 =3,
3 2 2
是sp2杂化,连接两个O原子,立体构型为V形,故O 分子的立体构型也为V形;相
3
同原子形成的共价键的键长越短,键能越大,越稳定,从表中数据可知,O 的键长最短,
2
故最稳定的粒子是O ,
2
故答案为:V形;O ;
2
(4)该晶胞中含有Ce4+个数为8× +6× =4,含有O2﹣个数为8;
①阿伏伽德罗常数的值为 N ,CeO 相对分子质量为 M,晶体密度为 ρg•cm﹣3,则
A 2
,则晶胞边长的计量表达式为a= ,
第22页 | 共27页故答案为: ;
②A离子位于晶胞左侧面心,坐标为(0, , ),则位于晶胞体内,由上面心、后面
心、右侧面心、右侧上后顶点的Ce4+构成的正四面体中心的B离子的坐标为( , ,
),
故答案为:( , , );
③在边长为2anm的立方体晶粒中,含有8个该立方晶胞,可看作上层四个、下层四个,
则位于表面的Ce4+最多有:晶胞面心的4个、四个晶胞共用的顶点1个在晶粒的面上,
有5×6=30,顶点8、棱心12个,共50个,
故答案为:50。
【点评】本题主要考查电子排布图、电负性、晶胞的计算、氢键、简单离子或分子的空
间构型等知识,题目难度一般。
[选修5:有机化学基础]
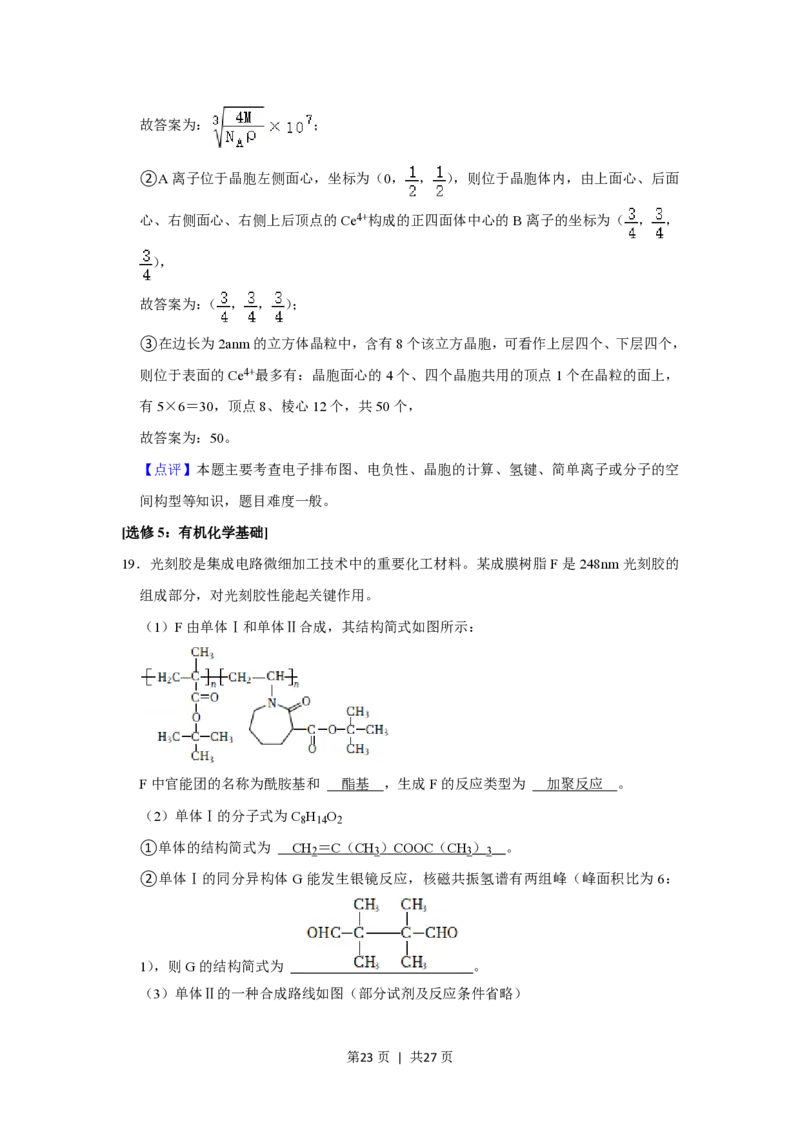
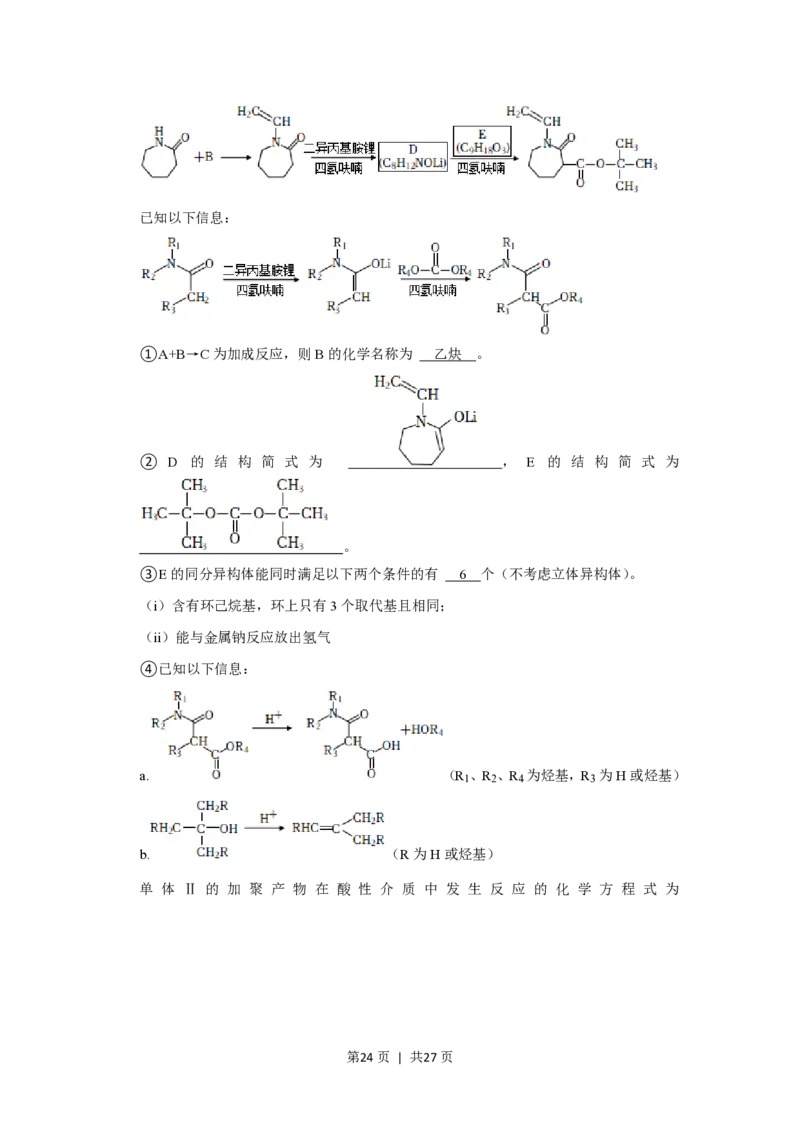
19.光刻胶是集成电路微细加工技术中的重要化工材料。某成膜树脂F是248nm光刻胶的
组成部分,对光刻胶性能起关键作用。
(1)F由单体Ⅰ和单体Ⅱ合成,其结构简式如图所示:
F中官能团的名称为酰胺基和 酯基 ,生成F的反应类型为 加聚反应 。
(2)单体Ⅰ的分子式为C H O
8 14 2
①单体的结构简式为 CH =C(CH )COOC(CH ) 。
2 3 3 3
②单体Ⅰ的同分异构体G能发生银镜反应,核磁共振氢谱有两组峰(峰面积比为6:
1),则G的结构简式为 。
(3)单体Ⅱ的一种合成路线如图(部分试剂及反应条件省略)
第23页 | 共27页已知以下信息:
①A+B→C为加成反应,则B的化学名称为 乙炔 。
② D 的 结 构 简 式 为 , E 的 结 构 简 式 为
。
③E的同分异构体能同时满足以下两个条件的有 6 个(不考虑立体异构体)。
(i)含有环己烷基,环上只有3个取代基且相同;
(ii)能与金属钠反应放出氢气
④已知以下信息:
a. (R 、R 、R 为烃基,R 为H或烃基)
1 2 4 3
b. (R为H或烃基)
单 体 Ⅱ 的 加 聚 产 物 在 酸 性 介 质 中 发 生 反 应 的 化 学 方 程 式 为
第24页 | 共27页+(CH )C=CH 。
3 2 2
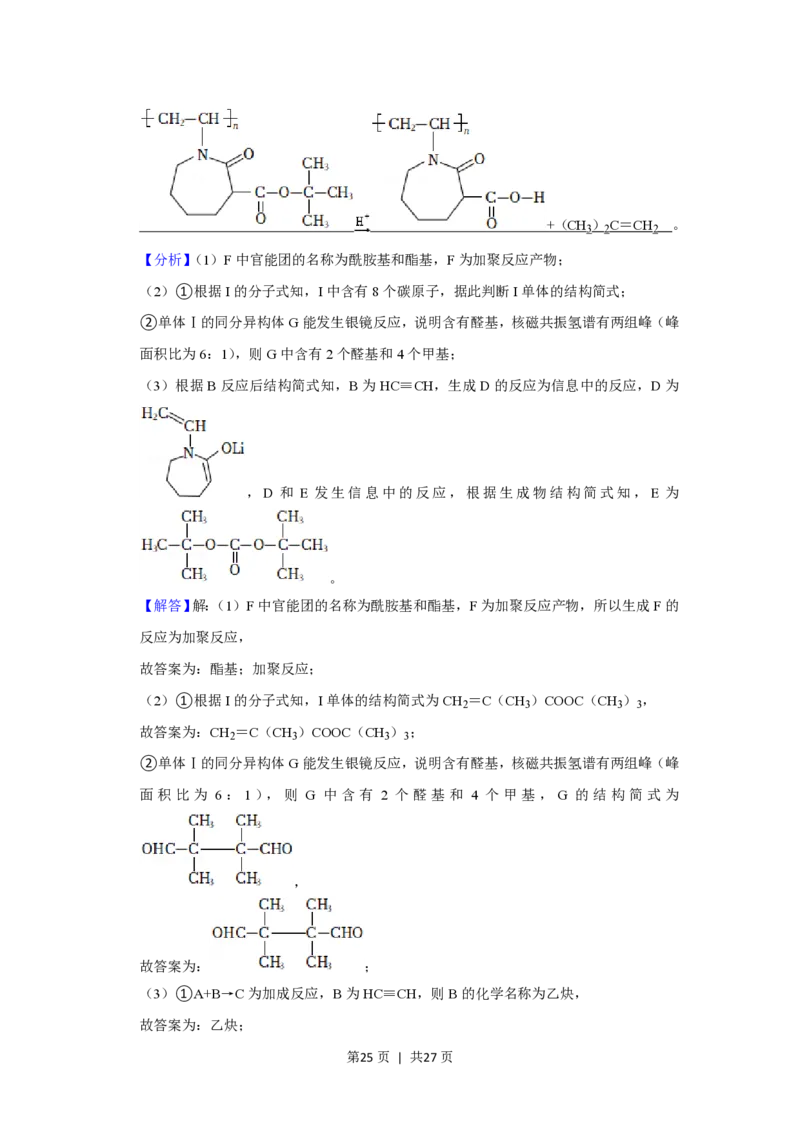
【分析】(1)F中官能团的名称为酰胺基和酯基,F为加聚反应产物;
(2)①根据I的分子式知,I中含有8个碳原子,据此判断I单体的结构简式;
②单体Ⅰ的同分异构体G能发生银镜反应,说明含有醛基,核磁共振氢谱有两组峰(峰
面积比为6:1),则G中含有2个醛基和4个甲基;
(3)根据B反应后结构简式知,B为HC≡CH,生成D的反应为信息中的反应,D为
,D 和 E 发生信息中的反应,根据生成物结构简式知,E 为
。
【解答】解:(1)F中官能团的名称为酰胺基和酯基,F为加聚反应产物,所以生成F的
反应为加聚反应,
故答案为:酯基;加聚反应;
(2)①根据I的分子式知,I单体的结构简式为CH =C(CH )COOC(CH ) ,
2 3 3 3
故答案为:CH =C(CH )COOC(CH ) ;
2 3 3 3
②单体Ⅰ的同分异构体G能发生银镜反应,说明含有醛基,核磁共振氢谱有两组峰(峰
面积比为 6:1),则 G 中含有 2 个醛基和 4 个甲基,G 的结构简式为
,
故答案为: ;
(3)①A+B→C为加成反应,B为HC≡CH,则B的化学名称为乙炔,
故答案为:乙炔;
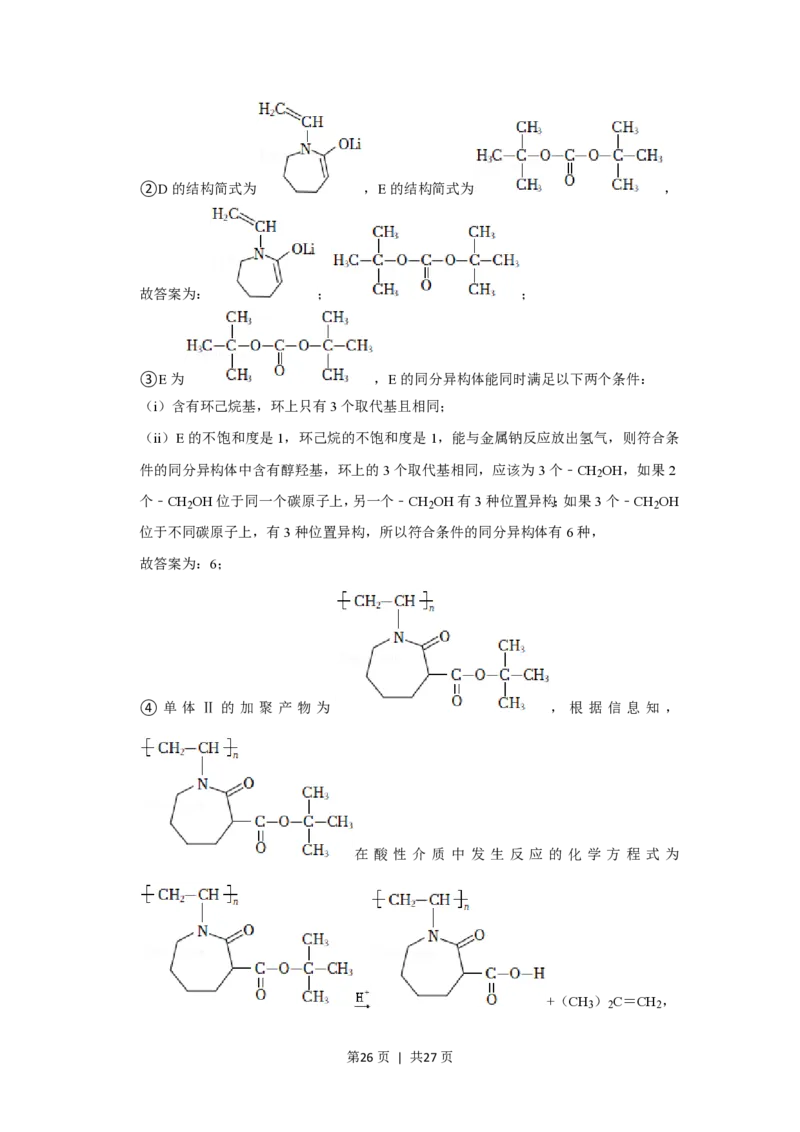
第25页 | 共27页②D的结构简式为 ,E的结构简式为 ,
故答案为: ; ;
③E为 ,E的同分异构体能同时满足以下两个条件:
(i)含有环己烷基,环上只有3个取代基且相同;
(ii)E的不饱和度是1,环己烷的不饱和度是1,能与金属钠反应放出氢气,则符合条
件的同分异构体中含有醇羟基,环上的3个取代基相同,应该为3个﹣CH OH,如果2
2
个﹣CH OH位于同一个碳原子上,另一个﹣CH OH有3种位置异构;如果3个﹣CH OH
2 2 2
位于不同碳原子上,有3种位置异构,所以符合条件的同分异构体有6种,
故答案为:6;
④ 单 体 Ⅱ 的 加 聚 产 物 为 , 根 据 信 息 知 ,
在 酸 性 介 质 中 发 生 反 应 的 化 学 方 程 式 为
+(CH ) C=CH ,
3 2 2
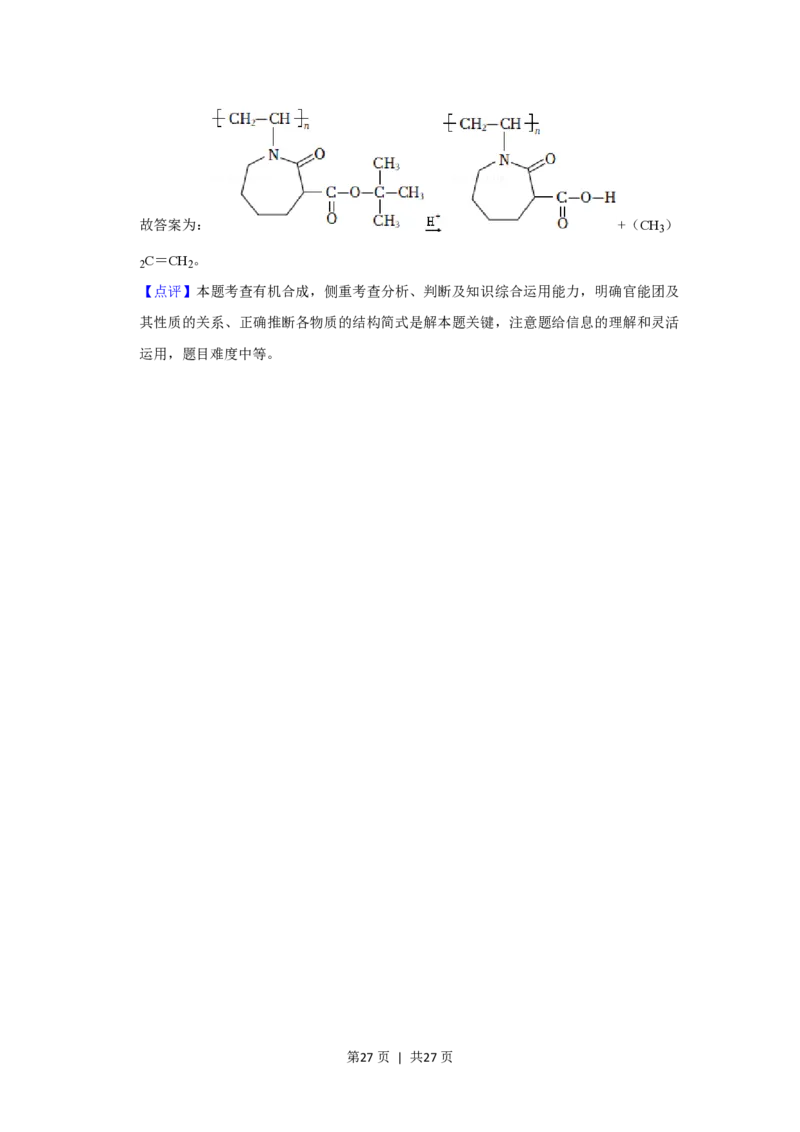
第26页 | 共27页故答案为: +(CH )
3
C=CH 。
2 2
【点评】本题考查有机合成,侧重考查分析、判断及知识综合运用能力,明确官能团及
其性质的关系、正确推断各物质的结构简式是解本题关键,注意题给信息的理解和灵活
运用,题目难度中等。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布日期:2022/7/28 20:16:35;用户:177******05;邮箱:A9C4F49D02B1356BCB9F3152DA52BF7A@huawei.jyeoo.com;学号:43705123
第27页 | 共27页