文档内容
专练 62 实验方案的设计与评价
授课提示:对应学生用书123页
1.[2022·全国甲卷]根据实验目的,下列实验及现象、结论都正确的是( )
选项 实验目的 实验及现象 结论
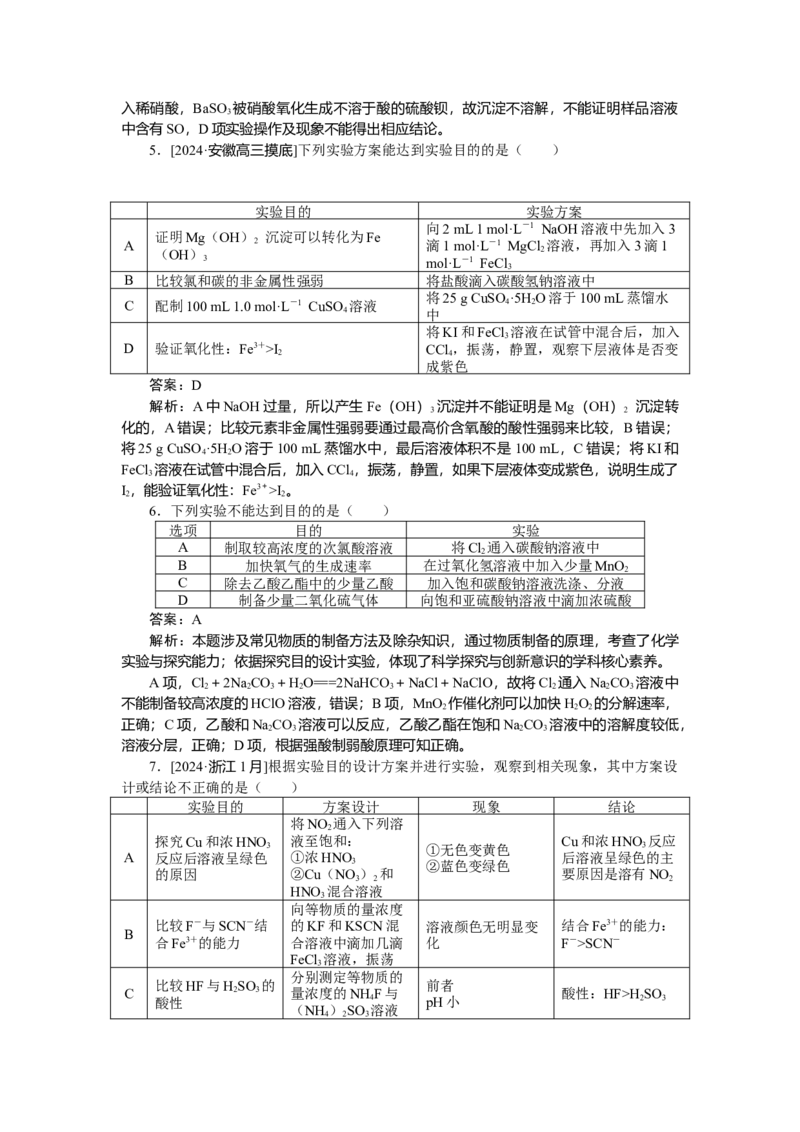
分别测浓度均为0.1 mol·L
比较CHCOO-和HCO的 -1的CHCOONH 和 K (CHCOO-)I CCl ,振荡,静置,观察下层液体是否变
2 4
成紫色
答案:D
解析:A中NaOH过量,所以产生Fe(OH) 沉淀并不能证明是Mg(OH) 沉淀转
3 2
化的,A错误;比较元素非金属性强弱要通过最高价含氧酸的酸性强弱来比较,B错误;
将25 g CuSO ·5H O溶于100 mL蒸馏水中,最后溶液体积不是100 mL,C错误;将KI和
4 2
FeCl 溶液在试管中混合后,加入CCl ,振荡,静置,如果下层液体变成紫色,说明生成了
3 4
I,能验证氧化性:Fe3+>I 。
2 2
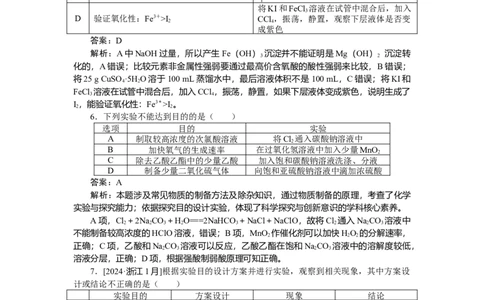
6.下列实验不能达到目的的是( )
选项 目的 实验
A 制取较高浓度的次氯酸溶液 将Cl 通入碳酸钠溶液中
2
B 加快氧气的生成速率 在过氧化氢溶液中加入少量MnO
2
C 除去乙酸乙酯中的少量乙酸 加入饱和碳酸钠溶液洗涤、分液
D 制备少量二氧化硫气体 向饱和亚硫酸钠溶液中滴加浓硫酸
答案:A
解析:本题涉及常见物质的制备方法及除杂知识,通过物质制备的原理,考查了化学
实验与探究能力;依据探究目的设计实验,体现了科学探究与创新意识的学科核心素养。
A项,Cl +2NaCO +HO===2NaHCO +NaCl+NaClO,故将Cl 通入NaCO 溶液中
2 2 3 2 3 2 2 3
不能制备较高浓度的HClO溶液,错误;B项,MnO 作催化剂可以加快HO 的分解速率,
2 2 2
正确;C项,乙酸和NaCO 溶液可以反应,乙酸乙酯在饱和NaCO 溶液中的溶解度较低,
2 3 2 3
溶液分层,正确;D项,根据强酸制弱酸原理可知正确。
7.[2024·浙江1月]根据实验目的设计方案并进行实验,观察到相关现象,其中方案设
计或结论不正确的是( )
实验目的 方案设计 现象 结论
将NO 通入下列溶
2
探究Cu和浓HNO 液至饱和: Cu和浓HNO 反应
3 ①无色变黄色 3
A 反应后溶液呈绿色 ①浓HNO 后溶液呈绿色的主
3 ②蓝色变绿色
的原因 ②Cu(NO ) 和 要原因是溶有NO
3 2 2
HNO 混合溶液
3
向等物质的量浓度
比较F-与SCN-结 的KF和KSCN混 溶液颜色无明显变 结合Fe3+的能力:
B
合Fe3+的能力 合溶液中滴加几滴 化 F->SCN-
FeCl 溶液,振荡
3
分别测定等物质的
比较HF与HSO 的 前者
C 2 3 量浓度的NH F与 酸性:HF>H SO
酸性 4 pH小 2 3
(NH )SO 溶液
4 2 3的pH
等体积、等物质的
探究温度对反应速 量浓度的NaSO 温度高的溶液中先 温度升高,该反应
D 2 2 3
率的影响 与HSO 溶液在不 出现浑浊 速率加快
2 4
同温度下反应
答案:C
解析:Cu和浓HNO 反应后得到Cu(NO ) 和HNO 的混合溶液,通过比较①和②的
3 3 2 3
实验现象可知,溶液呈绿色的主要原因是溶有NO ,A项正确;Fe3+遇SCN-溶液变成血红
2
色,但实验现象中溶液颜色无明显变化,说明Fe3+没有与SCN-结合而与F-结合,则结合
Fe3+的能力:F->SCN-,B项正确;同浓度的NH F与(NH ) SO 溶液中NH浓度不等,
4 4 2 3
无法形成对比实验,不能进行比较,并且亚硫酸的酸性大于氢氟酸,C项错误;实验中只
有温度一个变量,能探究温度对反应速率的影响,且温度高的溶液中先出现浑浊,说明温
度升高,反应速率加快,D项正确。
8.[2022·江苏卷]室温下,下列实验探究方案不能达到探究目的的是( )
选项 探究方案 探究目的
向盛有FeSO 溶液的试管中滴加几滴KSCN溶液,振
A 4 Fe2+具有还原性
荡,再滴加几滴新制氯水,观察溶液颜色变化
向盛有SO 水溶液的试管中滴加几滴品红溶液,振荡,
B 2 SO 具有漂白性
加热试管,观察溶液颜色变化 2
向盛有淀粉KI溶液的试管中滴加几滴溴水,振荡,观察
C Br 的氧化性比I 的强
溶液颜色变化 2 2
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 CHCOOH是弱电解质
3
答案:D
解析:A项,向FeSO 溶液中滴加几滴KSCN溶液,无现象,振荡,再滴加几滴新制
4
氯水,溶液变为红色,说明Fe2+被新制氯水氧化,能证明Fe2+具有还原性,不符合题意;
B项,向SO 水溶液中滴加几滴品红溶液,品红溶液褪色,振荡,加热试管,溶液又恢复
2
红色,能证明SO 具有漂白性,不符合题意;C项,向盛有淀粉KI溶液的试管中滴加几滴
2
溴水,振荡,溶液变为蓝色,说明Br 将KI氧化成了I,能证明Br 的氧化性比I 的强,不
2 2 2 2
符合题意;D项,没有给出醋酸和盐酸的浓度,故不能通过pH判断CHCOOH是弱电解质,
3
符合题意。
9.[2024·哈尔滨师大附中高三开学考试]下列三组实验进行一段时间后,溶液中均有白
色沉淀生成,下列结论不正确的是( )
实验① 实验② 实验③
A.实验①中生成的沉淀是BaCO
3
B.实验①中有气体生成
C.实验②沉淀中可能含有BaSO
4
D.实验③生成沉淀的离子方程式是:Ba2++HSO ===BaSO ↓+2H+
2 3 3
答案:D
解析:碳酸氢钠溶液中存在碳酸氢根离子的电离过程,电离生成的碳酸根离子能够与
钡离子反应生成碳酸钡沉淀,故A正确;实验①中形成沉淀时促进碳酸氢根离子的电离,
溶液的酸性逐渐增强,氢离子与碳酸氢根离子反应放出二氧化碳气体,故 B正确;实验②中亚硫酸钠与氯化钡反应生成亚硫酸钡沉淀,亚硫酸钡被空气中的氧气氧化生成硫酸钡,
故C正确;实验③中,如果发生Ba2++HSO ===BaSO ↓+2H+,生成的亚硫酸钡能够被
2 3 3
氢离子溶解,应该是亚硫酸被氧化生成了硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,故 D
错误。
10.下列实验操作能达到实验目的的是( )
A.用经水湿润的pH试纸测量溶液的pH
B.将 4.0 g NaOH 固体置于 100 mL 容量瓶中,加水至刻度,配制 1.000 mol·L-1
NaOH溶液
C.用装置甲蒸干AlCl 溶液制无水AlCl 固体
3 3
D.用装置乙除去实验室所制乙烯中的少量SO
2
答案:D
解析:A项,用pH试纸测溶液的pH时,用水湿润pH试纸相当于稀释溶液,可能导
致测量的pH出现误差,错误;B项,不能在容量瓶中直接溶解固体溶质,错误;C项,
AlCl 易水解,在加热蒸干AlCl 溶液时,HCl挥发,留下的固体是Al(OH) ,错误;D
3 3 3
项,SO 可被NaOH溶液吸收,CH===CH 与NaOH溶液不反应且不溶于NaOH溶液,正
2 2 2
确。
11.[2024·辽宁六校协作体上学期联考]Y形管是一种特殊的仪器,与其他仪器组合可
以进行某些实验探究。利用下图装置可以探究SO 与BaCl 反应生成BaSO 沉淀的条件。下
2 2 3
列判断正确的是( )
A.玻璃管的作用是连通大气,平衡压强
B.c、d两根导管都必须插入BaCl 溶液中,保证气体与Ba2+充分接触
2
C.Y形管乙中产生的为氧化性气体,将BaSO 氧化为BaSO 沉淀
3 4
D.e、f两管中的试剂可以分别是浓氨水和浓HSO
2 4
答案:A
解析:玻璃管的作用是连通大气,平衡压强,以便左右两边产生的气体顺利导入, A
正确; 如果产生的是氨气,氨气极易溶于水,为了防止倒吸,产生氨气的导管不能插入
BaCl 溶液中, B错误; SO 与BaCl 不反应,氧化性气体将溶液中的亚硫酸根离子氧化
2 2 2
成硫酸根离子,而不是将BaSO 氧化为BaSO 沉淀, C错误;e、f两管中的试剂可以分别
3 4
是浓氨水和NaOH,产生氨气碱性气体与SO 反应生成SO, 从而生成BaSO 沉淀,而浓
2 3
氨水与浓HSO 不能产生NH ,D错误。
2 4 3