文档内容
责任编辑 黄金国 经上海市中小学教材审查委员会 高级中学课本
高
整体设计 陈 蕾
审查准予试用 准用号 Ⅱ -GB-2007019
级
中
学
课
本
化
学
高
中
二
年
级
第
一
学 高中二年级第一学期
期
) (试用本)
试
用
本
)
高级中学课本
化 学
高中二年级第一学期
(试用本)
上海市中小学(幼儿园)课程改革委员会
上海世纪出版股份有限公司
出版
上 海 科 学 技 术 出 版 社
(上海钦州南路71号,邮政编码200235)
上海新华书店发行 上海中华印刷厂印刷
开本890×1240 1/16 印张4.5
上
2007年8月第1版 2007年8月第1次印刷
海
印数: 1-00 000
科
ISBN 978-7-5323-8971-1 学
技
术
定价:5.25元
出
版
上海市物价局价格审查批准文号:沪价商专(2007)24号 此书如有印、装质量问题,请径向本社调换 社
全国物价举报电话:12358 上海科学技术出版社电话:64089888
上海科学技术出版社高级中学课本
高中二年级第一学期
(试用本)
上海科学技术出版社目 录
8
走进精彩纷呈的金属世界
GO INTO THE SPLENDID
METALLIC WORLD
3◆ 8.1 应用广泛的金属材料——钢铁
13◆ 8.2 铝和铝合金的崛起
9
初识元素周期律
PRELIMINARY RECOGNIZE
PERIODIC LAW OF ELEMENTS
27◆ 9.1 元素周期律
32◆ 9.2 元素周期表
目录110
学习几种定量测定方法
STUDY SOME METHODS OF
QUANTITATIVE ESTIMATION
47◆ 10.1 测定1 mol气体的体积
52◆ 10.2 结晶水合物中结晶水含量的测定
56◆ 10.3 酸碱滴定
附录
65◆ Ⅰ 元素周期表
66◆ Ⅱ 化学词汇英中文对照表
2目录8
走进精彩纷呈的金属世界
GO INTO THE SPLENDID METALLIC WORLD
◆ 金属和金属键 ◆ 铝的性质
◆ 铁的性质 ◆ 铝合金
◆ 铁合金
1
out-8ok Page 1 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC在
人类社会发展的历史上,经历了以金属命
名的青铜器时代、铁器时代,它们分别标
志生产力发展的不同阶段。产业革命后钢
铁的大规模发展和应用,使金属在材料中占了绝对优势。
在构成宇宙万物的一百多种元素中,金属约占了80%,
它们在现代工业和新材料、新技术研究中具有至关重要
的意义。
随着科学技术的飞速发展,金属材料虽然部分被合
成高分子材料与无机材料所替代,但是以金属为基体的
新材料不断涌现,功能多种多样。金属材料在一个国家
的国民经济中仍占举足轻重的地位。
本章我们既要学习一些重要的金属,如铁、铝,了
解它们在社会生产和人类生活中的重要作用,还要了解
21世纪为人瞩目的金属钛。
让我们一起到金属世界中遨游吧!
2
out-8ok Page 2 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC应用广泛的金属材料——钢铁
8
.1
(METALLIC MATERIALS WITH WIDE USE —— STEEL)
【资料库】
甘肃灵台出
由石器、青铜器到铁器
土秦国冶炼的铁
制品。
人类使用铁(iron)的历史,可以追溯到距今五千多
年前,在阿拉伯有“天上的金雨落在沙漠变成了黑铁”的
说法。那时候的铁是从天而降的陨铁,初期的铁十分珍
贵。人类从坐等“天石”到主动向地球索取铁,始于公元
前1500年左右,而真正使用铁制工具,则是公元前五六
百年的事了。
从石器时代到青铜器和铁器时代,是人类社会生产力
发展的不同阶段,铁制工具的使用,使生产力获得了巨大
发展。人类使用生产工具的进步推动着人类社会向前发展。
图 8.1 铜柄铁剑
图 8.2 古代炼铁
3
out-8ok Page 3 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC化学史话
铜和铁的冶炼史
铜是最早被人类广泛应用的金属。埃及在约公元前5000年开始利用红
铜与自然铜,公元前3500年制得青铜。中国约在公元前3000年的新石器时
代晚期开始使用红铜和青铜。在古埃及法老坟墓中的铜器、巴比伦废墟中的
铜饼和我国甘肃武威县出土的新石器晚期遗址中的铜器,都是人类利用天然
铜加工的器皿。
天然铜十分稀少,人类在制陶器的过程中,学会用炭还原铜矿,于是炼
铜技术应运而生。
自然界的铜矿常含锡、铅等金属氧化物,在还原铜时,这些金属也一起
被还原出来,形成青铜合金。青铜合金的制得和应用标志着人类从石器时代
进入了青铜器时代。
人类炼铁比炼铜要晚得多。在距今两千多年前,文明古国如埃及、巴比
伦、印度、中国等先后掌握了炼铁技术。
原始的炼铁方法是利用炭不完全燃烧时产生的一氧化碳,与铁矿石反
应,由于温度不高,生成的铁以固体状态沉在炉底,只有冷却后打破炼铁炉
才能取铁。用这种方法制得的铁,质地疏松,含有大量杂质,必须经过煅打,
除去杂质后才能使用。古诗中曾有描述“十年铸一剑,今日把示君”,反映
了铸剑之难。
我国在春秋战国时期使用了鼓风机,它使炼铁炉的温度高达1 200℃,可
以把炼得的熔铁从炉底放出,再浇铸成铁块。至西汉时期,我国已能将粗炼
得到的铁块掺炭,利用淬火技术得到坚硬的钢,以后又发明了灌钢技术。我
国古代先进的炼钢方法要比西方早一千多年。
金属和金属键
铜和铁以及19世纪后期崛起的铝都是用途广泛的金属。
金属和砖瓦、陶瓷等无机材料不同,具有金属的共性。
金属表面一般都有光泽,黄金、白银、铂金等饰品就是
利用了这一性质。
金属具有良好的延展性,可将它们拉成细丝或 击成薄
片。
图 8.3 黄金饰品
4
out-8ok Page 4 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC金属既能导电,又有优良的导热性。银的导电性和导
热性居金属首位。但由于价格问题,除在某些电子工业中
使用外,一般的电线都是用铜制成的。
金属具有共性,是因为它们具有相似的结构。金属原
子一般都以有规则的密堆积的方式形成金属晶体。由于金
属原子的半径较大,最外层电子容易释放成为自由电子。因
此金属晶体的结构实际上是释放出自由电子的金属离子按
一定的规律堆积起来的。金属离子间依靠自由电子而产生 图 8.4 铜丝
的强的相互作用就是金属键(metallic bond)。
若给金属通直流电,它的自由电子可以定向流动形成
电流。因此,金属都能导电。
当给金属的一端加热,金属内自由电子的热运动也易
从一端传到另一端。因此,金属都易导热。
金属块在受到外力击打或拉伸时,密堆积的金属原子
会移动使金属块变形,变成薄片或拉成丝,变形成薄片或
丝的金属,仍由金属离子和自由电子组成,它们的相互作 Ag Cu Au Al Zn Fe Pb Hg
图 8.5 几种金属的导电性
用(金属键)使金属薄片和金属丝具有一定的强度。因此,
(蓝色柱体)和导热性(红色柱
金属具有延展性。
体)比较
金属除了共性以外,各种金属还具有各自不同特性和
【资料库】
金属之最
熔点最高的金属
——钨
熔点最低的金属
——汞
图 8.6 金属晶体示意图 图 8.7 金属两端接直流电源后,
硬度最大的金属
电子在金属内定向流动示意图
——铬
密度最大的金属
——锇
密度最小的金属
——锂
人体内最多的金
属元素——钙
地壳中含量最多的
金属元素——铝
人类冶炼最多的金
图 8.8 金属受到外力的作用而变形
属——铁
5
out-8ok Page 5 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC用途。随着科学技术的发展,人们正在利用自然界里各种
金属元素为人类服务。迄今为止人类冶炼最多的金属是铁。
拓展视野
金属和金属氧化物的超导性
1911年荷兰物理学家卡末林·昂内斯(H.Kamerlingh-Onnes 1853—
1926)发现在液氦温度下(4.3K,摄氏温度为-268.85℃),汞的电阻突然
消失。1912年他又发现铅和锡的电阻也在低温下消失,提出了某些金属在很
低温度下有“超导电性”这一新的物理概念。卡末林·昂内斯由于低温物理
学方面的贡献而荣获1913年诺贝尔物理学奖。
1957年巴丁(J.Badeen 1908—1991)、库珀(L.Cooper 1930— )和
施里弗(J.Schrieffer 1931— )三位物理学家提出了以他们姓氏第一个字
母命名的BCS理论,解释了金属的低温超导现象而获1972年诺贝尔物理学
奖。在BCS理论指导下,人们又发现了某些金属的低温超导现象。现在已发
现26种金属在低温时有超导性。
没有电阻的金属有巨大的应用价值,但由于维持低温的液氦耗费很大,
而限制了它的应用。目前仅在一些需强大电流的仪器中应用。
1986年IBM公司在瑞士研究所的研究员贝德诺尔兹(J.Bednorz 1950
..
— )和米勒(K.Muller 1927— )在已经发现金属氧化物在低温时也具有
超导性的基础上,进一步发现Ba-Cu-O体系存在着温度高达35K的超
导体,大幅度提高了超导体的转变温度而获1987年诺贝尔物理学奖。1987
年中国科学院物理研究所的赵忠贤等研究员和美籍华人科学家朱经武分别发
现Y-Ba-Cu-O体系中存在100K和92K的超导体。1993年5月瑞士苏
黎世ETH实验室席林(A.Schilling)制成了Hg-Ba-Ca-Cu-O超导体,
转变温度高达133.8K。
金属和金属氧化物超导现象的发现表明精彩纷呈的金属世界中金属有许
多奇妙的性质。科学家们正在努力研究以发现前所未知的性质为人类服务。
思考与练习
1.金属通直流电后,自由电子能定向移动,金属具有
________性。
2.给金属加热,自由电子能传递热量,金属具有__
______性。
3.金属受到外力的作用,层间彼此滑动,金属具有
________性。
6
out-8ok Page 6 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC常温下,铁跟水不反应。红热的铁能跟水蒸气反应生成
四氧化三铁和氢气。
3Fe+4H O(g) 高 温 Fe O +4H
2 3 4 2
思考与练习
1.上述反应中铁的化合价变化有规律吗?
2.写出铁分别跟盐酸、硫酸铜溶液反应的离子方程式:
____________________。
从上面一些反应中可以看出,铁在化合物中呈+2价或
+3价。Fe2+的溶液呈浅绿色,Fe3+的溶液呈棕黄色。溶液
中的Fe2+容易被溶于溶液中的氧氧化成Fe3+。四氧化三铁
是磁铁矿的主要成分。在四氧化三铁里,存在着铁的两种
不同的价态,其中三分之一是+2价铁,三分之二是+3价
铁。许多磁性材料上都有四氧化三铁薄膜。
拓展视野
透明氧化铁系列颜料
透明氧化铁系列颜料是我国重点开发的新技术产品,目前已有红、黄、
黑、绿、棕五个品种,品质已达到国际一流水平。透明氧化铁属于纳米级材
料,具有高彩度、高着色力和高透明度等良好的性能,经过特殊处理后,有
良好的研磨分散性。
把透明氧化铁加入各种漆料中,可制成透明色漆,再加入少量非浮性的
铝粉浆,则可制成有闪烁感的金属效应漆,该漆与不同颜色的底漆配套,可
作汽车、仪器、仪表、木器等装饰之用。
透明氧化铁颜料无毒、无味,保色性好,具有强烈吸收紫外线等优点,
可作为高档环保型内外墙涂料的着色剂。
铁是人体中一种重要的金属元素。血红蛋白中存在着
+2价铁。没有铁,血红蛋白就不能结合氧分子进行输氧。
当人体患缺铁性贫血症时,服用的补血剂里就含有+2价形
态的铁元素。
8
out-8ok Page 8 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC拓展视野
铁与人体健康
铁是人体必需的微量元素之一,人体内约
铁
铁
含铁4.2~6.1 g,其中有70%存在于血红蛋白和
铁 铁
肌红蛋白, 25%以铁蛋白形式分布在肝、肾、骨 铁
髓中。血红蛋白中的铁是体内氧的输送者。铁在
人体内以二价铁、三价铁形式存在,人体缺铁,
会引起贫血。铁在人体生理活动中起着重要的
作用。
在工农业生产和日常生活中,大部分的金属制品都不 【资料库】
是由纯金属制成的,而是用合金制造的。合金是指两种或
两种以上的金属,或金属与非金属经熔合形成的均匀而具 1998年6月升空的
有金属特性的物质。金属虽具有许多优良品质,但金属材 阿尔法磁谱仪是首台
料中90%以上都是合金。合金常具有纯金属没有的许多优 太空磁谱仪,可在外
层空间寻找反物质、
良品质。生铁和钢(steel)都是铁-碳合金。
暗物质和进行研究宇
宙射线的实验。它的
表8.1 铁合金的成分和性能
主体是在一个圆筒状
合 金 成 分 性 能
的结构中,放置以钕
含碳、硫、磷
生铁 硬、脆 铁硼为材料的磁场强
(2.11%~4.3%)
度很高的永久磁铁,
含碳
普通钢 硬而韧,有弹性
(0.03%~2.11%) 它由磁铁后方的探测
器来记录带不同电荷
锰钢
特 物质在通过磁场后的
种
钨钢 含碳、钨 耐热、熔点高、坚硬 偏转轨迹。
钢
不锈钢 含铬、镍 抗腐蚀性强、坚硬
9
out-8ok Page 9 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC化学史话
不锈钢的发现
你知道吗?光彩夺目的不锈钢竟然是从垃圾堆里发现的。早在第一次世
界大战期间,英国科学家亨利·布里尔受兵工厂的委托,要研制出不易磨损
的金属材料,用于步枪枪膛。布里尔做了大量试验在钢里加入各种元素,制
得的合金钢都不符合要求。他失望地把它们扔进了垃圾堆。但过了一段时期
后,奇迹出现了,垃圾堆里大部分废钢铁都锈蚀了,但有几块钢在闪闪发光。
布里尔取出了钢块进行分析,发现其中含碳0.24%,含铬12.8%。这就是早
期的不锈钢。于是,布里尔办了一个餐具厂,生产不锈钢刀具,一下子轰动
了欧洲。
以后科学家们还发现,如在钢中加
进12%以上的铬(有的含铬17%~19%,
含镍8%~13%)就得到一种抗腐蚀强、
不易被氧化的不锈钢。将不锈钢进行适
当的表面处理,可得到各种彩色不锈钢。
不锈钢已成为合金里的大家族,它的种
类不下数百种。不锈钢的发现似乎偶然,
但却是科学家孜孜不倦研究的必然结果。
图 8.10 不锈钢制品
思考与练习
查阅资料,填写汽车配件的
材料:
汽车配件 金属或合金
电线
汽车外壳
灯箱
排气管
图 8.11 各种特种钢
10
out-8ok Page 10 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC拓展视野
为什么大多数合金比其组成金属的硬度大、熔点低
合金的结构和性质与纯金属不同,在纯金属中,所有原子的大小都是
相同的。而在合金中,加入了较大或较小的原子。这些原子改变了金属中规
则的层状排列,层与层之间的滑动变得困难,所以合金常比组成合金的纯金
属更硬、更坚固。
固体的熔点与原子排列是否整齐
有关。纯金属中,原子大小相同,排
列整齐;而合金中的原子大小不同,
排列没有纯金属那么整齐,原子间作
用力减小。所以,合金的熔点一般比
其组成金属的熔点低。
图 8.12 合金中的原子
[思考与复习8.1]
1.金属单质具有的通性是( )。
(A) 具有金属光泽、导电、导热、有延展性
(B) 硬度大
(C) 熔、沸点较低
(D) 质软
2.生铁的熔点是1 100~1 200℃,纯铁的熔点是( )。
(A) 1 055℃ (B) 1 100℃
(C) 1 200℃ (D) 1 535℃
3.下列化合物中,不是黑色的是( )。
(A) Fe O (B) FeS
2 3
(C) Fe O (D) FeO
3 4
4.下列物质中,属于纯净物的是( )。
(A) 绿矾 (B) 生铁
(C) 钢 (D) 赤铁矿
5.下列各组元素中,熔入普通钢里,成为不锈钢的是( )。
(A) Mg、 Zn (B) Cu、 Sn
(C) Al、 Pb (D) Ni、 Cr
11
out-8ok Page 11 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC6.血红蛋白中含有的金属元素是________,血红蛋白的主要功能是________。
7.录像带中所用的磁铁粉含有Co·Fe O ,其中钴(Co)和铁的化合价可能有+2、+3
3-x 3+x
价。试写出该物质的化学式,并指出铁和钴的化合价。
12
out-8ok Page 12 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC铝和铝合金的崛起
8
.2
(RISING OF ALUMINIUM AND ALUMINIUM ALLOY)
铝和铝合金
铝在地壳中的含量为7.73%,仅次于氧和硅,是地壳里
含量最多的金属元素。在自然界里,铝以化合态存在,它广
泛分布于岩石、泥土和动植物体内,含铝的矿物有长石、云
母、铝土矿、明矾石等。
铝的发现较晚。一般的还原剂如碳、氢气等都难以把
铝从铝的化合物中还原出来,直到1825年丹麦化学家用无
水氯化铝与钾作用,才第一次获得金属铝,当时铝的价格
十分昂贵,被称为“银色的金子”。
19世纪后期发明了电解法生产铝,金属铝的产量迅速
增长,使铝的价格大大降低,金属铝才被广泛应用。
图 8.13 铝的广泛用途
铝是银白色的轻金属,密度 2.7 g/cm3,熔点 660.4℃,
沸点 2 467℃。铝和铝合金具有许多优良的性质,用途广泛。
近几年来铝的世界年产量约为2.5×107 t。
13
out-8ok Page 13 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC【资料库】
20世纪初,德国
冶金学家维尔姆将铜、
查阅资料,填写铝的物理性质及其相关用途:
镁、锰等加到铝中,得
到了强度比铝高得多 物理性质 用途
的合金,并获得了专
利,人们将这种新型
铝合金称为硬铝。
拓展视野
铝 合 金
硬铝具有坚硬、美观、轻巧、耐用、长久不锈的优点,是制造飞机的理
想材料。据统计,一架飞机大约有50万个硬铝做的铆钉。用铝和铝合金材料
制造的飞机元件质量占飞机总质量的70%,宇宙飞船用的金属材料中,铝合
金约占75%。
铝-锂合金具有低密度、高强度的特
点,用其代替常规的铝合金,可使构件质
量减轻10%~20%,强度提高15%~20%,
具有较高的工作温度、较好的高温韧性与
加工性能,价格比先进复合材料便宜得多,
因此是21世纪航空飞行器较理想的结构材
料之一。美国“发现号”航天飞机的外贮
图 8.14 硬铝制成的飞机
箱就是用铝-锂合金制造的。
铝是比较活泼的金属,在化学反应中较容易失去3个电
+13 2 8 3 子变成带3个单位正电荷的阳离子。
图 8.15 铝原子的结构示意图
14
out-8ok Page 14 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC学生实验
铝的一些化学性质
1.取一条铝箔,下端用小孔系住一根火柴,然后用镊
子夹住上端,引燃后,迅速伸入盛有氯气的集气瓶中。
实验现象:__________________
______________。
化学方程式:_________________
______________。
图 8.16 铝在氯气中燃烧
2.用两张圆形滤纸折成漏斗,把5 g氧化铁粉末和2 g
铝粉混合均匀,放在纸漏斗中,在底部剪一个孔,用水润湿
后,放在用硬纸做成的三角漏斗里,把漏斗架在铁圈上,下
面放置一个盛砂的蒸发皿。在纸漏斗中再加入少量氯酸钾,
在混合物中间插上一根镁带,用小木条引火点燃镁带。
实验现象:__________________
_____________。
化学方程式:_________________
_____________。
图 8.17 铝热反应
铝粉和氧化铁的混合物叫做铝热剂。当加热反应时,反
应中会放出大量的热,使混合物达到很高的温度,生成氧
化铝和液态铁,这个反应叫做铝热反应。
某些金属氧化物(如V O 、 Cr O 、 MnO 等)与氧化铁
2 5 2 3 2
相似,能发生铝热反应。工业上利用这些反应来冶炼某些
难熔的金属(如钒、铬、锰等)。
课堂实验
铝的氧化
用砂皮擦去铝条表面的氧化膜*,把铝条插入硝酸汞溶液里。稍后,取出铝
条,用滤纸轻轻地把表面吸干,再把铝条放在干燥的滤纸上。
观察与分析:__________________________。
结论:_____________________________。
* 在空气中,铝的表面会形成一层致密的氧化铝薄膜,铝在冷的浓硝酸和浓硫酸中发生钝化现象。
15
out-8ok Page 15 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC铝跟热水反应生成了氢气和氢氧化铝。
△
2Al+6H O 2Al(OH) +3H ↑
2 3 2
在日常生活中,人们常使用铝制炊具,但铝制品却不
为什么可以用铝锅、 能用来存放酸性和碱性的物质。
铝壶作炊具?
学生实验
铝跟强碱溶液反应
用砂纸擦去铝条表面的物质,将铝条浸入6 mol/L的氢氧化钠溶液中。
观察与分析:_________________________
_________________________。
推理1:反应过程中,生成的Al(OH) 与NaOH_____(填能或不能)反
3
应。
推理2:反应中Al(OH) 起_____(填酸或碱)作用。
3
结论:_____________________________
_______________________。
从铝跟氢氧化钠溶液反应得知,反应中生成的氢氧化
铝能跟氢氧化钠反应,所以氢氧化铝显示弱酸性。
氢氧化铝的弱酸性和弱碱性
【资料库】
氢氧化铝(aluminium hydroxide)是胃舒平的主要成
氢氧化铝在水中存
分,它作为一种弱碱可用于治疗胃酸过多。我们已推理得
在下列电离平衡:
知,氢氧化铝能跟氢氧化钠溶液反应显示弱酸性。下面我
H O+AlO-+H+
2 2 们进一步探究氢氧化铝与酸碱反应的条件和原理。
Al(OH) Al3++
3
3OH-
16
out-8ok Page 16 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC学生实验
氢氧化铝的弱碱性和弱酸性
1.在一支试管里加入1.5 mL 0.5 mol/L的硫酸铝溶液,向硫酸铝溶液
里逐滴加入2 mol/L的氢氧化钠溶液,直至生成大量的白色胶状氢氧化铝沉
淀为止。将沉淀分装在两支试管里,在一支试管里滴加2 mol/L盐酸,在另
一支试管里滴加2 mol/L氢氧化钠溶液。
观察与分析:________________________。
结论:___________________________。
2.氢氧化铝能溶于弱碱吗?
在一支试管里加入1 mL 0.5 mol/L的硫酸铝溶液,向硫酸铝溶液里逐
滴加入过量的2 mol/L的氨水。
观察与分析:________________________。
结论:___________________________。
3.将实验2中得到的悬浊液分别装在两支试管中。
在一支试管中逐滴加入盐酸,再在另一支试管中用玻璃管吹入二氧化碳
气体。
观察与分析:________________________。
结论:___________________________。
氢氧化铝能分别跟强酸和强碱溶液反应,是两性物质。
【资料库】
氧化铝(aluminium oxide)能否溶于强酸和强碱溶液?
氧化铝是白
色难熔的物质,
思考与练习
熔点2 054℃,
写出氢氧化铝、氧化铝分别跟盐酸和氢氧化钠溶液反应 沸点2 980℃。
的化学方程式。
刚玉是较纯
__________________________
的氧化铝。
__________________________
__________________________
__________________________
17
out-8ok Page 17 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC拓展视野
红宝石和蓝宝石
红宝石和蓝宝石是含少量不同氧化物杂质的优质刚玉(属于α型氧化铝
晶体),是制作名贵首饰的材料。红宝石是宝石中的珍品。天然产的透明红
色刚玉,由于含少量氧化铬而显红色。迄今为止,世界上发现最大的天然红
宝石为3 450克拉,产自缅甸,世界著名的巨大星光红宝石重138.7克拉。
蓝宝石因含有少量铁和钛而显蓝色。世界上蓝宝石主要产自澳大利亚和
斯里兰卡,两国约集中了世界蓝宝石资源的80%。其中,澳大利亚就占60%。
世界上最大的蓝宝石重19 kg,产自斯里兰卡。
人造红宝石的研究始于1877年。真正实现人工制造宝石,并能投入规
模化生产,要归功于法国化学家维尔纳叶。1891年维尔纳叶发明火焰熔融
法,1904年正式制造出人造红宝石。该法一直沿用到现代,至今仍是世界上
生产人造宝石的主要方法,人称“维尔纳叶”法。
1960年7月7日,纽约时报报道了美
国科学家梅曼制成了世界上第一台红宝石
激光器的消息。
1961年8月,我国第一台红宝石激光
器由中国科学院长春光学精密机械研究所
研制成功。这表明,当时我国在激光领域
的研究已达到世界先进水平。
图 8.18 红宝石激光器
拓展视野
金 属 钛
钛(titanium)是一种重要的金
属,1791年英国化学家格雷哥尔在钛
铁矿中发现钛的氧化物。1795年德国
科学家克拉普罗特在研究金红石矿石
时,再次发现钛。钛在地壳中的含量
约为0.42%,蕴藏量很丰富,但在自
然界的分布很分散,广泛存在于各种
图 8.19 钛合金制成的人工关节
18
out-8ok Page 18 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC岩石中,特别是砂石和黏土中。石油、煤炭、天然水、动植物、火山灰烬、
海底淤泥,以及陨石中也都含有钛。
钛的外形很像钢铁,但比钢铁坚硬,质量只有同样大小的钢铁的一半。
在常温下,钛可以安然无恙地“躺”在各种强酸、强碱中,就连“王水”也
不能腐蚀它。
钛是银灰色金属,有延展性,熔点1 660℃,沸点3 287℃,密度4.5 g/cm3。
钛的密度比铝稍大,硬度却比铝高2倍。如制成合金,强度可提高2~4倍。
钛是目前金属材料中比强度(物质的强度与密度的比值)最大的金属。钛在
高温、低温条件下都具有良好的性能,在-250~500℃这样宽的温度范围内,
都能保持高强度。正因为钛的本领非凡,所以有着广泛用途。例如,钛合金
可作为导弹、火箭的外壳,宇宙飞船的船舱、骨架及高压容器的结构材料。
用钛合金制造潜水艇,既能抗海水腐蚀,又能抗深层压力。
钛的提炼比较困难。因为钛在高温下可以与氧、碳、氮,以及其他许多
元素化合。目前工业上从矿石中提炼钛是先将钛铁矿或金红石在碳存在下加
热,通入氯气使二氧化钛(TiO )转化为挥发性的四氯化钛(TiCl ),再用熔融状
2 4
态的镁跟气态四氯化钛反应。用这种方法制得的钛疏松多孔,呈海绵状,必
须在真空下或稀有气体中熔化提炼,才能制得较纯净和致密的钛。随着科学
技术的发展,钛的冶炼方法会不断改进,它的产量将迅速增加,必将成为仅
次于铁和铝的金属。
图 8.20 钛用于制造太空船 图 8.21 潜水艇外壳用钛合金
19
out-8ok Page 19 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC[思考与复习8.2]
1.下列方法中,可以制得Al(OH) 的是( )。
3
(A) Al O 与水共热
2 3
(B) 少量氯化铝溶液滴入氢氧化钠溶液中
(C) 少量氢氧化钠溶液滴入氯化铝溶液中
(D) 氨水加入氯化铝溶液中
2.将铝投入下列物质中,有H 产生的是( )。
2
(A) 氢氧化钠溶液 (B) 食盐水
(C) 浓硫酸 (D) 盐酸
3.将少量镁铝合金投入盐酸溶液中,完全溶解后,再加入过量的氢氧化钠溶液,
生成的沉淀是( )。
(A) Mg(OH) (B)Al(OH) 和Mg(OH)
2 3 2
(C) MgO (D) Al O
2 3
4.现代建筑的门框架,常用古铜色的硬铝制造。硬铝含有的元素是( )。
(A) Al、Mg (B) Al、Cu、Mg、Mn、Si
(C) Al、Si (D) Al、Zn
5.铝在人体中积累可使人慢性中毒, 1989年世界卫生组织正式将铝“确定为食品
污染源之一”。铝的下列用途中,曾经不属于食品污染源的是( )。
(A) 明矾和苏打做食品膨化剂 (B) 制电线电缆
(C) 制易拉罐 (D) 制牙膏皮
6.实验室里怎样用Al O 来制取Al(OH) ?写出有关化学方程式。
2 3 3
7.欲测定某铁铝合金的含量,将样品溶于盐酸,然后加入足量的烧碱溶液,待沉
淀全部转化为红褐色时,过滤,将沉淀灼烧,最后得到红褐色粉末。经称量恰好跟原
合金质量相等,则合金中铝的质量分数为__________。
8.在一个空的金属易拉罐内放入少量的某白色晶体,摇动几下后,立即向罐内
注入6 mol/L氢氧化钠溶液10 mL,迅速用胶布严封罐口。过一段时间后,罐壁凹而
瘪;再过一段时间,瘪的罐壁重新鼓起。从实验得知,此易拉罐的金属是
______________________,白色晶体是______________________,罐壁再鼓起的原因
是______________________,化学方程式是______________。
9.把1.71 g硫酸铝配成100 mL溶液,为了抑制水解,在配制过程中加入少量稀
硫酸。若在上述溶液中逐滴加入0.8 mol/L的氢氧化钠溶液,直至过量。试述在滴加氢
氧化钠溶液过程中产生的现象,并说明原因。
20
out-8ok Page 20 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC10.将含有X+、Y2+、Z3+三种金属离子的水溶液进行如下试验:
白色沉淀
足量盐酸
X+、Y2+、Z3+
过滤
Y2+、Z3+
加入氨水
白色沉淀 滤液
通入HS
2
黑色沉淀
据此判断这三种金属离子是( )。
(A) Ag+、Cu2+、Al3+ (B) K+、Cu2+、Fe3+
(C) Ag+、Fe2+、Al3+ (D) Ag+、Ba2+、Fe3+
21
out-8ok Page 21 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC小 结 与 思 考
1.金属及合金。
(1)金属的通性。
金属都具有金属光泽,能导电、能传热,具有良好的延展性。
(2)金属键: 金属晶体是由释放出自由电子的金属离子按一定规律堆积而成的。金属
离子间依靠自由电子产生的强的相互作用就是金属键。
(3)合金。
用两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质。
2.铁。
(1)铁和铁合金的广泛应用。
(2)铁是比较活泼的金属,铁的化合价有+2价、 +3价。铁在一定条件下能分别跟非金
属单质(硫、氯气、氧气等)、水、酸和盐溶液反应。
3.铝。
(1)铝和铝合金的广泛应用。
(2)铝的化学性质。
铝是比较活泼的金属,铝能跟许多非金属、酸及盐溶液起反应。在常温条件下,铝在浓
硝酸、浓硫酸里发生钝化。
铝既能溶于强酸溶液,又能溶于强碱溶液。
铝能跟氧化铁和某些金属氧化物(如V O 、Cr O 等)反应生成氧化铝和液态铁或其他
2 5 2 3
金属单质。
铝粉跟氧化铁等金属氧化物的混合物叫铝热剂。
(3)氧化铝和氢氧化铝。
氧化铝和氢氧化铝都是两性化合物,它们既能跟强酸反应,又能跟强碱溶液反应。
4.金属是热和电的良导体,因为它( )。
(A) 表面富光泽 (B) 由电子组成
(C) 有自由运动的电子 (D) 有可成键的电子
5.下列物质中,不能用金属跟稀硫酸反应来制取的是( )。
(A) Fe(SO ) (B) MgSO
2 4 3 4
(C) Al(SO ) (D) ZnSO
2 4 3 4
6.下列物质中,属于纯净物的是( )。
(A) 生铁 (B) 铝热剂
(C) 漂粉精 (D) 胆矾
7.常温下,将5.6 g铁片投放到下列溶液中,溶液质量变化最小的是( )。
(A) 浓硝酸 (B) 硫酸铜
(C) 盐酸 (D) 硝酸银
22
out-8ok Page 22 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC8.下列反应中,不属于铝热反应的是( )。
(A) 2Al+Fe O 2Fe+Al O
2 3 2 3
(B) 2Al+WO Al O +W
3 2 3
煅烧
(C) 2Al(OH) Al O +3H O
3 2 3 2
(D) 4Al+3MnO 2Al O +3Mn
2 2 3
9.在下列混合溶液中,加入过量的氨水产生沉淀,再加入过量的氢氧化钠溶液,沉淀
消失的是( )。
(A) NaCl和MgCl (B) NaNO 和AgNO
2 3 3
(C) K SO 和Al(SO ) (D) MgCl 和AlCl
2 4 2 4 3 2 3
10.要从含Al3+、Fe3+、Ba2+、Ag+的溶液中分别沉淀出Fe3+、Ba2+、Ag+,加入试剂的
顺序正确的是( )。
(A) HCl、H SO 、NaOH (B) NaOH、HCl、H SO
2 4 2 4
(C) HCl、H SO 、NH·H O (D) HCl、NaOH、H SO
2 4 3 2 2 4
11.将10.2 g的氧化铝溶于一定浓度的500 mL的盐酸溶液中,充分反应后,再逐滴加
入1 mol/L的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液的体积关系
如下图所示,试计算:
沉淀的质量(g)
O 20 氢氧化钠溶液体积(mL)
(1)最大沉淀的质量。
(2)当沉淀从最大值到恰好完全消失时,耗用多少毫升的氢氧化钠溶液?
12.实验室里怎样用废铁屑来制取氧化铁颜料,试设计实验方案,写出所需仪器、药
品、实验步骤及有关反应的化学方程式。
13.阅读下列英文,讨论金属元素和非金属元素的性质差别。
Metals have some or all of the following properties.
① They have a metallic shine or luster.
② With only one exception, they are solids at room temperature.
③ They are malleable and ductile.
④ They conduct heat and electricity.
⑤ They exist as extended arrays of atoms. There are no molecules in a metal.
⑥ They combine with other metals to form alloys, which still behave like metals.
⑦ They combine with nonmetals to form ionic compounds, or salts, which have the properties
of neither metals nor nonmetals.
23
out-8ok Page 23 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC⑧ They form positive ions, such as the Na+, Mg2+, Fe3+ and Cu2+ ions.
Nonmetals have almost exactly the opposite properties.
① They seldom have a metallic luster.
② They are often gases at room temperature.
③ They are neither malleable nor ductile.
④ They are poor conductors of both heat and electricity.
⑤ They often form molecules in their elemental form.
⑥ They combine with other nonmetals to form covalent compounds.
⑦ They combine with metals to form ionic compounds, or salts, which have the properties of
neither metals nor nonmetals.
⑧ They tend to form negative ions, such as the F-, Cl-, O2-, S2-, P3-, SO 2-, PO3-, and NO- ions.
4 4 3
The differences between the chemical and physical properties of metals and nonmetals can be
traced to differences in their electron configurations, radii, ionization energies, and electron
affinities.
24
out-8ok Page 24 2011.4.7, 3:43 AM Adobe PageMaker 6.5C/PPC9
初识元素周期律
PRELIMINARY RECOGNIZE PERIODIC LAW OF ELEMENTS
◆ 元素周期律 ◆ 元素周期表
◆ 同周期元素性质的递变规律 ◆ 同主族元素性质的递变规律
◆ 元素周期表的应用
25宇
宙万物是由元素构成的。各种元素的性
质各异,具有各自不同的用途。它们的
性质究竟是否具有一定的规律是19世
纪科学家们努力探究的重要方面之一。19世纪60年代
俄国化学家门捷列夫在当时还只知道60多种元素的情
况下,把各种元素按它们的性质和相对原子质量排队列
表,构成了世界上第一张元素周期表,指出了元素性质
变化的规律——元素周期律。
在元素周期律的指引下,科学家们不仅找到了地球
上存在的94种元素,而且通过核反应合成出了20余种
新元素。至今已正式命名的元素已有111种。
我们要了解自然,充分合理地利用自然界的物质资
源,就要了解元素的性质及其变化规律。让我们从学习
了解元素周期律开始吧。
269 元素周期律
.1
(PERIODIC LAW OF ELEMENTS)
随着人们对元素性质、原子结构认识的逐步深入,发
现元素的性质和原子的核电荷数是密切相关的。人们按核
电荷数由小到大的顺序给元素编号,这个序号,叫做该元
素的原子序数(atomic number)。原子序数在数值上和这种
元素原子的核电荷数相等。
化学史话
元素周期律的发现
元素周期律从发现到逐步完善曾经历了半个世纪。19世纪,人们已经发
现了几十种元素,这些元素之间有没有内在联系呢?它们的性质变化有什么
规律呢?科学家们期待着解决这些问题。
早在1829年,人们已发现54种元素,德国化学家德贝莱纳把其中15种
元素按3个元素一组,组成5组:
Li Ca P S Cl
Na Sr As Se Br
K Ba Sb Te I
他发现每3种元素的化学性质很相似,称为“三素组”。
1864年,德国化学家迈耶尔,把“三元素”进一步增加到“六元素”。
1865年,英国化学家纽兰兹又把“六元素”扩大成“八元素”一组,称
之为“八音律”。纽兰兹按原子量(相对原子质量)大小将元素排列起来时,发
现第一个元素与第九个元素性质相似。科学家们的探索,步步逼近了科学的
真理,但还没有揭示元素分类的本质。
俄国化学家门捷列夫( 1834—1907)在前人
的基础上,继续探索化学元素之间最根本的规律。门捷列夫把每一种元素的
化学符号,原子量,以及主要性质都写在一张纸牌上,按原子量大小进行有
序排列。1869年门捷列夫写下了一张表格,即《根据元素的原子量及其相似
的化学性质所制定的元素系统表》。门捷列夫发现每隔7种元素,便有一种
27元素在性质上与这种元素十分相似。门捷列夫总结了这一规律,提出“单质
的性质,以及各元素的化合物的形态和性质,与元素的原子量的数值成周期
性的关系”。这便是早期元素周期律的概念。
20世纪以来,人们发现元素的性质和元素原子的核电
荷数是密切相关的。随着元素原子核电荷数的递增,元素
原子的最外层电子排布呈周期性的变化,元素的性质也呈
周期性的变化。
元素性质的周期性变化
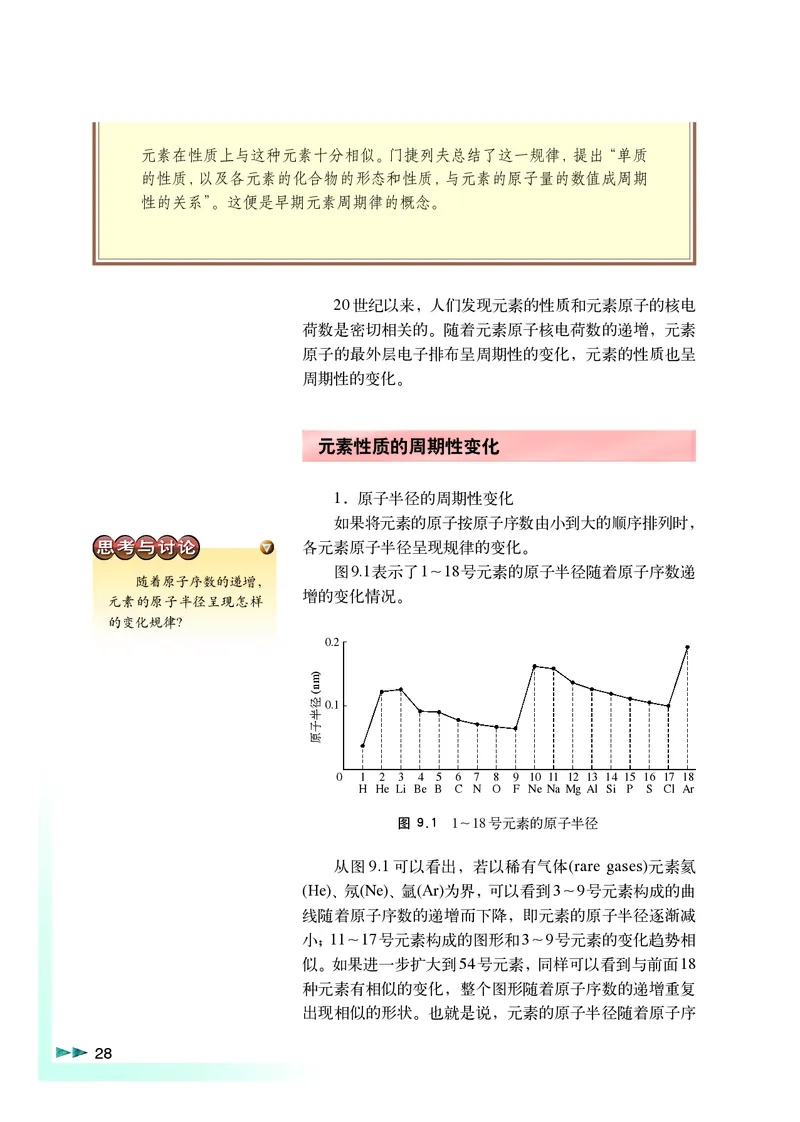
1.原子半径的周期性变化
如果将元素的原子按原子序数由小到大的顺序排列时,
各元素原子半径呈现规律的变化。
图9.1表示了1~18号元素的原子半径随着原子序数递
随着原子序数的递增,
增的变化情况。
元素的原子半径呈现怎样
的变化规律?
0.2
m)
n
径
(
0.1
半
子
原
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar
图 9.1 1~18号元素的原子半径
从图9.1可以看出,若以稀有气体(rare gases)元素氦
(He)、氖(Ne)、氩(Ar)为界,可以看到3~9号元素构成的曲
线随着原子序数的递增而下降,即元素的原子半径逐渐减
小;11~17号元素构成的图形和3~9号元素的变化趋势相
似。如果进一步扩大到54号元素,同样可以看到与前面18
种元素有相似的变化,整个图形随着原子序数的递增重复
出现相似的形状。也就是说,元素的原子半径随着原子序
28数的递增而呈现周期性的变化。
2.元素主要化合价*的周期性变化
*元素的主要化合价是指
随着原子序数的递增,元素的主要化合价又有什么变 元素的最高价和最低价。
化呢?
+7
+6
+5
+4
+3
+2
+1
0
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar
-1 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
-2
-3
-4
图 9.2 1~18号元素的主要化合价
从第11号元素到第17号元素在极大程度上重复着从
第3号元素到第9号元素所表现的化合价的变化,正价从
+1(Na)逐渐递变到+7(Cl),从中间的元素开始有负价,负
价从-4(Si)递变到-1(Cl)。如果研究第18号元素以后的元
素的化合价,同样可以看到和前面18种元素的变化相似。也
就是说元素的化合价随着原子序数的递增也呈现周期性的
变化。
如果按原子序数由小到大的顺序排列,我们可以发现
典型金属元素和典型非金属元素都会周期性地重复出现, 同
样,稀有元素也会周期性地重复出现。
思考与练习
1~20号元素中典型的金属元素有_________
(写名称),典型的非金属元素有_________,稀有
元素有_________。
以上事实可以归纳出这样一条规律;即元素的性质随
着原子序数的递增而呈周期性的变化。这个规律叫做元素
周期律(periodic law of elements)。元素周期律揭示了元素
性质的变化规律。这种变化规律表明,元素之间必定存在
一定的内在联系。
29原子核外电子排布的周期性
思考与练习 为什么元素的性质随着原子序数的递增会呈周期性的
变化呢?
根据原子序数1~18
原子序数从1~2号的元素,即从氢到氦,有一个电子
号元素的原子结构示意
层,电子由1个增到2个,达到稳定结构。原子序数从3~
图,找出最外电子层上电
子个数的变化规律。 10号的元素,即从锂到氖,有两个电子层,最外层电子从
1个递增到8个,达到稳定结构。原子序数从11~18号的元
素,即从钠到氩,有三个电子层,最外层电子也从1个递增
到8个,达到稳定结构。如果我们继续研究18号以后的元
素,同样可以发现,每隔一定数目的元素,会重复出现原子
最外层电子数从1个递增到8个的情况。也就是说,随着原
子序数的递增,元素原子最外层电子排布呈周期性的变化。
正是这种变化引起了元素性质的周期性变化。随着原子序
数递增,最外层电子数周期性地出现1~7个电子。例如,周
期性地出现性质相似的最外层有7个电子的卤族元素。
[思考与复习9.1]
1.表中哪一种元素代表质量数为9的原子的结构?
原子结构
元素
质子 中子 电子
A 4 4 5
B 4 5 4
C 5 4 4
D 5 5 4
2.下列哪种元素可能是金属?
元素 元素的原子序数
A 8
B 10
C 12
D 17
303.X元素的原子序数是9,下列哪一原子序数的元素与X具有相似的化学性质?( )。
(A) 1 (B) 8 (C)17 (D)18
4.下列关于核外电子排布的叙述,正确的是( )。
(A) 最外层为8个电子
(B)M层上的电子一定多于L层上的电子
(C) 第n层上最多可容纳2n2个电子
(D) 稀有气体元素原子最外层电子数是所有元素中最多的
5.某元素的最高正价和最低负价的绝对值相等,原子核内质子数与中子数也相等,气
态氢化物中该元素含量为87.5%,该元素是( )。
(A) C (B)N (C) S (D)Cl
6.下列各原子序数的元素,能够形成AB 型离子化合物的是( )。
2
(A)11与9 (B)12与17 (C)6与16 (D)1与8
7.下列各组微粒半径大小的比较,错误的是( )。
(A)Cl-<Br-<I- (B)Al3+>Mg2+>Na+
(C) Rb>K>Na (D) P>S>O
319 元素周期表
.2
(PERIODIC TABLE OF ELEMENTS)
元素周期表
为了寻找一种简单明了的形式揭示各元素性质的内在
联系,科学家们在元素周期律的基础上创造出多种形式的
元素周期表。
1869年,俄国化学家门捷列夫编制了第一个元素周期
表,以后经过不断的研究和修正,元素周期表才发展为现
在的形式。
元素周期表的结构
把1~20号元素按原子序数递增的顺序从左到右排成
行,并按电子层数递增的顺序由上而下排成列,就可得出
将1~20号元素以一 如下所示的一部分元素周期表。
定的方式排列,寻找元素 按照上述编排原则,把100多种元素中电子层数相同的
间的内在联系。
各种元素,按原子序数递增的顺序从左到右排成行,再把
图 9.3 元素周期表的一部分(1~20号元素)
32不同行中最外电子层的电子数相同的元素按电子层数递增
的顺序由上而下排成列,则可得到最常见的元素周期表(见
附录)。
元素周期表有7个行,每一行的电子层数相同,为一个
周期,周期的序数就是该周期元素原子具有的电子层数。第
一、二、三周期叫短周期,第四、五、六周期叫长周期,第
七周期叫不完全周期。周期表有18个列,第八、九、十列
叫做第Ⅷ族,其余15个列,每个列称为一族。由短周期元
素和长周期元素共同构成的族,叫做主族;副族是完全由 图 9.4 门捷列夫
长周期元素构成的。主族元素的族序数为ⅠA、ⅡA…,副
族元素的族序数为ⅠB、ⅡB…,稀有气体元素为0族。
在已发现的元素中,大约有五分之四是金属元素,它
们都位于元素周期表的左下部。
族 ⅠA 0
周期
1 ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2
3 ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ ⅠB ⅡB
4
5
6
7
图 9.5 金属元素在周期表中的位置 【资料库】
国际纯化学
思考与练习
和应用化学联合会
1.查阅元素周期表,指出下列元素在周期表中的位置。 (IUPAC)在1985年
(1) 钾___________________ 推荐的元素周期表
(2) 钙___________________ 不分主族和副族,
(3) 铝___________________ 把18个列定为1~
(4) 铁___________________ 18族,该元素周期
(5) 氮___________________ 表已逐渐为世界上
(6) 氩___________________ 愈来愈多的国家和
(7) 溴___________________ 地区所采用。
2.查阅元素周期表,指出铊元素的 原子序数,铊元素
原子的相对原子质量及核外电子排布。
33在元素周期表中,同一主族和同一周期的元素性质存
在一定的递变规律。
元素性质的递变规律
1.同一周期中,随着核电荷数的增大,主族元素的原子半径有怎样的变化
规律?
2.同一主族中,随着电子层数逐渐增多,原子半径有怎样的变化规律?
0.152 0.111 0.088 0.077 0.070 0.066 0.064
0.186 0.160 0.143 0.117 0.110 0.104 0.099
0.231 0.197 0.122 0.122 0.121 0.116 0.115
0.244 0.215 0.162 0.14 0.141 0.137 0.133
0.262 0.217 0.171 0.175 0.146 0.14 0.140
*1nm=1×10-9m 图 9.6 元素原子半径的变化示意图(单位:nm*)
结论:(1)__________________________。
(2)__________________________ 。
34在同一周期中,主族元素的原子半径随着原子序数的
递增依次减小。这是因为同一周期中主族元素原子的电子
层数相同,随着原子序数增大,原子的核电荷数增多,原子
核对外层电子的吸引力增大,因而原子半径逐渐减小。
在同一主族中,元素的原子半径大小主要决定于电子
层数,从上到下,原子的电子层数逐渐增多,原子半径逐渐
增大。
元素的金属性表示元素原子失去电子能力的强弱,元
素非金属性表示元素原子获得电子能力的强弱。
原子半径越大,最外层电子数越少,越容易失去电子,
金属性越强。原子半径越小,最外层电子数越多,越容易得
到电子,非金属性越强。
探究与实践
1.同一周期中,随着核电荷数的增大,主族元素的金属性和非金属性
有怎样的递变规律?
2.同一主族中,随着核电荷数的增大,元素的金属性和非金属性有怎
样的递变规律?
结论:____________________________
________________________________。
在同一周期中,各元素的原子核外的电子层虽然相同,
但随着核电荷数的增多,从左到右原子半径逐渐减小,失
电子能力逐渐减弱,得电子能力逐渐增强,所示元素的金
属性逐渐减弱,非金属性逐渐增强。
同一主族的元素,随着核电荷数的递增,从上到下电
子层数增多,原子半径增大,失电子能力逐渐增强,得电
子能力逐渐减弱,所以元素的金属性逐渐增强,非金属性
逐渐减弱。
35根据主族元素性质的递变规律,在周期表中,非金属
元素集中在右上部分,金属元素集中在左下部分,在硼、硅、
砷、碲、砹跟铝、锗、锑、钋之间划一条虚线,这就是金属
元素和非金属元素的分界线。
虚线左面是金属元素,右面是非金属元素。位于分界
线附近的元素,既表现某些金属的性质,又表现某些非金
属的性质。
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
1
2 B F
3 Al Si
思考与练习 4 Ge As
5 Sb Te
1.在元素周期表中,金 6 Cs Po At
属性最强的元素是__,非
图 9.7 金属元素和非金属元素的划分
金属性最强的元素是__。
2.第三周期中,原子半
径最大的金属元素是__,
金属性最强的是___。 在同一周期或同一主族元素中,不仅元素的基本性质
3.第ⅦA中,原子半径 呈现周期性变化,而且它们所形成的单质和化合物的性质
最小的是___。
也具有一定的变化规律。
课堂实验
比较钠、镁、铝金属活泼性
1.取两支试管,加入3 mL水,各滴入2滴酚酞试液,分别加入一小粒
金属钠和少量镁粉,观察现象。将加入镁粉的试管加热至沸腾,观察现象。
实验现象:______________________。
2.取一小片铝和一小块镁带,用砂纸擦去表面的氧化膜,分别投入盛有
2 mL 1 mol/L盐酸的两个试管中,观察现象。
实验现象:______________________。
结论:________________________。
36从实验知道,*钠跟冷水能发生剧烈反应。镁跟冷水不
* 2Na+2H O——→2NaOH+H↑
2 2
易反应,但加热后能发生反应而产生大量的气体。
△
Mg+2H O Mg(OH) +H ↑
2 2 2
镁和铝都能跟盐酸反应,但镁跟盐酸的反应更剧烈些。
Mg+2HCl MgCl +H ↑
2 2
2Al+6HCl 2AlCl +3H ↑
3 2
下表列出第三周期元
在第三周期中,第11、12、13号元素钠、镁、铝的金 素的最高价氧化物对应水
化物的酸、碱性以及气态
属活泼性逐渐减弱,它们的氧化物对应水化物的碱性逐渐
氢化物的热稳定性,试归
减弱,氢氧化钠是强碱,氢氧化镁是中强碱,而氢氧化铝是
纳同一周期中元素的单质
两性氢氧化物。
和化合物性质的递变规律。
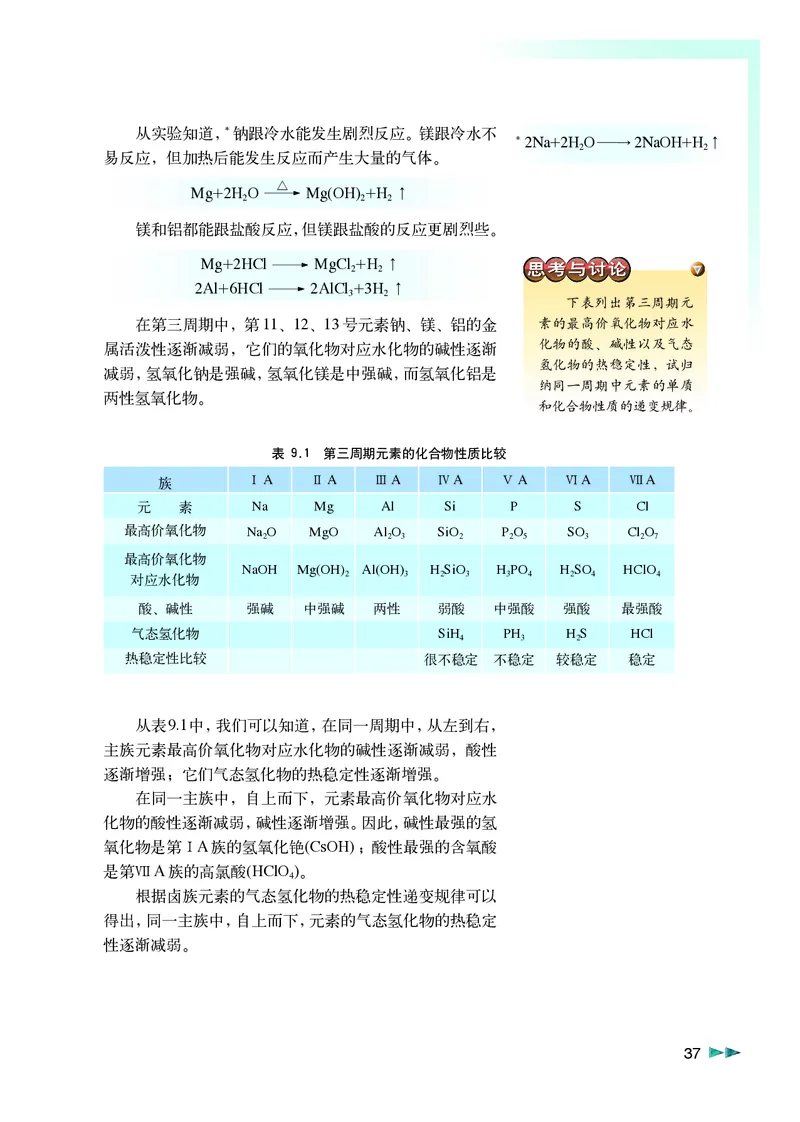
表 9.1 第三周期元素的化合物性质比较
族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
元 素 Na Mg Al Si P S Cl
最高价氧化物 Na O MgO Al O SiO P O SO Cl O
2 2 3 2 2 5 3 2 7
最高价氧化物
NaOH Mg(OH) Al(OH) H SiO H PO H SO HClO
对应水化物 2 3 2 3 3 4 2 4 4
酸、碱性 强碱 中强碱 两性 弱酸 中强酸 强酸 最强酸
气态氢化物 SiH PH H S HCl
4 3 2
热稳定性比较 很不稳定 不稳定 较稳定 稳定
从表9.1中,我们可以知道,在同一周期中,从左到右,
主族元素最高价氧化物对应水化物的碱性逐渐减弱,酸性
逐渐增强;它们气态氢化物的热稳定性逐渐增强。
在同一主族中,自上而下,元素最高价氧化物对应水
化物的酸性逐渐减弱,碱性逐渐增强。因此,碱性最强的氢
氧化物是第ⅠA族的氢氧化铯(CsOH) ;酸性最强的含氧酸
是第ⅦA族的高氯酸(HClO )。
4
根据卤族元素的气态氢化物的热稳定性递变规律可以
得出,同一主族中,自上而下,元素的气态氢化物的热稳定
性逐渐减弱。
37思考与练习
1.元素周期表中最强的含
氧酸是___,最稳定的气态氢
填表:
化物是____。
主 族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
2.比较下列物质酸性或碱
主要化合价
性的强弱(用>或<符号表示)。
气态氢化物
酸性:H SiO ______H PO
2 3 3 4 的通式
碱性:NaOH______LiOH
最高价氧化
3.氢氧化钙溶液和氢氧化
物通式
钡溶液,哪一种碱性强?
最高价氧化
4.比较硒化氢(H 2 Se)和氯化 物对应水化
氢的热稳定性。 物的通式
元素周期表的应用
元素周期表是元素周期律的具体表现形式。
元素周期表是学习和研究化学的重要工具。俄国化学
家门捷列夫曾用它预测未知元素并获得成功。科学家们在
元素周期表的指导下,对元素的性质进行系统的研究,推
动了物质结构理论的发展。人们根据元素性质的周期性变
化,对元素进行分类研究,推测元素及其单质、化合物的性
质。元素周期律的学习对系统研究元素化合物知识具有重
要的实践意义。
元素周期表对工农业生产也具有一定的指导作用。由
于在周期表中位置靠近的元素性质相近。人们在金属和非
金属的分界线附近寻找半导体材料。在B族和Ⅷ族中寻找
催化剂,以及耐高温、耐腐蚀的合金材料。又如,农药中常
含有氯、硫、磷等元素,这些元素都位于周期表的右上角。
通过对这个区域的元素化合物进行研究,有助于找到对人
畜安全的高效农药。
元素性质、原子结构和该元素在周期表中的位置,三
者有着密切的关系。我们可以根据元素在周期表中的位置,
推测它的原子结构和一定的性质,也可以根据元素的原子
结构来推测它在周期表中的位置。周期表将指导我们更好
地学好化学。
38元素周期律还有力地论证了事物变化由量变引起质变
的规律性。
思考与练习
1.已知元素R的原子核外的电子层结构为
(1) 试确定元素R处于周期表中哪一周期,哪一族?
(2) 写出它的最高价氧化物的化学式和该氧化物的对应
水化物的化学式。
(3) 该水化物呈现碱性还是酸性?
(4) 元素R能否形成气态氢化物,能够的话,写出它的
化学式,并跟同一族中你所知道的氢化物的稳定性进行比较。
2.某元素的原子序数为19,试指出它属于哪一周期,
哪一主族,是什么元素?
拓展视野
稀土元素
稀土元素又称稀土金属,是周期表第ⅢB族中钪、钇和镧系17种元素的
总称。除钪、钇外,它们的原子都有6个电子层,其最外电子层上有2个电
子,化学性质十分相似。在自然界里,这17种金属共生在同一矿物中。
稀土元素在地壳中分布比较稀散,它们的氧化物外观酷似泥土,所以叫
做稀土元素。其实稀土元素在地壳中并不稀少,约占地壳总量的0.016%。
我国是世界上稀土元素资源大国,储量占世界的80%。我国在20世纪
60年代就开始研究稀土元素的应用,80年代中期以后取得迅速发展。
钢铁工业是我国使用稀土元素最多的领域,我国已研制出低合金高强度
钢,可以在不增加构件质量的条件下,显著提高其强度,因而已广泛应用于
各种类型的结构件、运输设备和管道上。
近年来,稀土元素材料的应用发展很快。例如,稀土元素在石油化学工
业上用作催化剂;稀土元素永磁材料已成为电子通信的重要材料;稀土元素
贮氢材料用于能源、化工、电子、宇航、军事等方面;稀土元素发光材料和
荧光材料用于彩电显像管、节能灯。
稀土家族在众多新材料中起着十分重要的作用,与现代高科技的发展关
系极为密切。稀土新材料在能源、环境、信息等诸多领域发挥着不可替代的
作用。随着研究与开发的深入,新的稀土元素材料还将不断涌现出来。
39[思考与复习9.2]
1.查阅元素周期表,指出金、银、铜、锌、钛在周期表中的位置。
2.在元素周期表中,在金属元素和非金属元素分界线附近能找到( )。
(A) 制半导体的元素
(B) 制催化剂的元素
(C) 制农药的元素
(D) 制耐高温合金的元素
3.下列说法中,错误的是( )。
(A) 第ⅠA族都是活泼的金属元素
(B) 第ⅡA族元素形成单质,常温下都是固体
(C) 第ⅣA族中有金属元素,也有非金属元素
(D) 第ⅦA族元素形成单质,常温下有气、固、液三种状态
4.已知短周期元素的离子 A2+、B+、C3+、D2-都具有相同的电子层结构,则下列
a b c d
性质比较中正确的是( )。
(A) 原子半径: A>B>D>C
(B) 原子序数: C>A>B>D
(C) 离子半径: C>D>B>A
(D) 单质的还原性: A>B>D>C
5.短周期元素M和N的离子M2+和N3-具有相同的电子层结构,则下列说法正确
的是( )。
(A) M2+的离子半径比N3-小
(B) M的原子序数比N小
(C) M和N原子的电子层数相同
(D) M和N原子最外层电子数相同
6.同周期的X、Y、Z三种元素,已知最高价氧化物的水化物酸性由强到弱顺序是
HXO >H YO >H ZO ,则下列说法正确的是( )。
4 2 4 3 4
(A) 原子半径: X>Y>Z
(B) 非金属性: X>Y>Z
(C) 气态氢化物的热稳定性: ZH >H Y>HX
3 2
(D) 还原性: X2->Y2->Z2-
7.“绿色化学”要求从经济、技术和环保来设计可行的化学反应,生产应尽量减少
对环境的负作用。下列反应符合“绿色化学”的是( )。
△
(A) 制CuSO: Cu+2H SO(浓) CuSO +SO ↑+2H O
4 2 4 4 2 2
40△
(B) 制CuSO: 2Cu+O 2CuO
4 2
CuO+H SO(稀) CuSO +H O
2 4 4 2
△
(C) 制Cu(NO ): 3Cu+8HNO(稀) 3Cu(NO ) +2NO↑+4H O
3 2 3 3 2 2
(D) 制Cu(NO ): Cu+4HNO(浓) Cu(NO ) +2NO↑+2H O
3 2 3 3 2 2
41小 结 与 思 考
1.元素周期律。
元素的性质随着核电荷数(原子序数)的递增,而呈现出周期性变化的规律,称为元素周
期律。
2.元素周期表。
元素周期表以表格的形式体现了元素周期律,它反映了元素性质的变化规律。元素周期
表共包括了7个周期和16个族。
(1)周期。
周期表的每个横行称为一个周期。在元素周期表中,将电子层数相同的元素排列在同一
周期。
(2)族。
周期表的每个纵列称为一族(Ⅷ族除外,为三个纵列)。由短周期元素和长周期元素共
同构成的族称为主族,仅由长周期元素构成的族称为副族。
3.元素在元素周期表中的位置与其原子结构的关系。
周期表的位置(周期、族)
周期序数=电子层数
主族序数=最外层电子数 性质的递变规律
原子序数=质子数
元素的性质
原子半径
原子结构 主要化合价
金属性和非金属性
4.同周期主族元素性质的递变规律。
相同周期元素的原子具有相同的电子层数,随着核电荷数的递增,元素性质有以下递变
规律:
(1)原子半径逐渐减小。
(2)元素金属性逐渐减弱,非金属性逐渐增强。
(3)元素最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强。
(4)元素气态氢化物的热稳定性逐渐增强。
425.同主族元素性质的递变规律。
同主族元素的原子具有相同的最外层电子数,随着核电荷数的递增,元素性质有以下递
变规律:
(1)原子半径逐渐增大。
(2)元素金属性逐渐增强,非金属性逐渐减弱。
(3)元素最高价氧化物的水化物碱性逐渐增强,酸性逐渐减弱。
(4)元素气态氢化物的热稳定性逐渐减弱。
6.元素性质呈现周期性变化的根本原因是( )。
(A)元素原子电子层数增大
(B)元素的化合价呈现周期性变化
(C)元素原子最外层电子数呈现周期性变化
(D)核电荷数依次增大
7.下列各组元素中,元素的非金属性随着原子序数递增而增强的是( )。
(A)Na、K、Rb (B) N、P、As
(C) O、S、Se (D)P、S、Cl
8.下列气态氢化物中,最不稳定的是( )。
(A)NH (B)H S (C)PH (D)H O
3 2 3 2
9.Xm+与 Yn-具有相同的电子层结构,则b与m、n、a的关系是( )。
a b
(A)b=a-m+n (B)b=a-m-n
(C)b=a+m+n (D)b=m-n+a
10.同周期的三种非金属元素X、Y、Z,它们的原子半径由小到大的顺序是X<Y<
Z,则下列判断中正确的是( )。
(A)非金属性:X<Y<Z
(B)气态氢化物的热稳定性按X、Y、Z顺序增强
(C)X、Y、Z的最高价氧化物的水化物酸性由强到弱
(D) X、Y、Z的最外层电子数依次增多
11.镭元素在周期表处于第七周期ⅡA族,下列关于镭的性质描述不正确的是( )。
(A) 在化合物中呈+2价 (B) 氢氧化物具有两性
(C) 单质能跟水反应放出氢气 (D) 镭比钙的金属性强
12.主族元素A、B、C、D、E、F核电荷数依次增大。已知A、C、F三原子的核外最
外层共有10个电子,且这三种元素的最高价氧化物的水化物之间两两均能反应,生成盐和
水,E元素的原子最外层比次外层少3个电子。试回答:
(1)写出A、C、F三种元素的符号:
A__,C__,F__。
43(2)E元素在周期表中的位置是第__周期,第__族。
(3)原子半径比较:
r(C)__r(D)__r(E)__r(F)。(填>或<)
(4)A、C两元素的最高价氧化物的水化物反应的化学方程式:
13.下列各种事实跟原子结构的哪一部分有关?
(1)元素在周期表中的排列顺序
(2)相对原子质量的大小
(3)元素具有同位素
(4)主族元素的化学性质
(5)元素在周期表里处于哪个周期
(6)主族元素在周期表里处于哪个族
(7)主族元素的化合价
4410
学习几种定量测定方法
STUDY SOME METHODS OF QUANTITATIVE ESTIMATION
◆ 测定1 mol气体的体积 ◆ 酸碱滴定
◆ 结晶水合物中结晶水含量的测定
45
out-10ok Page 45 2011.4.9, 10:37 PM Adobe PageMaker 6.5C/PPC化
学实验是人们探究物质组成、性质及变化的重要实
践活动。化学实验有定性的,也有定量的。从电解
水得到氢气和氧气的实验,可以知道水是由氢氧两
种元素组成的。但要确定水的分子式H O,还必须测定电解水所得
2
到的氢气和氧气的体积。前者是定性实验,后者就是定量实验,显
然定量实验要求更高。在现代化工生产中,定量测定是控制生产的
必要条件。现代化学的发展在很大程度上是与定量测定技术的进步
密切相关的。
定量实验要使用许多定量仪器,如电子天平、量筒、滴定管、
温度计、秒表等。定量实验要做到准确,不仅要测定原理科学,方
法合理,还要正确使用定量仪器,准确地读出数值。
让我们通过本章的三个实验,了解测定原理,学会测定方法,
体验定量实验在化学中的重要性。
46
out-10ok Page 46 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC10 测定 1 mol 气体的体积
.1
(DETERMINE THE VOLUME OF 1 MOLE OF A GAS)
我们知道, 1 mol任何气体的体积在同温、同压下是相
同的,在0℃、101 kPa时约为22.4 L;而1 mol气体的质
测定气体的体积,为
量各不相同。要测定1 mol气体的体积,如取氢气作试样,
什么要标明温度和压强?
则要测定2.016 g氢气(氢的摩尔质量为1.008 g/mol)所
常温、常压(假设为
占的体积;如取二氧化碳作试样,则是测定44.009 g二氧 101 kPa)时, 1 mol气体的
化碳所占的体积。 体积比标准状况下的22.4 L
大还是小?原因是什么?
测定1 mol气体体积的方法
化学实验室中,可以在一定温度下直接取一定体积(V)
的某种气体,称出它的质量(m),或称取一定质量(m)的某种
气体,量出它的体积(V),再根据这种气体的摩尔质量,计
算出该温度下1 mol气体的体积:
用镁跟足量的稀硫酸
V(L)
1 mol气体的体积= - - - - - ×M(g/mol) 反应制取氢气,并测定
m(g)
1 mol氢气的体积。
然而,直接测定气体的体积和质量,操作上比较繁复, 1.称量什么物质,通
我们可以设想用其他方法来测定。例如,镁跟稀硫酸反应 过换算可以得到氢气的质
量或物质的量?
来产生氢气。称取一定质量的镁[m(Mg)]跟酸完全反应,那
2.怎样收集氢气并测
末,一定质量的镁通过换算可以得到氢气的质量(或物质
量它的体积?
的量)。
氢气的体积[V(H )]可用排水法收集在一个有刻度的容
2
器中来测量出氢气的体积。
V(H ) V(H )
2 2
1 mol氢气的体积=———×M(H )=———×M(Mg)
m(H ) 2 m(Mg)
2
47
out-10ok Page 47 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC化学反应气体体积测定装置
化学反应中产生的气体体积,可用化学反应气体体
积测定仪来测定(如图10.1所示)。该测定仪由三部分组
127 mL
成,左边是气体发生器(A瓶),中间是储液瓶(B瓶),右
边是液体量瓶(C瓶)。A瓶下部侧面有加料口;B瓶上部
储液瓶
数字式温度计的探头,用于测定气体的温度。C瓶的瓶
颈上有110~130 mL刻度线,可准确读出进入量瓶的液
气体 体的体积。全部装置固定在专用底座上。气体发生器、
液体量瓶
发生器
液体量瓶的位置下有螺旋,能作高低的微调。
如要测定1 mol氢气的体积,则取一定质量的镁带
跟稀硫酸在A瓶中完全反应,产生的氢气把B瓶中液
加料口
体(品红溶液)通过导管压入C瓶,读出液体数据转换成
底座
A B C 氢气的体积,进行计算来推算出该温度时1 mol氢气
图 10.1 化学反应气体体积测定仪 的体积。
课堂实验
化学反应气体体积测定仪的装配
1.如图10.1所示,向B瓶内加入品红溶液至刻度线,盖上瓶塞。
2.把A瓶固定在底座左边位置上,把C瓶即液体量瓶固定在底座右边位置
上,用螺旋调节高低,用胶管把A瓶、B瓶和C瓶紧密连接。
3.用橡皮塞塞紧A瓶加料口,进行气密性检查。当橡皮塞塞紧时,B瓶内
导管中的液面会上升,上升液柱在1 min内不下降,确认装置气密性良好。
怎样检查装置的气密性? 下一页的课题能达到哪些实验目的?
完成这一课题需要哪些实验用品?
将讨论的结论填入有关实验报告中。
48
out-10ok Page 48 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC学生实验
测定某温度下1 mol氢气的体积
课题要求:应用化学反应气体体积测定仪来测定某温度下1 mol氢气的体积。
实验步骤:
B
1.装配好化学反应气体体积测定仪,作气密性检查。
A
2.用砂皮擦去镁带表面的氧化物,称取0.100~0.110 g镁
C
带(精确至0.001 g),把数值记录于表格。
3.在A瓶出气口处拆下胶管,使A瓶倾斜,取下A瓶
加料口橡皮塞,用小烧杯加入约20 mL水于A瓶中(目的
是降低反应时硫酸的浓度),再把已称量的镁带加到A瓶底
部,用橡皮塞塞紧加料口。
4.用注射器在A瓶加料口抽气,使B瓶导管内液面和导
管外液面持平(图10.2所示状况)。注射器拔出时要注意捏住针
头拔出。
图 10.2
5.用注射器吸取10 mL 3 mol/L硫酸,用针头扎进A
瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头。
观察现象,记录气体温度(用于计算测定理论值)。
6.当镁带完全反应后,读出C瓶中液体的体积,读数估计至0.1 mL,记录于
表格。
7.用注射器在A瓶加料口抽气,使B瓶中导管内外液面持平。记录抽出气体
的体积,把数据记录于表格。
思考:液体量瓶的读数是否就是氢气的体积?
将计算后的氢气体积填入表格。
重复上述操作进行第二次实验(将C瓶中品红溶液倒回B瓶;倒去A瓶内反应
液,洗净后使用)。
实验记录:温度_______。
实验 镁带质量 硫酸体积 液体量瓶中 抽出气体的 氢气体积* 计算1mol氢气
次数 (g) (mL) 液体体积(mL) 体积(mL) (mL) 体积(mL)
1
2
*氢气体积=液体量瓶中液体体积-硫酸体积+抽出气体体积
两次实验平均值:_________________。
实验温度下,1 mol氢气体积的理论值(由教师提供):_________________。
实验值-理论值
实验误差:------------- ×100% =_________。
理论值
49
out-10ok Page 49 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC拓展视野
常温下1 mol气体体积的理论值的确定方法
先从有关手册上查出某气体在标准状况下的密度(如表10.1所示),并
计算出标准状况下1 mol该气体的体积,然后根据以下公式,换算成某温度、
某压强下的体积(即理论值)。
p V p V
0 0 1 1
——=——
T T
0 1
例如,氢气在标准状况下密度为0.089 9 g/L。
2.016
标准状况下, 1 mol氢气的体积=———=22.42(L)。
0.089 9
273+25
25℃、 101 kPa时, 1 mol氢气的体积=22.42×————=24.5(L)。
273
【资料库】
实验误差的原因分析
表 10.1 标准状况下
气体的密度(g/L)
任何定量测定的方法,得到的数据都有一定的精确范
H O CO Cl
2 2 2 2
围,或者说存在一定的误差。
0.089 9 1.43 1.96 3.17
我们的测定结果如果与理论值偏差很大,那就应在实
验装置、所用试剂的纯度以及操作上寻找原因。例如,装置
漏气会造成氢气体积减少,使测定结果偏小(误差为负值),
又如反应放热,氢气的温度高于室温,而体积增大,使结果
偏大(误差为正值)。
以下几种情况会产生 通过分析可以知道,实验误差有的来自于仪器装置自
怎样的误差?使实验结果 身或试剂的品质,有的来自于操作的失误。定量测定的误
偏大还是偏小? 差允许在一个范围内。
1.分析气体摩尔体积 你的实验结果如何,是否在允许的误差范围内?回忆
测定装置本身,是否存在 自己的实验过程,分析产生误差的各种原因,写入实验报
产生误差的因素? 告中。
2.镁带含有跟硫酸不
反应的杂质。
3.没有擦去镁带表面
的氧化镁。
50
out-10ok Page 50 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC拓展视野
系统误差、偶然误差和过失误差
误差分为多种。一种是来源于仪器装置和药品自身的误差,仪器的精密
度高、试剂品质好,误差就小;反之,误差就大。这一种误差叫系统误差
(systematic error)。另一种是来源于测定时的某些偶然因素,如测定时,环境
温度的变化,这种误差叫偶然误差(accidental error)。操作失误所引起的误差
叫过失误差,或叫测量错误,如液体的读数偏差、装置漏气等。
定量测定实验时,当原理、装置和试剂确定后,系统误差有专门的方法
来处理。偶然误差可用多次平行实验求平均值来减小。而过失误差应由测定
人的正确操作来消除。
[思考与复习10.1]
1.对定量测定实验,有学生认为:我们主要是学习实验方法,结果不重要,定量读
数不必太认真。
你是否同意这种说法,谈谈你的看法。
2.某温度下,测得150.25 mL氢气的质量为0.013 3 g,则该温度时,1 mol氢气的体
积为多少升?
3.取500 mL(已折算为标准状况)某种气体称得质量为0.982 g。试应用标准状况
的气体摩尔体积(22.4 L/moL)来计算这种气体的摩尔质量。
4.用化学反应气体体积测定仪测定某温度下1 mol H 的体积。如有下述情况,试分
2
析其测定结果偏大,还是偏小?同时说明原因。
(1)装置漏气。
(2)反应完成后未对储液瓶(B瓶)作抽气操作。
(3)使用的镁带不纯。 (提示:杂质成分不同,影响不同)
5.实验设计:测定常温下1 mol二氧化碳的体积。
设计要点:
(1)制取气体:选用什么试剂和怎样的实验装置来制取?
(2)测定体积:用什么方法和装置来测定二氧化碳的体积?
(3)如选用化学反应体积测定仪,根据二氧化碳和氢气性质上的差异,那么测定方法
要作哪些改变?
51
out-10ok Page 51 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC结晶水合物中结晶水含量的测定
10
(DETERMINATION OF CRYSTAL WATER IN
.2
CRYSTAL HYDRATES)
测定物质的组成,确定其化学式是定量实验的重要
内容之一。
硫酸铜的化学式是CuSO ,硫酸铜晶体中带有结晶水,
4
本节将通过实验确定其化学式为CuSO ·5H O,体验化学
4 2
是怎样探求物质组成的奥秘的。
结晶水含量测定的原理
我们知道,结晶水合物受热能够失去结晶水,硫酸铜
晶体(因结晶水含量待测定,设化学式为CuSO·xH O)失
4 2
水的化学方程式:
△
CuSO ·xH O CuSO +xH O
4 2 4 2
1 mol x mol
那么,称取一定质量的硫酸铜晶体,将其加热失去全
部结晶水后再进行称量,就可以知道硫酸铜晶体中硫酸铜
的质量和结晶水的质量,然后根据硫酸铜和水的摩尔质量,
计算出1 mol硫酸铜晶体中含多少摩结晶水:
m (CuSO ) m (H O)
4 2
∶ =1∶x
M (CuSO ) M (H O)
4 2
依据以上原理,如何设计实验方案以确定硫酸铜晶体化
学式(CuSO·5H O)?
4 2
实验方案如果仅设计为:(1)称量(硫酸铜晶体) (2)
加热(失去其结晶水) ( 3)冷却 ( 4)再称量(无水硫酸铜),
还不符合定量测定的要求。原因是缺少“恒重操作”。什么
是恒重操作呢?
52
out-10ok Page 52 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC【资料库】
恒重操作
硫 酸 铜 晶 体
为确保实验的准确性,操作上除了要求称量准确、加 (蓝色)在110℃开
热时晶体不能飞溅损失等,关键是判断硫酸铜晶体加热时 始失去部分结晶水,
150℃时失去全部结
是否完全变成了无水硫酸铜。
晶水,生成白色的
如果用肉眼来观察,以蓝色的晶体全部变成白色作判
无水硫酸铜。650℃
断,误差太大。化学实验中,便设计了一种叫恒重(constant
时硫酸铜分解成黑
weight)的操作(如图10.3所示),来确保硫酸铜晶体中结
色的氧化铜。硫酸
晶水全部失去。即我们在完成第一次加热、冷却、称量后, 铜晶体受热时,结
再进行第二次加热、冷却、称量;如果第二次的质量在减 晶水逸出,使有规
则外形的晶体爆裂,
小,还要作第三次加热、冷却、称量,直到连续两次称量的
有飞溅现象。
结果相差不超过0.001 g为止。
第一次加热后
冷却后第一次
冷却
称量
第二次称量
再一次冷却
如恒重则结束
作第二次加热
图 10.3 恒重操作
课堂实验
恒重操作
1.在瓷坩埚中加入约2 g硫酸铜晶体,放在泥三角上用酒精灯慢慢加
热,直到硫酸铜晶体完全变白,然后,把瓷坩埚放在干燥器中冷却至室温(在
空气中冷却会吸收空气中的水蒸气),作第一次称量。记录数据。
2.将盛有无水硫酸铜的瓷坩埚再一次加热2 min,放在干燥器中冷却
后,再次进行称量,直到两次称量的结果相差不超过0.001 g。
53
out-10ok Page 53 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC学生实验
硫酸铜晶体中结晶水含量的测定
实验步骤:
1.准确称量瓷坩埚的质量(m g),精确至
0
0.001 g (下同)。 这一课题能达到哪些
实验目的?完成这一课题
2.在瓷坩埚中加入约2 g硫酸铜晶体,
需要哪些实验用品?
并称量(m g)。
1 将讨论的结论填入有
3.把盛有硫酸铜晶体的瓷坩埚用坩埚钳
关实验报告中。
放在泥三角上慢慢加热,直到蓝色完全变
白,然后把瓷坩埚移至干燥器中冷却到室
温,并称量。
4.进行恒重操作,直至两次称量结果相差不超过0.001 g为止,记录
质量(m g)。
2
另取硫酸铜晶体,再作一次测定。
表 10.2 实验记录
质量(g)
名 称
第一次 第二次
瓷坩埚质量(m )
0
瓷坩埚和硫酸铜晶体质量(m )
1
瓷坩埚和无水硫酸铜晶体质量(m )
2
硫酸铜晶体质量(m -m )
1 0
无水硫酸铜质量(m -m )
2 0
结晶水质量(m -m )
1 2
数据处理和结论:
设1 mol硫酸铜晶体中有x mol结晶水。
用表格数据计算x值:第一次___,第二次___。
1 mol硫酸铜晶体中含有___mol水(平均值,精确至小数点后2位)。
计算实验误差,并作误差分析。
54
out-10ok Page 54 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC测定值与理论值有偏差的原因
1 mol硫酸铜晶体中结晶水含量是5 mol,这是一个理
论值。实验使用的电子天平读数可精确到0.001 g,考虑到
以下几种情况会产生
硫酸铜和水的摩尔质量的精确度(严格地说,铜和氢的摩
怎样的误差?使实验结果
尔质量应使用63.5 g/mol和1.008 g/mol),假如实验结果
偏大,还是偏小?
测得1 mol硫酸铜晶体的结晶水含量在4.90~5.10 mol范围 (1)加热硫酸铜晶体
内,仍可认为是合理的结果。 时,结晶水没有完全逸出。
如果测定结果与理论值偏差很大,那就应寻找原因。
(2)在冷却过程中,无
水硫酸铜又吸收了空气中
你的实验结果偏大,还是偏小?反思自己的实验过程,
的水蒸气。
找到造成误差的具体原因,填入实验报告中。
(3)加热硫酸铜晶体
时,晶体爆溅。
[思考与复习10.2]
1.某学生因实验误差太大,实验报告中抄了邻座同学的数据。他认为:我已经知道
了自己失误在哪里,也看了邻座同学的全部实验过程,他的结果也可作为我的结果。
你是否同意这种说法,谈谈你的看法。
2.某学生测定出硫酸铜晶体中结晶水含量有6.10 mol,试分析造成偏大的可能原因。
3.一位学生的测定结果为1 mol硫酸铜晶体中含5.00 mol结晶水,能否说明这位学
生的误差为0?操作上完全正确?
4.某碳氢化合物(CH),取一定量完全燃烧后,使其燃烧产物依次通过浓硫酸和石灰
x y
水,测得浓硫酸质量增加0.720 g,石灰水中沉淀的质量为4.00 g。试计算该化合物中碳、
氢元素的物质的量之比。若再测出该碳氢化合物的式量为56,写出它的分子式。
55
out-10ok Page 55 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC10 酸碱滴定
.3
(ACID-BASE TITRATION)
酸碱滴定又称中和(neutralization)滴定。中和滴定在
科学研究、医疗卫生、工农业生产上有广泛的应用。这是一
种用已知浓度的酸(或碱)溶液来测定未知浓度碱(或酸)
溶液的一种方法。
酸碱溶液浓度的测定
在20.00 mL氢氧化钠溶液中逐滴加入0.121 8 mol/L
盐酸溶液,当滴至18.60 mL时,恰好完全反应。试计算氢
氧化钠溶液的浓度。
解: NaOH+HCl NaCl+H O
2
1 mol 1 mol
完全反应时, n (HCl)=n (NaOH)
c (HCl)·V (HCl)=c (NaOH)·V (NaOH)
18.60×0.121 8=c (NaOH)×20.00
c (NaOH)=0.113 3 (mol/L)
如果把上述问题转化为一个实验操作,就是用已知浓
度的盐酸溶液去测定未知的氢氧化钠溶液的浓度,这就是
中和滴定。
在中和滴定的操作中,已知准确浓度的盐酸或氢氧化
钠溶液叫做标准酸液(standardized acid solution)或标准碱
液(standardized basic solution),未知浓度的氢氧化钠溶液
或盐酸溶液叫待测碱液或待测酸液,待测液的体积预先准
确量取,而标准液的体积则要通过实验测定。
56
out-10ok Page 56 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC探究与实践
判断滴定终点的方法
在用已知浓度盐酸滴定氢氧化钠溶液时,读出消耗标准酸液的体积之
前,必须先要知道滴入的盐酸何时恰好跟氢氧化钠完全反应,即滴定终点
(endpoint of titration)。试设计一个方法,判断滴定终点。
设计提示:
(1)酸碱指示剂在酸、碱性溶液中呈现不同的颜色。
(2)逐滴加入盐酸时,溶液的pH变化。
显然,中和滴定的关键,一是正确判断滴定的终点,二是准确测定液体的
体积。
中和滴定基本操作
1.滴定管的使用。
滴定管(burette)是测量放出液体体积的定量仪器,规
格为25 mL(或50 mL等),最小刻度为0.1 mL,读数可
估计到0.01 mL。
操作练习:
在清洗干净的滴定管(管壁不挂水珠)中注入少量蒸
馏水,检查活塞是否漏水,旋转是否灵活自如。然后注入
蒸馏水至刻度“0”或“0”以下位置。
滴定管上标有棕色刻度线,观察背景是白底蓝线,由
于光在空气、水中折射率不同,蓝线在液面下变粗,观察
蓝线的粗
时旋转滴定管使蓝线处于一直线,蓝线的粗细交界点所对
细交界点
应的刻度即是准确读数(如图10.4所示)。
3.50 mL
从滴定管中准确放出10.00 mL蒸馏水。
2.滴定终点的判断。
操作练习:
取一支干燥的滴定管准确量取20.00 mL盐酸溶液,慢
慢放入锥形瓶中,加入2滴酚酞试液。
另取一支滴定管,注入氢氧化钠溶液至刻度“0”或“0”
以下位置,进行中和滴定。
图 10.4 滴定管
滴定时,一手控制活塞,一手握住锥形瓶瓶颈轻轻摇
57
out-10ok Page 57 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC【资料库】 动(如图10.5所示)。开始滴定时,溶液滴出的速度可以稍
快些,随着滴定的进行,滴定的速度要减慢,最后要一滴一
指示剂的变 滴加入,当最后一滴使溶液由无色变成粉红色,充分摇动
色范围 后红色在半分钟内不褪时,即为滴定终点。
pH 酚酞甲基橙 石蕊
0 【资料库】
红
2 无 滴定管活塞手柄有
色 红
3.1 红色、蓝色两种,一般
橙 红色的用于盛放酸液,
4
4.4 蓝色的用于盛放碱液,
5
使用方法完全相同。
6
紫
8 8 8
粉
红 黄
10 10 图 10.5 滴定操作
蓝
重复操作一次。
红
12
用盐酸溶液滴定氢氧化钠溶液时,一般用甲基橙作指
示剂,当加入最后1滴盐酸溶液后,黄色变为橙色(0.5 min)
14
不立即变回黄色时,此时为滴定终点。
化学史话
滴定法的改进
1729年,法国人日夫鲁瓦为测定醋酸的浓度,用碳酸钾为标准物,将待
测醋酸滴入碳酸钾溶液,以气泡停止产生作为滴定终点,这是第一次将滴定
法用于化学分析。
此后,滴定法迅速获得改进。1750年,法国人弗浪索用标准硫酸滴定某
矿泉水中的含碱量时,首次使用指示剂(紫罗兰浸出液)来判断滴定终点。
1786年法国人德克劳西设计了滴定管。这些都大大提高了中和滴定的准确性
和应用价值。
过去使用的滴定管分两种,一种是酸式滴定管,一种是碱式滴定管,如图
10.6所示。
酸式滴定管下端有玻璃活塞,它不能盛放碱性溶液,因为碱性溶液会腐
蚀玻璃,使活塞难以转动。碱式滴定管下端由橡皮管连接一尖端玻璃管,橡
皮管内有玻璃珠,用来控制溶液的流出。碱式滴定管的玻璃珠以下的部分容
易产生气泡,排除气泡的方法如图10.7所示。使用时,用手控住玻璃珠,向
58
out-10ok Page 58 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC一边挤压,使液体流出,防止产生气泡。
这类滴定管没有蓝底白线的观察背景,读数时应观
碱 酸
式 式 察溶液凹液面下缘最低处的刻度数值,如图10.8所示。
滴 滴
定 定 目前,酸碱滴定已发展为氧化还原滴定、络合滴定
管 管
等种类繁多的容量分析体系,成为化学分析的重要方
法。自动滴定仪中pH计、pH传感器的出现,使滴定更
快捷、准确。
图 10.6 酸式滴定管和 图 10.7 碱式滴定管的 图 10.8 酸式滴定管和
碱式滴定管 排除气泡 碱式滴定管的读数
这一课题能达到哪些实验目的?完成这一课题需要哪些
实验用品?
将讨论的结论填入有关实验报告中。
59
out-10ok Page 59 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC学生实验
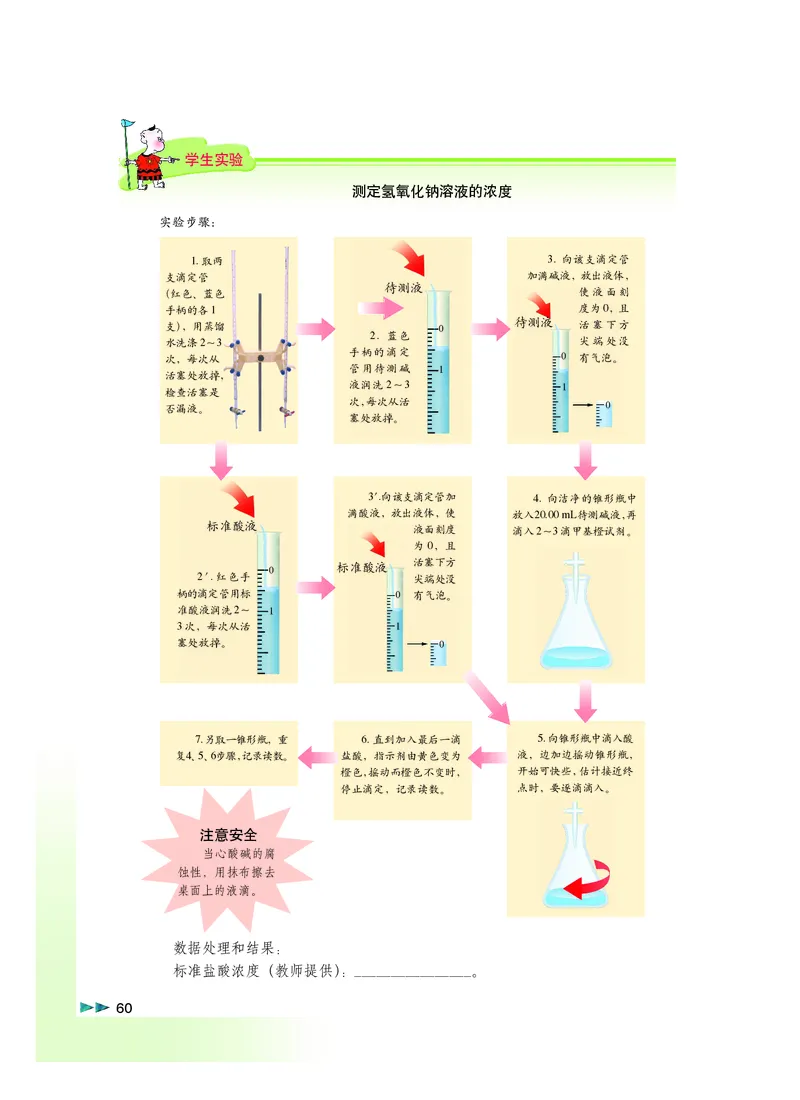
测定氢氧化钠溶液的浓度
实验步骤:
1. 取两 3. 向该支滴定管
支滴定管 加满碱液,放出液体,
待测液
(红色、蓝色 使液面刻
手柄的各1 度为0,且
支),用蒸馏 0 待测液 活塞下方
2. 蓝色
水洗涤2~3 尖端处没
手柄的滴定
次,每次从 0 有气泡。
管用待测碱 1
活塞处放掉,
液润洗2~3 1
检查活塞是
次,每次从活
否漏液。 0
塞处放掉。
3′.向该支滴定管加 4. 向洁净的锥形瓶中
满酸液,放出液体,使 放入20.00 mL待测碱液,再
标准酸液
液面刻度 滴入2~3滴甲基橙试剂。
为0,且
活塞下方
标准酸液
0
2′.红色手 尖端处没
柄的滴定管用标 0 有气泡。
准酸液润洗2~ 1
3次,每次从活 1
塞处放掉。 0
7. 另取一锥形瓶,重 6. 直到加入最后一滴 5. 向锥形瓶中滴入酸
复4、 5、 6步骤,记录读数。 盐酸,指示剂由黄色变为 液,边加边摇动锥形瓶,
橙色,摇动而橙色不变时, 开始可快些,估计接近终
停止滴定,记录读数。 点时,要逐滴滴入。
注意安全
当心酸碱的腐
蚀性,用抹布擦去
桌面上的液滴。
数据处理和结果:
标准盐酸浓度(教师提供):________________。
60
out-10ok Page 60 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC待测氢氧化钠溶 标准盐酸体积(mL) 氢氧化钠溶液
实验次数
液体积(mL) 初读数 末读数 体 积 浓度(mol/L)
1
2
氢氧化钠溶液浓度平均值:______________。
氢氧化钠溶液浓度准确值(教师提供):______________。
(实验值-理论值)
实验误差:————————×100% =______________。
理论值
影响中和滴定准确性的因素分析
测定氢氧化钠溶液浓
度的滴定中,下列操作对实
验结果有没有影响?若有影
中和滴定是一种有一定精确程度的定量实验。超过了
响,则使测定结果偏大,还
范围的实验误差主要由于操作失误而产生。
是偏小?
反思自己的实验过程,对自己测定结果进行误差分析。
1.滴定管用蒸馏水润洗
后,直接注入标准盐酸溶液。
2.最后滴入数滴成串
盐酸时,发现锥形瓶中颜色
由黄变橙,作为滴定终点。
[思考与复习10.3]
1.有学生在实验前完成了实验报告,且做得十分清晰。他认为:这是“打有准备之仗”,
我的实验也会是这个结果,先做好有何不可?
你是否同意这种说法,谈谈你的看法。
2.在中和滴定实验中,如发生下列情况,对测定结果有没有影响?简要说明理由。
(1)盛放标准酸液的滴定管在蒸馏水洗净后未用标准酸液润洗 。
(2)滴定时,锥形瓶摇动太剧烈,有少量溶液溅出。
(3)锥形瓶用蒸馏水洗涤后,用氢氧化钠溶液润洗后加入氢氧化钠溶液。
3.某学生用0.168 2 mol/L标准盐酸滴定待测氢氧化钠溶液,氢氧化钠先取20.00 mL,
但标准盐酸滴过头了,该学生又加了2.80 mL碱液,继续做实验。这种操作是否适当?若标
准盐酸滴定管的初读数为0.20 mL,最后的末读数为18.95 mL,试计算氢氧化钠溶液的浓度。
4.运用中和滴定的原理设计一个实验方案,用标准氢氧化钠溶液测定家用食醋的浓度。
资料提供: 食醋中含有醋酸,化学式为CH COOH,是一元弱酸。
3
提示:强碱滴定弱酸,滴定终点的pH大于7,但仍可用酚酞作指示剂。
61
out-10ok Page 61 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC5.阅读下面英文资料。
We can measure the concentration of a solution by a technique known as titration. The solution
being studied is slowly added to a known quantity of a reagent, with which it reacts until an indicator
tells us that exactly equivalent number of moles of the reagents are present.
Phenolphthalein is an example of an indicator for acid-base reactions. When added to solutions
that contain an acid, phenolphthalein is colorless. In the presence of a base, it has a light pink color.
Phenolphthalein can therefore indicate when exactly enough base has been added to consume all of
the acid in a solution, because it turns from colorless to pink just after the point when equivalent
numbers of moles of acid and base have been added to the solution.
We can illustrate the calculations behind a titration experiment by looking at the reaction
between hydrobromic acid (HBr) and sodium hydroxide (NaOH).
HBr(aq)+NaOH(aq) NaBr(aq)+H O(l)
2
Exercise
Calculate the concentration of an hydrobromic acid solution if a titration experiment shows that
it takes 34.0 milliliters of a 0.100 mol/L NaOH solution to consume all of the hydrobromic acid in
a 25.0 milliliter sample.
Solution
Which solution should we start with, NaOH or hydrobromic acid? We only know the volume
of the hydrobromic acid solution, but we know both the volume and the concentration of the NaOH
solution. Thus, it seems reasonable to start by calculating the number of moles of NaOH in this
solution.
mol
0.100——NaOH×0.034 0 L=3.40×10-3 mol NaOH
L
Now what? We have a balanced chemical equation for the reaction that occurs when the two
solutions are mixed. We also know the number of moles of NaOH consumed in the reaction. We can
therefore calculate the number of moles of HBr needed to consume this NaOH.
1 mol HBr
3.40×10-3 mol NaOH×——————=3.40×10-3 mol HBr
1 mol NaOH
We now know the number of moles of HBr in the original hydrobromic acid solution, and we
also know the volume of this solution. We can therefore calculate the number of moles of
hydrobromic acid per liter, or the molarity of the solution.
3.40×10-3 mol HBr
—————————=0.136 mol/L HBr
0.250 L
The concentration of the hydrobromic acid solution is 0.136 mole per liter.
回答:
(1) 把上面例题解答译成中文。
(2) 用中文回答下面习题。
Calculate the concentration of a sulfuric acid solution if a titration experiment shows that is takes
28.0 milliliters of a 0.200 mol/L NaOH solution to consume all of the sulfuric acid in a 25.0 milliliter sample.
62
out-10ok Page 62 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC小 结 与 思 考
1.三个实验的实验原理和关键操作。
本章由3个定量测定实验组成,代表了化学定量测定的三种常用方法。应在理解测定的
化学原理和实验步骤中哪些是关键操作的基础上学会定量仪器的操作。请完成下表:
实验名称 实验原理 主要定量仪器 关键操作
测定某温度下 取一定质量的镁 ________ 确保一定量镁带全
1 mol氢气的体积 跟稀硫酸完全反应, ________ 部反应。还有___
测定产生氢气的体 _________
积,再依据镁的摩 _________
尔质量计算。计算 ________
式为______
_______
测定硫酸铜晶体 加热一定质量 ________ 准确称量。还有_
中结晶水的含量 CuSO·x H O晶体, ________ _________
4 2
测得无水硫酸铜的 ________
质量,再依据硫酸
铜和水的摩尔质量
计算出x数值。计算
式为______
________
酸碱滴定: 用已知浓度的标 ________ 正确判断滴定终点。
测定氢氧化钠溶 准盐酸滴定一定体 ________ 还有_______
液的浓度 积的待测氢氧化钠 _________
溶液,根据消耗盐 ______
酸的体积计算。计
算式为_____
________
思考:
(1)测定常温下1 mol氢气的体积的实验中,排出液体的体积数为什么不是氢气的体积?
(2)测定硫酸铜晶体结晶水含量中,为什么必须进行恒重操作?
(3)在酸碱滴定中能否用未知待测液滴定已知浓度的标准液?
63
out-10ok Page 63 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC2.中学定量仪器的读数。
名 称 最小量度单位 读 数
10 mL量筒 0.1 mL 可估计至0.05 mL
25 mL滴定管 0.1 mL 可估计至0.05 mL
电子天平 0.001 g(实验室用) 读至0.001 g
化学反应气体体积测定仪装 0.5 mL 可估计至0.2~0.3 mL
置中液体量瓶
3.定量实验中的误差分析。
思考:
(1)为什么说任何定量测定的实验结果都存在一定的误差?
(2)误差是怎样产生的?
(3)谈谈在定量测定中,正确操作、准确读数和记录的意义?
(4)你在实验报告中是否作了误差分析?你对实验误差分析是否符合你的实际实验情况?
4.定量测定实验设计的一般思路。
明确课题的条件和目标;
根据已有的知识及查阅到的相关资料确定达到目标的方法原理(有关反应、需测定
哪些物理量、计算方法等);
选择试剂和仪器,完成实验装置;
预计实验操作可能产生的问题,设想采取的措施;
讨论实验结果,进行误差分析的准备。
5.实验设计。
课题:现有氯化钠和氢氧化钠粉末的混合物(已称得质量为m g),请设计两种方法测
定该混合物中氢氧化钠的质量分数。(提示:若使氯离子变为沉淀,则先用硝酸酸化,再加
入硝酸银溶液)
完成设计:
测定原理 简要实验步骤 需直接测定的物理量 主要仪器和试剂
64
out-10ok Page 64 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC表
期
周
素
元
Ⅰ
录
附
65
out-10ok Page 65 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPCⅡ 化学词汇英中文对照表
aluminium hydroxide 氢氧化铝
aluminium oxide 氧化铝
atomic number 原子序数
burette 滴定管
constant weight 恒重
iron 铁
metallic bond 金属键
neutralization 中和
periodic law of elements 元素周期律
rare gases 稀有气体
standardized acid solution 标准酸液
standardized basic solution 标准碱液
steel 钢
titanium 钛
66
out-10ok Page 66 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC说 明
本册教材根据上海市中小学(幼儿园)课程改革委员会制定的课程
方案和《上海市中学化学课程标准(试行稿)》编写,供高中二年级第一
学期试用。
本教材由上海市长宁区教育局主持编写,经上海市中小学教材审查
委员会审查准予试用。
本册教材的编写人员有:
主编:姚子鹏 副主编:陈基福 洪东府
特约撰稿人:(按姓氏笔划为序)阮锦莲 陆惊帆 徐永初
欢迎广大师生来电来函指出教材的差错和不足,提出宝贵意见。上
海市中小学(幼儿园)课程改革委员会办公室地址:上海市陕西北路500
号(邮政编码:200041),联系电话:62560016(总机转)、52136338;出
版社电话:64089888。
声明 按照《中华人民共和国著作权法》第二十三条,关于“为实
施九年制义务教育和国家教育规划而编写出版教科书,除作者事先声明
不许使用的外,可以不经著作权人许可,在教科书中汇编已经发表的作
品片段或者短小的文字作品、音乐作品或单幅的美术作品、摄影作品,但
应当按照规定支付报酬,指明作者姓名、作品名称”的有关规定,我们
已尽量寻找原作者支付报酬。原作者如有关于支付报酬事宜可及时与出
版社联系。
67
out-10ok Page 67 2011.4.9, 10:38 PM Adobe PageMaker 6.5C/PPC责任编辑 黄金国
经上海市中小学教材审查委员会
整体设计 陈 蕾
审查准予试用 准用号 Ⅱ -GB-2007019
高级中学课本
化 学
高中二年级第一学期
(试用本)
上海市中小学(幼儿园)课程改革委员会
上海世纪出版股份有限公司
出版
上 海 科 学 技 术 出 版 社
(上海钦州南路71号,邮政编码200235)
上海新华书店发行 上海中华印刷有限公司印刷
开本890×1240 1/16 印张4.5 字数95000
2007年8月第1版 2011年5月第5次印刷
ISBN 978-7-5323-8971-1/G.1955
定价:5.25元
上海市物价局价格审查批准文号:沪价商专(2007)24号
此书如有印、装质量问题,请径向本社调换
全国物价举报电话:12358
上海科学技术出版社电话:64089888