文档内容
2024年大连市高三双基测试卷
化学
命题人:苗冬雁 于梅 廖庄 校对人:孙宇辰
注意事项:
1.请在答题纸上作答,在试卷上作答无效;
2.本试卷共100分,考试时间75分钟。
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 Mg-24 Ti-48 Ni-59
第Ⅰ卷(选择题,共45分)
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的4个选项中,只有一项是符合题目要求的。
1.2023年,第31届世界大学生夏季运动会在成都举行。下列说法错误的是
A.“锦绣之路”的蜀锦含有大量桑蚕丝,其主要成分为蛋白质
B.“绿电”是指甘孜、凉山等大山深处的水电、风电等二次能源
C.“蓉宝”机器人使用的芯片主要成分为能导电的SiO₂
D.“三星堆”群舞演员佩戴的面具材料青铜是一种铜合金
2.H₂O₂(分子结构如右图所示)是一种绿色氧化剂,应用广泛。下列说法错误的是
A.H₂O₂的电子式为
B.H₂O₂是极性分子
C.H₂O₂分子间可形成氢键
D.H₂O₂中氧原子杂化方式为sp
3.设 N 为阿伏加德罗常数的值。氮化硅(Si₃N₄)常用于制备高温结构陶瓷,可由如下反应制备:3𝑆𝑖𝑂 +6𝐶+2𝑁
A 2 2
高温𝑆𝑖 𝑁 +6𝐶𝑂。下列说法正确的是
3 4
A.Si₃N₄是共价晶体
B.28gN₂中含π键数目N
A
C.1molSiO₂中含有Si-O键的数目为2N
A
D.每生成22.4LCO转移电子数为2N
A
4.多巴胺是一种神经传导物质,其合成路线如下图所示。下列说法错误的是
A.L-酪氨酸分子中所有碳原子可能同平面
B.1molL-多巴最多可以与4molH₂发生加成反应
C.多巴胺可与FeCl₃溶液发生显色反应·
D.L-酪氨酸、L-多巴和多巴胺均可与HCl溶液反应
5.下列关于离子反应的说法正确的是
A.CuSO₄溶液与过量氨水混合:𝐶𝑢2−+2𝑁𝐻 ⋅𝐻 𝑂 =𝐶𝑢(𝑂𝐻) ↓+2𝑁𝐻+
3 2 2 4
𝐵.0.1𝑚𝑜𝑙⋅𝐿⁻¹𝑁𝑎𝐻𝐶𝑂₃溶液:Na⁺、Al³⁺、Cl⁻、NO₃一定能大量共存
C.常温下,pH=2的溶液:Na⁻、Mg²⁻、Cl⁻、S₂O 2⁻定能大量共存
3
D.向Agl悬浊液中滴加Na₂S溶液:2𝐴𝑔𝐼(𝑠)+𝑆2−(𝑎𝑞)= Ag S(s)+2I-(aq)
2
6.可用于治疗支原体肺炎的药物阿奇霉素的结构简式如下图所示。下列说法正确的是
A.属于高分子化合物 B.含氧官能团只有羟基、酯基X
C.分子中含有手性碳原子 D.所含元素第一电离能小于N的有2种
7.清华大学王保国教授等人提出了一种双极膜硝酸盐还原电合成氨工艺,其反应原理为 KNO +2H O 电解𝑁𝐻 ↑
3 2 3
+2𝑂 ↑+𝐾𝑂𝐻。下列说法正确的是
2
2024年大连市高三双基测试卷 化学 第1页 共6页 大连教育学院
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}A.m是电源正极B.阳极反应为4𝑂𝐻⁻−4𝑒⁻=2𝐻₂𝑂+𝑂₂↑
C.双极膜中OH⁻移向a极区D.每有1mole⁻通过外电路,消耗1𝑚𝑜𝑙𝑁𝑂−
3
8.工业上用电解饱和NaCl溶液生成的氯气为原料生产溴酸钾(𝐾𝐵𝑟𝑂₃)的工艺流程如下。下列说法错误的是
A.合成I中的氧化剂与还原剂的物质的量之比为1:5
B.合成Ⅱ中利用了物质的溶解度差异
C.粗产品𝐾𝐵𝑟𝑂₃可通过重结晶进行提纯
D.KBrO₃是一种含有共价键的离子化合物
9.下列实验操作、现象和结论均正确的是
操作 现象 结论
A 向菠菜汁中加入少量稀硝酸和KSCN溶液 溶液变红 菠菜汁中含有铁元素
加热1-溴丁烷、氢氧化钠和乙醇的混合溶液,将产生
B 溶液褪色 有烯烃生成
气体通入酸性高锰酸钾溶液中
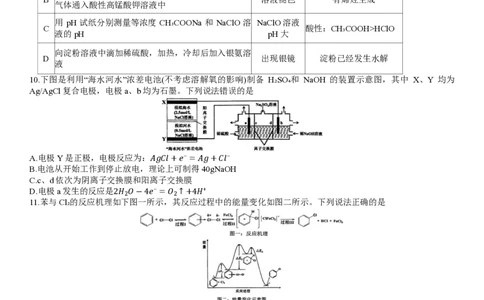
用 pH 试纸分别测量等浓度 CH₃COONa 和 NaClO 溶 NaClO溶液
C 酸性:CH₃COOH>HClO
液的pH pH大
向淀粉溶液中滴加稀硫酸,加热,冷却后加入银氨溶
D 出现银镜 淀粉已经发生水解
液
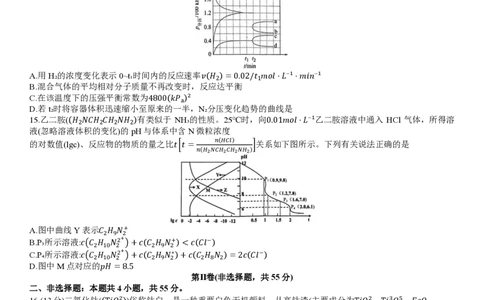
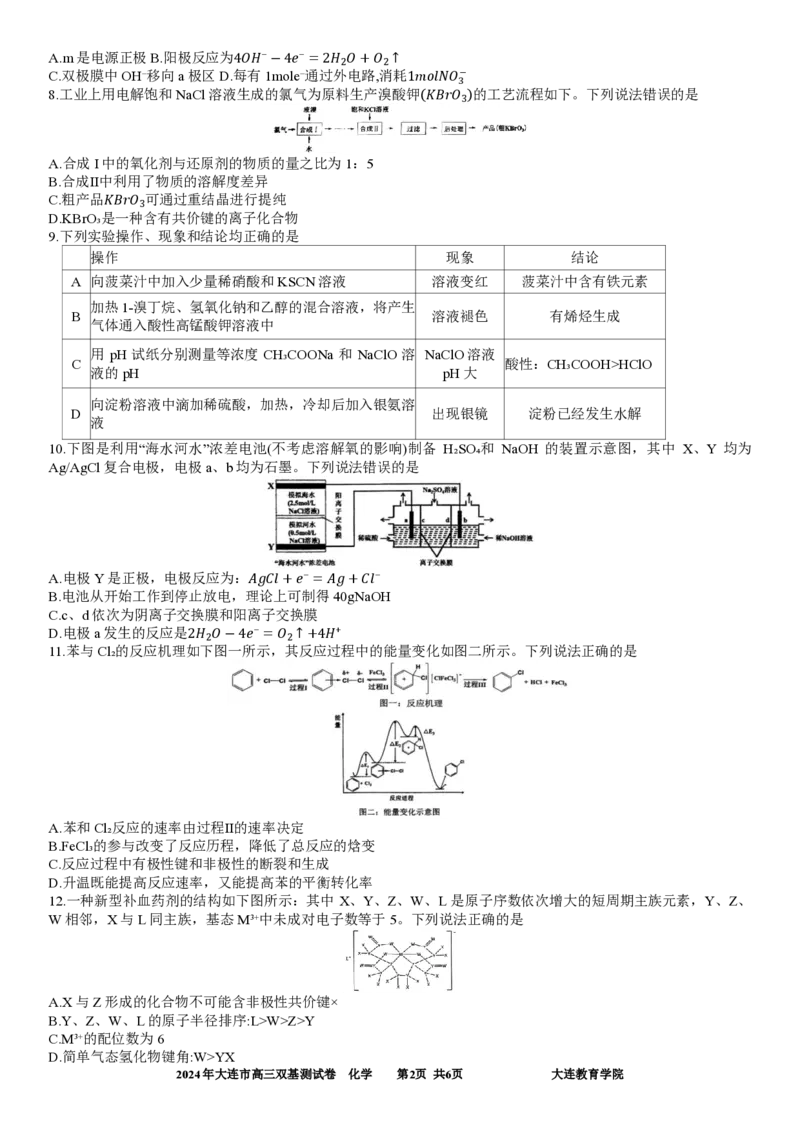
10.下图是利用“海水河水”浓差电池(不考虑溶解氧的影响)制备 H₂SO₄和 NaOH 的装置示意图,其中 X、Y 均为
Ag/AgCl复合电极,电极a、b均为石墨。下列说法错误的是
A.电极Y是正极,电极反应为:𝐴𝑔𝐶𝑙+𝑒⁻=𝐴𝑔+𝐶𝑙⁻
B.电池从开始工作到停止放电,理论上可制得40gNaOH
C.c、d依次为阴离子交换膜和阳离子交换膜
D.电极a发生的反应是2𝐻₂𝑂−4𝑒⁻=𝑂₂↑+4𝐻⁺
11.苯与Cl₂的反应机理如下图一所示,其反应过程中的能量变化如图二所示。下列说法正确的是
A.苯和Cl₂反应的速率由过程Ⅱ的速率决定
B.FeCl₃的参与改变了反应历程,降低了总反应的焓变
C.反应过程中有极性键和非极性的断裂和生成
D.升温既能提高反应速率,又能提高苯的平衡转化率
12.一种新型补血药剂的结构如下图所示:其中 X、Y、Z、W、L是原子序数依次增大的短周期主族元素,Y、Z、
W相邻,X与L同主族,基态M³⁺中未成对电子数等于5。下列说法正确的是
A.X与Z形成的化合物不可能含非极性共价键×
B.Y、Z、W、L的原子半径排序:L>W>Z>Y
C.M³⁺的配位数为6
D.简单气态氢化物键角:W>YX
2024年大连市高三双基测试卷 化学 第2页 共6页 大连教育学院
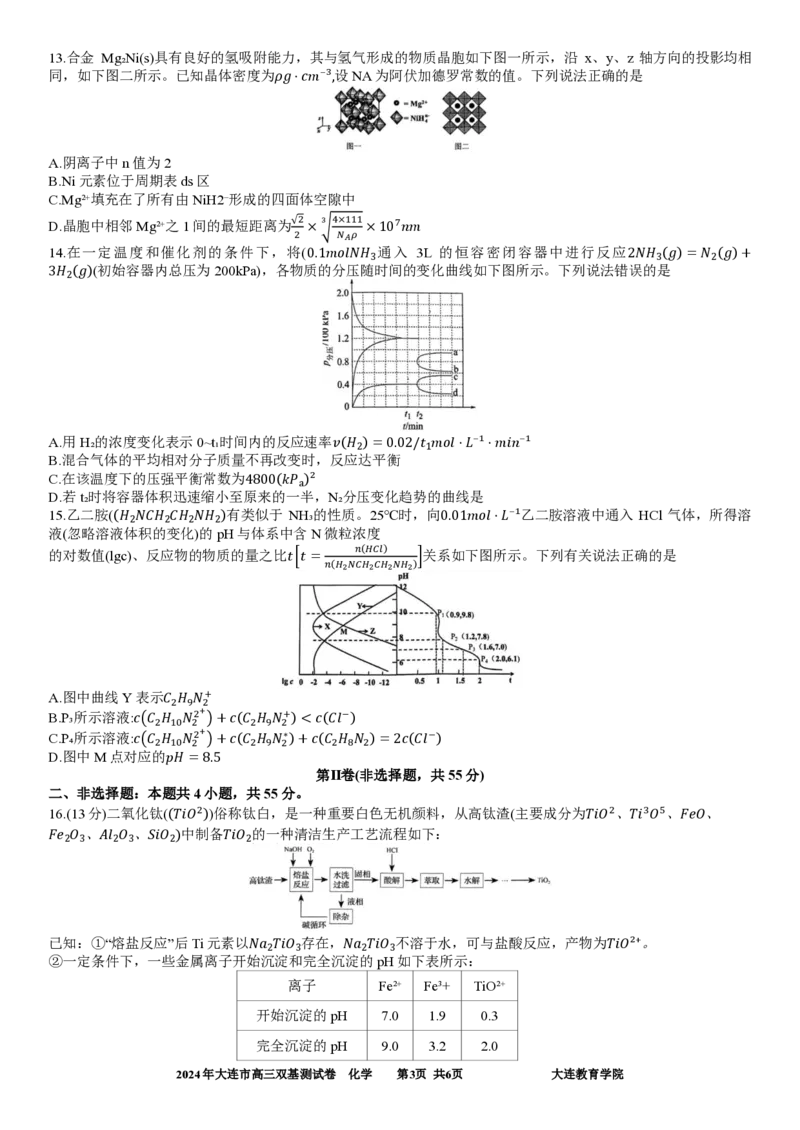
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}13.合金 Mg₂Ni(s)具有良好的氢吸附能力,其与氢气形成的物质晶胞如下图一所示,沿 x、y、z 轴方向的投影均相
同,如下图二所示。已知晶体密度为𝜌𝑔⋅𝑐𝑚⁻³,设NA为阿伏加德罗常数的值。下列说法正确的是
A.阴离子中n值为2
B.Ni元素位于周期表ds区
C.Mg²⁺填充在了所有由NiH2⁻形成的四面体空隙中
D.晶胞中相邻Mg²⁺之1间的最短距离为√2 × 3 √ 4×111 ×107𝑛𝑚
2 𝑁𝐴𝜌
14.在一定温度和催化剂的条件下,将(0.1𝑚𝑜𝑙𝑁𝐻₃通入 3L 的恒容密闭容器中进行反应2𝑁𝐻₃(𝑔)=𝑁₂(𝑔)+
3𝐻₂(𝑔)(初始容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。下列说法错误的是
A.用H₂的浓度变化表示0~t₁时间内的反应速率𝑣(𝐻₂)=0.02/𝑡₁𝑚𝑜𝑙⋅𝐿⁻¹⋅𝑚𝑖𝑛⁻¹
B.混合气体的平均相对分子质量不再改变时,反应达平衡
C.在该温度下的压强平衡常数为4800(𝑘𝑃ₐ)²
D.若t₂时将容器体积迅速缩小至原来的一半,N₂分压变化趋势的曲线是
15.乙二胺((𝐻₂𝑁𝐶𝐻₂𝐶𝐻₂𝑁𝐻₂)有类似于 NH₃的性质。25℃时,向0.01𝑚𝑜𝑙⋅𝐿⁻¹乙二胺溶液中通入 HCl 气体,所得溶
液(忽略溶液体积的变化)的pH与体系中含N微粒浓度
𝑛(𝐻𝐶𝑙)
的对数值(lgc)、反应物的物质的量之比𝑡[𝑡 = ]关系如下图所示。下列有关说法正确的是
𝑛(𝐻2𝑁𝐶𝐻2𝐶𝐻2𝑁𝐻2 )
A.图中曲线Y表示𝐶 𝐻 𝑁+
2 9 2
B.P₃所示溶液:𝑐(𝐶 𝐻 𝑁2+ )+𝑐(𝐶 𝐻 𝑁+)<𝑐(𝐶𝑙−)
2 10 2 2 9 2
C.P₄所示溶液:𝑐(𝐶 𝐻 𝑁2+ )+𝑐(𝐶 𝐻 𝑁∗)+𝑐(𝐶 𝐻 𝑁 )=2𝑐(𝐶𝑙−)
2 10 2 2 9 2 2 8 2
D.图中M点对应的𝑝𝐻 =8.5
第Ⅱ卷(非选择题,共55分)
二、非选择题:本题共4小题,共55分。
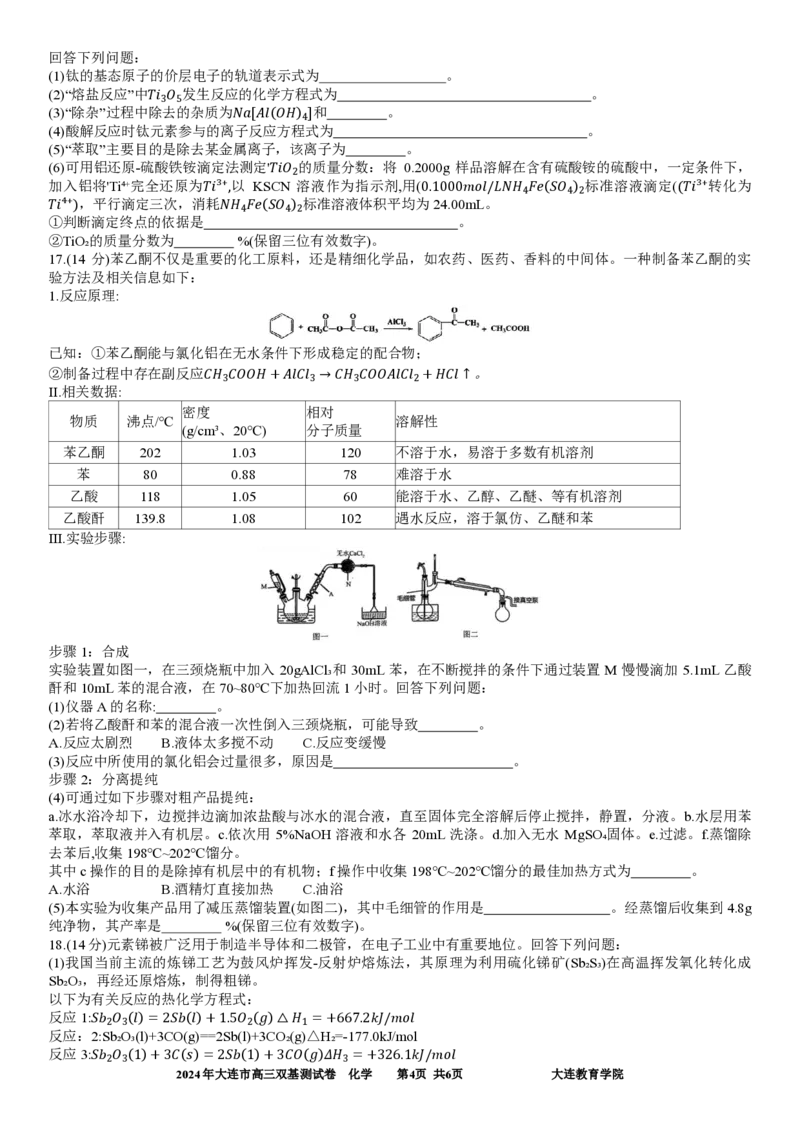
16.(13分)二氧化钛((𝑇𝑖𝑂2))俗称钛白,是一种重要白色无机颜料,从高钛渣(主要成分为𝑇𝑖𝑂2、𝑇𝑖3𝑂5、𝐹𝑒𝑂、
𝐹𝑒₂𝑂₃、𝐴𝑙₂𝑂₃、𝑆𝑖𝑂₂)中制备𝑇𝑖𝑂₂的一种清洁生产工艺流程如下:
已知:①“熔盐反应”后Ti元素以𝑁𝑎₂𝑇𝑖𝑂₃存在,𝑁𝑎₂𝑇𝑖𝑂₃不溶于水,可与盐酸反应,产物为𝑇𝑖𝑂²⁺。
②一定条件下,一些金属离子开始沉淀和完全沉淀的pH如下表所示:
离子 Fe²⁺ Fe³+ TiO²⁺
开始沉淀的pH 7.0 1.9 0.3
完全沉淀的pH 9.0 3.2 2.0
2024年大连市高三双基测试卷 化学 第3页 共6页 大连教育学院
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}回答下列问题:
(1)钛的基态原子的价层电子的轨道表示式为 。
(2)“熔盐反应”中𝑇𝑖₃𝑂₅发生反应的化学方程式为 。
(3)“除杂”过程中除去的杂质为𝑁𝑎[𝐴𝑙(𝑂𝐻)₄]和 。
(4)酸解反应时钛元素参与的离子反应方程式为 。
(5)“萃取”主要目的是除去某金属离子,该离子为 。
(6)可用铝还原-硫酸铁铵滴定法测定'𝑇𝑖𝑂₂的质量分数:将 0.2000g 样品溶解在含有硫酸铵的硫酸中,一定条件下,
加入铝将'Ti⁴⁺完全还原为𝑇𝑖³⁺,以 KSCN 溶液作为指示剂,用(0.1000𝑚𝑜𝑙/𝐿𝑁𝐻₄𝐹𝑒(𝑆𝑂₄)₂标准溶液滴定((𝑇𝑖³⁺转化为
𝑇𝑖⁴⁺),平行滴定三次,消耗𝑁𝐻₄𝐹𝑒(𝑆𝑂₄)₂标准溶液体积平均为24.00mL。
①判断滴定终点的依据是 。
②TiO₂的质量分数为 %(保留三位有效数字)。
17.(14 分)苯乙酮不仅是重要的化工原料,还是精细化学品,如农药、医药、香料的中间体。一种制备苯乙酮的实
验方法及相关信息如下:
1.反应原理:
已知:①苯乙酮能与氯化铝在无水条件下形成稳定的配合物;
②制备过程中存在副反应𝐶𝐻₃𝐶𝑂𝑂𝐻+𝐴𝑙𝐶𝑙₃→𝐶𝐻₃𝐶𝑂𝑂𝐴𝑙𝐶𝑙₂+𝐻𝐶𝑙 ↑。
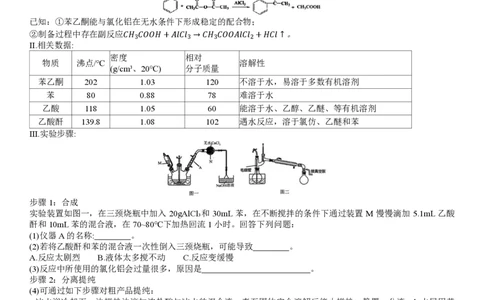
II.相关数据:
密度 相对
物质 沸点/℃ 溶解性
(g/cm³、20℃) 分子质量
苯乙酮 202 1.03 120 不溶于水,易溶于多数有机溶剂
苯 80 0.88 78 难溶于水
乙酸 118 1.05 60 能溶于水、乙醇、乙醚、等有机溶剂
乙酸酐 139.8 1.08 102 遇水反应,溶于氯仿、乙醚和苯
Ⅲ.实验步骤:
步骤1:合成
实验装置如图一,在三颈烧瓶中加入 20gAlCl₃和 30mL苯,在不断搅拌的条件下通过装置 M慢慢滴加 5.1mL乙酸
酐和10mL苯的混合液,在70~80℃下加热回流1小时。回答下列问题:
(1)仪器A的名称: 。
(2)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致 。
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢
(3)反应中所使用的氯化铝会过量很多,原因是 。
步骤2:分离提纯
(4)可通过如下步骤对粗产品提纯:
a.冰水浴冷却下,边搅拌边滴加浓盐酸与冰水的混合液,直至固体完全溶解后停止搅拌,静置,分液。b.水层用苯
萃取,萃取液并入有机层。c.依次用 5%NaOH 溶液和水各 20mL 洗涤。d.加入无水 MgSO₄固体。e.过滤。f.蒸馏除
去苯后,收集198℃~202℃馏分。
其中c操作的目的是除掉有机层中的有机物;f操作中收集198℃~202℃馏分的最佳加热方式为 。
A.水浴 B.酒精灯直接加热 C.油浴
(5)本实验为收集产品用了减压蒸馏装置(如图二),其中毛细管的作用是 。经蒸馏后收集到4.8g
纯净物,其产率是 %(保留三位有效数字)。
18.(14分)元素锑被广泛用于制造半导体和二极管,在电子工业中有重要地位。回答下列问题:
(1)我国当前主流的炼锑工艺为鼓风炉挥发-反射炉熔炼法,其原理为利用硫化锑矿(Sb₂S₃)在高温挥发氧化转化成
Sb₂O₃,再经还原熔炼,制得粗锑。
以下为有关反应的热化学方程式:
反应1:𝑆𝑏₂𝑂₃(𝑙)=2𝑆𝑏(𝑙)+1.5𝑂₂(𝑔)△𝐻₁=+667.2𝑘𝐽/𝑚𝑜𝑙
反应:2:Sb₂O₃(l)+3CO(g)==2Sb(l)+3CO₂(g)△H₂=-177.0kJ/mol
反应3:𝑆𝑏₂𝑂₃(1)+3𝐶(𝑠)=2𝑆𝑏(1)+3𝐶𝑂(𝑔)𝛥𝐻₃=+326.1𝑘𝐽/𝑚𝑜𝑙
2024年大连市高三双基测试卷 化学 第4页 共6页 大连教育学院
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}① 碳燃烧热的热化学方程式为 。
② 反应 1、2和 3的△G随温度的变化关系如下图所示。工业还原熔炼粗锑的温度一般为 1423K~1473K,结合图像
从热力学角度分析,宜选用 (填“C”或者“CO”)作还原剂,理由是 。
(2)某企业对粗铜精炼阳极泥中锑元素进行回收。
①向脱铜阳极泥中加入硫酸和氯化钠进行浸出,使𝑆𝑏₂𝑂₃转化为较稳定的 SbCl₄,反应的离子方程式
为 。
③ 经硫酸和氯化钠浸出后的 Sb(Ⅲ)在一定条件下可发生水解反应进而沉淀出锑,为了寻求最佳沉锑条件,分别对
水解时间、浸出液稀释倍数、温度等因素进行探究,结果如图所示。水解沉锑的最佳条件为 。
时间(分钟)
(3)水溶液中的 Sb(III)易被氧化成 Sb(V),Sb(V)主要以:𝑆𝑏(𝑂𝐻) 、𝑆𝑏(𝑂𝐻)−的形式存在。在 298K条件下,方解石(主
5 6
要成分𝐶𝑎𝐶𝑂₃)在天然水体中会逐渐溶解并释放𝐶𝑎2÷,与水体中的 Sb(OH)。形成(𝐶𝑎[𝑆𝑏(𝑂𝐻)₆]₂难溶物,进一步聚集
生长而固定在方解石表面。体系中 pH 与 lgc 关系如下图所示,c 为𝑆𝑏(𝑂𝐻) 、𝑆𝑏(𝑂𝐻)−、𝐶𝑎2+、𝐶𝑂2−的浓度,单
5 6 3
位为mol/L。已知天然水体表面(𝐶𝑂₂的分压保持恒定。
① 图中A线代表的粒子为 。
②𝑆𝑏(𝑂𝐻)₅的电离方程式可以写成𝑆𝑏(𝑂𝐻) +𝐻 𝑂 =𝑆𝑏(𝑂𝐻)−+𝐻+,其电离平衡常数为 。
5 2 6
19.(14分)苯烯莫德是一种小分子药物,因可抑制多种自身免疫性疾病而成为研究热点。其合成路线如下:
2024年大连市高三双基测试卷 化学 第5页 共6页 大连教育学院
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}回答下列问题:
(1)A中官能团名称为,苯烯莫德的分子式为 。
(2)合成路线中碘甲烷的主要作用是 。
(3)B→C的化学反应方程式为 。
(4)D→E的反应类型分别为 。
(5)芳香化合物W是D的同分异构体,请写出其中核磁共振氢谱显示有3组峰,且峰面积之比为3:2:1的同分异
构体的结构简式。 (不考虑立体异构,写出其中1种即可)
(6)参照流程,选择合适的试剂,写出由 制备 的合成路线。
2024年大连市高三双基测试卷 化学 第6页 共6页 大连教育学院
{#{QQABTYyAgggAQBAAARhCEQHoCAGQkBECCAoGAAAAsAAAwRFABCA=}#}