文档内容
龙岩市 2025 年高中毕业班三月教学质量检测
化学试题
(考试时间:75分钟 满分:100分)
注意:
1.请将答案填写在答题卡上
2.可能用到的相对原子质量:
一、选择题:本题共10小题,每小题4分,共40分。每小题只有一个选项符合题目要求。
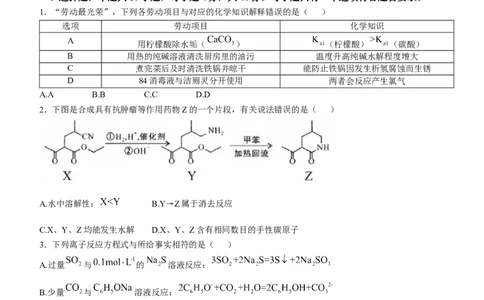
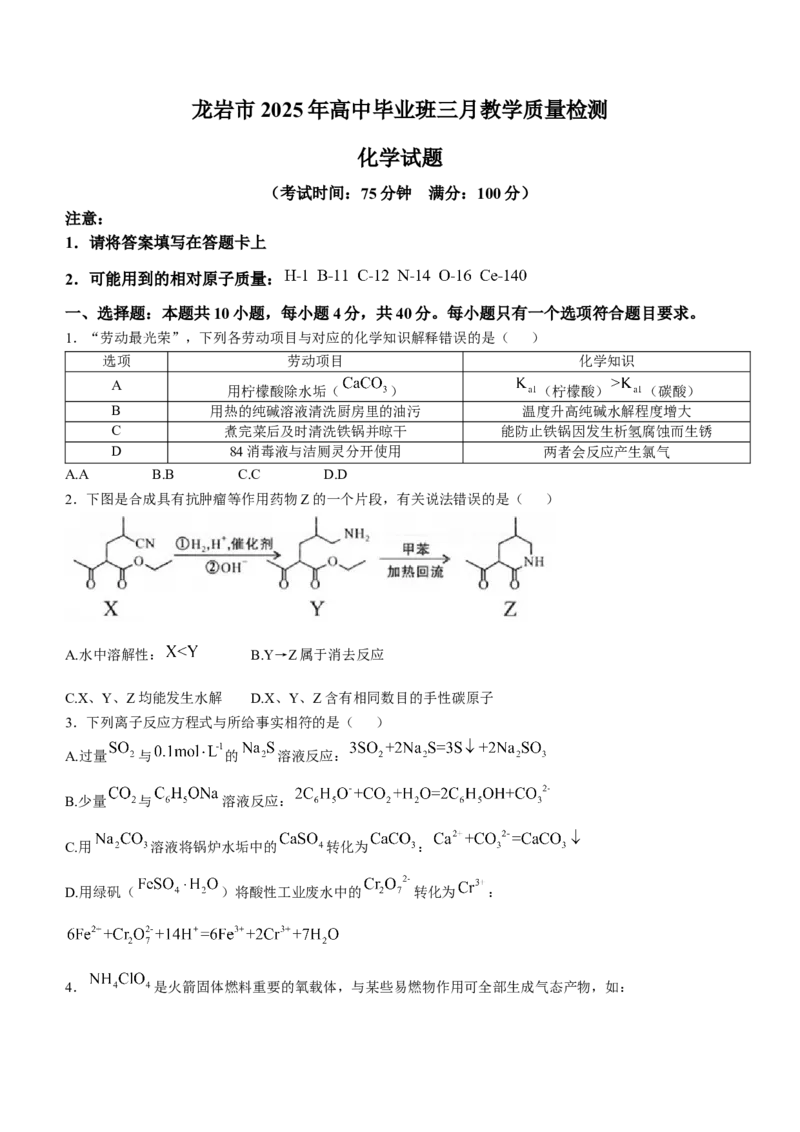
1.“劳动最光荣”,下列各劳动项目与对应的化学知识解释错误的是( )
选项 劳动项目 化学知识
A
用柠檬酸除水垢( ) (柠檬酸) (碳酸)
B 用热的纯碱溶液清洗厨房里的油污 温度升高纯碱水解程度增大
C 煮完菜后及时清洗铁锅并晾干 能防止铁锅因发生析氢腐蚀而生锈
D 84消毒液与洁厕灵分开使用 两者会反应产生氯气
A.A B.B C.C D.D
2.下图是合成具有抗肿瘤等作用药物Z的一个片段,有关说法错误的是( )
A.水中溶解性: B.Y→Z属于消去反应
C.X、Y、Z均能发生水解 D.X、Y、Z含有相同数目的手性碳原子
3.下列离子反应方程式与所给事实相符的是( )
A.过量 与 的 溶液反应:
B.少量 与 溶液反应:
C.用 溶液将锅炉水垢中的 转化为 :
D.用绿矾( )将酸性工业废水中的 转化为 :
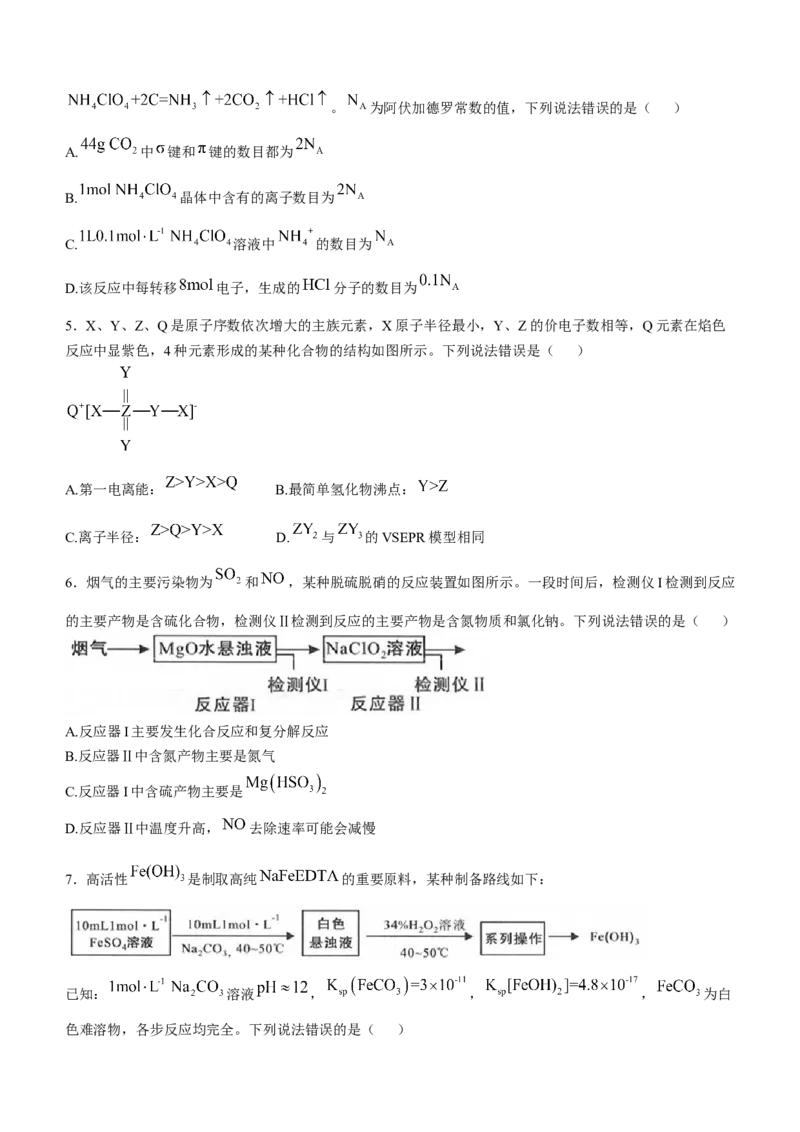
4. 是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,如:。 为阿伏加德罗常数的值,下列说法错误的是( )
A. 中 键和 键的数目都为
B. 晶体中含有的离子数目为
C. 溶液中 的数目为
D.该反应中每转移 电子,生成的 分子的数目为
5.X、Y、Z、Q是原子序数依次增大的主族元素,X原子半径最小,Y、Z的价电子数相等,Q元素在焰色
反应中显紫色,4种元素形成的某种化合物的结构如图所示。下列说法错误是( )
A.第一电离能: B.最简单氢化物沸点:
C.离子半径: D. 与 的VSEPR模型相同
6.烟气的主要污染物为 和 ,某种脱硫脱硝的反应装置如图所示。一段时间后,检测仪I检测到反应
的主要产物是含硫化合物,检测仪Ⅱ检测到反应的主要产物是含氮物质和氯化钠。下列说法错误的是( )
A.反应器I主要发生化合反应和复分解反应
B.反应器Ⅱ中含氮产物主要是氮气
C.反应器I中含硫产物主要是
D.反应器Ⅱ中温度升高, 去除速率可能会减慢
7.高活性 是制取高纯 的重要原料,某种制备路线如下:
已知: 溶液 , , , 为白
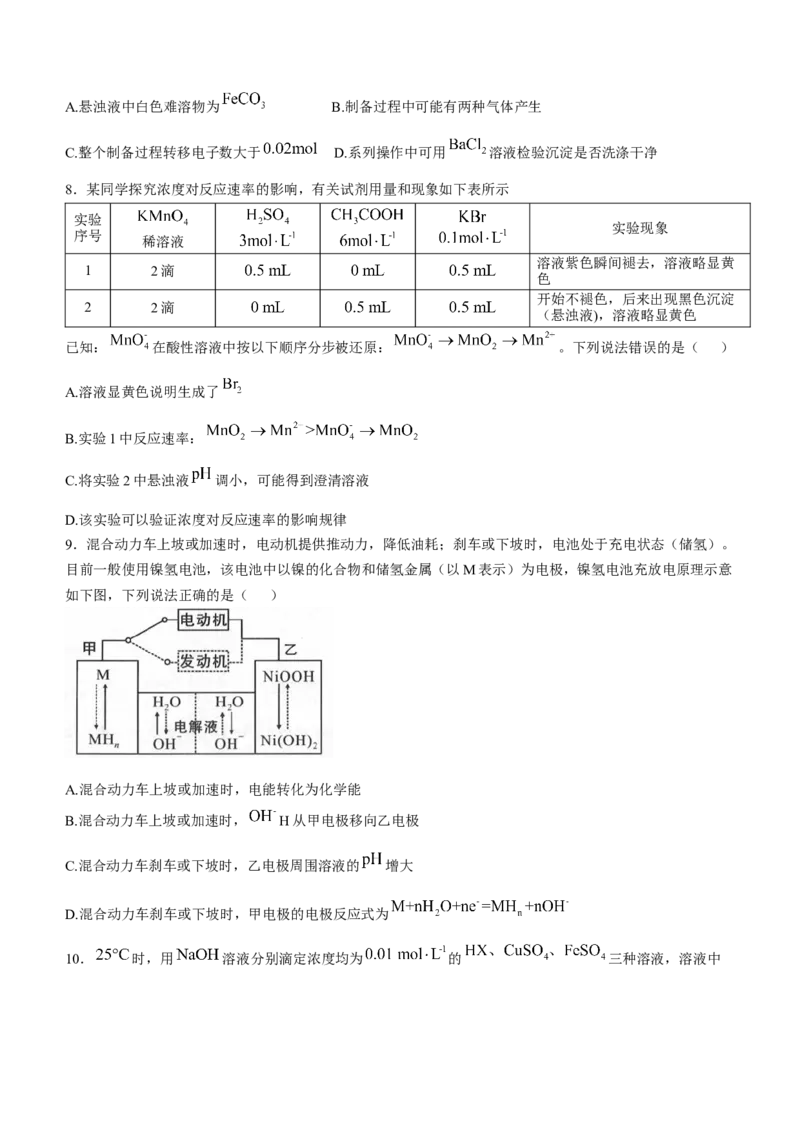
色难溶物,各步反应均完全。下列说法错误的是( )A.悬浊液中白色难溶物为 B.制备过程中可能有两种气体产生
C.整个制备过程转移电子数大于 D.系列操作中可用 溶液检验沉淀是否洗涤干净
8.某同学探究浓度对反应速率的影响,有关试剂用量和现象如下表所示
实验
实验现象
序号
稀溶液
溶液紫色瞬间褪去,溶液略显黄
1 2滴
色
开始不褪色,后来出现黑色沉淀
2 2滴
(悬浊液),溶液略显黄色
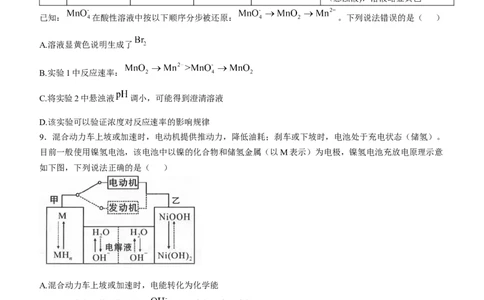
已知: 在酸性溶液中按以下顺序分步被还原: 。下列说法错误的是( )
A.溶液显黄色说明生成了
B.实验1中反应速率:
C.将实验2中悬浊液 调小,可能得到澄清溶液
D.该实验可以验证浓度对反应速率的影响规律
9.混合动力车上坡或加速时,电动机提供推动力,降低油耗;刹车或下坡时,电池处于充电状态(储氢)。
目前一般使用镍氢电池,该电池中以镍的化合物和储氢金属(以M表示)为电极,镍氢电池充放电原理示意
如下图,下列说法正确的是( )
A.混合动力车上坡或加速时,电能转化为化学能
B.混合动力车上坡或加速时, H从甲电极移向乙电极
C.混合动力车刹车或下坡时,乙电极周围溶液的 增大
D.混合动力车刹车或下坡时,甲电极的电极反应式为
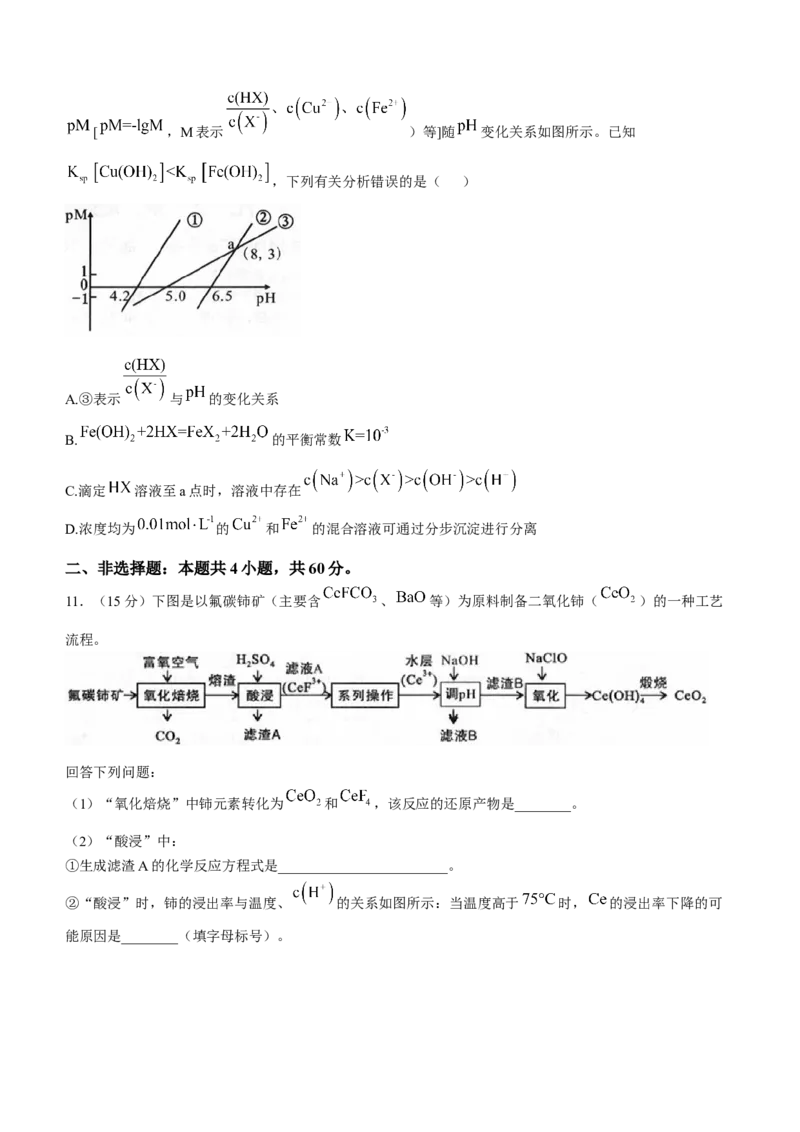
10. 时,用 溶液分别滴定浓度均为 的 三种溶液,溶液中[ ,M表示 )等]随 变化关系如图所示。已知
,下列有关分析错误的是( )
A.③表示 与 的变化关系
B. 的平衡常数
C.滴定 溶液至a点时,溶液中存在
D.浓度均为 的 和 的混合溶液可通过分步沉淀进行分离
二、非选择题:本题共4小题,共60分。
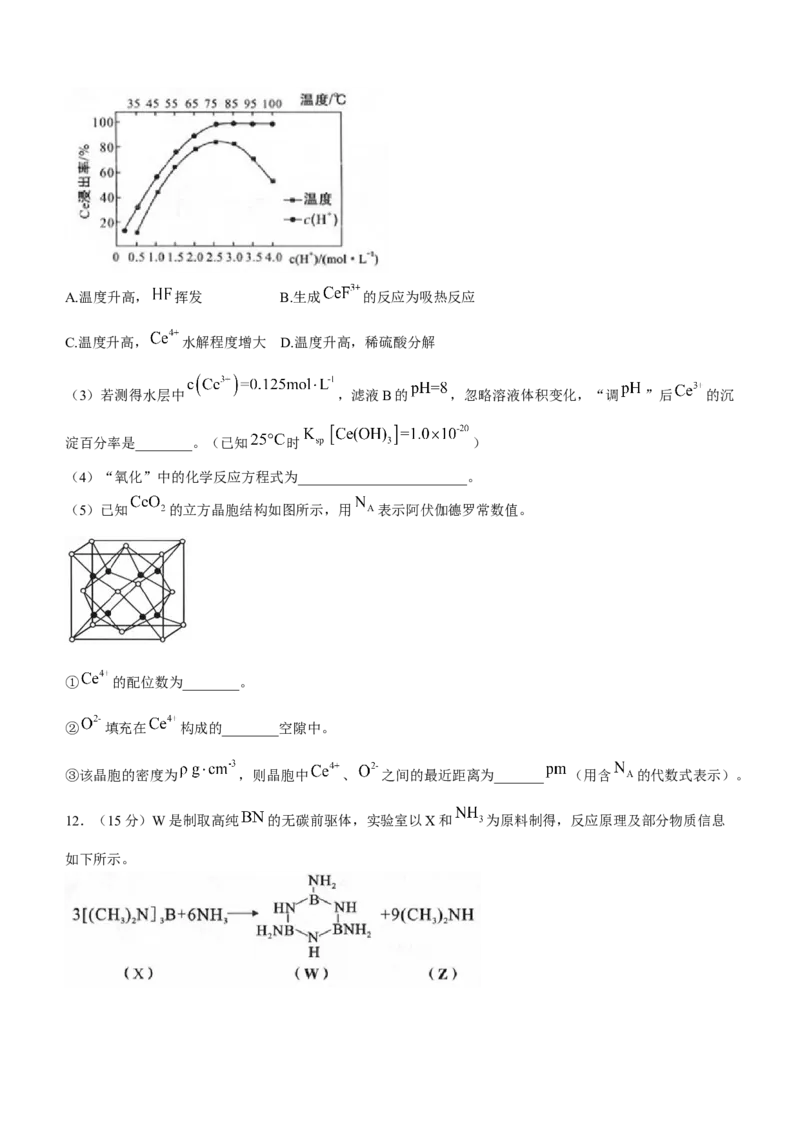
11.(15分)下图是以氟碳铈矿(主要含 、 等)为原料制备二氧化铈( )的一种工艺
流程。
回答下列问题:
(1)“氧化焙烧”中铈元素转化为 和 ,该反应的还原产物是________。
(2)“酸浸”中:
①生成滤渣A的化学反应方程式是________________________。
②“酸浸”时,铈的浸出率与温度、 的关系如图所示:当温度高于 时, 的浸出率下降的可
能原因是________(填字母标号)。A.温度升高, 挥发 B.生成 的反应为吸热反应
C.温度升高, 水解程度增大 D.温度升高,稀硫酸分解
(3)若测得水层中 ,滤液B的 ,忽略溶液体积变化,“调 ”后 的沉
淀百分率是________。(已知 时 )
(4)“氧化”中的化学反应方程式为________________________。
(5)已知 的立方晶胞结构如图所示,用 表示阿伏伽德罗常数值。
① 的配位数为________。
② 填充在 构成的________空隙中。
③该晶胞的密度为 ,则晶胞中 、 之间的最近距离为_______ (用含 的代数式表示)。
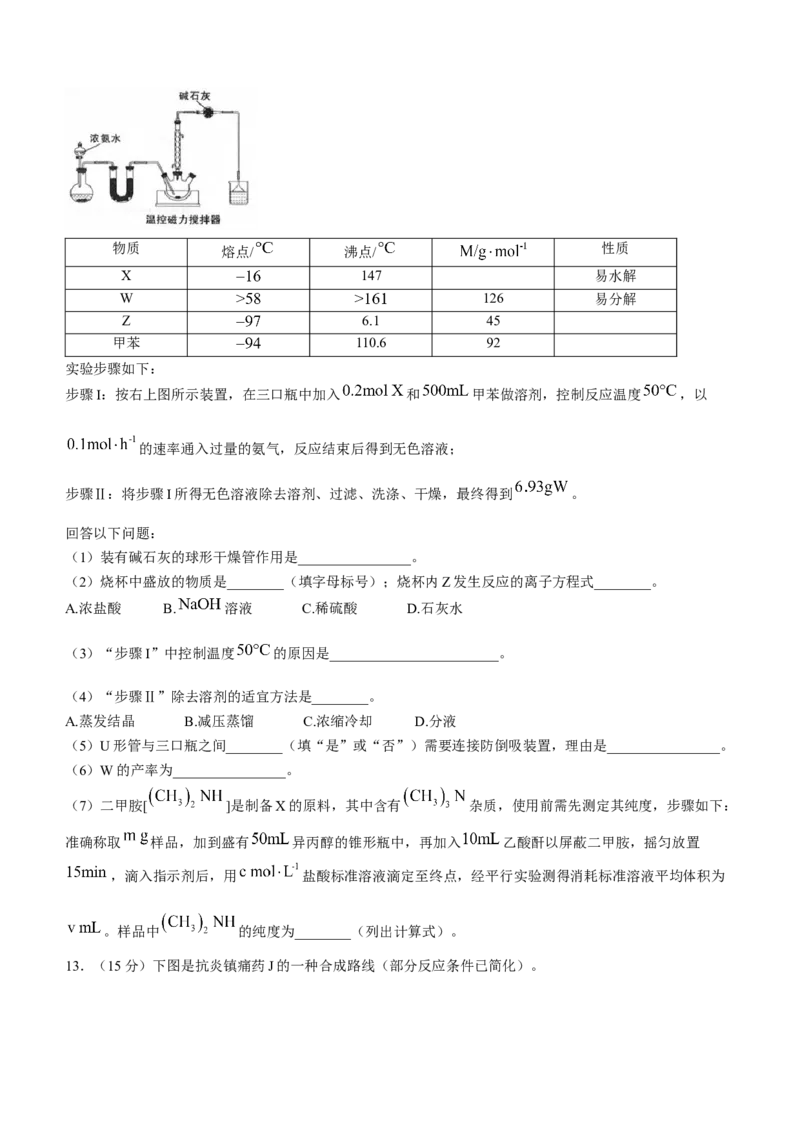
12.(15分)W是制取高纯 的无碳前驱体,实验室以X和 为原料制得,反应原理及部分物质信息
如下所示。物质 熔点/ 沸点/ 性质
X 147 易水解
W 126 易分解
Z 6.1 45
甲苯 110.6 92
实验步骤如下:
步骤I:按右上图所示装置,在三口瓶中加入 和 甲苯做溶剂,控制反应温度 ,以
的速率通入过量的氨气,反应结束后得到无色溶液;
步骤Ⅱ:将步骤I所得无色溶液除去溶剂、过滤、洗涤、干燥,最终得到 。
回答以下问题:
(1)装有碱石灰的球形干燥管作用是________________。
(2)烧杯中盛放的物质是________(填字母标号);烧杯内Z发生反应的离子方程式________。
A.浓盐酸 B. 溶液 C.稀硫酸 D.石灰水
(3)“步骤I”中控制温度 的原因是________________________。
(4)“步骤Ⅱ”除去溶剂的适宜方法是________。
A.蒸发结晶 B.减压蒸馏 C.浓缩冷却 D.分液
(5)U形管与三口瓶之间________(填“是”或“否”)需要连接防倒吸装置,理由是________________。
(6)W的产率为________________。
(7)二甲胺[ ]是制备X的原料,其中含有 杂质,使用前需先测定其纯度,步骤如下:
准确称取 样品,加到盛有 异丙醇的锥形瓶中,再加入 乙酸酐以屏蔽二甲胺,摇匀放置
,滴入指示剂后,用 盐酸标准溶液滴定至终点,经平行实验测得消耗标准溶液平均体积为
。样品中 的纯度为________(列出计算式)。
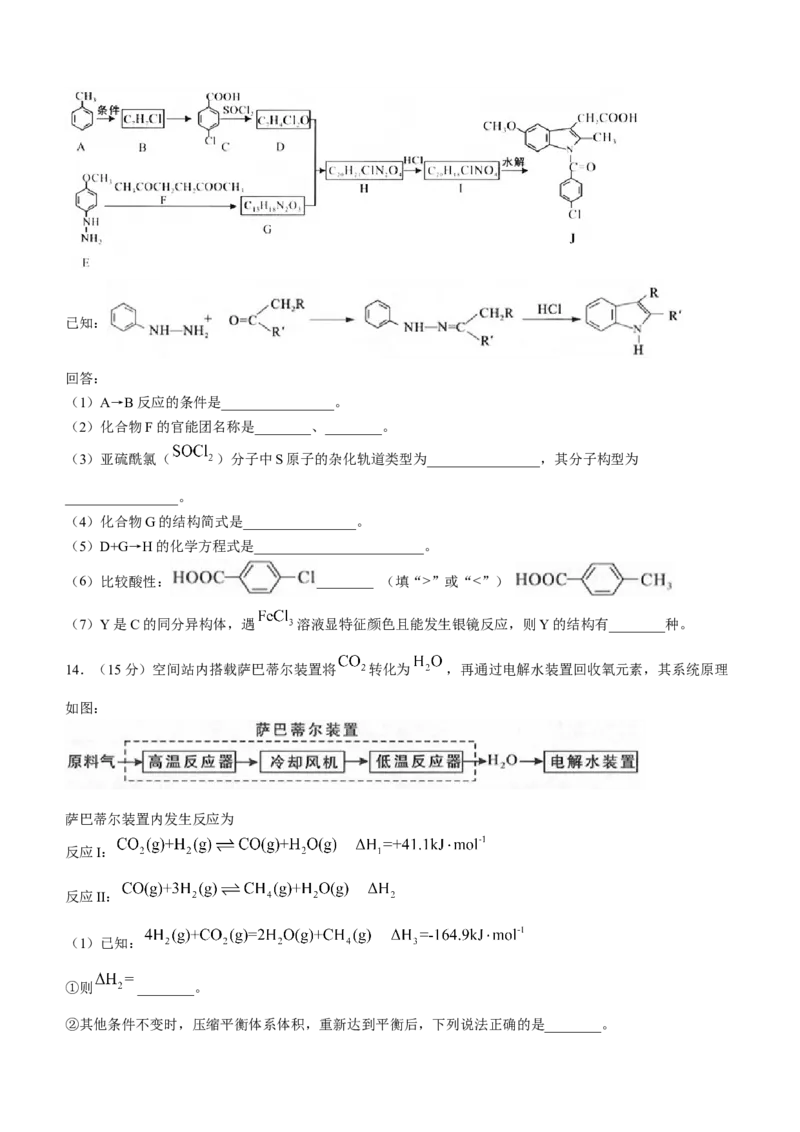
13.(15分)下图是抗炎镇痛药J的一种合成路线(部分反应条件已简化)。已知:
回答:
(1)A→B反应的条件是________________。
(2)化合物F的官能团名称是________、________。
(3)亚硫酰氯( )分子中S原子的杂化轨道类型为________________,其分子构型为
________________。
(4)化合物G的结构简式是________________。
(5)D+G→H的化学方程式是________________________。
(6)比较酸性: ________ (填“>”或“<”)
(7)Y是C的同分异构体,遇 溶液显特征颜色且能发生银镜反应,则Y的结构有________种。
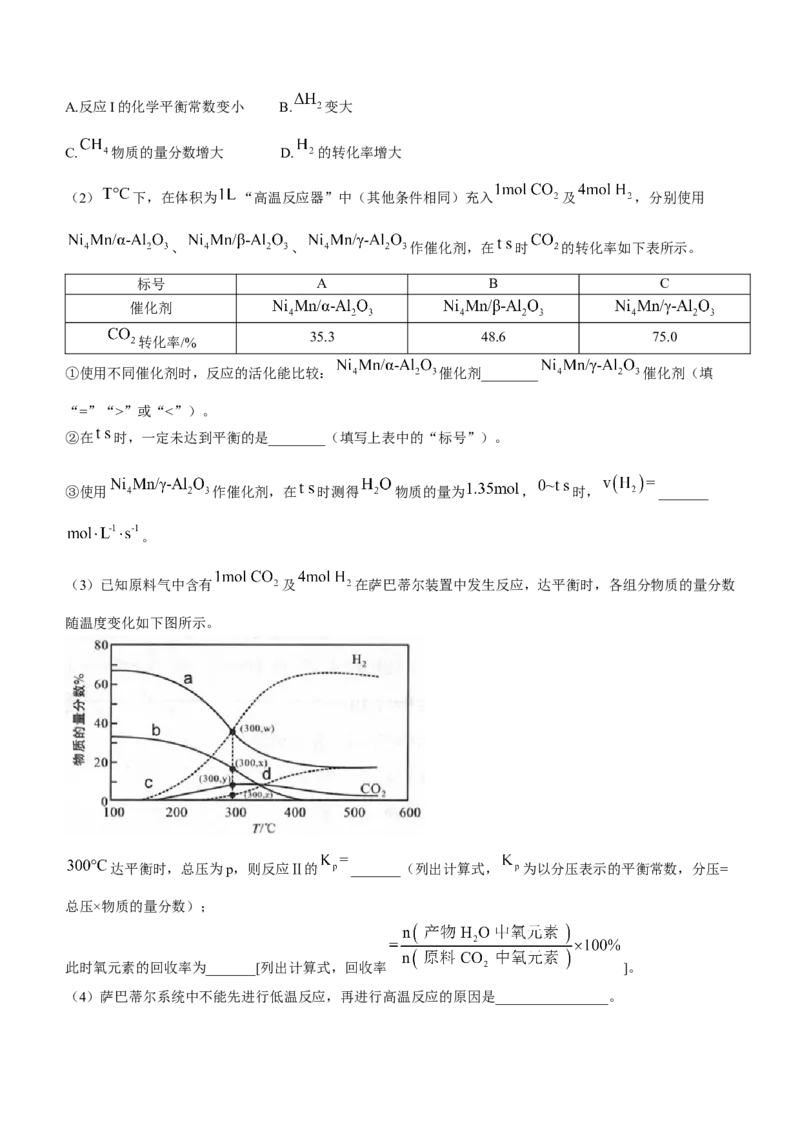
14.(15分)空间站内搭载萨巴蒂尔装置将 转化为 ,再通过电解水装置回收氧元素,其系统原理
如图:
萨巴蒂尔装置内发生反应为
反应I:
反应II:
(1)已知:
①则 ________。
②其他条件不变时,压缩平衡体系体积,重新达到平衡后,下列说法正确的是________。A.反应I的化学平衡常数变小 B. 变大
C. 物质的量分数增大 D. 的转化率增大
(2) 下,在体积为 “高温反应器”中(其他条件相同)充入 及 ,分别使用
、 、 作催化剂,在 时 的转化率如下表所示。
标号 A B C
催化剂
35.3 48.6 75.0
转化率/%
①使用不同催化剂时,反应的活化能比较: 催化剂________ 催化剂(填
“=”“>”或“<”)。
②在 时,一定未达到平衡的是________(填写上表中的“标号”)。
③使用 作催化剂,在 时测得 物质的量为 , 时, _______
。
(3)已知原料气中含有 及 在萨巴蒂尔装置中发生反应,达平衡时,各组分物质的量分数
随温度变化如下图所示。
达平衡时,总压为p,则反应Ⅱ的 _______(列出计算式, 为以分压表示的平衡常数,分压=
总压×物质的量分数);
此时氧元素的回收率为_______[列出计算式,回收率 ]。
(4)萨巴蒂尔系统中不能先进行低温反应,再进行高温反应的原因是________________。龙岩市 2025 年高中毕业班三月教学质量检测
化学试题参考答案
一、选择题(每小题4分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 C B D C A B A D D B
二、非选择题(共60分)
11. (15分)
(1)CeO (2分)
2
(2)①BaO+H SO =BaSO +H O(2分)
2 4 4 2
②AC(2分)
(3)92%(2分)
(4)2Ce(OH) +NaClO+H O=2Ce(OH) +NaCl(2分)
3 2 4
(5)①8(1分)
②正四面体(2分)
③ (2分)
12. (15分)
(1)防止烧杯中水蒸气进入三口瓶(2分)
(2)C (1分) H++(CH ) NH=(CH ) NH +(2分)
3 2 3 2 2
(3)温度低于50℃,反应速率过慢;温度高于50℃,W可能发生分解(2分)
(4)B(2分)
(5)否 X、W均为非极性或极性很弱的分子,氨分子为强极性分子,它们之间难以互溶,不
会引起倒吸(2分)
(6)82.5%(2分)
(7)(1- )×100%(2分)
13. (15分)
(1)氯气,铁粉或FeCl (2分)
3
(2)酮羰基、酯基(2分)
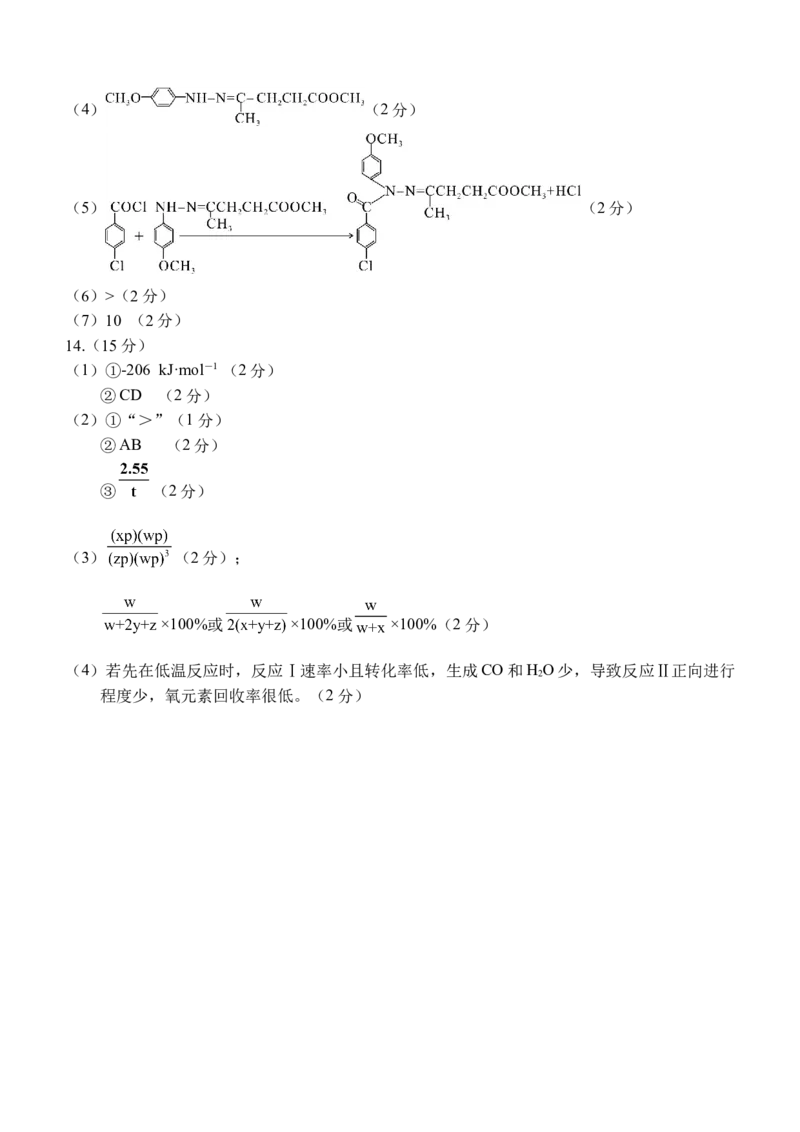
(3)sp3(1分) 三角锥形(2分)(4) (2分)
(5) (2分)
(6)>(2分)
(7)10 (2分)
14.(15分)
(1)①-206 kJ·mol-1 (2分)
②CD (2分)
(2)①“>”(1分)
②AB (2分)
③ (2分)
(3) (2分);
×100%或 ×100%或 ×100%(2分)
(4)若先在低温反应时,反应Ⅰ速率小且转化率低,生成CO和H O少,导致反应Ⅱ正向进行
2
程度少,氧元素回收率很低。(2分)