文档内容
吉林一中 23 级 2025~2026 学年度上学期第一次质量检测
化学学科
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Mg 24 Al 27 Cl 35.5
Ca 40 Cu 64
一、选择题(本题共 15 小题,每小题 3 分,共 45 分。每小题只有一个选项符合题意)。
1. 我国东北地区是古代文明发源地之一、下列文物主要由无机非金属材料制成的是
A. “宣和元宝”金币 B. 查海遗址龙形石堆塑
C. 赤柏松遗址铁器 D. 夫余鎏金铜面具
2. 家务劳动中蕴含着丰富的化学知识。下列相关解释错误的是
A. 用过氧乙酸溶液对居住环境消毒:CHCOOOH 具有较强氧化性
3
B. 做豆腐时,用石膏作凝固剂:CaSO·2H O 是硫酸盐结晶水合物
4 2
C. 制作腌菜、酱菜时添加食盐:高浓度的 NaCl 溶液迫使微生物脱水失活
D. 使用漂粉精洗衣服时添加醋酸:Ca(ClO) 和醋酸反应生成 HClO
2
3. 下列关于各实验装置的描述中,不恰当的是
A. 图 1 的实验可以证明过氧化钠与水反应放热
B. 图 2 中的溶液要提前驱除溶解的氧气,以制备
C. 图 3 的装置可以用于去除碳酸钠中的碳酸氢钠
D 用图 4 装置提纯 胶体
4. 物质的性质决定用途和保存方式,下列两者对应关系不正确的是
A. 见光易分解,浓硝酸用棕色瓶保存
B. 具有强氧化性,可用于杀菌消毒
第 1页/共 8页C. 具有还原性,可用于漂白纸浆
D. 难溶于稀盐酸,医学上常用作“钡餐”
5. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
选项 粒子组 判断和分析
A 透明溶液中:Mg2+、Cu2+、Br-、 不能大量共存,因为 Cu2+呈蓝色
能溶解 Al
2
O
3
的溶液中:Na+ 、 、Cl-、
B 能大量共存,粒子间不反应
C NaCl 溶液中:Fe3+、I-、Ba2+、CHCOO- 不能大量共存,Fe3+和 I- 会发生氧化还原反应
3
D NaHSO
4
溶液中:K+ 、Cl-、 、 不能大量共存, 和 发生反应
A. A B. B C. C D. D
6. 稀有气体化合物的合成更新了对“惰性”的认知。已知: ,
设 为阿伏加德罗常数的值。下列说法错误的是
A. 1 mol 中心原子的孤电子对数目为
B. 18 g 中所含质子数目为
C. 生成 1 mol ,转移电子数目为
D. 3.36 L HF(标准状况)所含的分子数为
7. 中国科学院天津工业生物技术研究所又出新成果,研发出了从二氧化碳、甲醇、甲醛等碳一化合物到淀
粉(C H O) 和已糖的合成方法,实现了较高转化效率与精准可控构型的己糖人工合成。下列说法正确的是
6 10 5 n
A. 淀粉的摩尔质量为 162n
B. 1L1mol·L-1 的甲醇水溶液中含有 1molH+
C. 50g 质量分数为 64%的甲醇水溶液中含有 3molO-H 键
D. 一定条件下,4.4gCO 全部转化为甲醇( )时,转移 0.2mol 电子
2
8. 下列离子方程式中,正确的是
第 2页/共 8页A. 溶于水中:
B. 向 、 混合溶液中滴加醋酸:
C. 将 溶液滴入 溶液中:
D. 向漂白粉溶液中通入少量 :
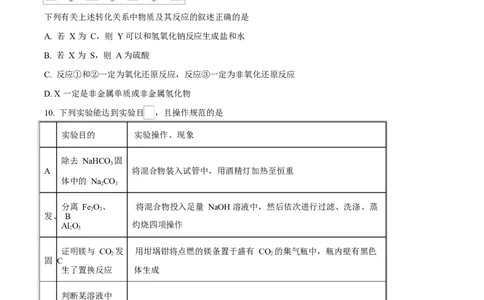
9. 已知某物质 X 能发生如图转化:
下列有关上述转化关系中物质及其反应的叙述正确的是
A. 若 X 为 C,则 Y 可以和氢氧化钠反应生成盐和水
B. 若 X 为 S,则 A 为硫酸
C. 反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
D. X 一定是非金属单质或非金属氢化物
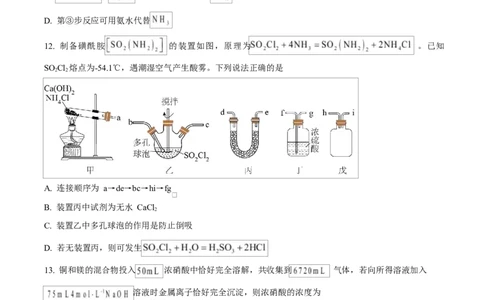
10. 下列实验能达到实验目 ,且操作规范的是
实验目的 实验操作、现象
除去 NaHCO 固
3
A 将混合物装入试管中,用酒精灯加热至恒重
体中的 NaCO
2 3
分离 Fe O、 将混合物投入足量 NaOH 溶液中,然后依次进行过滤、洗涤、蒸
2 3
发、 B
Al O 灼烧四项操作
2 3
证明镁与 CO 发 用坩埚钳将点燃的镁条置于盛有 CO 的集气瓶中,瓶内壁有黑色
2 2
固 C
生了置换反应 体生成
判断某溶液中
D 有 Na+ ,并且没 用洁净的铂丝蘸取溶液在酒精灯的外焰上灼烧,观察到火焰呈黄色
有 K+
A. A B. B C. C D. D
11. 氮化硅( )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工
艺流程如图所示,下列说法正确的是
第 3页/共 8页已知: 在潮湿的空气中易水解,产生白雾。
A. 该流程中可循环使用的物质是
B. 第①步反应中产生的气体能使澄清石灰水变浑浊
C. 和 所含共价键数目均为
D. 第③步反应可用氨水代替
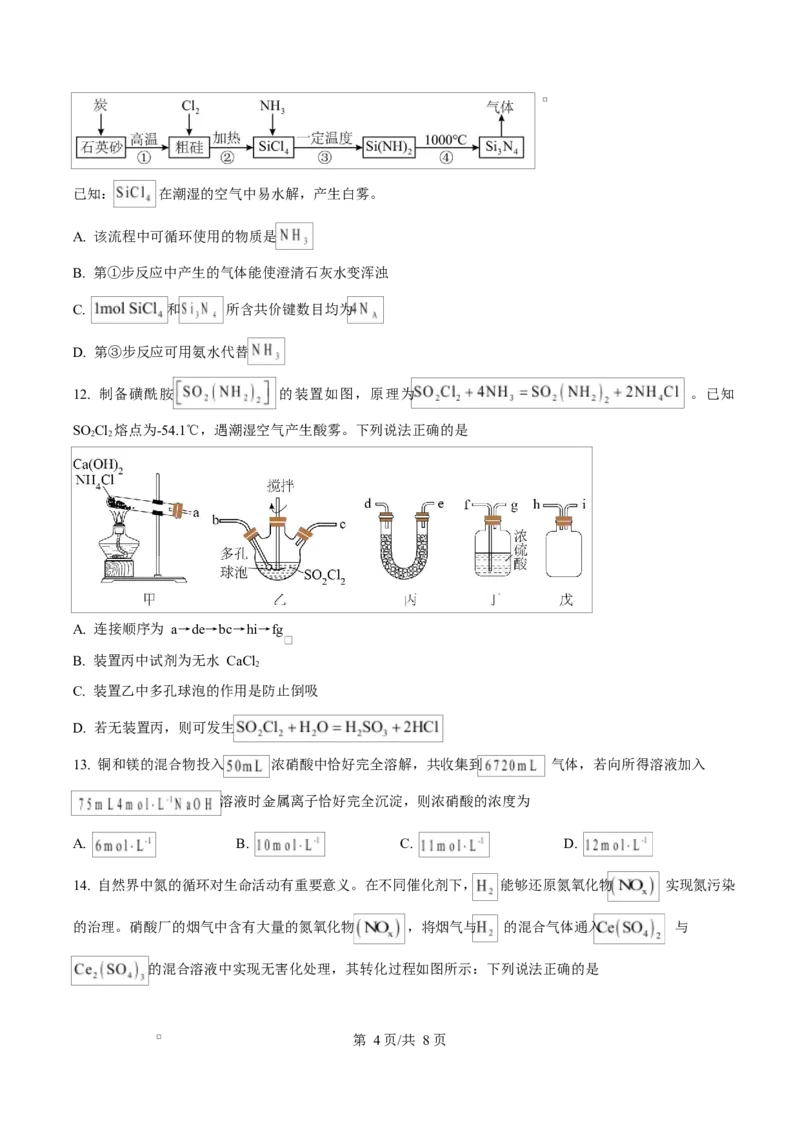
12. 制备磺酰胺 的装置如图,原理为 。已知
SO Cl 熔点为-54.1℃,遇潮湿空气产生酸雾。下列说法正确的是
2 2
A. 连接顺序为 a→de→bc→hi→fg
B. 装置丙中试剂为无水 CaCl
2
C. 装置乙中多孔球泡的作用是防止倒吸
D. 若无装置丙,则可发生
13. 铜和镁的混合物投入 浓硝酸中恰好完全溶解,共收集到 气体,若向所得溶液加入
溶液时金属离子恰好完全沉淀,则浓硝酸的浓度为
A. B. C. D.
14. 自然界中氮的循环对生命活动有重要意义。在不同催化剂下, 能够还原氮氧化物 实现氮污染
的治理。硝酸厂的烟气中含有大量的氮氧化物 ,将烟气与 的混合气体通入 与
的混合溶液中实现无害化处理,其转化过程如图所示:下列说法正确的是
第 4页/共 8页A. 该处理过程中,起催化作用的离子是
B. 若该过程中,每转移 电子消耗 氮氧化物 ,则 x 为 1.5
C. 当 时,反应Ⅱ中还原产物与氧化产物物质 量之比为
D. 当无害化处理标况下 时,使用等量的 可以无害化处理 (不考虑 和 的
转化)
15. 某工业废水中可能含有 、 、 、 、 、 、 、 、 、 中的几种,
且各离子物质的量浓度均为 0.2 mol/L(忽略水的电离及离子的水解),欲探究废水的组成,进行了如下实验:
Ⅰ、取该无色溶液 5 mL,滴加一滴氨水有沉淀生成,且离子种类增加
Ⅱ、用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰
Ⅲ、另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV、向Ⅲ中所得溶液中加入 溶液,有白色沉淀生成。
下列推断不正确的是
A. 溶液中一定不含的阳离子是 、 、 、
B. 该工业废水中一定含有的离子为 、 、 、 、
C. Ⅲ中加入盐酸生成无色气体的离子方程式为
D. 另取 100 mL 原溶液,加入足量的 NaOH 溶液,充分反应后过滤、洗涤、灼烧沉淀至恒重,得到固体的
质量为 0.8 g
二、非选择题(本题共 4 小题,共 55 分)
16. 化学工业为医药行业提供了强有力的物质支撑。请回答下列问题:
(1)研究表明病毒可通过气溶胶传播,气溶胶中粒子 直径大小为___________,可以___________来鉴别
气溶胶。
(2)常温下,NaO、乙醇、Cl、NaClO 溶液都为常用的消毒剂,其中能导电的是___________,属于电解
2 2 2
第 5页/共 8页质的是___________。
(3)某家用制氧机使用的是过碳酸钠(2Na CO·3H O),该药品被称为固体双氧水,兼具碳酸钠和双氧水的
2 3 2 2
双重性质,可以利用过氧化氢在二氧化锰的催化下分解产生氧气。
①写出过碳酸钠在二氧化锰催化下产生氧气的化学方程式:___________。
②下列物质不会使过碳酸钠失效的是___________(填字母)。
A.HCl B.NaHCO C.MnO D.HS
3 2 2
(4)医药行业中测温枪发挥了极大的作用。在测温枪电池制备过程中会生成 LiTi O (Ti 为+4 价),1 mol
2 5 15
LiTi O 中过氧键的数目为___________。
2 5 15
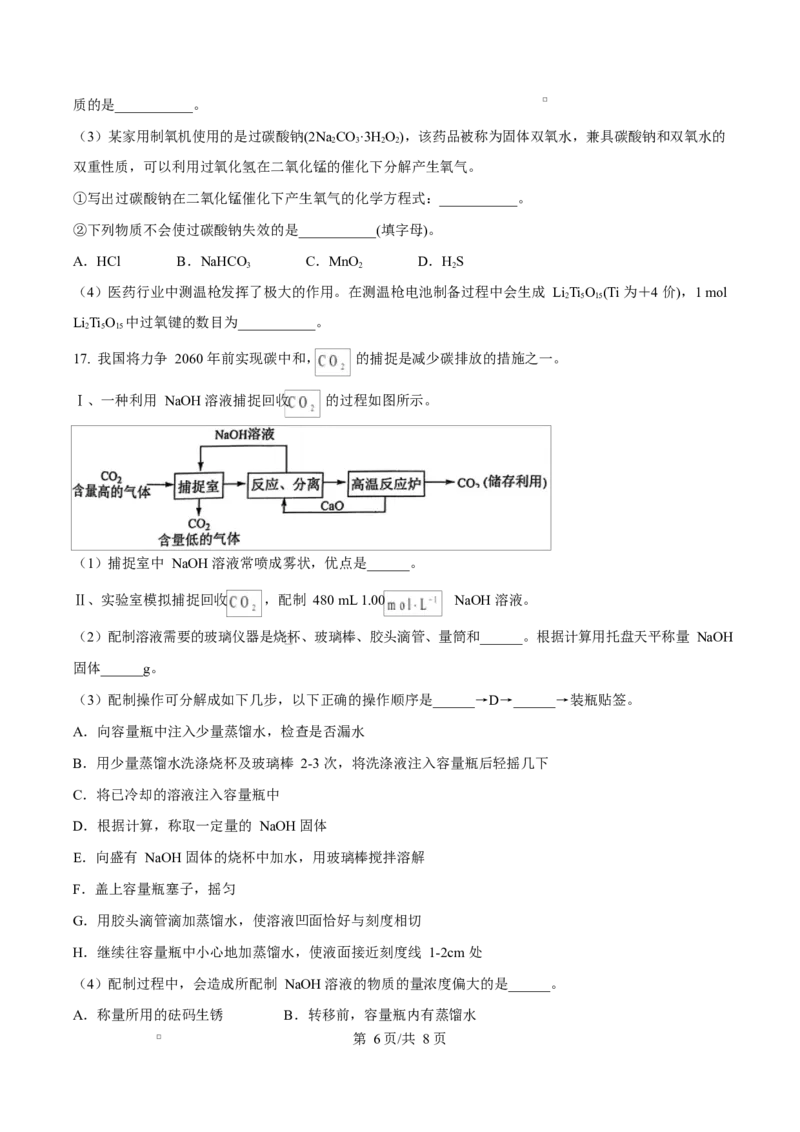
17. 我国将力争 2060 年前实现碳中和, 的捕捉是减少碳排放的措施之一。
Ⅰ、一种利用 NaOH 溶液捕捉回收 的过程如图所示。
(1)捕捉室中 NaOH 溶液常喷成雾状,优点是______。
Ⅱ、实验室模拟捕捉回收 ,配制 480 mL 1.00 NaOH 溶液。
(2)配制溶液需要的玻璃仪器是烧杯、玻璃棒、胶头滴管、量筒和______。根据计算用托盘天平称量 NaOH
固体______g。
(3)配制操作可分解成如下几步,以下正确的操作顺序是______→D→______→装瓶贴签。
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒 2-3 次,将洗涤液注入容量瓶后轻摇几下
C.将已冷却的溶液注入容量瓶中
D.根据计算,称取一定量的 NaOH 固体
E.向盛有 NaOH 固体的烧杯中加水,用玻璃棒搅拌溶解
F.盖上容量瓶塞子,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线 1-2cm 处
(4)配制过程中,会造成所配制 NaOH 溶液的物质的量浓度偏大的是______。
A.称量所用的砝码生锈 B.转移前,容量瓶内有蒸馏水
第 6页/共 8页C.未冷至室温就转移定容 D.定容时仰视刻度线
E.定容时水加多用胶头滴管吸出 F.称量 NaOH 时间过长
Ⅲ、CaO 固体也可以捕捉回收 ,研究表明 热分解制得的 CaO 疏松多孔,具有良好的
捕捉性能。取 1.46 g 进行加热,固体质量随温度变化如图所示:
(注:曲线中共涉及到三步分解反应)。
(5)写出 400-600℃范围内分解反应的化学方程式:______。
(6)据图分析,CaO 捕捉 的反应温度应______(填“高于”或“低于”)800℃。
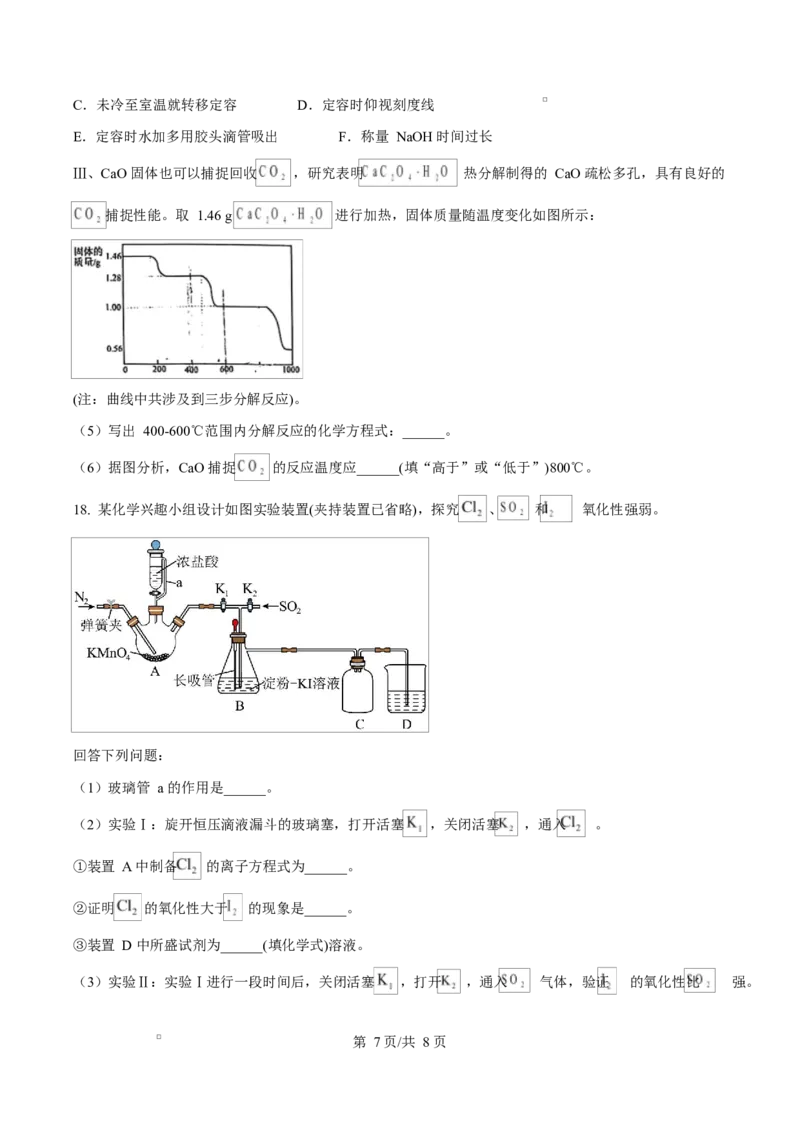
18. 某化学兴趣小组设计如图实验装置(夹持装置已省略),探究 、 和 氧化性强弱。
回答下列问题:
(1)玻璃管 a 的作用是______。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞 ,关闭活塞 ,通入 。
①装置 A 中制备 的离子方程式为______。
②证明 的氧化性大于 的现象是______。
③装置 D 中所盛试剂为______(填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞 ,打开 ,通入 气体,验证 的氧化性比 强。
第 7页/共 8页① 发生反应的化学方程式为______。
②实验完成后,打开弹簧夹,持续通入 的目的是______。
(4)淀粉-KI 溶液中 的测定:取 10.00 mL 淀粉-KI 溶液,加入足量的硫酸酸化的 溶液,然后加
入少量的 粉末除去 ,然后用 0.1000 的 标准溶液滴定,达到滴定终点时三次
测量平均消耗 标准溶液的体积为 25.00 mL( ,
)。
①滴定终点现象是______。
② ______ 。
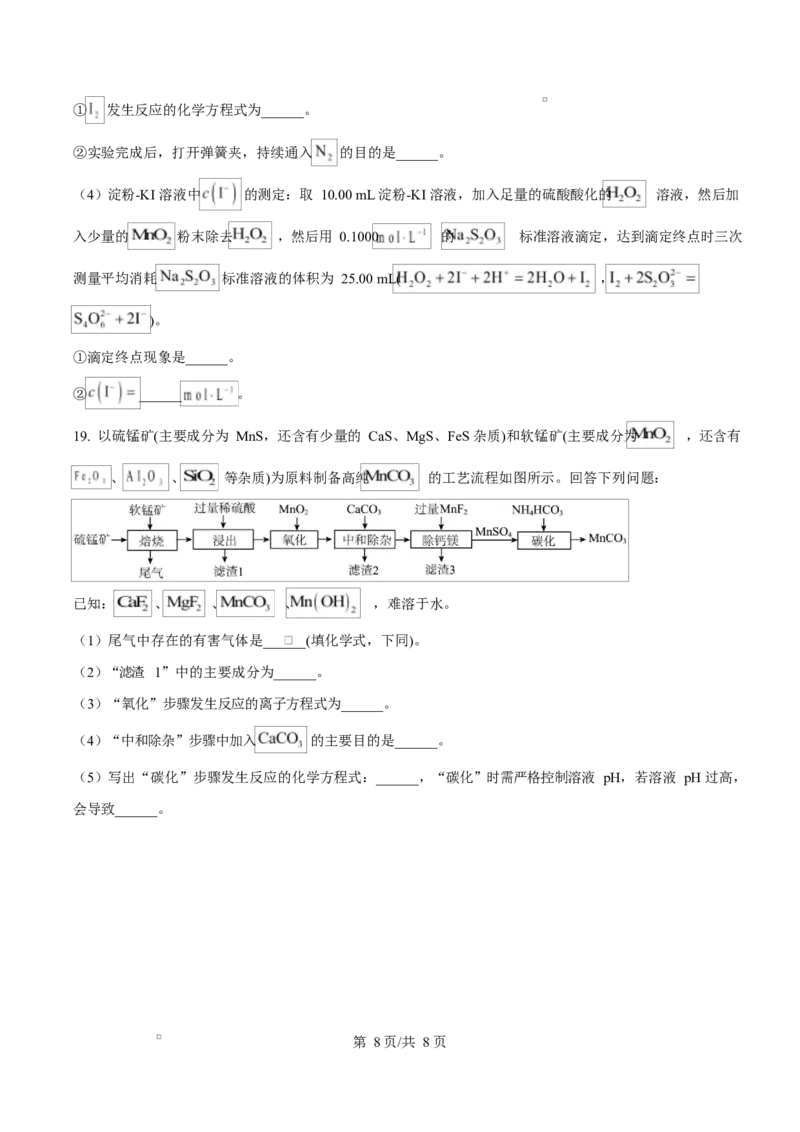
19. 以硫锰矿(主要成分为 MnS,还含有少量的 CaS、MgS、FeS 杂质)和软锰矿(主要成分为 ,还含有
、 、 等杂质)为原料制备高纯 的工艺流程如图所示。回答下列问题:
已知: 、 、 、 ,难溶于水。
(1)尾气中存在的有害气体是______(填化学式,下同)。
(2)“滤渣 1”中的主要成分为______。
(3)“氧化”步骤发生反应的离子方程式为______。
(4)“中和除杂”步骤中加入 的主要目的是______。
(5)写出“碳化”步骤发生反应的化学方程式:______,“碳化”时需严格控制溶液 pH,若溶液 pH 过高,
会导致______。
第 8页/共 8页