文档内容
年高考模拟考试
2025
化学试题
2025.04
注意事项:
答卷前 考生务必将自己的姓名 考生号等填写在答题卡和试卷指定位置
1. , 、 。
回答选择题时 选出每小题答案后 用铅笔把答题卡上对应题目的答案标号涂黑 如需
2. , , 。
改动 用橡皮擦干净后 再选涂其他答案标号 回答非选择题时 将答案写在答题卡上 写在本
, , 。 , ,
试卷上无效
。
可能用到的相对原子质量
:H1 C12 N14 O16 Na23 S32 Cl35.5 Fe56 Cu64
一、选择题:本题共 小题,每小题 分,共 分。每小题只有一个选项符合题目要求。
10 2 20
中华传统文化博大精深 蕴含着丰富的化学知识 下列说法错误的是
1. , 。
易经 记载的 泽中有火 上火下泽 涉及烃类的燃烧
A.《 》 “ ”“ ”
成语 刀耕火耨 是指伐去树木烧掉野草 余灰可降低土壤碱性
B. “ ” ,
北宋汝窑瓷器是以黏土为主要原料 经高温烧结而成
C. ,
榆荚只能随柳絮 等闲撩乱走空园 其中的柳絮富含糖类
D.“ , ”,
物质性质决定用途 下列对应关系正确的是
2. ,
氮气具有稳定性 可用于冷冻麻醉
A. ,
溶解度小 可用于制作豆腐
B.CaSO4 ,
聚乳酸易降解 可用作手术缝合线
C. ,
硅酸钠耐热性好 其水溶液可用作黏合剂
D. ,
下列化学用语或图示正确的是
3.
中的 键为 键
3 2
A.CH3COOH C-C :sp-spσ
的名称 二乙酸乙二酯
B. :
一元酸次磷酸 的结构简式为
C. (H3PO2) :
的 模型为
D.H2O VSEPR :
下列属于非极性分子的是
4.
A.O3 B.SeO3 C.Cl2O D.CH2F2
下列实验操作或处理方法错误的是
5.
通过 溶液可除去 中的 杂质
A. CuSO4 C2H2 H2S
用浓氨水溶解试管内壁上的氯化银固体
B.
实验室取用少量白磷时 可在水中用小刀进行切割
C. ,
用过滤法分离苯和三溴苯酚的混合物
D.
化学试题 第 页 共 页
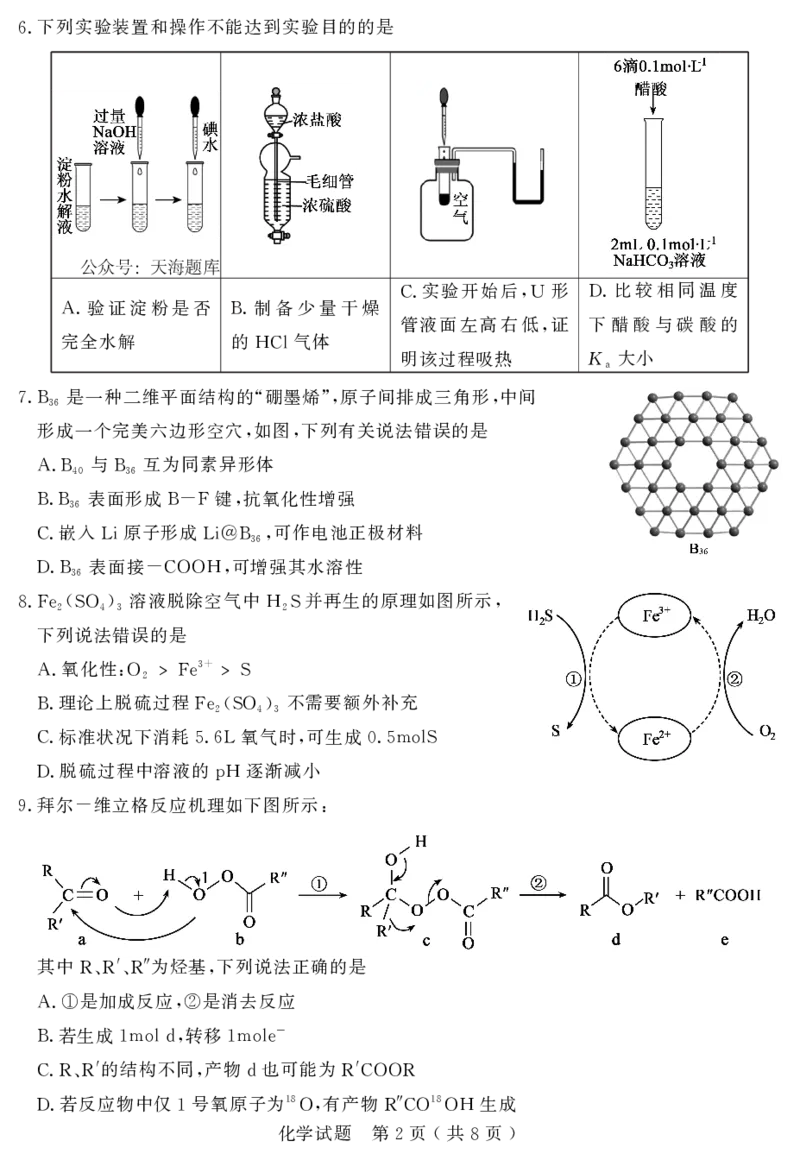
1 ( 8 )下列实验装置和操作不能达到实验目的的是
6.
公众号:天海题库
实验开始后 形 比较相同温度
验证淀粉是否 制备少量干燥 C. ,U D.
A. B. 管液面左高右低 证 下醋酸与碳酸的
完全水解 的 气体 ,
HCl 明该过程吸热 K 大小
a
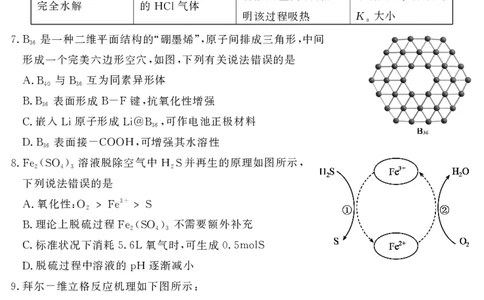
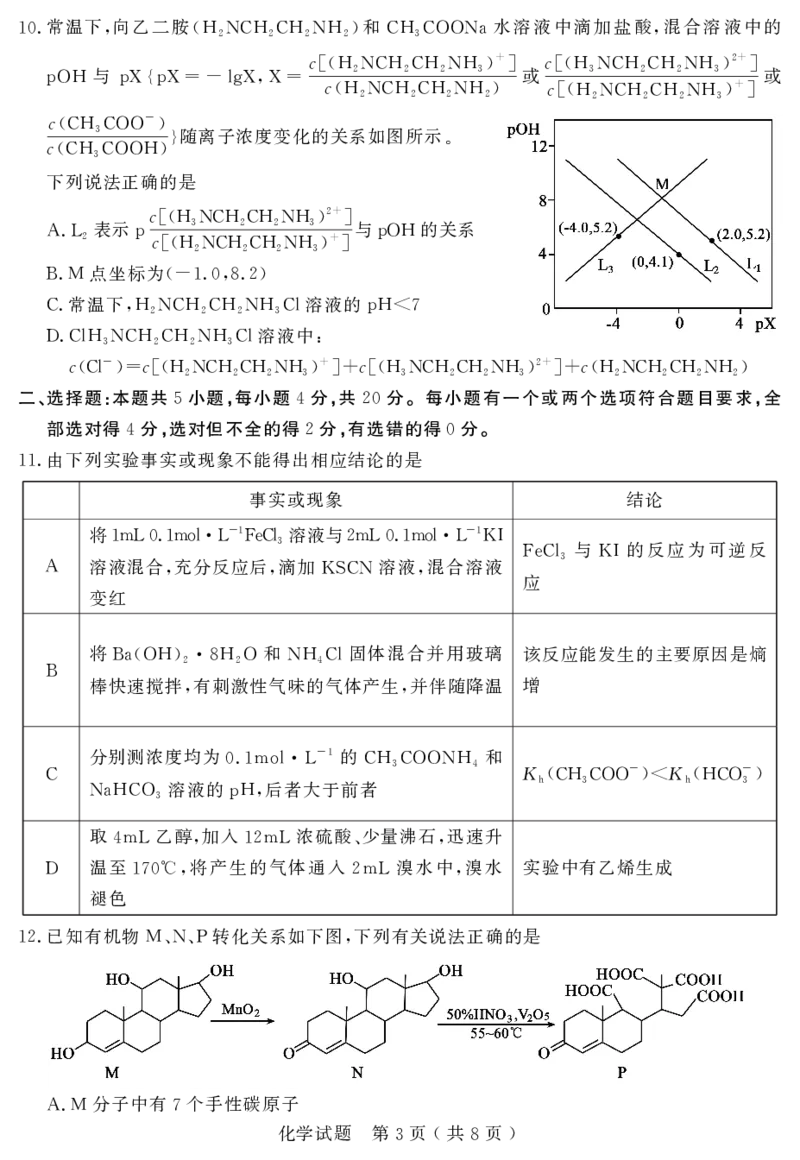
是一种二维平面结构的 硼墨烯 原子间排成三角形 中间
7.B36 “ ”, ,
形成一个完美六边形空穴 如图 下列有关说法错误的是
, ,
与 互为同素异形体
A.B40 B36
表面形成 键 抗氧化性增强
B.B36 B-F ,
嵌入 原子形成 可作电池正极材料
C. Li Li@B36,
表面接 可增强其水溶性
D.B36 -COOH,
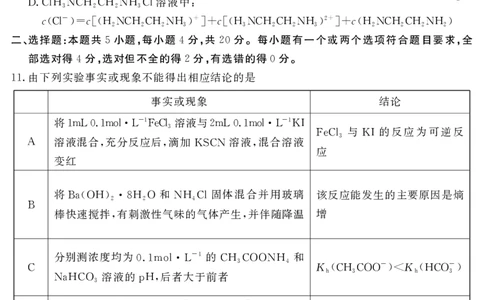
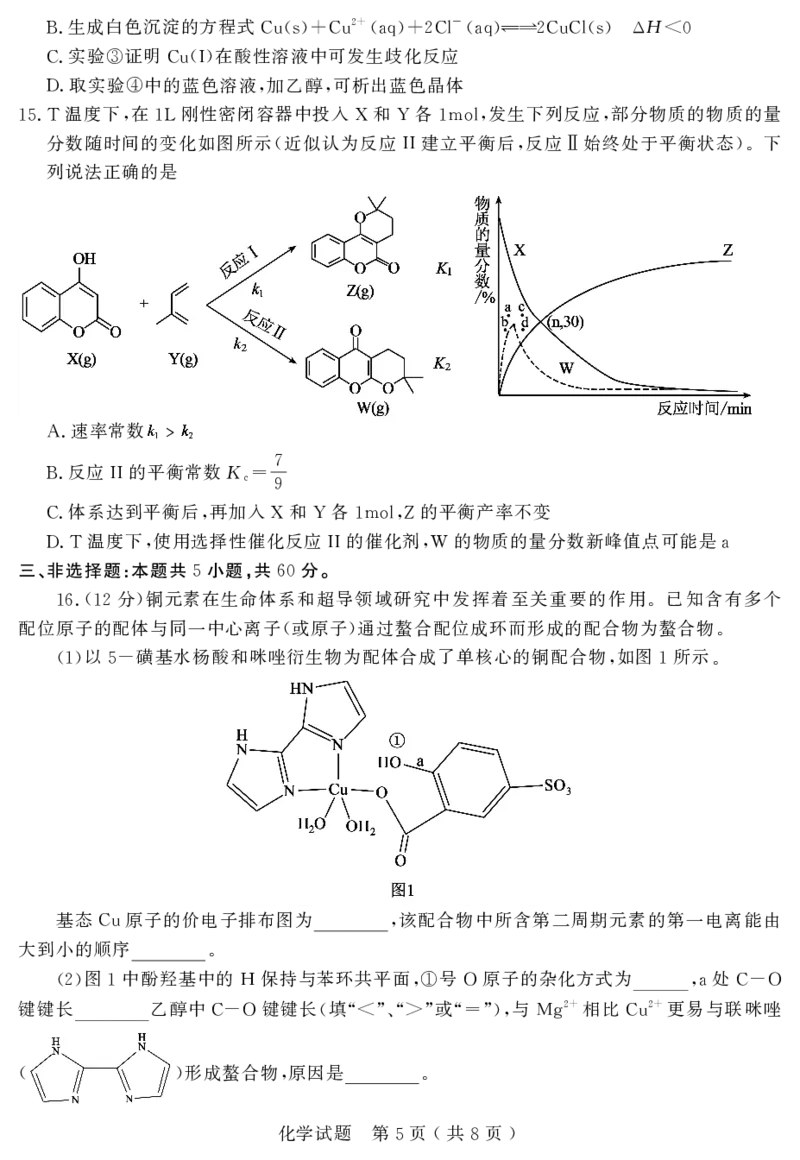
溶液脱除空气中 并再生的原理如图所示
8.Fe2(SO4)3 H2S ,
下列说法错误的是
氧化性 ﹥ ﹥
3+
A. :O2 Fe S
理论上脱硫过程 不需要额外补充
B. Fe2(SO4)3
标准状况下消耗 氧气时 可生成
C. 5.6L , 0.5molS
脱硫过程中溶液的 逐渐减小
D. pH
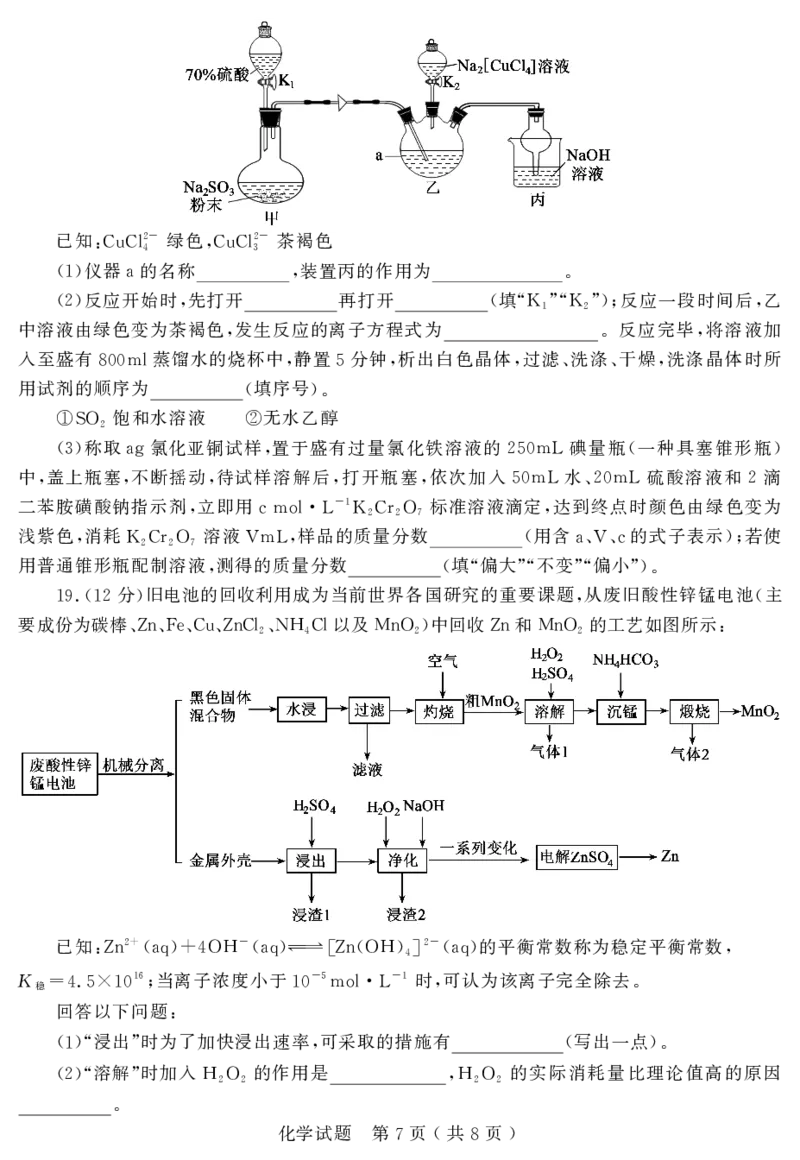
拜尔 维立格反应机理如下图所示
9. - :
其中 为烃基 下列说法正确的是
R、R'、R″ ,
是加成反应 是消去反应
A.① ,②
若生成 转移
-
B. 1mold, 1mole
的结构不同 产物 也可能为
C.R、R' , d R'COOR
若反应物中仅 号氧原子为 有产物 生成
18 18
D. 1 O, R″CO OH
化学试题 第 页 共 页
2 ( 8 )常温下 向乙二胺 和 水溶液中滴加盐酸 混合溶液中的
10. , (H2NCH2CH2NH2) CH3COONa ,
c + c 2+
与 [(H2NCH2CH2NH3)]或 [(H3NCH2CH2NH3) ]或
pOH pX{pX=-lgX,X= c (H2NCH2CH2NH2) c [(H2NCH2CH2NH3) + ]
c -
(CH3COO )随离子浓度变化的关系如图所示
c } 。
(CH3COOH)
下列说法正确的是
c 2+
表示 [(H3NCH2CH2NH3) ]与 的关系
A.L2 pc + pOH
[(H2NCH2CH2NH3)]
点坐标为
B.M (-1.0,8.2)
常温下 溶液的
C. ,H2NCH2CH2NH3Cl pH<7
溶液中
D.ClH3NCH2CH2NH3Cl :
c - c + c 2+ c
(Cl )= [(H2NCH2CH2NH3)]+ [(H3NCH2CH2NH3) ]+ (H2NCH2CH2NH2)
二、选择题:本题共 小题,每小题 分,共 分。每小题有一个或两个选项符合题目要求,全
5 4 20
部选对得 分,选对但不全的得 分,有选错的得 分。
4 2 0
由下列实验事实或现象不能得出相应结论的是
11.
事实或现象 结论
将 溶液与
-1 -1
1mL0.1mol·L FeCl3 2mL0.1mol·L KI 与 的反应为可逆反
溶液混合 充分反应后 滴加 溶液 混合溶液 FeCl3 KI
A , , KSCN , 应
变红
将 和 固体混合并用玻璃 该反应能发生的主要原因是熵
Ba(OH)2·8H2O NH4Cl
B 棒快速搅拌 有刺激性气味的气体产生 并伴随降温 增
, ,
分别测浓度均为 的 和
-1
0.1mol·L CH3COONH4 K - K -
C 溶液的 后者大于前者 h(CH3COO )< h(HCO3)
NaHCO3 pH,
取 乙醇 加入 浓硫酸 少量沸石 迅速升
4mL , 12mL 、 ,
温至 将产生的气体通入 溴水中 溴水 实验中有乙烯生成
D 170℃, 2mL ,
褪色
已知有机物 转化关系如下图 下列有关说法正确的是
12. M、N、P ,
分子中有 个手性碳原子
A.M 7
化学试题 第 页 共 页
3 ( 8 )分子在一定条件下能发生加聚和缩聚反应
B.N
的消去产物有四种
C.N
由上述机理可知
D. :
金属 对全钒液流电池负极有催化作用 放电时负极反应分两步进行 其中一步为
13. Bi , ,
电池工作原理如图所示
2+ + 3+
xV +xH +Bi=BiHx+xV , 。
下列有关说法正确的是
放电时另一步负极电极反应式
- +
A. :BiHx-xe =xH +Bi
充电时 极的电极电势大于 极
B. a b
放电过程中转移 正极区 减少
- +
C. 1mole , H 1mol
充电时 极区 的物质的量增大
D. ,b H2O
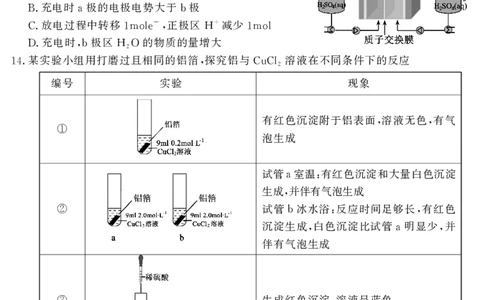
某实验小组用打磨过且相同的铝箔 探究铝与 溶液在不同条件下的反应
14. , CuCl2
编号 实验 现象
有红色沉淀附于铝表面 溶液无色 有气
, ,
① 泡生成
试管 室温 有红色沉淀和大量白色沉淀
a :
生成 并伴有气泡生成
,
试管 冰水浴 反应时间足够长 有红色
② b : ,
沉淀生成 白色沉淀比试管 明显少 并
, a ,
伴有气泡生成
生成红色沉淀 溶液呈蓝色
③ ,
形成无色溶液 置于空气中溶液呈蓝色
④ ,
下列说法错误的是
无色气体为 红色沉淀为
A. H2, Cu
化学试题 第 页 共 页
4 ( 8 )生成白色沉淀的方程式 2+ - H
B. Cu(s)+Cu (aq)+2Cl (aq)2CuCl(s) Δ <0
实验 证明 在酸性溶液中可发生歧化反应
C. ③ Cu(I)
取实验 中的蓝色溶液 加乙醇 可析出蓝色晶体
D. ④ , ,
温度下 在 刚性密闭容器中投入 和 各 发生下列反应 部分物质的物质的量
15.T , 1L X Y 1mol, ,
分数随时间的变化如图所示 近似认为反应 建立平衡后 反应 始终处于平衡状态 下
( II , Ⅱ )。
列说法正确的是
速率常数 ﹥
A.
反应 的平衡常数K 7
B. II c=
9
体系达到平衡后 再加入 和 各 的平衡产率不变
C. , X Y 1mol,Z
温度下 使用选择性催化反应 的催化剂 的物质的量分数新峰值点可能是
D.T , II ,W a
三、非选择题:本题共 小题,共 分。
5 60
分 铜元素在生命体系和超导领域研究中发挥着至关重要的作用 已知含有多个
16.(12 ) 。
配位原子的配体与同一中心离子 或原子 通过螯合配位成环而形成的配合物为螯合物
( ) 。
以 磺基水杨酸和咪唑衍生物为配体合成了单核心的铜配合物 如图 所示
(1) 5- , 1 。
基态 原子的价电子排布图为 该配合物中所含第二周期元素的第一电离能由
Cu ,
大到小的顺序
。
图 中酚羟基中的 保持与苯环共平面 号 原子的杂化方式为 处
(2) 1 H ,① O ,a C-O
键键长 乙醇中 键键长 填 或 与 相比 更易与联咪唑
2+ 2+
C-O ( “<”、“>” “=”), Mg Cu
形成螯合物 原因是
( ) , 。
化学试题 第 页 共 页
5 ( 8 )某含铜 化合物晶体结构如图 所示 该化合物的化学式为 如图 所
(3) (II) 2 。 ; 3
示的含氧空位的晶胞结构中 化合价不变n 2+ n +
,La ,(Cu )∶ (Cu )= 。
分 是制备那韦类抗 药物的关键中间体 其合成路线如下
17.(12 )G HIV , :
已知 为 的简写
:-Boc
中所含官能团的名称为 的化学名称为
(1)A ,① 。
的结构简式为
(2)C 。
的反应类型是
(3)N→E 。
的化学方程式为
(4)A→M 。
写出符合下列条件的 的同分异构体的结构简式 写出一种即可
(5) G : ( )。
含苯环 且能发生银镜反应 分子中含有 种不同化学环境的氢
① , ;② 3 。
写出以 为主要原料制备 的合成路线流程图 无机试
(6) (
剂和流程中的有机试剂任选
) 。
分 氯化亚铜为白色晶体 在空气中易被氧化 微溶于水 不溶于醇 实验室制备氯
18.(12 ) , , , 。
化亚铜的部分实验装置如图所示 夹持装置略
( )。
化学试题 第 页 共 页
6 ( 8 )已知 绿色 茶褐色
2- 2-
:CuCl4 ,CuCl3
仪器 的名称 装置丙的作用为
(1) a , 。
反应开始时 先打开 再打开 填 反应一段时间后 乙
(2) , ( “K1”“K2”); ,
中溶液由绿色变为茶褐色 发生反应的离子方程式为 反应完毕 将溶液加
, 。 ,
入至盛有 蒸馏水的烧杯中 静置 分钟 析出白色晶体 过滤 洗涤 干燥 洗涤晶体时所
800ml , 5 , , 、 、 ,
用试剂的顺序为 填序号
( )。
饱和水溶液 无水乙醇
①SO2 ②
称取 氯化亚铜试样 置于盛有过量氯化铁溶液的 碘量瓶 一种具塞锥形瓶
(3) ag , 250mL ( )
中 盖上瓶塞 不断摇动 待试样溶解后 打开瓶塞 依次加入 水 硫酸溶液和 滴
, , , , , 50mL 、20mL 2
二苯胺磺酸钠指示剂 立即用 标准溶液滴定 达到终点时颜色由绿色变为
-1
, cmol·L K2Cr2O7 ,
浅紫色 消耗 溶液 样品的质量分数 用含 的式子表示 若使
, K2Cr2O7 VmL, ( a、V、c );
用普通锥形瓶配制溶液 测得的质量分数 填 偏大 不变 偏小
, ( “ ”“ ”“ ”)。
分 旧电池的回收利用成为当前世界各国研究的重要课题 从废旧酸性锌锰电池 主
19.(12 ) , (
要成份为碳棒 以及 中回收 和 的工艺如图所示
、Zn、Fe、Cu、ZnCl2、NH4Cl MnO2) Zn MnO2 :
已知 的平衡常数称为稳定平衡常数
2+ - 2-
:Zn (aq)+4OH (aq) Zn(OH)4 (aq) ,
K稳
=4.5×10
16
;
当离子浓度小于
10
-5
mol·L
-1 时
,
可认为该离子完全除去
。
回答以下问题
:
浸出 时为了加快浸出速率 可采取的措施有 写出一点
(1)“ ” , ( )。
溶解 时加入 的作用是 的实际消耗量比理论值高的原因
(2)“ ” H2O2 ,H2O2
。
化学试题 第 页 共 页
7 ( 8 )沉锰 时 发生反应的离子方程式为 煅烧 时参加反应的气体与生成气体
(3)“ ” , ,“ ”
的物质的量之比为
。
已知 浸出 液中 的浓度均为 净化 时 需调节溶液 的合
2+ 2+ -1
(4) “ ” Fe 、Zn 0.1mol·L ,“ ” , pH
理范围是
。
化合物
Zn(OH)2 Fe(OH)2 Fe(OH)3
K 近似值 -17 -17 -38
sp 10 10 10
为两性氢氧化物 可与 溶液发生反应
-
Zn(OH)2 , NaOH Zn(OH)2(s)+2OH (aq)
2-
其平衡常数K
Zn(OH)4 (aq), = 。
分 利用 硝基苯乙烯 制备 乙基苯胺 涉及反应如下
20.(12 ) 3- (NS) 3- (EA), :
ΔH ΔS
已知 K 1 为常数 在温度变化范围不大时 同一反应的ΔHΔS为常数
:ln =- · + (R , , 、 )
R T R
反应 的焓变 H 用含 H H H 的代数式表示 反应 的平
(1) ④ Δ 4= ( Δ 1、Δ 2、Δ 3 ), ①
衡常数K 用含K K K 的代数式表示
1= ( 2、 3、 4 )。
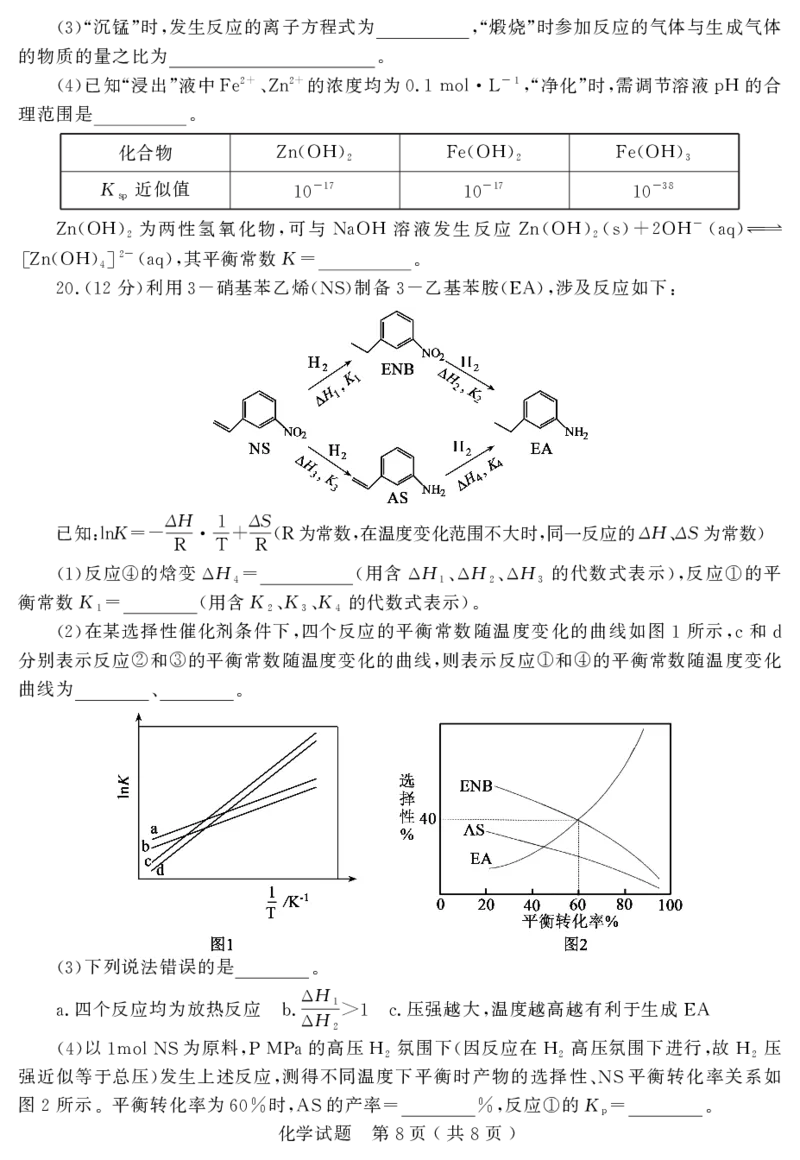
在某选择性催化剂条件下 四个反应的平衡常数随温度变化的曲线如图 所示 和
(2) , 1 ,c d
分别表示反应 和 的平衡常数随温度变化的曲线 则表示反应 和 的平衡常数随温度变化
② ③ , ① ④
曲线为
、 。
下列说法错误的是
(3) 。
H
四个反应均为放热反应 Δ 1 压强越大 温度越高越有利于生成
a. b.H >1 c. , EA
Δ 2
以 为原料 的高压 氛围下 因反应在 高压氛围下进行 故 压
(4) 1molNS ,PMPa H2 ( H2 , H2
强近似等于总压 发生上述反应 测得不同温度下平衡时产物的选择性 平衡转化率关系如
) , 、NS
图 所示 平衡转化率为 时 的产率 反应 的K
2 。 60% ,AS = %, ① p= 。
化学试题 第 页 共 页
8 ( 8 )