文档内容
秘密 启用前
★
年高考考前适应性测试(冲刺卷)
2025
化学参考答案详解及评分说明
评分说明:
考生如按其他方法或步骤解答,正确的,同样给分;有错的,根据错误的性质,参照评分参考中相应的规定评分。
一、选择题:本题共 小题,每小题 分,共 分。
14 3 42
1.C
【解析】硫化汞常温下不容易被空气中的氧气氧化,所以雕塑彩绘历经千年仍然色彩艳丽,选项错误。
C
2.D
【解析】 、、 的第一电离能由大到小的顺序为 , 选项错误。氨分子的 模型是四面体结构,
C N O N>O>C A VSEPR B
选项错误。干冰晶体和冰晶体的晶胞结构不相同, 选项错误。由洪特规则可知,基态原子中,填入简并轨道
C
时,电子总是尽可能分占不同的轨道且自旋平行, 选项中核外电子轨道表示式违背了洪特规则, 选项正确。
D D
3.C
【解析】若不慎将苯酚沾到皮肤上,应立即用乙醇冲洗,再用水清洗,选项错误。
C
4.D
【解析】标准状况下, ( ) 与 ( ) 恰好发生反应 ==== ,生成 ,但是
22.4L 1mol NO 11.2L 0.5mol O2 2NO+O2 2NO2 1molNO2
容器中存在反应: ,所以容器内气体分子数小于N , 选项错误。 的物质的量为
2NO2 N2O4 A A 32 g S8
32g 1 ,所含共价键数目为N ,同理, 所含共价键数目为N ,所以 ( )与
= mol A 32 g S6 A 32 g S8 S6
8 × 32g/mol 8
( )的混合物中所含共价键数为N ,选项错误。标准状况下, 的物质的量为 ,通入水
A B 11.2LCl2 0.5mol
中后只有一部分 与水反应生成 、 和 ,所以溶液中氯离子数小于 N ,选项错误。
+ -
Cl2 H Cl HClO 0.5 A C
5.A
【解析】明矾净水的原因是铝离子水解生成的氢氧化铝胶体吸附水中的杂质,达到净水的目的,明矾不能杀菌消
毒, 选项错误。
A
6.D
【解析】本题考查离子共存。 具有强氧化性,能与 及 、 发生氧化还原反应,故不能大量共存,
2+ + −
KMnO4 Fe H Cl A
选项不符合题意。 与 生成 沉淀,故不能大量共存, 选项不符合题意。氨水显碱性,会与 反应,不
+ − 2+
Ag I AgI B Cu
能大量共存,选项不符合题意。
C
7.D
【解析】图 为镀件镀铜时,应将铜片作为阳极,镀件作为阴极, 选项不能达到实验目的。装置为敞口体系,热量
1 A
损失严重,且 溶液应一次性全部倒入 溶液中,不能用胶头滴管滴加,故不能用该装置测定中和反应
H2SO4 NaOH
的反应热,选项不能达到实验目的。 () () ()为气体分子数不变的反应,缩小容器容积,平衡
B H2 g +I2 g 2HI g
不移动,气体颜色加深是因为缩小容器容积,的浓度增大,选项不能达到实验目的。
I2 C
8.A
【解析】 的溶解度小于 的溶解度,是因为 晶体结构中的 之间能形成氢键,不利于
-
NaHCO3 Na2CO3 NaHCO3 HCO3
与水分子之间形成氢键,而 能与水分子之间形成氢键,故 在水中的溶解度小于 在水中
- 2-
HCO3 CO3 NaHCO3 Na2CO3
的溶解度, 选项错误。
A
化学试题答案 第 页(共 页)
1 49.C
【解析】 是硫的氢化物, 的化学式是 ,可以用启普发生器制备, 选项正确。 在自然界以游离态和化合态
A A H2S A S
的形式存在,选项正确。 是硫元素的最高价含氧酸盐,即硫酸盐,检验 中阴离子的实验操作及现象是取少
B H H
量 溶于水,先滴加稀盐酸,没有明显现象,再滴加 溶液,若有白色沉淀产生,则可推断 中含有 ,选
2-
H BaCl2 H SO4 C
项错误。食品中加入适量 可起到漂白、防腐、抗氧化的作用, 选项正确。
SO2 D
10.D
【解析】 有 种不同的氢,故核磁共振氢谱有 组峰, 选项错误。 中所有原子不一定处于同一平面,中所有
X 8 8 A X Z
原子不处于同一平面,选项错误。相同物质的量的 、、与 反应,消耗 的物质的量不相同,选
B X Y Z NaOH NaOH C
项错误。 为内酯,在水中溶解度较小, 选项正确。
Y D
11.A
【解析】根据题中信息,短周期元素 、、、、的原子序数依次增大,由甲、乙两种物质的结构可知, 形成一
W R X Y Z W
个共价键,且原子序数最小, 为 ;、 为带 个单位正电荷的阳离子, 为 , 为 ; 与 个 原子成键后
W H R Y 1 R Li Y Na X 4 W
所得离子带 个单位负电荷,与 个 原子成键后所得离子也带 个单位负电荷,且 、同主族,甲、乙两种物
1 Z 4 W 1 X Z
质分别与水反应都能产生氢气, 为 ,为 。锂和钠较活泼,需要特殊保存, 选项错误。 为 ,在甲、乙中
X B Z Al A W H
都显 价,选项正确。
+
的半径大于
3+
的,选项正确。 -和 -都为四面体结构, 选项正确。
-1 B Na Al C BH4 AlH4 D
12.C
【解析】·表示未成对电子,所以 ·不带电荷,因氢元素的化合价为 价,所以氧元素的化合价为 价, 选项
HO +1 -1 A
正确。随着 的增大,活性炭上吸附的 增多,生成· 增多,去除速率增大; 继续增大时, 将 转
- - +
pH OH OH pH OH NH4
化为 ,不利于活性炭对氨氮的吸附,选项错误。
NH3 C
13.C
【解析】放电时, 失电子,发生氧化反应, 选项正确。充电时,石墨毡为阳极,与电源正极相连, 选项正确。
Zn A B
水和二氯甲烷的不互溶性和密度差能够将正极与负极分隔开,故不能倒置,放电时,阴离子移向负极,故 移
-
PF6
向水层,选项错误。放电时, 板每减轻 ,转移电子的物质的量为 ,有 移动到水层,故
-
C Zn 6.5g 0.2mol 0.2molPF6
水层增重 , 选项正确。
0.2mol×145g/mol+6.5g=35.5g D
14.C
【解析】由题图可知,将 加入 溶液中优先与 反应,再与 反应,而加入 溶液中优先
- +
NaOH NH4HX HX NH4 NH4HCO3
与 反应,再与 反应, 选项不正确。 、 点时,均有c( ) c( ),而温度不变,K 值相
+ - +
NH4 HCO3 A P Q NH3·H2O = NH4 b
同,c( ) c( )时,K c( ),故此时 相等, 选项不正确。由图可知,加入 氢氧化钠
+ -
NH3·H2O = NH4 b = OH pH B 0.20 mol
时,两种溶液中的溶质反应趋向于完全,此时溶液中的溶质分别为 和 、 和 ,两种
NH3·H2O Na2X NH3·H2O Na2CO3
溶液中 均大于 , 选项正确。 选项中等式不符合元素守恒, 选项不正确。
pH 7 C D D
二、非选择题:本题共 小题,共 分。
4 58
( 分)
15. 14
()通过向集气瓶中鼓入空气( 分)
1 1
()不能( 分)
2 1
()( 分) 使氧气过量,氨气与过量的氧气充分反应,避免硝酸铵的生成( 分)
3 B 1 2
()( 分) 继续通入氧气使 、 与氧气和水反应,生成硝酸,防止氮氧化物污染空气( 分)
4 B 1 NO NO2 2
催化剂
() ============ ( 分) 保证气流流通,增大氨气与氧气的接触面积,使氨的催化氧化反
5 4NH3+5O2 4NO+6H2O 2
△
应更充分( 分)
2
() ==== ( 分)、 ==== ( 分)
6 4NO+3O2+2H2O 4HNO3 1 4NO2+O2+2H2O 4HNO3 1
【解析】本题主要考查硝酸的制备和学生实验探究的能力。
化学试题答案 第 页(共 页)
2 4()实验时,通过向集气瓶中鼓入空气,使氨气缓慢、均匀地产生。
1
()碱石灰的作用是干燥氨气,氯化钙不可以干燥氨气。
2
()实验开始时,先通入氧气,排除装置中的空气同时充满氧气,使氧气过量,氨气与过量的氧气充分反应,避免
3
硝酸铵的生成。
()实验结束时,停止鼓入氨气,继续缓缓通入氧气,待装置内气体反应一段时间后,停止通入氧气。装置内氮
4
氧化物与氧气和水反应生成硝酸,免去了尾气处理,降低了实验对通风设备的要求,整个实验更加绿色安全。
()使用玻璃纤维毡堆放催化剂的原因是保证气流流通,增大氨气与氧气的接触面积,使氨的催化氧化反应更
5
充分。
( 分)
16. 14
() ( 分) 低温( 分)
1 -194 2 2
() ( 分) ( 分) 1 P( 分)
2 ①DE 2 ②> 2 ③ 0 3
12
() ~ 时,反应历程 的速率大于反应历程 的速率; ~ 时,反应历程 的速率小于反应历
3 550 650℃ ⅱ ⅲ 650 750℃ ⅱ
程 的速率( 分)
ⅲ 3
【解析】() 项,当v ( ) v ( )时,说明反应已经达到平衡状态;项,体系压强保持不变,能说
2 ①A 正 HCHO = 逆 CH3OH B
明反应已经达到平衡状态;项,氢气体积分数不变,可以说明反应已经达到平衡状态; 项,该反应在体积不变
C D
的容器中进行,反应过程中混合气体的密度始终不变,故混合气体的密度不变时,不能说明反应已经达到平衡
状态;项,非绝热条件下,体系温度不变时,不能说明反应已经达到平衡状态。 平衡时混合体系中 ()
E ② HCHO g
x
的体积分数为 ,若甲醇消耗的物质的量为x ,则 ,解得x ,所以 内,
20% mol x × 100% = 20% = 2 5 min
+ 8
v( ) 2mol ( ),则 内,v( ) ( )。 反应达到平衡时,
CH3OH = = 0.2 mol/ L·min 2.5 min CH3OH > 0.2 mol/ L·min ③
2L×5min
()、 ()、()的物质的量分别为 、 、 ,P P,该条件下反应的平衡常数K = 1 P。
CH3OH g HCHO g H2 g 6mol 2mol 2mol =1.25 0 P 0
12
()由题图可知, ~ 时,甲醛的选择性增大,即生成的甲醛增多, 减少,所以反应历程 的速率大于
3 550 650℃ CO ⅱ
反应历程 的速率; ~ 时,甲醇的转化率增大,而甲醛的选择性变小,即生成的甲醛减少, 增多,所
ⅲ 650 750℃ CO
以反应历程 的速率小于反应历程 的速率。
ⅱ ⅲ
( 分)
17. 15
()第四周期第 族( 分)
1 Ⅷ 1
()可以增大反应速率和提高原料利用率( 分) 和 ( 分) 和 ( 分)
2 1 SiO2 CaSO4 1 MgF2 CaF2 1
() ==== ( 分) ( 分)
2+ + 3+
3 2Fe +H2O2+2H 2Fe +2H2O 2 > 2
() ( 分)
4 5.2~6.6 2
()八面体( 分) 59 + 48 + 16 × 3 或 155 ( 分)
5 1 a N a N 2
3 -30 3 -30
× 10 A × 10 A
() ( 分)
6 Co3O4 2
【解析】钴矿石中加入稀硫酸和 ,可得 、 、 、 、 ,加入的 主要是将 、 还原为
2+ 2+ 3+ 2+ 2+ 3+ 3+
Na2SO3 Co Fe Al Mg Ca Na2SO3 Co Fe
、 ,然后向滤液中加入 将 氧化为 ,加入 调节溶液 ,使 、 形成 ( )、
2+ 2+ 2+ 3+ 3+ 3+
Co Fe H2O2 Fe Fe Na2CO3 pH Fe Al Fe OH 3
( )沉淀,过滤后所得滤液中主要含有 、 、 ,再用 除去 、 ,过滤后,向滤液中加入草酸
2+ 2+ 2+ 2+ 2+
Al OH 3 Co Mg Ca NaF Ca Mg
铵得到二水合草酸钴,煅烧后制得 。
Co2O3
()根据图示, 位于 形成的八面体空隙中心。
5 Ti O
根据晶胞结构可知,一个晶胞中含有 的数目为 1 ,含有 的数目为 ,含有 的数目为 1 ,晶胞
Co 8× =1 Ti 1 O 6× =3
8 2
化学试题答案 第 页(共 页)
3 4(59 + 48 + 16 × 3)g
m N
的质量为(59 + 48 + 16 × 3)g,晶胞体积为(a ) 3 (a -10 ) 3 ,晶体密度为 A
N pm = × 10 cm V = a =
-10 3
A ( × 10 cm)
59 + 48 + 16 × 3(或 155 ) 3 。
a N a N g/cm
3 -30 3 -30
× 10 A × 10 A
()
6 CoC2O4·2H2O→CoC2O4→CoCO3→CoO
183 147 119 75
为了计算的简便,题目中各数字乘以 ,则 、点固体成分是 ,点应为钴的氧化物, 的物质的量为 ,
10 A B CoC2O4 C Co 1mol
x
中氧的物质的量为80.3− 59 ,所以 3,其化学式为 。
CoxOy ≈1.33mol y ≈ Co3O4
16 4
( 分)
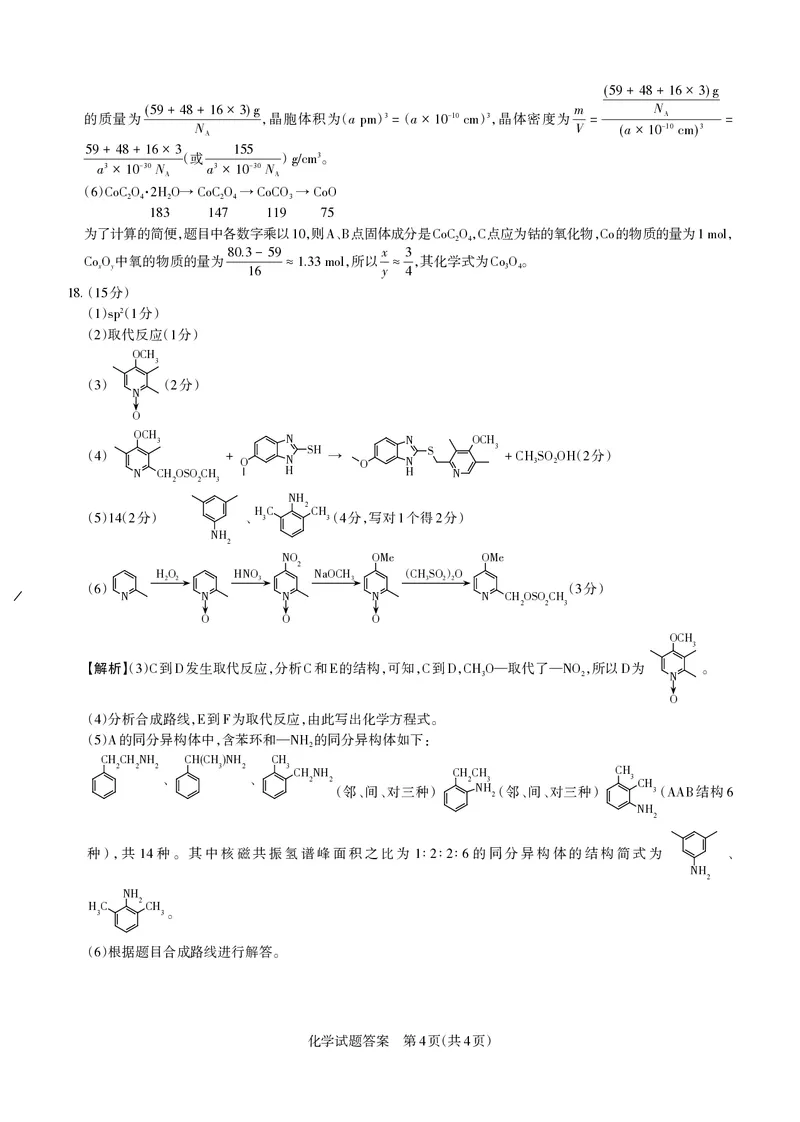
18. 15
() ( 分)
2
1 sp 1
()取代反应( 分)
2 1
OCH
3
() ( 分)
3 2
N
O
OCH
3 N N OCH
() SH S 3 ( 分)
4 + O N → O N +CH3SO2OH 2
N CHOSOCH H H N
2 2 3
NH
2
() ( 分) 、HC CH( 分,写对 个得 分)
5 14 2 3 3 4 1 2
NH
2
NO OMe OMe
2 ( )
()
H2O2 HNO3 NaOCH3 CH3SO2 2O
( 分)
6 3
N N N N N CHOSOCH
2 2 3
O O O
OCH
3
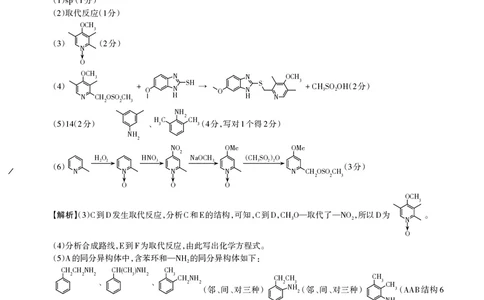
【解析】() 到 发生取代反应,分析 和 的结构,可知,到 , —取代了— ,所以 为 。
3 C D C E C D CH3O NO2 D
N
O
()分析合成路线,到 为取代反应,由此写出化学方程式。
4 E F
() 的同分异构体中,含苯环和— 的同分异构体如下:
5 A NH2
CHCHNH CH(CH)NH CH
2 2 2 3 2 3
、 、 CH 2 NH 2 CH 2 CH 3 CH 3
(邻、间、对三种) (邻、间、对三种) CH( 结构
NH 3
2 AAB 6
NH
2
种),共 种。其中核磁共振氢谱峰面积之比为 ∶∶∶ 的同分异构体的结构简式为 、
14 1 2 2 6
NH
2
NH
2
HC CH 。
3 3
()根据题目合成路线进行解答。
6
化学试题答案 第 页(共 页)
4 4