文档内容
2024年安徽省高考化学试卷
一、单选题
1.下列资源利用中,在给定工艺条件下转化关系正确的是
干馏 分馏 皂化 水解
A.煤→煤油 B.石油→乙烯 C.油脂→甘油 D.淀粉→乙醇
❑ ❑ ❑ ❑
【答案】C
【详解】A.煤的干馏是将煤隔绝空气加强热使之分解的过程,干馏的过程不产生煤油,煤油是石油分馏的产物,
A错误;
B.石油分馏是利用其组分中的不同物质的沸点不同将组分彼此分开,石油分馏不能得到乙烯,B错误;
C.油脂在碱性条件下水解生成甘油和高级脂肪酸盐,C正确;
D.淀粉是多糖,其发生水解反应生成葡萄糖,D错误;
故答案选C。
2.下列各组物质的鉴别方法中,不可行的是
A.过氧化钠和硫黄:加水,振荡 B.水晶和玻璃:X射线衍射实验
C.氯化钠和氯化钾:焰色试验 D.苯和甲苯:滴加溴水,振荡
【答案】D
【详解】A.过氧化钠可以与水发生反应生成可溶性的氢氧化钠,硫不溶于水,A可以鉴别;
B.水晶为晶体,有独立的晶格结构,玻璃为非晶体,没有独立的晶格结构,可以用X射线衍射实验进行鉴别,B
可以鉴别;
C.钠的焰色为黄色,钾的焰色为紫色(需透过蓝色钴玻璃),二者可以用焰色试验鉴别,C可以鉴别;
D.苯和甲苯都可以溶解溴水中的溴且密度都比水小,二者都在上层,不能用溴水鉴别苯和甲苯,D不可以鉴别;
故答案选D。
3.青少年帮厨既可培养劳动习惯,也能将化学知识应用于实践。下列有关解释合理的是
A.清洗铁锅后及时擦干,能减缓铁锅因发生吸氧腐蚀而生锈
B.烹煮食物的后期加入食盐,能避免NaCl长时间受热而分解
C.将白糖熬制成焦糖汁,利用蔗糖高温下充分炭化为食物增色
D.制作面点时加入食用纯碱,利用NaHCO 中和发酵过程产生的酸
3
【答案】A
【详解】A.铁发生吸氧腐蚀时,正极上O 得电子结合水生成氢氧根离子,清洗铁锅后及时擦干,除去了铁锅表
2
面的水分,没有了电解质溶液,能减缓铁锅因发生吸氧腐蚀而生锈,A正确;
B.食盐中含有碘酸钾,碘酸钾受热不稳定易分解,因此烹煮食物时后期加入食盐,与NaCl无关,B错误;
C.焦糖的主要成分仍是糖类,同时还含有一些醛类、酮类等物质,蔗糖在高温下并未炭化,C错误;
D.食用纯碱主要成分为NaCO,制作面点时加入食用纯碱,利用了NaCO 中和发酵过程产生的酸,D错误;
2 3 2 3
故答案选A。
4.下列选项中的物质能按图示路径在自然界中转化,且甲和水可以直接生成乙的是
选
甲 乙 丙
项
A Cl NaClO NaCl
2B SO H SO CaSO
2 2 4 4
C Fe O Fe(OH) FeCl
2 3 3 3
D CO H CO Ca(HCO )
2 2 3 3 2
A.A B.B C.C D.D
【答案】D
【详解】A.Cl 与水反应生成HClO和HCl,无法直接生成NaClO,A错误;
2
B.SO 与水反应生成亚硫酸而不是硫酸,B错误;
2
C.氧化铁与水不反应,不能生成氢氧化铁沉淀,C错误;
D.CO 与水反应生成碳酸,碳酸与碳酸钙反应生成碳酸氢钙,碳酸氢钙受热分解生成二氧化碳气体,D正确;
2
故答案选D。
5.D-乙酰氨基葡萄糖(结构简式如下)是一种天然存在的特殊单糖。下列有关该物质说法正确的是
A.分子式为C H O N B.能发生缩聚反应
8 14 6
C.与葡萄糖互为同系物 D.分子中含有σ键,不含π键
【答案】B
【详解】A.由该物质的结构可知,其分子式为:C H ON,故A错误;
8 15 6
B.该物质结构中含有多个醇羟基,能发生缩聚反应,故B正确;
C.组成和结构相似,相差若干个CH 原子团的化合物互为同系物,葡萄糖分子式为C H O,该物质分子式为:
2 6 12 6
C H ON,不互为同系物,故C错误;
8 15 6
D.单键均为σ键,双键含有1个σ键和1个π键,该物质结构中含有C=O键,即分子中σ键和π键均有,故D
错误;
故选B。
二、未知
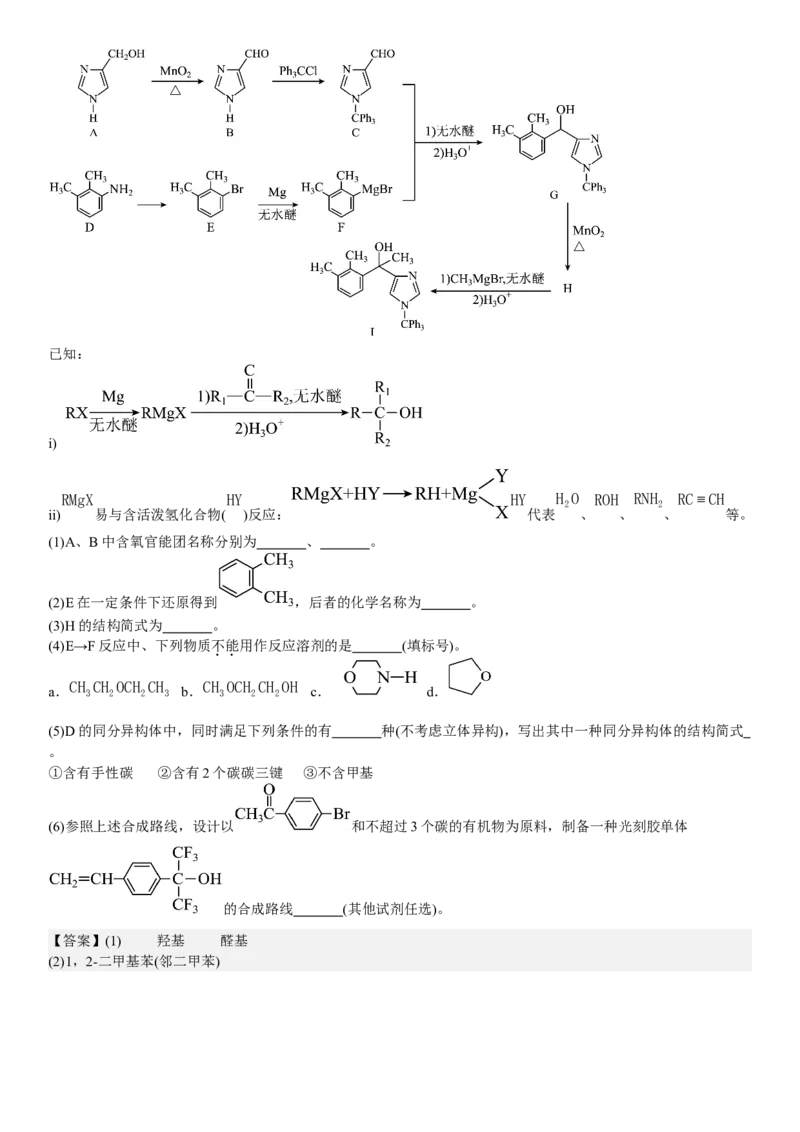
地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化物),羟胺(NH OH)以中间产
2
物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反应的产物盐酸羟胺([NH OH]Cl)广泛用
3
子药品、香料等的合成。已知 25℃ 时, K (HNO )=7.2×10-4 , K (NH ⋅H O)=1.8×10-5 ,
a 2 b 3 2
。
K (NH OH)=8.7×10-9
b 2
完成下列小题。6.N 是阿伏加德罗常数的值。下列说法正确的是
A
A.标准状况下,2.24L X和Y混合气体中氧原子数为0.1N
A
B. 溶液中 和 数均为
1L 0.1mol⋅L-1NaNO Na+ NO- 0.1N
2 2 A
C. 完全转化为 时,转移的电子数为
3.3g NH OH NO- 0.6N
2 2 A
D.2.8g N 中含有的价电子总数为0.6N
2 A
7.下列有关物质结构或性质的比较中,正确的是
A.键角:
NH >NO-
3 3
B.熔点:NH OH>[NH OH]Cl
2 3
C.25℃同浓度水溶液的pH:[NH OH]Cl>NH Cl
3 4
D.羟胺分子间氢键的强弱:O-H…O>N-H…N
【答案】6.A 7.D
【分析】
NO-
在亚硝酸盐还原酶的作用下转化为X,X在X还原酶的作用下转化为Y,X、Y均为氮氧化物,即X
2
为NO,Y为NO。
2
6.A.标准状况下,2.24L NO和NO混合气体物质的量为0.1mol,氧原子数为0.1N ,A正确;
2 A
B.HNO 为弱酸,因此 能够水解为HNO, 溶液中 数目小于 ,B错误;
2 NO- 2 1L 0.1mol⋅L-1NaNO NO- 0.1N
2 2 2 A
C. 完全转化为 时,N的化合价由-1上升到+3, 物质的量为0.1mol,转移的电子数为
NH OH NO- 3.3g NH OH
2 2 2
0.4N ,C错误;
A
D.2.8g N 物质的量为0.1mol,N的价电子数等于最外层电子数为5,2.8g N 含有的价电子总数为N ,D错误;
2 2 A
故选A。
1
7.A.NH 中N原子的价层电子对数=3+ (5-3×1)=3+1=4,为sp3杂化,键角为107°,NO-中N的价层电子对
3 2 3
1
数=3+ (5+1-3×2)=3+0=3,为sp2杂化,键角为120°,故键角:NH <NO-,A错误;
2 3 3
B.NH OH为分子晶体,[NH OH]Cl为离子晶体,故熔点:NH OH<[NH OH]Cl,B错误;
2 3 2 3
C.由题目信息可知,25℃下,K (NH ⋅H O)>K (NH OH),故NH OH的碱性比NH ⋅H O弱,故同浓度的水溶液
b 3 2 b 2 2 3 2
中,
[NH OH]
+的电离程度大于
NH+
的电离程度,同浓度水溶液的pH:
[NH OH]Cl<NH Cl
,C错误;
3 4 3 4
D.O的电负性大于N,O-H键的极性大于N-H键,故羟胺分子间氢键的强弱O-H⋯O>N-H⋯N,D正确;
故选D。
三、单选题
8.某催化剂结构简式如图所示。下列说法错误的是
A.该物质中Ni为+2价 B.基态原子的第一电离能:Cl>PC.该物质中C和P均采取sp2杂化 D.基态Ni原子价电子排布式为3d84s2
【答案】C
【详解】A.由结构简式可知,P原子的3个孤电子与苯环形成共用电子对,P原子剩余的孤电子对与Ni形成配位
键,Cl-提供孤电子对,与Ni形成配位键,由于整个分子呈电中性,故该物质中Ni为+2价,A项正确;
B.同周期元素随着原子序数的增大,第一电离能有增大趋势,故基态原子的第一电离能:Cl>P,B项正确;
C.该物质中,C均存在于苯环上,采取sp2杂化,P与苯环形成3对共用电子对,剩余的孤电子对与Ni形成配位
键,价层电子对数为4,采取sp3杂化,C项错误;
D.Ni的原子序数为28,位于第四周期第Ⅷ族,基态Ni原子价电子排布式为3d84s2,D项正确;
故选C。
9.仅用下表提供的试剂和用品,不能实现相应实验目的的是
选
实验目的 试剂 用品
项
MgCl 溶液、AlCl 溶液、氨
A 比较镁和铝的金属性强弱 2 3 试管、胶头滴管
水
乙醇、乙酸、浓硫酸、饱和 试管、橡胶塞、导管、乳胶管铁架台(带铁夹)、
B 制备乙酸乙酯
Na CO 溶液 碎瓷片、酒精灯、火柴
2 3
C 制备[Cu(NH ) ]SO 溶液 CuSO 溶液、氨水 试管、胶头滴管
3 4 4 4
利用盐类水解制备 烧杯、胶头滴管、石棉网、三脚架、酒精灯、火
D 饱和FeCl 溶液、蒸馏水
Fe(OH) 胶体 3 柴
3
A.A B.B C.C D.D
【答案】A
【详解】A.MgCl 溶液、AlCl 溶液与过量氨水反应时现象相同,分别产生白色Mg(OH) 、Al(OH) 沉淀,不能比
2 3 2 3
较Mg(OH) 和Al(OH) 碱性的强弱,从而不能比较Mg和Al的金属性强弱,可将氨水换成过量的NaOH溶液,A
2 3
项不能实现实验目的;
B.在一支试管中依次加入一定量的乙醇、浓硫酸、乙酸,并且放入几粒碎瓷片,另一支试管中加入适量饱和碳酸
钠溶液,如图 连接好装置,用酒精灯小心加热,乙酸与乙醇在浓硫酸存在、加热条件下发生酯
化反应生成乙酸乙酯和水,在饱和碳酸钠溶液液面上收集乙酸乙酯,发生反应的化学方程式为
浓硫酸
CH 3 COOH+CH 3 CH 2 OH ⇌ CH 3 COOCH 2 CH 3 +H 2 O,B项能实现实验目的;
Δ
C.向盛有CuSO 溶液的试管中滴加氨水,首先产生蓝色Cu(OH) 沉淀,继续滴加氨水,沉淀溶解得到深蓝色的
4 2
[Cu(NH )]SO 溶液,发生反应的化学方程式为CuSO +4NH∙H O=[Cu(NH )]SO +4H O,C项能实现实验目的;
3 4 4 4 3 2 3 4 4 2
D.将烧杯中的蒸馏水加热至沸腾,向沸水中加入5~6滴饱和FeCl 溶液,继续加热至液体呈红褐色即制得Fe(OH)
3 3
Δ
胶体,反应的化学方程式为FeCl +3H O Fe(OH) (胶体)+3HCl,D项能实现实验目的;
3 2 3
¿
¿
答案选A。
10.某温度下,在密闭容器中充入一定量的X(g),发生下列反应:X(g)
⇌
Y(g)(ΔH <0),
1
Y(g)
⇌
Z(g)(ΔH <0),测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意的是
2A. B.
C. D.
【答案】B
【分析】由图可知,反应初期随着时间的推移X的浓度逐渐减小、Y和Z的浓度逐渐增大,后来随着时间的推移
X和Y的浓度逐渐减小、Z的浓度继续逐渐增大,说明X(g)⇌Y(g)的反应速率大于Y(g)⇌Z(g)的反应速率,则反
应X(g)⇌Y(g)的活化能小于反应Y(g)⇌Z(g)的活化能。
【详解】A.X(g)⇌Y(g)和Y(g)⇌Z(g)的∆H都小于0,而图像显示Y的能量高于X,即图像显示X(g)⇌Y(g)为吸
热反应,A项不符合题意;
B.图像显示X(g)⇌Y(g)和Y(g)⇌Z(g)的∆H都小于0,且X(g)⇌Y(g)的活化能小于Y(g)⇌Z(g)的活化能,B项符
合题意;
C.图像显示X(g)⇌Y(g)和Y(g)⇌Z(g)的∆H都小于0,但图像上X(g)⇌Y(g)的活化能大于Y(g)⇌Z(g)的活化能,
C项不符合题意;
D.图像显示X(g)⇌Y(g)和Y(g)⇌Z(g)的∆H都大于0,且X(g)⇌Y(g)的活化能大于Y(g)⇌Z(g)的活化能,D项不
符合题意;
选B。
11.我国学者研发出一种新型水系锌电池,其示意图如下。该电池分别以Zn-TCPP(局部结构如标注框内所示)形成
的稳定超分子材料和Zn为电极,以ZnSO 和KI混合液为电解质溶液。下列说法错误的是
4
A.标注框内所示结构中存在共价键和配位键
放电
B.电池总反应为:I-+Zn
⇌
Zn2++3I-
3
充电C.充电时,阴极被还原的Zn2+主要来自Zn-TCPP
D.放电时,消耗0.65g Zn,理论上转移0.02mol电子
【答案】C
【分析】由图中信息可知,该新型水系锌电池的负极是锌、正极是超分子材料;负极的电极反应式为
,则充电时,该电极为阴极,电极反应式为 ;正极上发生 ,则充电时,
Zn-2e-=Zn2+ Zn2++2e-=Zn I-+2e-=3I-
3
该电极为阳极,电极反应式为 。
3I--2e-=I-
3
【详解】A.标注框内所示结构属于配合物,配位体中存在碳碳单键、碳碳双键、碳氮单键、碳氮双键和碳氢键等
多种共价键,还有由N提供孤电子对、Zn2+提供空轨道形成的配位键,A正确;
放电
B.由以上分析可知,该电池总反应为I-+Zn
⇌
Zn2++3I-,B正确;
3
充电
C.充电时,阴极电极反应式为Zn2++2e-=Zn,被还原的Zn2+主要来自电解质溶液,C错误;
D.放电时,负极的电极反应式为Zn-2e-=Zn2+,因此消耗0.65 g Zn(物质的量为0.01mol),理论上转移0.02
mol电子,D正确;
综上所述,本题选C。
12.室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下 浓度随时间变化关系如下图。
SeO2- SeO2-
4 4
实验序号 水样体积/mL 纳米铁质量/mg 水样初始pH
① 50 8 6
② 50 2 6
③ 50 2 8
下列说法正确的是
A.实验①中,0~2小时内平均反应速率
v(SeO2-)=2.0mol⋅L-1 ⋅h-1
4
B.实验③中,反应的离子方程式为:
2Fe+SeO2-+8H+=2Fe3++Se+4H O
4 2
C.其他条件相同时,适当增加纳米铁质量可加快反应速率
D.其他条件相同时,水样初始 越小, 的去除效果越好
pH SeO2-
4
【答案】C
【详解】A. 实验①中,0~2小时内平均反应速率
(5.0×10-3-1.0×10-3 )mol⋅L-1
v(SeO2-)= =2.0×10-3mol⋅L-1 ⋅h-1,A不正确;
4 2h
B. 实验③中水样初始pH=8,溶液显弱碱性,发生反应的离子方程式中不能用H+配电荷守恒,B不正确;
C. 综合分析实验①和②可知,在相同时间内,实验①中 浓度的变化量大,因此,其他条件相同时,适当增
SeO2-
4
加纳米铁质量可加快反应速率,C正确;D. 综合分析实验③和②可知,在相同时间内,实验②中 浓度的变化量大,因此,其他条件相同时,适当减
SeO2-
4
小初始 , 的去除效果越好,但是当初始 太小时, 浓度太大,纳米铁与 反应速率加快,会导致与
pH SeO2- pH H+ H+
4
反应的纳米铁减少,因此,当初始 越小时 的去除效果不一定越好,D不正确;
SeO2- pH SeO2-
4 4
综上所述,本题选C。
13.环境保护工程师研究利用Na S、FeS和H S处理水样中的Cd2+。已知25℃时,H S饱和溶液浓度约为
2 2 2
, , , , 。下列说法错误的
0.1mol⋅L-1 K (H S)=10-6.97 K (H S)=10-12.90 K (FeS)=10-17.20 K (CdS)=10-26.10
a1 2 a2 2 sp sp
是
A.Na S溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-)
2
B. 溶液中:
0.01mol⋅L-1Na S c(Na+)>c(S2-)>c(OH-)>c(HS-)
2
C.向c(Cd2+)=0.01mol⋅L-1的溶液中加入FeS,可使c(Cd2+)<10-8mol⋅L-1
D.向c(Cd2+)=0.01mol⋅L-1的溶液中通入H
2
S气体至饱和,所得溶液中:c(H+)>c(Cd2+)
【答案】B
【详解】A.Na S溶液中只有5种离子,分别是H+ 、Na+ 、OH- 、HS- 、S2-,溶液是电中性的,存在电荷守恒,
2
可表示为c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-),A正确;
B. 溶液中, 水解使溶液呈碱性,其水解常数为
0.01mol⋅L-1Na S S2-
2
K = c(OH- )⋅c(HS- ) = K W = 10-14 =10-1.1 ,根据硫元素守恒可知 c(HS- )<10-1.1mol⋅L-1 ,所以c(OH- ) >1 ,则
h c(S2- ) K 10-12.9 c(S2- )
a2
,B不正确;
c(OH- )>c(S2-
)
C.K
sp
(FeS)远远大于K
sp
(CdS),向c(Cd2+)=0.01mol⋅L-1的溶液中加入FeS时,可以发生沉淀的转化,该反应
的平衡常数为 K (FeS) 10-17.20 ,因此该反应可以完全进行, 的饱和溶液中
K= sp = =108.9 ≫105 CdS
K (CdS) 10-26.10
sp
,若加入足量 时可使 ,C正确
c(Cd2+)=√10-26.1mol⋅L-1=10-13.05mol⋅L-1 FeS c(Cd2+)<10-8mol⋅L-1
D. Cd2++H S ❑ CdS+2H+ 的平衡常数 K= c2(H+ ) = K a1 ⋅K a2= 10-6.97×10-12.90 =106.23 ≫105,
2 ⇌ c(Cd2+ )⋅c(H
2
S) K
sp
10-26.10
该反应可以完全进行,因此,当向c(Cd2+)=0.01mol⋅L-1的溶液中通入H
2
S气体至饱和,Cd2+可以完全沉淀,所得
溶液中c(H+)>c(Cd2+),D正确;
综上所述,本题选B。
14.研究人员制备了一种具有锂离子通道的导电氧化物(Li La TiO ),其立方晶胞和导电时Li+迁移过程如下图所
x y 3
示。已知该氧化物中Ti为+4价,La为+3价。下列说法错误的是1
A.导电时,Ti和La的价态不变 B.若x= ,Li+与空位的数目相等
3
C.与体心最邻近的O原子数为12 D.导电时、空位移动方向与电流方向相反
【答案】B
【详解】A.根据题意,导电时Li+发生迁移,化合价不变,则Ti和La的价态不变,A项正确;
1 1 1
B.根据“均摊法”,1个晶胞中含Ti:8× =1个,含O:12× =3个,含La或Li或空位共:1个,若x= ,则
8 4 3
2 2 1
La和空位共 ,n(La)+n(空位)= ,结合正负化合价代数和为0,(+1)× +(+3)×n(La)+(+4)×1+(-2)×3=0,解得n(La)=
3 3 3
5 1
、n(空位)= ,Li+与空位数目不相等,B项错误;
9 9
C.由立方晶胞的结构可知,与体心最邻近的O原子数为12,即位于棱心的12个O原子,C项正确;
D.导电时Li+向阴极移动方向,即与电流方向相同,则空位移动方向与电流方向相反,D项正确;
答案选B。
四、解答题
15.精炼铜产生的铜阳极泥富含Cu、Ag、Au等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的
流程,如下图所示。
回答下列问题:
(1)Cu位于元素周期表第 周期第 族。
(2)“浸出液1”中含有的金属离子主要是 。
(3)“浸取2”步骤中,单质金转化为HAuCl 的化学方程式为 。
4
(4)“浸取3”步骤中,“浸渣2”中的 (填化学式)转化为 3-。
[Ag(S O ) ]
2 3 2
(5)“电沉积”步骤中阴极的电极反应式为 。“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为
(填化学式)。
(6)“还原”步骤中,被氧化的N H 与产物Au的物质的量之比为 。
2 4
(7) 可被 氧化为 。从物质结构的角度分析 的结构为(a)而不是(b)的原因: 。
Na S O I Na S O S O2-
2 2 3 2 2 4 6 4 6
【答案】(1) 四 ⅠB
(2)Cu2+
(3)2Au+8HCl+3H O =2HAuCl +6H O
2 2 4 2(4)AgCl
(5) [Ag(S O ) ] 3-+e-=Ag↓+2S O2- Na S O
2 3 2 2 3 2 2 3
(6)3:4
(7)(a)结构中电子云分布较均衡,结构较为稳定,(b)结构中正负电荷中心不重合,极性较大,较不稳定,且存在过
氧根,过氧根的氧化性大于I,故NaSO 不能被I 氧化成(b)结构
2 2 2 3 2
【分析】精炼铜产生的铜阳极泥富含Cu、Ag、Au等元素,铜阳极泥加入硫酸、HO 浸取,Cu被转化为Cu2+进入
2 2
浸取液1中,Ag、Au不反应,浸渣1中含有Ag和Au;浸渣1中加入盐酸、HO 浸取,Au转化为HAuCl 进入浸
2 2 4
取液2,Ag转化为AgCl,浸渣2中含有AgCl;浸取液2中加入NH 将HAuCl 还原为Au,同时NH 被氧化为
2 4 4 2 4
N 2 ;浸渣2中加入 Na S O ,将AgCl转化为 [Ag(S O ) ] 3- ,得到浸出液3,利用电沉积法将 [Ag(S O ) ] 3- 还原为
2 2 3 2 3 2 2 3 2
Ag。
【详解】(1)Cu的原子序数为29,位于第四周期第ⅠB族;
(2)由分析可知,铜阳极泥加入硫酸、HO 浸取,Cu被转化为Cu2+进入浸取液1中,故浸取液1中含有的金属离
2 2
子主要是Cu2+;
(3)浸取2步骤中,Au与盐酸、HO 反应氧化还原反应,生成HAuCl 和HO,根据得失电子守恒及质量守恒,
2 2 4 2
可得反应得化学方程式为:2Au+8HCl+3H O =2HAuCl +6H O;
2 2 4 2
(4)根据分析可知,浸渣2中含有AgCl,与
Na S O
反应转化为
[Ag(S O ) ] 3-
;
2 2 3 2 3 2
(5)电沉积步骤中,阴极发生还原反应,
[Ag(S O ) ] 3-
得电子被还原为Ag,电极反应式为:
2 3 2
[Ag(S O ) ] 3-+e-=Ag↓+2S O2- ;阴极反应生成 S O2- ,同时阴极区溶液中含有Na+,故电沉积步骤完成后,阴极
2 3 2 2 3 2 3
区溶液中可循环利用得物质为Na S O ;
2 2 3
(6)还原步骤中, HAuCl 被还原为Au,Au化合价由+3价变为0价,一个HAuCl 转移3个电子,NH 被氧化为
4 4 2 4
N,N的化合价由-2价变为0价,一个NH 转移4个电子,根据得失电子守恒,被氧化的NH 与产物Au的物质
2 2 4 2 4
的量之比为3:4;
(7)(a)结构中电子云分布较均衡,结构较为稳定,(b)结构中正负电荷中心不重合,极性较大,较不稳定,且存在
过氧根,过氧根的氧化性大于I,故NaSO 不能被I 氧化成(b)结构。
2 2 2 3 2
16.测定铁矿石中铁含量的传统方法是SnCl -HgCl -K Cr O ,滴定法。研究小组用该方法测定质量为ag的某赤
2 2 2 2 7
铁矿试样中的铁含量。
【配制溶液】
① 标准溶液。
c mol⋅L-1K Cr O
2 2 7
②SnCl 溶液:称取6g SnCl ⋅2H O溶于20mL浓盐酸,加水至100mL,加入少量锡粒。
2 2 2
【测定含量】按下图所示(加热装置路去)操作步骤进行实验。
已知:氯化铁受热易升华;室温时 ,可将 氧化为 。难以氧化 ; 可被 还原为 。回
HgCl Sn2+ Sn4+ Fe2+ Cr O2- Fe2+ Cr3+
2 2 7
答下列问题:
(1)下列仪器在本实验中必须用到的有 (填名称)。(2)结合离子方程式解释配制SnCl 溶液时加入锡粒的原因: 。
2
(3)步骤I中“微热”的原因是 。
(4)步琛Ⅲ中,若未“立即滴定”,则会导致测定的铁含量 (填“偏大”“偏小”或“不变”)。
(5)若消耗 标准溶液 ,则 试样中 的质量分数为 (用含a、c、V的代数式表示)。
c mol⋅L-1K Cr O V mL a g Fe
2 2 7
(6)SnCl -TiCl -KMnO 滴定法也可测定铁的含量,其主要原理是利用SnCl 和TiCl 将铁矿石试样中Fe3+还原为
2 3 4 2 3
Fe2+,再用KMnO 标准溶液滴定。
4
①从环保角度分析,该方法相比于SnCl -HgCl -K Cr O ,滴定法的优点是 。
2 2 2 2 7
②为探究KMnO 溶液滴定时,Cl-在不同酸度下对Fe2+测定结果的影响,分别向下列溶液中加入1滴
4
溶液,现象如下表:
0.1mol⋅L-1KMnO
4
溶液 现象
空白实
2mL 0.3mol⋅L-1NaCl溶液+0.5mL试剂X 紫红色不褪去
验
2mL 0.3mol⋅L-1NaCl溶液
实验I 紫红色不褪去
+0.5 mL 0.1mol⋅L-1硫酸
2mL 0.3mol⋅L-1NaCl溶液+0.5 mL 6mol⋅L-1
实验ⅱ 紫红色明显变浅
硫酸
表中试剂X为 ;根据该实验可得出的结论是 。
【答案】(1)容量瓶、量筒
(2)Sn2+易被空气氧化为Sn4+,离子方程式为 ,加入Sn,发生反应 ,
2Sn2++O +4H+=2Sn4++2H O Sn4++Sn=2Sn2+
2 2
可防止Sn2+氧化
(3)助溶,使铁矿石在酸液中全部溶解
(4)偏小
33.6cV
(5) %
a
(6) 更安全,对环境更友好 HO 酸性越强,KMnO 的氧化性越强,Cl-被KMnO 氧化的可能性越大,
2 4 4
对Fe2+测定结果造成干扰的可能性越大,因此在KMnO 标准液进行滴定时,要控制溶液的pH值
4
【分析】浓盐酸与试样反应,使得试样中Fe元素以离子形式存在,滴加稍过量的SnCl 使Fe3+还原为Fe2+,冷却后
2
滴加HgCl ,将多余的Sn2+氧化为Sn4+,加入硫酸和磷酸混合液后,滴加指示剂,用KCr O 进行滴定,将Fe2+氧化
2 2 2 7
为Fe3+,化学方程式为 。
6Fe2++Cr O2-+14H+=2Cr3++6Fe3++7H O
2 7 2
【详解】(1)配制SnCl 溶液需要用到容量瓶和量筒,滴定需要用到酸式滴定管,但给出的为碱式滴定管,因此
2
给出仪器中,本实验必须用到容量瓶、量筒;
(2)Sn2+易被空气氧化为Sn4+,离子方程式为 ,加入Sn,发生反应
2Sn2++O +4H+=2Sn4++2H O
2 2
Sn4++Sn=2Sn2+,可防止Sn2+氧化;
(3)步骤I中“微热”是为了助溶,使铁矿石在酸液中全部溶解;
(4)步琛Ⅲ中,若未“立即滴定”,Fe2+易被空气中的O 氧化为Fe3+,导致测定的铁含量偏小;
2(5)根据方程式
6Fe2++Cr O2-+14H+=2Cr3++6Fe3++7H O
可得:
n(Fe2+)=6×n(Cr O2-)=6×10-3cVmol
,
2 7 2 2 7
0.336cVg 33.6cV
ag试样中Fe元素的质量为6×10-3cVmol×56g/mol=0.336cVg,质量分数为 ×100%= %
ag a
(6)①SnCl -HgCl -K Cr O 方法中,HgCl 氧化Sn2+的离子方程式为:Hg2++Sn2+=Sn4++Hg,生成的Hg有剧
2 2 2 2 7 2
毒,因此SnCl -TiCl -KMnO 相比于SnCl -HgCl -K Cr O 的优点是:更安全,对环境更友好;
2 3 4 2 2 2 2 7
②2mL 0.3mol⋅L-1NaCl溶液+0.5mL试剂X,为空白试验,因此X为HO;由表格可知,酸性越强,KMnO 的
2 4
氧化性越强,Cl-被KMnO 氧化的可能性越大,对Fe2+测定结果造成干扰的可能性越大,因此在KMnO 标准液进行
4 4
滴定时,要控制溶液的pH值。
17.乙烯是一种用途广泛的有机化工原料。由乙烷制乙烯的研究备受关注。回答下列问题:
【乙烷制乙烯】
(1)C H 氧化脱氢反应:
2 6
2C H (g)+O (g)=2C H (g)+2H O(g) ΔH =-209.8kJ⋅mol-1
2 6 2 2 4 2 1
C H (g)+CO (g)=C H (g)+H O(g)+CO(g) ΔH =178.1kJ⋅mol-1
2 6 2 2 4 2 2
计算:2CO(g)+O (g)=2CO (g) ΔH = kJ⋅mol-1
2 2 3
(2)C H 直接脱氢反应为C H (g)=C H (g)+H (g) ΔH ,C H 的平衡转化率与温度和压强的关系如图所示,则
2 6 2 6 2 4 2 4 2 6
ΔH = 0(填“>”“<”或“=”)。结合下图。下列条件中,达到平衡时转化率最接近40%的是 (填标号)。
4
a.600°C,0.6MPa b.700°C,0.7MPa c.800°C,0.8MPa
(3)一定温度和压强下、反应i C H (g) ⇌ C H (g)+H (g) K
2 6 2 4 2 a1
反应ⅱ C H (g)+H (g) ⇌ 2CH (g) K (K 远大于K )(K 是以平衡物质的量分数代替平衡浓度计算的平衡常数)
2 6 2 4 a2 a2 a1 x
①仅发生反应i时。C H 的平衡转化宰为25.0%,计算K = 。
2 6 a1
②同时发生反应i和ⅱ时。与仅发生反应i相比,C H 的平衡产率 (填“增大”“减小”或“不变”)。
2 4
【乙烷和乙烯混合气的分离】
(4)通过Cu+修饰的Y分子筛的吸附-脱附。可实现C H 和C H 混合气的分离。Cu+的 与C H 分子的π键电子
2 4 2 6 2 4
形成配位键,这种配位键强弱介于范德华力和共价键之间。用该分子筛分离C H 和C H 的优点是 。
2 4 2 6
(5)常温常压下,将C H 和C H 等体积混合,以一定流速通过某吸附剂。测得两种气体出口浓度(c)与进口浓度(c )
2 4 2 6 0
之比随时间变化关系如图所示。下列推断合理的是 (填标号)。A.前30min,两种气体均未被吸附
B.p点对应的时刻,出口气体的主要成分是C H
2 6
C.a-b对应的时间段内,吸附的C H 逐渐被C H 替代
2 6 2 4
【答案】(1)-566
(2) > b
1
(3) 增大
15
(4) 4s空轨道 识别度高,能有效将C H 和C H 分离,分离出的产物中杂质少,纯度较高
2 4 2 6
(5)BC
【详解】(1)将两个反应依次标号为反应①和反应②,反应①-反应②×2可得目标反应,则ΔH=ΔH -
3 1
2ΔH=(-209.8-178.1×2)kJ/mol=-566kJ/mol。
2
(2)从图中可知,压强相同的情况下,随着温度升高,C H 的平衡转化率增大,因此该反应为吸热反应,
2 6
ΔH>0。
4
a.600℃,0.6MPa时,C H 的平衡转化率约为20%,a错误;
2 6
b.700℃,0.7MPa时,C H 的平衡转化率约为50%,最接近40%,b正确;
2 6
c.700℃,0.8MPa时,C H 的平衡转化率接近50%,升高温度,该反应的化学平衡正向移动,C H 转化率增大,
2 6 2 6
因此800℃,0.8MPa时,C H 的平衡转化率大于50%,c错误;
2 6
故答案选b。
(3)①仅发生反应i,设初始时C H 物质的量为1mol,平衡时C H 转化率为25%,则消耗C H0.25mol,生成
2 6 2 6 2 6
0.2×0.2 1
C H0.25mol,生成H0.25mol,K = = 。
2 4 2 a1
0.6 15
②只发生反应i时,随着反应进行,气体总物质的量增大,压强增大促使化学平衡逆向移动,同时发生反应i和反
应ii,且从题干可知K 远大于K ,反应ii为等体积反应,因为反应ii的发生相当于在单独发生反应i的基础上减
a2 a1
小了压强,则反应i化学平衡正向移动,C H 平衡产率增大。
2 4
(4)配合物中,金属离子通常提供空轨道,配体提供孤电子对,则Cu+的4s空轨道与C H 分子的π键电子形成配
2 4
位键。C H 能与Cu+形成配合物而吸附在Y分子筛上,C H 中无孤电子对不能与Cu+形成配合物而无法吸附,通过
2 4 2 6
这种分子筛分离C H 和C H,优点是识别度高,能有效将C H 和C H 分离,分离出的产物中杂质少,纯度较高。
2 4 2 6 2 4 2 6
c
(5)A.前30min, 等于0,出口浓度c为0,说明两种气体均被吸附,A错误;
c
0
c c
B.p点时,C H 对应的 约为1.75,出口处C H 浓度较大,而C H 对应的 较小,出口处C H 浓度较小,说明
2 6 c 2 6 2 4 c 2 4
0 0
此时出口处气体的主要成分为C H,B正确;
2 6
c c
C.a点处C H 的 =1,说明此时C H 不再吸附在吸附剂上,而a点后C H 的 >1,说明原来吸附在吸附剂上的
2 6 c 2 6 2 6 c
0 0
c
C H 也开始脱落,同时从图中可知,a点后一段时间,C H 的 仍为0,说明是吸附的C H 逐渐被C H 替代,p
2 6 2 4 c 2 6 2 4
0
点到b点之间,吸附的C H 仍在被C H 替代,但是速率相对之前有所减小,同时吸附剂可能因吸附量有限等原因
2 6 2 4
c
无法一直吸附C H,因此p点后C H 的 也逐步增大,直至等于1,此时吸附剂不能再吸附两种物质,C正确;
2 4 2 4 c
0
故答案选BC。
18.化合物1是一种药物中间体,可由下列路线合成(Ph代表苯基,部分反应条件略去):已知:
i)
RMgX HY HY H O ROH RNH RC≡CH
2 2
ii) 易与含活泼氢化合物( )反应: 代表 、 、 、 等。
(1)A、B中含氧官能团名称分别为 、 。
(2)E在一定条件下还原得到 ,后者的化学名称为 。
(3)H的结构简式为 。
(4)E→F反应中、下列物质不能用作反应溶剂的是 (填标号)。
CH CH OCH CH CH OCH CH OH
a.
3 2 2 3
b.
3 2 2
c. d.
(5)D的同分异构体中,同时满足下列条件的有 种(不考虑立体异构),写出其中一种同分异构体的结构简式
。
①含有手性碳 ②含有2个碳碳三键 ③不含甲基
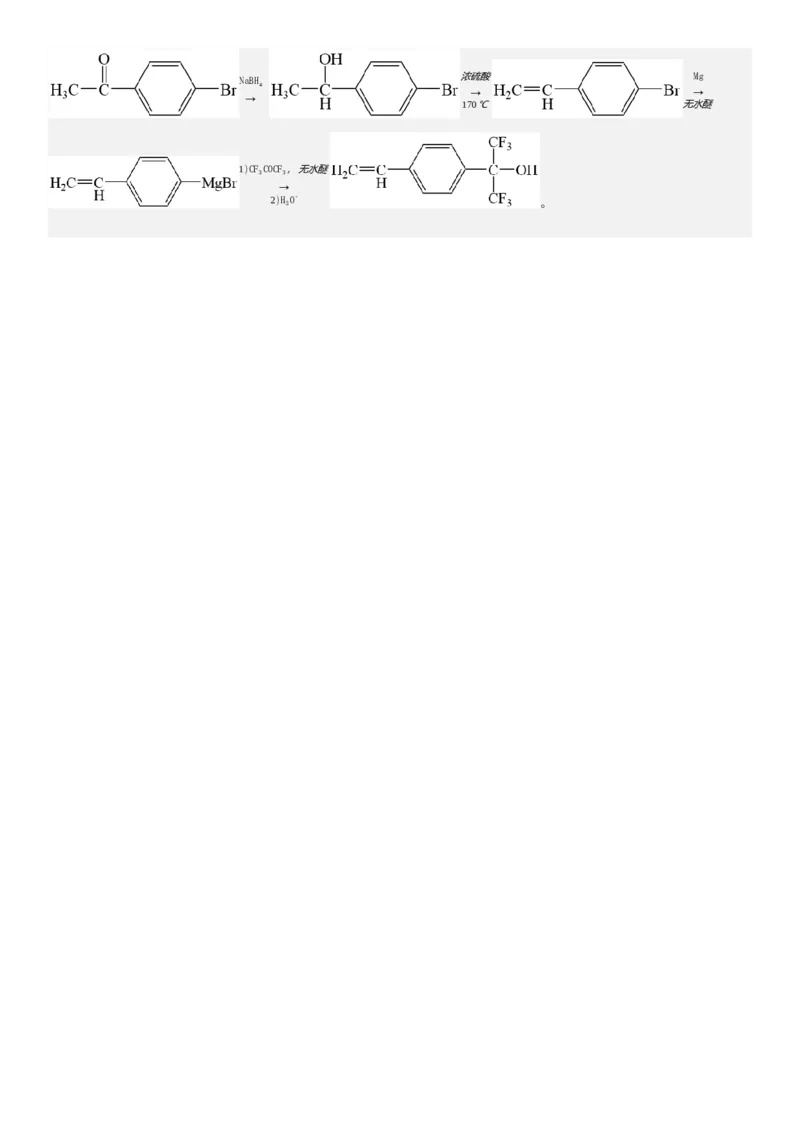
(6)参照上述合成路线,设计以 和不超过3个碳的有机物为原料,制备一种光刻胶单体
的合成路线 (其他试剂任选)。
【答案】(1) 羟基 醛基
(2)1,2-二甲基苯(邻二甲苯)(3)
(4)bc
(5) 4 CH≡C-CH -CH-CH-CH(NH)-C≡CH
2 2 2 2
NaBH 浓硫酸 Mg
4 → →
→
170℃ 无水醚
(6):
1)CF COCF,无水醚
3 3
→
2)H
3
O+
【分析】
有机物A中的羟基在MnO 的催化下与氧气反应生成醛基,有机物B与Ph CCl发生取代反应生成有机物C;有机
2 3
物D中的氨基发生取代反应生成有机物E,D中的氨基变为E中的Cl,E发生已知条件i的两步反应与有机物C作
用最终生成有机物 G;有机物 G 在 MnO 的催化先与氧气反应生成有机物 H,有机物 H 的结构为
2
,有机物H最终发生已知条件i的反应生成目标化合物I。
【详解】(1)根据流程中A和B的结构,A中的含氧官能团为羟基,B中的含氧官能团为醛基。
(2)根据题目中的结构,该结构的化学名称为1,2-二甲基苯(邻二甲苯)。
(3)
根据分析,H的结构简式为 。
(4)根据已知条件ii,RMgX可以与含有活泼氢的化合物(HO、ROH、RNH 、RC≡CH等)发生反应,b中含有
2 2
羟基,c中含有N-H,其H原子为活泼H原子,因此不能用b、c作溶剂。
(5)根据题目所给条件,同分异构体中含有2个碳碳三键,说明结构中不含苯环,结构中不含甲基,说明三键在
物质的两端,同分异构体中又含有手性碳原子,因此,可能的结构有:CH≡C-CH -CH-CH-CH(NH)-C≡CH、
2 2 2 2
CH≡C-CH -CH-CH(NH)-CH -C≡CH、H≡C-CH-CH(CH NH )-CH -CH-C≡CH、H≡C-CH-CH(CH CHNH )-CH -
2 2 2 2 2 2 2 2 2 2 2 2 2 2
C≡CH,共4种。
(6)
根据题目给出的流程,先将原料中的羰基还原为羟基,后利用浓硫酸脱水生成双键,随后将物质与Mg在无水醚中
反应生成中间产物,后再与CFCOCF 在无水醚中反应再水解生成目标化合物,具体的流程如下:
3 3NaBH 浓硫酸 Mg
4 → →
→
170℃ 无水醚
1)CF COCF,无水醚
3 3
→
2)H
3
O+ 。