文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(甘肃卷)
高三化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.中国的文化源远流长,下列文物的主要成分属于金属材料的是
A B C D
凤舞九天木雕 彩绘云凤纹漆圆壶(木板剜凿而成) 战国晚期木觚 青铜尊盘
2.化学与生活密切相关。下列说法中错误的是
A.ClO 既可用于自来水的消毒杀菌,又可除去水中的悬浮杂质
2
B.废旧电池必须回收处理,防止造成汞、镉及铅等重金属污染
C.CaF 与浓HSO 糊状混合物可用于刻蚀玻璃
2 2 4
D.面包师用小苏打作发泡剂烘焙面包是依据碳氢酸钠加热分解反应的原理
3.反应CaC +2H O=Ca(OH) +C H 个可用于制取乙炔。下列说法正确的是
2 2 2 2 2
A.C 的电子式:
B.基态碳原子的价层电子轨道表示式:
C.C H 的空间填充模型:
2 2
D.Ca(OH) 的电离方程式:Ca(OH) Ca2++2OH-
2 2
4.设 为阿伏加德罗常数的值。下列叙述正确的是
A. 溶液中由水电离出的 数目为
B. 溶液中阳离子数目大于更多全科试卷,请关注公众号:高中试卷君
C.天然气碱性燃料电池负极上还原 气体时转移电子数目为
D.常温常压下, ( 为重氢)气体含中子数目为
5.以下实验方案设计,能达到实验目的的是
选项 A B C D
比较Cl、C、Si的 获得纯净的乙 验证溴乙烷发生消去
实验目的 探究铁的吸氧腐蚀
非金属性大小 烷 反应
实验方案
6.下列关于物质结构与性质的说法不正确的是
A.石墨片层中存在大π键,所以沿片层方向容易导电
B.苯甲酸容易形成分子间氢键,形成二聚分子,所以熔沸点较高
C.碳链可以连接很长,但硅链不可以连接很长,因为Si-Si键的键能小于C-C键的键能
D.依据元素周期律,与相同浓度的稀硫酸反应,Pb比Sn反应剧烈
7.制备铁触媒的主要原料—三草酸合铁酸钾 可在光照下发生分解:
。已知含有未成对电子的物质置于外磁场中,
会使磁场强度增大,称其为顺磁性。下列判断错误的是
A. 分子中 键和 键数目比为1:1
B. 中存在极性共价键和非极性共价键
C. 具有顺磁性
D. 与 中碳原子的杂化方式相同
8.为实现实验目的,下列实验操作和现象均正确的是
选项 实验目的 实验操作 实验现象
A 证明金属性 少量金属Na与胆矾隔绝空气加热 有红色固体生成
注射器内气体颜色加
验证压强对化学平衡的影 先将注射器充满 气体,然后将活塞往
B 深,证明加压平衡朝生
响 里推
成 气体的方向移动
验证常温下,溶度积: 常温下,向盛有2滴 溶液 先有白色沉淀生成,后
C
又产生黄色沉淀
的试管中滴加 溶液,再更多全科试卷,请关注公众号:高中试卷君
向其中滴加 溶液
加热浓硫酸、NaCl固体与 固体的混合
D 证明浓硫酸具有强氧化性 有黄绿色气体产生
物
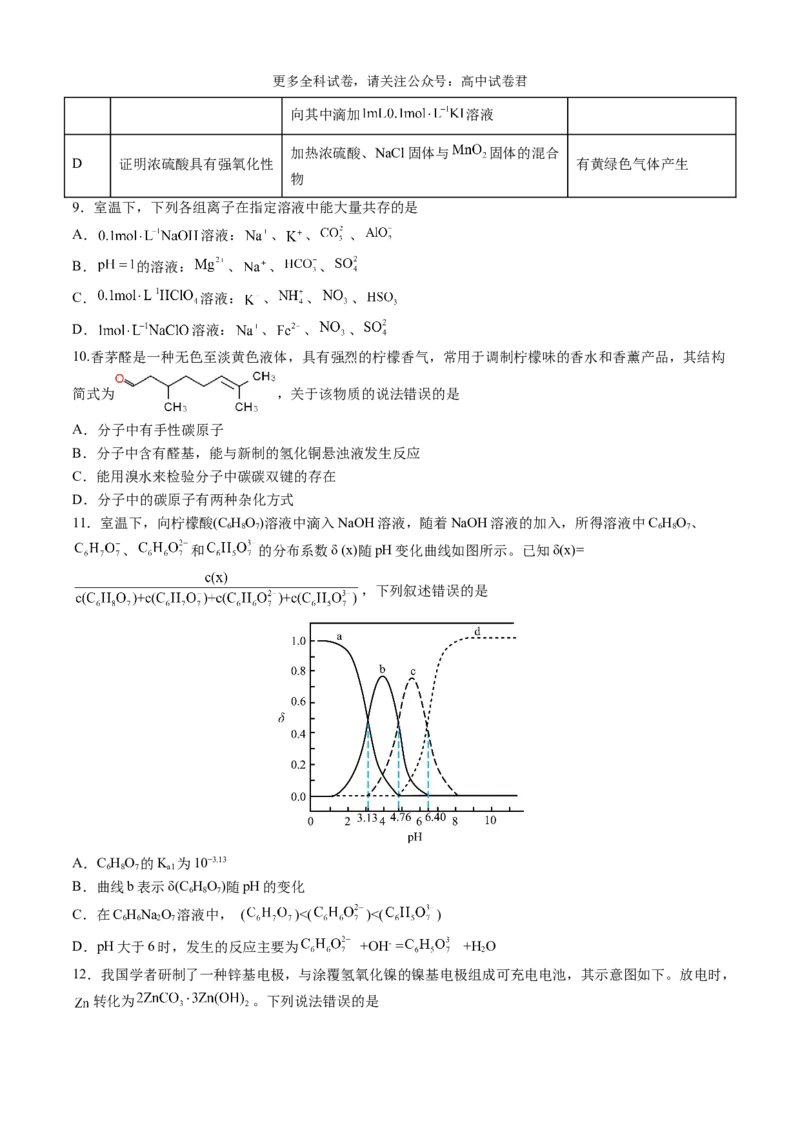
9.室温下,下列各组离子在指定溶液中能大量共存的是
A. 溶液: 、 、 、
B. 的溶液: 、 、 、
C. 溶液: 、 、 、
D. 溶液: 、 、 、
10.香茅醛是一种无色至淡黄色液体,具有强烈的柠檬香气,常用于调制柠檬味的香水和香薰产品,其结构
简式为 ,关于该物质的说法错误的是
A.分子中有手性碳原子
B.分子中含有醛基,能与新制的氢化铜悬浊液发生反应
C.能用溴水来检验分子中碳碳双键的存在
D.分子中的碳原子有两种杂化方式
11.室温下,向柠檬酸(C HO)溶液中滴入NaOH溶液,随着NaOH溶液的加入,所得溶液中C HO、
6 8 7 6 8 7
、 和 的分布系数δ (x)随pH变化曲线如图所示。已知δ(x)=
,下列叙述错误的是
A.C HO 的K 为10−3.13
6 8 7 a1
B.曲线b表示δ(C HO)随pH的变化
6 8 7
C.在C HNaO 溶液中, ( )<( )<( )
6 6 2 7
D.pH大于6时,发生的反应主要为 +OH- = +H O
2
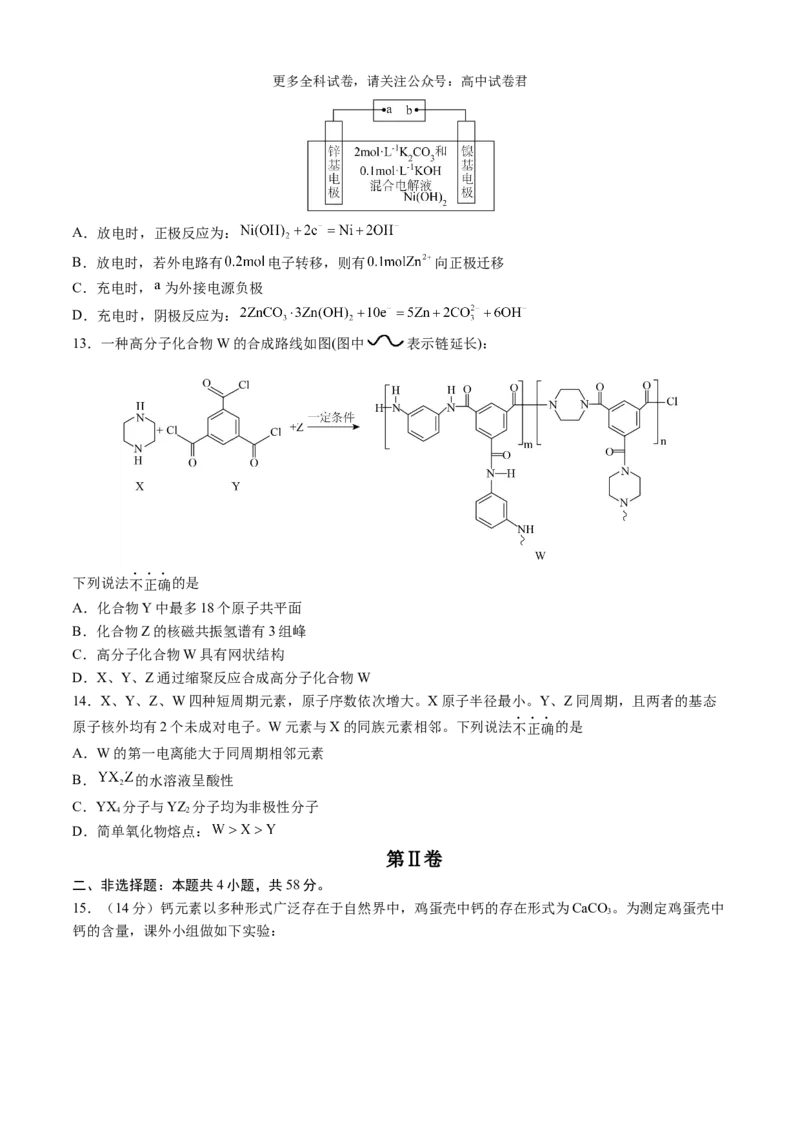
12.我国学者研制了一种锌基电极,与涂覆氢氧化镍的镍基电极组成可充电电池,其示意图如下。放电时,
转化为 。下列说法错误的是更多全科试卷,请关注公众号:高中试卷君
A.放电时,正极反应为:
B.放电时,若外电路有 电子转移,则有 向正极迁移
C.充电时, 为外接电源负极
D.充电时,阴极反应为:
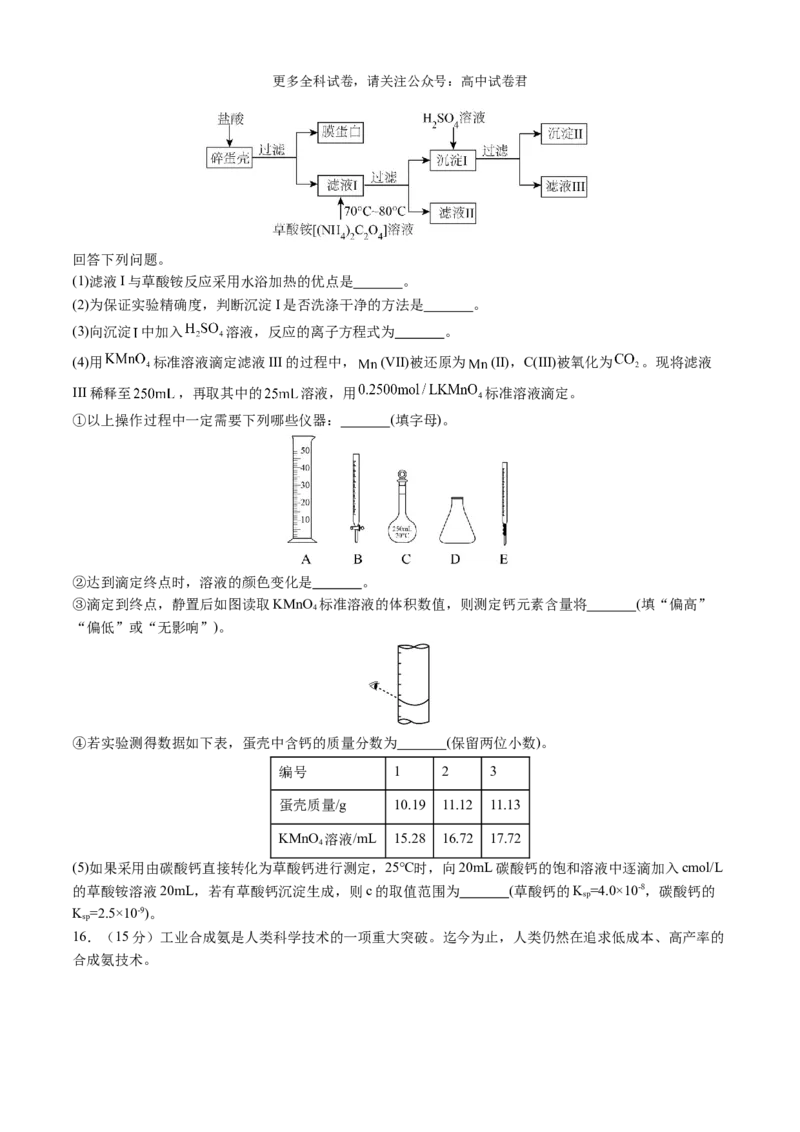
13.一种高分子化合物W的合成路线如图(图中 表示链延长):
下列说法不正确的是
A.化合物Y中最多18个原子共平面
B.化合物Z的核磁共振氢谱有3组峰
C.高分子化合物W具有网状结构
D.X、Y、Z通过缩聚反应合成高分子化合物W
14.X、Y、Z、W四种短周期元素,原子序数依次增大。X原子半径最小。Y、Z同周期,且两者的基态
原子核外均有2个未成对电子。W元素与X的同族元素相邻。下列说法不正确的是
A.W的第一电离能大于同周期相邻元素
B. 的水溶液呈酸性
C.YX 分子与YZ 分子均为非极性分子
4 2
D.简单氧化物熔点:
第Ⅱ卷
二、非选择题:本题共4小题,共58分。
15.(14分)钙元素以多种形式广泛存在于自然界中,鸡蛋壳中钙的存在形式为CaCO 。为测定鸡蛋壳中
3
钙的含量,课外小组做如下实验:更多全科试卷,请关注公众号:高中试卷君
回答下列问题。
(1)滤液I与草酸铵反应采用水浴加热的优点是 。
(2)为保证实验精确度,判断沉淀I是否洗涤干净的方法是 。
(3)向沉淀 中加入 溶液,反应的离子方程式为 。
(4)用 标准溶液滴定滤液III的过程中, (VII)被还原为 (II),C(III)被氧化为 。现将滤液
III稀释至 ,再取其中的 溶液,用 标准溶液滴定。
①以上操作过程中一定需要下列哪些仪器: (填字母)。
②达到滴定终点时,溶液的颜色变化是 。
③滴定到终点,静置后如图读取KMnO 标准溶液的体积数值,则测定钙元素含量将 (填“偏高”
4
“偏低”或“无影响”)。
④若实验测得数据如下表,蛋壳中含钙的质量分数为 (保留两位小数)。
编号 1 2 3
蛋壳质量/g 10.19 11.12 11.13
KMnO 溶液/mL 15.28 16.72 17.72
4
(5)如果采用由碳酸钙直接转化为草酸钙进行测定,25℃时,向20mL碳酸钙的饱和溶液中逐滴加入cmol/L
的草酸铵溶液20mL,若有草酸钙沉淀生成,则c的取值范围为 (草酸钙的K =4.0×10-8,碳酸钙的
sp
K =2.5×10-9)。
sp
16.(15分)工业合成氨是人类科学技术的一项重大突破。迄今为止,人类仍然在追求低成本、高产率的
合成氨技术。更多全科试卷,请关注公众号:高中试卷君
(1)已知 时, 的燃烧热 ;
。
①某种新型储氢材料的晶胞如图1所示,八面体中心为某价态铁的离子,顶点均为 配体;四面体中心
为硼原子,顶点均为氢原子。该化合物的化学式为 ,化合物中铁的电子排布式为 。
②有人提出利用 反应制备 的思路。请结合有关数据说明该反应
难以实现的原因: 。
(2)经过理论计算并结合实验测量得出铁触媒表面合成氨反应全过程的能量变化如图2所示。其中(ad)表示
吸附在催化剂表面。我国科学家提出了一种使用双温双控催化剂提高合成氨产率的新方法。该催化剂是在
纳米铁表面复合少量具有光学活性的 ,通过光辐射产生温差(如体系温度为495℃时, 的温度能
达到547℃,而 表面为415℃)。其催化合成氨机理如图3所示。
①500℃下 的平衡浓度较400℃低的原因是 。
②与传统的催化合成氨(铁触媒、400~500℃)相比, 双催化剂双温催化合成氨更具优势的原
因是 。
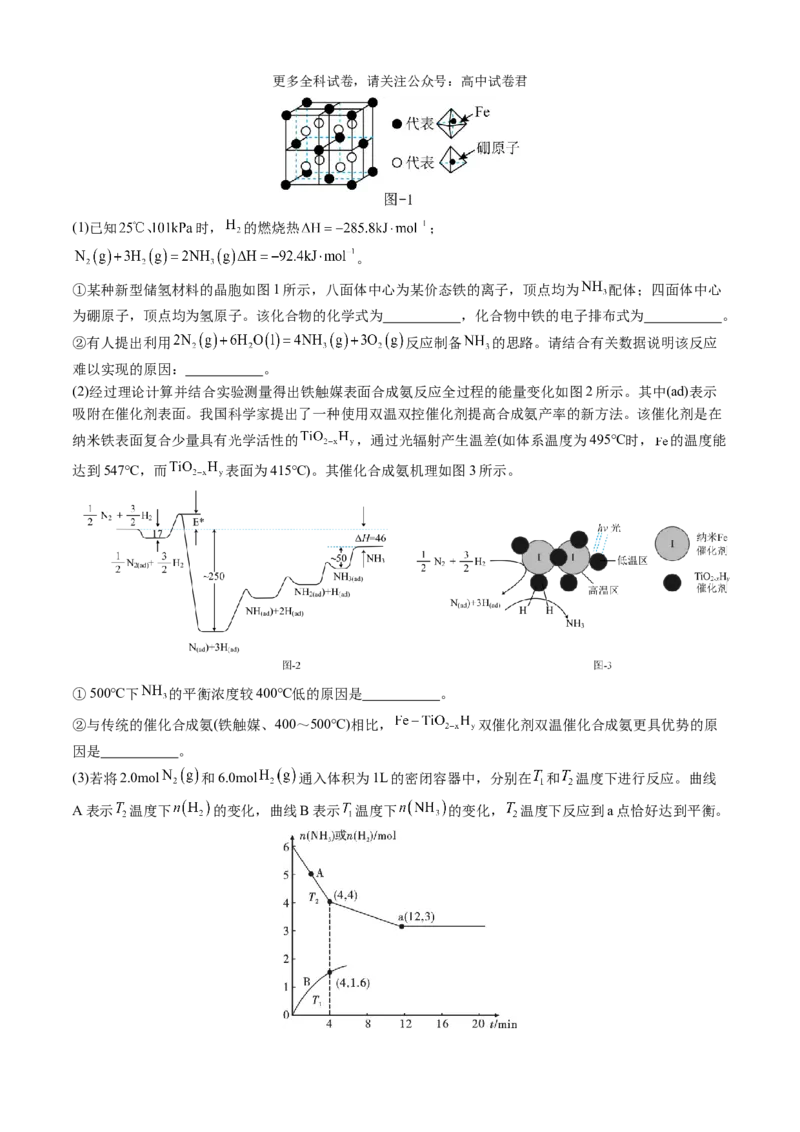
(3)若将2.0mol 和6.0mol 通入体积为1L的密闭容器中,分别在 和 温度下进行反应。曲线
A表示 温度下 的变化,曲线B表示 温度下 的变化, 温度下反应到a点恰好达到平衡。更多全科试卷,请关注公众号:高中试卷君
①温度 (填“>”、“<”或“=”,下同) 。 温度下恰好平衡时,曲线B上的点为 ,
则m 12,n 3。
② 温度下,若某时刻容器内气体的压强为起始时的80%,则此时 (填“>”、“<”或“=”)
。
③计算 温度下,Kc= 。
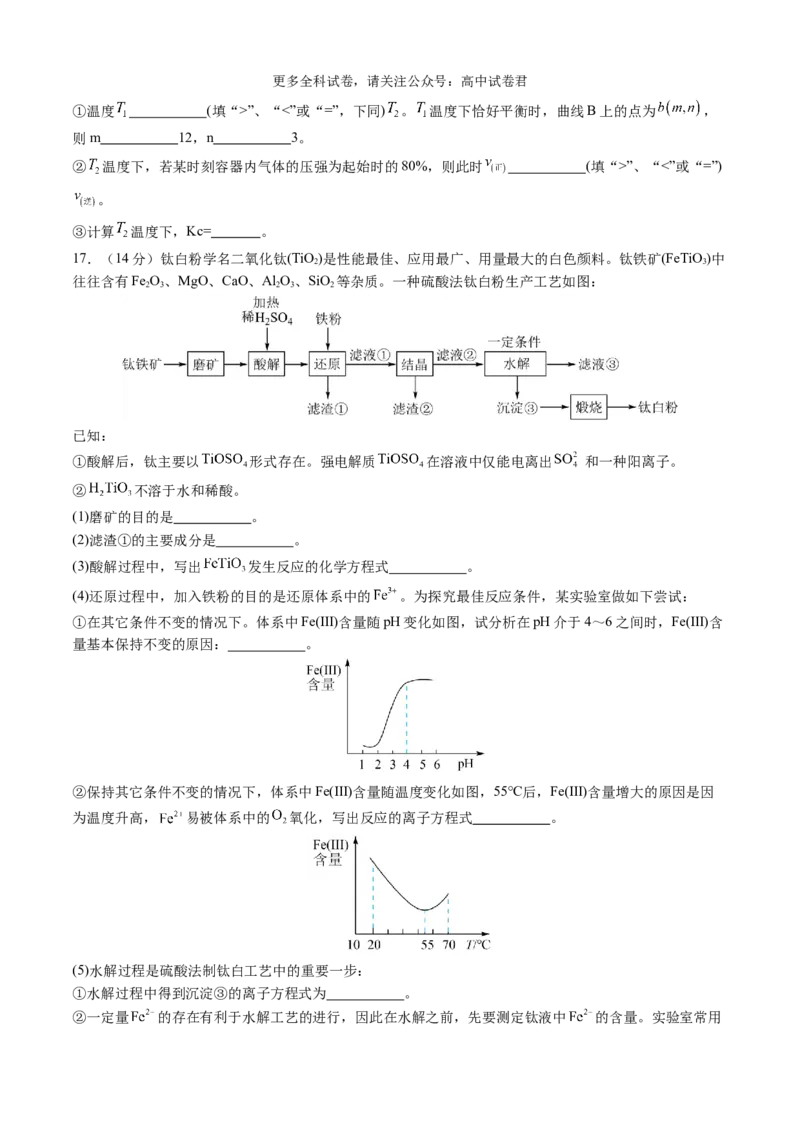
17.(14分)钛白粉学名二氧化钛(TiO)是性能最佳、应用最广、用量最大的白色颜料。钛铁矿(FeTiO)中
2 3
往往含有Fe O、MgO、CaO、Al O、SiO 等杂质。一种硫酸法钛白粉生产工艺如图:
2 3 2 3 2
已知:
①酸解后,钛主要以 形式存在。强电解质 在溶液中仅能电离出 和一种阳离子。
② 不溶于水和稀酸。
(1)磨矿的目的是 。
(2)滤渣①的主要成分是 。
(3)酸解过程中,写出 发生反应的化学方程式 。
(4)还原过程中,加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做如下尝试:
①在其它条件不变的情况下。体系中Fe(Ⅲ)含量随pH变化如图,试分析在pH介于4~6之间时,Fe(Ⅲ)含
量基本保持不变的原因: 。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图,55℃后,Fe(Ⅲ)含量增大的原因是因
为温度升高, 易被体系中的 氧化,写出反应的离子方程式 。
(5)水解过程是硫酸法制钛白工艺中的重要一步:
①水解过程中得到沉淀③的离子方程式为 。
②一定量 的存在有利于水解工艺的进行,因此在水解之前,先要测定钛液中 的含量。实验室常用更多全科试卷,请关注公众号:高中试卷君
酸性高锰酸钾溶液进行滴定,用离子方程式表示其原理 。
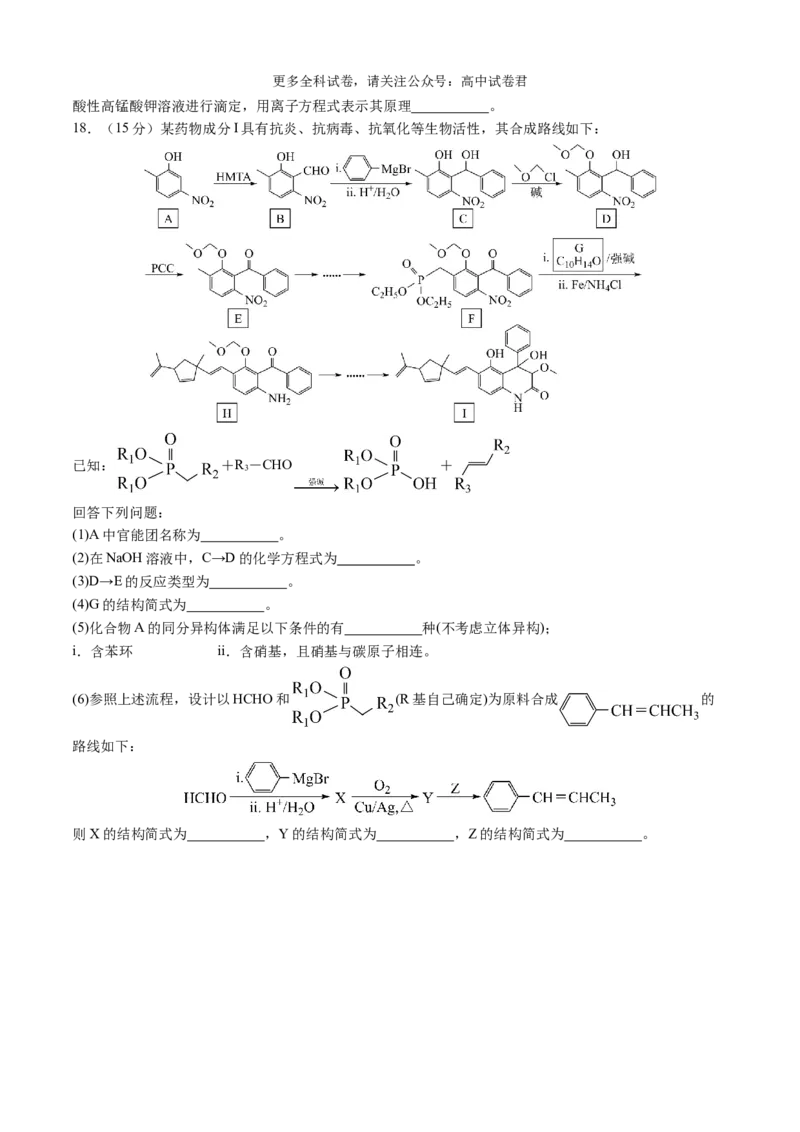
18.(15分)某药物成分I具有抗炎、抗病毒、抗氧化等生物活性,其合成路线如下:
已知: +R -CHO +
3
回答下列问题:
(1)A中官能团名称为 。
(2)在NaOH溶液中,C→D的化学方程式为 。
(3)D→E的反应类型为 。
(4)G的结构简式为 。
(5)化合物A的同分异构体满足以下条件的有 种(不考虑立体异构);
i.含苯环 ii.含硝基,且硝基与碳原子相连。
(6)参照上述流程,设计以HCHO和 (R基自己确定)为原料合成 的
路线如下:
则X的结构简式为 ,Y的结构简式为 ,Z的结构简式为 。