文档内容
更多全科试卷,请关注公众号:高中试卷君
2024 年 1 月“九省联考”考后提升卷(贵州卷)
高三化学
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ca 40 Zn 65
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学创造美好生活,下列说法有关物质的性质与用途正确的是
A.电子跃迁到激发态过程中释放能量产生紫色光—钾盐可用作紫色烟花的原料
B.不锈钢具有高强度、高密度的性质,可用作太空探测器的结构材料
C. 具有较强的还原性—可以在葡萄酒中添加 作为抗氧化剂食品保鲜
D.SiC硬度很大,可用作砂轮的磨料,是一种新型硅酸盐材料
2.下列化学用语表述错误的是
A.HClO的电子式:
B.中子数为10的氧原子:
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
3.设N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.100mL 1mol/L NH Cl溶液中含有阳离子的数目大于0.1N
4 A
B.0.1mol的11B中,含有0.6N 个电子
A
C.25℃时,pH=13的Ba(OH) 溶液中含有氢氧根离子数为0.1N
2 A更多全科试卷,请关注公众号:高中试卷君
D.标准状况下,5.6L CO 中含有的共用电子对数为0.5 N
2 A
4.下列实验仪器或装置能达到实验目的的是
A.制备乙酸乙酯 B.制取并收集 C.分离苯和溴苯 D.收集
A.A B.B C.C D.D
5.下列实验操作对应的离子方程式错误是
A.电解饱和MgCl 溶液:2Cl-+2H O Cl ↑+H ↑+2OH-
2 2 2 2
B.向Al (SO ) 溶液中滴入NaHCO 溶液:Al3++3 =Al(OH) ↓+3CO ↑
2 4 3 3 3 2
C.向Na S O 溶液中滴入稀H SO 溶液:2H++ =S↓+SO ↑+H O
2 2 3 2 4 2 2
D.用Na CO 溶液处理水垢中的CaSO : (aq)+CaSO (s) CaCO (s)+ (aq)
2 3 4 4 3
⇌
6.某有机物结构简式如图所示。下列说法正确的是
A.该有机物分子中所有原子均在同一平面上
B.该有机物的分子式为
C.分子中碳原子的杂化方式为 、
D.该有机物能发生加成反应、氧化反应、消去反应
7.劳动创造幸福是中华民族的优良传统,下列劳动项目与所涉及的化学知识关联错误的是更多全科试卷,请关注公众号:高中试卷君
选
劳动项目 化学知识
项
A 科学研究:用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 工厂生产:接触法制硫酸 涉及氧化还原反应
C 社区服务:演示用泡沫灭火器灭火 盐酸与小苏打反应产生大量二氧化碳
D 家务劳动:用“84”消毒液漂洗衣服 “84”消毒液具有漂白性
A.A B.B C.C D.D
8.短周期主族元素R、X、Y和Z在周期表中相对位置如图所示,其中R的氧化物可形成酸雨。下列说法错
误的是
A.最高价氧化物对应水化物的酸性:Z>Y>X
B.R的气态氢化物能使湿润的红色石蕊试纸变蓝
C.化合物Y Z 中只含极性共价键
2 2
D.X、Z可形成各原子最外层上均达到8电子结构的XZ 分子
4
9.某有机物的结构简式如图所示。下列关于该有机物分子的说法不正确的是
A.所含元素中电负性最小的是
B. 的键能大于 的键能
C.所有 原子采用 杂化
D.σ键与π键数目之比为
10.完成下列实验所选用的试剂和操作、现象和结论均正确的是
选
实验 试剂和操作 现象和结论
项
A 检验某有机物是否 取少许该有机物滴入盛有银氨溶 产生光亮的银镜,该有机物为醛类更多全科试卷,请关注公众号:高中试卷君
为醛类 液的试管中水浴加热
检验过氧化钠溶于
将过量过氧化钠投入滴有酚酞溶 溶液最终变为红色,过氧化钠与水反应生
B 水是否生成碱性物
液的水中 成碱性物质
质
向浓度均为0.1 mol·L 的
比较 和 先看到有蓝色沉淀生成,
C 和 的混合溶液中
的溶度积
逐滴加入NaOH溶液
检验苯中是否含有
D 向溶液中滴加少量浓溴水、振荡 无白色沉淀,溶液中无苯酚
苯酚
A.A B.B C.C D.D
11.实验室由炼钢污泥(主要成分为铁的氧化物)制备软磁性材料 ,主要实验流程如下:
下列有关说法错误的是
A.可通过适当延长“酸浸”时间来提高铁元素的浸出率
B.“还原”过程中除生成Fe2+外,还可能有H 生成
2
C.“除杂”过程中若溶液pH偏低可导致CaF 沉淀不完全
2
D.“沉铁”时生成的沉淀为FeCO ,再焙烧得到 时需要隔绝空气
3
12.在25℃时对氨水进行如下操作,正确的是
A.若向氨水中加少量硫酸铵固体,则溶液中 将增大
B.若向氨水中加稀硫酸,使氨水恰好被中和,所得溶液
C.向氨水中加稀硫酸至溶液的 ,此时溶液 ,则
D.将 的氨水和 的盐酸等体积混合,所得溶液
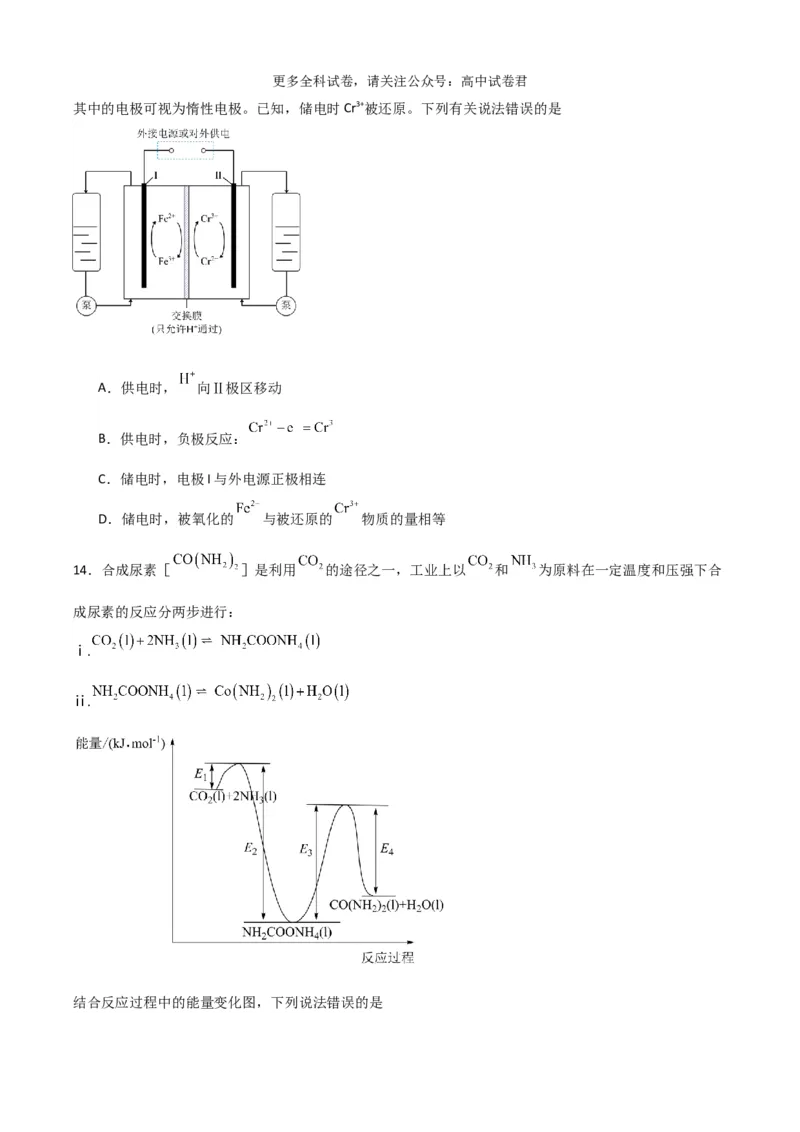
13.2023年2月,全球最大容量铁-铬液流储能电池在内蒙古自治区成功试运行。该电池示意图如图所示,更多全科试卷,请关注公众号:高中试卷君
其中的电极可视为惰性电极。已知,储电时Cr3+被还原。下列有关说法错误的是
A.供电时, 向Ⅱ极区移动
B.供电时,负极反应:
C.储电时,电极I与外电源正极相连
D.储电时,被氧化的 与被还原的 物质的量相等
14.合成尿素[ ]是利用 的途径之一,工业上以 和 为原料在一定温度和压强下合
成尿素的反应分两步进行:
ⅰ.
ⅱ.
结合反应过程中的能量变化图,下列说法错误的是更多全科试卷,请关注公众号:高中试卷君
A.活化能:反应ⅰ<反应ⅱ
B.反应ⅰ为放热反应,反应ⅱ为吸热反应
C.增大 的投料比,二氧化碳的平衡转化率增大
D. 的
第Ⅱ卷
二、非选择题:本题共4小题,共58分。
15.Na S又称臭碱、臭苏打,在生产、生活中有广泛应用。某化学兴趣小组在实验室制备、提纯硫化钠并
2
探究其性质,测定硫化钠产品的纯度。
实验(一)制备并提纯硫化钠。
该化学兴趣小组在实验室模拟工业用煤粉还原法制备硫化钠,将芒硝(Na SO ·10H O)与过量的煤粉混合于
2 4 2
800 ~ 1100°C高温下煅烧还原,生成物经冷却后用稀碱液热溶解、过滤,将滤液进行浓缩,再进行抽滤、
洗涤、干燥,制得硫化钠产品。
(1)写出“高温还原”过程中的主要化学方程式: 。
(2)抽滤又称减压过滤,相比普通过滤,抽滤的主要优点是 。(答一条即可)
实验(二)探究硫化钠的性质。
(3)为了探究Na S的还原性,该小组按如图装置进行实验。
2
接通K,发现电流表指针发生偏转,左侧烧杯中溶液颜色逐渐变浅。实验完毕后,该小组查阅资料后猜测,
S2-被氧化为 。设计实验验证:取出少量右侧烧杯中溶液于试管中, ,则该猜测成立。写
出正极的电极反应式 。
实验(三)测定Na S·xH O产品纯度。
2 2更多全科试卷,请关注公众号:高中试卷君
称取wg产品溶于水,配制成250mL溶液,准确量取25. 00mL溶液于锥形瓶中,加入V mLc mol·L-1I 溶液
1 1 2
(过量),过滤,滴几滴淀粉溶液,用c mol·L-1 Na S O 标准溶液滴定至终点,消耗标准溶液V mL。
2 2 2 3 2
(4)滴定终点的现象是 。选择 (填“酸”或“碱”)式滴定管量取I 溶液。
2
(5)滴定反应:Na S+I =2NaI+S,I +2Na S O = Na S O + 2NaI。该产品含Na S·xH O的质量分数为
2 2 2 2 2 3 2 4 6 2 2
(用含x、 c 、c 、V 、V 、w的代数式表示)。假设其他操作都正确,滴定终点时俯视读数,测定结果
1 2 1 2
(填“偏高”“偏低”或“无影响”)。
16.氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓 、铁酸锌 、
]制备GaN的工艺流程如下:
已知:
①Ga与Al同主族,化学性质相似。
②常温下, , , 。
③ 、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
反萃取率/%
盐酸浓度/mol/L
2 86.9 9.4
4 69.1 52.1
6 17.5 71.3
回答下列问题:
(1)“酸浸”时能提高反应速率的措施有 (答1条即可),“酸浸”时 发生反应的离子
方程式为 。“酸溶”所得滤渣的主要成分是(填化学式)。
(2)“酸浸”所得浸出液中 、 浓度分别为 、 。常温下,为尽可能多地提取 并更多全科试卷,请关注公众号:高中试卷君
确保不混入 ,用CaO“调pH”时须不能大于 (假设调pH时溶液体积不变)。
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a= ,b= (选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是 (用离子方程式表
示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的 与 在高温下反应可制得GaN,同时生成另一
种产物,该反应化学方程式为 。
(6)①GaN的熔点为1700℃, 的熔点为77.9℃,推测它们的晶体类型依次为 、
。
②基态Ga原子的价层电子排布图为 。
GaN晶体的一种立方晶胞如图所示。该晶胞边长为anm,GaN的式量为Mr,则该晶体密度为
g/cm3(列出计算式, 为阿伏加德罗常数的值)。
17.工业上先将金红石 (TiO )转化为 ,然后可制得在医疗等领域具有重要用途的钛(Ti)。按要求回答
2
下列问题。
(1)钛的价层电子排布式为 ;预测钛元素的最高化合价为 。
(2)已知在一定条件下如下反应的热化学方程式及平衡常数:
ⅰ. ;
ⅱ. ;
ⅲ.碳氯化法: ;
① ; (用含 的代数式表示)。
②反应ⅲ自发进行的条件为 (填“低温”“高温”或“任意温度”)。更多全科试卷,请关注公众号:高中试卷君
③在反应ⅰ中加入石墨制备 ,用平衡移动原理分析其目的: 。
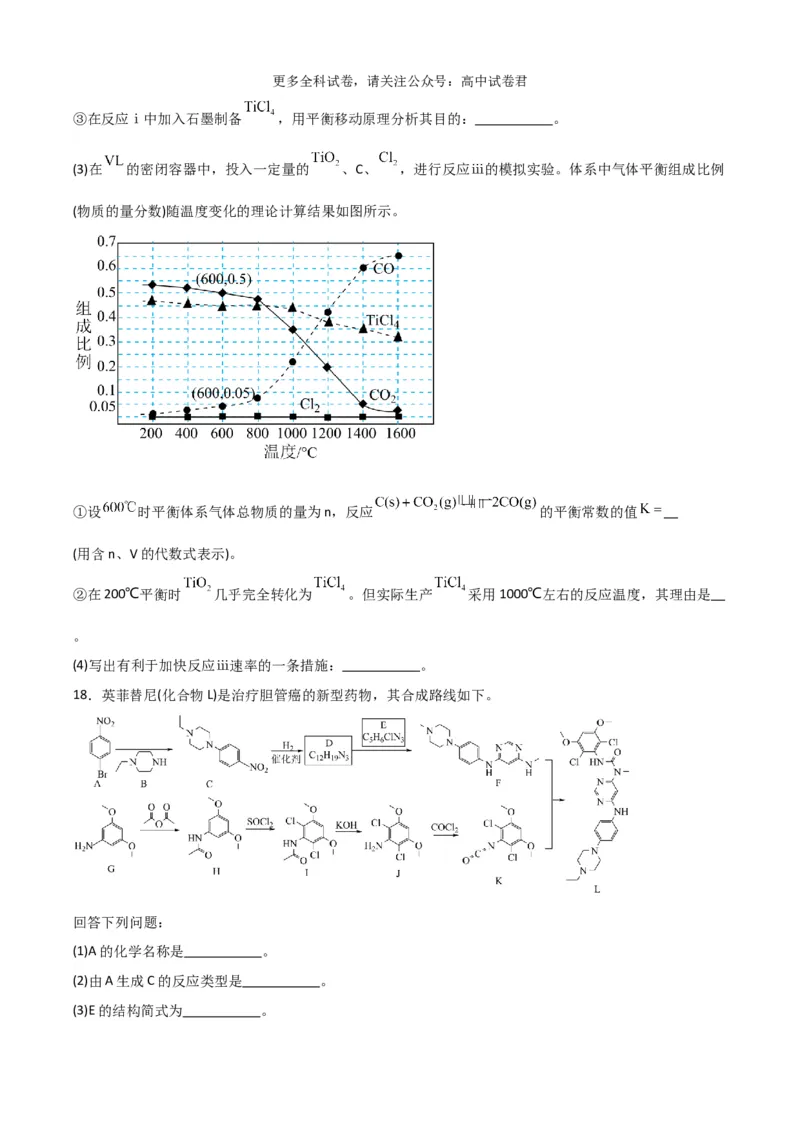
(3)在 的密闭容器中,投入一定量的 、C、 ,进行反应ⅲ的模拟实验。体系中气体平衡组成比例
(物质的量分数)随温度变化的理论计算结果如图所示。
①设 时平衡体系气体总物质的量为n,反应 的平衡常数的值
(用含n、V的代数式表示)。
②在200℃平衡时 几乎完全转化为 。但实际生产 采用1000℃左右的反应温度,其理由是
。
(4)写出有利于加快反应ⅲ速率的一条措施: 。
18.英菲替尼(化合物L)是治疗胆管癌的新型药物,其合成路线如下。
回答下列问题:
(1)A的化学名称是 。
(2)由A生成C的反应类型是 。
(3)E的结构简式为 。更多全科试卷,请关注公众号:高中试卷君
(4)由G→J的转化过程可知,G转化为H的目的是
(5)符合下列条件的B的同分异构体共有 种,其中一种的结构简式为 。
①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)L中氮原子的杂化方式为 。
(7)1,3-二苯基脲( )是某些药物分子的重要结构单元。参照上述合成路线,写出以
苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。