文档内容
人教版(2019)高一 第一章第二节 离子反应 第2课时 离
子反应及其发生条件
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.在强酸性或强碱性溶液中,都能共存的离子组是
A.K+、Na+、SO 、CO B.NH 、Cu2+、Cl-、NO
C.Ba2+、Na+、NO 、SO D.Ba2+、K+、Cl-、NO
2.下列离子方程式书写不正确的是
A.FeCl 溶液腐蚀铜印刷电路板:2Fe3++Cu=2Fe2++Cu2+
3
B.盛放NaOH溶液的试剂瓶不能使用玻璃塞:SiO+2OH-=SiO 2-+HO
2 3 2
C.在Ca(HCO ) 溶液中滴加NaOH溶液至沉淀不再增加:Ca2++HCO-+OH-=
3 2 3
CaCO ↓+H O
3 2
D.漂白粉溶液中通入少量SO :SO +Ca2++2ClO-+H O=CaSO↓+2HClO
2 2 2 3
3.下列离子方程式书写正确的是
A.稀HSO 与铁粉反应:2Fe+6H+=2Fe3++3H ↑
2 4 2
B.氧化铜与稀硫酸反应:2H++O2-=H O
2
C.稀盐酸滴入澄清石灰水中:Ca(OH) +2H+=Ca2++2H O
2 2
D.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag
4.下列各组中的离子能大量共存的是( )
A.H+、Na+、NO -、SO 2- B.NH +、K+、Cl-、OH-
3 3 4
C.Fe3+、NH +、NO -、SO 2- D.K+、Fe3+、SO 2-、Cl-
4 3 4 3
5.离子方程式:CO2-+2H+=CO ↑+H O可表示的意义是( )
3 2 2
A.一切碳酸盐和盐酸反应生成CO 和水
2
B.碳酸盐和强酸反应生成CO 和水
2
C.可溶性碳酸盐和一切强酸反应生成CO 和水
2
D.可溶性酸式碳酸盐和一切强酸反应生成CO 和水
2
6.下列过程中的化学反应,相应的离子方程式正确的是
A.NH HCO 溶液与足量KOH溶液混合: HCO +OH-= +H O
4 3 2
B.用Cu作电极,电解NaOH溶液的阳极反应: 4OH--4e-=2H O+O↑
2 2C.向NaSO 溶液中滴加稀硫酸: +2H+=S↓+ SO ↑+H O
2 2 3 2 2
D.用碳酸钠溶液处理锅炉水垢中的CaSO:Ca2++ =CaCO
4 3
7.下列反应的离子方程式错误的是
A.小苏打与盐酸反应HCO +H+=CO ↑+H O
2 2
B.碳酸氢钙与足量氢氧化钠溶液反应Ca2++2HCO +OH-=CaCO ↓+H O+CO
3 2
C.钠与水反应 2Na+2HO=2Na++2OH-+H ↑
2 2
D.氢氧化钠与三氯化铁溶液反应 Fe3++3OH-=Fe(OH) ↓
3
8.下列离子方程式书写正确的是
A.碳酸钙与盐酸反应:CO2-+2H+=CO↑+H O
3 2 2
B.向氢氧化钠溶液中通入过量二氧化碳:OH-+ CO = HCO -
2 3
C.澄清石灰水与稀盐酸反应:Ca (OH) + 2H+ = Ca2++ 2H O
2 2
D.铁钉放入硫酸铜溶液中:Fe+3Cu2+=2Fe3++3Cu
9.下列指定反应的离子方程式正确的是
A.将铜插入稀硝酸中:Cu+4H++2NO =Cu2++2NO↑+H O
2 2
B.向NaSiO 溶液中滴加稀盐酸:NaSiO+2H+=H SiO↓+2Na+
2 3 2 3 2 3
C.向Al (SO ) 溶液中加入过量氨水:Al3++4OH-=AlO +2H O
2 4 3 2
D.向Fe (SO ) 溶液中加入过量铁粉:2Fe3++Fe=3Fe2+
2 4 3
10.下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是
A.Cu(OH) 和盐酸;Mg(OH) 和HSO B.BaCl 和NaSO ;Ba(OH) 和CuSO
2 2 2 4 2 2 4 2 4
C.NaHCO 和HSO ;NaCO 和NaHSO D.石灰石与硝酸:碳酸钙与盐酸
3 2 4 2 3 4
11.常温下,下列各组离子在指定溶液中能大量共存的是
A.含有大量 的溶液中: 、 、 、
B.滴加酚酞试剂显红色的溶液中: 、 、 、
C.无色透明的溶液中: 、 、 、
D.加入镁粉产生 的溶液中: 、 、 、
12.室温下,下列各组离子在指定溶液中能大量共存的是
试卷第2页,共3页A.0.1 mol·L−1NaOH溶液:Na+、K+、 、
B.0.1 mol·L−1FeCl 溶液:K+、Mg2+、 、
2
C.0.1 mol·L−1KCO 溶液:Na+、Ba2+、Cl−、OH−
2 3
D.0.1 mol·L−1HSO 溶液:K+、 、 、
2 4
13.在某溶液中滴加酚酞试剂呈红色。下列离子在该溶液中能大量存在的是( )
A.Fe3+ B.Na+ C.H+ D.Al3+
14.在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO 2—
4
B.含有0.1 mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO —
3
C.含有0.1 mol·L-1Ca2+的溶液中:Na+、K+、CO2—、Cl-
3
D.室温下,pH=1的溶液中:Na+、Fe3+、NO —、SO 2—
3 4
15.下列无色透明的碱性溶液中能大量共存的离子是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
16.在下列给定条件的溶液中,一定能大量共存的离子是
A.滴加甲基橙试剂显红色的溶液中:Na +、Fe 2+、Cl-、NO -
3
B.由水电离的c(H+)=1.0×10-13 mol·L﹣1的溶液中:K +、Na +、AlO-、CO2-
2 3
C.常温下,pH="7" 溶液中:NH +、Al3+、NO -、CO2-
4 3 3
D.K /c(H+)=0.1 mol·L-1的溶液:Na+、K+、SiO2-、NO -
W 3 3
17.无色透明的强酸性溶液中,能大量共存的离子组是
A.CO2-、Br-、K+、Na+ B.NH +、SO 2-、Cl-、NO -
3 4 4 3
C.K+、Na+、ClO-、Cl- D.K+、SO 2-、HCO -、Mg2+
4 3
18.配制某植物用营养液中含 、 、 和M共4种离子,它们的微粒数之比
为4:3:3:1(提示:溶液中阴阳离子电荷代数和为零),则M有可能为以下四种的哪
一种
A. B. C. D.
19.有甲、乙、丙三种试液,在氢氧化钡溶液中加入甲有白色沉淀生成,在沉淀中加
入乙,沉淀溶解并产生气泡,最后再加入丙又产生白色沉淀。则甲、乙、丙依次可能
是A.KCO、HCl、CaCl B.NaCO、HNO 、MgSO
2 3 2 2 3 3. 4
C.NaCO 、HNO、AgNO D.HSO 、NaCO、AgNO
2 3. 3 3 2 4. 2 3 3
二、元素或物质推断题
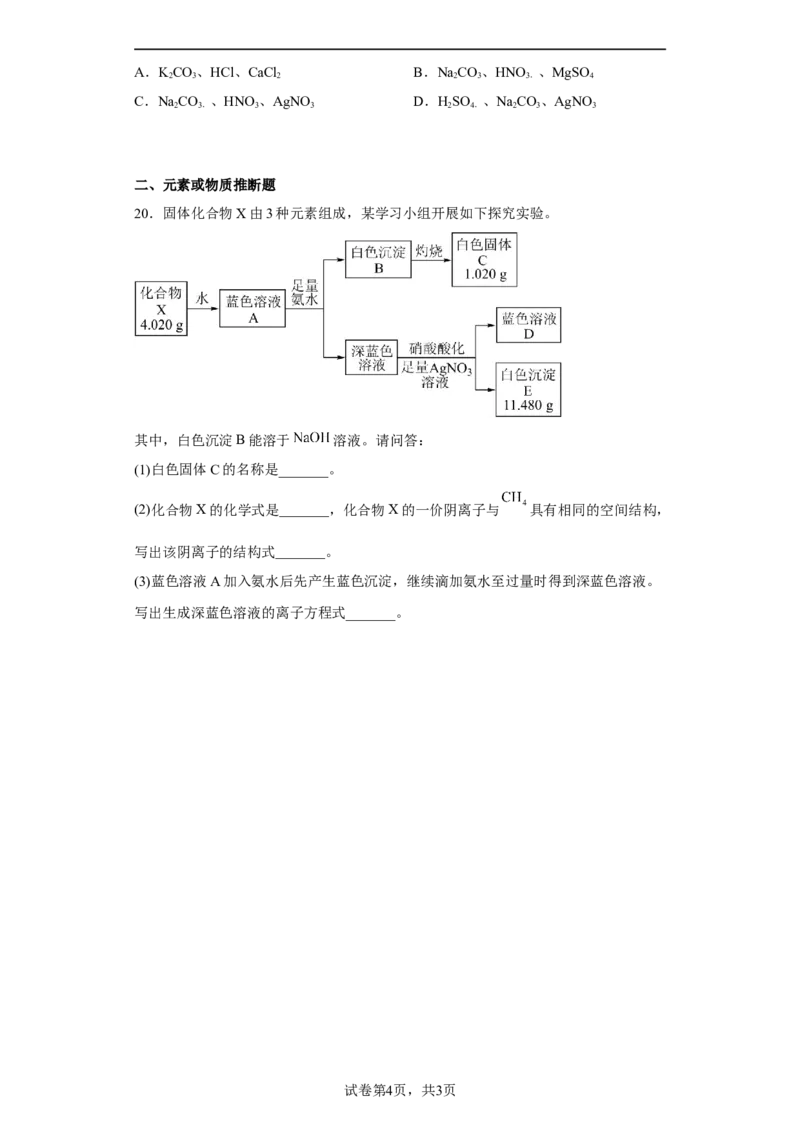
20.固体化合物X由3种元素组成,某学习小组开展如下探究实验。
其中,白色沉淀B能溶于 溶液。请问答:
(1)白色固体C的名称是_______。
(2)化合物X的化学式是_______,化合物X的一价阴离子与 具有相同的空间结构,
写出该阴离子的结构式_______。
(3)蓝色溶液A加入氨水后先产生蓝色沉淀,继续滴加氨水至过量时得到深蓝色溶液。
写出生成深蓝色溶液的离子方程式_______。
试卷第4页,共3页参考答案:
1.D
【详解】A.强酸性条件下,CO 和H+反应生成二氧化碳,不能大量共存,A错误;
B.碱性条件下,Cu2+和OH-反应生成沉淀 , NH 和OH-反应生成 ,B
错误;
C. Ba2+和SO 反应生成白色沉淀,C错误;
D. Ba2+、K+、Cl-、NO 强酸性或强碱性溶液中,都能共存,D正确;
故答案选D。
2.D
【详解】A. FeCl 溶液腐蚀铜印刷电路板:2Fe3++Cu=2Fe2++Cu2+,A正确;
3
B. 盛放NaOH溶液的试剂瓶不能使用玻璃塞:SiO+2OH-=SiO 2-+HO,B正确;
2 3 2
C. 在Ca(HCO ) 溶液中滴加NaOH溶液至沉淀不再增加:Ca2++HCO-+OH-=
3 2 3
CaCO ↓+H O,C正确;
3 2
D. 漂白粉溶液中通入少量SO ,因为漂白粉具有强氧化性,所以产物中不能生成亚硫酸钙,
2
D错误。
故选D。
3.D
【详解】A.稀HSO 与铁粉反应时发生反应的离子方程式为Fe+2H+=Fe2++H ↑,故A错误;
2 4 2
B.氧化铜与稀硫酸反应时发生反应的离子方程式为2H++CuO=Cu2++H O,故B错误;
2
C.稀盐酸滴入澄清石灰水中时发生反应的离子方程式为OH-+H+=H O,故C错误;
2
D.铜片插入硝酸银溶液中时发生反应的离子方程式为Cu+2Ag+=Cu2++2Ag,故D正确;
故答案为D。
4.C
【详解】A. H+与NO -在一起相当于硝酸,具有强氧化性,能把SO 2-氧化成SO 2-,故A错
3 3 4
误;
B. NH +与OH-反应生成一水合氨,不能大量共存,故B错误;
4
C. Fe3+、NH +、NO -、SO 2-能大量共存,故C正确;
4 3 4
D. Fe3+与SO 2-能发生氧化还原反应,不能大量共存,故D错误;
3
故选C。【点睛】能够发生反应的离子就不能共存,不能发生反应的离子才可以共存。
1、在溶液中某些离子间能互相反应生成难溶性物质时,这些离子就不能大量共存。
2、离子间能结合生成难电离物质时,则这些离子不能大量共存。
3、离子间能结合生成挥发性物质时,则这些离子不能大量共存。
4、离子之间能发生氧化还原反应时,则这些离子不能大量共存。
5、还应注意题目是否给出溶液的酸碱性,是否给定溶液是无色的。
5.C
【分析】难溶性碳酸盐在离子反应中保留化学式,酸式碳酸盐中酸式酸根离子不可拆分,
以此来解答。
【详解】可溶性碳酸盐和强酸反应生成CO 和水的离子反应用CO2-+2H+=CO ↑+H O表示,
2 3 2 2
而难溶性碳酸盐在离子反应中保留化学式,酸式碳酸盐中酸式酸根离子不可拆分,显然只
有C符合,故答案选C。
6.C
【详解】A.盐NH HCO 电离产生的 、 都与KOH反应,KOH足量时离子方程
4 3
式应该为: + +2OH-=NH·H O+ +H O,A错误;
3 2 2
B.Cu是活性电极,用Cu作阳极,Cu失去电子变为Cu2+,与溶液中的OH-结合形成
Cu(OH) ,则电解NaOH溶液的阳极的电极反应式:Cu-2e-+2OH-=Cu(OH) ,B错误;
2 2
C.向NaSO 溶液中滴加稀硫酸,反应产生NaCl、S、SO 、HO,反应的离子方程式为:
2 2 3 2 2
+2H+=S↓+ SO ↑+H O,C正确;
2 2
D.CaSO 微溶于水,主要以固体存在,其与NaCO 发生沉淀的转化,反应的离子方程式
4 2 3
为:CaSO+ =CaCO + ,D错误;
4 3
故合理选项是C。
7.B
【详解】A.小苏打是易溶性盐,盐酸是易溶性强酸,拆分成离子,但 是弱酸的酸式
酸根,不能拆分,方程式写法无误,A正确;
B.方程式中氢原子不守恒,电荷不守恒,B错误;
答案第2页,共2页C.水是弱电解质,不能拆分,NaOH是易溶性强碱,拆分成离子,方程式写法无误,C正
确;
D.NaOH是易溶性强碱,FeCl 是易溶性盐,拆分成离子,Fe(OH) 是难溶性碱,不能拆分,
3 3
方程式写法无误,D正确;
故选B。
8.B
【详解】试题解析:A、反应生成氯化钙、水和二氧化碳,碳酸钙在离子反应中应写化学
式,则碳酸钙中滴加盐酸的离子反应为CaCO +2H+=CO ↑+H O+Ca2+,故A错误;B.氢氧
3 2 2
化钠溶液中通入过量CO 生成碳酸氢钠,离子方程式正确,故B正确;C.澄清石灰水与
2
稀盐酸反应的离子反应为OH-+H+=H O,故C错误;D.铁钉放入硫酸铜溶液中的离子反应
2
为Fe+Cu2+=Fe2++Cu,故D错误。
考点:离子方程式的正误判断
9.D
【详解】A.稀硝酸的还原产物为NO,正确的离子方程式为:
,故A错误;
B.硅酸钠为可溶性盐,应拆成离子形式,正确的离子方程式为: ,
故B错误;
C.氨水为弱碱,不可拆,且氢氧化铝不溶于氨水,正确的离子方程式为:
,故C错误;
D.铁与Fe3+反应生成Fe2+,反应的离子方程式为:2Fe3++Fe=3Fe2+,故D正确;
故答案选D。
10.D
【详解】A.Cu(OH) 为难溶性碱,Mg(OH) 为难溶性碱,书写时不能拆开,两个离子反应
2 2
不能用同一离子方程式表示,故A不符合题意;
B.氯化钡与硫酸钠反应生成硫酸钡沉淀和氯化钠,氢氧化钡和硫酸铜反应生成硫酸钡沉
淀和氢氧化铜沉淀,两个离子反应生成的沉淀不完全一样,不能用同一离子方程式表示,
故B不符合题意;
C.碳酸氢根为弱酸的酸式根,在书写时不能拆写为碳酸根,两个离子反应不能用同一离子方程式表示,故C不符合题意;
D.盐酸和硝酸都是强酸,与碳酸钙反应的离子方程式均为CaCO +2H+=H O+CO↑+Ca2+,
3 2 2
故D符合题意;
故选D。
11.B
【详解】A.Ba2+与 生成BaSO 沉淀,描述错误,不符题意;
4
B.酚酞显红色的溶液有强碱性,选项中离子间以及与OH-均不反应,描述正确,符合题意;
C. 在溶液中显紫红色,描述错误,不符题意;
D.溶液环境显酸性,故CHCOO-会与H+形成弱电解质CHCOOH,描述错误,不符题意;
3 3
综上,本题选B。
12.A
【分析】此题考的是离子共存问题,应从选项的条件获取信息,再从中判断在此条件的环
境中是否有离子会互相反应,能大量共存就是没有可以互相发生反应的离子存在。
【详解】A.是一个碱性环境,离子相互间不反应,且与OH-不反应,能大量共存;
B.MnO-具有强氧化性,Fe2+具有还原性,两者会发生氧化还原反应而不能大量共存;
4
C.Ba2+可以与CO2-发生反应生成沉淀而不能大量存在;
3
D.酸性条件下H+与HSO -不能大量共存,同时酸性条件下NO -表现强氧化性会将HSO -氧
3 3 3
化而不能大量共存;
故选A。
【点睛】本题考查离子共存,掌握离子的性质和离子不能大量共存的原因是解题的关键。
离子间不能大量共存的原因有:①离子间发生复分解反应生成水、沉淀或气体,如题中C
项;②离子间发生氧化还原反应,如题中B项;③离子间发生双水解反应,如Al3+与
HCO -等;④离子间发生络合反应,如Fe3+与SCN-等;⑤注意题中的附加条件的影响,如
3
NO -在酸性条件下会表现强氧化性等。
3
13.B
【详解】某溶液中滴加酚酞试剂呈红色,则溶液呈碱性,含有较多量的OH-。
A. Fe3+与OH-能反应,生成Fe(OH) 沉淀,A中Fe3+在此溶液中不能大量共存;
3
B. Na+与OH-不反应,B中Na+在此溶液中能大量共存;
C. H+与OH-能反应生成水,C中H+在此溶液中不能大量共存;
D. Al3+与OH-能反应生成Al(OH) 沉淀,D中Al3+在此溶液中不能大量共存。
3
答案第4页,共2页故选B。
14.D
【详解】A、强碱性溶液存在大量的OH-,所以Al3+不能大量共存,故A错误;
B、Fe3+和I-因发生氧化还原反应而不能大量共存,故B错误;
C、Ca2+和CO2-因发生复分解反应而不能大量共存,故C错误;
3
D、室温下,pH=1的溶液中,四种离子互不反应,可以大量共存,故D正确;
答案选D。
15.D
【详解】A. 在水溶液中呈紫色,A不符合题意;
B. 在水溶液中呈棕黄色,B不符合题意;
C.在碱性溶液中, 不能大量存在,C不符合题意;
D.在无色透明的碱性溶液中, 、 、 、 都能稳定存在,D符合题意;
故选D。
16.D
【详解】试题分析:A.滴加甲基橙试剂显红色的溶液显酸性,酸性溶液中Fe 2+、NO -之
3
间发生氧化还原反应,不能大量共存,A错误;B.由水电离的c(H+)=1.0×10-13 mol·L﹣1
的溶液中水的电离平衡被抑制,溶液可能显酸性,也可能显碱性,如果显酸性则AlO-、
2
CO2-均不能大量共存,B错误;C.常温下,pH="7" 溶液中Al3+与CO2-水解相互促进不
3 3
能大量共存,C错误;D.K /c(H+)=0.1 mol·L-1的溶液中氢氧根的浓度是0.1mol/L,溶
W
液显碱性,Na+、K+、SiO2-、NO -之间不反应,可以大量共存,D正确,答案选D。
3 3
考点:考查离子共存正误判断
17.B
【详解】试题分析:A. CO 2-、Br-、K+、Na+ 中 CO2-和氢离子不共存; C. K+、Na
3 3
+、ClO-、Cl- 中次氯酸跟和氢离子组合是强氧化剂,会把氯离子氧化, D. K+、SO 2-、
4
HCO -、Mg2+ 中HCO -和氢离子不能大量共存;故选B。
3 3
考点:离子共存
点评:审题时还应特别注意以下几点:(1)注意溶液的酸性对离子间发生氧化还原反应的
影响。如:Fe2+与NO -能共存,但在强酸性条件下(即Fe2+、NO -、H+相遇)不能共存;
3 3MnO -与Cl-在强酸性条件下也不能共存;S2-与SO 2-在钠、钾盐时可共存,但在酸性条件下
4 3
则不能共存。(2)酸式盐的含氢弱酸根离子不能与强碱(OH-)、强酸(H+)共存。
如HCO -+OH-=CO 2-+H O(HCO -遇碱时进一步电离);HCO -+H+=CO ↑+H O。
3 3 2 3 3 2 2
18.B
【详解】根据电荷守恒,溶液呈电中性,按照 、 、 和M四种离子的顺序可列
式 ,可得到 ,所以为1个一价的阴离子,而营养液不可
能为强碱性的 ,故 , , , 中 复合题意;
故答案选B。
19.B
【详解】A.在氢氧化钡溶液中加入甲有白色沉淀生成,沉淀为碳酸钡,加盐酸沉淀溶解,
但再加氯化钙不反应,不能符合上述转化,故A不选;B.在氢氧化钡溶液中加入甲有白
色沉淀生成,沉淀为碳酸钡,加硝酸沉淀溶解生成硝酸钡,最后向所得溶液中加入硫酸镁
生成硫酸钡沉淀,与上述现象一致,则甲、乙、丙依次是NaCO、HNO、MgSO ,故B
2 3 3 4
选;C.在氢氧化钡溶液中加入甲有白色沉淀生成,沉淀为碳酸钡,加硝酸沉淀溶解生成
硝酸钡,再加硝酸银不反应,不能符合上述转化,故C不选;D.氢氧化钡溶液中加入甲
有白色沉淀生成,沉淀为硫酸钡,加碳酸钠不反应,沉淀不能溶解,不能符合上述转化,
故D不选;故选B。
点睛:本题考查物质的检验及性质,为高频考点,把握常见物质的性质及发生的化学反应
为解答的关键。注意白色沉淀的判断及硫酸钡不能溶于酸为解答的易错点。
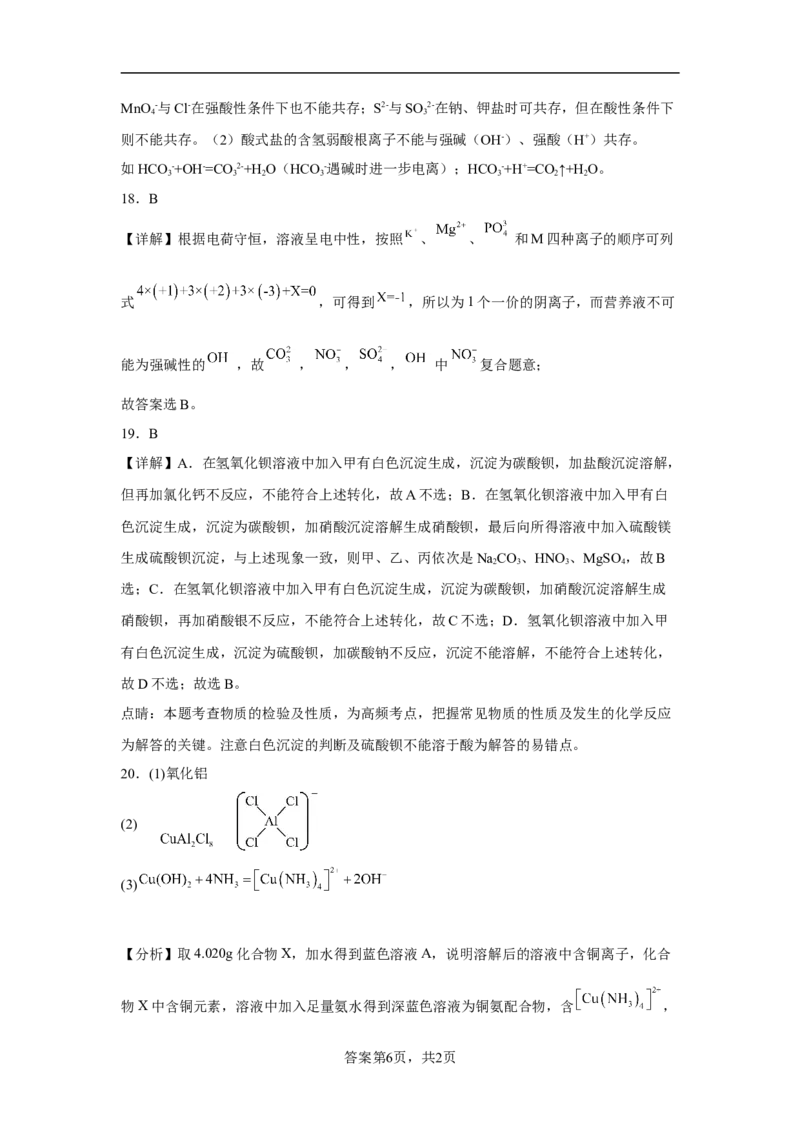
20.(1)氧化铝
(2)
(3)
【分析】取4.020g化合物X,加水得到蓝色溶液A,说明溶解后的溶液中含铜离子,化合
物X中含铜元素,溶液中加入足量氨水得到深蓝色溶液为铜氨配合物,含 ,
答案第6页,共2页加入硝酸酸化的硝酸银溶液,生成蓝色溶液和白色沉淀,白色沉淀E为氯化银,质量为
11.480g,物质的量n(AgCl)= =0.08mol,说明X中含氯元素,其物质的量为
0.08mol,白色沉淀B能溶于 溶液,说明B为氢氧化铝,灼烧得到白色固体C为氧化
铝,质量为1.020g,说明X中含铝元素,物质的量n(Al)=2 =0.02mol,则X中含
铜元素的物质的量为n(Cu)= =0.01mol,X的化
学式中n(Cu):n(Al):n(Cl)=0.01mol:0.02mol:0.08mol=1:2:8,化学式为:CuAl Cl。
2 8
(1)
由分析可知,白色固体C为氧化铝。
(2)
由分析可知,化合物X的化学式是:CuAl Cl,化合物X的一价阴离子与CH 具有相同的
2 8 4
空间结构,由于甲烷是正四面体结构,说明CuAl Cl 的阴离子为AlCl ,其结构式为:
2 8
。
(3)
蓝色溶液A加入氨水后先产生蓝色沉淀,蓝色沉淀为氢氧化铜沉淀,继续滴加氨水至过量
时得到深蓝色溶液,氢氧化铜沉淀继续与氨水反应得到 ,则生成深蓝色溶液
的离子方程式为: 。答案第8页,共2页