文档内容
人教版(2019)必修第一册第二章第三节 物质的量
课时训练六
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列说法中正确的是
A.1 mol H SO 的质量为98 g·mol-1 B.SO 的摩尔质量为64 g·mol-1
2 4 2
C.SO 的摩尔质量与SO 的相对分子质量相等 D.1 mol氧的质量为32 g
2 2
2.40.5 g某金属氯化物RCl 含有0.6 mol氯离子,则金属R的摩尔质量为
2
A.135g B.135g·mol−1 C.64 D.64g·mol−1
3.已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A.64g B.32g C.64g/mol D.32g/mol
4.如图所示,甲、乙、丙常温下都为气体,2mol甲反应生成1mol丙和3mol乙,下列
判断不正确的是
A.1个乙分子中含有2个H原子
B.甲的摩尔质量为17 g∙mol−1
C.同温同压下,生成丙和乙的体积比为1∶3
D.化学反应中各物质的质量之比等于2:1:3
5.下列说法正确的是
A.摩尔是国际单位制中的基本物理量
B.1mol HO中所含氧原子的质量为16g
2
C.铁原子的摩尔质量和它的相对原子质量相等
D.某物质含有6.02×1023个原子,则该物质的物质的量为1mol
6.偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推
2 8 2
动力。下列叙述正确的是
A.偏二甲肼的摩尔质量为60g
B.6.02×1023个偏二甲肼分子的质量约为60g
C.1mol偏二甲肼的质量为60g·mol-1
D.6g偏二甲肼含有N 个偏二甲肼分子
A7.下列关于阿伏加德罗常数的说法错误的是
A.6.02×1023就是阿伏加德罗常数
B.0.012kg12C含有的碳原子数就是阿伏加德罗常数
C.含有阿伏加德罗常数个粒子的物质的量是1mol
D.1mol氨气所含的原子数约为2.408×1024
8.下列说法中正确的是
A.摩尔既是物质的数量单位又是物质的质量单位
B.阿伏加德罗常数是12 kg 12C中含有的碳原子数
C.1 mol水中含有2 mol氢原子和1 mol氧原子
D.阿伏加德罗常数就是6.02×1023 mol-1
9.设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,N 为阿伏加德罗
A
常数的值。下列说法不正确的是
A.H(g)+ O(g)=HO(l) ΔH=-286 kJ·mol−1,则每1 mol [H (g)+ O(g)]生成1
2 2 2 2 2
mol [HO(l)]放热286 kJ
2
B.Cr O2-+ne−+14H+=2Cr3++7HO,则每生成1 mol Cr3+转移电子数为3N
2 7 2 A
C.Al3++4OH−=[Al(OH) ]−,说明1 mol Al(OH) 电离出H+数为N
4 3 A
D.1 mol CO 与NaOH溶液完全反应,则n(CO2-)+n(HCO -)+n(H CO)=1 mol
2 3 3 2 3
10.设N 为阿伏加德罗常数的值,下列叙述不正确的是
A
A.0.1mol14C中,含有0.8N 个中子
A
B.含N 个CO 的NaCO 溶液中,Na+数目大于2N
A 2 3 A
C.一定条件下,将1molN 与3molH 充入一密闭容器内充分反应后,容器内气体分子
2 2
数小于2N
A
D.向含有FeI 的溶液中通入适量氯气,当有1molFe2+被氧化时,反应中转移电子的数
2
目至少为3N
A
11.标准状况下,现有 ①4.48LCH ②3.01×1023个HCl ③10.2gH S ④0.2mol
4 2
C HOH ,则对这四种物质的关系有以下四种表述,其中不正确的是
2 5
A.体积:②>③>①>④ B.密度:④>②>③>①
C.质量:②>③>④>① D.氢原子个数:④>③>①>②
12.ClO沸点3.8°C,熔点-116°C,是很好的氯化剂,利用HgO+2Cl =HgCl +ClO可
2 2 2 2
以制备高纯度的ClO。下列说法正确的是(N 为阿伏伽德罗常数)
2 A
A.标准状况下,2.24LCl O含有分子数为0.1N
2 A
B.0.2mol氯气与足量的HgO反应,转移电子数为0.2N
A
试卷第2页,共3页C.HgO与稀硝酸反应的离子方程式为O2-+2H+=H O
2
D.ClO与氢氧化钠溶液反应的离子方程式为ClO+2OH-=Cl-+ClO-+H O
2 2 2
13.当温度和压强恒定不变时,影响气体体积大小的主要因素是
A.分子直径大小 B.分子间的距离大小
C.分子数目的多少 D.密度大小
14.标准状况下,由0.5 gH、11g CO 和4 gO 组成的混合气体,其体积约为
2 2 2
A.8.4 L B.11.2 L C.14.0 L D.16.8 L
15.下列说法正确的是
A.气体摩尔体积就是22.4L
B.任何状况下,1mol任何气体的体积一定是22.4L
C.标准状况下22.4L水含有6.02×1023个分子
D.1molH 和O 的混合气体在标准状况下的体积约22.4L
2 2
二、填空题
16.按要求计算并填空。
(1)32gSO 标况下的体积为_______L,含有_______个氧原子。
2
(2)1.204×1023个NH 分子所含的氢原子数与_______molCH 含有的氢原子数相同。
3 4
(3)标况下,某CO 和H 混合气体的密度为1.25g/L,则混合气体中CO 和H 的体积比
2 2 2 2
约为_______。
(4)200mL某硫酸盐溶液中含SO 1.5N 个,含金属离子N 个,则该硫酸盐溶液的物
A A
质的量浓度为_______mol/L。
(5)把VmL含有Al (SO ) 和(NH )SO 的混合溶液分成两等份,一份加入含足量NaOH
2 4 3 4 2 4
的溶液并加热,铵根离子完全反应生成amolNH (已知NH +OH- NH ↑+H O);另一份
3 3 2
加入含bmolBaCl 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中
2
Al3+的浓度为_______mol/L。
(6)A、B、C三种一元碱,它们的摩尔质量之比是3:5:7,如果把7molA,5molB和
3molC混合均匀,取混合碱5.36g恰好能中和0.15mol的HCl。试求A的摩尔质量为
_______g/mol。
(7)将Wg胆矾(CuSO ·5H O)溶解在VmL水中,得到饱和溶液,测得该饱和溶液的密度
4 2
为pg·cm3,则溶液的物质的量浓度为_______,该温度下,CuSO 的溶解度为_______。
4(8)取8.58gNa CO·xH O溶于水配成溶液然后逐滴滴入质量分数为36.5%,密度为
2 3 2
1.20g/cm3的盐酸直至没有气体放出,用去盐酸5.0mL。则生成标况下CO 气体的体积
2
为_______;x的值_______
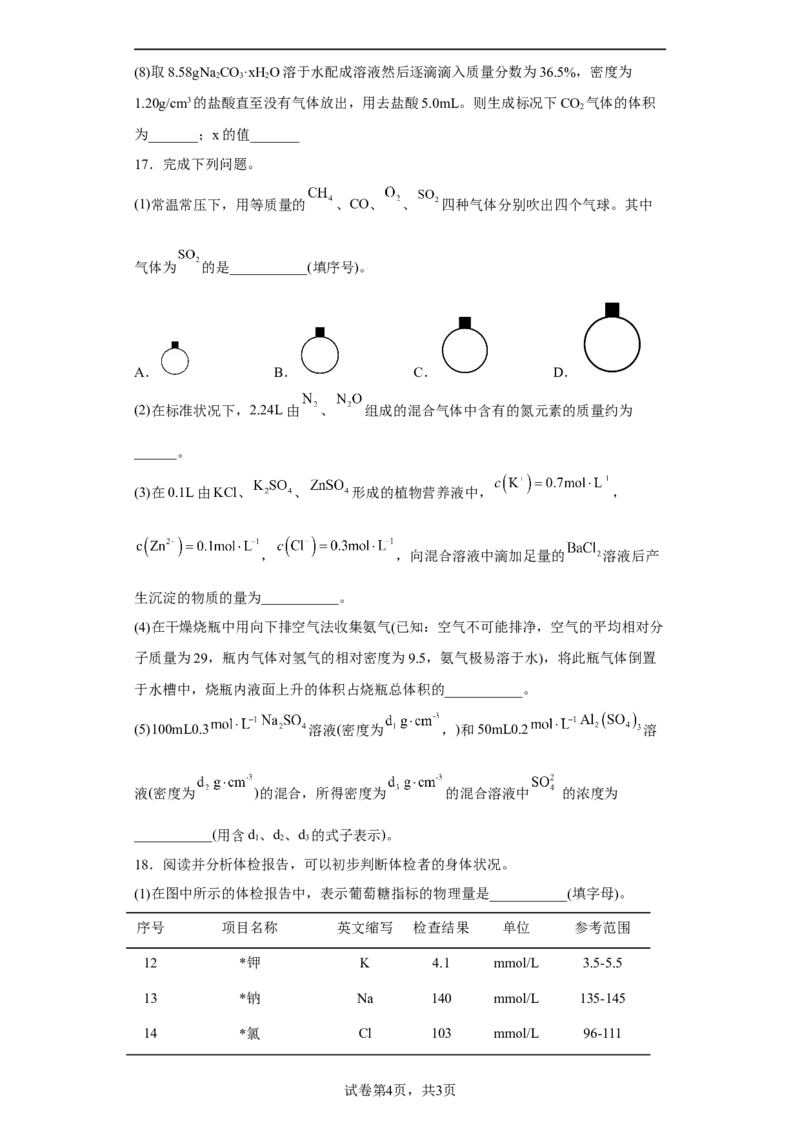
17.完成下列问题。
(1)常温常压下,用等质量的 、CO、 、 四种气体分别吹出四个气球。其中
气体为 的是___________(填序号)。
A. B. C. D.
(2)在标准状况下,2.24L由 、 组成的混合气体中含有的氮元素的质量约为
______。
(3)在0.1L由KCl、 、 形成的植物营养液中, ,
, ,向混合溶液中滴加足量的 溶液后产
生沉淀的物质的量为___________。
(4)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分
子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置
于水槽中,烧瓶内液面上升的体积占烧瓶总体积的___________。
(5)100mL0.3 溶液(密度为 ,)和50mL0.2 溶
液(密度为 )的混合,所得密度为 的混合溶液中 的浓度为
___________(用含d、d、d 的式子表示)。
1 2 3
18.阅读并分析体检报告,可以初步判断体检者的身体状况。
(1)在图中所示的体检报告中,表示葡萄糖指标的物理量是___________(填字母)。
序号 项目名称 英文缩写 检查结果 单位 参考范围
12 *钾 K 4.1 mmol/L 3.5-5.5
13 *钠 Na 140 mmol/L 135-145
14 *氯 Cl 103 mmol/L 96-111
试卷第4页,共3页15 钙 Ca 0.68 mmol/L 2.13-2.70
16 胱抑素 CyaC 0.78 mg/L 0.59-1.03
18 *尿素 Urea 4.18 mmol/L 2.78-7.14
19 *葡萄糖 Glu 5.1 mmol/L 3.9-6.1
21 *无机磷 P 1.19 mmol/L 0.81-1.45
22 *总胆固醇 TC 4.65 mmol/L 2.85-5.70
23 *甘油三酯 TG 1.50 mmol/L 0.45-1.70
24 高密度脂蛋白胆固醇 HDL-V 1.08 mmol/L 0.93-1.83
a.质量分数 b.溶解度 c.摩尔质量 d.物质的量浓度
(2)查看自己或家人的体检报告,哪些项目的指标是用物质的量浓度表示的?
___________
(3)检测人的血液中葡萄糖(简称血糖,葡萄糖的相对分子质量为180)的含量,参考指标
常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL)。以“mmol/L”表示时,
人的血糖正常值为3.9~6.1mmol/L。如果以“mg/dL”表示,血糖正常值范围是
___________?若某人的血糖检测结果为92mg/dL,他(她)的血糖正常吗?___________
19.某化学研究性学习小组使用0.2mol/LKCl和 配制含有
的植物营养液500mL。
实验室提供的药品有: 和蒸馏水。
提供的实验仪器有:药匙、托盘天平、烧杯、胶头滴管、量筒。
(1)该植物营养液中, 的物质的量浓度为_______。
(2)该研究小组配制该植物营养液时,还须用到的玻璃仪器有_______、_______。
(3)若使用 和 三种物质进行配制,则需硫酸铵的质量为
_______。
(4)若配制该营养液的其他操作均正确,下列操作将使所配制溶液的浓度偏低的是
_______(填字母)。
A.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的溶液向容量瓶中转移时,容量瓶中有少量的水C.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
D.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
E.摇匀后发现液面低于容量瓶刻度线,又加水至刻度线
20.根据所学知识填空(N 表示阿伏加德罗常数):
A
(1)0.2 mol Cl 含有_______mol Cl。
2
(2)1.5 mol H O中,氢原子与氧原子个数之比为_______,质量比为_______。
2
(3)1.204×1022个CO 分子,含O的质量为_______。
2
(4)1 mol OH-中含有_______mol 电子。
(5)同温同压下,同体积的N 和SO 分子数之比为_______,物质的量之比为_______,
2 2
质量之比为_______。
三、实验题
21.取30.0g牛奶样品,将所含蛋白质中的氮元素全部转化为氨,用25.00mL1.00mol/L
硫酸将其完全吸收,再加入19.00mL2.00mol/L氢氧化钠溶液恰好生成硫酸钠和硫酸铵。
请计算:
(1)所用NaOH的物质的量为__mol。
(2)样品中蛋白质转化生成的氨的物质的量为__mol。
(3)若蛋白质中氮元素的质量分数为14.0%,则样品中蛋白质的质量分数为___。
22.在 浓度为0.5mol/L的某澄清溶液中,还可能含有的离子有K+、Ag+、Mg2+、
Ba2+、NO 、CO 、 、SO 。现取该溶液100mL进行如下实验(气体体积均在标准
状况下测定):
Ⅰ.向该溶液中加入足量稀硝酸,放出0.56L气体;
Ⅱ.向Ⅰ的反应混合液中滴加硝酸银溶液,有白色沉淀生成,将沉淀洗涤、烘干,称
量所得固体的质量为2.87g;
Ⅲ.另取10mL原溶液,滴加氯化钡溶液,产生白色沉淀,再加入足量的稀盐酸,沉
淀完全溶解。
请回答下列问题:
(1)通过实验Ⅰ能确定一定不存在的离子是___________(填离子符号)。
(2)实验Ⅱ中生成沉淀的离子方程式为___________。
(3)综上所述,填写下表中阴离子的浓度(能计算出的填写计算结果,一定不存在的离子
填“0”,不能确定是否存在的离子填“?”)。
试卷第6页,共3页阴离子 Cl-
NO CO SO
c(mol·L-1) ①___________ ②___________ ③___________ 0
(4)判断K+是否存在:___________(填“存在”或“不存在”);若存在,则其最小浓度
为___________mol/L。参考答案:
1.B
【详解】A.1 mol H SO 的质量是98 g,错误;
2 4
B.SO 的摩尔质量为64 g·mol-1,正确;
2
C.两者数值相等,单位不同,错误;
D.1 mol氧指代不明,错误。
故选B。
2.D
【详解】RCl 的物质的量为0.3 mol,RCl 的摩尔质量为 ,则R的摩尔
2 2
质量为135 -35.5×2=64 g·mol-1,答案选D。
3.D
【详解】根据n=N/N ,计算出1.505×1023个X气体分子的物质的量为0.25mol,结合其质
A
量为8g,利用n=m/M的关系,可得M(X)=32g/mol。
故选D。
4.D
【分析】根据图示,甲是氨气、丙是氮气,2 mol甲反应生成1 mol丙和3 mol乙,根据原
子守恒,乙是氢气。
【详解】A.由题给反应知,甲为氨气,丙为氮气,乙为氢气,1个乙分子即1个H 中含
2
有2个H原子,故A正确;
B.甲为氨气,氨气的摩尔质量为17 g∙mol−1,故B正确;
C.同温同压下,气体的体积之比等于分子数之比,所以生成丙和乙的体积比为1∶3,故C
正确;
D.化学反应中各物质的质量之比为2×17:1×28:3×2=17:14:3,故D错误;
综上所述,答案为D。
5.B
【详解】A.摩尔是国际单位制中的基本单位,A项错误;
B.1mol HO中所含氧原子的物质的量为1mol,则氧原子的质量为 ,B
2
项正确;
C.铁原子的摩尔质量和它的相对原子质量在数值上相等,C项错误;
D.某物质含有6.02×1023个原子,则该物质含有的原子为1mol,但该物质的物质的量不一定为1mol,D项错误;
答案选B。
6.B
【详解】A.偏二甲肼(C HN)的摩尔质量为(12×2+1×8+14×2)g/mol=60g/mol,故A
2 8 2
错误;
B.6.02×1023个偏二甲肼的物质的量为 ,所以1 mol 偏二甲
肼的质量为60 g,故B正确;
C.1mol偏二甲肼的质量为60 g,故C错误;
D.偏二甲肼的物质的量为 ,含有的分子数为0.1×N ,故D错误。
A
故选:B。
7.A
【详解】A.阿伏加德罗常数是指0.012 kg 12C含有的碳原子数,单位是mol-1,其近似值
为6.02×1023mol-1,故A错误,
B.根据阿伏伽德罗常数的定义知,0.012kg12C含有的碳原子数就是阿伏加德罗常数,故B
正确;
C.阿伏加德罗常数的定义,含有阿伏加德罗常数个粒子的物质的量是1 mol ,故C正确;
D.1mol氨气的原子个数约为1mol×4×6.02×1023mol-1=2.408×1024,故D正确。
故选A。
8.C
【详解】A.摩尔是物质的量的单位,故A错误;
B.1 mol粒子集体所含的粒子数是阿伏加德罗常数,与0.012 kg 12C中所含的碳原子数相
同,故B错误;
C.1个水分子由2个氢原子和1个氧原子构成,1 mol水中含有2 mol氢原子和1 mol氧原
子,故C正确;
C.阿伏加德罗常数是1 mol粒子所含的粒子数,在数值上等于12 g12C所含的碳原子数,
是个具体的值,6.02×1023mol-1是阿伏加德罗常数的近似值,故D错误;
选C。
9.C
答案第2页,共2页【详解】A项、由热化学方程式可知,氢气在氧气中的燃烧为放热反应,1 mol [H (g)+
2
O(g)]生成1 mol [H O(l)]放热286 kJ,故A正确;
2 2
B项、由铬元素化合价变化可知,生成2 mol Cr3+转移6mol电子,则生成1 mol Cr3+转移电
子数为3N ,故B正确;
A
C项、氢氧化铝是两性氢氧化物,在溶液中发生酸式电离部分电离出氢离子,则1 mol
Al(OH) 电离出H+数小于N ,故C错误;
3 A
D项、由碳原子个数守恒可知,1 mol CO 与NaOH溶液完全反应生成的盐溶液中,n(CO2-)
2 3
+n(HCO -)+n(H CO)=1 mol,故D正确;
3 2 3
故选C。
【点睛】氢氧化铝是两性氢氧化物,在溶液中发生酸式电离部分电离出氢离子是解答关键,
也是易错点。
10.C
【详解】A.1个 中含有8个中子, 中含有 个中子,故A正确;
B. 电离产生 、 个数比为 ,在溶液中 由于发生水解反应而消耗,所
以若溶液中含 个 ,则 数目大于 ,故B正确;
C.合成氨反应为可逆反应,不能进行彻底,故 与 不能完全转化为 ,
且该反应正反应方向气体分子数减小,故容器内气体分子数大于 ,故C错误;
D.通入适量氯气,有 被氧化,说明溶液中 ,因为还原性
,所以 全部被氧化,氧化 转移电子 ,氧化 转移 电子,故该反应
转移电子数至少为 ,故D正确;
故选C。
11.D【分析】①4.48L 的物质的量为 ;②3.01×1023个HCl分子的物质的量为 ;
③10.2g 的物质的量为: ;④0.2mol ,由此结合相关公式解
答。
【详解】A.标准状况下 为液体,体积最小,所以体积:②>③>①>④,描述正确,
不符题意;
B.相同条件下气体密度之比等于摩尔质量之比,标准状况下 为液体密度最大,
所以密度:④>②>③>①,描述正确,不符题意;
C.① 的物质的量为 ,质量为: ;②3.01×1023个HCl分子的物质的
量为 ,质量为 ;④0.2mol 的质量为: ,所以质量:
②>③>④>①,描述正确,不符题意;
D.氢原子的物质的量分别为: 、 、 、 ,个数:④>①>③>②,
描述错误,符合题意;
综上,本题选D。
12.B
【详解】A.标准状况下ClO为液体,无法计算2.24LCl O含有的分子数,A错误;
2 2
B.在反应HgO+2Cl =HgCl +ClO中,氯由0价变为HgCl 中-1价的氯和ClO中+1价氯,
2 2 2 2 2
该反应转移2个电子,故0.2mol氯气与足量的HgO反应,转移电子数为0.2N ,B正确;
A
C.HgO为金属氧化物,在写离子方程式的时候,正确的离子方程式为:
HgO+2H+=H O+Hg2+,C错误;
2
D.在该反应中氧元素不守恒,D错误;
故选B。
13.C
【详解】影响体积大小的因素有分子直径的大小、分子间距离的大小、分子数目的多少,
在一定温度和压强下,气体分子间的距离相等,因气体分子间距离远大于气体分子大小,
则影响其所占体积大小的主要因素是分子数目的多少,故选C。
答案第4页,共2页14.C
【详解】0.5g H、11g CO 和4g O 的体积分别是:
2 2 2
氢气: ×22.4L/mol=5.6L;
二氧化碳: =5.6L;
氧气: =2.8L,
所以混合气体的体积V=5.6L+5.6L+2.8L=14.0L,故C正确。
故选C。
15.D
【详解】A.气体摩尔体积指在一定温度和压强下,单位物质的量气体所占的体积,标准
状况下,气体摩尔体积为22.4 L/mol,其他条件下不一定是22.4 L/mol,A错误;
B.标准状况下,1 mol气体体积约为22.4 L,其他条件下不一定,B错误;
C.标准状况下,水为非气体,故22.4 L水物质的量不等于1 mol,C错误;
D.1 mol任何气体(包括混合气体),在标准状况下体积约为22.4 L,D正确;
故答案选D。
16.(1) 11.2 6.02×1023或N
A
(2)0.15
(3)13:8
(4)2.5
(5)
(6)24g/mol
(7) mol/L
(8) 0.672L 10
【解析】(1)32gSO 标况下的体积为: ,含有
2
,故答案为:11.2;6.02×1023或
N ;
A
(2)
根据 ,则 ,解得 ;
(3)
标况下,某CO 和H 混合气体的密度为1.25g/L,混合气体的平均摩尔质量是1.25g/
2 2
L×22.4L/mol=28g/mol,设CO 和H 的物质的量分别是xmol、ymol, ,
2 2
,则混合气体中CO 和H 的体积比约为13:8;
2 2
(4)
200 mL某硫酸盐溶液中含SO 1.5 N 个,含金属离子N 个,则SO 、金属离子的物质
A A
的量分别是1.5mol、1mol,该盐的化学式可表示为R (SO ),该硫酸盐的物质的量是
2 4 3
0.5mol,则该硫酸盐溶液的物质的量浓度为 =2.5mol/L;
(5)
一份加入含b mol BaCl 的溶液,恰好使硫酸根离子完全沉淀为硫酸钡,说明硫酸根离子的
2
物质的量为bmol;一份加入足量NaOH的溶液并加热,生成amol NH,则(NH )SO 的物
3 4 2 4
质的量是 mol ;则Al (SO ) 的物质的量是 mol,Al3+的物质的量是 mol,原混
2 4 3
合溶液中Al3+的浓度为 mol/L;
答案第6页,共2页(6)
由酸与碱中和反应的实质可知n(H+) = n(OH-),据此计算5.36g混合一元碱的总的物质的量,
混合碱5.36g恰好能中和0.15mol的HCl,所以n(OH- ) = 0.15mol,所以一元碱的总物质的
量也为0.15mol,设A、B、C三种碱的摩尔质量分别为3x、5x、 7x, 故一元碱的平均摩
尔质量即为: ,解得,x=8,
故A的摩尔质量为:24g/mol;
(7)
Wg胆矾(CuSO ·5H O)中硫酸铜的物质的量n(CuSO )= = mol,溶液的体积
4 2 4
= = mL,溶液的物质的量浓度= = mol/L;
= ,则溶解度为 g;
(8)
根据公式:C=(1000×P×W)/M;所用盐酸的物质的浓度C= =12mol·L-1;
NaCO+2HCl=2NaCl+H O+CO;2HCl~CO ;盐酸消耗12×5×103=0.06mol;V(CO )=
2 3 2 2 2 2
×22.4=0.672L;NaCO·xH O~2HCl; =12×5×10-3解之得X=10。
2 3 2
17.(1)A
(2)2.8g
(3)0.03mol
(4)(5)
【解析】(1)
在相同条件下,气体的物质的量越大,气体的体积越大,四种气体的质量相等,根据
可知,气体的摩尔质量越大,物质的量越小,四种气体中二氧化硫的摩尔质量最大,
物质的量最小,体积最小,故答案为:A;
(2)
在标准状况下,2.24L由 、 组成的混合气体的物质的量是0.1mol,因为一个 和
分子中都含有2个氮原子,所以不论 和 的比例如何,N的物质的量就是混合
气体的物质的量的2倍,故2.24L由 、 组成的混合气体中含有的氮元素的物质的量
为0.2mol,氮元素的质量为 ,故答案为:2.8g;
(3)
由溶液呈电中性可知, +2 = +2 ,溶液中硫酸根离子的浓度
,则硫酸根离子的物质的
量为 ,则向混合溶液中滴加足量的 溶液后产生硫酸钡沉淀
的物质的量为0.03mol,故答案为:0.03mol;
(4)
用排空气法收集到的氨气气体不纯,混合气体的平均相对分子质量为 。设烧瓶
的容积为V,氨气的体积为x,空气的体积为V-x,则有
,解得 ,将此瓶气体倒置于水槽中,进
答案第8页,共2页入烧瓶的液体体积为氨气的体积,即 ,故答案为: ;
(5)
混合溶液的质量为 ,混合后溶液的体积为 ,混合溶液中
,混合溶液中 的浓度为
,故答案为: 。
18.(1)d
(2)除了第16项胱抑素C外,其余指标都是用物质的量浓度表示的
(3) 70.2-109.8mg/dL 血糖正常
【解析】(1)
葡萄糖为5.1mmol/L,涉及单位为mmol/L,为物质的量浓度的单位,而质量分数无单位,
溶解度的单位是g,摩尔质量的单位为g/mol;所以表示葡萄糖指标的物理量是物质的量浓
度,故选d;
(2)
根据体检报告,除了第16项胱抑素C外,其余指标都是用物质的量浓度表示的;
(3)
主要是把葡萄糖的单位mmol/L转化为mg/dL,即mmol/10dL→180 mg/10dL→18 mg/dL;
血糖正常值为3.9~6.1mmol/L,以mg/dL为单位时,血糖正常值为70.2-109.8mg/dL,
92mg/dL属于正常值。
19.(1)1.6mol/L
(2) 500mL容量瓶 玻璃棒
(3)39.6g
(4)ACE
【解析】(1)该植物营养液中 ,溶液体积为 ,所以铵根离子的浓度为
。
(2)
配制 溶液,需要在 容量瓶中定容;溶解固体时需要玻璃棒搅拌,向容量瓶中
转移溶液时要用玻璃棒引流,所以还须用到的玻璃仪器有 容量瓶、玻璃棒。
(3)
要求该营养液中 ,则需要 ,营养液中 ,所以
还需要硫酸铵提供铵根离子的物质的量为 ,则需要 硫酸铵,
质量为 。
(4)
将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒,溶质物质的量偏小,所得溶液浓度偏低,
故A符合题意:将烧杯内的溶液向容量瓶中转移时,容量瓶中有少量的水,对浓度无影响,
故B不符合题意;将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶,
会使溶质物质的量偏小,所得溶液浓度偏低,故C符合题意;用胶头滴管向容量瓶中加水
时,俯视容量瓶刻度线,会使溶液体积偏小,所得溶液浓度偏高,故D不符合题意;摇匀
后发现液面低于容量瓶刻度线,再加水至刻度线,会使溶液体积偏大,所得溶液浓度偏低,
故E符合题意。故选ACE。
20. 0.4 2:1 1:8 0.64g 10 1:1 1:1 7:16
【详解】(1)0.2mol Cl 含有Cl的物质的量为:0.2mol×2=0.4mol,故答案为:0.4;
2
(2)1.5mol HO中氢原子与氧原子个数之比为2:1;含有H、O的质量之比=(2×1):
2
(1×16)=1:8,故答案为:2:1;1:8;
(3)1.204×1022个CO 分子的物质的量为: ,含有O的物质的量
2
为:0.02mol×2=0.04mol,含有O的质量为16g/mol×0.04mol=0.64g,故答案为:0.64g;
(4)1个OH-中含有的电子数为8+1+1=10,则1mol OH-中含有电子的物质的量为
1mol×10=10mol,故答案为:10;
(5)同温同压下,同体积的N 和SO 分子数之比为等于物质的量之比,等于体积之比,等于
2 2
答案第10页,共2页1:1;质量之比等于摩尔质量之比,等于28:64=7:16,故答案为:1:1;1:1;7:16。
21.(1)0.0380
(2)0.0120
(3)4.00%
【分析】(1)
由 ,故答案为:0.0380;
(2)
将所含蛋白质中的氮元素全部转化为氨,用25.00mL1.00mol/L硫酸将其完全吸收,再加入
19.00mL2.00mol/L氢氧化钠溶液恰好生成硫酸钠和硫酸铵可得
,故答案为:
0.0120;
(3)
蛋白质中氮元素的质量分数为14.0%,则蛋白质的质量为 ;则
样品中蛋白质的质量分数为 ,故答案为:
4.00%。
22.(1)Ag+、Mg2+、Ba2+
(2)Ag + +Cl- =AgCl↓
(3) ? 0.25mol·L-1 0.2mol·L-1
(4) 存在 0.2
【分析】由实验Ⅰ知原溶液中一定存在 ,根据碳元素守恒知n( )=n(CO)=
2
,c( )= ,由于存在 ,故原溶液一定
不含Ag+、Mg2+、Ba2+;根据实验Ⅲ知,原溶液不存在 ;再由实验Ⅱ知,原溶液一定存在Cl-,所得沉淀为AgCl,由氯元素守恒得:n(Cl-)=n(AgCl)= ,
c(Cl-)= , 、Cl-所带负电荷浓度=0.25×2+0.2=0.7 mol/L,大于Na+所
带正电荷浓度0.5 mol/L,故原溶液一定存在K+,由于 可能存在,根据电荷守恒知,
c(K+)≥0.7-0.5=0.2 mol/L。
(1)
由分析知,原溶液一定不含Ag+、Mg2+、Ba2+,故此处填:Ag+、Mg2+、Ba2+;
(2)
由分析知,实验Ⅱ所得沉淀为AgCl,对应离子方程式为:Ag++Cl-=AgCl↓;
(3)
由分析知, 不能确定是否存在,故此处填:?; 、Cl-浓度依次为0.25 mol/L、0.2
mol/L;
(4)
由分析知,K+一定存在,其浓度最小为0.2 mol/L,故此处填:存在、0.2。
答案第12页,共2页