文档内容
第二章 第二节 第2课时 氯气的实验室制法及氯离子的检验 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 下列关于实验室用MnO 制取Cl 的叙述不正确的是( )
2 2
A.用向下排空气法收集Cl
2
B.缓慢加热反应
C.MnO 与浓盐酸共热
2
D.多余的Cl 常用较浓的碱液吸收
2
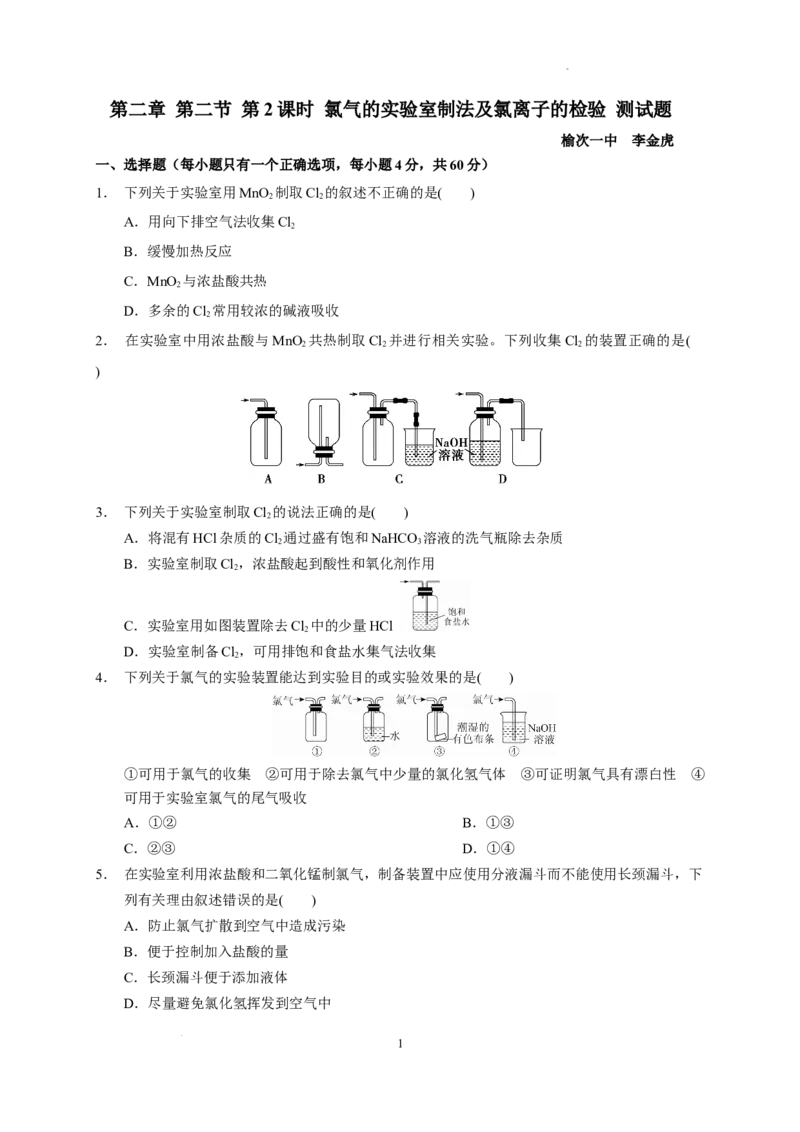
2. 在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。下列收集Cl 的装置正确的是(
2 2 2
)
3. 下列关于实验室制取Cl 的说法正确的是( )
2
A.将混有HCl杂质的Cl 通过盛有饱和NaHCO 溶液的洗气瓶除去杂质
2 3
B.实验室制取Cl,浓盐酸起到酸性和氧化剂作用
2
C.实验室用如图装置除去Cl 中的少量HCl
2
D.实验室制备Cl,可用排饱和食盐水集气法收集
2
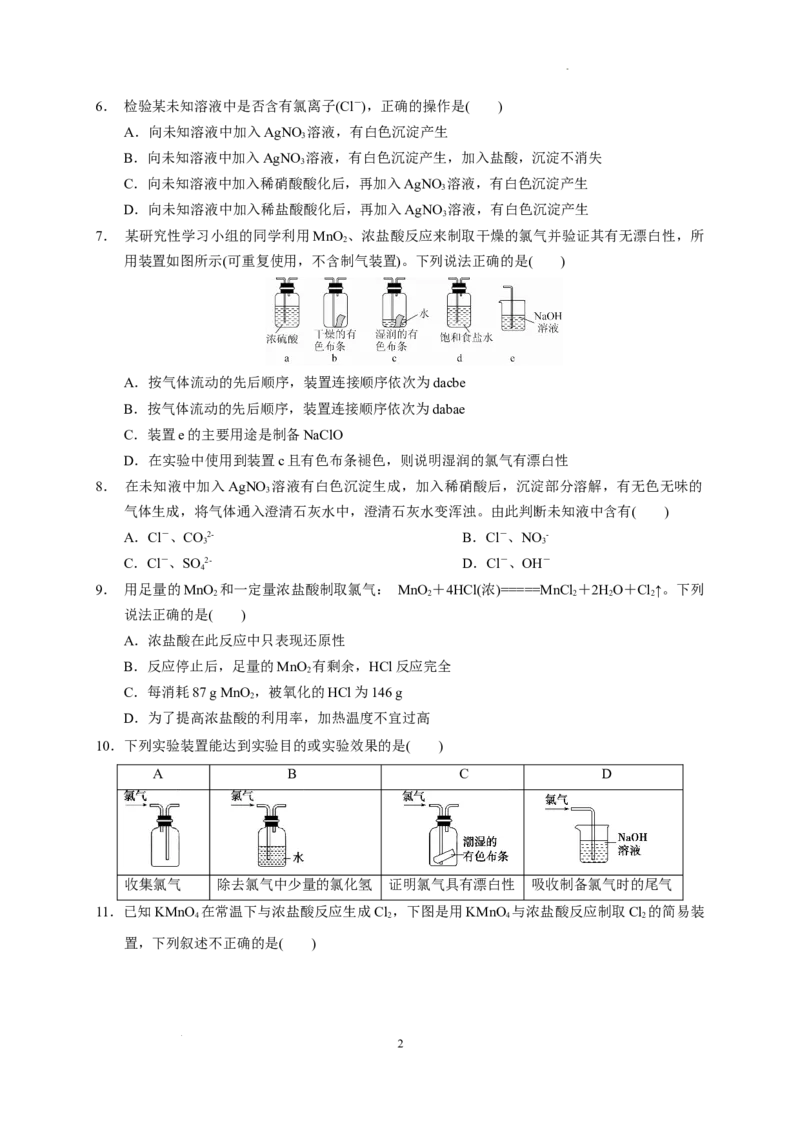
4. 下列关于氯气的实验装置能达到实验目的或实验效果的是( )
①可用于氯气的收集 ②可用于除去氯气中少量的氯化氢气体 ③可证明氯气具有漂白性 ④
可用于实验室氯气的尾气吸收
A.①② B.①③
C.②③ D.①④
5. 在实验室利用浓盐酸和二氧化锰制氯气,制备装置中应使用分液漏斗而不能使用长颈漏斗,下
列有关理由叙述错误的是( )
A.防止氯气扩散到空气中造成污染
B.便于控制加入盐酸的量
C.长颈漏斗便于添加液体
D.尽量避免氯化氢挥发到空气中
1
学科网(北京)股份有限公司6. 检验某未知溶液中是否含有氯离子(Cl-),正确的操作是( )
A.向未知溶液中加入AgNO 溶液,有白色沉淀产生
3
B.向未知溶液中加入AgNO 溶液,有白色沉淀产生,加入盐酸,沉淀不消失
3
C.向未知溶液中加入稀硝酸酸化后,再加入AgNO 溶液,有白色沉淀产生
3
D.向未知溶液中加入稀盐酸酸化后,再加入AgNO 溶液,有白色沉淀产生
3
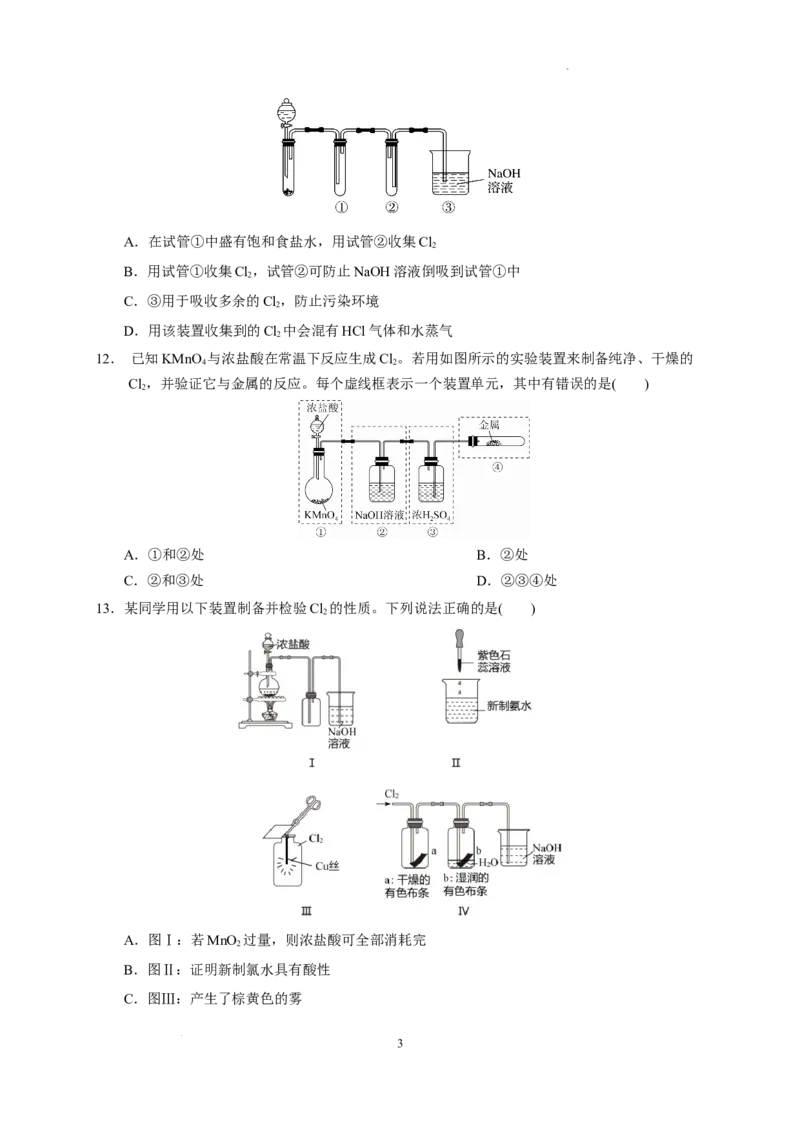
7. 某研究性学习小组的同学利用MnO 、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所
2
用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )
A.按气体流动的先后顺序,装置连接顺序依次为dacbe
B.按气体流动的先后顺序,装置连接顺序依次为dabae
C.装置e的主要用途是制备NaClO
D.在实验中使用到装置c且有色布条褪色,则说明湿润的氯气有漂白性
8. 在未知液中加入AgNO 溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的
3
气体生成,将气体通入澄清石灰水中,澄清石灰水变浑浊。由此判断未知液中含有( )
A.Cl-、CO2- B.Cl-、NO -
3 3
C.Cl-、SO 2- D.Cl-、OH-
4
9. 用足量的MnO 和一定量浓盐酸制取氯气: MnO +4HCl(浓)=====MnCl +2HO+Cl↑。下列
2 2 2 2 2
说法正确的是( )
A.浓盐酸在此反应中只表现还原性
B.反应停止后,足量的MnO 有剩余,HCl反应完全
2
C.每消耗87 g MnO ,被氧化的HCl为146 g
2
D.为了提高浓盐酸的利用率,加热温度不宜过高
10.下列实验装置能达到实验目的或实验效果的是( )
A B C D
收集氯气 除去氯气中少量的氯化氢 证明氯气具有漂白性 吸收制备氯气时的尾气
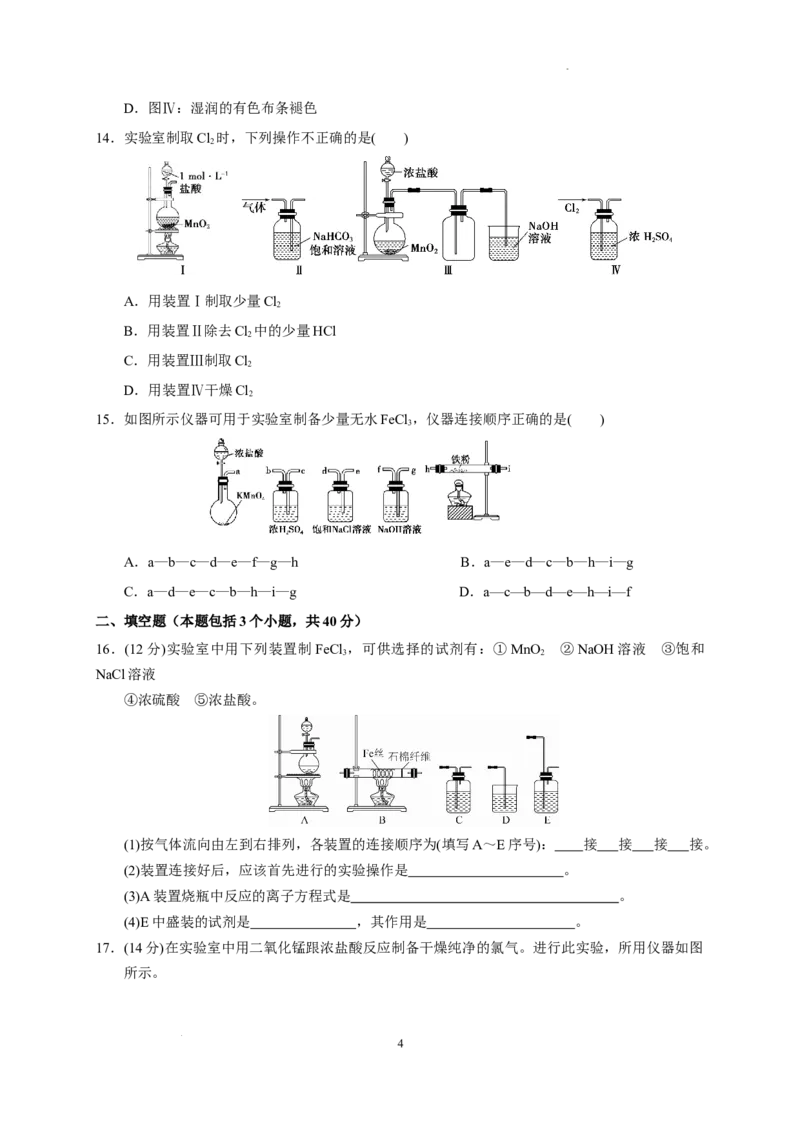
11.已知KMnO 在常温下与浓盐酸反应生成Cl ,下图是用KMnO 与浓盐酸反应制取Cl 的简易装
4 2 4 2
置,下列叙述不正确的是( )
2
学科网(北京)股份有限公司A.在试管①中盛有饱和食盐水,用试管②收集Cl
2
B.用试管①收集Cl,试管②可防止NaOH溶液倒吸到试管①中
2
C.③用于吸收多余的Cl,防止污染环境
2
D.用该装置收集到的Cl 中会混有HCl气体和水蒸气
2
12. 已知KMnO 与浓盐酸在常温下反应生成Cl。若用如图所示的实验装置来制备纯净、干燥的
4 2
Cl,并验证它与金属的反应。每个虚线框表示一个装置单元,其中有错误的是( )
2
A.①和②处 B.②处
C.②和③处 D.②③④处
13.某同学用以下装置制备并检验Cl 的性质。下列说法正确的是( )
2
A.图Ⅰ:若MnO 过量,则浓盐酸可全部消耗完
2
B.图Ⅱ:证明新制氯水具有酸性
C.图Ⅲ:产生了棕黄色的雾
3
学科网(北京)股份有限公司D.图Ⅳ:湿润的有色布条褪色
14.实验室制取Cl 时,下列操作不正确的是( )
2
A.用装置Ⅰ制取少量Cl
2
B.用装置Ⅱ除去Cl 中的少量HCl
2
C.用装置Ⅲ制取Cl
2
D.用装置Ⅳ干燥Cl
2
15.如图所示仪器可用于实验室制备少量无水FeCl ,仪器连接顺序正确的是( )
3
A.a—b—c—d—e—f—g—h B.a—e—d—c—b—h—i—g
C.a—d—e—c—b—h—i—g D.a—c—b—d—e—h—i—f
二、填空题(本题包括3个小题,共40分)
16.(12分)实验室中用下列装置制FeCl ,可供选择的试剂有:①MnO ②NaOH溶液 ③饱和
3 2
NaCl溶液
④浓硫酸 ⑤浓盐酸。
(1)按气体流向由左到右排列,各装置的连接顺序为(填写A~E序号): 接 接 接 接。
(2)装置连接好后,应该首先进行的实验操作是 。
(3)A装置烧瓶中反应的离子方程式是 。
(4)E中盛装的试剂是 ,其作用是 。
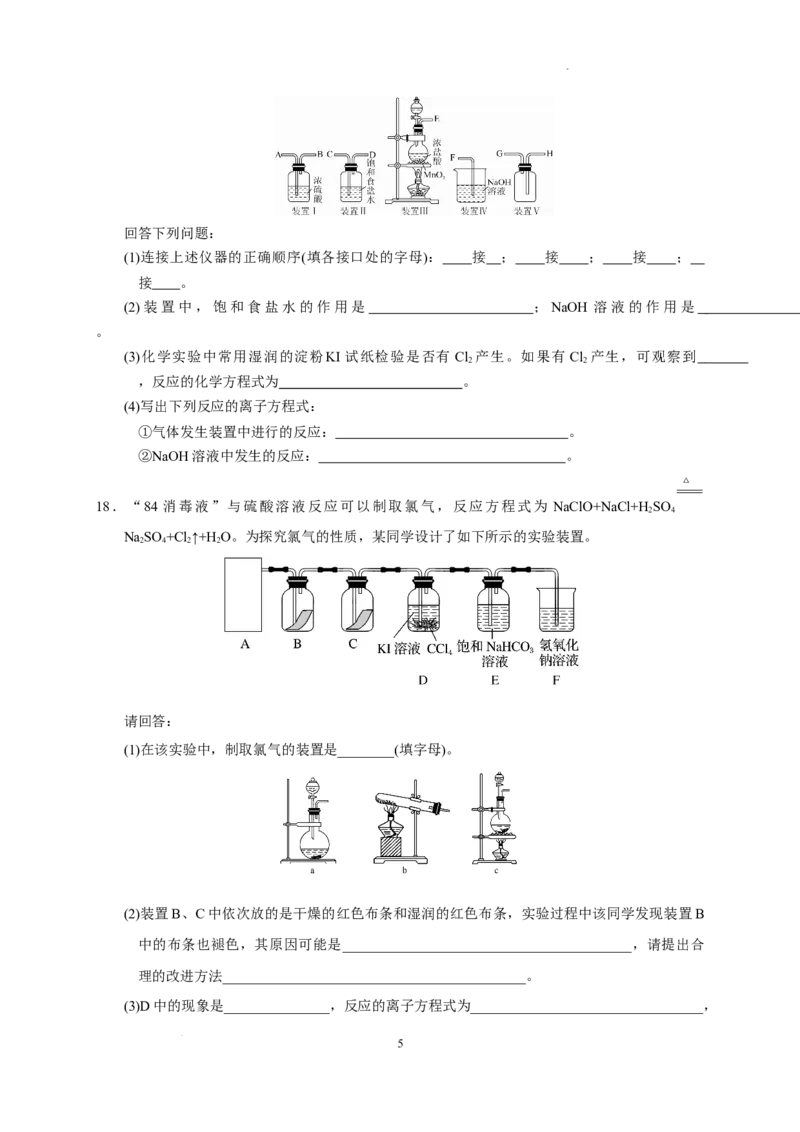
17.(14分)在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图
所示。
4
学科网(北京)股份有限公司回答下列问题:
(1)连接上述仪器的正确顺序(填各接口处的字母): 接 ; 接 ; 接 ;
接 。
(2)装置中,饱和食盐水的作用是 ;NaOH 溶液的作用是
。
(3)化学实验中常用湿润的淀粉KI 试纸检验是否有 Cl 产生。如果有 Cl 产生,可观察到
2 2
,反应的化学方程式为 。
(4)写出下列反应的离子方程式:
①气体发生装置中进行的反应: 。
②NaOH溶液中发生的反应: 。
18.“84 消毒液”与硫酸溶液反应可以制取氯气,反应方程式为 NaClO+NaCl+H SO
2 4
NaSO +Cl↑+H O。为探究氯气的性质,某同学设计了如下所示的实验装置。
2 4 2 2
请回答:
(1)在该实验中,制取氯气的装置是________(填字母)。
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B
中的布条也褪色,其原因可能是_________________________________________,请提出合
理的改进方法___________________________________________。
(3)D中的现象是_______________,反应的离子方程式为_________________________________,
5
学科网(北京)股份有限公司分离D中液体的方法是______________。
(4)写出氯气与NaOH溶液反应的离子方程式______________________________,该反应中氧化
剂与还原剂的个数之比为________。为验证尾气吸收后的溶液中存在 Cl−,正确的操作是
____________________。
(5)氯气通入饱和NaHCO 溶液能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明
3
Cl 与HO反应的产物中含有________。
2 2
1.答案:A
解析:Cl 的密度比空气的密度大,故应用向上排空气法收集 Cl ;由于浓HCl易挥发,故必须缓慢
2 2
加热以减少HCl的挥发; Cl 极易与碱反应:Cl +2NaOH===NaCl+NaClO+HO,故应用较浓的
2 2 2
碱液吸收多余的Cl。
2
2.答案:C
解析:集气瓶中使用单孔橡胶塞塞紧,只能进气,不能排气,则瓶内压强增大到一定程度,可能将
橡胶塞弹出,不安全,A项错误;因为Cl 的密度比空气大,Cl 应短管进,B项错误;该装置既能
2 2
收集Cl,又能进行尾气处理,C项正确;由于Cl 和NaOH反应,所以不能收集到Cl,D项错误。
2 2 2
3.答案:D
解析:Cl 通入饱和NaHCO 溶液反应生成CO ,引入新的杂质,并且消耗Cl ,A项不正确;实验
2 3 2 2
室制取Cl ,浓盐酸起到酸性和还原剂的作用,B项不正确;用饱和食盐水除去Cl 中的HCl气体时,
2 2
导气管应长进短出,C项不正确;实验室用排饱和食盐水法收集Cl 是因为Cl 难溶于饱和食盐水,
2 2
而能溶于水,D项正确。
4.答案:D
解析:氯气密度比空气大,可用向上排空气法收集氯气,①可用于氯气的收集,正确;氯气能溶于
水,难溶于饱和食盐水,可用饱和食盐水除去氯气中少量的氯化氢气体,②错误;氯气不具有漂白
性,③错误;氯气可与氢氧化钠溶液反应,④可用于实验室氯气的尾气吸收,正确。
5.答案:C
解析:用分液漏斗既可防止氯化氢挥发与氯气逸出污染环境,同时又可控制滴加盐酸的量和快慢,
从而控制反应速率,提高盐酸的利用率。
6.答案:C
解析:A项操作不正确,不能排除CO的干扰;B项操作不正确,因为Ag CO 跟HCl反应时,生成
2 3
的AgCl仍是白色沉淀;D项操作不正确,用盐酸酸化引入了Cl-,不能确定原溶液中是否有Cl-。
7.答案:B
解析:为验证干燥的氯气有无漂白性,就需要使进入到b装置中的氯气不含HCl及水蒸气,故应先
用饱和食盐水除去HCl,再用浓硫酸除去水蒸气,为防止e装置中的水蒸气进入b装置中,在b、e
6
学科网(北京)股份有限公司装置之间还应加装一个a装置,尾气用NaOH溶液吸收,故A、C两项错误,B项正确;本实验的
目的是验证干燥的Cl 是否具有漂白性,故不需要使用装置c,且Cl 使湿润的有色布条褪色是因为
2 2
氯气与水反应生成的HClO具有漂白性,D项错误。
8.答案:A
解析:能使澄清石灰水变浑浊的无色无味气体应是CO ,又因为加入稀HNO 后沉淀部分溶解,故
2 3
原溶液中除含有CO2-外,还有Cl-。
3
9.答案:D
解析:A项,浓盐酸在反应中表现还原性(生成Cl)和酸性(生成MnCl ),错误;B项,随反应的进
2 2
行,浓盐酸变为稀盐酸后反应将停止,故盐酸不能完全反应,HCl和MnO 都有剩余,错误;C项,
2
根据方程式计算,每消耗87 g MnO ,消耗146 g HCl,但被氧化的HCl应为73 g,错误;D项,为
2
避免高温下HCl挥发过多降低利用率,加热温度不宜过高,正确。
10.答案:D
解析:A.氯气密度大于空气,应采用向上排空气法收集,则导气管采用“长进短出”,故A错误;
B.HCl极易溶于水,氯气也能溶于水,应该用饱和食盐水洗气法除去氯气中的HCl,故B错误;C.
氯气没有漂白性,次氯酸有漂白性,该实验不能证明氯气有漂白性,故 C错误;D.氯气能和碱性物
质反应,可以用NaOH溶液吸收氯气,故D正确。
11.答案:A
解析:根据导管的进出长短可知试管①用于收集 Cl ,试管②用于防止NaOH溶液倒吸入①中,
2
NaOH溶液吸收多余的Cl,防止污染环境,①中收集到的Cl 不纯,混有HCl和水蒸气。
2 2
12.答案:D
解析:②中的NaOH溶液与Cl 反应,Cl 被吸收;③中的内部左边的导气管过短,右边的导气管过
2 2
长,这样Cl 不能通过该瓶;④中只有进气管没有出气管,一段时间后试管内压强增大,可能导致
2
橡胶塞弹开,有毒的Cl 逸出污染环境,且缺少加热装置酒精灯。
2
13.答案:D
解析:A.二氧化锰与浓盐酸反应,随着反应的进行,浓盐酸变稀,二氧化锰不与稀盐酸反应,即
使二氧化锰过量,盐酸也不能全部消耗完,A错误;B.图Ⅱ中溶液先变红后褪色,不仅能证明新
制氯水具有酸性,还可以证明新制氯水具有漂白性,B错误;C.铜丝在氯气中燃烧,生成棕黄色
的烟,不是雾,C错误;D.氯气没有漂白性,图Ⅳ中氯气遇到湿润有色布条与水反应生成HClO,
HClO具有漂白性,可使有色布条褪色,D正确;答案选D。
14.答案:D
解析:A.实验室制取Cl 用浓盐酸和MnO 反应,而不用稀盐酸;B.除去Cl 中的HCl气体用饱和食
2 2 2
盐水,NaHCO 溶液与Cl 反应并放出CO 气体,且气体应“长进短出”;C.MnO 与浓盐酸需在加
3 2 2 2
热条件下反应。
15.答案:B
7
学科网(北京)股份有限公司解析:按制气→除HCl→除HO→制备FeCl →吸收Cl 顺序连接。
2 3 2
16.答案:(1) AECBD (2)检查装置的气密性
(3) MnO+4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(4)饱和食盐水 除去氯化氢
解析:(1)要制备FeCl ,需先制备氯气,然后净化和干燥,再制备FeCl ,最后进行尾气吸收,所以
3 3
按气体流向由左到右排列,各装置的连接顺序为AECBD。(2)装置连接好后,应该首先进行的实验
操作是检查装置的气密性。(3)A装置是实验室制氯气的装置,烧瓶中反应的离子方程式是 MnO +
2
4H++2Cl-=====Mn2++Cl↑+2HO。(4)制备的氯气中有HCl和水蒸气,应先除HCl,E中盛装的
2 2
试剂是饱和食盐水,其作用是除去HCl。
17.答案: (1) E接C;D接A;B接H;G接F 。
(2)除去氯气中的HCl杂质 吸收过量的氯气
(3)试纸变蓝 2KI+Cl===2KCl+I
2 2
(4)①MnO +4H++2Cl-=====Mn2++Cl↑+2HO。
2 2 2
②2OH-+Cl===Cl-+ClO-+HO。
2 2
解析:装置Ⅲ为氯气的制取装置,二氧化锰和浓盐酸共热,反应生成氯化锰、氯气和水;浓盐酸具
有挥发性,选用装置Ⅱ除去氯气中混有的氯化氢;选用装置Ⅰ干燥氯气;氯气的密度比空气大,选
用装置Ⅴ收集氯气应该长进短出;氯气有毒,选用装置Ⅳ吸收氯气,防止污染环境。
(1) 氯 气 的 密 度 大 于 空 气 , 应 该 采 用 向 上 排 空 气 法 收 集 , 仪 器 连 接 顺 序 为
E→C→D→A→B→H→G→F。(2)氯气中混有氯化氢杂质,氯化氢能溶于饱和食盐水中,但是氯气
难溶,可以用饱和食盐水除去氯气中的氯化氢气体;氯气有毒,NaOH溶液的作用是吸收过量的氯
气,防止污染环境。(3)Cl 氧化KI生成碘,碘单质遇淀粉变蓝。(4)①气体发生装置中二氧化锰和
2
浓盐酸共热反应生成氯化锰、氯气和水,反应的离子方程式为MnO +4H++2Cl-=====Mn2++
2
Cl↑+2HO;②NaOH溶液与氯气反应生成氯化钠、次氯酸钠和水,反应的离子方程式为 2OH-+
2 2
Cl===Cl-+ClO-+HO。
2 2
18.答案: (1)c
(2)Cl 中混有少量HO(g) 在A~B之间增加装有浓HSO 的洗气瓶
2 2 2 4
(3)下层CCl 层呈紫红色 Cl+2I−===I +2Cl− 分液
4 2 2
(4)Cl +2OH−===Cl−+ClO−+H O 1∶1 取少量烧杯内吸收Cl 后的溶液,加入足量的稀
2 2 2
HNO 酸化,再加入AgNO 溶液,若有白色沉淀生成,证明其中含有Cl−
3 3
(5)盐酸
解解析析::(1)根据“固+液 气”原理可知应选择c装置制取Cl。(2)布条褪色证明Cl 中混有
2 2
HO(g),生成了HClO,应增加除HO(g)的装置。(3)Cl +2I−===I +2Cl−,CCl 将I 萃取出来,I 溶于
2 2 2 2 4 2 2
CCl ,溶液呈紫红色,分离两种互不相溶的液体采用分液法。(4)Cl 与NaOH溶液反应的离子方程
4 2
式为Cl+2OH−===Cl−+ClO−+H O,根据反应前后氯元素化合价变化可知Cl 既作氧化剂,又作还原
2 2 2
8
学科网(北京)股份有限公司剂,且物质的量之比为1∶1;检验Cl−,应先用稀HNO 酸化中和溶液中的OH−,并将ClO−转化为
3
HClO,再加AgNO 溶液,若有AgCl白色沉淀生成,证明含有Cl−。(5)因酸性HCl>HCO>
3 2 3
HClO,HCl与NaHCO 反应:HCl+NaHCO ===NaCl+HO+CO↑,而HClO不与NaHCO 反应,故
3 3 2 2 3
氯气与HO反应的产物中含盐酸。
2
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司