文档内容
【冲刺期末】高二化学期末单元复习测试
第四单元 化学反应与电能
(时间:90分钟 满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
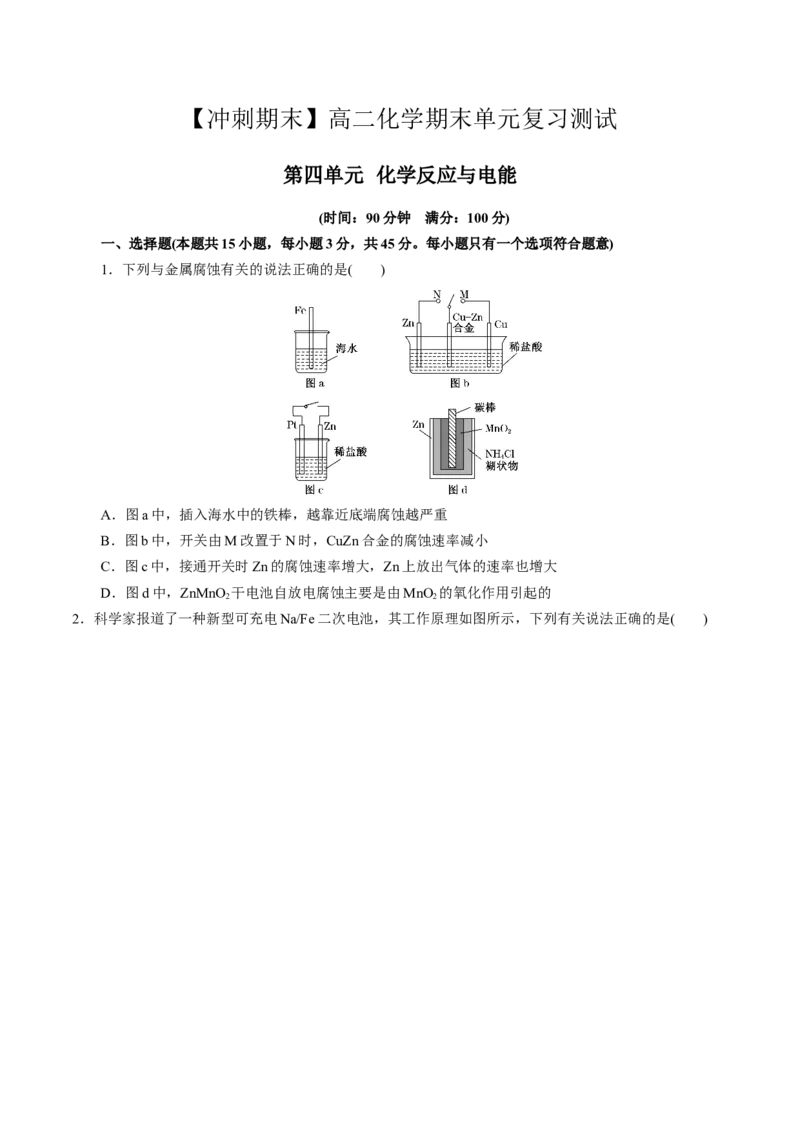
1.下列与金属腐蚀有关的说法正确的是( )
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,CuZn合金的腐蚀速率减小
C.图c中,接通开关时Zn的腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,ZnMnO 干电池自放电腐蚀主要是由MnO 的氧化作用引起的
2 2
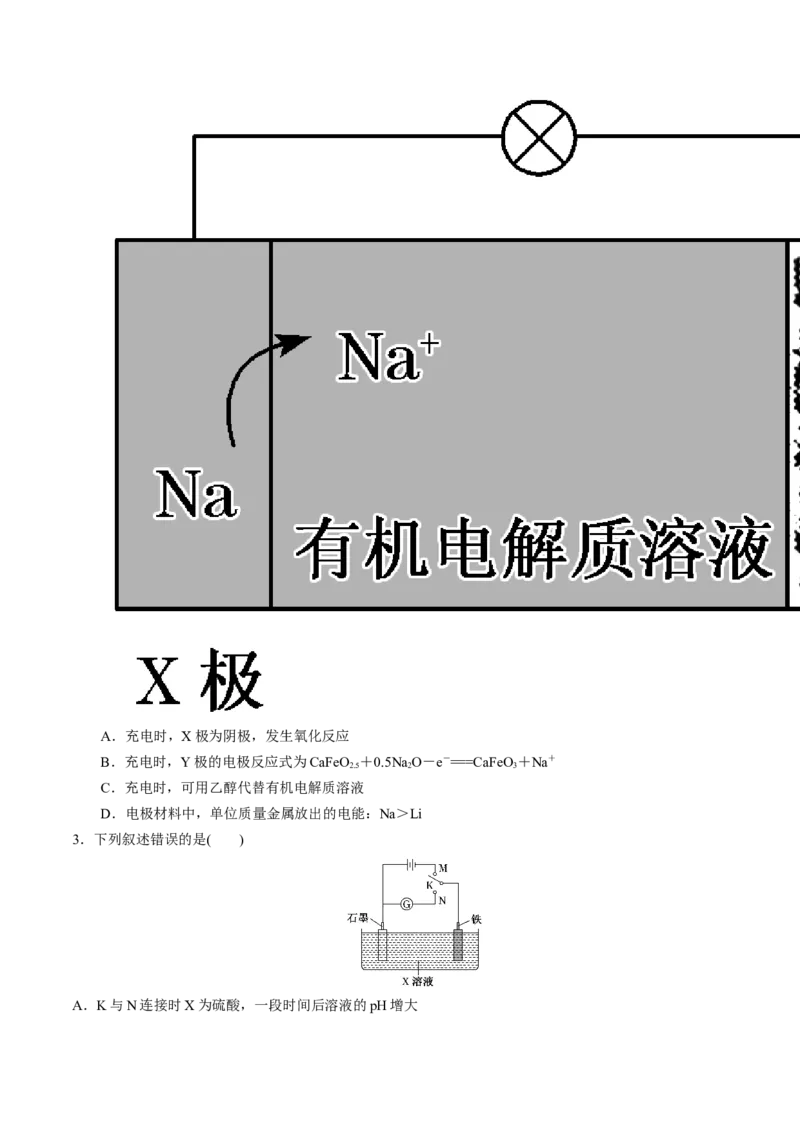
2.科学家报道了一种新型可充电Na/Fe二次电池,其工作原理如图所示,下列有关说法正确的是( )A.充电时,X极为阴极,发生氧化反应
B.充电时,Y极的电极反应式为CaFeO +0.5Na O-e-===CaFeO +Na+
2.5 2 3
C.充电时,可用乙醇代替有机电解质溶液
D.电极材料中,单位质量金属放出的电能:Na>Li
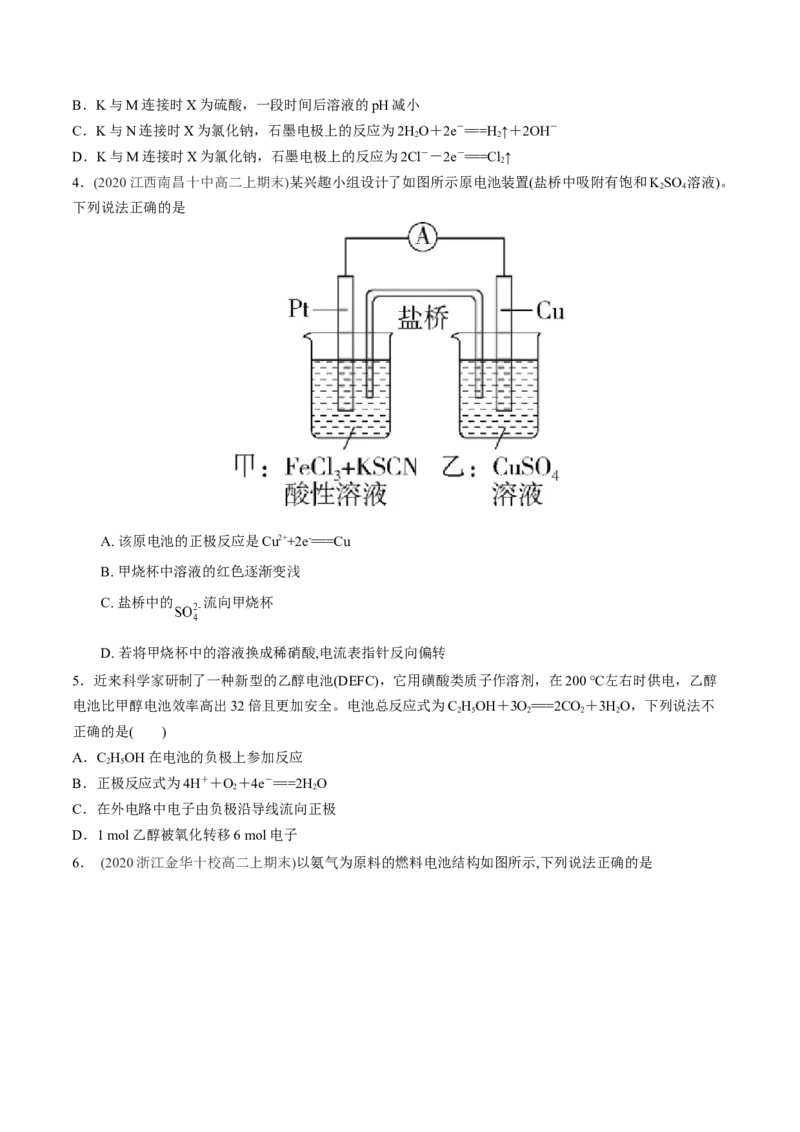
3.下列叙述错误的是( )
A.K与N连接时X为硫酸,一段时间后溶液的pH增大B.K与M连接时X为硫酸,一段时间后溶液的pH减小
C.K与N连接时X为氯化钠,石墨电极上的反应为2HO+2e-===H ↑+2OH-
2 2
D.K与M连接时X为氯化钠,石墨电极上的反应为2Cl--2e-===Cl↑
2
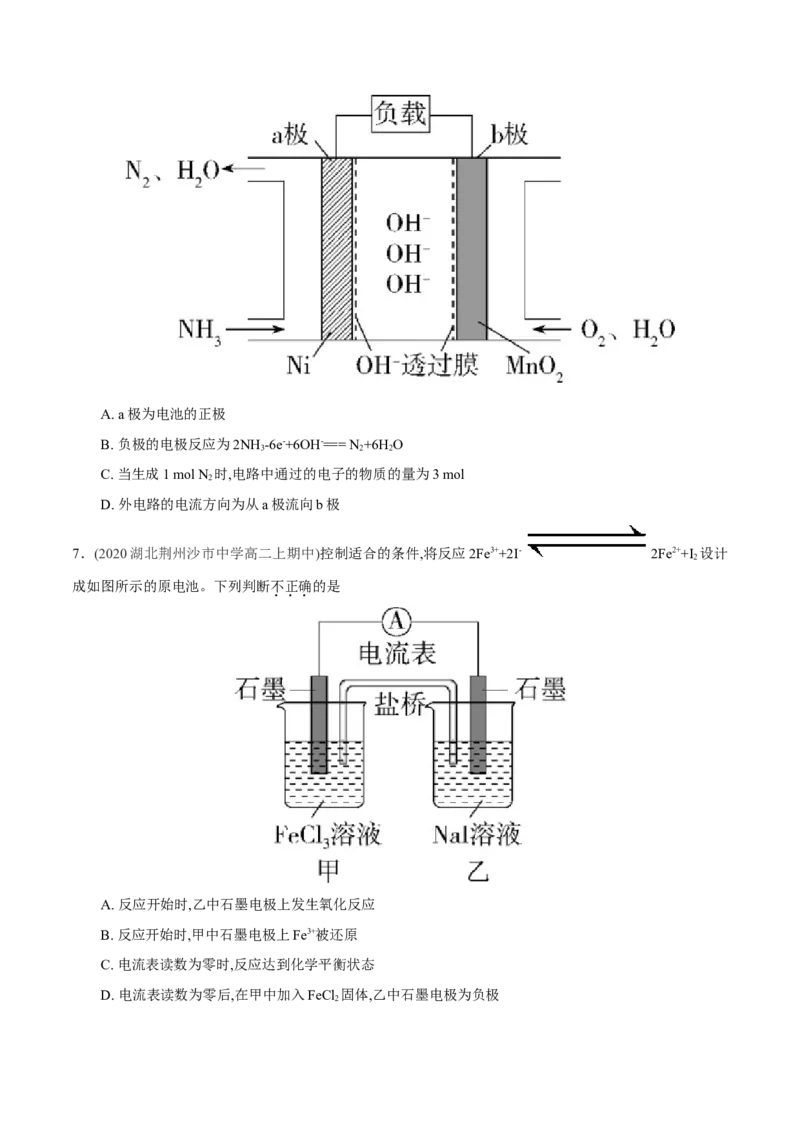
4.(2020江西南昌十中高二上期末)某兴趣小组设计了如图所示原电池装置(盐桥中吸附有饱和KSO 溶液)。
2 4
下列说法正确的是
A. 该原电池的正极反应是Cu2++2e-===Cu
B. 甲烧杯中溶液的红色逐渐变浅
C. 盐桥中的 流向甲烧杯
D. 若将甲烧杯中的溶液换成稀硝酸,电流表指针反向偏转
5.近来科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子作溶剂,在200 ℃左右时供电,乙醇
电池比甲醇电池效率高出32倍且更加安全。电池总反应式为C HOH+3O===2CO +3HO,下列说法不
2 5 2 2 2
正确的是( )
A.C HOH在电池的负极上参加反应
2 5
B.正极反应式为4H++O+4e-===2H O
2 2
C.在外电路中电子由负极沿导线流向正极
D.1 mol乙醇被氧化转移6 mol电子
6. (2020浙江金华十校高二上期末)以氨气为原料的燃料电池结构如图所示,下列说法正确的是A. a极为电池的正极
B. 负极的电极反应为2NH -6e-+6OH-=== N +6H O
3 2 2
C. 当生成1 mol N 时,电路中通过的电子的物质的量为3 mol
2
D. 外电路的电流方向为从a极流向b极
7.(2020湖北荆州沙市中学高二上期中)控制适合的条件,将反应2Fe3++2I- 2Fe2++I 设计
2
成如图所示的原电池。下列判断不正确的是
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 反应开始时,甲中石墨电极上Fe3+被还原
C. 电流表读数为零时,反应达到化学平衡状态
D. 电流表读数为零后,在甲中加入FeCl 固体,乙中石墨电极为负极
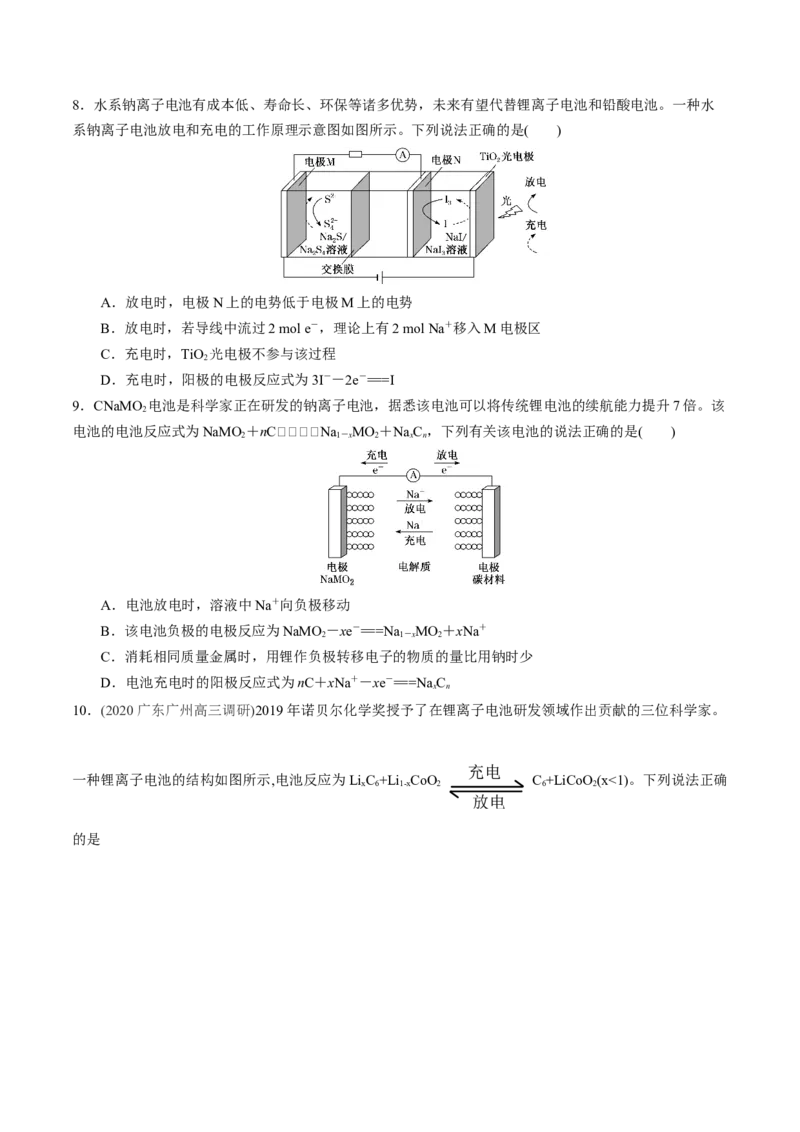
28.水系钠离子电池有成本低、寿命长、环保等诸多优势,未来有望代替锂离子电池和铅酸电池。一种水
系钠离子电池放电和充电的工作原理示意图如图所示。下列说法正确的是( )
A.放电时,电极N上的电势低于电极M上的电势
B.放电时,若导线中流过2 mol e-,理论上有2 mol Na+移入M电极区
C.充电时,TiO 光电极不参与该过程
2
D.充电时,阳极的电极反应式为3I--2e-===I
9.CNaMO 电池是科学家正在研发的钠离子电池,据悉该电池可以将传统锂电池的续航能力提升7倍。该
2
电池的电池反应式为NaMO +nCNa MO +NaC ,下列有关该电池的说法正确的是( )
2 1-x 2 x n
A.电池放电时,溶液中Na+向负极移动
B.该电池负极的电极反应为NaMO -xe-===Na MO +xNa+
2 1-x 2
C.消耗相同质量金属时,用锂作负极转移电子的物质的量比用钠时少
D.电池充电时的阳极反应式为nC+xNa+-xe-===NaC
x n
10.(2020广东广州高三调研)2019年诺贝尔化学奖授予了在锂离子电池研发领域作出贡献的三位科学家。
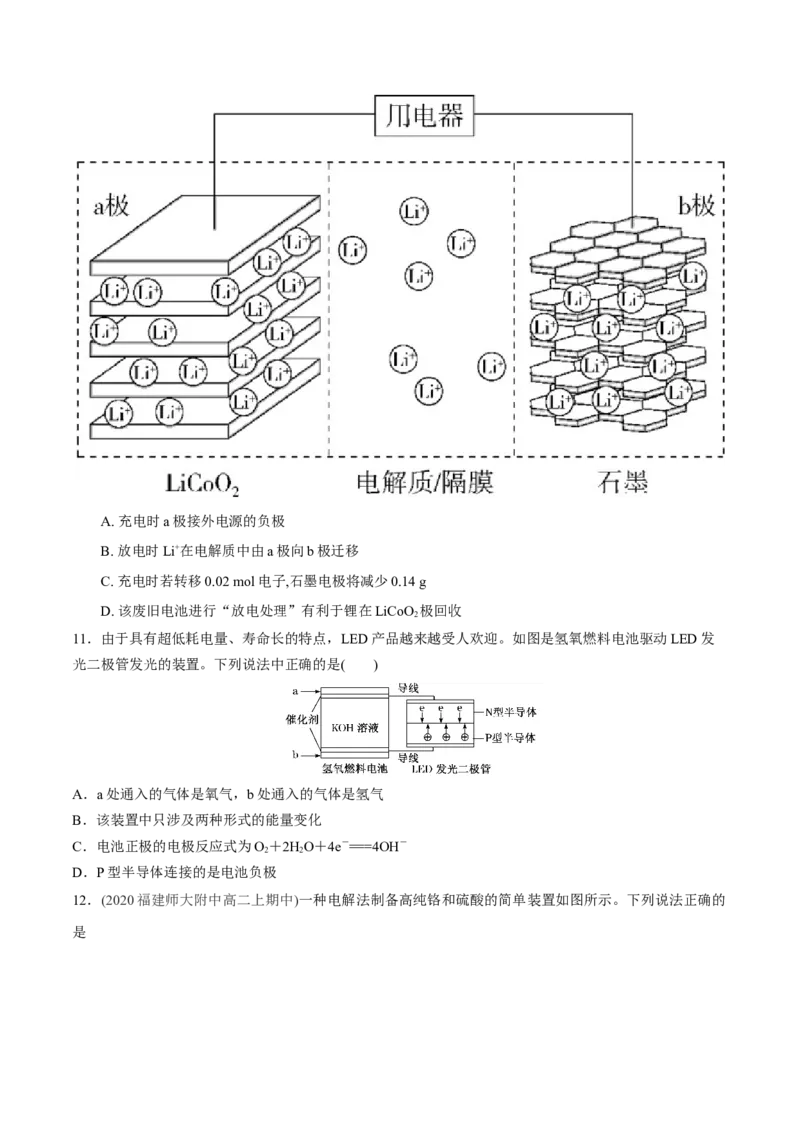
充电
一种锂离子电池的结构如图所示,电池反应为LiC +Li CoO C +LiCoO(x<1)。下列说法正确
x 6 1-x 2 6 2
放电
的是A. 充电时a极接外电源的负极
B. 放电时Li+在电解质中由a极向b极迁移
C. 充电时若转移0.02 mol电子,石墨电极将减少0.14 g
D. 该废旧电池进行“放电处理”有利于锂在LiCoO 极回收
2
11.由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎。如图是氢氧燃料电池驱动LED发
光二极管发光的装置。下列说法中正确的是( )
A.a处通入的气体是氧气,b处通入的气体是氢气
B.该装置中只涉及两种形式的能量变化
C.电池正极的电极反应式为O+2HO+4e-===4OH-
2 2
D.P型半导体连接的是电池负极
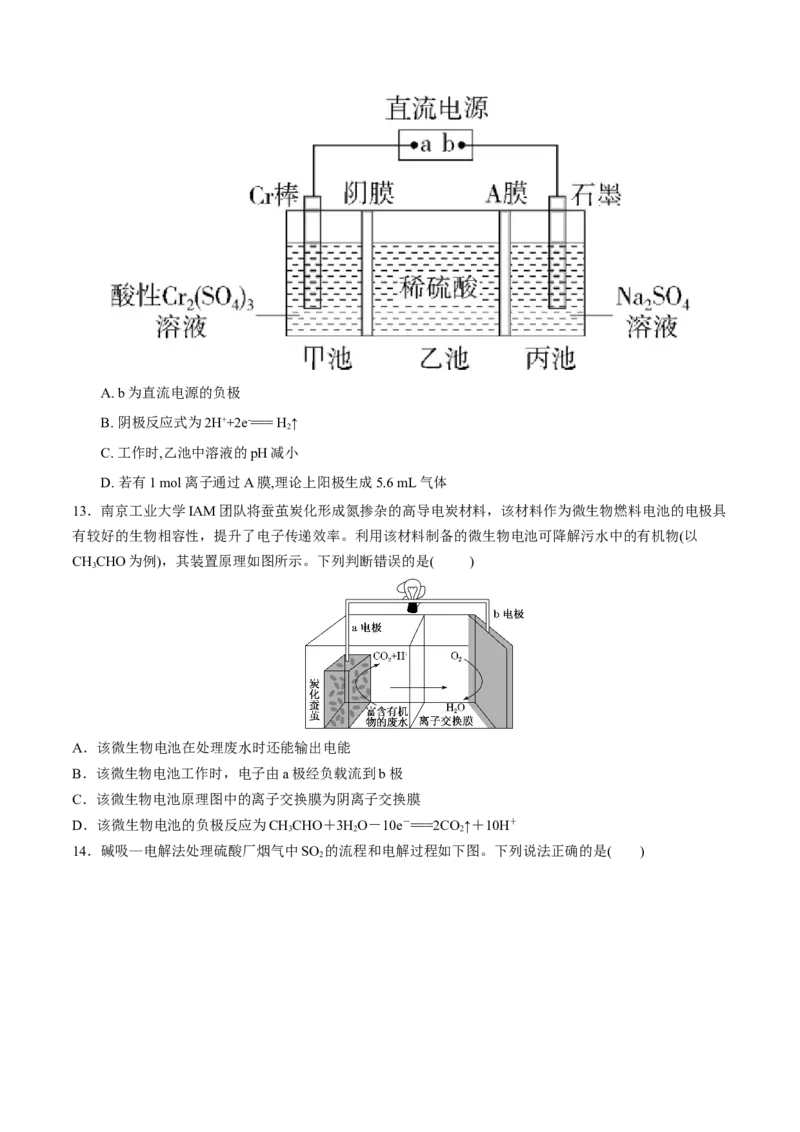
12.(2020福建师大附中高二上期中)一种电解法制备高纯铬和硫酸的简单装置如图所示。下列说法正确的
是A. b为直流电源的负极
B. 阴极反应式为2H++2e-=== H ↑
2
C. 工作时,乙池中溶液的pH减小
D. 若有1 mol离子通过A膜,理论上阳极生成5.6 mL气体
13.南京工业大学IAM团队将蚕茧炭化形成氮掺杂的高导电炭材料,该材料作为微生物燃料电池的电极具
有较好的生物相容性,提升了电子传递效率。利用该材料制备的微生物电池可降解污水中的有机物(以
CHCHO为例),其装置原理如图所示。下列判断错误的是( )
3
A.该微生物电池在处理废水时还能输出电能
B.该微生物电池工作时,电子由a极经负载流到b极
C.该微生物电池原理图中的离子交换膜为阴离子交换膜
D.该微生物电池的负极反应为CHCHO+3HO-10e-===2CO ↑+10H+
3 2 2
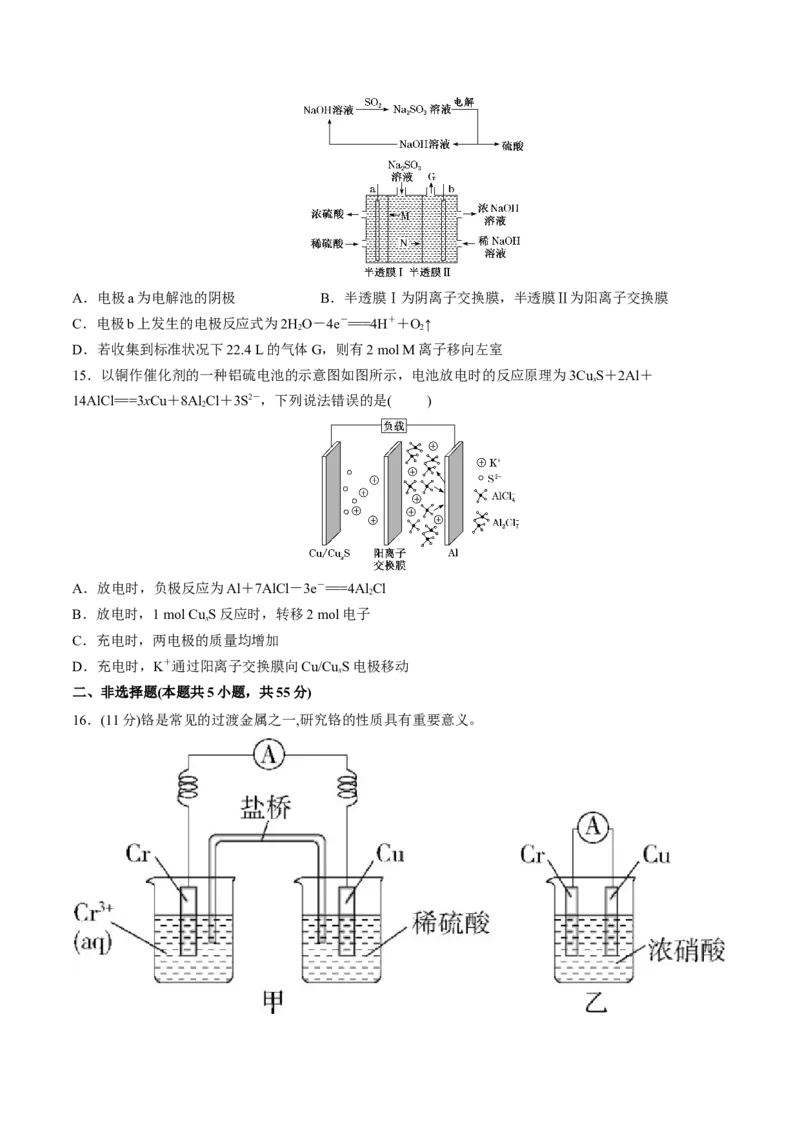
14.碱吸—电解法处理硫酸厂烟气中SO 的流程和电解过程如下图。下列说法正确的是( )
2A.电极a为电解池的阴极 B.半透膜Ⅰ为阴离子交换膜,半透膜Ⅱ为阳离子交换膜
C.电极b上发生的电极反应式为2HO-4e-===4H++O↑
2 2
D.若收集到标准状况下22.4 L的气体G,则有2 mol M离子移向左室
15.以铜作催化剂的一种铝硫电池的示意图如图所示,电池放电时的反应原理为3CuS+2Al+
x
14AlCl===3xCu+8Al Cl+3S2-,下列说法错误的是( )
2
A.放电时,负极反应为Al+7AlCl-3e-===4AlCl
2
B.放电时,1 mol CuS反应时,转移2 mol电子
x
C.充电时,两电极的质量均增加
D.充电时,K+通过阳离子交换膜向Cu/CuS电极移动
x
二、非选择题(本题共5小题,共55分)
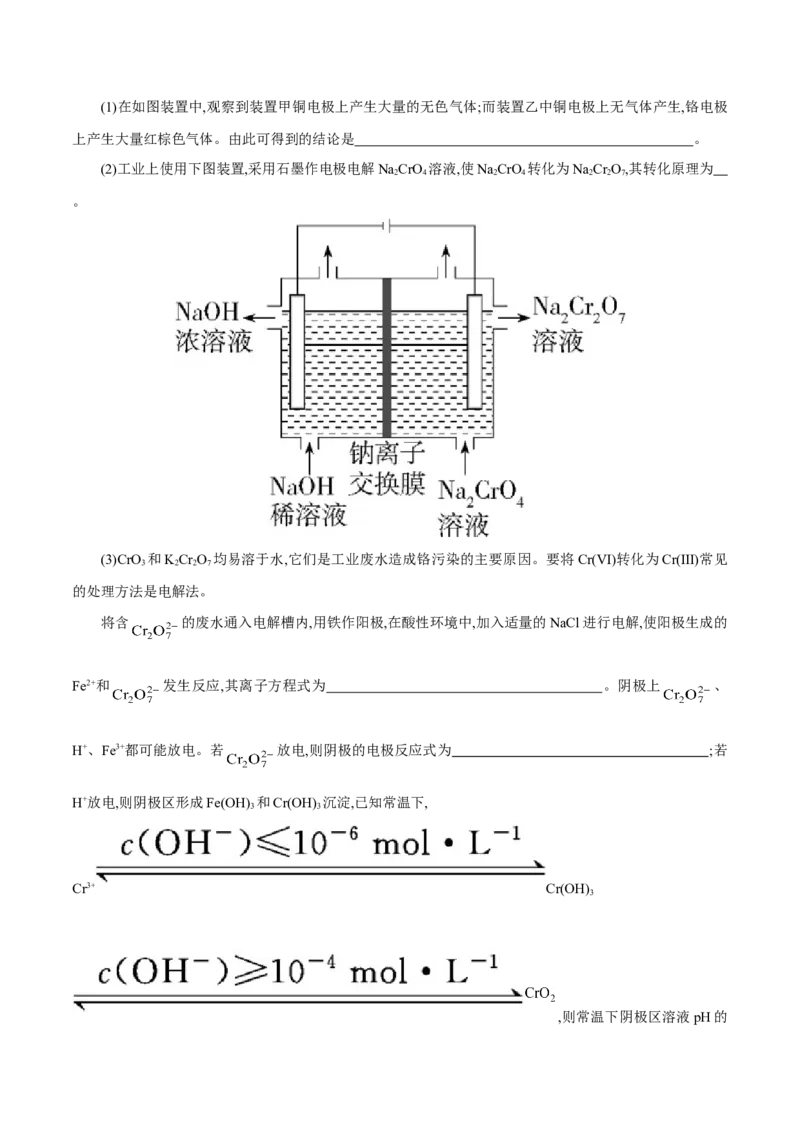
16.(11分)铬是常见的过渡金属之一,研究铬的性质具有重要意义。(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极
上产生大量红棕色气体。由此可得到的结论是 。
(2)工业上使用下图装置,采用石墨作电极电解NaCrO 溶液,使NaCrO 转化为NaCr O,其转化原理为
2 4 2 4 2 2 7
。
(3)CrO 和KCr O 均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见
3 2 2 7
的处理方法是电解法。
将含 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极生成的
Fe2+和 发生反应,其离子方程式为 。阴极上 、
H+、Fe3+都可能放电。若 放电,则阴极的电极反应式为 ;若
H+放电,则阴极区形成Fe(OH) 和Cr(OH) 沉淀,已知常温下,
3 3
Cr3+ Cr(OH)
3
,则常温下阴极区溶液pH的范围为 。
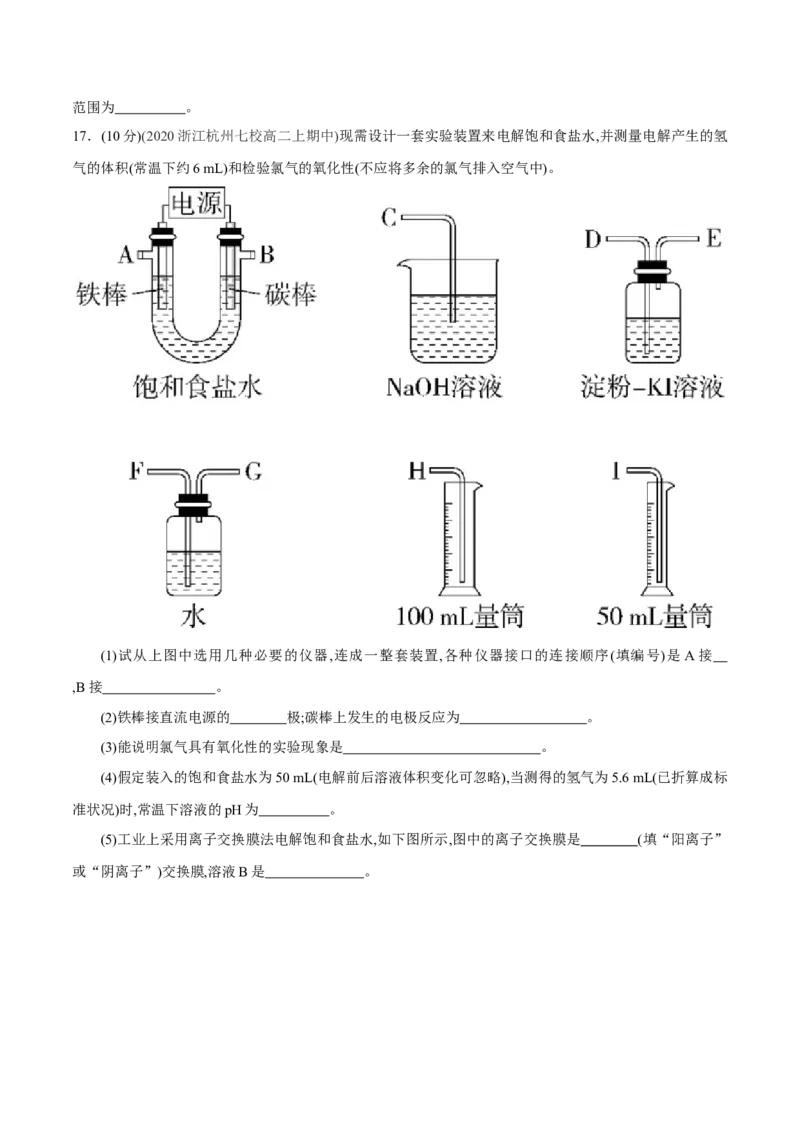
17.(10分)(2020浙江杭州七校高二上期中)现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢
气的体积(常温下约6 mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
(1)试从上图中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是A接
,B接 。
(2)铁棒接直流电源的 极;碳棒上发生的电极反应为 。
(3)能说明氯气具有氧化性的实验现象是 。
(4)假定装入的饱和食盐水为50 mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6 mL(已折算成标
准状况)时,常温下溶液的pH为 。
(5)工业上采用离子交换膜法电解饱和食盐水,如下图所示,图中的离子交换膜是 (填“阳离子”
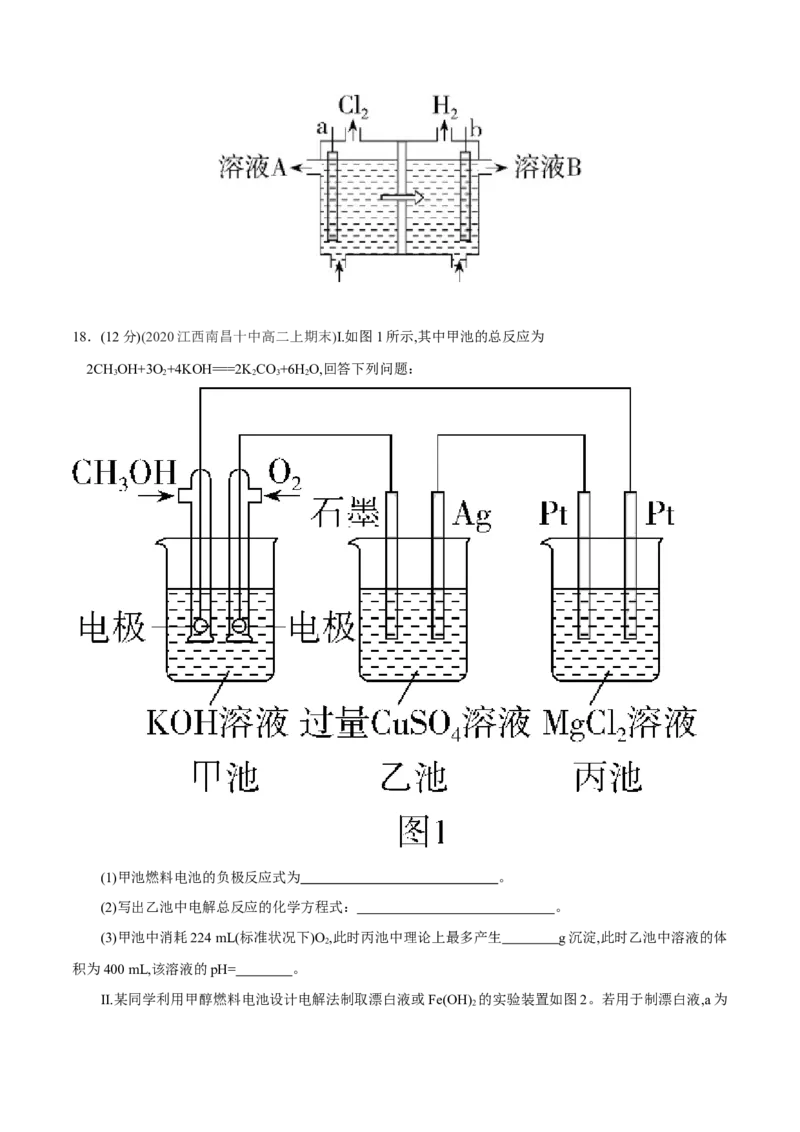
或“阴离子”)交换膜,溶液B是 。18.(12分)(2020江西南昌十中高二上期末)Ⅰ.如图1所示,其中甲池的总反应为
2CHOH+3O +4KOH===2KCO+6H O,回答下列问题:
3 2 2 3 2
(1)甲池燃料电池的负极反应式为 。
(2)写出乙池中电解总反应的化学方程式: 。
(3)甲池中消耗224 mL(标准状况下)O ,此时丙池中理论上最多产生 g沉淀,此时乙池中溶液的体
2
积为400 mL,该溶液的pH= 。
Ⅱ.某同学利用甲醇燃料电池设计电解法制取漂白液或Fe(OH) 的实验装置如图2。若用于制漂白液,a为
2电池的 极,电解质溶液最好用 。若用于制Fe(OH) ,使用硫酸钠溶液作电解质溶液,阳极
2
选用 作电极。
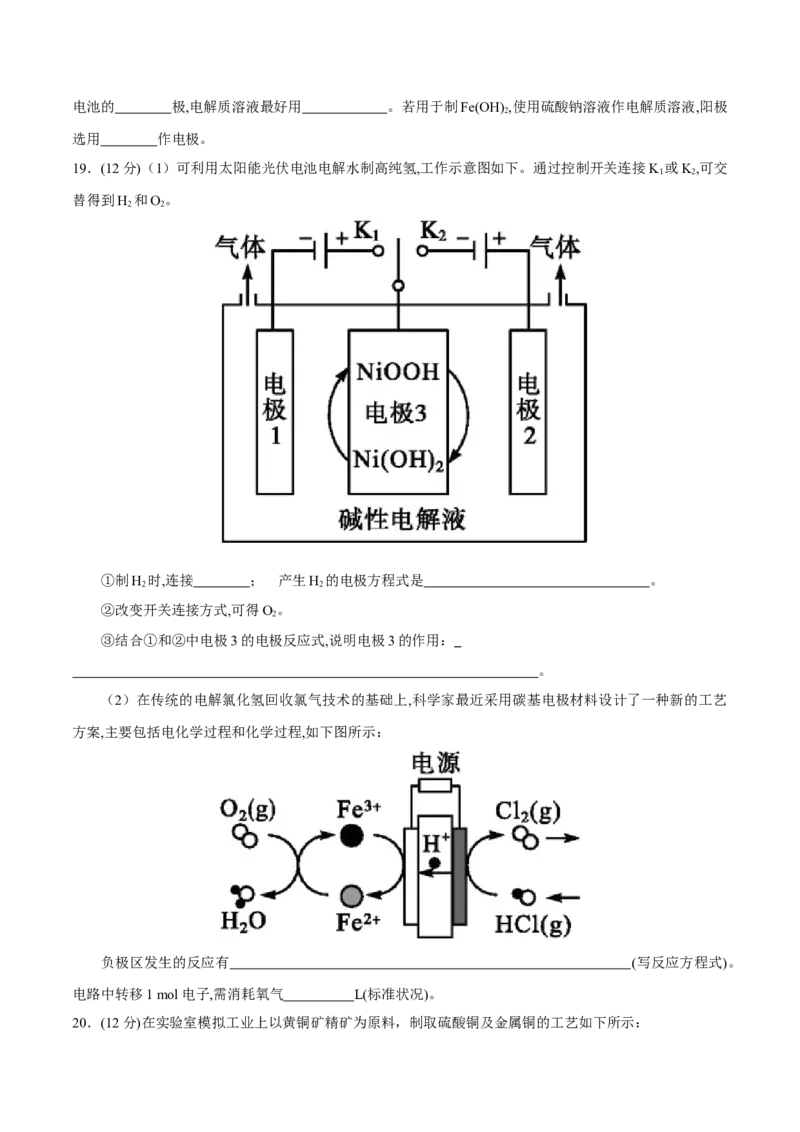
19.(12分)(1)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K 或K,可交
1 2
替得到H 和O。
2 2
①制H 时,连接 ; 产生H 的电极方程式是 。
2 2
②改变开关连接方式,可得O。
2
③结合①和②中电极3的电极反应式,说明电极3的作用:
。
(2)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺
方案,主要包括电化学过程和化学过程,如下图所示:
负极区发生的反应有 (写反应方程式)。
电路中转移1 mol电子,需消耗氧气 L(标准状况)。
20.(12分)在实验室模拟工业上以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:Ⅰ.将黄铜矿精矿(主要成分为CuFeS,含有少量CaO、MgO、Al O)粉碎。
2 2 3
Ⅱ.采用如下装置进行电化学浸出实验。
将精选黄铜矿粉加入电解槽阳极区,匀速搅拌,使矿粉溶解。在阴极区通入氧气,并加入少量催化剂。
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)发生反应:
2RH(有机相)+Cu2+(水相)
R Cu(有机相)+2H+(水相)
2
分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ.电解硫酸铜溶液制得金属铜。
(1)精选黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
CuFeS+4H+===Cu2++Fe2++2HS
2 2
2Fe3++HS===2Fe2++S↓+2H+
2
①阳极区硫酸铁的主要作用是____________________。
②电解过程中,阳极区Fe3+的浓度基本保持不变,原因是________________________(填离子方程式)。
(2)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是________;加入有机萃取剂的目的是
____________________________________________________。
(3)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是
________________________________________________________________________
________________________________________________________________________。
(4)步骤Ⅳ,若电解200 mL 0.5 mol·L-1的CuSO 溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的
4
顺序是______________。(忽略电解前后溶液体积的变化)