文档内容
河南省天立教育2025—2026学年度秋期高二年级期中联考
化学试题卷
本试题卷共6页,两大题,19小题,满分100分。考试时间75分钟。
注意事项:
1. 答卷前,考生务必将自己的姓名、班级、考场号、座位号、考生号填写在答题卡上。
2. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,
再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3. 考试结束后,将本试题卷和答题卡一并交回。
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 加入MnO2 能加快H2O2 分解
C. 在NO2 生成N2O4 的反应中,升高温度,红棕色加深
D. 溴水中存在平衡Br2 +H2O⇌HBr+HBrO,当加入少量AgNO3 固体后,溶液颜色
变浅
2. 下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热ΔH为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B. S(g)+O2(g)=SO2(g) ΔH1 ,S(s)+O2(g)=SO2(g) ΔH2 ,则ΔH1 <ΔH2
C. 500 ℃、30 MPa下,将0.5 mol N2 和1.5 mol H2 置于密闭的容器中充分反应生成
NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)=2NH3(g) ΔH=-38.6 kJ·mol-1
D. 已知25 ℃、101 kPa条件下:4Al(s)+3O2(g)=2Al2O3(s) ΔH=-2834.9 kJ·mol
-1,4Al(s)+2O3(g)=2Al2O3(s) ΔH=-3119.1 kJ·mol-1,则O3 比O2 稳定
3. 溶液的酸碱性对人类的生产、生活有十分重要的影响。下列有关叙述中正确的是
A. 室温下,pH=3的HNO3 溶液与pH=11的KOH溶液等体积混合后的溶液中:c
平
(H+)<c (OH-)
平
B. 室温下,将1 mL 1×10-6 mol·L-1的稀盐酸稀释至1000 mL,所得溶液的pH为9
C. 将pH=2的盐酸稀释一倍后,pH变为2.3(已知lg 2=0.3)
D. 将pH=2的盐酸与醋酸溶液各1 mL分别稀释至100 mL。所得醋酸溶液的pH更大
4. 在1 L的恒温密闭容器中,充入3 mol A和3 mol B发生反应2A(s)+3B(g)⇌C(g)+2D(g),经4 min后B的物质的量
减少1.2 mol。下列说法正确的是
A. 用B表示4 min末的反应速率是0.3 mol·L-1·min-1
B. 4 min时物质A的浓度为2.2 mol·L-1C. 不同条件下反应速率分别为:v(B)=0.03 mol·L-1·s-1,v(C)=0.1 mol·L-1·min-
1,则v(B)>v(C)
D. 当时3v (B)=2v (D),表明该反应已达到平衡
正 逆
5. 设NA 代表阿伏加德罗常数的值,下列叙述正确的是
A. 2 mol NO和1 mol O2 混合后,体系中的分子总数小于2NA
B. 2 mol SO2 与0.5 mol O2 充分反应生成的SO3 分子数为NA
C. 32 g氧气和臭氧的混合气体中含有的氧原子数目为1.5NA
D. 1 mol H2 和1 mol I2 于密闭容器中充分反应后,其分子总数小于2NA
6. 将甲醇蒸气转化为氢气的两种反应原理如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是
A. CH3OH的燃烧热为192.9 kJ·mol-1
B. 64 g CH3OH(g)按照反应①制取氢气,吸收能量49 kJ
C. 根据①和②推知:H2(g)+ O2(g)=H2O(g) ΔH=-241.9 kJ·mol-1
D. CH3OH(l)+ O2(g)=CO2(g)+2H2(g) ΔH<-192.9 kJ·mol-1
7. 肼(N2H4)与氧化剂剧烈反应,释放大量的热量,可作火箭燃料。已知下列反应:
①2NH3(g)+3N2O(g)=4N2 +3H2O(l) ΔH1 =-a kJ·mol-1
②N2O(g)+3H2(g)=N2H4(l)+H2O(l) ΔH2 =-b kJ·mol-1
③N2H4(l)+9H2(g)+4O2(g)=2NH3(g)+8H2O(l) ΔH3 =-c kJ·mol-1
则反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的ΔH(kJ·mol-1)为
A. (a-3b+c) B. (a+3b-c) C. (c-a-
3b)D. (3b-a-c)
8. 一定条件下,合成氨反应:N2(g)+3H2(g)⇌2NH3(g)。图1为该反应的能量变化图;图2表示在2 L的恒容密闭容
器中反应时N2 的物质的量随时间的变化曲线;图3表示在其他条件不变的情况下,改变起始物H2 的物质的量对
该反应平衡的影响。下列说法正确的是
A. 工业合成氨采用400~500℃是为了加快反应速率和提高反应物的转化率
B. 由图1可知,活化分子变成2 mol生成物分子放出的能量为92 kJC. 由图2信息,从11 min起其他条件不变,增加N2 的量,n(N2)则的变化曲线为c
D. 图3中温度:T1 <T2 ,e、f、g三点所处的平衡状态中,反应物N2 的转化率最高
的是g点
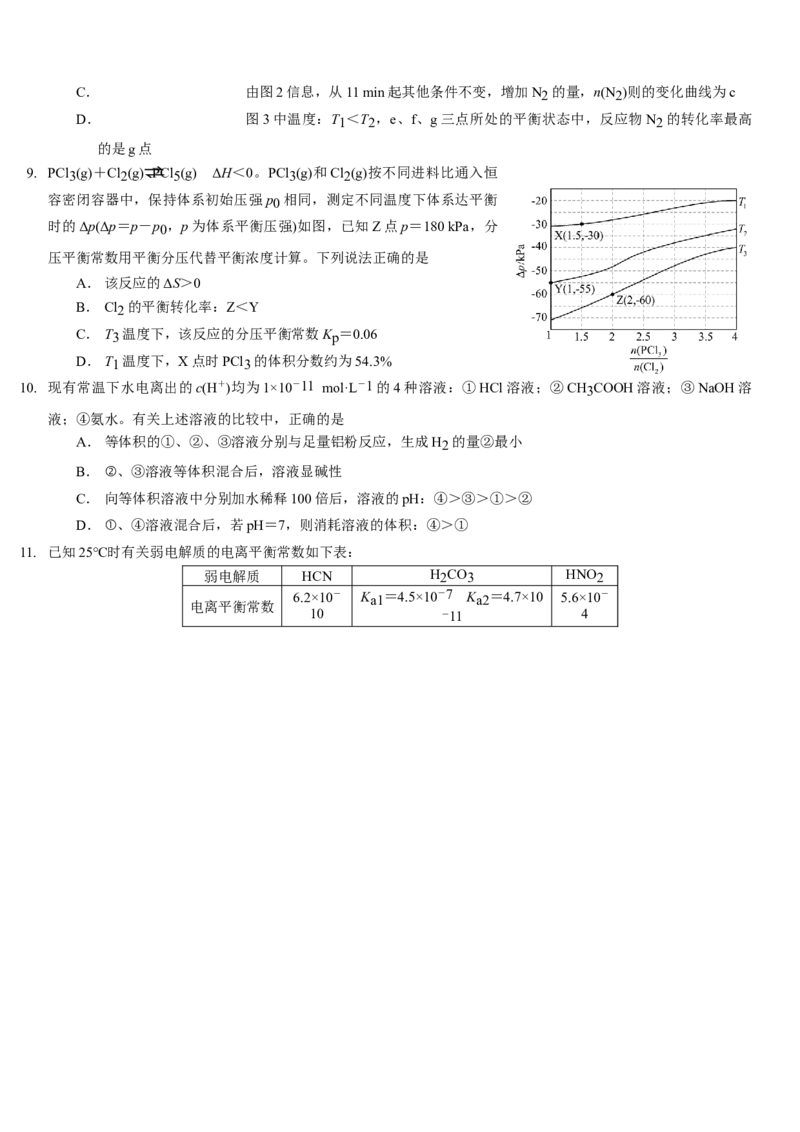
9. PCl3(g)+Cl2(g)⇌PCl5(g) ΔH<0。PCl3(g)和Cl2(g)按不同进料比通入恒
容密闭容器中,保持体系初始压强p0 相同,测定不同温度下体系达平衡
时的Δp(Δp=p-p0 ,p为体系平衡压强)如图,已知Z点p=180 kPa,分
压平衡常数用平衡分压代替平衡浓度计算。下列说法正确的是
A.该反应的ΔS>0
B. Cl2 的平衡转化率:Z<Y
C. T3 温度下,该反应的分压平衡常数Kp =0.06
D.T1 温度下,X点时PCl3 的体积分数约为54.3%
10. 现有常温下水电离出的c(H+)均为1×10-11 mol·L-1的4种溶液:①HCl溶液;②CH3COOH溶液;③NaOH溶
液;④氨水。有关上述溶液的比较中,正确的是
A.等体积的①、②、③溶液分别与足量铝粉反应,生成H2 的量②最小
B. ②、③溶液等体积混合后,溶液显碱性
C. 向等体积溶液中分别加水稀释100倍后,溶液的pH:④>③>①>②
D.①、④溶液混合后,若pH=7,则消耗溶液的体积:④>①
11. 已知25℃时有关弱电解质的电离平衡常数如下表:
弱电解质 HCN H2CO3 HNO2
6.2×10- Ka1 =4.5×10-7 Ka2 =4.7×10 5.6×10-
电离平衡常数
10 -11 4下列说法正确的是
A.相同温度,1 mol·L-1的HX溶液的pKa 大于0.1 mol·L-1的HX溶液的pKa
B. NaCN溶液与少量CO2 反应的离子反应方程式为2CN-+CO2 +H2O=CO2
3
-+2HCN
C. 结合H+的能力:NO->HCO->CN->CO2-
2 3 3
D.25℃时,0.1 mol·L-1的HCN溶液中c(H+)= mol·L-1
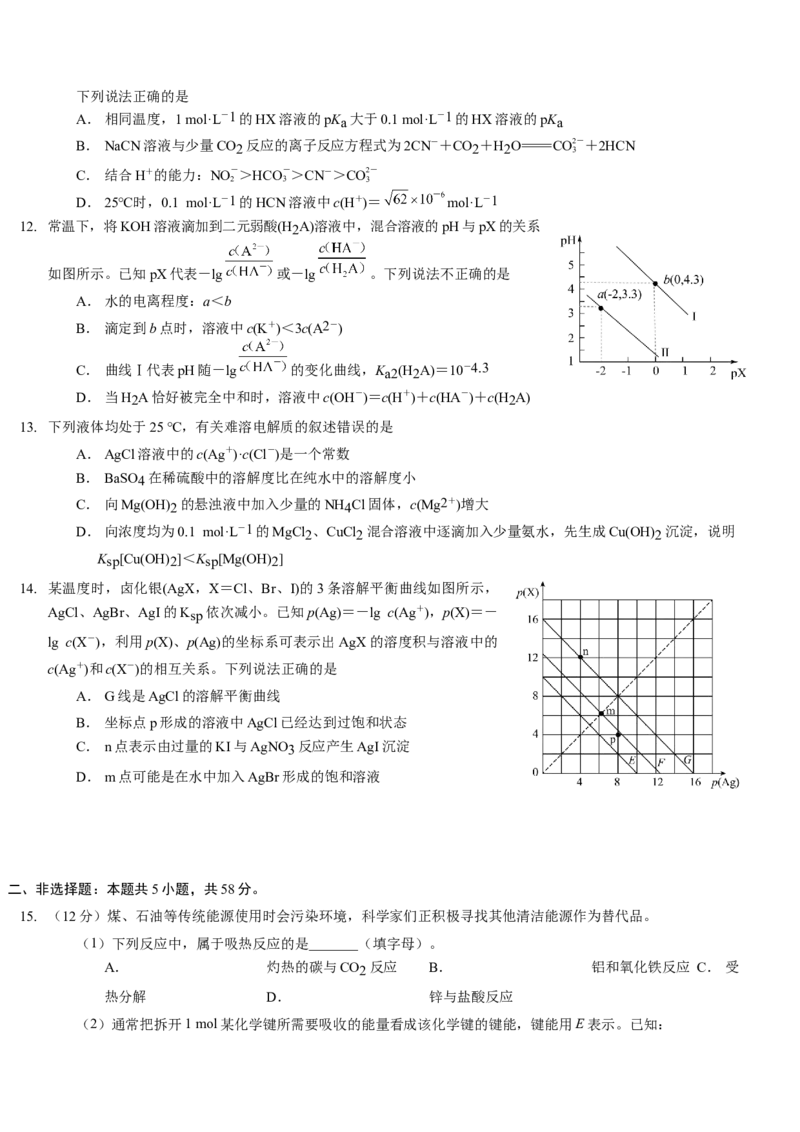
12. 常温下,将KOH溶液滴加到二元弱酸(H2A)溶液中,混合溶液的pH与pX的关系
如图所示。已知pX代表-lg 或-lg 。下列说法不正确的是
A.水的电离程度:a<b
B. 滴定到b点时,溶液中c(K+)<3c(A2-)
C. 曲线Ⅰ代表pH随-lg 的变化曲线,Ka2(H2A)=10-4.3
D.当H2A恰好被完全中和时,溶液中c(OH-)=c(H+)+c(HA-)+c(H2A)
13. 下列液体均处于25 ℃,有关难溶电解质的叙述错误的是
A.AgCl溶液中的c(Ag+)·c(Cl-)是一个常数
B. BaSO4 在稀硫酸中的溶解度比在纯水中的溶解度小
C. 向Mg(OH)2 的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
D.向浓度均为0.1 mol·L-1的MgCl2 、CuCl2 混合溶液中逐滴加入少量氨水,先生成Cu(OH)2 沉淀,说明
Ksp[Cu(OH)2]<Ksp[Mg(OH)2]
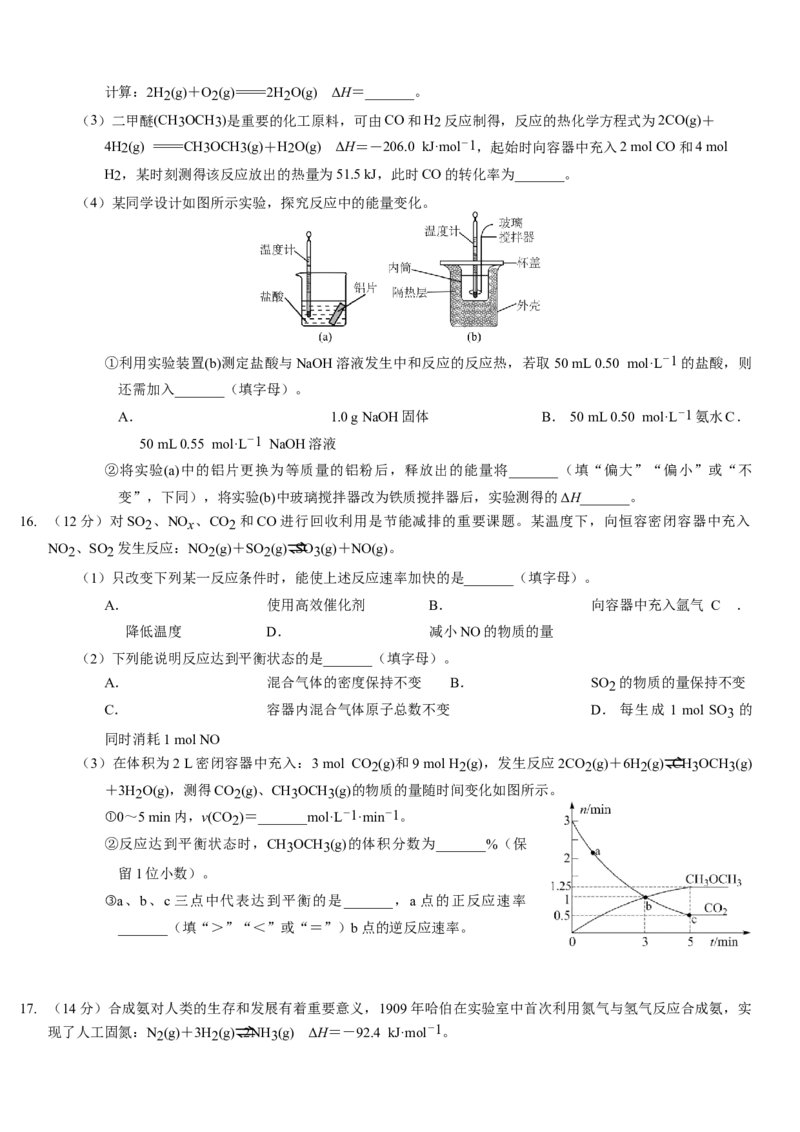
14. 某温度时,卤化银(AgX,X=Cl、Br、I)的3条溶解平衡曲线如图所示,
AgCl、AgBr、AgI的Ksp 依次减小。已知p(Ag)=-lg c(Ag+),p(X)=-
lg c(X-),利用p(X)、p(Ag)的坐标系可表示出AgX的溶度积与溶液中的
c(Ag+)和c(X-)的相互关系。下列说法正确的是
A.G线是AgCl的溶解平衡曲线
B. 坐标点p形成的溶液中AgCl已经达到过饱和状态
C. n点表示由过量的KI与AgNO3 反应产生AgI沉淀
D.m点可能是在水中加入AgBr形成的饱和溶液
二、非选择题:本题共5小题,共58分。
15. (12分)煤、石油等传统能源使用时会污染环境,科学家们正积极寻找其他清洁能源作为替代品。
(1)下列反应中,属于吸热反应的是_______(填字母)。
A. 灼热的碳与CO2 反应 B. 铝和氧化铁反应 C. 受
热分解 D. 锌与盐酸反应
(2)通常把拆开1 mol某化学键所需要吸收的能量看成该化学键的键能,键能用E表示。已知:化学键 H—H OO O—H
E/(kJ·mol-
436 497.3 462.8
1)计算:2H2(g)+O2(g)=2H2O(g) ΔH=_______。
(3)二甲醚(CH3OCH3)是重要的化工原料,可由CO和H2反应制得,反应的热化学方程式为2CO(g)+
4H2(g) =CH3OCH3(g)+H2O(g) ΔH=-206.0 kJ·mol-1,起始时向容器中充入2 mol CO和4 mol
H2,某时刻测得该反应放出的热量为51.5 kJ,此时CO的转化率为_______。
(4)某同学设计如图所示实验,探究反应中的能量变化。
①利用实验装置(b)测定盐酸与NaOH溶液发生中和反应的反应热,若取50 mL 0.50 mol·L-1的盐酸,则
还需加入_______(填字母)。
A. 1.0 g NaOH固体 B. 50 mL 0.50 mol·L-1氨水C.
50 mL 0.55 mol·L-1 NaOH溶液
②将实验(a)中的铝片更换为等质量的铝粉后,释放出的能量将_______(填“偏大”“偏小”或“不
变”,下同),将实验(b)中玻璃搅拌器改为铁质搅拌器后,实验测得的ΔH_______。
16. (12分)对SO2 、NOx 、CO2 和CO进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容器中充入
NO2 、SO2 发生反应:NO2(g)+SO2(g)⇌SO3(g)+NO(g)。
(1)只改变下列某一反应条件时,能使上述反应速率加快的是_______(填字母)。
A. 使用高效催化剂 B. 向容器中充入氩气 C .
降低温度 D. 减小NO的物质的量
(2)下列能说明反应达到平衡状态的是_______(填字母)。
A. 混合气体的密度保持不变 B. SO2 的物质的量保持不变
C. 容器内混合气体原子总数不变 D.每生成 1 mol SO3 的
同时消耗1 mol NO
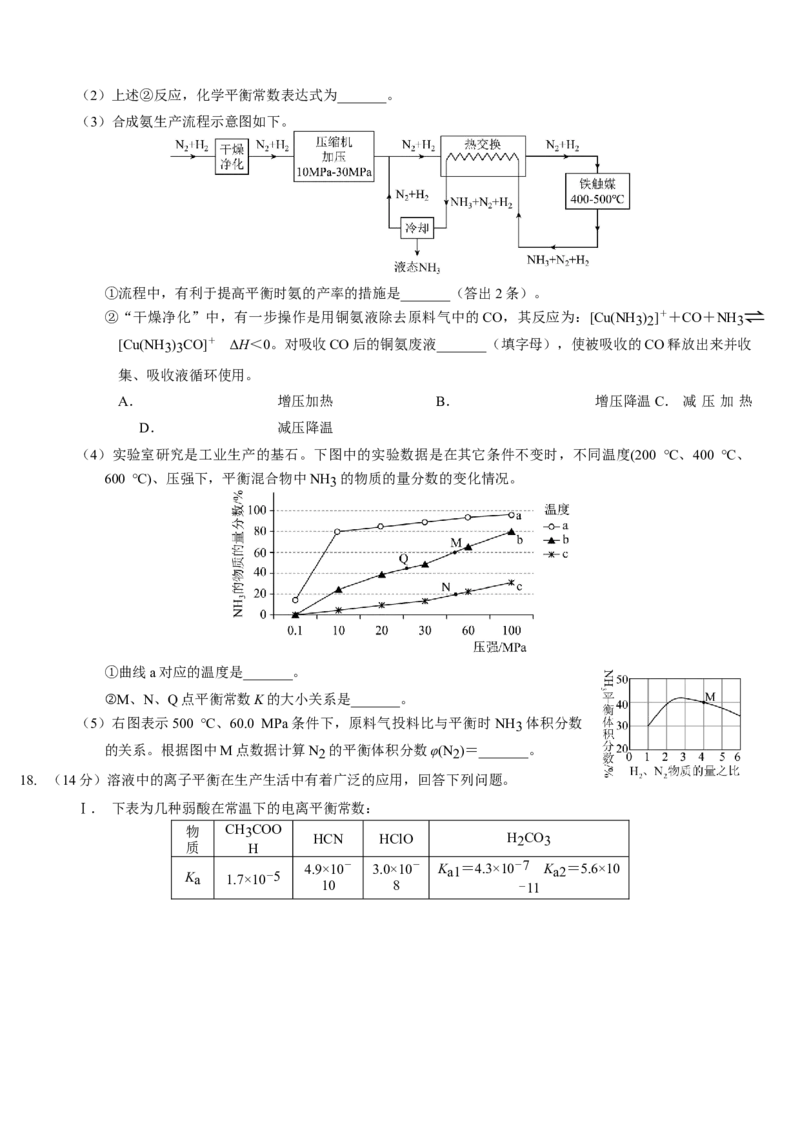
(3)在体积为2 L密闭容器中充入:3 mol CO2(g)和9 mol H2(g),发生反应2CO2(g)+6H2(g)⇌CH3OCH3(g)
+3H2O(g),测得CO2(g)、CH3OCH3(g)的物质的量随时间变化如图所示。
①0~5 min内,v(CO2)=_______mol·L-1·min-1。
②反应达到平衡状态时,CH3OCH3(g)的体积分数为_______%(保
留1位小数)。
③a、b、c 三点中代表达到平衡的是_______,a 点的正反应速率
_______(填“>”“<”或“=”)b点的逆反应速率。
17. (14分)合成氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首次利用氮气与氢气反应合成氨,实
现了人工固氮:N2(g)+3H2(g)⇌2NH3(g) ΔH=-92.4 kJ·mol-1。(1)请结合下列数据分析,工业上选用氮气与氢气反应固氮,而没有选用氮气和氧气反应固氮的原因是
_______。
序号 化学反应 K(298K)的数值
① N2(g)+O2(g)⇌2NO(g) 5.0×10-31
② N2(g)+3H2(g)⇌2NH3(g) 4.1×106(2)上述②反应,化学平衡常数表达式为_______。
(3)合成氨生产流程示意图如下。
①流程中,有利于提高平衡时氨的产率的措施是_______(答出2条)。
②“干燥净化”中,有一步操作是用铜氨液除去原料气中的CO,其反应为:[Cu(NH3)2]++CO+NH3⇌
[Cu(NH3)3CO]+ ΔH<0。对吸收CO后的铜氨废液_______(填字母),使被吸收的CO释放出来并收
集、吸收液循环使用。
A. 增压加热 B. 增压降温C. 减 压 加 热
D. 减压降温
(4)实验室研究是工业生产的基石。下图中的实验数据是在其它条件不变时,不同温度(200 ℃、400 ℃、
600 ℃)、压强下,平衡混合物中NH3 的物质的量分数的变化情况。
①曲线a对应的温度是_______。
②M、N、Q点平衡常数K的大小关系是_______。
(5)右图表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3 体积分数
的关系。根据图中M点数据计算N2 的平衡体积分数φ(N2)=_______。
18. (14分)溶液中的离子平衡在生产生活中有着广泛的应用,回答下列问题。
Ⅰ. 下表为几种弱酸在常温下的电离平衡常数:
物 CH3COO
HCN HClO H2CO3
质 H
4.9×10- 3.0×10- Ka1 =4.3×10-7 Ka2 =5.6×10
Ka 1.7×10-5
10 8 -11(1)CO2
3
-水解常数的表达式Kh =_______。
(2)常温下,浓度均为0.1 mol·L-1的下列5种溶液:①NaHCO3 溶液;②NaCN溶液;③NaClO溶液;
④CH3COONa溶液;⑤Na2CO3 溶液。它们pH由大到小的顺序是_______(填序号)。
Ⅱ. FeCl3 溶液通过控制条件,在加热下可获得铁黄(FeOOH)沉淀。
(3)①写出制备铁黄的离子方程式:______________。
②制备过程中可以边加热边加水,其目的是______________。
(4)向FeCl3 溶液中加入NH4HCO3 溶液可获得铁黄,该反应的化学方程式为______________。
Ⅲ. 某样品为KClO4 和KCl混合物,为测定产品含量进行如下实验:准确称取100.1 g样品溶于水中,配成
250 mL溶液。从中取出25.00 mL于锥形瓶中,加入适量葡萄糖,加热使ClO-全部转化为Cl-(反应为
4
3KClO4 +C6H12O6=6H2O+6CO2↑+3KCl)。加入少量K2CrO4 溶液作指示剂,用2.000 mol·L-1
AgNO3 溶液滴定至终点,消耗AgNO3 溶液体积50.00 mL。滴定达到终点时,产生砖红色Ag2CrO4 沉
淀。
(5)已知Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.1×10-12,若终点时c(CrO2
4
-)=1.1×10-4 mol·L-1,则此
时c(Cl-)=_______mol·L-1。
(6)样品中KClO4 与KCl的物质的量之比为_______。
19. (6分)一种吸收SO2 再经氧化得到硫酸盐的过程如图所示。室温下,用 0.1 mol·L-1的NaOH溶液吸收SO2 ,通
入SO2 所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c
总
=c(H2SO3)+c(HSO-
3
)+c(SO2
3
-)。
H2SO3 的电离平衡常数分别为Ka1 =1.29×10-2、Ka2 =6.24×10-8。
“吸收”后得到的溶液pH=5,该溶液由水电离出的c(H+)=_______mol·L-1,“氧化”时主要发生反应的离
子方程式为______________;将“氧化”所得溶液用 0.1 mol·L-1的NaOH溶液调节至 pH=7,再与 0.1
mol·L-1的BaCl2 溶液等体积混合,最终溶液中c(SO2
4
-)=_______ mol·L-1[室温下,Ksp(BaSO4)=1×10-
10]。