文档内容
2007 年广东高考化学真题及答案
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27
S-32
Cl-35.5 K-39 Ca-40 Mn-55 Fe-56 Pt-195
第Ⅰ卷 选择题(共70分)
一、选择题(每小题只有一个正确答案,每小题3分,10小题共30分)
1、铋(Bi)在医药方面有重要应用。下列关于2 0 9 B i 和 21 0 B i 的说法正确的是
83 83
A、2 09 B i和 2 1 0 B i都含有83个中子; B、 20 9 B i和 2 10 B i 互为同位素
83 83 83 83
C、2 09 B i 和 2 10 B i 的核外电子数不同; D、2 0 9 B i 和 21 0 B i 分别含有126和127个
83 83 83 83
质子
2、下列可用于测定溶液pH且精确度最高的是
A、酸碱指示剂 B、pH计 C、精密pH试纸 D、广泛pH试纸
3、下列叙述正确的是
A、48gO 气体含有6.02×1023个O 分子
3 3
B、常温常压下,4.6gNO 气体含有1.81×1023个NO 分子
2 2
C、0.5mol·L-1CuCl 溶液中含有3.01×1023个Cu2+
2
D、标准状况下,33.6LHO含有9.03×1023个HO分子
2 2
4、许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A、氯、溴、碘 B、钠、镁、铝
C、烧碱、氢气 D、食盐、淡水
5、氯气是一种重要的工业原料。工业上利用反应在 3Cl + 2NH = N + 6HCl检查氯气管
2 3 2
道是否漏气。下列说法错误的是
A、若管道漏气遇氨就会产生白烟; B、该反应利用了Cl 的强氧化性
2
C、该反应属于复分解反应; D、生成1molN 有6mol电子转移
2
6、下列说法正确的是
A、硅材料广泛用于光纤通讯 B、工艺师利用盐酸刻蚀石英制作艺术
品
C、水晶项链和餐桌上的瓷盘都是硅酸盐制品; D、粗硅制备单晶硅不涉及氧化还原反
应
7、下列说法中正确的是
A、石油裂解可以得到氯乙烯
B、油脂水解可得到氨基酸和甘油
C、所有烷烃和蛋白质中都存在碳碳单键D、淀粉和纤维素的组成都是(CH O),水解最终产物都是葡萄糖
6 10 5 n
8、下列符合化学实验“绿色化”的有:
① 在萃取操作的演示实验中,将CCl 萃取溴水改为CCl 萃取碘水
4 4
② 在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
③ 将实验室的废酸液和废碱液中和后再排放
A、①② B、①③ C、②③ D、①②③
9、科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入
以磷酸为电解质的燃料电池发电。电池负极反应为:
A、H + 2OH- =2HO+2e- B、O + 4H+ + 4e- = 2HO
2 2 2 2
C、H = 2H+ + 2e- D、O + 2HO + 4e- = 4OH-
2 2 2
10、下列实验操作完全正确的是
编号 实验 操作
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小
A 钠与水反应
心放入装满水的烧杯中
配制一定浓度的氯化 准确称取氯化钾固体,放入到1000ml的容量瓶中,加
B
钾溶液1000mL 水溶解,振荡摇匀,定容
排除碱式滴定管尖嘴 将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻
C
部分的气泡 轻挤压玻璃珠,使溶液从尖嘴流出
取出分液漏斗中所需 下层液体从分液漏斗下端管口放出,关闭活塞,换一
D
的上层液体 个接收容器,上层液体继续从分液漏斗下端管口放出
二、选择题(每小题有1~2个正确答案,每小题4分,10小题共40分)
11、下列化学反应的离子方程式正确的是
A、用小苏打治疗胃酸过多: HCO- + H+ == CO↑+ HO
3 2 2
B、往碳酸镁中滴加稀盐酸: CO2- + 2H+ == CO↑+ HO
3 2 2
C、往氨水中滴加氯化铝: Al3+ + 4OH- == AlO- + 2HO
2 2
D、氢氧化钡溶液与稀硫酸反应: Ba2+ + SO2- + H+ + OH- == BaSO↓+ HO
4 4 2
12、为了避免青铜器生成铜绿,以下方法正确的是
A、将青铜器放在银质托盘上; B、将青铜器保存在干燥的环境中
C、将青铜器保存在潮湿的空气中; D、在青铜器的表面覆盖一层防渗的高分子膜
13、顺式Pt(NH)Cl(式量为300)是临床广泛使用的搞肿瘤药物。下列有关该物质的说法
3 2 2
中正确的是
A、由4种元素组成 B、含有NH 分子
3
C、Pt的化合价为+4 D、Pt元素的质量百分含量为65%
14、将VmL1.0mol/L HCl溶液和VmL未知浓度的
1 2
30
NaOH溶液混合均匀后测量并记录溶液温度,实验
28
结果如右图所示(实验中始终保持 V + V= 50mL)。
1 2
26
下列叙述正确的是
24
A、做该实验时环境温度为22℃
B、该实验表明化学能可能转化为热能 22
20
0 10 20 30 40 50
V /
1
mL
℃
/
度温C、NaOH溶液的浓度约为1.0mol/L
D、该实验表明有水生成的反应都是放热反应
15、下列各溶液中,微粒的物质的量浓度关系正确的是
A、1.0mol/LNaCO 溶液:c(OH-) = c(HCO-) + c(H+) + 2c(HCO)
2 3 3 2 3
B、1.0mol/LNHCl溶液:c(NH+) = c(Cl-)
4 4
C 、 向 醋 酸 钠 溶 液 中 加 入 适 量 醋 酸 , 得 到 的 酸 性 混 合 溶 液 :
c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO-)
3
16、灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
① Sn(s、白) + 2HCl(aq)= SnCl(aq)+ H(g) △H
2 2 1
② Sn(s、灰) + 2HCl(aq)= SnCl(aq)+ H(g) △H
2 2 2
③ Sn(s、灰) > 1 3 .2 ℃ Sn(s、白) △H= + 2.1kJ/mol
< 13.2℃ 3
下列说法正确的是
A、△H >△H
1 2
B、锡在常温下以灰锡状态存在
C、灰锡转化为白锡的反应是放热反应
D、锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
17、短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、
Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子
数的3倍。下列说法正确的是
A、X的氢化物溶于水显酸性 B、Y的氧化物是离子化合物
C、Z的氢化物的水溶液在空气中存放不易变质
D、X和Z的最高价氧化物对应的水化物都是弱酸
18、下述实验能达到预期目的的是
编号 实验内容 实验目的
A 将SO 通入酸性KMnO 溶液中 证明SO 2 具有氧化性
2 4
B 将Cl 通入NaBr溶液中 比较氯与溴的氧化性强弱
2
将铜与浓硝酸反应生成的气体收集后用冰水 研究温度对化学平衡的影响
C
混合物冷却降温
分别向2支试管中加入相同体积不同浓度的 研究催化剂对 HO 分解速率
D 2 2
HO 溶液,再向其中1支加入少量MnO 的影响
2 2 2
19、下列说法正确的是
A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D、天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
20、三氧化二镍(NiO )可用于制造高能电池,其电解法制备过程如下:用 NaOH调NiCl
2 3 2
溶液pH至7.5,加放适量硫酸钠后进行电解。电解过程中产生的Cl 在弱碱性条件下生
2成ClO-,把二价镍氧化为三价镍。以下说法正确的是
A、可用铁作阳极材料
B、电解过程中阳极附近溶液的pH升高
C、阳极反应方程式为: 2Cl- - 2e- = Cl
2
D、1mol二价镍全部转化为三价镍时,外电路中通过了1mol电子。
第Ⅱ卷 非选择题(共80分)
三、(本题包括3小题,共29分)
21、(10分)
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
氯化钠 NaSO
2 4
混合 蒸发 趁热
滤液
硫酸铵 溶解 浓缩 过滤 滤液 冷却 过滤
结晶
NH 4 Cl 洗涤 干燥 NH 4 Cl产品
80
70
氯化铵
60
50
40
30
20
20 30 40 50 60 70 80 90 100
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNHCl,理论上需 NaCl g。
4
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NHCl晶体的合适温度为 。
4
(4)不用其它试剂,检查NHCl产品是否纯净的方法及操作是 。
4
(5)若NHCl产品中含有硫酸钠杂质,进一步提纯产品的方法是 。
4
22、(8分)
“碘钟”实验中,3I- + SO2- = I- + 2SO2-的反应速率可以用I-与加入的淀粉溶液
2 8 3 4 3
显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,
得到的数据如下表:
实验编号 ① ② ③ ④ ⑤
c(I-)/mol·L- 0.040 0.080 0.080 0.160 0.120
c(SO2-)/mol·L- 0.040 0.040 0.080 0.020 0.040
4
t /s 88.0 44.0 22.0 44.0 t
2
回答下列问题:
g/度解溶
硫酸钠
温
度/℃( 1 ) 该 实 验 的 目 的 是
。
(2)显色时间t= .
2
(3)温度对该反应的反应速率的影响符合一般规律,若在 40℃下进行编号③对应浓度的
实验,显色时间t 的范围为 (填字母)
2
A、<22.0s B、22.0~44.0s C、>44.0s D、数据不足,无法判断
( 4 ) 通 过 分 析 比 较 上 表 数 据 , 得 到 的 结 论 是
。
23、(11分)
已知某混合金属粉末,除铝处还含有铁、铜中的一种或两种,所含金属的量都在 5%以
上。请设计合理实验探究该混合物金属粉末中铁、铜元素的存在。
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L
硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液。
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有 元素;
假设2 该混合金属粉末中除铝外还含有 元素;
假设1 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
【提示】Ⅰ.在答题卡上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超过答题卡空间。
编号 实验操作 预期现象和结论
①
②
③
④
四、(本题包括3小题,共32分)
24、(10分)二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备
高纯二氧化锰的流程如下:
H 2 SO 4 过量FeSO 4 氨水
滤渣 液 MnS
软锰矿 酸浸 过滤 调pH 滤渣A 液
滤液 至5.4 过滤 加热至 滤渣
液 滤液 沸 过滤
液 滤液→…→高纯MnO
2
液 液
某软锰矿的主要成分为 MnO ,还含有 Si(16.27%)、Fe(5.86%)、Al(3.42%)、
2
Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉
淀时溶液的pH见下表,回答下列问题:
沉淀物 Al(OH) Fe(OH) Fe(OH) Mn(OH) Cu(OH) Zn(OH) CuS ZnS MnS FeS
3 3 2 2 2 2
pH 5.2 3.2 9.7 10.4 6.7 8.0 ≥-0.4 ≥2.5 ≥7 ≥7
2
(1)硫酸亚铁在酸性条件下将MnO 还原为MnSO ,酸浸时发生的主要反应的化学方程式
2 4
为 。
(2)滤渣A的主要成分是 。
(3)加入MnS的目的是除去 杂质。
( 4 ) 碱 性 锌 锰 电 池 中 , MnO 参 与 的 电 极 反 应 方 程 式 为
2
。
(5)从废旧碱性锌锰电池中可以回收利用的物质有 (写两种)。
25、(10分)
黄铁矿(主要成分为FeS)是工业制取硫酸的重要原料,其煅烧产物为SO 和FeO。
2 2 3 4
(1)将0.050molSO(g)和0.030molO(g)放入容积为1L的密闭容器中,反应:2SO(g)
2 2 2
+ O(g)
2
2SO(g)在一定条件下达到平衡,测得c(SO)=0.040mol/L。计算该条件下反应的平衡
3 3
常数K和SO 的平衡转化率(写出计算过程)。
2
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列
措施中有利于提高SO 平衡转化率的有 (填字母)
2
A、升高温度 B、降低温度 C、增大压强
D、减小压强 E、加入催化剂 G、移出氧气
(3)SO 尾气用饱和NaSO 溶液吸收可得到更要的化工原料,反应的化学方程式为
2 2 3
。
(4)将黄铁矿的煅烧产物FeO 溶于HSO 后,加入铁粉,可制备FeSO 。酸溶过程中需
3 4 2 4 4
保持溶液足够酸性,其原因是 。
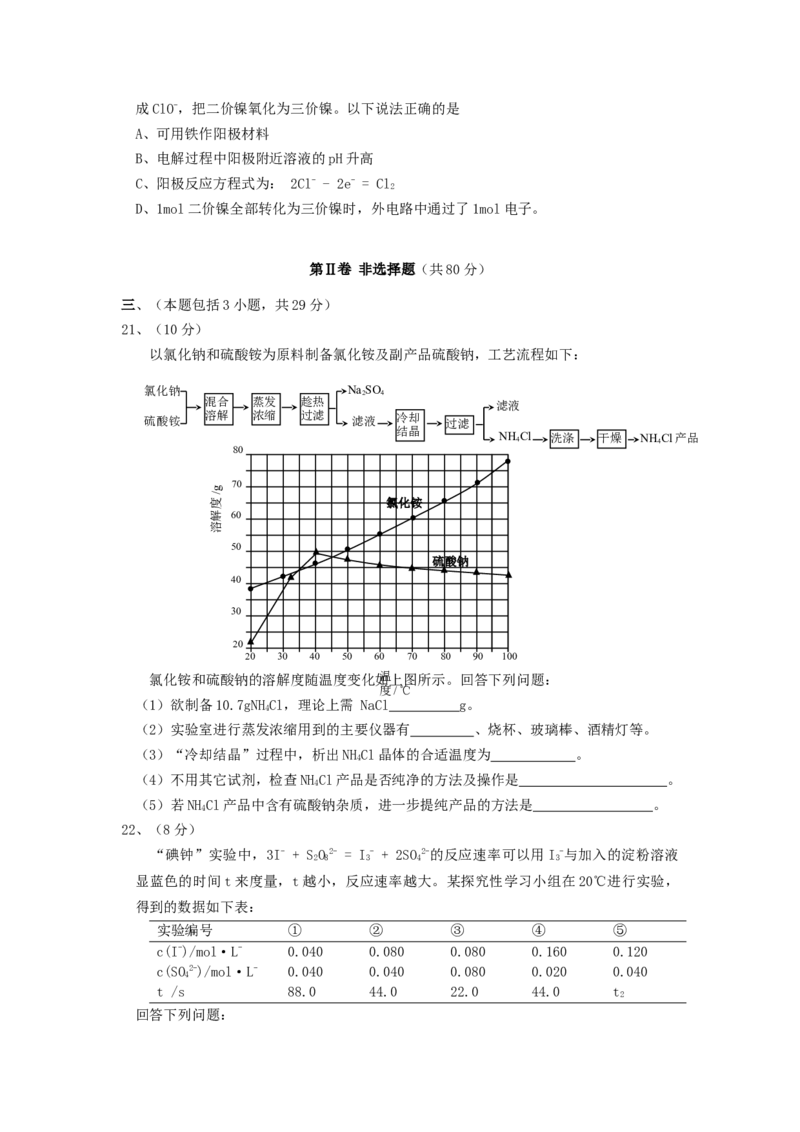
26、(12分)羟基磷灰石[Ca(PO)OH]是一种一种重要的生物无机材料。其常用的制备方法有两种:
5 4 3
方法A:用浓氨水分别调Ca(NO) 和(NH)HPO 溶液的pH约为12;在剧烈搅拌下,将
3 2 4 2 4
(NH)HPO 溶液缓慢滴入Ca(NO) 溶液中。
4 2 4 3 2
方法B:剧烈搅拌下,将HPO 溶液缓慢滴加到Ca(OH) 悬浊液中。
3 4 2
0
-1
-2
-3
-4
-5
-6
-7
4 6 8 10 12 14
3种钙盐的溶解度随溶液pH的变化如上图所示(图中纵坐标是钙离子浓度的对数),
回答下列问题:
(1)完成方法A和方法B中制备Ca(PO)OH的化学反应方程式:
5 4 3
①5 Ca(NO) + 3(NH)HPO + 4NH·HO = Ca(PO)OH↓+ +
3 2 4 2 4 3 2 5 4 3
②5Ca(OH) + 3HPO =
2 3 4
( 2 ) 与 方 法 A 相 比 , 方 法 B 的 优 点 是
。
(3)方法B中,如果HPO 溶液滴加过快,制得的产物不纯,其原因是
3 4
。
(4)图中所示3种钙盐在人体中最稳定的存在形式是 (填化学式)。
(5)糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。结合化学平衡移动原
理 , 分 析 其 原 因
。
五、(本题包括1小题,9分)
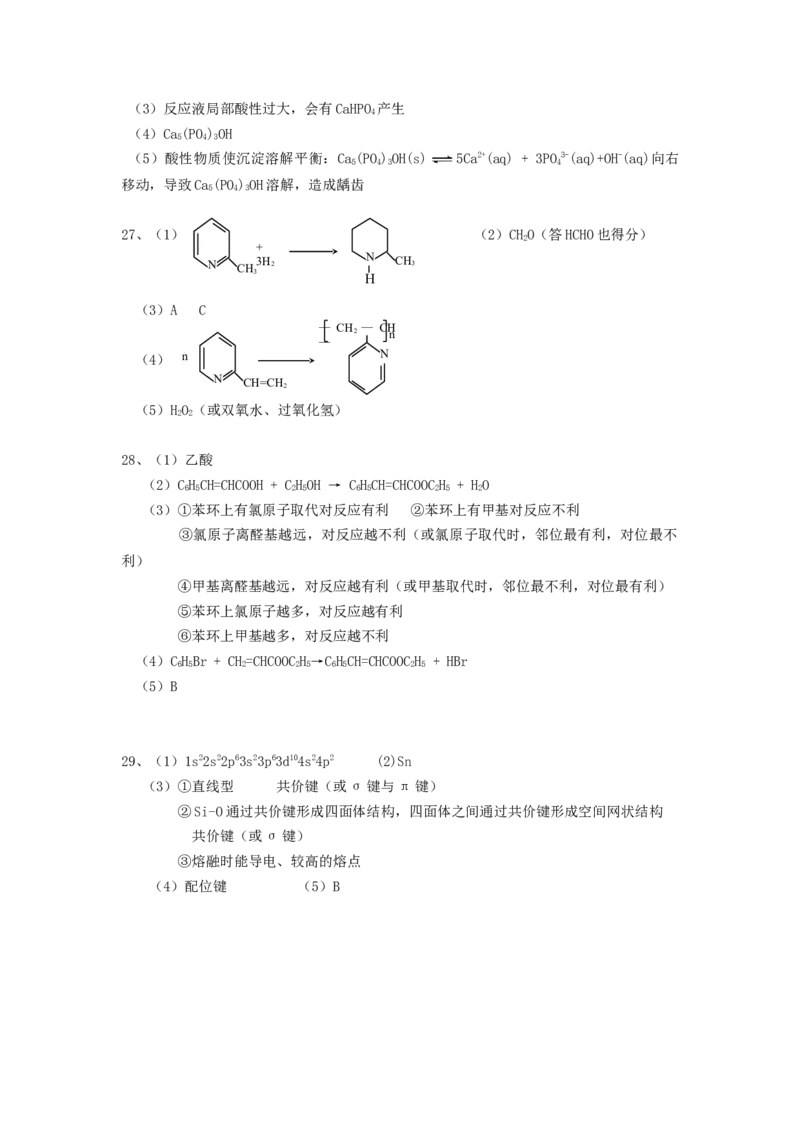
27、(9分)
克矽平是一种治疗矽肺病的药物,其合成路线如下(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以一定条件下与氢气发生加成反应
生成
,其反应方程式为 (不要求标出反应条
)+2aC(cgl
CaHPO 4
Ca (PO )
2 4 3
Ca (PO ) OH
5 4 3
pH
— CH — CH — CH — CH
2 n 2 n
— —
N N→O
N CH N CHCHOH N CH=CH
3 2 2 2
Ⅰ Ⅱ Ⅲ Ⅳ 克矽平
N CH
3
H件)
(2)化合物I生成化合物Ⅱ是原子利用率100%的反应,所需另一种反应物的分子式为
(3)下列关于化合物和化合物Ⅲ的化学性质,说法正确的是 (填字母)
A、化合物Ⅱ可以与CHCOOH发生酯化反应
3
B、化合物Ⅱ不可以与金属钠生成氢气
C、化合物Ⅲ可以使溴的四氯化碳溶液褪色
D、化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)化合物Ⅲ生成化合物Ⅳ的反应方程式为 (不要求
标出反应条件)
(5)用氧化剂氧化化合物Ⅳ生成克矽平和水,则该氧化剂为 。
六、选做题(本题包括2小题,每小题10分,考生只能选做一题。28小题为“有机化学基
础”内容的试题,29题为“物质结构与性质”内容的试题)
28、(10分)
已知苯甲醛在一定条件下可以通过 Perkin反应生成肉桂酸(产率45~50%),另一个
产物A也呈酸性,反应方程式如下:
CHCHO + (CHCO)O → CHCH=CHCOOH + A
6 5 3 2 6 5
苯甲醛 肉桂酸
(1)Perkin反应合成肉桂酸的反应式中,反应物的物质的量之比为1 :1。产物A的名
称是
。
(2)一定条件下,肉桂酸与乙醇反应生成香料肉桂酸乙酯,其反应方程式为
(不要求标出反应
条件)
(3)取代苯甲醛也能发生Perkin反应,相应产物的产率如下:
CH CH
3 3
取代苯甲醛
—CH 3 CH 3 — —CHO —CHO
—CHO —CHO
CH
产率(%) 15 23 33 0 3
Cl Cl
取代苯甲醛 —Cl
—CHO Cl— —CHO —CHO
—CHO
产率(%) 71 63 52 82 Cl
可见,取代基对Perkin反应的影响有(写出3条即可):
①
②
③
(4)溴苯(CHBr)与丙烯酸乙酯(CH=CHCOOCH )在氯化钯催化下可直接合成肉桂酸
6 5 2 2 5乙酯,该反应属于Beck反应,是芳香环上的一种取代反应,其反应方程式为
(不要求标出反应
条件)
(5)Beck反应中,为了促进反应的进行,通常可加入一种显 (填字母)的物质
A、弱酸性 B、弱碱性 C、中性 D、强酸性
29、(10分)
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应
用。请回答下列问题:
(1) Ge的原子核外电子排布式为
(2) C、Si、Sn三种元素的单质中,能够形成金属晶体的是
(3) 按要求指出下列氧化物的空间构型、成键方式或性质
①CO 分子的空间构型及碳氧之间的成键方式 ;
2
② SiO 晶 体 的 空 间 构 型 及 硅 氧 之 间 的 成 键 方 式
2
;
③已知SnO 是离子晶体,写出其主要物理性质 (写出2条即
2
可)
(4) CO可以和很多金属形成配合物,如Ni(CO),Ni与CO之间的键型为
4
(5) 碳氧键的红外伸缩振动频率与键的强度成正比,已知 Ni(CO) 中碳氧键的伸
4
缩振动频率为 2060cm-1,CO 分子中碳氧键的伸缩振动频率为 2143cm-1,则
Ni(CO) 中碳氧键的强度比CO分子中碳氧键的强度 (填字母)
4
A、强 B、弱 C、相等 D、无法判断参考答案
1B 2B 3A 4D 5C 6A 7D 8D 9C 10C
11A 12BD 13AD 14B 15AD 16D 17B 18BC 19BD 20CD
21(1)11.7 (2)蒸发皿 (3)35℃(33~40℃均可得分)
(4)加热法;取少量氯化铵产品于试管底部,加热,若试管底部无残留物,表明氯化铵
产品纯净。 (5)重结晶
22、(1)研究反应物I-与SO2-的浓度对反应速率的影响
2 8
(2)29.3s (3)A
(4)反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反
比)
23(1)Cu;Fe(顺序可交换)
(3)
编号 实验操作 预期现象和结论
用药匙取少许样品,加入试管A中,再 样品部分溶解,并有气体放出
用滴管取过量NaOH溶液并滴加到试管
①
A中,充分反应后,静置,弃去上层清
液,剩余固体备用
往试管A的剩余固体中加过量稀硫酸, 固体部分溶解,并有气体放出,溶液
② 充分反应后,静置。取上层清液于试管 呈浅绿色,可能含铁
B中,剩余固体备用
往试管B中加入少许稀硝酸,再滴加 溶液先变黄色,加KSCN后显血红色,
③
KSCN溶液 结合②可知,一定含铁
往②剩余固体中加入稀硝酸,再滴加 固体溶解,有无色刺激性气体产生并
NaOH溶液 很快变成红棕色,溶液显蓝色,加
④
NaOH溶液后有蓝色沉淀产生,一定含
铜。
24、(1)MnO +2FeSO + 2HSO = MnSO + Fe(SO) + 2HO
2 4 2 4 4 2 4 3 2
(2) Fe(OH) Al(OH)
3 3
(3)Cu2+ Zn2+
(4)MnO + HO + e- = MnOOH + OH-(或2MnO + HO + 2e- = MnO + 2OH-)
2 2 2 2 2 3
(5)锌、二氧化锰
25、(1)1.6×103L/mol 80% (计算过程略)
(2)B C
(3)SO + HO + NaSO = 2NaHSO
2 2 2 3 3
(4)抑制Fe2+、Fe3+的水解,防止Fe2+被氧化成Fe3+
26(1)①10NHNO 3HO ②Ca(PO)OH↓+ 9HO
4 3 2 5 4 3 2
(2)唯一副产物为水,工艺简单(3)反应液局部酸性过大,会有CaHPO 产生
4
(4)Ca(PO)OH
5 4 3
(5)酸性物质使沉淀溶解平衡:Ca(PO)OH(s) 5Ca2+(aq) + 3PO3-(aq)+OH-(aq)向右
5 4 3 4
移动,导致Ca(PO)OH溶解,造成龋齿
5 4 3
27、(1) (2)CHO(答HCHO也得分)
2
+
N CH 3H 2 N CH 3
3
H
(3)A C
— CH — CH
2 n
—
(4) n N
N
CH=CH
2
(5)HO(或双氧水、过氧化氢)
2 2
28、(1)乙酸
(2)CHCH=CHCOOH + CHOH → CHCH=CHCOOCH + HO
6 5 2 5 6 5 2 5 2
(3)①苯环上有氯原子取代对反应有利 ②苯环上有甲基对反应不利
③氯原子离醛基越远,对反应越不利(或氯原子取代时,邻位最有利,对位最不
利)
④甲基离醛基越远,对反应越有利(或甲基取代时,邻位最不利,对位最有利)
⑤苯环上氯原子越多,对反应越有利
⑥苯环上甲基越多,对反应越不利
(4)CHBr + CH=CHCOOCH→CHCH=CHCOOCH + HBr
6 5 2 2 5 6 5 2 5
(5)B
29、(1)1s22s22p63s23p63d104s24p2 (2)Sn
(3)①直线型 共价键(或σ键与π键)
②Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构
共价键(或σ键)
③熔融时能导电、较高的熔点
(4)配位键 (5)B