文档内容
C.46g NO 和N O 混合气体中含有原子总数为3N
2011 年全国统一高考化学试卷(全国卷Ⅰ) 2 2 4 A
D.1 mol Na 与足量 O 反应,生成Na O和Na O 的混合物,钠失去N 个电子
2 2 2 2 A
一、选择题
8.某含铬(Cr O 2﹣)废水用硫酸亚铁铵[FeSO •(NH ) SO •6H O]处理,反应后铁元素和铬元
2 7 4 4 2 4 2
1.等浓度的下列稀溶液:①乙酸、②苯酚、③碳酸、④乙醇,它们的pH由小到大排列正确的是
素完全转化为沉淀.该沉淀经干燥后得到n mol FeO•Fe Cr O .不考虑处理过程中的实际损耗,
y x 3
( )
下列叙述错误的是( )
A.④②③① B.③①②④ C.①②③④ D.①③②④
A.消耗硫酸亚铁的物质的量为n(2﹣x)mol
2.下列叙述错误的是( )
B.处理废水中的Cr O 2﹣的物质的量为 mol
2 7
A.用金属钠可区分乙醇和乙醚
B.用高锰酸钾酸性溶液可区分己烷和3﹣己烯 C.反应中发生转移的电子数为3nxmol
C.用水可区分苯和溴苯 D.在FeO•Fe Cr O 中,3x=y
y x 3
D.用新制的银氨溶液可区分甲酸甲酯和乙醛
3.在容积可变的密闭容器中,2mol N 和8mol H 在一定条件下发生反应,达到平衡时,H 的转 二、解答题(共4小题,满分60分)
2 2 2
化率为25%,则平衡时的氮气的体积分数接近于( ) 9.(15分)如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二
A.5% B.10% C.15% D.20% 元化合物.已知:①反应C+G B+H能放出大量的热,该反应曾应用于铁轨的焊接;②I是
4.室温时,将浓度和体积分别为c 、V 的NaOH溶液和c 、V 的CH COOH溶液相混合,下列关
1 1 2 2 3
一种常见的温室气体,它和 E 可以发生反应: ,F 中的 E 元素的质量分数为
于该混合溶液的叙述错误的是( )
A.若PH>7时,则一定是c V =c V 60%.回答问题:
1 1 2 2
B.在任何情况下都是c(Na+)+c(H+)=c(CH COO﹣)+c(OH﹣) (1)①中反应的化学方程式为 ;
3
C.当pH=7时,若V =V ,则一定是c >c (2)化合物Ⅰ的电子式为 ,它的空间构型是 ;
1 2 2 1
D.若V =V 、c =c ,则c(CH COO﹣)+c(CH COOH)=c(Na+) (3)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量(写出离子方程式
1 2 1 2 3 3
5.用石墨做电极电解CuSO 溶液.通电一段时间后,欲使用电解液恢复到起始状态,应向溶液中 和计算过程);
4
加入适量的( ) (4)C与过量NaOH溶液反应的离子方程式为 ,反应后溶液与过量化合物Ⅰ反应的离子方程
A.CuSO B.H O C.CuO D.CuSO •5H O 式为 ;
4 2 4 2
6.将足量CO 通入下列各溶液中,所含离子还能大量共存的是( ) (5)E在I中燃烧观察到的现象是 .
2
A.K+、SiO 2﹣、Cl﹣、NO ﹣ B.H+、NH +、Al3+、SO 2﹣
3 3 4 4
C.Na+、S2﹣、OH﹣、SO 2﹣ D.Na+、C H O﹣、CH COO﹣、HCO ﹣
4 6 5 3 3
7.N 为阿伏伽德罗常数,下列叙述错误的是( )
A
A.18gH O中含的质子数为10N
2 A
B.12g 金刚石含有的共价键数为4N
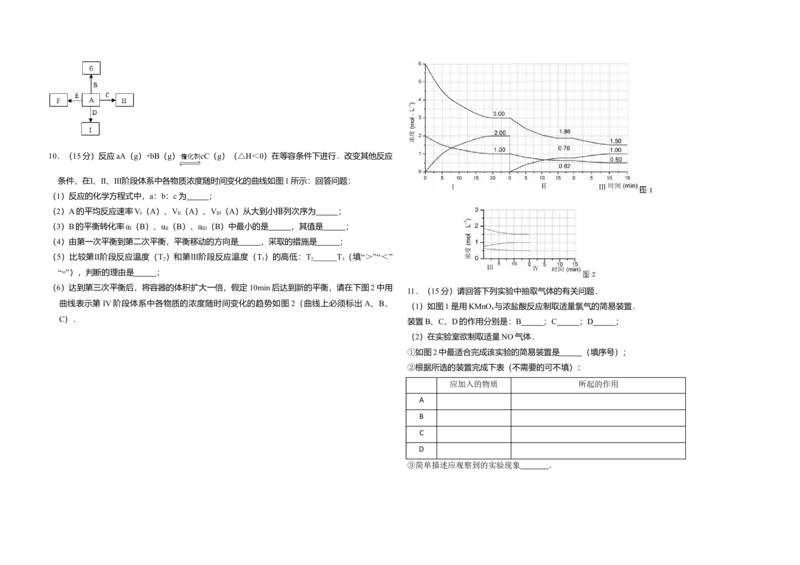
A10.(15分)反应aA(g)+bB(g) cC(g)(△H<0)在等容条件下进行.改变其他反应
条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图1所示:回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率V(A)、V (A)、V (A)从大到小排列次序为 ;
Ⅰ Ⅱ Ⅲ
(3)B的平衡转化率α(B)、α (B)、α (B)中最小的是 ,其值是 ;
Ⅰ Ⅱ Ⅲ
(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(5)比较第Ⅱ阶段反应温度(T )和第Ⅲ阶段反应温度(T )的高低:T T (填“>”“<”
2 3 2 3
“=”),判断的理由是 ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定 10min后达到新的平衡,请在下图2中用
11.(15分)请回答下列实验中抽取气体的有关问题.
曲线表示第 IV阶段体系中各物质的浓度随时间变化的趋势如图 2(曲线上必须标出 A、B、
(1)如图1是用KMnO 与浓盐酸反应制取适量氯气的简易装置.
4
C).
装置B、C、D的作用分别是:B ;C ;D ;
(2)在实验室欲制取适量NO气体.
①如图2中最适合完成该实验的简易装置是 (填序号);
②根据所选的装置完成下表(不需要的可不填):
应加入的物质 所起的作用
A
B
C
D
③简单描述应观察到的实验现象 .(4)已知烯烃能发生如下反应: RCHO+R′CHO
请写出下列反应产物的结构简式: ;
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热
氧化可以得到对苯二甲酸[提示:苯环上的烷基(﹣CH ,﹣CH R,﹣CHR )或烯基侧链经高
3 2 2
锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构): .
图1
图2
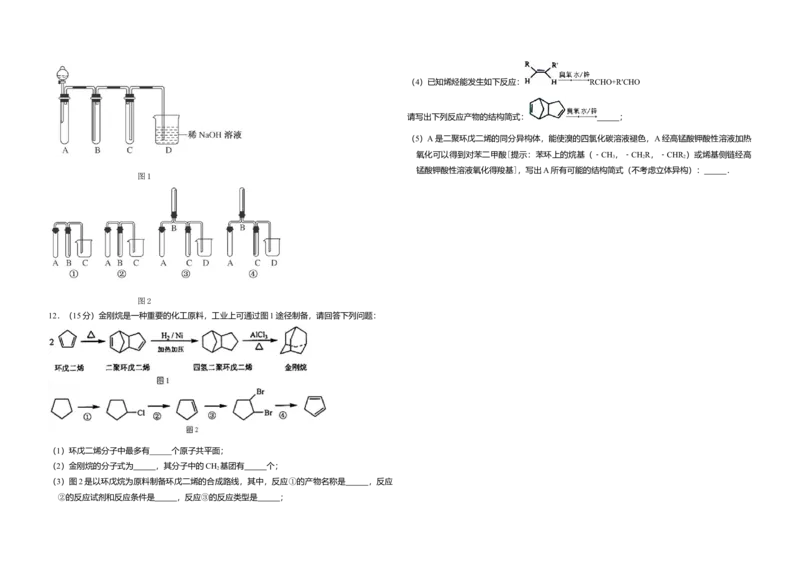
12.(15分)金刚烷是一种重要的化工原料,工业上可通过图1途径制备,请回答下列问题:
(1)环戊二烯分子中最多有 个原子共平面;
(2)金刚烷的分子式为 ,其分子中的CH 基团有 个;
2
(3)图2是以环戊烷为原料制备环戊二烯的合成路线,其中,反应①的产物名称是 ,反应
②的反应试剂和反应条件是 ,反应③的反应类型是 ;