文档内容
丰台区 2021-2022 学年度第一学期期末练习
初 三 化 学
2022.01
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Si-28
第一部分 选择题(共25分)
(每小题只有一个选项符合题意。每小题1分)
1. 下列属于金属元素的是
A. H B. Mg C. Cl D. P
2. 下列气体中,参与植物光合作用的是
A. B. C. D.
3. 下列图标中,表示“禁止烟火”的是
A. B. C. D.
4. 决定元素种类的是
A. 核外电子数 B. 中子数 C. 最外层电子数 D. 质子数
5. 废弃的易拉罐和塑料瓶属于
A. 厨余垃圾 B. 其他垃圾 C. 可回收物 D. 有害垃圾
6. 食用碘盐可预防甲状腺肿大等疾病。这里的“碘”是指
A. 碘元素 B. 碘原子 C. 碘单质 D. 碘离子
7. 百花盛开,阵阵花香,沁人心脾。花香四溢的现象说明 ( )
A. 分子是不断运动的 B. 分子是由原子构成的
C. 分子具有一定的质量 D. 分子之间有一定的间隔
8. 下列物质能在空气中燃烧,且产生大量白烟的是
A. 木炭 B. 硫粉 C. 红磷 D. 铁丝
的
9. 2021世界水日 主题:珍惜水、爱护水。下列做法不正确的是
A. 工业废水处理达标后排放 B. 使用节水淋浴喷头
C. 淘米水浇花 D. 洗手涂肥皂时不关闭水龙头
10. 下列仪器不能加热的是A. 烧杯 B. 试管 C. 量筒 D. 燃烧匙
11. 下列符号中,能表示2个氧分子的是
A. 2O B. 2O C. 2HO D. H O
2 2 2 2
12. 净水时,活性炭的作用是
A. 沉降 B. 蒸馏 C. 消毒 D. 吸附
13. —种氟原子的原子核内有9个质子和10个中子,该原子的核电荷数为( )
A. 7 B. 9 C. 10 D. 19
14. 我国向世界承诺,在2030年实现碳达峰,2060年实现碳中和。下列行为不利于实现碳中和的是
A. 使用新技术提高传统能源的利用效率 B. 研发新工艺将二氧化碳转化为化工产品
C. 植树造林扩大绿化面积 D. 露天焚烧垃圾
15. 锰元素的相关信息如图所示。下列说法不正确的是
A. 元素符号为Mn B. 原子核内质子数为25
C. 元素名称为锰 D. 在地壳中的含量为54.94%
16. 下列实验操作正确的是
A. 点燃酒精灯 B. 倾倒液体
C. 称量食盐 D. 加热液体
17. 下列有关氮气的用途中,主要利用其物理性质的是
A. 液氮用作冷冻剂 B. 焊接金属时用作保护气
C. 制造硝酸和氮肥 D. 食品包装中充氮气防腐
18. 下列属于氧化物的是
A. KMnO B. HCl C. CO D. C HOH
4 2 2 519. 下列反应中属于化合反应的是
A. CaO + H O=Ca(OH)
2 2
B. 3CO + Fe O 2 Fe + 3 C O
2 3 2
C. CO + 2NaOH=NaCO + H O
2 2 3 2
D. CaCO Ca O+ CO ↑
3 2
20. 下列物质的化学式书写正确的是
A. 铁FE B. 氯化钠NaCl C. 硫酸铜CuSO D. 氧化铝AlO
2 4
21. 用灯帽盖灭酒精灯的灭火原理是( )
A. 清除可燃物 B. 降低酒精的着火点
C. 隔绝空气 D. 降低温度至酒精的着火点以下
22. 柑橘类水果中含有柠檬酸(化学式为C HO),柠檬酸可用于除水垢,下列关于柠檬酸的说法不正确
6 8 7
的是
A. 柠檬酸由碳、氢、氧元素组成
B. 柠檬酸分子中碳、氧原子的个数比6:7
C. 一个柠檬酸分子中含4个氢分子
D. 柠檬酸可能与水垢中的成分反应
23. 下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 除去CO 中少量的CO 通过澄清石灰水
2
B 除去浑浊河水中的泥沙 过滤
C 鉴别氧气和空气 伸入带火星的木条
D 鉴别硬水和软水 加入肥皂水
A. A B. B C. C D. D
24. 中国芯彰显中国“智”造。芯片的基材主要是高纯硅,其反应微观示意图如下,下列说法中错误的是的
A. 一个甲分子中有三个氯原子 B. 乙 化学式是H
2
C. 在该反应中乙和丙的质量比为1:14 D. 该反应中乙和丁的分子个数比为1:1
25. 用下图所示装置及药品进行实验,能达到对应实验目的的是
A.验证质量守恒定 C.监控O 流 D.验证蜡烛中含有氢、氧元
B.证明CO 的密度比空气大 2
律 2 速 素
A. A B. B C. C D. D
第二部分 非选择题(共45分)
【生活现象解释】
26. 从A或B两题中任选一个做答,若两题均作答,按A计分。
A B
固体二氧化碳的用途之一是______。 固体二氧化碳的俗称是______。
27. “用张北的风点亮北京的灯”,北京冬奥会将实现所有场馆绿色电力全覆盖。
(1)目前人们使用的燃料主要来自化石燃料,如煤、______和天然气
(2)天然气主要成分为甲烷(CH),其完全燃烧的化学方程式为______。
4
(3)下列获取电能的方式符合绿色电力技术的是______。(填字母序号)
A. 风力发电 B. 火力发电
28. 近年来我国在航天领域取得了重大成就。
(1)长征二号F遥十三运载火箭使用液氢和液氧做助推剂,利用了液氧______的性质。
(2)中国空间站首次太空授课,站内空气与地球大气组成基本一致,其中体积分数最大的是______。
(3)站内的备用O 由分解高氯酸锂(LiClO)获得,同时还生成氯化锂(LiCl),该反应中含有氧元素
2 4
的物质是______。【科普阅读理解】
29. 阅读下面科普短文。
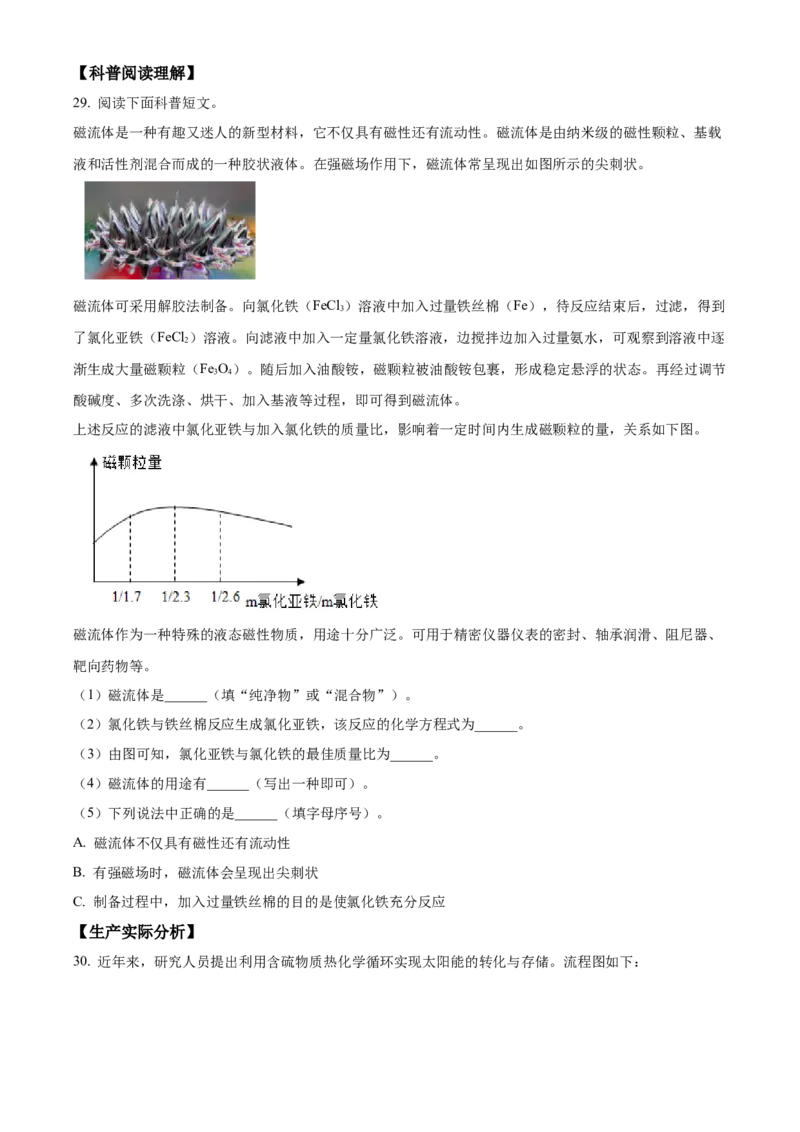
磁流体是一种有趣又迷人的新型材料,它不仅具有磁性还有流动性。磁流体是由纳米级的磁性颗粒、基载
液和活性剂混合而成的一种胶状液体。在强磁场作用下,磁流体常呈现出如图所示的尖刺状。
磁流体可采用解胶法制备。向氯化铁(FeCl )溶液中加入过量铁丝棉(Fe),待反应结束后,过滤,得到
3
了氯化亚铁(FeCl )溶液。向滤液中加入一定量氯化铁溶液,边搅拌边加入过量氨水,可观察到溶液中逐
2
渐生成大量磁颗粒(Fe O)。随后加入油酸铵,磁颗粒被油酸铵包裹,形成稳定悬浮的状态。再经过调节
3 4
酸碱度、多次洗涤、烘干、加入基液等过程,即可得到磁流体。
上述反应的滤液中氯化亚铁与加入氯化铁的质量比,影响着一定时间内生成磁颗粒的量,关系如下图。
磁流体作为一种特殊的液态磁性物质,用途十分广泛。可用于精密仪器仪表的密封、轴承润滑、阻尼器、
靶向药物等。
(1)磁流体是______(填“纯净物”或“混合物”)。
(2)氯化铁与铁丝棉反应生成氯化亚铁,该反应的化学方程式为______。
(3)由图可知,氯化亚铁与氯化铁的最佳质量比为______。
(4)磁流体的用途有______(写出一种即可)。
(5)下列说法中正确的是______(填字母序号)。
A. 磁流体不仅具有磁性还有流动性
B. 有强磁场时,磁流体会呈现出尖刺状
C. 制备过程中,加入过量铁丝棉的目的是使氯化铁充分反应
【生产实际分析】
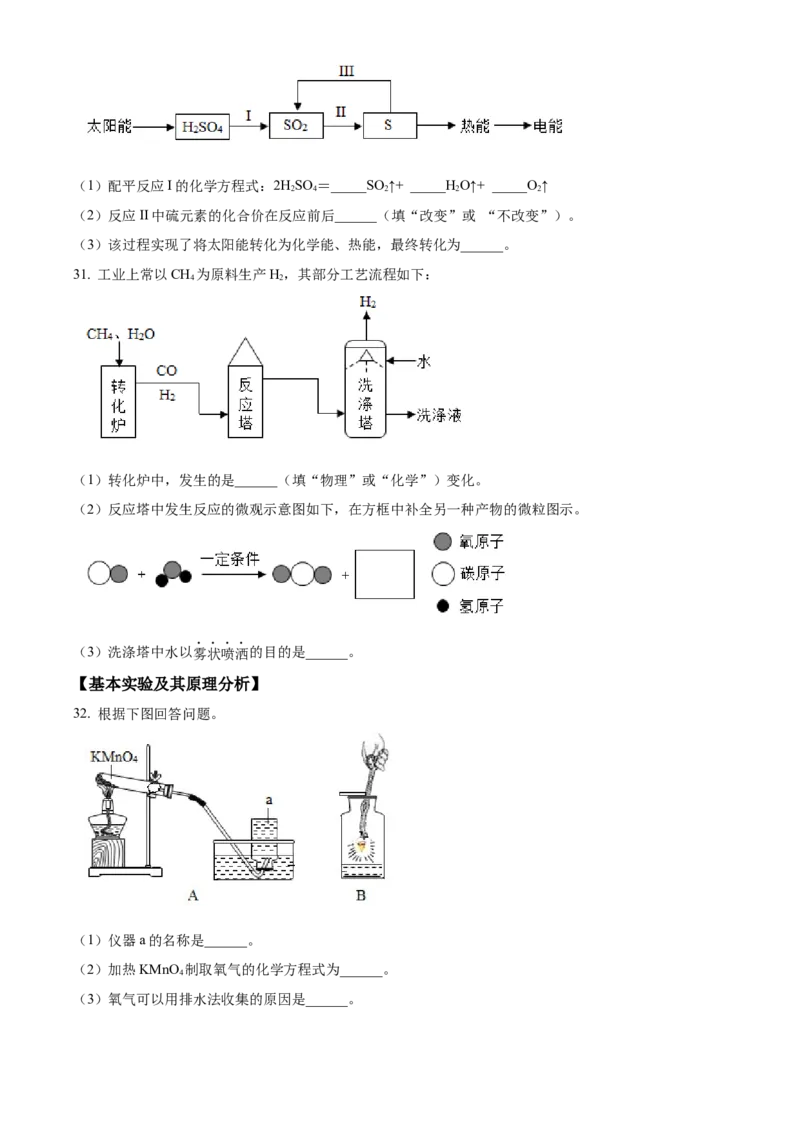
30. 近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。流程图如下:(1)配平反应I的化学方程式:2HSO =_____SO ↑+ _____HO↑+ _____O↑
2 4 2 2 2
(2)反应II中硫元素的化合价在反应前后______(填“改变”或 “不改变”)。
(3)该过程实现了将太阳能转化为化学能、热能,最终转化为______。
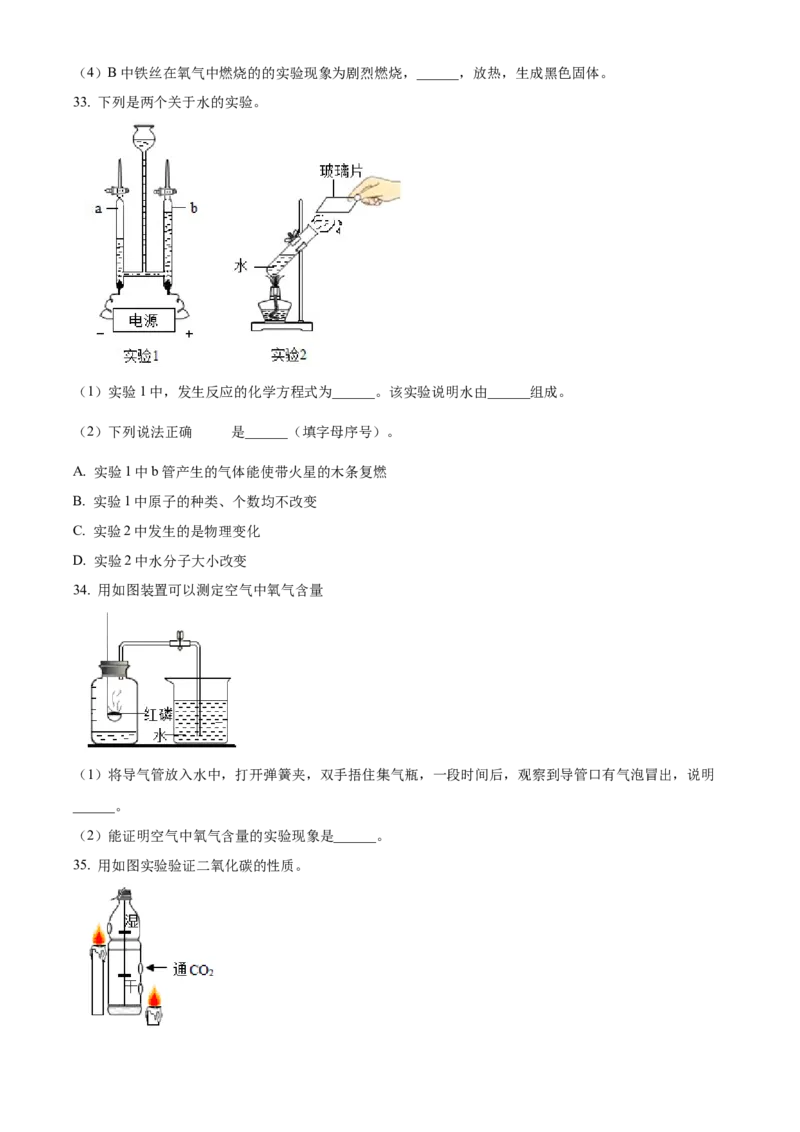
31. 工业上常以CH 为原料生产H,其部分工艺流程如下:
4 2
(1)转化炉中,发生的是______(填“物理”或“化学”)变化。
(2)反应塔中发生反应的微观示意图如下,在方框中补全另一种产物的微粒图示。
(3)洗涤塔中水以雾状喷洒的目的是______。
【基本实验及其原理分析】
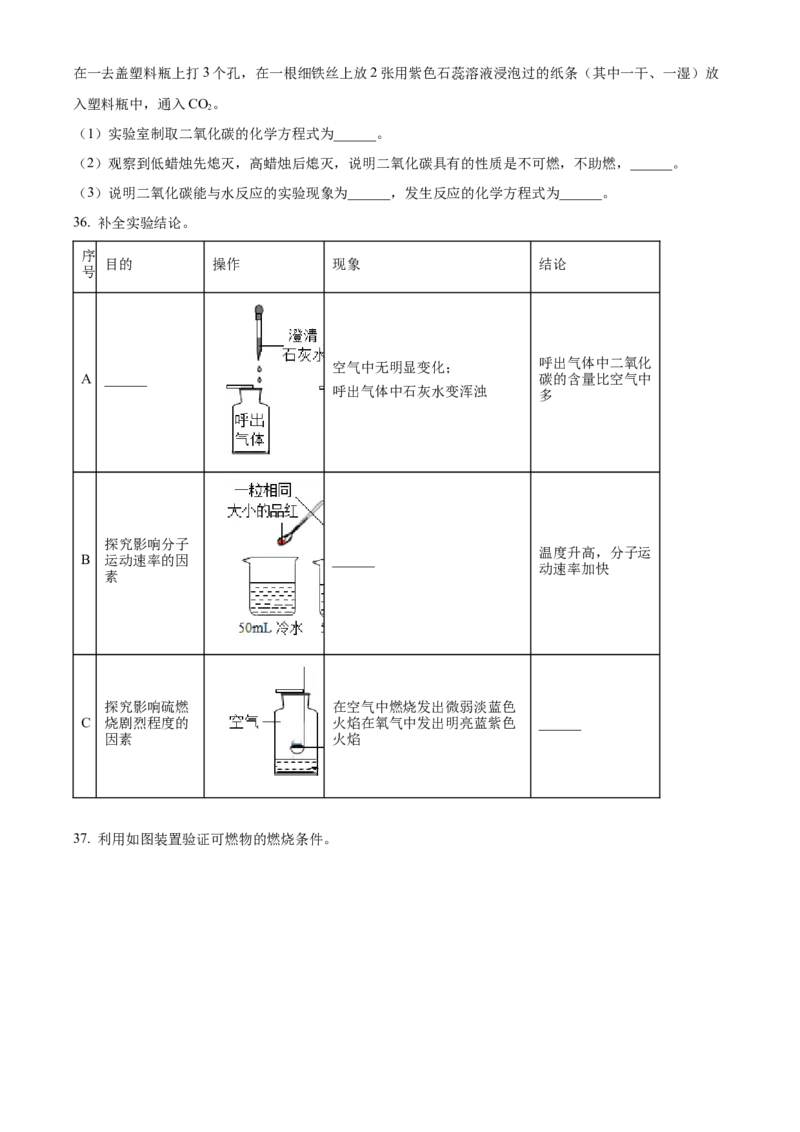
32. 根据下图回答问题。
(1)仪器a的名称是______。
(2)加热KMnO 制取氧气的化学方程式为______。
4
(3)氧气可以用排水法收集的原因是______。(4)B中铁丝在氧气中燃烧的的实验现象为剧烈燃烧,______,放热,生成黑色固体。
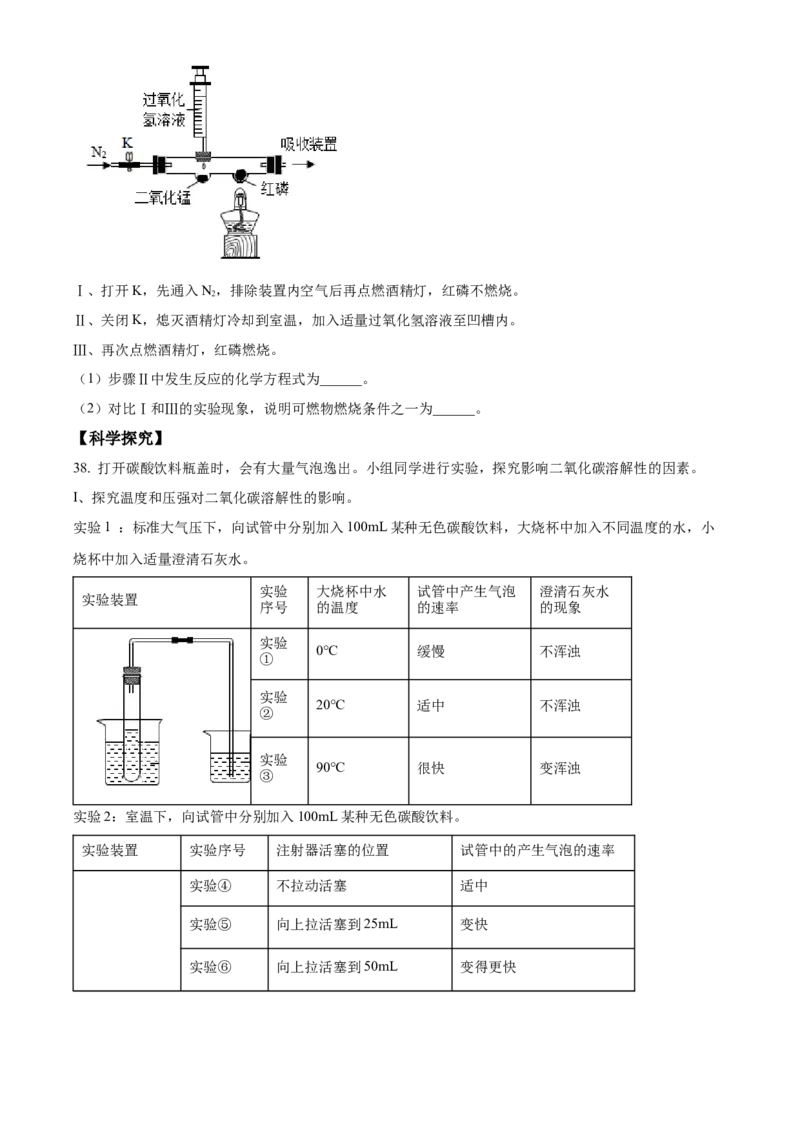
33. 下列是两个关于水的实验。
(1)实验1中,发生反应的化学方程式为______。该实验说明水由______组成。
的
(2)下列说法正确 是______(填字母序号)。
A. 实验1中b管产生的气体能使带火星的木条复燃
B. 实验1中原子的种类、个数均不改变
C. 实验2中发生的是物理变化
D. 实验2中水分子大小改变
34. 用如图装置可以测定空气中氧气含量 。
(1)将导气管放入水中,打开弹簧夹,双手捂住集气瓶,一段时间后,观察到导管口有气泡冒出,说明
______。
(2)能证明空气中氧气含量的实验现象是______。
35. 用如图实验验证二氧化碳的性质。在一去盖塑料瓶上打3个孔,在一根细铁丝上放2张用紫色石蕊溶液浸泡过的纸条(其中一干、一湿)放
入塑料瓶中,通入CO。
2
(1)实验室制取二氧化碳的化学方程式为______。
(2)观察到低蜡烛先熄灭,高蜡烛后熄灭,说明二氧化碳具有的性质是不可燃,不助燃,______。
(3)说明二氧化碳能与水反应的实验现象为______,发生反应的化学方程式为______。
36. 补全实验结论。
序
目的 操作 现象 结论
号
空气中无明显变化; 呼出气体中二氧化
A ______ 碳的含量比空气中
呼出气体中石灰水变浑浊 多
探究影响分子
温度升高,分子运
B 运动速率的因 ______
动速率加快
素
探究影响硫燃 在空气中燃烧发出微弱淡蓝色
C 烧剧烈程度的 火焰在氧气中发出明亮蓝紫色 ______
因素 火焰
37. 利用如图装置验证可燃物的燃烧条件。Ⅰ、打开K,先通入N,排除装置内空气后再点燃酒精灯,红磷不燃烧。
2
Ⅱ、关闭K,熄灭酒精灯冷却到室温,加入适量过氧化氢溶液至凹槽内。
Ⅲ、再次点燃酒精灯,红磷燃烧。
(1)步骤Ⅱ中发生反应的化学方程式为______。
(2)对比Ⅰ和Ⅲ的实验现象,说明可燃物燃烧条件之一为______。
【科学探究】
38. 打开碳酸饮料瓶盖时,会有大量气泡逸出。小组同学进行实验,探究影响二氧化碳溶解性的因素。
Ⅰ、探究温度和压强对二氧化碳溶解性的影响。
实验1 :标准大气压下,向试管中分别加入100mL某种无色碳酸饮料,大烧杯中加入不同温度的水,小
烧杯中加入适量澄清石灰水。
实验 大烧杯中水 试管中产生气泡 澄清石灰水
实验装置
序号 的温度 的速率 的现象
实验
0℃ 缓慢 不浑浊
①
实验
20℃ 适中 不浑浊
②
实验
90℃ 很快 变浑浊
③
实验2:室温下,向试管中分别加入100mL某种无色碳酸饮料。
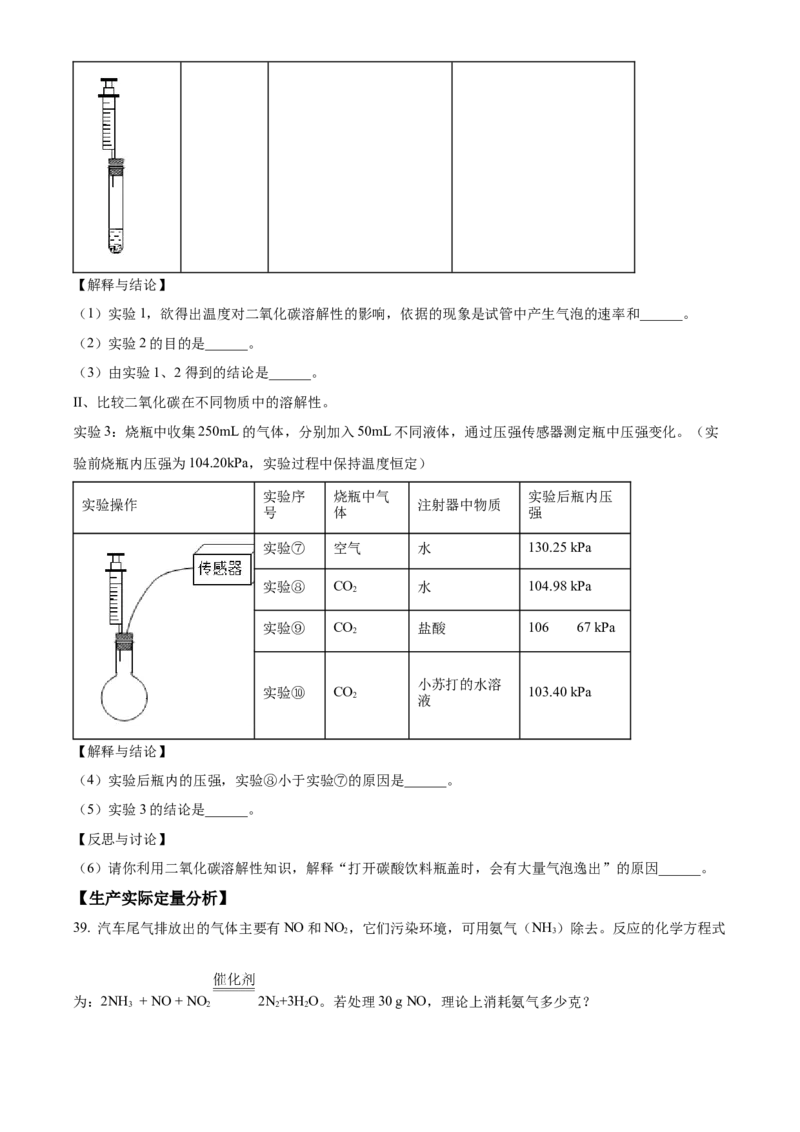
实验装置 实验序号 注射器活塞的位置 试管中的产生气泡的速率
实验④ 不拉动活塞 适中
实验⑤ 向上拉活塞到25mL 变快
实验⑥ 向上拉活塞到50mL 变得更快【解释与结论】
(1)实验1,欲得出温度对二氧化碳溶解性的影响,依据的现象是试管中产生气泡的速率和______。
(2)实验2的目的是______。
(3)由实验1、2得到的结论是______。
Ⅱ、比较二氧化碳在不同物质中的溶解性。
实验3:烧瓶中收集250mL的气体,分别加入50mL不同液体,通过压强传感器测定瓶中压强变化。(实
验前烧瓶内压强为104.20kPa,实验过程中保持温度恒定)
实验序 烧瓶中气 实验后瓶内压
实验操作 注射器中物质
号 体 强
实验⑦ 空气 水 130.25 kPa
实验⑧ CO 水 104.98 kPa
2
.
实验⑨ CO 盐酸 106 67 kPa
2
小苏打的水溶
实验⑩ CO 103.40 kPa
2 液
【解释与结论】
(4)实验后瓶内的压强,实验⑧小于实验⑦的原因是______。
(5)实验3的结论是______。
【反思与讨论】
(6)请你利用二氧化碳溶解性知识,解释“打开碳酸饮料瓶盖时,会有大量气泡逸出”的原因______。
【生产实际定量分析】
39. 汽车尾气排放出的气体主要有NO和NO ,它们污染环境,可用氨气(NH )除去。反应的化学方程式
2 3
为:2NH + NO + NO 2N+3H O。若处理30 g NO,理论上消耗氨气多少克?
3 2 2 2