文档内容
第 12 讲 Na CO 、NaHCO 碱金属
2 3 3
复习目标 1.了解碳酸钠、碳酸氢钠的性质,知道碱金属及其化合物的通性,并能用物质
分类的思想预测陌生碱金属及其化合物的性质。2.掌握碳酸钠、碳酸氢钠的转化关系。3.了
解焰色反应的操作并熟记几种常见金属的焰色。
考点一 Na CO 和 NaHCO
2 3 3
1.碳酸钠和碳酸氢钠的比较
物质 碳酸钠 碳酸氢钠
俗名 苏打、纯碱 小苏打
溶解度 较大 较小
相同温度、相同浓度溶液的碱性 较强 较弱
热稳定性 稳定 不稳定
与酸反应放出CO 的快慢 放出气体较慢 放出气体较快
2
主要用途 制玻璃、肥皂,造纸 制药、发酵粉,作灭火器原料
2.碳酸钠与碳酸氢钠的相互转化
(1)转化关系
NaCONaHCO
2 3 3
(2)转化关系应用
依据二者性质的差异确定除杂方法(后者为杂质)
序号 混合物 除杂方法
① NaCO(s)、NaHCO (s)
2 3 3
② NaHCO (aq)、NaCO(aq)
3 2 3
③ NaCO(aq)、NaHCO (aq)
2 3 3
答案 ①加热法 ②通入足量CO ③滴加适量NaOH溶液
2
3.碳酸钠、碳酸氢钠与酸反应的特点
(1)向碳酸氢钠溶液中逐滴滴入盐酸
①现象:________________________________________________________________________。
②离子方程式: _______________________________________________________。
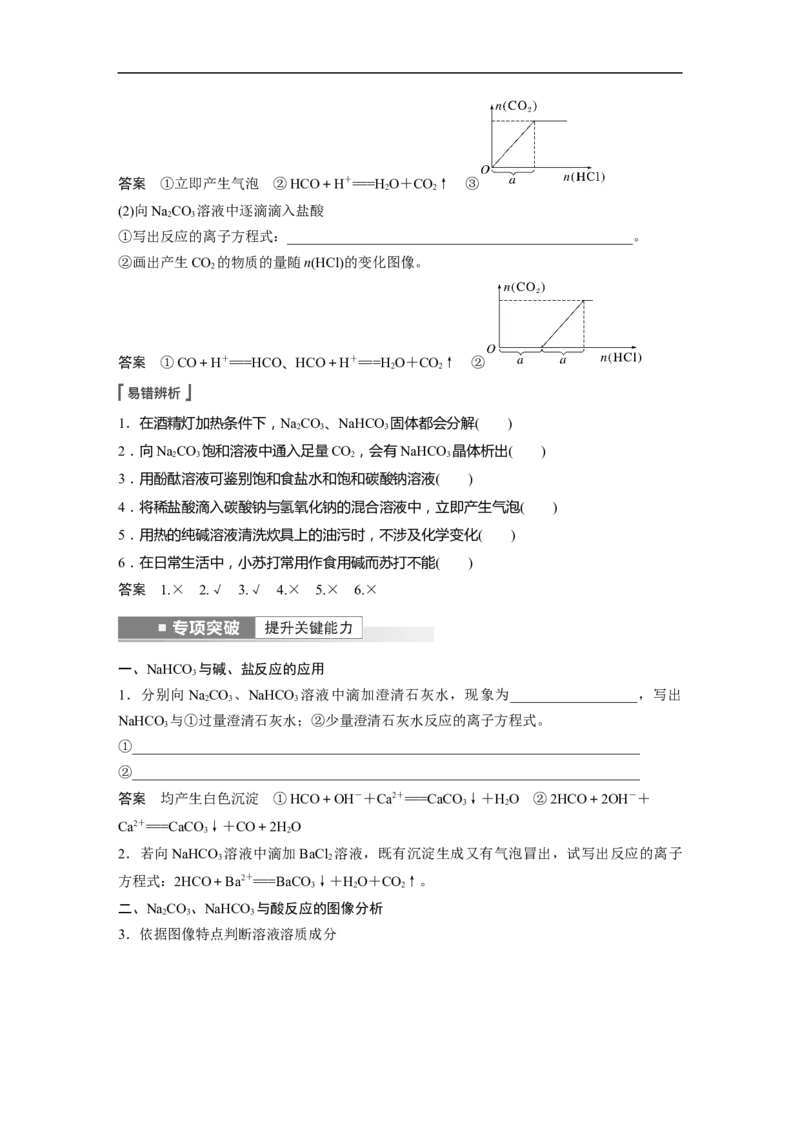
③画出产生CO 的物质的量随n(HCl)的变化图像。
2答案 ①立即产生气泡 ②HCO+H+===HO+CO↑ ③
2 2
(2)向NaCO 溶液中逐滴滴入盐酸
2 3
①写出反应的离子方程式:_________________________________________________。
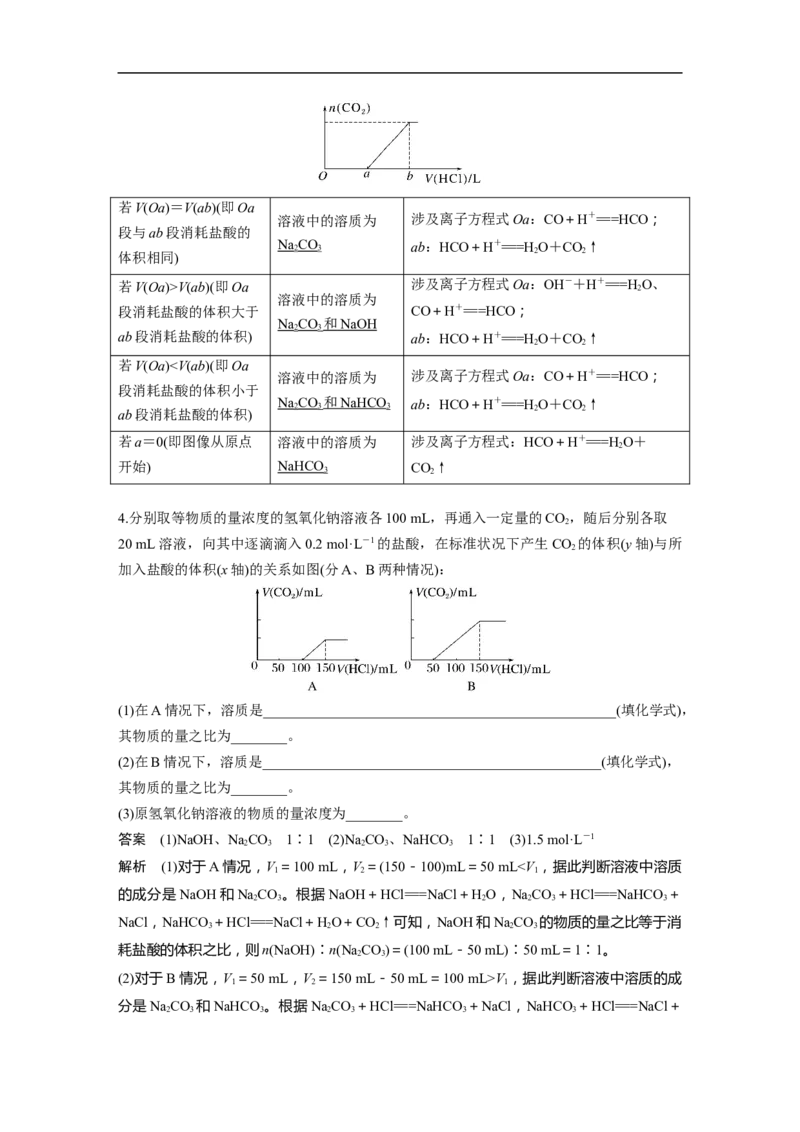
②画出产生CO 的物质的量随n(HCl)的变化图像。
2
答案 ①CO+H+===HCO、HCO+H+===HO+CO↑ ②
2 2
1.在酒精灯加热条件下,NaCO、NaHCO 固体都会分解( )
2 3 3
2.向NaCO 饱和溶液中通入足量CO,会有NaHCO 晶体析出( )
2 3 2 3
3.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液( )
4.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡( )
5.用热的纯碱溶液清洗炊具上的油污时,不涉及化学变化( )
6.在日常生活中,小苏打常用作食用碱而苏打不能( )
答案 1.× 2.√ 3.√ 4.× 5.× 6.×
一、NaHCO 与碱、盐反应的应用
3
1.分别向NaCO 、NaHCO 溶液中滴加澄清石灰水,现象为__________________,写出
2 3 3
NaHCO 与①过量澄清石灰水;②少量澄清石灰水反应的离子方程式。
3
①________________________________________________________________________
②________________________________________________________________________
答案 均产生白色沉淀 ①HCO+OH-+Ca2+===CaCO ↓+HO ②2HCO+2OH-+
3 2
Ca2+===CaCO ↓+CO+2HO
3 2
2.若向NaHCO 溶液中滴加BaCl 溶液,既有沉淀生成又有气泡冒出,试写出反应的离子
3 2
方程式:2HCO+Ba2+===BaCO ↓+HO+CO↑。
3 2 2
二、NaCO、NaHCO 与酸反应的图像分析
2 3 3
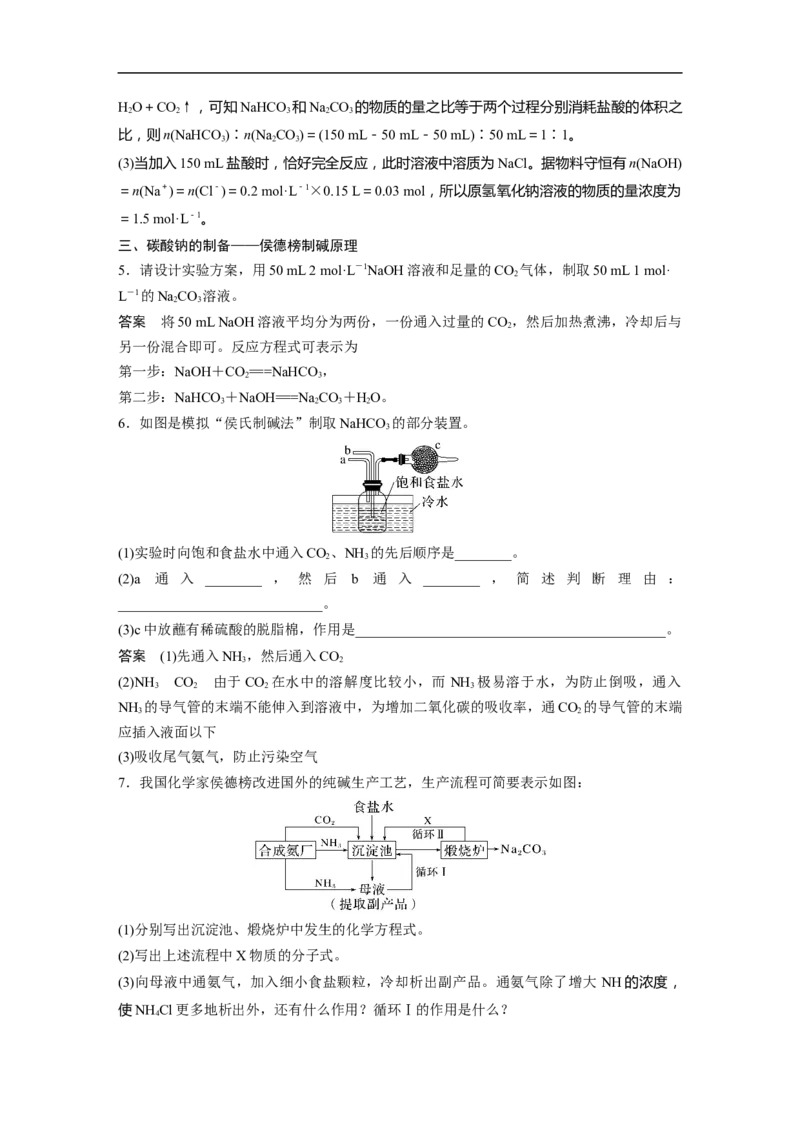
3.依据图像特点判断溶液溶质成分若V(Oa)=V(ab)(即Oa
溶液中的溶质为 涉及离子方程式Oa:CO+H+===HCO;
段与ab段消耗盐酸的
Na
2
CO
3
ab:HCO+H+===H
2
O+CO
2
↑
体积相同)
若V(Oa)>V(ab)(即Oa 涉及离子方程式Oa:OH-+H+===H
2
O、
溶液中的溶质为
段消耗盐酸的体积大于 CO+H+===HCO;
NaCO 和 NaOH
2 3
ab段消耗盐酸的体积) ab:HCO+H+===HO+CO↑
2 2
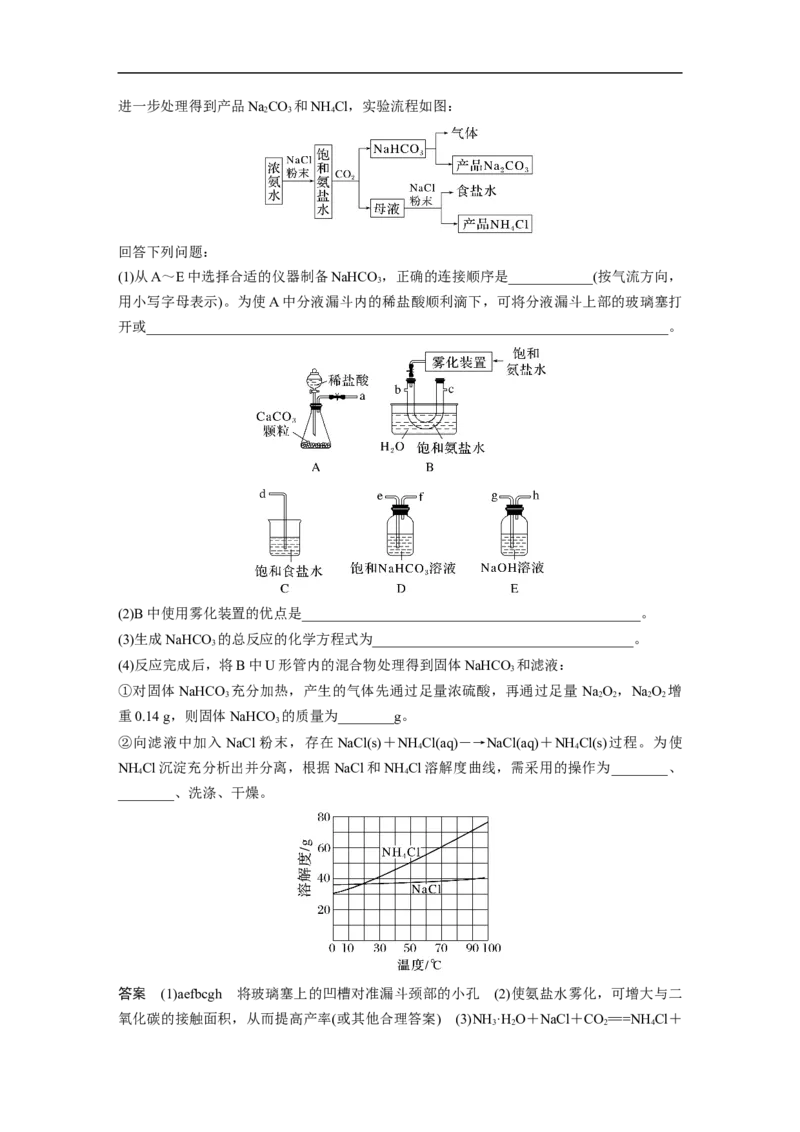
若V(Oa)V ,据此判断溶液中溶质的成
1 2 1
分是NaCO 和NaHCO 。根据NaCO +HCl===NaHCO +NaCl,NaHCO +HCl===NaCl+
2 3 3 2 3 3 3HO+CO↑,可知NaHCO 和NaCO 的物质的量之比等于两个过程分别消耗盐酸的体积之
2 2 3 2 3
比,则n(NaHCO )∶n(Na CO)=(150 mL-50 mL-50 mL)∶50 mL=1∶1。
3 2 3
(3)当加入150 mL盐酸时,恰好完全反应,此时溶液中溶质为NaCl。据物料守恒有n(NaOH)
=n(Na+)=n(Cl-)=0.2 mol·L-1×0.15 L=0.03 mol,所以原氢氧化钠溶液的物质的量浓度为
=1.5 mol·L-1。
三、碳酸钠的制备——侯德榜制碱原理
5.请设计实验方案,用50 mL 2 mol·L-1NaOH溶液和足量的CO 气体,制取50 mL 1 mol·
2
L-1的NaCO 溶液。
2 3
答案 将50 mL NaOH溶液平均分为两份,一份通入过量的CO ,然后加热煮沸,冷却后与
2
另一份混合即可。反应方程式可表示为
第一步:NaOH+CO===NaHCO ,
2 3
第二步:NaHCO +NaOH===NaCO+HO。
3 2 3 2
6.如图是模拟“侯氏制碱法”制取NaHCO 的部分装置。
3
(1)实验时向饱和食盐水中通入CO、NH 的先后顺序是________。
2 3
(2)a 通 入 ________ , 然 后 b 通 入 ________ , 简 述 判 断 理 由 :
_____________________________。
(3)c中放蘸有稀硫酸的脱脂棉,作用是____________________________________________。
答案 (1)先通入NH ,然后通入CO
3 2
(2)NH CO 由于CO 在水中的溶解度比较小,而 NH 极易溶于水,为防止倒吸,通入
3 2 2 3
NH 的导气管的末端不能伸入到溶液中,为增加二氧化碳的吸收率,通CO 的导气管的末端
3 2
应插入液面以下
(3)吸收尾气氨气,防止污染空气
7.我国化学家侯德榜改进国外的纯碱生产工艺,生产流程可简要表示如图:
(1)分别写出沉淀池、煅烧炉中发生的化学方程式。
(2)写出上述流程中X物质的分子式。
(3)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品。通氨气除了增大 NH的浓度,
使NH Cl更多地析出外,还有什么作用?循环Ⅰ的作用是什么?
4(4)如何检验产品碳酸钠中是否含有碳酸氢钠?
答案 (1)NH +CO +NaCl+HO===NH Cl+NaHCO ↓(或NH +CO +HO===NH HCO 、
3 2 2 4 3 3 2 2 4 3
NH HCO +NaCl===NH Cl+NaHCO ↓)、2NaHCO =====NaCO+HO+CO↑
4 3 4 3 3 2 3 2 2
(2)CO
2
(3)使NaHCO 转化为NaCO ,提高析出的NH Cl纯度。循环Ⅰ的作用是提高原料氯化钠的
3 2 3 4
利用率
(4)加热,若产生能使澄清石灰水变浑浊的气体,说明碳酸钠中含有碳酸氢钠,否则,不含
有碳酸氢钠
考点二 碱金属 焰色反应
1.碱金属的相似性和递变性
相似性 递变性(由Li→Cs)
电子层数逐渐增多;核电荷数逐
原子结构 最外层均为 1 个 电子
渐增大;原子半径逐渐增大
都具有较强的金属性,最高正价
元素性质 金属性逐渐增强
均为 + 1 价
单 物理 (除Cs外)都呈银白色,密度较 密度逐渐增大(钾反常),熔、沸点
质 性质 小,熔、沸点较低 逐渐降低
性 化学 还原性逐渐增强;与O 反应越来
2
都具有较强的还原性
质 性质 越剧烈,产物越来越复杂
2.碱金属的特性
(1)碱金属的密度一般随核电荷数的增大而增大,但钾的密度比钠的小。
(2)碱金属一般都保存在煤油中,但由于锂的密度小于煤油的密度而将锂保存在石蜡中。
(3)碱金属跟氢气反应生成的碱金属氢化物都是离子化合物,其中氢以H-形式存在,显-1
价,碱金属氢化物是强还原剂。
(4)试剂瓶中的药品取出后,一般不能放回原瓶,但Na、K等需放回原瓶。
(5)锂与O 反应与钠不同,只生成LiO。
2 2
3.焰色反应
(1)焰色反应的概念
某些金属或它们的化合物在灼烧时都会使火焰呈现出特殊的颜色,属于物理变化,是元素的
性质。(2)焰色反应的操作
①清洗铂丝:将铂丝蘸稀盐酸在无色火焰上灼烧至无色。
②灼烧试样:蘸取试样在无色火焰上灼烧,观察火焰颜色。
③清洗铂丝:将铂丝再蘸稀盐酸灼烧至无色。
提醒 做钾的焰色反应时,需透过蓝色钴玻璃观察现象。
(3)熟记常见金属的焰色
钠元素:黄色;钾元素:紫色(透过蓝色钴玻璃观察);铜元素:绿色;钡元素:黄绿色;钙
元素:砖红色。
1.钠、氧化钠、碳酸钠的焰色反应均显黄色( )
2.做焰色反应时,用稀HSO 洗涤铂丝( )
2 4
3.钠的还原性比钾的弱,但工业上制取钾可用Na和熔融KCl在高温下反应制备( )
4.Li在空气中加热可快速反应生成LiO( )
2 2
5.焰色反应是金属化合物的性质( )
6.碱金属元素由Li到Cs,随着核电荷数的递增,单质密度逐渐增大,熔、沸点逐渐降低(
)
答案 1.√ 2.× 3.√ 4.× 5.× 6.×
碱金属单质及其化合物有广泛应用。回答下列问题:
(1)锂是最轻的活泼金属,常用于制造高效锂电池。电解池中的电解液不能用水作溶剂,原
因是___________________________________________________________________________。
(2)金属钾是一种活泼的金属,下列有关其性质的说法正确的是________(填字母)。
A.钾在空气中燃烧时,只生成KO
2
B.钾与水反应,由于反应剧烈可能会发生爆炸
C.1 mol·L-1KOH溶液比1 mol·L-1NaOH溶液碱性强
(3)KH是一种野外供氢剂,其电子式为________,与水反应放出氢气,化学方程式为
___________________________________________________________________________。
生成1 mol氢气时,反应中转移电子数为____________________________________。
(4)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O),脱锈过程中
2 3
生成两种产物,其反应的化学方程式: _______________________________________。
答案 (1)锂可以与水反应 (2)B
(3)K+[H]- KH+HO===KOH+H↑ N
2 2 A
(4)3NaH+Fe O===2Fe+3NaOH
2 3碱金属单质及其氢化物都是强还原剂,遇水立即反应产生氢气和碱金属的氢氧化物。
1.判断下列说法的正误
(1)NaHCO 的热稳定性比NaCO 强(2020·浙江7月选考,8B)( )
3 2 3
(2)在给定条件下能实现转化:NaCl(aq)――→NaHCO (s)――→NaCO(s)
3 2 3
(2020·江苏,10B)( )
(3)盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良(2019·天津,3C)(
2 3
)
(4)碳酸钠可用于去除餐具的油污(2018·全国卷Ⅱ,7A)( )
(5)因NaHCO 受热易分解,可用于制胃酸中和剂(2018·江苏,3A)( )
3
(6)溶解度:NaCONa>K
D.碱性:氢氧化铯>氢氧化钠
答案 B
解析 锂的活动性比钠弱,与水反应不如钠剧烈,故A正确;锂没有过氧化物,故B错误;
碱金属元素从Li到Cs ,熔、沸点逐渐降低,故C正确;从Li到Cs ,元素的金属性逐渐
增强,其最高价氧化物对应水化物的碱性依次增强,即碱性:CsOH>NaOH ,故D正确。
5.钠在空气中的变化过程为( )
A.Na→NaO→ NaOH→ Na CO·10H O→NaCO
2 2 2 3 2 2 3
B.Na→NaO→NaOH→NaCO·10H O→NaCO
2 2 3 2 2 3
C.Na→NaO→NaOH→NaCO·10H O→NaHCO
2 2 2 3 2 3
D.Na→NaO→NaOH→NaCO·10H O→NaHCO
2 2 3 2 3
答案 B
6.侯德榜是我国杰出的化学家,“侯氏制碱法”的创始人。NaCl+CO +NH +HO===
2 3 2
NaHCO ↓+NH Cl是“侯氏制碱法”的重要反应。下面是4位同学对该反应涉及的有关知
3 4
识发表的部分见解,其中不正确的是( )
A.甲同学说:该条件下NaHCO 的溶解度较小
3B.乙同学说:NaHCO 不是纯碱
3
C.丙同学说:析出NaHCO 固体后的溶液中只含氯化铵
3
D.丁同学说:该反应是在饱和食盐水中先通入氨气,再通入二氧化碳
答案 C
解析 碳酸氢钠是小苏打,纯碱是碳酸钠,B项正确;析出碳酸氢钠,说明剩余的溶液为碳
酸氢钠的饱和溶液,C项错误;先通入氨气至饱和,再通入过量二氧化碳,这样可以保证在
碱性条件下生成更多的HCO,D项正确。
7.将一定量的碳酸氢钠(含少量氯化钠)固体加热一段时间,再加入足量的盐酸完全反应。
下列有关叙述正确的是( )
A.原固体中碳酸氢钠含量越多,钠元素的含量也越多
B.若原固体加热质量减少3.1 g,固体中碳酸氢钠的质量为8.4 g
C.若反应后溶液中含0.1 mol Na+,原固体的质量可能为8.0 g
D.原固体分解越完全,消耗盐酸的量越少
答案 C
解析 假设固体都是NaHCO ,钠元素的含量为×100%≈27.4%,若都是NaCl,钠元素的含
3
量为×100%≈39.3%,故NaCl越多钠元素的含量越高,故A错误;168 g NaHCO 分解生成
3
NaCO 、HO、CO ,反应中固体质量减少62 g(H O+CO),若原固体加热质量减少3.1 g,
2 3 2 2 2 2
固体中反应的碳酸氢钠质量为8.4 g,但碳酸氢钠不一定全部分解,故原固体中碳酸氢钠质
量可能大于8.4 g,故B错误;结合极值计算分析判断,若为碳酸氢钠,则质量为 8.4 g,若
为氯化钠,则质量为5.85 g,原固体的质量可能为8.0 g,故C正确;固体分解不完全时,固
体有NaHCO 和NaCO ,根据化学方程式NaHCO +HCl===NaCl+HO+CO↑,则1 mol
3 2 3 3 2 2
NaHCO 消耗1 mol HCl,由NaCO+2HCl===2NaCl+HO+CO↑,则1 mol Na CO 消耗
3 2 3 2 2 2 3
2 mol HCl,则相同的物质的量的条件下 NaCO 消耗的盐酸多,故固体完全分解都变成
2 3
NaCO,会导致消耗盐酸的量增加,故D错误。
2 3
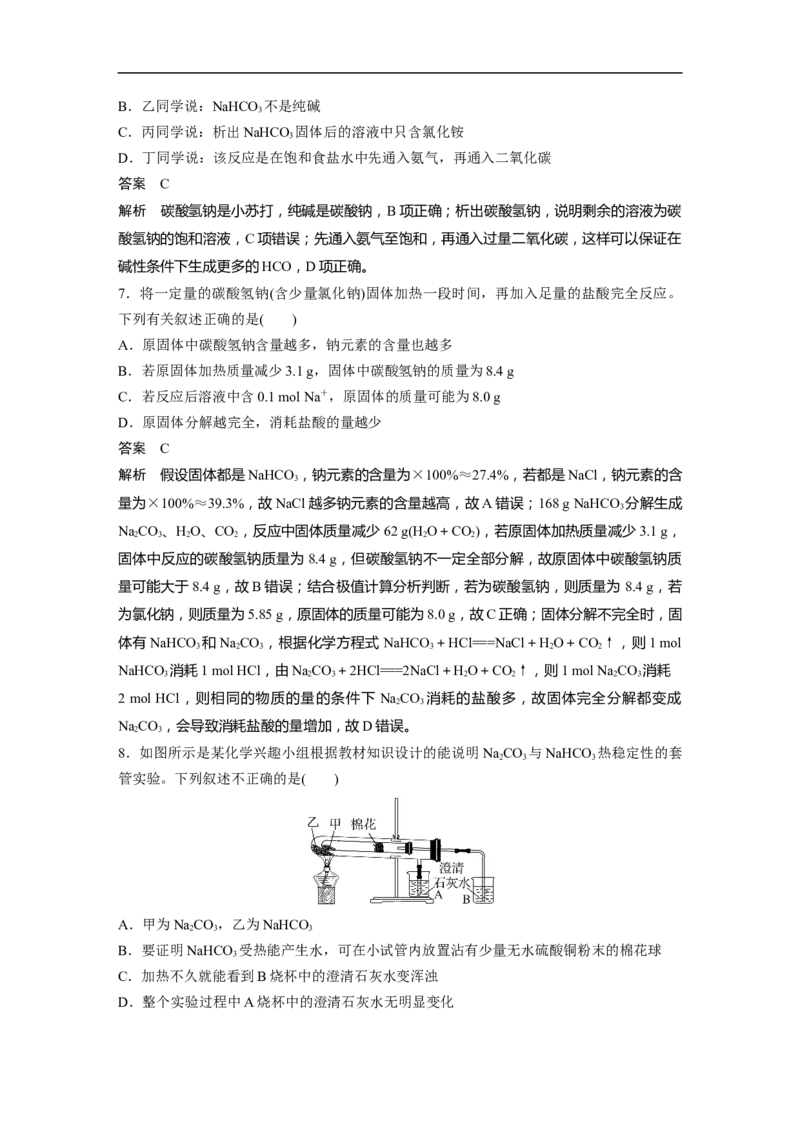
8.如图所示是某化学兴趣小组根据教材知识设计的能说明NaCO 与NaHCO 热稳定性的套
2 3 3
管实验。下列叙述不正确的是( )
A.甲为NaCO,乙为NaHCO
2 3 3
B.要证明NaHCO 受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球
3
C.加热不久就能看到B烧杯中的澄清石灰水变浑浊
D.整个实验过程中A烧杯中的澄清石灰水无明显变化答案 A
解析 甲为NaHCO ,乙为NaCO ,A项错误;无水硫酸铜遇水变成蓝色,B项正确;
3 2 3
NaHCO 不稳定,受热分解产生的CO 进入B中,使澄清石灰水变浑浊,C项正确;NaCO
3 2 2 3
稳定,受热不分解,A中的澄清石灰水不会变浑浊,D项正确。
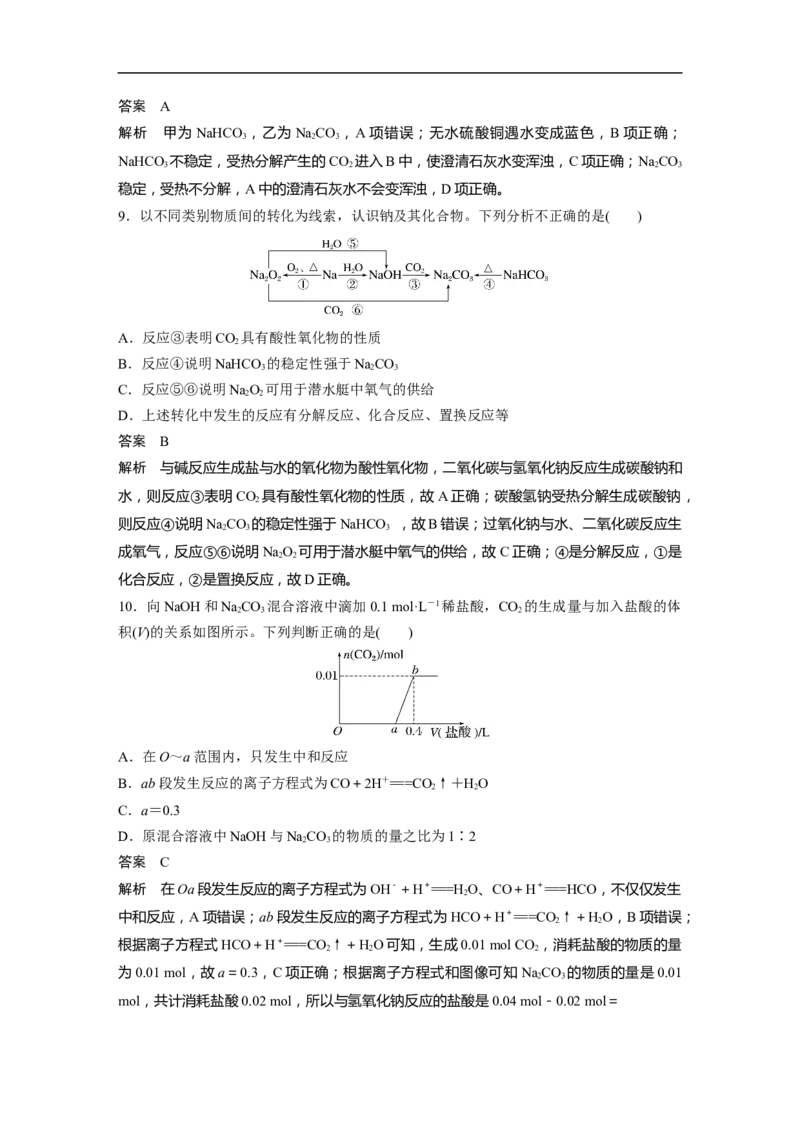
9.以不同类别物质间的转化为线索,认识钠及其化合物。下列分析不正确的是( )
A.反应③表明CO 具有酸性氧化物的性质
2
B.反应④说明NaHCO 的稳定性强于NaCO
3 2 3
C.反应⑤⑥说明NaO 可用于潜水艇中氧气的供给
2 2
D.上述转化中发生的反应有分解反应、化合反应、置换反应等
答案 B
解析 与碱反应生成盐与水的氧化物为酸性氧化物,二氧化碳与氢氧化钠反应生成碳酸钠和
水,则反应③表明CO 具有酸性氧化物的性质,故A正确;碳酸氢钠受热分解生成碳酸钠,
2
则反应④说明NaCO 的稳定性强于NaHCO ,故B错误;过氧化钠与水、二氧化碳反应生
2 3 3
成氧气,反应⑤⑥说明NaO 可用于潜水艇中氧气的供给,故C正确;④是分解反应,①是
2 2
化合反应,②是置换反应,故D正确。
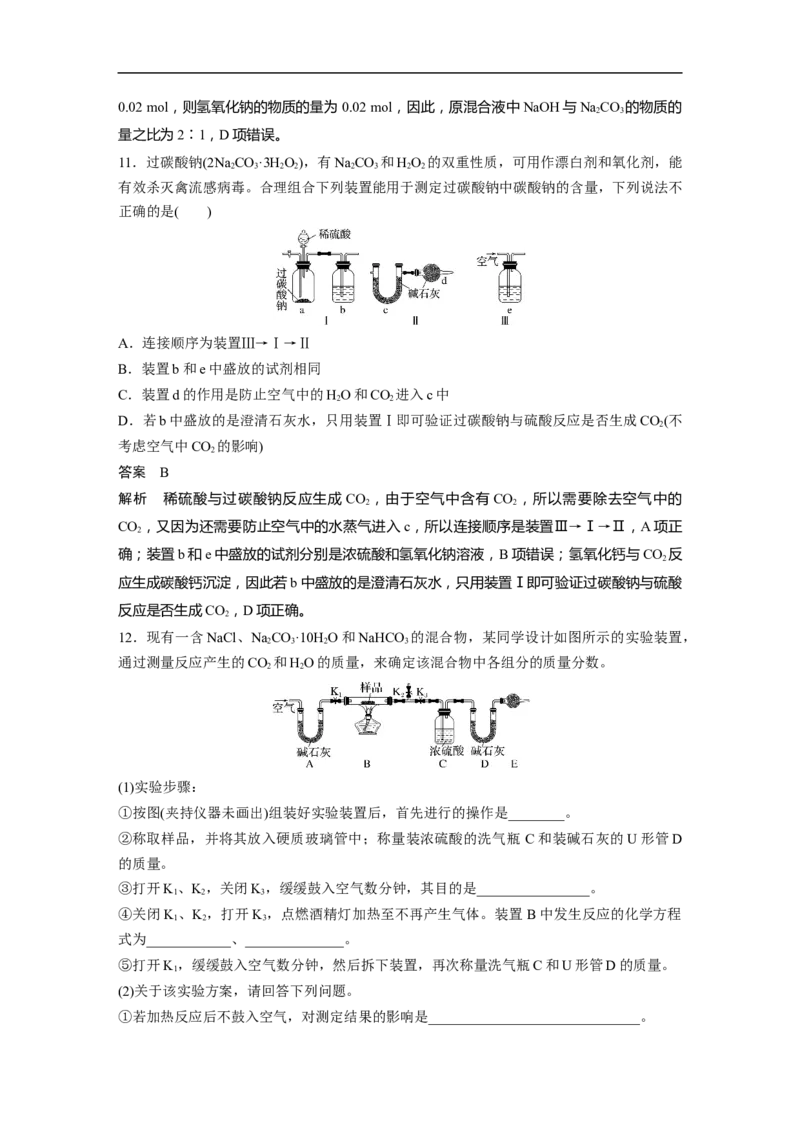
10.向NaOH和NaCO 混合溶液中滴加0.1 mol·L-1稀盐酸,CO 的生成量与加入盐酸的体
2 3 2
积(V)的关系如图所示。下列判断正确的是( )
A.在O~a范围内,只发生中和反应
B.ab段发生反应的离子方程式为CO+2H+===CO↑+HO
2 2
C.a=0.3
D.原混合溶液中NaOH与NaCO 的物质的量之比为1∶2
2 3
答案 C
解析 在Oa段发生反应的离子方程式为OH-+H+===HO、CO+H+===HCO,不仅仅发生
2
中和反应,A项错误;ab段发生反应的离子方程式为HCO+H+===CO↑+HO,B项错误;
2 2
根据离子方程式HCO+H+===CO↑+HO可知,生成0.01 mol CO ,消耗盐酸的物质的量
2 2 2
为0.01 mol,故a=0.3,C项正确;根据离子方程式和图像可知NaCO 的物质的量是0.01
2 3
mol,共计消耗盐酸0.02 mol,所以与氢氧化钠反应的盐酸是0.04 mol-0.02 mol=0.02 mol,则氢氧化钠的物质的量为0.02 mol,因此,原混合液中NaOH与NaCO 的物质的
2 3
量之比为2∶1,D项错误。
11.过碳酸钠(2Na CO·3H O),有NaCO 和HO 的双重性质,可用作漂白剂和氧化剂,能
2 3 2 2 2 3 2 2
有效杀灭禽流感病毒。合理组合下列装置能用于测定过碳酸钠中碳酸钠的含量,下列说法不
正确的是( )
A.连接顺序为装置Ⅲ→Ⅰ→Ⅱ
B.装置b和e中盛放的试剂相同
C.装置d的作用是防止空气中的HO和CO 进入c中
2 2
D.若b中盛放的是澄清石灰水,只用装置Ⅰ即可验证过碳酸钠与硫酸反应是否生成CO(不
2
考虑空气中CO 的影响)
2
答案 B
解析 稀硫酸与过碳酸钠反应生成 CO ,由于空气中含有CO ,所以需要除去空气中的
2 2
CO ,又因为还需要防止空气中的水蒸气进入c,所以连接顺序是装置Ⅲ→Ⅰ→Ⅱ,A项正
2
确;装置b和e中盛放的试剂分别是浓硫酸和氢氧化钠溶液,B项错误;氢氧化钙与CO 反
2
应生成碳酸钙沉淀,因此若b中盛放的是澄清石灰水,只用装置Ⅰ即可验证过碳酸钠与硫酸
反应是否生成CO,D项正确。
2
12.现有一含NaCl、NaCO·10H O和NaHCO 的混合物,某同学设计如图所示的实验装置,
2 3 2 3
通过测量反应产生的CO 和HO的质量,来确定该混合物中各组分的质量分数。
2 2
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶 C和装碱石灰的U形管D
的质量。
③打开K、K,关闭K,缓缓鼓入空气数分钟,其目的是________________。
1 2 3
④关闭K 、K ,打开K ,点燃酒精灯加热至不再产生气体。装置 B中发生反应的化学方程
1 2 3
式为____________、______________。
⑤打开K,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
1
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是______________________________。②E处干燥管中盛放的药品是________,其作用是___________________________________,
如果实验中没有该装置,则会导致测得的NaHCO 的质量________(填“偏大”“偏小”或
3
“无影响”)。
③若样品质量为 w g,反应后 C、D装置增加的质量分别为 m g、m g,则混合物中
1 2
NaCO·10H O的质量分数为____________(用含w、m、m 的代数式表示)。
2 3 2 1 2
答 案 (1)① 检 查 装 置 的 气 密 性 ③ 除 去 装 置 中 的 水 蒸 气 和 二 氧 化 碳
④2NaHCO =====NaCO+HO↑+CO↑ NaCO·10H O=====NaCO+10HO↑
3 2 3 2 2 2 3 2 2 3 2
(2)①NaCO·10H O和NaHCO 的质量分数测定结果偏小,NaCl的质量分数测定结果偏大
2 3 2 3
②碱石灰 防止空气中的CO 和水蒸气进入D中影响测定结果 偏大 ③×100%
2
解析 (2)①加热后有部分CO 和水蒸气会残留在装置中,必须鼓入空气使其完全被吸收,
2
若不鼓入空气,则测得的NaHCO 和NaCO·10H O的质量分数会偏小,NaCl的质量分数会
3 2 3 2
偏大。②装置E的作用是防止空气中的CO 和水蒸气进入装置D,故干燥管中盛放的药品是
2
碱石灰,如果没有该装置,会使测得的 NaHCO 的质量偏大。③由题目信息知反应放出的
3
CO 的质量为m g,根据反应2NaHCO =====NaCO +HO↑+CO↑,可计算出该反应中
2 2 3 2 3 2 2
产生水的质量为 g,从而计算出 NaCO·10H O 分解产生水的质量为(m -) g,再根据
2 3 2 1
NaCO·10H O=====NaCO +10HO↑,计算出NaCO·10H O的质量,最后计算出混合物
2 3 2 2 3 2 2 3 2
中NaCO·10H O的质量分数。
2 3 2