文档内容
热点强化 5 化学计算方法在热重分析中的应用
(1)设晶体为1 mol。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步的m(剩余),×100%=固体残留率。
(4)晶体中金属质量不减少,仍在m(剩余)中。
(5)失重最后一般为金属氧化物,由质量守恒得m(O),由n(金属)∶n(O),即可求出失重后物
质的化学式。
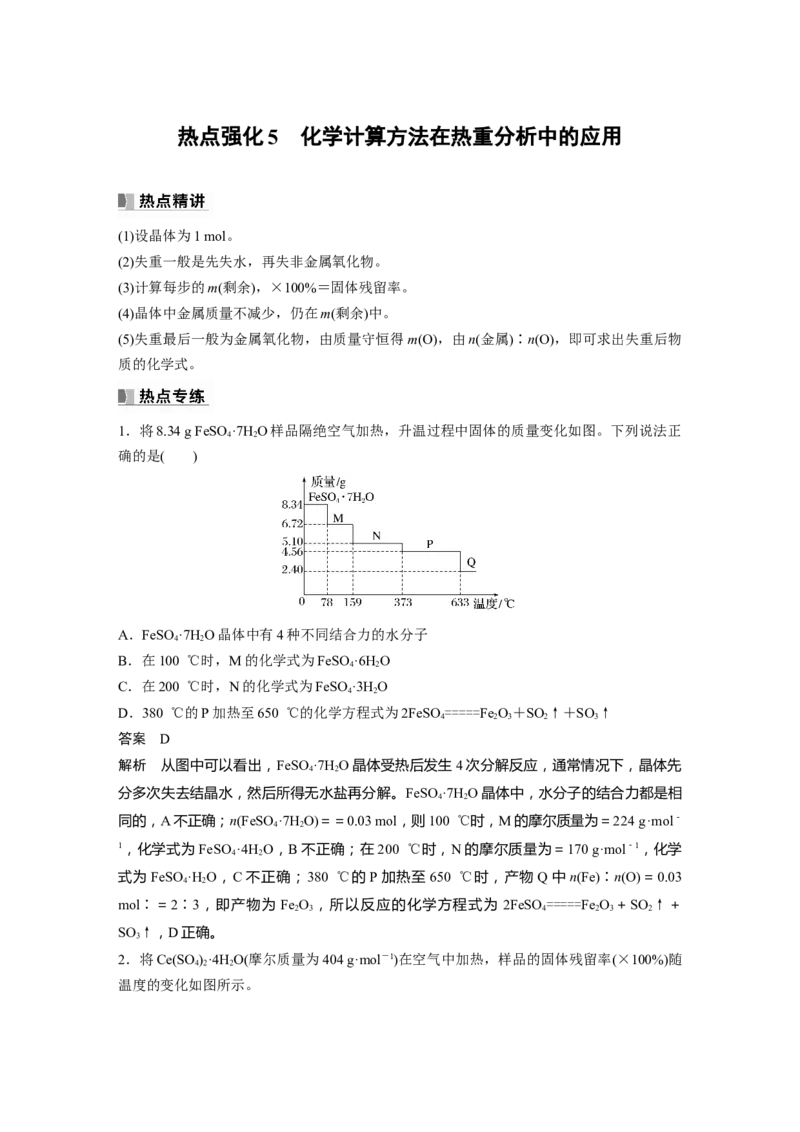
1.将8.34 g FeSO ·7H O样品隔绝空气加热,升温过程中固体的质量变化如图。下列说法正
4 2
确的是( )
A.FeSO ·7H O晶体中有4种不同结合力的水分子
4 2
B.在100 ℃时,M的化学式为FeSO ·6H O
4 2
C.在200 ℃时,N的化学式为FeSO ·3H O
4 2
D.380 ℃的P加热至650 ℃的化学方程式为2FeSO =====Fe O+SO ↑+SO ↑
4 2 3 2 3
答案 D
解析 从图中可以看出,FeSO ·7H O晶体受热后发生4次分解反应,通常情况下,晶体先
4 2
分多次失去结晶水,然后所得无水盐再分解。FeSO ·7H O晶体中,水分子的结合力都是相
4 2
同的,A不正确;n(FeSO ·7H O)==0.03 mol,则100 ℃时,M的摩尔质量为=224 g·mol-
4 2
1,化学式为FeSO ·4H O,B不正确;在200 ℃时,N的摩尔质量为=170 g·mol-1,化学
4 2
式为FeSO ·H O,C不正确;380 ℃的P加热至650 ℃时,产物 Q中n(Fe)∶n(O)=0.03
4 2
mol∶=2∶3,即产物为 Fe O ,所以反应的化学方程式为 2FeSO =====Fe O +SO ↑+
2 3 4 2 3 2
SO ↑,D正确。
3
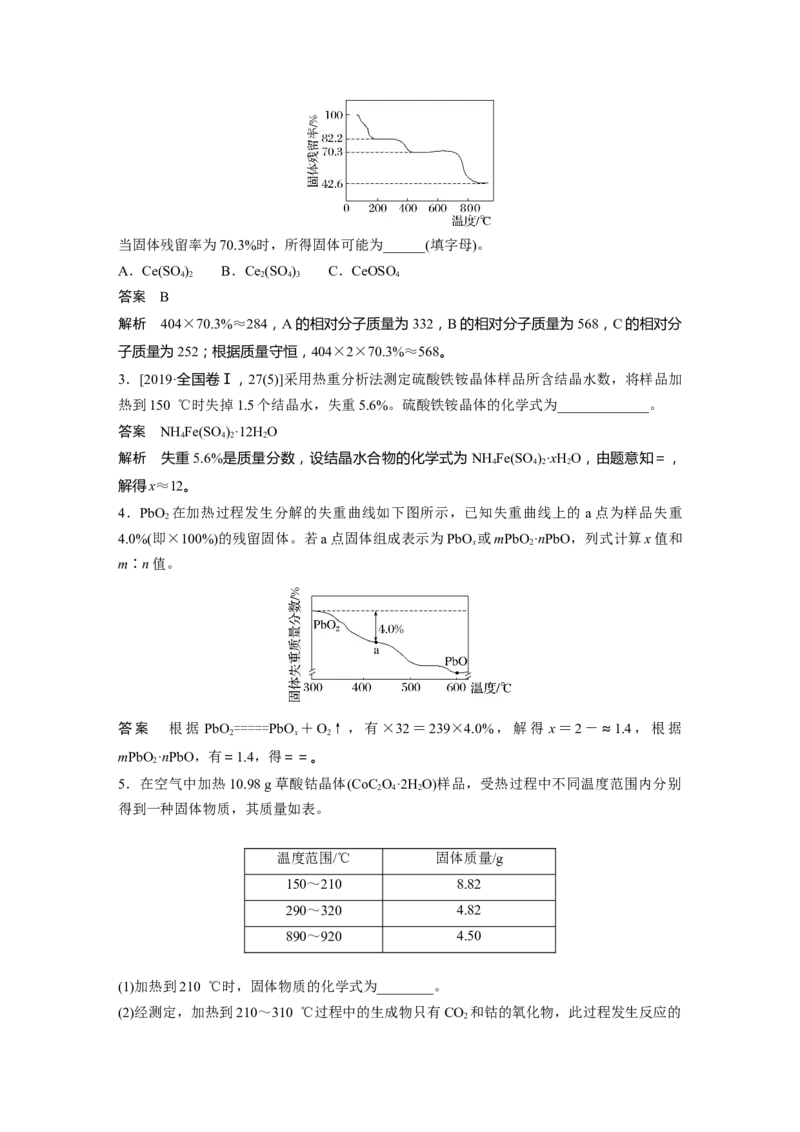
2.将Ce(SO)·4H O(摩尔质量为404 g·mol-1)在空气中加热,样品的固体残留率(×100%)随
4 2 2
温度的变化如图所示。当固体残留率为70.3%时,所得固体可能为______(填字母)。
A.Ce(SO) B.Ce (SO ) C.CeOSO
4 2 2 4 3 4
答案 B
解析 404×70.3%≈284,A的相对分子质量为332,B的相对分子质量为568,C的相对分
子质量为252;根据质量守恒,404×2×70.3%≈568。
3.[2019·全国卷Ⅰ,27(5)]采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加
热到150 ℃时失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为_____________。
答案 NH Fe(SO )·12H O
4 4 2 2
解析 失重5.6%是质量分数,设结晶水合物的化学式为NH Fe(SO )·xHO,由题意知=,
4 4 2 2
解得x≈12。
4.PbO 在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的 a点为样品失重
2
4.0%(即×100%)的残留固体。若a点固体组成表示为PbO 或mPbO ·nPbO,列式计算x值和
x 2
m∶n值。
答案 根据 PbO =====PbO +O↑,有×32=239×4.0%,解得 x=2-≈1.4,根据
2 x 2
mPbO ·nPbO,有=1.4,得==。
2
5.在空气中加热10.98 g草酸钴晶体(CoC O·2H O)样品,受热过程中不同温度范围内分别
2 4 2
得到一种固体物质,其质量如表。
温度范围/℃ 固体质量/g
150~210 8.82
290~320 4.82
890~920 4.50
(1)加热到210 ℃时,固体物质的化学式为________。
(2)经测定,加热到210~310 ℃过程中的生成物只有CO 和钴的氧化物,此过程发生反应的
2化学方程式为______________________________________________________________。
答案 (1)CoC O (2)3CoC O+2O=====Co O+6CO
2 4 2 4 2 3 4 2
解析 (1)n(CoC O·2H O)=0.06 mol,
2 4 2
Δm=(10.98-8.82) g=2.16 g=m(H O),
2
故210 ℃时固体为CoC O。
2 4
(2)根据钴原子守恒可知
m(Co)=3.54 g,m(O)=(4.82-3.54) g=1.28 g,
n(O)=0.08 mol,n(Co)∶n(O)=3∶4,
可写出化学方程式:3CoC O+2O=====Co O+6CO。
2 4 2 3 4 2
6.(2022·浙江模拟)CuSO ·5H O 在不同温度下失水和分解,随着温度升高分别生成
4 2
CuSO →CuO→Cu O→Cu,现称取5.000 g CuSO ·5H O在敞口容器加热一定时间后,得到
4 2 4 2
1.520 g固体,测得生成的SO 的体积为0.224 L(已折算为标准状况),求:
2
(1)固体的成分及物质的量之比:________。
(2)标准状态下生成O 的体积:________。
2
答案 (1)n(CuO)∶n(Cu O)=2∶1
2
(2)0.168 L
解析 (1)5.000 g CuSO ·5H O物质的量为0.02 mol,若生成的全部是硫酸铜,则质量为3.2
4 2
g,若全部生成氧化铜,则质量为1.6 g,若全部生成氧化亚铜,则质量为1.44 g,而得到
1.520 g固体,说明固体的成分是氧化铜和氧化亚铜的混合物,设氧化铜物质的量为 x mol,
氧化亚铜物质的量为y mol,则有x+2y=0.02,80x+144y=1.52,解得x=0.01,y=0.005,
则物质的量之比n(CuO)∶n(Cu O)=2∶1。
2
(2)生成了标准状况下0.224 L二氧化硫,即物质的量为0.01 mol,分析知硫、铜化合价降低,
氧化合价升高,根据得失电子守恒得到O 物质的量为=0.007 5 mol,其标准状态下的体积为
2
0.007 5 mol×22.4 L·mol-1=0.168 L。
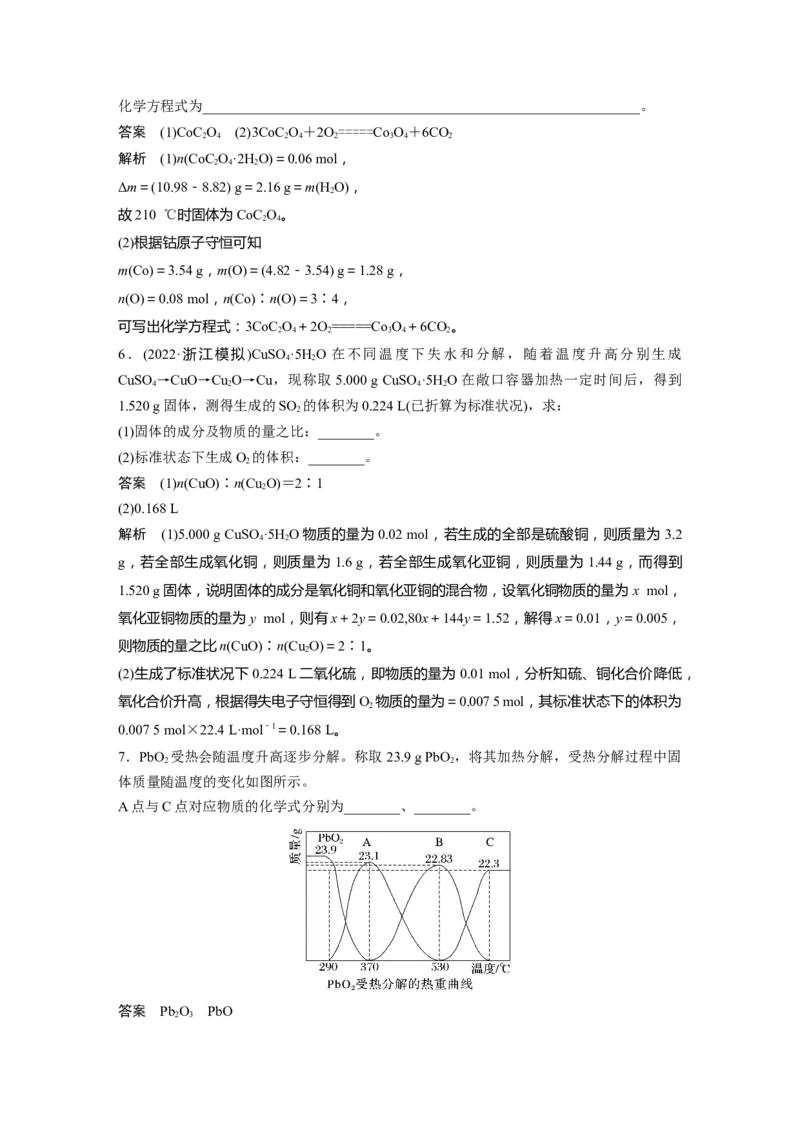
7.PbO 受热会随温度升高逐步分解。称取23.9 g PbO ,将其加热分解,受热分解过程中固
2 2
体质量随温度的变化如图所示。
A点与C点对应物质的化学式分别为________、________。
答案 Pb O PbO
2 3解析 二氧化铅是0.1 mol,其中氧原子是0.2 mol。A点固体减少0.8 g,则剩余氧原子的物
质的量是0.15 mol,此时剩余的铅和氧原子的个数之比是2∶3,A点对应的物质是Pb O 。
2 3
同理可得出C点对应的物质是PbO。
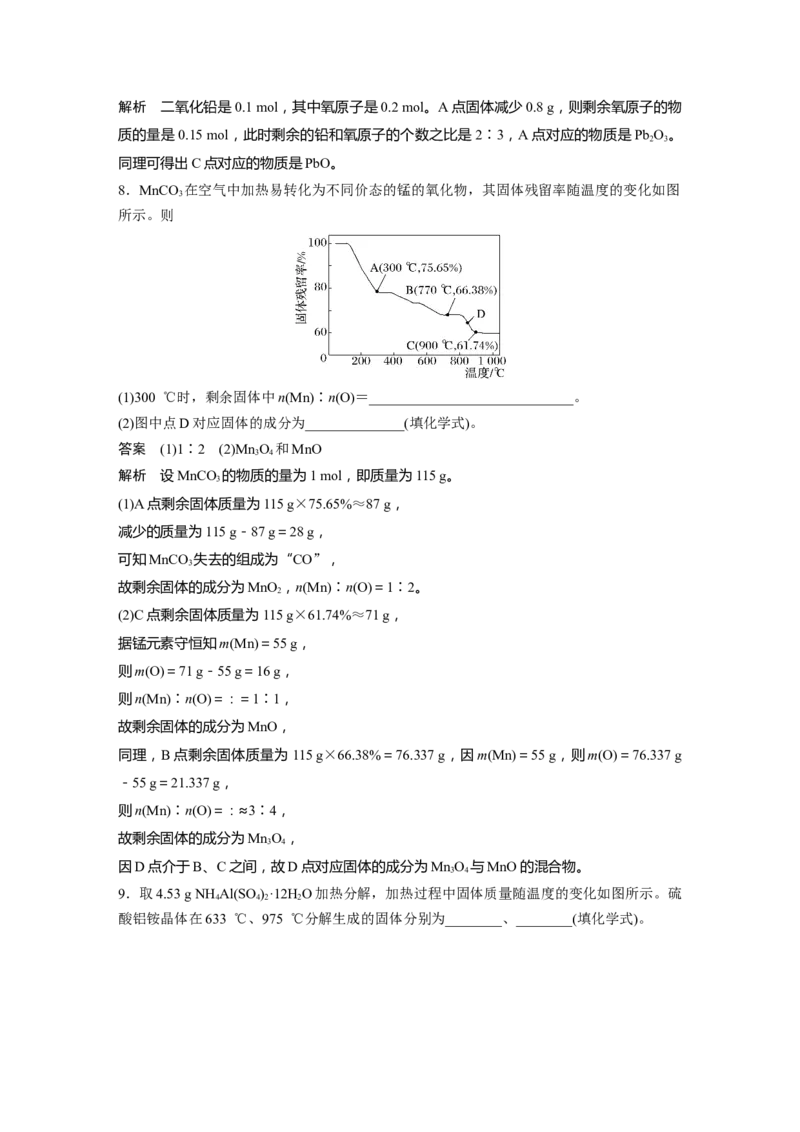
8.MnCO 在空气中加热易转化为不同价态的锰的氧化物,其固体残留率随温度的变化如图
3
所示。则
(1)300 ℃时,剩余固体中n(Mn)∶n(O)=_____________________________。
(2)图中点D对应固体的成分为______________(填化学式)。
答案 (1)1∶2 (2)Mn O 和MnO
3 4
解析 设MnCO 的物质的量为1 mol,即质量为115 g。
3
(1)A点剩余固体质量为115 g×75.65%≈87 g,
减少的质量为115 g-87 g=28 g,
可知MnCO 失去的组成为“CO”,
3
故剩余固体的成分为MnO ,n(Mn)∶n(O)=1∶2。
2
(2)C点剩余固体质量为115 g×61.74%≈71 g,
据锰元素守恒知m(Mn)=55 g,
则m(O)=71 g-55 g=16 g,
则n(Mn)∶n(O)=∶=1∶1,
故剩余固体的成分为MnO,
同理,B点剩余固体质量为115 g×66.38%=76.337 g,因m(Mn)=55 g,则m(O)=76.337 g
-55 g=21.337 g,
则n(Mn)∶n(O)=∶≈3∶4,
故剩余固体的成分为MnO,
3 4
因D点介于B、C之间,故D点对应固体的成分为MnO 与MnO的混合物。
3 4
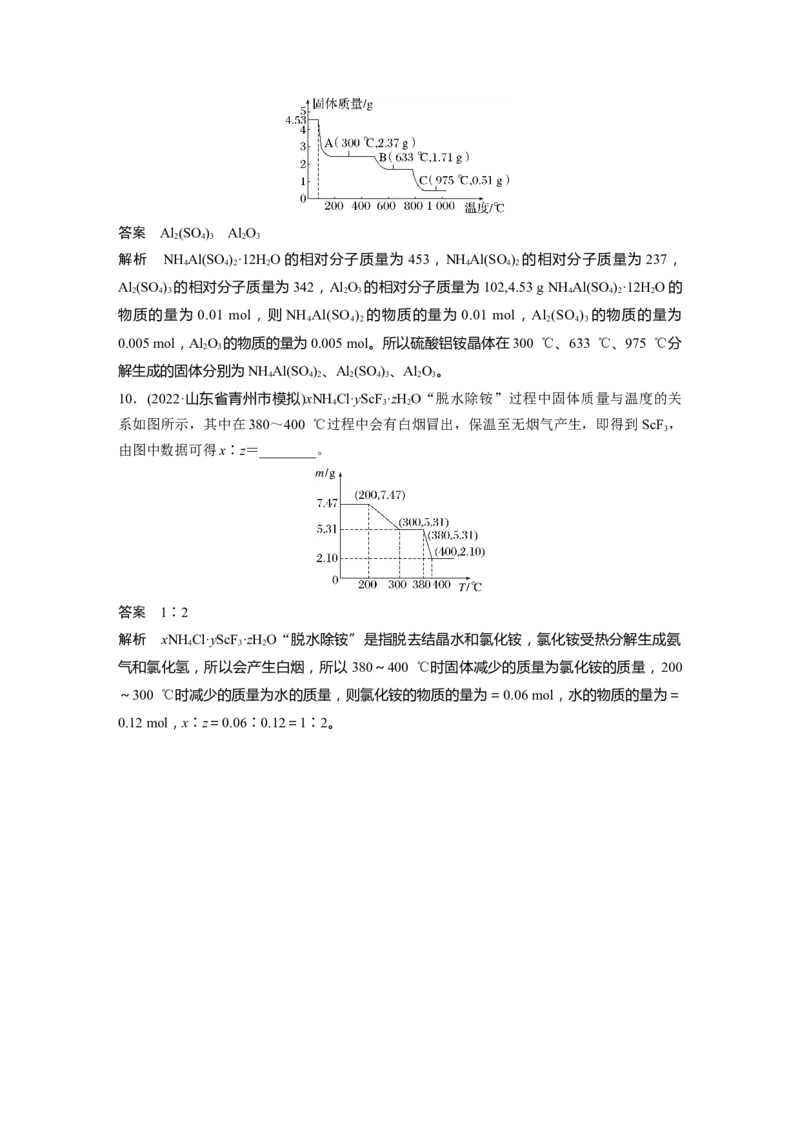
9.取4.53 g NHAl(SO )·12H O加热分解,加热过程中固体质量随温度的变化如图所示。硫
4 4 2 2
酸铝铵晶体在633 ℃、975 ℃分解生成的固体分别为________、________(填化学式)。答案 Al (SO ) Al O
2 4 3 2 3
解析 NH Al(SO )·12H O的相对分子质量为 453,NH Al(SO ) 的相对分子质量为 237,
4 4 2 2 4 4 2
Al (SO ) 的相对分子质量为342,Al O 的相对分子质量为102,4.53 g NH Al(SO )·12H O的
2 4 3 2 3 4 4 2 2
物质的量为 0.01 mol,则 NH Al(SO ) 的物质的量为 0.01 mol,Al (SO ) 的物质的量为
4 4 2 2 4 3
0.005 mol,Al O 的物质的量为0.005 mol。所以硫酸铝铵晶体在300 ℃、633 ℃、975 ℃分
2 3
解生成的固体分别为NH Al(SO )、Al (SO )、Al O。
4 4 2 2 4 3 2 3
10.(2022·山东省青州市模拟)xNH Cl·yScF·zHO“脱水除铵”过程中固体质量与温度的关
4 3 2
系如图所示,其中在380~400 ℃过程中会有白烟冒出,保温至无烟气产生,即得到ScF ,
3
由图中数据可得x∶z=________。
答案 1∶2
解析 xNH Cl·yScF·zHO“脱水除铵”是指脱去结晶水和氯化铵,氯化铵受热分解生成氨
4 3 2
气和氯化氢,所以会产生白烟,所以 380~400 ℃时固体减少的质量为氯化铵的质量,200
~300 ℃时减少的质量为水的质量,则氯化铵的物质的量为=0.06 mol,水的物质的量为=
0.12 mol,x∶z=0.06∶0.12=1∶2。