文档内容
专题 12 物质结构与性质
1.(2022·湖南高三模拟)重金属的化合物易对环境造成污染及引起人体伤害,元素砷本身无毒,其存在
于自然界各种金属矿中,它主要以各种砷化物的形式经呼吸道、消化道、皮肤进入体内引起人体中毒。回
答下列问题:
(1)基态砷原子核外电子排布中有___________个未成对电子;第一电离能数据I(As)大于I(Se),可能的原因
是___________。
(2)砷烷(AsH)的空间构型为___________;砷烷中心原子杂化方式为___________;AsH 的熔沸点高于
3 3
PH ,其主要原因是___________。NaAsO 可作杀虫剂,其组成元素的电负性大小顺序是___________。
3 3 4
(3)砷与铟(In)形成的化合物(X)具有优良的光电性能,广泛应用于光纤通信用激光器,其立方晶胞结构如图
所示,晶胞边长a=666.67pm,则其密度为___________g/cm3(边长a可用2000/3近似计算,设N =6.0×1023
A
mol-1)
(4)已知砷黄铁矿(FeAsS)煅烧可生成砒霜(As O)和红棕色固体,则该反应的化学方程式为___________。
2 3
2.(2022·山东日照市高三一模)工业上以纯碱、水、二氧化硫为原料,利用“干法”工艺制备食品抗氧
化剂焦亚硫酸钠(Na SO)。
2 2 5
回答下列问题:
(1)原料涉及的元素中,电负性最大的是____(填元素符号);纯碱中阴离子的中心原子杂化方式为____。
(2)二氧化硫易溶于水的原因除与水反应外,还有_____;与二氧化硫互为等电子体的阴离子有_______(填
化学式,写一种即可)。
(3)焦亚硫酸根的结构图为: ,标有“*”的硫的化合价为____。
(4)Na SO 加热至一定温度时分解为NaO和SO ,NaO晶胞为立方晶胞,结构如图,图中黑球代表阳离
2 2 5 2 2 2
子,白球代表阴离子(N 为阿伏加德罗常数的值)。
A
①阴离子的配位数为___。
②若晶胞参数为a nm,则晶胞的密度为___g·cm-3.(用含a、N 的式子表示)。
A3.(2022·广东广州市高三一模)HOGe(BH ) 是钙钛矿型化合物(ABX 型),量子化学计算结果显示,其
5 2 4 3 3
具有良好的光电化学性能。
回答下列问题:
(1)基态Ge的价层电子排布式为___________。
(2) 的结构如图所示。 含有共价键的类型是___________。1mol 含有化学键的个数为
___________。
(3)根据杂化轨道理论,BH 由B的4个___________(填杂化轨道类型)杂化轨道与4个H的1s轨道重叠而
成,因此BH 的空间构型是___________。
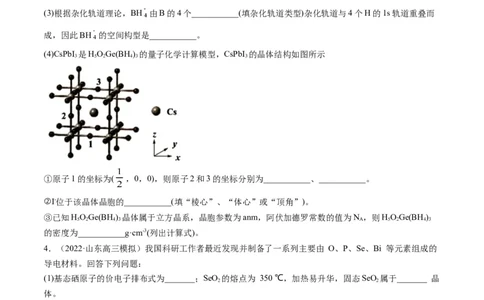
(4)CsPbI 是HOGe(BH ) 的量子化学计算模型,CsPbI 的晶体结构如图所示
3 5 2 4 3 3
①原子1的坐标为( ,0,0),则原子2和3的坐标分别为___________、___________。
②I-位于该晶体晶胞的___________(填“棱心”、“体心”或“顶角”)。
③已知HOGe(BH ) 晶体属于立方晶系,晶胞参数为anm,阿伏加德罗常数的值为N ,则HOGe(BH )
5 2 4 3 A 5 2 4 3
的密度为___________g·cm-3(列出计算式)。
4.(2022·山东高三模拟)我国科研工作者最近发现并制备了一系列主要由 O、P、Se、Bi 等元素组成的
导电材料。回答下列问题:
(1)基态硒原子的价电子排布式为_______;SeO 的熔点为 350 ℃,加热易升华,固态SeO 属于_______ 晶
2 2
体。
(2)O、P、S三种元素中,电负性最大的是_______;键角:HO_______H Se(填">"、"<"或"=")。
2 2
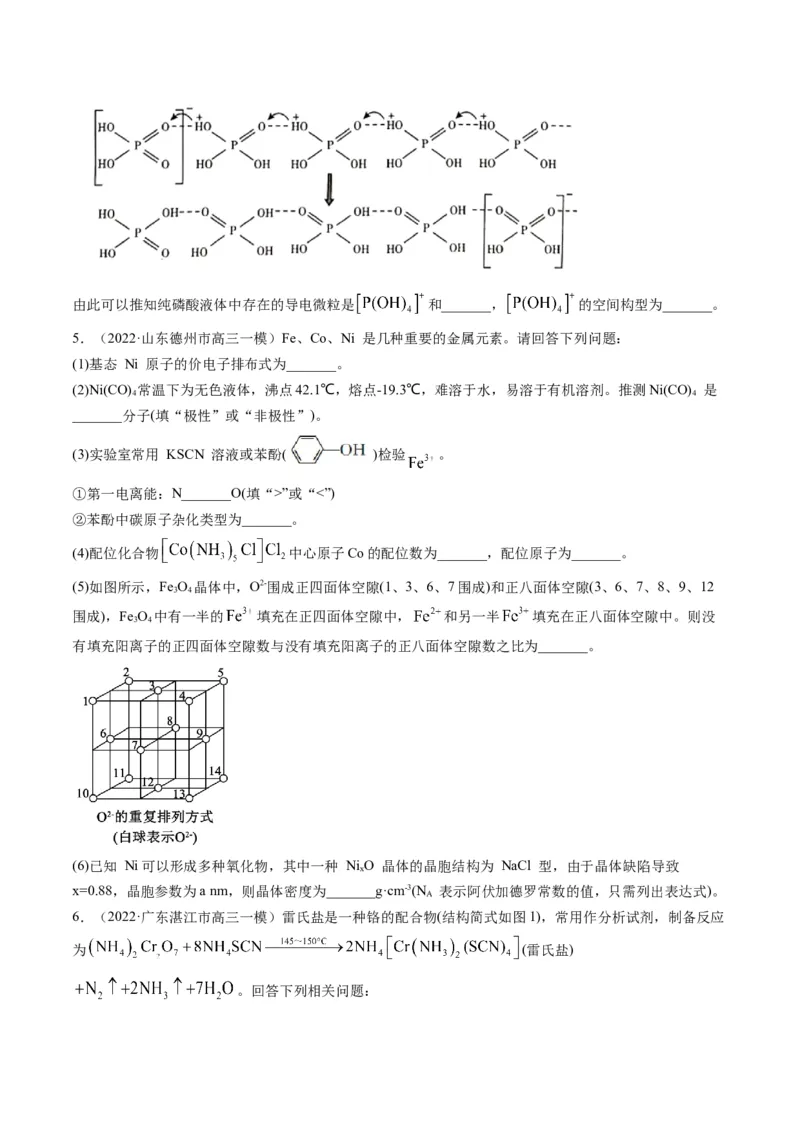
(3)纯净的磷酸粘度极大,随温度升高粘度迅速下降,原因是_______;熔融状态的磷酸导电性很好,这是
由于在纯磷酸中存在如下质子交换导电机理。由此可以推知纯磷酸液体中存在的导电微粒是 和_______, 的空间构型为_______。
5.(2022·山东德州市高三一模)Fe、Co、Ni 是几种重要的金属元素。请回答下列问题:
(1)基态 Ni 原子的价电子排布式为_______。
(2)Ni(CO) 常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO) 是
4 4
_______分子(填“极性”或“非极性”)。
(3)实验室常用 KSCN 溶液或苯酚( )检验 。
①第一电离能:N_______O(填“>”或“<”)
②苯酚中碳原子杂化类型为_______。
(4)配位化合物 中心原子Co的配位数为_______,配位原子为_______。
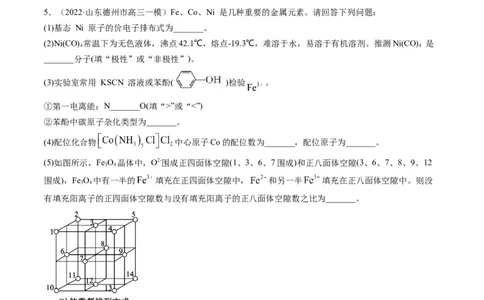
(5)如图所示,Fe O 晶体中,O2-围成正四面体空隙(1、3、6、7围成)和正八面体空隙(3、6、7、8、9、12
3 4
围成),Fe O 中有一半的 填充在正四面体空隙中, 和另一半 填充在正八面体空隙中。则没
3 4
有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为_______。
(6)已知 Ni可以形成多种氧化物,其中一种 Ni O 晶体的晶胞结构为 NaCl 型,由于晶体缺陷导致
x
x=0.88,晶胞参数为a nm,则晶体密度为_______g·cm-3(N 表示阿伏加德罗常数的值,只需列出表达式)。
A
6.(2022·广东湛江市高三一模)雷氏盐是一种铬的配合物(结构简式如图1),常用作分析试剂,制备反应
为 (雷氏盐)
。回答下列相关问题:(1) 的核外电子排布式为______;其基态原子核外电子的空间运动状态有______种;氟和氯处于同一
主族, 的熔点为1100℃, 的熔点为83℃,前者比后者高得多,是因为______。
(2)雷氏盐中与铬形成配位键的原子是______;中心原子的配位数为______。
(3) 中氮原子的杂化方式为______,其立体构型的名称为______。
(4) 所含元素中电负性最小的是______(填元素符号,下同),它们的基态原子的第一电离能最大
的是______。
(5)金属铬的晶胞结构如图2所示,设晶胞边长为 ,则铬的原子半径为______ 。
1.(2022·河北衡水高三一模)钙及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)基态钙原子的核外电子排布式为_______,能量最高的电子的电子云轮廓图形状是_______。
(2)含氟牙膏中氟离子将羟基磷酸钙[Ca (PO )OH]转化为耐腐蚀的氟磷酸钙[Ca (PO )F]。与 互为等电
5 4 3 5 4 3
子体的分子为_______(填一种)。
(3)元素T与钙位于同周期,在前四周期中基态T原子的未成对电子数最多。T的一种离子与H
2
NCH CHNH (后面简写为en)、OH-、HO组成配合物[T(OH) ( H O)(cn)]。
2 2 2 2 3 2
①该配合物配位中心离子是_______(填离子符号) ,其配位数为_______。
②该配合物中所含元素C、N、O分别可以和氢原子构成CH、NH 、HO三种分子的键角依次减小,其主
4 3 2
要原因是_______。
(4)CaF、CaCl 晶体的熔点依次为1402℃、782℃,二者熔点相差较大的主要原因是_______。
2 2
(5)CaSe(硒化钙)晶胞结构如图所示:
①该晶胞中,面心上6个Se2-相连构成的几何体是_______( 填字母)。
A.正四面体 B.立方体 C.正八面体 D.三角锥形
②已知硒化钙晶体的密度为dg∙cm-3,N 表示阿伏加德罗常数的值,则该晶胞中距离最近的Ca2+之间的距离
A为_______pm(用含d和N 的代数式表示)。
A
2.(2022·福建漳州市高三一模)铁元素是最重要的金属元素之一,很多含铁化合物具有重要作用。
(1)通常情况下,铁的+2价化合物没有+3价的稳定,请你从核外电子排布的角度解释其原因_______。
(2)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H O) ]2+。
2 5
①与N同周期的主族元素中,第一电离能比N大的元素是_______。
② [Fe(SCN)(H O) ]2+中Fe3+的配位数为_______。
2 5
③与SCN−互为等电子体的非极性分子的化学式为_______(任写一种)。
(3)血红素结构如图所示,在图中画出Fe2+与N原子间的化学键_______ (若是配位键,需要用箭头加以表
示),血红素中C原子的杂化方式是_______。
(4)FeCO 可作补血剂,CoCO 可用于陶瓷工业的着色剂。已知:①r(Fe2+)为61 pm,r(Co2+)为65 pm。②隔
3 3
绝空气加热:FeCO FeO+CO↑;CoCO CoO+CO↑。分别加热FeCO 和CoCO 时,FeCO 的分
3 2 3 2 3 3 3
解温度低于CoCO,其原因是_______。
3
(5)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。正六棱柱底边边长为x cm,高为y cm,N 为阿
A
伏加德罗常数的值,则晶胞的密度为_______g∙cm-3(列出计算式即可)。
3.(2021·湖南高三零模)VA族元素及其化合物在生产、生活中用途广泛。
(1)① 常用于制造火柴,P和S的第一电离能较大的是______。
② 俗称雄黄,其中基态 原子的核外电子排布式为 ______,有______个未成对电子。
③P、S、 电负性由大到小的顺序是______。
(2) 、 、 中沸点最高的是______,其主要原因是______。
(3)①白磷在氯气中燃烧可以得到 和 ,其中气态 分子的立体构型为______。②研究发现固态PCl 和PBr 均为离子晶体,但其结构分别为 和 ,分析PCl 和
5 5 5
PBr 结构存在差异的原因是______。
5
(4)锑酸亚铁晶胞如图所示,其晶胞参数分别为anm、bnm、cnm, ,则:
①锑酸亚铁的化学式为______。
②晶体的密度为______ (设 为阿伏加德罗常数的值)。
4.(2021·福建高三零模)ZnGeP 和KTiOPO 都是非线性光学晶体材料,在激光技术方面有广泛用途。
2 4
回答下列问题:
(1)基态Ge原子的价电子排布式为_______。
(2)O、 P、 K、 Zn按电负性由大到小的顺序排列为_______。
(3)H O、PH 、KH按熔点由高到低的顺序排列为_______,熔点差异的原因_______。
2 3
(4)以Zn为顶点的ZnGeP 晶胞结构如图所示。
2
①Zn的配位数为_______ 。
②以Ge为顶点的晶胞中,Zn原子位于_______。
5.(2021·湖南永州市高三二模)钛(Ti)被称为“未来金属”,广泛应用于国防、航空航天、生物材料等领
域。钛的氯化物有如下转变关系:2TiCl TiCl ↑+TiCl ,回答下列问题:
3 4 2
(1)基态钛原子的价电子排布式为___________。与钛同周期的第ⅡB族和ⅢA族两种元素中第一电离能较
大的是___________(写元素符号),原因是___________。
(2)钛的氯化物的部分物理性质如下表:氯化物 熔点/℃ 沸点/℃ 溶解性
TiCl -24 136 可溶于非极性的甲苯和氯代烃
4
TiCl 1035 1500 不溶于氯仿、乙醚
2
①TiCl 与TiCl 的晶体类型分别是___________、___________。
4 2
②TiCl 与 互为等电子体,因为它们___________相同; 中心原子的杂化方式是___________。
4
(3)Ti的配合物有多种。 的配体所含原子中电负性最小的是___________;
的球棍结构如图Ⅰ,Ti的配位数是___________。
(4)钙钛矿(CaTiO )是自然界中的一种常见矿物,其晶胞结构如图Ⅱ。
3
①设N 为阿伏加德罗常数的值,计算一个晶胞的质量为___________g。
A
②假设O2-采用面心立方最密堆积,Ti4+与O2-相切,则 ___________。
6.(2021·四川高三二模)2020年底,我国嫦娥五号月球探测器成功发射,进行无人采样后已顺利回收。
(1)月球表面的月海玄武岩中富含钛和铁,基态钛原子的核外电子排布式是____,基态铁原子核外电子占据
的最高能级是____。
(2)将月海玄武岩用硝酸溶解,所得溶液用KSCN检验,溶液呈红色。KSCN中K、C、N的电负性从大到
小的顺序是______,C 原子的杂化轨道类型是____,SCN-的空间构型是______,SCN- 中含有的 键数目
是______。
(3)嫦娥五号采样机中的钻杆是由中国科学院科学家研制的碳化硅增强铝基复合材料制成,具有轻质、高刚
度、高强度和耐磨损等特点。
①铝基复合材料中有一种重要的物质氮化铝(AlN, 熔点为2249°C),氮化铝属类金刚石氮化物,则它属于
______(填晶体类型名称)。氮化铝可用氧化铝(增点为2054°C)为原料来制取,从晶体类型角度分析AlN的
熔点比氧化铝高的原因是______。
②氮化铝的晶体结构如图所示,其中铝原子的配位数是___________,Al与N原子最近的距离为acm,则
该品体的密度为_____g/cm3 (写出表达式即可)。8.(2022·山东省潍坊市高三学科核心素养测评)铜和钴掺杂的含氮碳层材料是一种新型催化材料,具有氧
还原催化性能。回答下列问题:
(1)下列状态的N原子或离子的核外电子在跃迁时,用光谱仪可捕捉到发射光谱的是_____(填序号)。
A.1s22s22p3 B.1s22s2 C.1s22s12p4 D.1s22s22p6
(2)已知氮的两种化合物NH 和NH OH都能结合H+而具有弱碱性,二者的碱性强弱:NH_____NH OH(填
2 4 2 2 4 2
“强于”或“弱于”),理由是___。
(3)叠氮酸根NN -的空间结构是______,NONO -中含有的价层电子对数目为______。
3 2
(4)Co的第四电离能比铁的第四电离能______(填“大”或“小”),理由是____。
(5)高导电紫铜常用硼化钙提高导电率,其晶胞如图所示,具有立方晶系的对称性,B原子全部组成正八面
体,各个顶点通过B—B键连接成三维骨架,则该硼化钙的化学式是___________,B原子半径为r nm,阿
伏加德罗常数的值为N ,则硼化钙的密度 为___________g·cm-3。
A
9.(2022·山东省潍坊市高三联考)在工业上用磷化铜(Cu P)制造磷青铜,磷青铜是含少量钪、锡、磷的铜
3 2
合金,主要用作耐磨零件和弹性合金原件。
(1)基态Sc原子的价电子排布式为_______;同周期中未成对电子数与Sc相同的元素有_______种。
(2)磷青铜中的锡、磷两种元素电负性的大小为Sn_______P(填“>”“<”或“=”)。
(3)NH 易与Cu2+形成[Cu(NH )]2+配离子,在该配离子中H-N-H键角比NH 分子中H-N-H键角大的原因是
3 3 4 3
_______。[Cu(NH )]2+中2个NH 被2个HO取代,得到两种结构的配离子,则[Cu(NH )]2+的空间构型是
3 4 3 2 3 4
_______(填“正四面体”或“正四边形”)。
(4)某立方磷青铜晶体的晶胞结构如图所示。①原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0),B为(1,1,
0),C为(0,1,1),则D原子的分数坐标为_______。
②若晶体密度为ρg/cm3,最近的Cu原子核间距为_______pm(用含ρ、N 的代数式表示)。
A
10.(2022·四川省达州市第一次诊断考试)金属钛(Ti)及化合物在化工、医药、材料等领城具有广泛应用。
回答下列问题:
(1)Li Ti O 是电池的电极材料。与Li不同族但性质相似的元素是___________,其电子占据最高能级的电
4 5 12
子云轮廓图是___________
(2)K与Ti位于同一周期,K和Ti的第一电离能(I)较大的是___________,它们的第二电离能(I)分别为
1 2
3051kJ/mol、1310kJ/mol,其原因是___________。
(3)钛与卤素形成的化合物TiX 熔点如下表
4
TiX TiF TiCl TiBr TiI
4 4 4 4 4
熔点℃ 377 -24 38.3 153
它们熔点差异的原因___________
(4)Ti(IV)的某配合物可用于催化环烯烃聚合,其结构如图所示,该配合物中:Ti的配位数为___________,
与Ti形成配位键的元素是___________,碳碳键类型是___________;所含非金属元素的含氧酸根离子中心
原子杂化轨道类型是sp2的是___________、立体构型是V形的是___________
(5)已知N与Ti形成的化合物的晶胞结构如图所示,晶胞中Ti原子与N原子的最近距离为apm;晶胞的密
度为p=___________g/cm3(阿伏加德罗常数值为N ,N、Ti的相对原子质量分别用Ar(N)和Ar(Ti)表示)
A
11.(2022·重庆市高三第四次质量检测)钛是一种稀有金属,具有密度小、强度高、耐腐蚀等特点,钛和钛
的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。已知:阿伏加德罗常数的值为N 。
A
(1)基态钛原子价电子排布式为___________;与钛同周期的元素中,基态原子的未成对电子数与钛相同的
还有___________种。
(2)钛的一种常见化合物是[Ti(HO) ]Cl 。 该物质中含有σ键的数目为___________,配体HO的
2 6 3 2
VSEPR模型名称是___________,其沸点高于HS,原因是___________。
2(3)常温下,TiCl 是易溶于CCl 、易挥发的无色液体。TiCl 挥发过程中破坏的作用力类型是___________。
4 4 4
(4)Ti(NO ) 的结构如图所示,Ti(IV)的配位数为___________。分子或离子中的大π键可用符号 表示,其
3 4
中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为π 6),
6
则配体NO -中含有的大π键应表示为___________。
3
(5)氮化钛(TiN)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有 NaCl型结构,则
该晶体中阳离子的配位数为___________;已知该晶体的晶胞参数为423.5 pm,其晶体密度的计算表达式
为___________ g· cm-3。
12.(2022·湖南省五市十校教育教改共同体高三第二次大联考)主族元素N、P、 、 、 等的某些化
合物对工农业生产意义重大,回答下列问题:
(1)N、P、 电负性由大到小的顺序为___________, 的第一电离能比 的第一电离能大的原因为
___________。
(2)阿散酸(如图)是一种饲料添加剂,能溶于 溶液中,常含有HAsO 、 等杂质,该结构中 的
3 3
杂化方式为___________,AsO 3-的空间构型为___________。
3
(3)液氨可作制冷剂,汽化时吸收大量的热的原因是___________。
(4)CrCl 能与HO、NH 形成配位数为6的配合物,且相应两种配体的物质的量之比为2:1, 该配合
3 2 3
物溶于水,加入足量的硝酸银溶液可得 白色沉淀,则该配合物的化学式为___________。
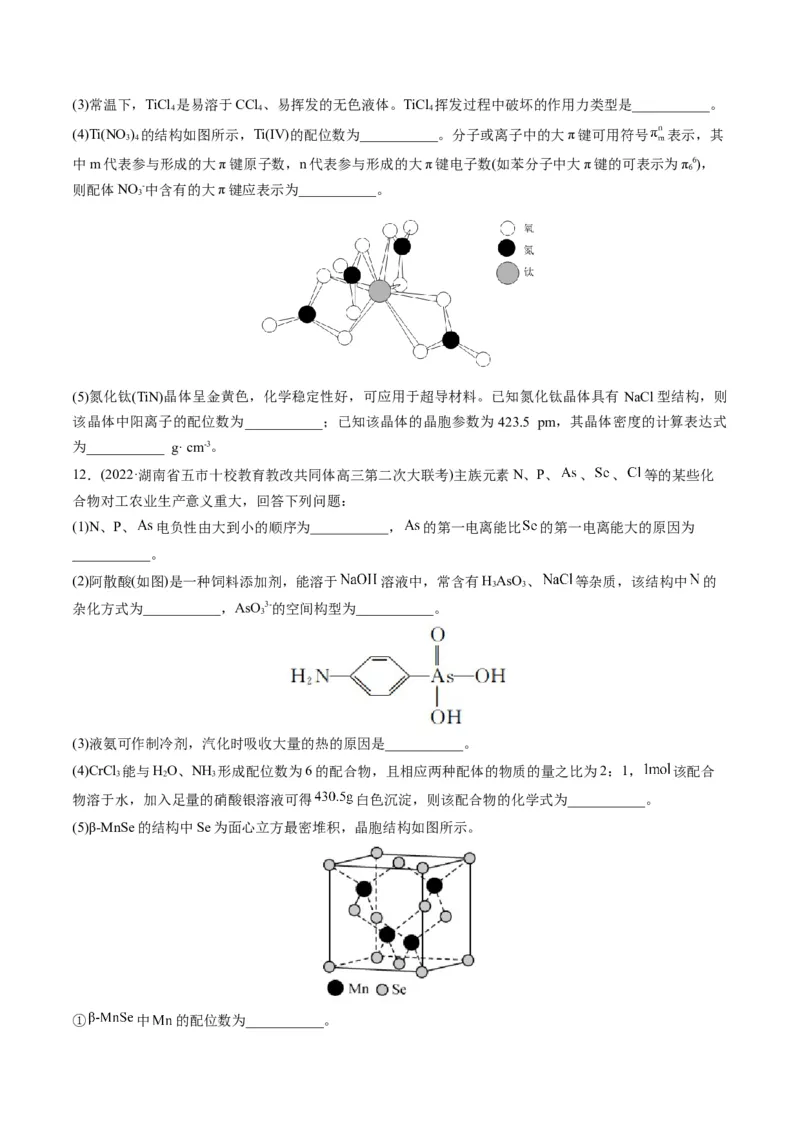
(5)β-MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。
① 中 的配位数为___________。②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为N ,则β-MnSe的密度 ___________(列出表达式)
A
g· cm-3。
13.(2022·辽宁省大连市八中高三期中)锌及锌的化合物应用广泛。例如,测定铜合金中的铅、锌时要利用
锌配离子的下列反应:
[Zn(CN) ]2++4HCHO+4H O= Zn2++4HOCH CN+4OH-
4 2 2
回答下列问题:
(1)基态Zn的价电子排布式为_____,基态C原子核外电子占据_______个空间运动状态不同的原子轨道。
(2)C、N、O三种元素的第一电离能由大到小的顺序为______,HOCH CN分子中含有的σ键与π键数目之
2
比为________。
(3)HCHO分子中碳原子轨道的杂化类型是_______,福尔马林是HCHO的水溶液,HCHO极易与水互溶的
主要原因是______。
(4)[Zn(CN) ]2+中Zn2+与CN-之间的化学键称为_____,提供孤电子对的成键原子是______。
4
(5)Zn与S形成某种化合物的晶胞如图所示:
① 填入 组成的_______空隙中;
A.四面体 B.六面体 C.八面体 D.十二面体
②已知晶体密度为 ,该晶胞的边长表达式为____pm(写计算表达式)。