文档内容
专题八 原电池 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
一、选择题(本题含16小题,每题3分,共48分。每题只有一个选项符合题意)
1.(2022秋·内蒙古鄂尔多斯·高三准格尔旗世纪中学校考期中)宏观辨识与微观探析
是化学学科核心素养之一。下列变化对应的离子方程式正确的是
A.向含氯化铁的氯化镁溶液中加入氧化镁:2Fe3++3MgO+3HO═2Fe(OH) ↓+3Mg2+
2 3
B.向碘化亚铁溶液中滴加少量稀硝酸:2NO +3Fe2++4H+═3Fe3++2NO↑+2HO
2
C.“84消毒液”中加少量醋增强漂白性:ClO﹣+H+═HClO
D.铅蓄电池放电时正极上的反应:PbO +2e﹣+4H+═Pb2++2H O
2 2
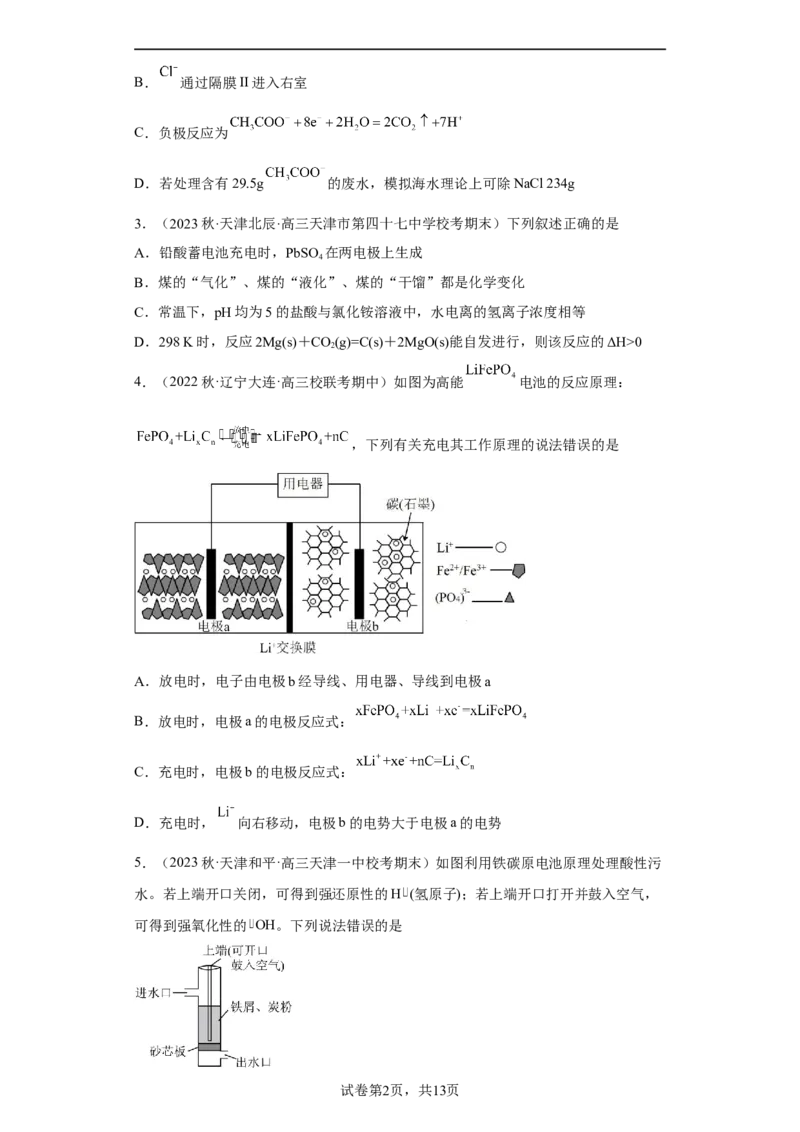
2.(2023秋·新疆乌鲁木齐·高二乌市八中校考期末)有一种新型电池既可以实现海水
淡化,又可以进行废水处理,还能获得电能。下列装置处理含 的废水。下列
说法正确的是
A.a极为负极,发生还原反应B. 通过隔膜II进入右室
C.负极反应为
D.若处理含有29.5g 的废水,模拟海水理论上可除NaCl 234g
3.(2023秋·天津北辰·高三天津市第四十七中学校考期末)下列叙述正确的是
A.铅酸蓄电池充电时,PbSO 在两电极上生成
4
B.煤的“气化”、煤的“液化”、煤的“干馏”都是化学变化
C.常温下,pH均为5的盐酸与氯化铵溶液中,水电离的氢离子浓度相等
D.298 K时,反应2Mg(s)+CO(g)=C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
2
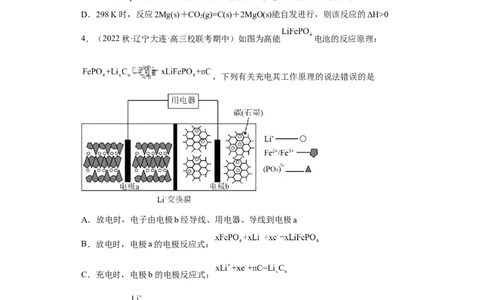
4.(2022秋·辽宁大连·高三校联考期中)如图为高能 电池的反应原理:
,下列有关充电其工作原理的说法错误的是
A.放电时,电子由电极b经导线、用电器、导线到电极a
B.放电时,电极a的电极反应式:
C.充电时,电极b的电极反应式:
D.充电时, 向右移动,电极b的电势大于电极a的电势
5.(2023秋·天津和平·高三天津一中校考期末)如图利用铁碳原电池原理处理酸性污
水。若上端开口关闭,可得到强还原性的H (氢原子);若上端开口打开并鼓入空气,
可得到强氧化性的 OH。下列说法错误的是
试卷第2页,共13页A.无论是否鼓入空气,负极:
B.上端开口关闭,正极:
C.鼓入空气,每生成 有 电子转移
D.处理含 的污水时,打开上端开口并鼓入空气
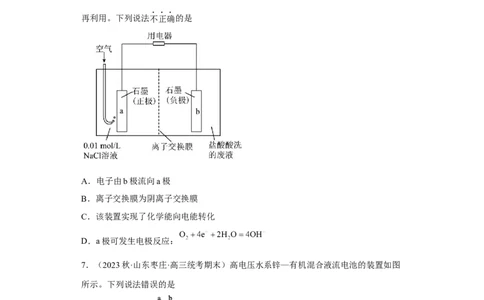
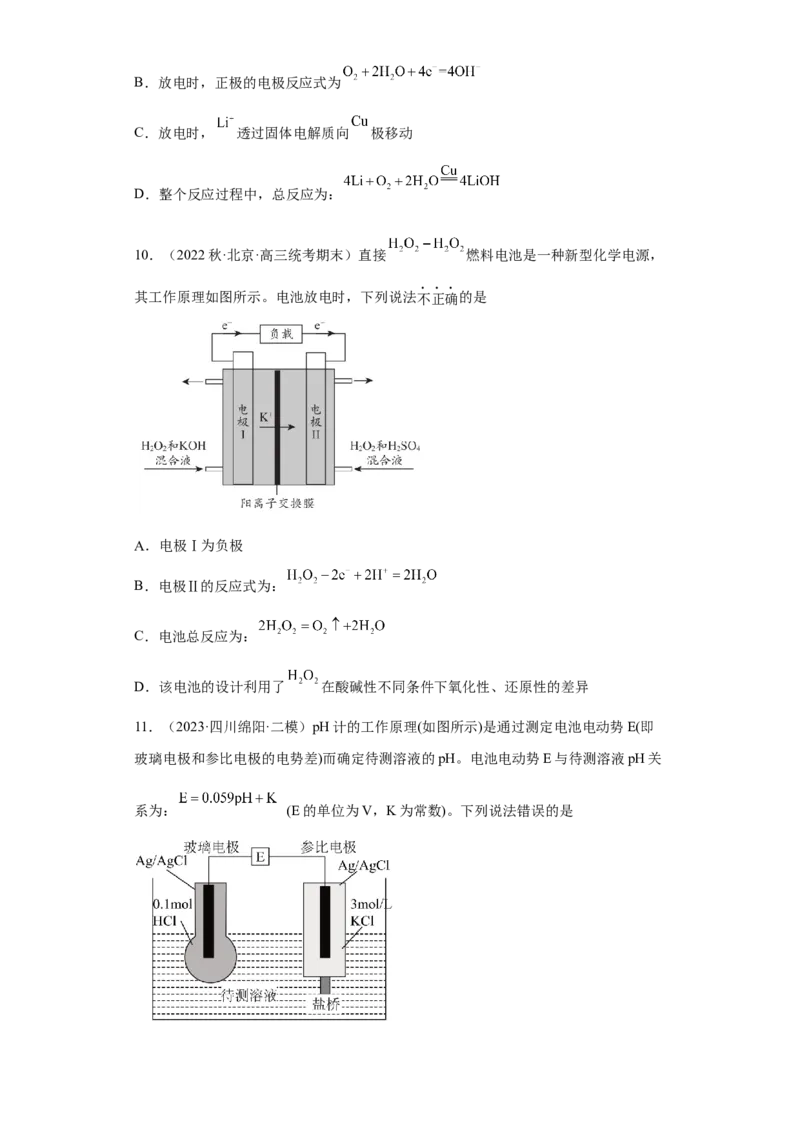
6.(2023秋·北京西城·高三统考期末)盐酸酸洗钢材的废液中含有大量的盐酸、
。研究人员利用如图装置可将部分铁元素在极区转化为沉淀,实现资源和能源的
再利用。下列说法不正确的是
A.电子由b极流向a极
B.离子交换膜为阴离子交换膜
C.该装置实现了化学能向电能转化
D.a极可发生电极反应:
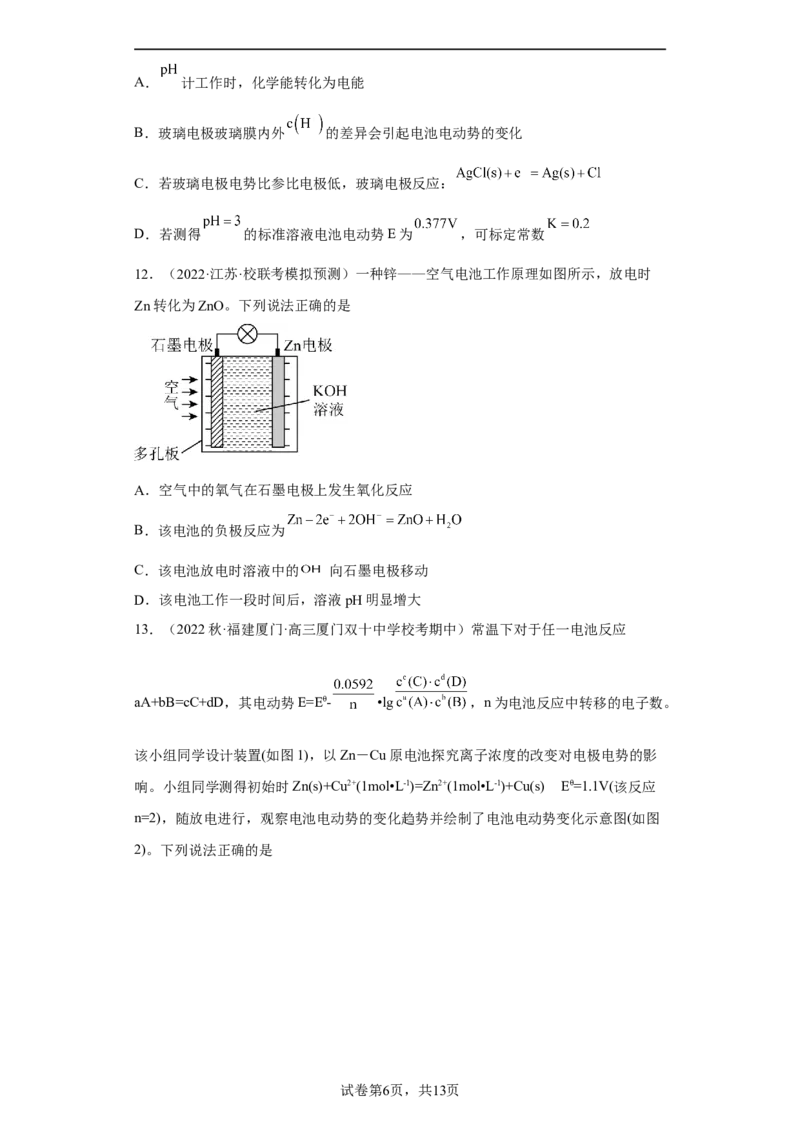
7.(2023秋·山东枣庄·高三统考期末)高电压水系锌—有机混合液流电池的装置如图
所示。下列说法错误的是
A.放电时,正极区溶液的pH增大
B.放电时,负极反应式:
C.充电时,电极a连接电源负极D.充电时,负极材料每增重13g,中性电解质溶液减少11.7g
8.(2023秋·天津北辰·高三天津市第四十七中学校考期末)一种可充电锂—空气电池
如图所示。当电池放电时,O 与Li+在多孔碳材料电极处生成LiO (x=0或1)。下列说
2 2 2-x
法不正确的是
A.放电时,多孔碳材料电极为正极
B.放电时,外电路电流由多孔碳材料电极流向锂电极
C.充电时,多孔碳材料电极反应为LiO - 2e- = 2Li++(1- )O ↑
2 2-x 2
D.充电时,电解质溶液中Li+向多孔碳材料区迁移
9.(2022秋·江苏·高三校联考期中)周期表中第二周期元素及其化合物广泛应用于材
料领域。锂常用作电池的电极材料; 可用作超导体材料;冠醚是一种环状碳的化合
物,可用于识别 与 ; 用于蚀刻微电子材料中 、 等,还常用于与
联合刻蚀玻璃材料, 可由电解熔融氟化氢铵( )制得,也可由 与 反应
生成,锂—铜空气燃料电池容量高、成本低。该电池通过一种复杂的铜腐蚀“现象”
产生电能,放电时发生反应: ,下列说法不正确的是
A.通空气时,铜被腐蚀,表面产生
试卷第4页,共13页B.放电时,正极的电极反应式为
C.放电时, 透过固体电解质向 极移动
D.整个反应过程中,总反应为:
10.(2022秋·北京·高三统考期末)直接 燃料电池是一种新型化学电源,
其工作原理如图所示。电池放电时,下列说法不正确的是
A.电极Ⅰ为负极
B.电极Ⅱ的反应式为:
C.电池总反应为:
D.该电池的设计利用了 在酸碱性不同条件下氧化性、还原性的差异
11.(2023·四川绵阳·二模)pH计的工作原理(如图所示)是通过测定电池电动势E(即
玻璃电极和参比电极的电势差)而确定待测溶液的pH。电池电动势E与待测溶液pH关
系为: (E的单位为V,K为常数)。下列说法错误的是A. 计工作时,化学能转化为电能
B.玻璃电极玻璃膜内外 的差异会引起电池电动势的变化
C.若玻璃电极电势比参比电极低,玻璃电极反应:
D.若测得 的标准溶液电池电动势E为 ,可标定常数
12.(2022·江苏·校联考模拟预测)一种锌——空气电池工作原理如图所示,放电时
Zn转化为ZnO。下列说法正确的是
A.空气中的氧气在石墨电极上发生氧化反应
B.该电池的负极反应为
C.该电池放电时溶液中的 向石墨电极移动
D.该电池工作一段时间后,溶液pH明显增大
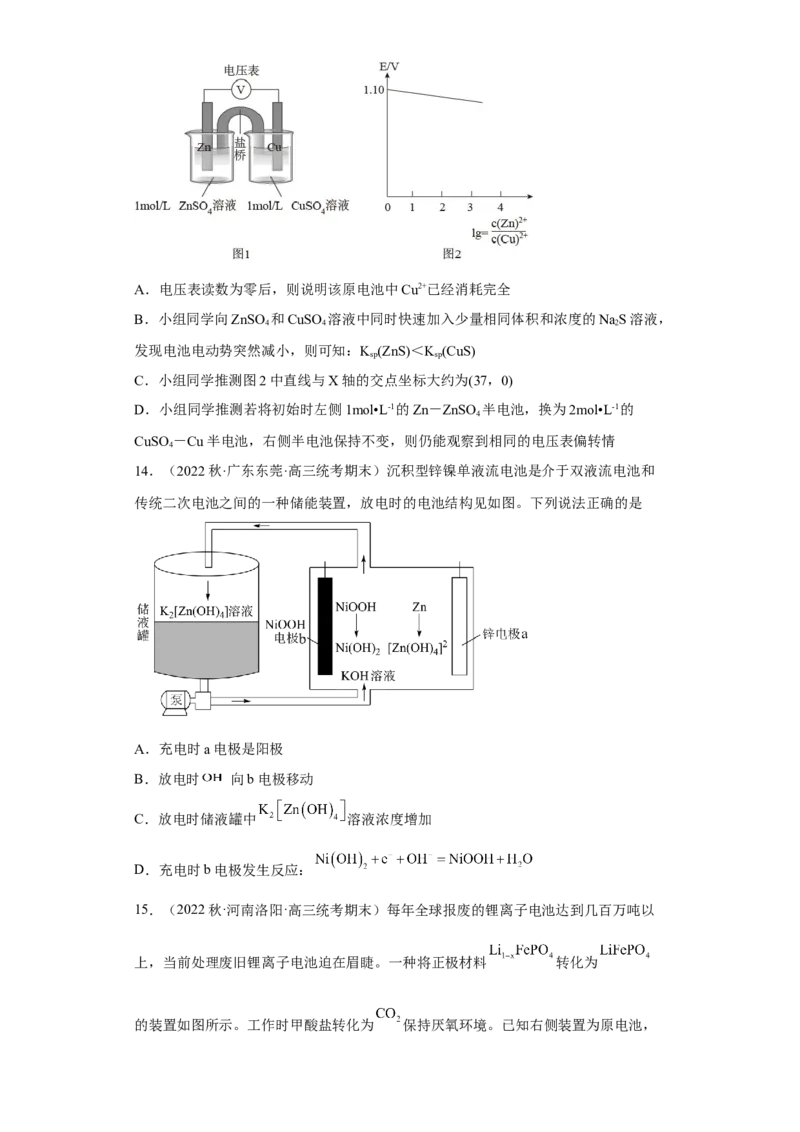
13.(2022秋·福建厦门·高三厦门双十中学校考期中)常温下对于任一电池反应
aA+bB=cC+dD,其电动势E=Eθ- •lg ,n为电池反应中转移的电子数。
该小组同学设计装置(如图1),以Zn-Cu原电池探究离子浓度的改变对电极电势的影
响。小组同学测得初始时Zn(s)+Cu2+(1mol•L-1)=Zn2+(1mol•L-1)+Cu(s) Eθ=1.1V(该反应
n=2),随放电进行,观察电池电动势的变化趋势并绘制了电池电动势变化示意图(如图
2)。下列说法正确的是
试卷第6页,共13页A.电压表读数为零后,则说明该原电池中Cu2+已经消耗完全
B.小组同学向ZnSO 和CuSO 溶液中同时快速加入少量相同体积和浓度的NaS溶液,
4 4 2
发现电池电动势突然减小,则可知:K (ZnS)<K (CuS)
sp sp
C.小组同学推测图2中直线与X轴的交点坐标大约为(37,0)
D.小组同学推测若将初始时左侧1mol•L-1的Zn-ZnSO 半电池,换为2mol•L-1的
4
CuSO -Cu半电池,右侧半电池保持不变,则仍能观察到相同的电压表偏转情
4
14.(2022秋·广东东莞·高三统考期末)沉积型锌镍单液流电池是介于双液流电池和
传统二次电池之间的一种储能装置,放电时的电池结构见如图。下列说法正确的是
A.充电时a电极是阳极
B.放电时 向b电极移动
C.放电时储液罐中 溶液浓度增加
D.充电时b电极发生反应:
15.(2022秋·河南洛阳·高三统考期末)每年全球报废的锂离子电池达到几百万吨以
上,当前处理废旧锂离子电池迫在眉睫。一种将正极材料 转化为
的装置如图所示。工作时甲酸盐转化为 保持厌氧环境。已知右侧装置为原电池,电极 、 、 均不参与反应。下列说法正确的是
A. 在b电极上被氧化
B. 电极反应式为
C.装置工作时,A室溶液 逐渐增大
D. 电极反应式为
16.(2023秋·北京西城·高三统考期末)某小组同学探究Al与 的反应,实验如下。
序
装置 试剂a 现象
号
2mL0.5mol
① 无明显变化,数小时后观察到铝片上仅有少量红色斑点
/L
溶液
2mL0.5mol 迅速产生红色固体和无色气泡,且气体的生成速率逐渐增
② /L 溶 大,反应放出大量的热。在铝片表面产生少量白色沉淀,
液
经检验为CuCl
下列说法不正确的是A.②中气体生成速率逐渐增大可能与Al和Cu在溶液中形成了
原电池有关
B.②中产生白色沉淀的可能原因:
C.向①中加入一定量NaCl固体,推测出现与②相似的实验现象
D.②比①反应迅速是由于 水解使②中的 更大,利于破坏铝片表面的氧化
膜
二、非选择题 (本题共5小题,1-3题每题10分,4-5题每题11分,共52分)
17.(2022秋·山东泰安·高三校考期中)捕集CO 的技术对解决全球温室效应意义重
2
试卷第8页,共13页大。回答下列问题。
(1)国际空间站处理CO 的一个重要方法是将CO 还原,所涉及的反应方程式为:
2 2
CO(g)+4H(g) CH(g)+2HO(g); H=-270kJ⋅mol-1,几种化学键的键能如表所示:
2 2 4 2
化学键 C-H H-H H-O C=O
键能/kJ⋅mol-1 413 436 a 745
则a=_______。
(2)将CO 还原为CH,是实现CO 资源化利用的有效途径之一,装置如图所示:
2 4 2
①H+的移动方向为_______(填“自左至右”或“自右至左”);d电极的电极反应式为
_______。
②若电源为(CH)NNH-O -KOH清洁燃料电池,当消耗0.1mol燃料(CH)NNH 时,离
3 2 2 2 3 2 2
子交换膜中通过_______molH+,该清洁燃料电池中的正极反应式为_______。
18.(2022秋·黑龙江哈尔滨·高三哈尔滨三中校考期中)海洋的水资源和其他化学资
源具有十分巨大的开发潜力。
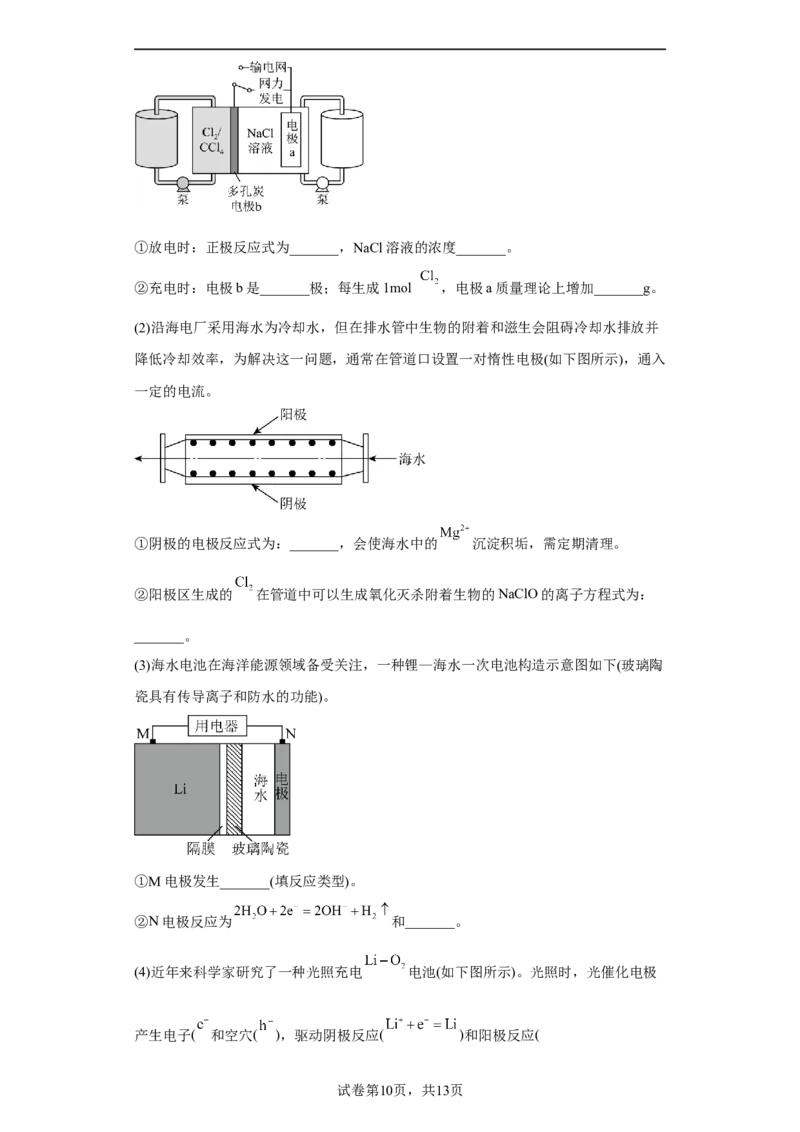
(1)“氯碱工业”电解饱和食盐水的化学方程式为:_______。制取的氯气是实验室和工
业上的常用气体,科学家基于 易溶于 的性质,发展了一种无需离子交换膜的
新型氯流电池,可作储能设备(如下图)。充电时,电极a的反应为:
。①放电时:正极反应式为_______,NaCl溶液的浓度_______。
②充电时:电极b是_______极;每生成1mol ,电极a质量理论上增加_______g。
(2)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并
降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如下图所示),通入
一定的电流。
①阴极的电极反应式为:_______,会使海水中的 沉淀积垢,需定期清理。
②阳极区生成的 在管道中可以生成氧化灭杀附着生物的NaClO的离子方程式为:
_______。
(3)海水电池在海洋能源领域备受关注,一种锂—海水一次电池构造示意图如下(玻璃陶
瓷具有传导离子和防水的功能)。
①M电极发生_______(填反应类型)。
②N电极反应为 和_______。
(4)近年来科学家研究了一种光照充电 电池(如下图所示)。光照时,光催化电极
产生电子( 和空穴( ),驱动阴极反应( )和阳极反应(
试卷第10页,共13页)对电池进行充电。
放电时, 从_______电极穿过离子交换膜向_______电极迁移,总反应为:_______。
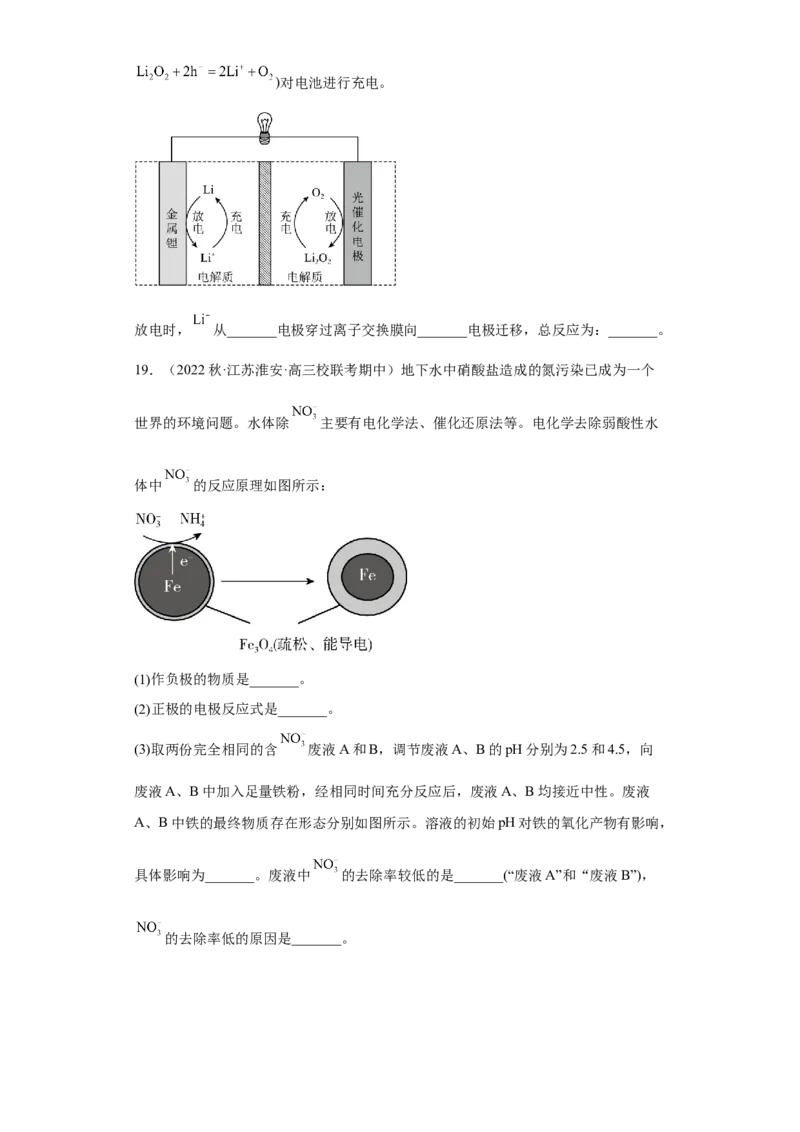
19.(2022秋·江苏淮安·高三校联考期中)地下水中硝酸盐造成的氮污染已成为一个
世界的环境问题。水体除 主要有电化学法、催化还原法等。电化学去除弱酸性水
体中 的反应原理如图所示:
(1)作负极的物质是_______。
(2)正极的电极反应式是_______。
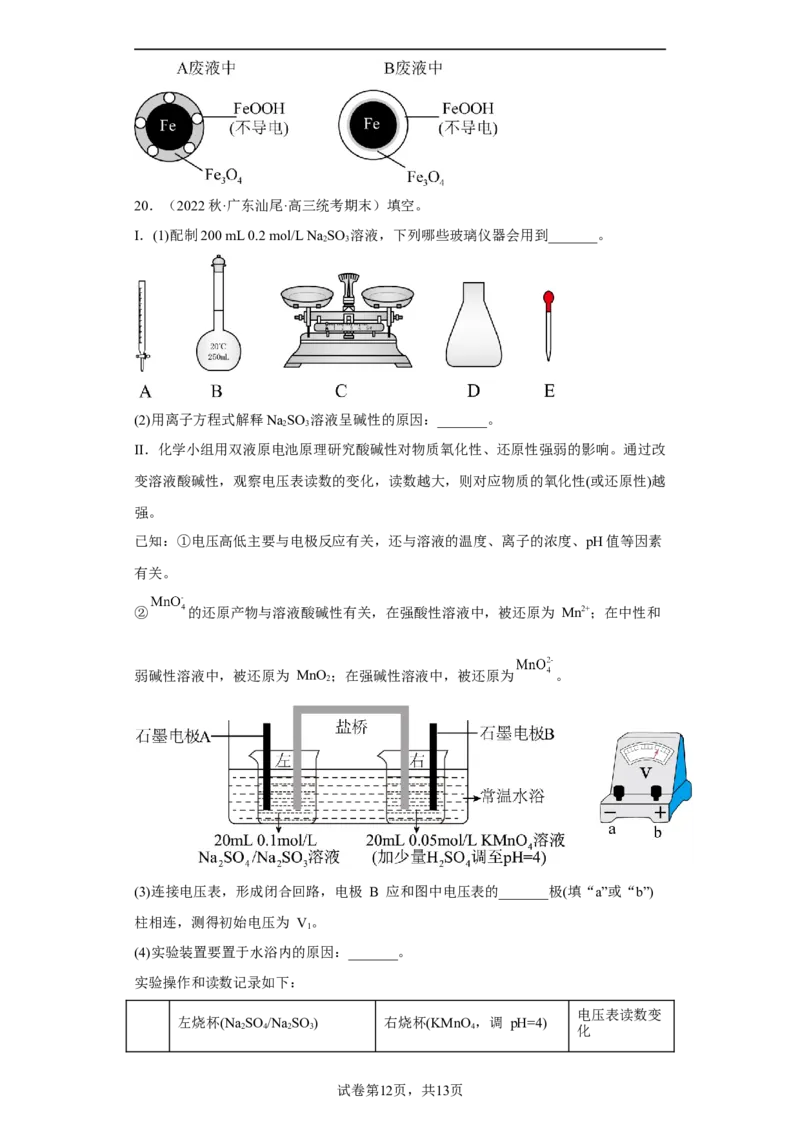
(3)取两份完全相同的含 废液A和B,调节废液A、B的pH分别为2.5和4.5,向
废液A、B中加入足量铁粉,经相同时间充分反应后,废液A、B均接近中性。废液
A、B中铁的最终物质存在形态分别如图所示。溶液的初始pH对铁的氧化产物有影响,
具体影响为_______。废液中 的去除率较低的是_______(“废液A”和“废液B”),
的去除率低的原因是_______。20.(2022秋·广东汕尾·高三统考期末)填空。
I.(1)配制200 mL 0.2 mol/L Na SO 溶液,下列哪些玻璃仪器会用到_______。
2 3
(2)用离子方程式解释NaSO 溶液呈碱性的原因:_______。
2 3
II.化学小组用双液原电池原理研究酸碱性对物质氧化性、还原性强弱的影响。通过改
变溶液酸碱性,观察电压表读数的变化,读数越大,则对应物质的氧化性(或还原性)越
强。
已知:①电压高低主要与电极反应有关,还与溶液的温度、离子的浓度、pH值等因素
有关。
② 的还原产物与溶液酸碱性有关,在强酸性溶液中,被还原为 Mn2+;在中性和
弱碱性溶液中,被还原为 MnO ;在强碱性溶液中,被还原为 。
2
(3)连接电压表,形成闭合回路,电极 B 应和图中电压表的_______极(填“a”或“b”)
柱相连,测得初始电压为 V。
1
(4)实验装置要置于水浴内的原因:_______。
实验操作和读数记录如下:
电压表读数变
左烧杯(Na SO /Na SO ) 右烧杯(KMnO,调 pH=4)
2 4 2 3 4 化
试卷第12页,共13页①逐滴加入5 mL 0.05 mol/L
① 由V 逐渐降低
HSO 1
2 4
② 逐滴加入5 mL 0.1 mol/L
② 由V 逐渐升高
NaOH 1
逐滴加入5 mL 0.05 mol/L
③ 由V 逐渐升高
HSO 1
2 4
④ 加入少量 0.1 mol/L NaOH 由V 略微下降
1
① 继续逐滴加入NaOH至5 mL 再迅速下降
(5)同学甲根据实验③推导出酸性增强,KMnO 的氧化性增强,实验②可以得出:
4
_______。
(6)同学乙认为实验①中,加入酸后,还原剂转化成了_______(填化学式)。
(7)同学丙认为实验设计不够严谨,以实验①②为例,应该往左边烧杯中加入_______,
测得电压为V,以此作为实验①②的初始电压。
2
(8)同学丁认为,实验④加入5 mL NaOH溶液后,右边烧杯内的电极反应为:_______。
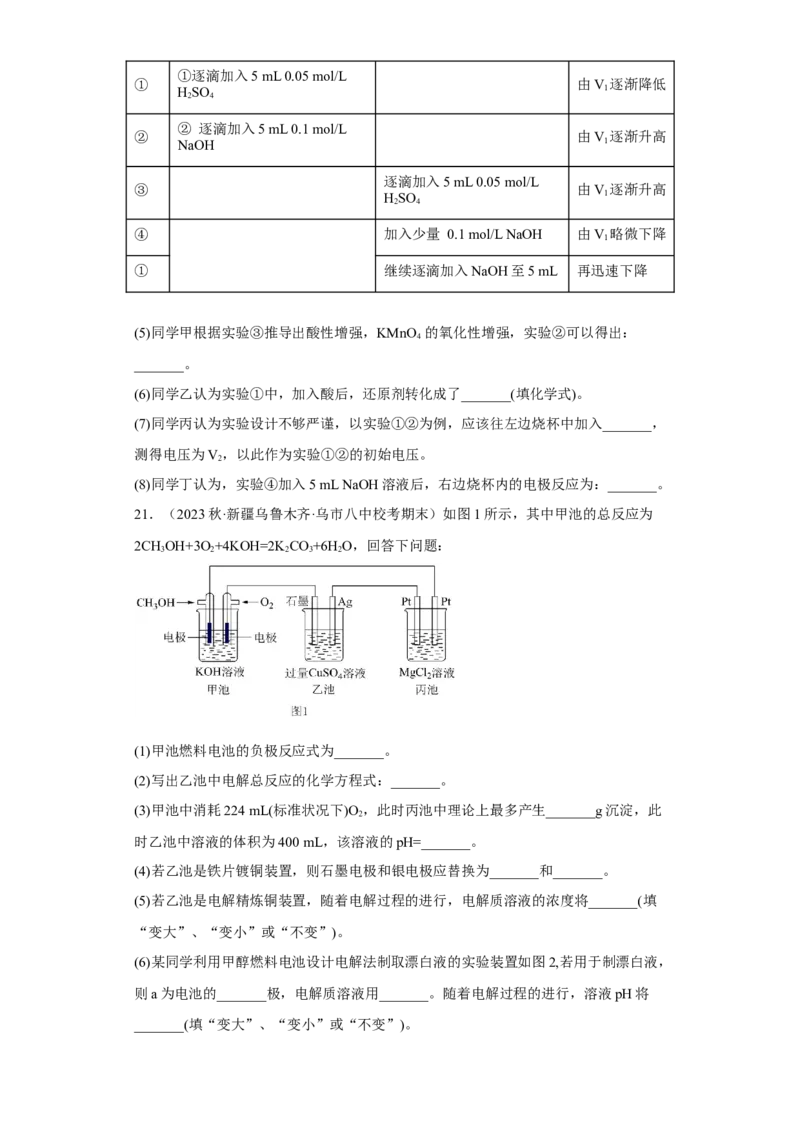
21.(2023秋·新疆乌鲁木齐·乌市八中校考期末)如图1所示,其中甲池的总反应为
2CHOH+3O +4KOH=2K CO+6H O,回答下问题:
3 2 2 3 2
(1)甲池燃料电池的负极反应式为_______。
(2)写出乙池中电解总反应的化学方程式:_______。
(3)甲池中消耗224 mL(标准状况下)O ,此时丙池中理论上最多产生_______g沉淀,此
2
时乙池中溶液的体积为400 mL,该溶液的pH=_______。
(4)若乙池是铁片镀铜装置,则石墨电极和银电极应替换为_______和_______。
(5)若乙池是电解精炼铜装置,随着电解过程的进行,电解质溶液的浓度将_______(填
“变大”、“变小”或“不变”)。
(6)某同学利用甲醇燃料电池设计电解法制取漂白液的实验装置如图2,若用于制漂白液,
则a为电池的_______极,电解质溶液用_______。随着电解过程的进行,溶液pH将
_______(填“变大”、“变小”或“不变”)。试卷第14页,共13页