文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01(广西专用)
化 学
考情速递
高考·新动向:2025年高考试题将会突出立德树人导向,在贴近教学和学生实际的同时突出化学的育人
价值,凸显化学实验学科特色,如第4题,第12题。注重思维逻辑能力考查,试题素材选取范围广,
内容富有时代气息,如第17题。试题内容综合性强,突出科学探究及科学研究思维方法,如第16题。
高考·新考法:试题以化学学科核心素养为主线,对标高中化学新课程标准,加强对基本规律和基本方
法的考查,突出了基础性,如第5题;优化丰富问题情境,体现了时代性,如第9题。加强对分析综合
能力、逻辑推理能力的考查,体现了选拔性,如第14题。试卷考查的知识内容基础、全面而不失新颖
与创新。
高考·新情境:以具有抗菌、抗病毒功效的金银花的一种提取物的结构为载体设题,体现了生活中处处
是化学及化学在人类进步中的作用,如第6题;结合药物的合成考查有机化学主干知识,如第 18题,
考查了官能团名称、有机反应类型、结构简式、手性碳原子、同分异构体、合成路线等。
命题·大预测:本套试卷以《中国高考评价体系》为指导,以《普通高中化学新课程标准》为依据进命
制。
试题立足学科特点,结合社会热点,选取最新科研素材,精心设计试题,能有效检测考生的实际应用能力。
试题涵盖了高考化学常考题型,同时引入新的考查角度,能拓宽考生的视野,考查考生的应变能力,为实现
高考改革的平稳过渡、引导高中化学课堂教学提供了参考。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Fe 56 Cu 64 Co 75
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.化学与人类社会可持续发展息息相关。下列说法不正确的是
A.钠和镁等非常活泼的金属,工业上常用电解法冶炼
B.石油催化裂化可提高轻质油的产量与质量
C.可用电化学氧化法处理氨氮废水(含 及 )D. 难溶于水,可作为X射线检查的内服药剂
2.下列化学用语表示正确的是
A.乙炔分子的空间填充模型:
B.羟基的电子式:
C.CS 的VSEPR模型为:平面三角形
2
D.碳原子核外价电子的轨道表示式:
3.高温结构陶瓷 可由反应 制得,下列说法正确的是
A.第一电离能:
B.该反应中反应物均为共价晶体
C.N 分子中σ键与π键的数目之比为1∶2
2
D.基态C原子共有6种不同空间运动状态的电子
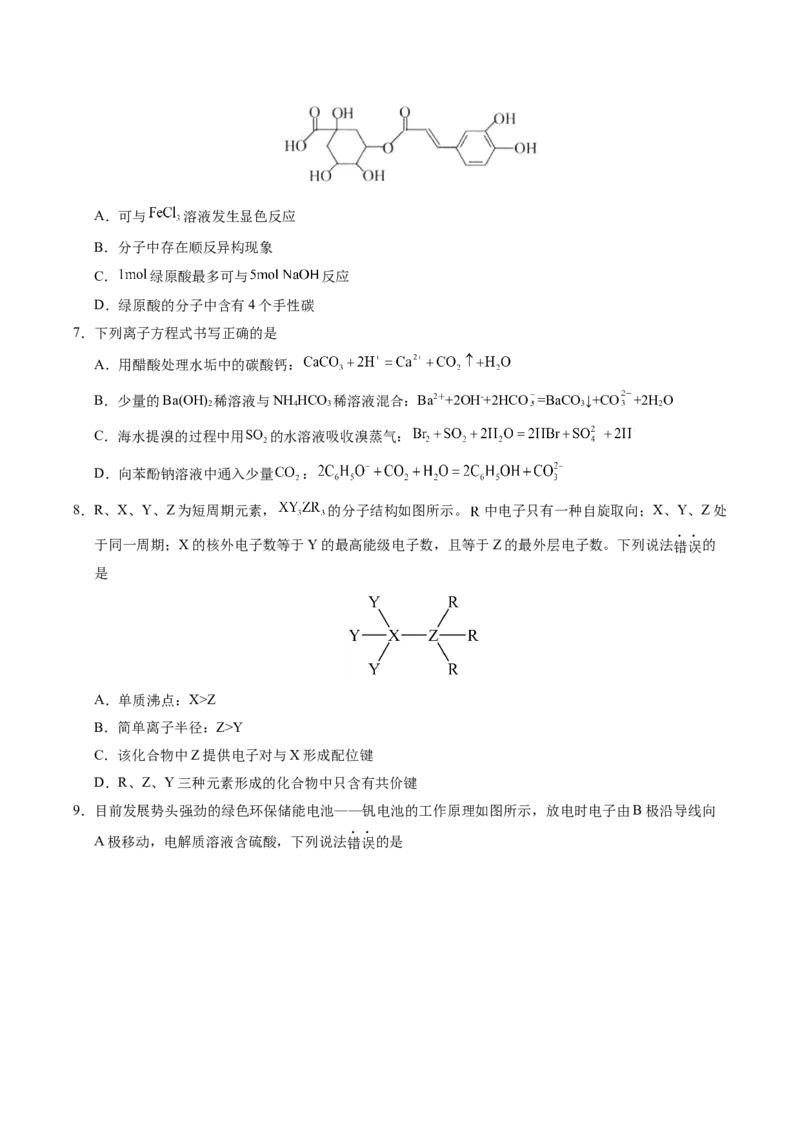
4.下列实验装置或操作能达到实验目的的是
C.除去 中的少量 D.制取少量
A.提纯乙酸乙酯 B.吸收氨气
A.A B.B C.C D.D
5.设 为阿伏加德罗常数的值。下列说法正确的是
A.常温下, 的 溶液中, 的数目为
B.常温常压下, 和 混合气体中含有的氧原子数目为
C.电解精炼铜时,电路中每通过 个电子时阳极溶解
D. 重水比 水多 个质子
6.广西多地盛产金银花,金银花微苦性寒,具有抗菌、抗病毒等功效。它的一种提取物绿原酸的结构如
下图,下列有关绿原酸的说法不正确的是A.可与 溶液发生显色反应
B.分子中存在顺反异构现象
C. 绿原酸最多可与 反应
D.绿原酸的分子中含有4个手性碳
7.下列离子方程式书写正确的是
A.用醋酸处理水垢中的碳酸钙:
B.少量的Ba(OH) 稀溶液与NH HCO 稀溶液混合:Ba2++2OH-+2HCO =BaCO ↓+CO +2H O
2 4 3 3 2
C.海水提溴的过程中用 的水溶液吸收溴蒸气:
D.向苯酚钠溶液中通入少量 :
8.R、X、Y、Z为短周期元素, 的分子结构如图所示。 中电子只有一种自旋取向;X、Y、Z处
于同一周期;X的核外电子数等于Y的最高能级电子数,且等于Z的最外层电子数。下列说法错误的
是
A.单质沸点:X>Z
B.简单离子半径:Z>Y
C.该化合物中Z提供电子对与X形成配位键
D.R、Z、Y三种元素形成的化合物中只含有共价键
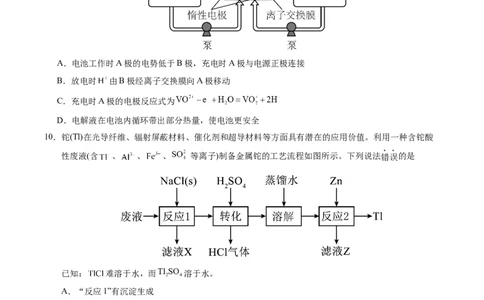
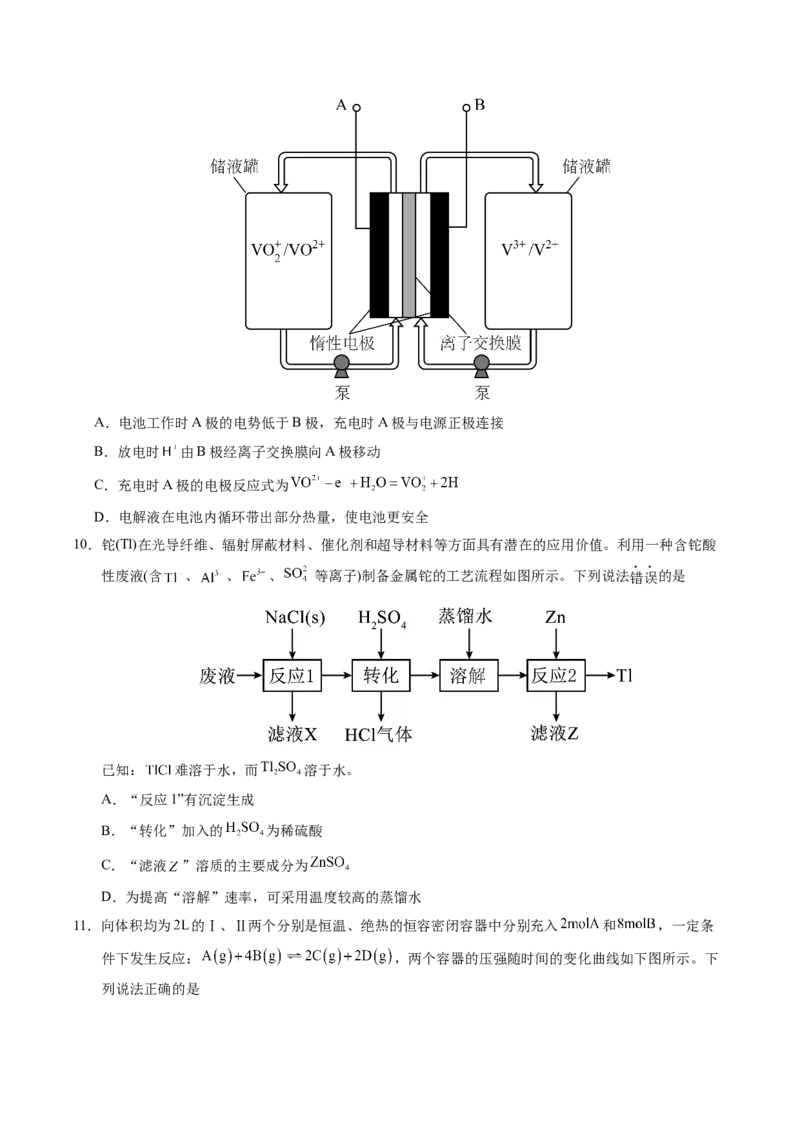
9.目前发展势头强劲的绿色环保储能电池——钒电池的工作原理如图所示,放电时电子由B极沿导线向
A极移动,电解质溶液含硫酸,下列说法错误的是A.电池工作时A极的电势低于B极,充电时A极与电源正极连接
B.放电时 由B极经离子交换膜向A极移动
C.充电时A极的电极反应式为
D.电解液在电池内循环带出部分热量,使电池更安全
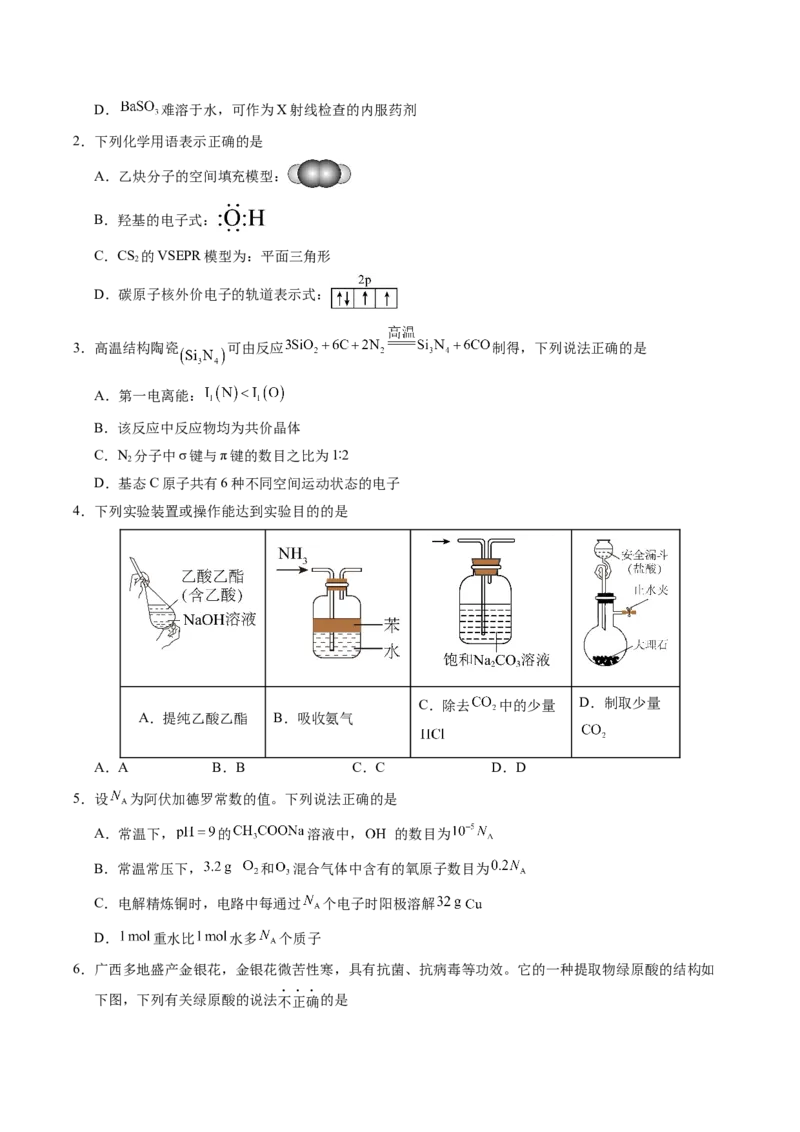
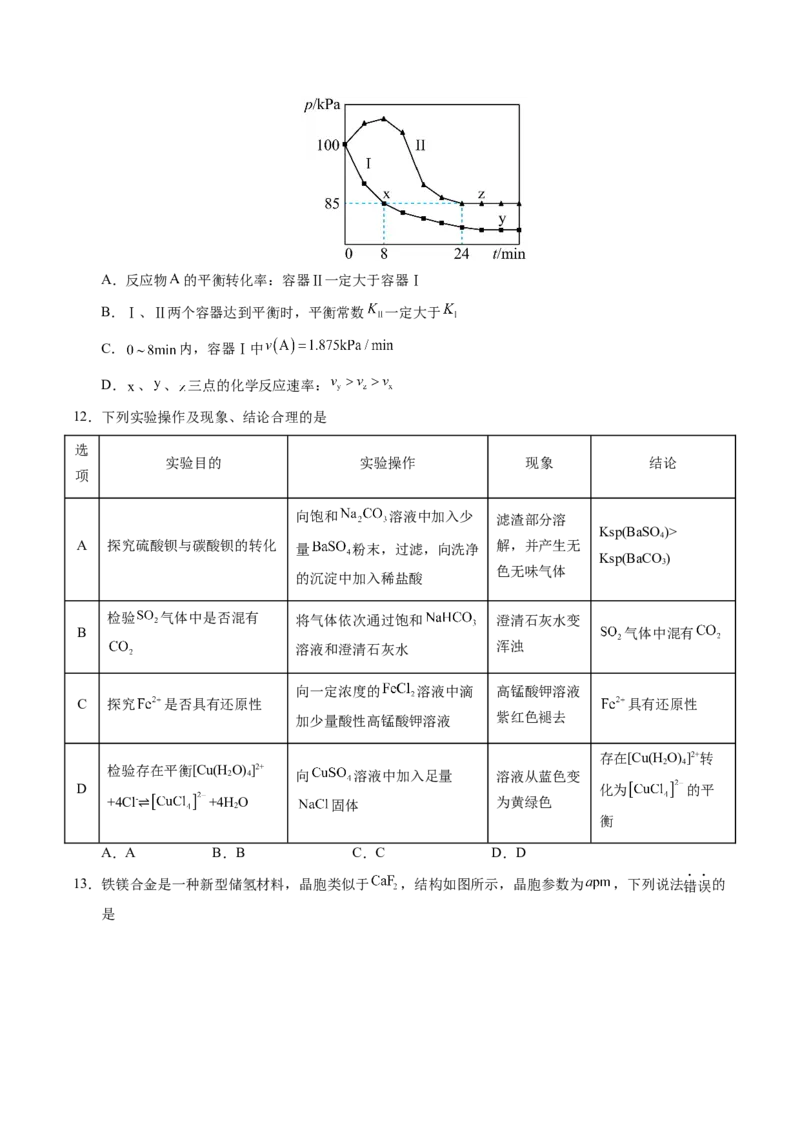
10.铊(Tl)在光导纤维、辐射屏蔽材料、催化剂和超导材料等方面具有潜在的应用价值。利用一种含铊酸
性废液(含 、 、 、 等离子)制备金属铊的工艺流程如图所示。下列说法错误的是
已知: 难溶于水,而 溶于水。
A.“反应1”有沉淀生成
B.“转化”加入的 为稀硫酸
C.“滤液 ”溶质的主要成分为
D.为提高“溶解”速率,可采用温度较高的蒸馏水
11.向体积均为 的Ⅰ、Ⅱ两个分别是恒温、绝热的恒容密闭容器中分别充入 和 ,一定条
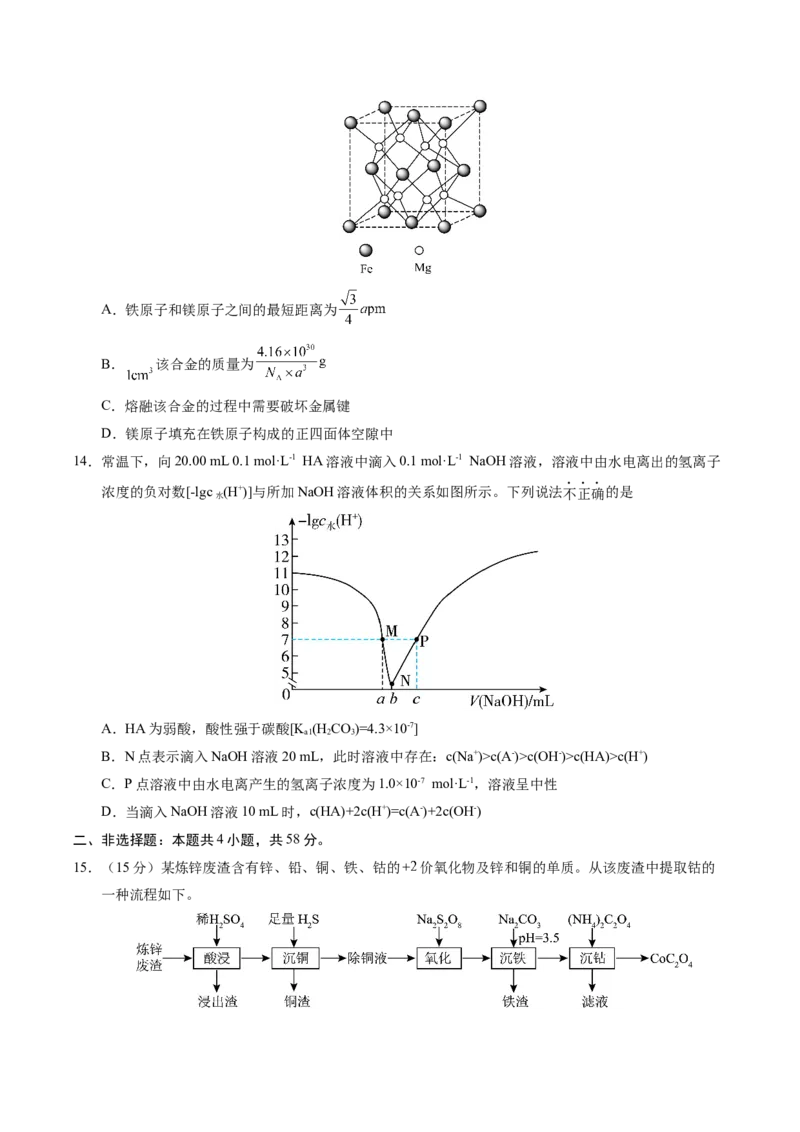
件下发生反应: ,两个容器的压强随时间的变化曲线如下图所示。下
列说法正确的是A.反应物 的平衡转化率:容器Ⅱ一定大于容器Ⅰ
B.Ⅰ、Ⅱ两个容器达到平衡时,平衡常数 一定大于
C. 内,容器Ⅰ中
D. 、 、 三点的化学反应速率:
12.下列实验操作及现象、结论合理的是
选
实验目的 实验操作 现象 结论
项
向饱和 溶液中加入少 滤渣部分溶
Ksp(BaSO )>
4
A 探究硫酸钡与碳酸钡的转化 量 粉末,过滤,向洗净 解,并产生无
Ksp(BaCO )
3
色无味气体
的沉淀中加入稀盐酸
检验 气体中是否混有 将气体依次通过饱和 澄清石灰水变
B 气体中混有
溶液和澄清石灰水 浑浊
向一定浓度的 溶液中滴 高锰酸钾溶液
C 探究 是否具有还原性 具有还原性
加少量酸性高锰酸钾溶液 紫红色褪去
存在[Cu(H O) ]2+转
2 4
检验存在平衡[Cu(H O) ]2+
2 4 向 溶液中加入足量 溶液从蓝色变
D 化为 的平
+4Cl- +4H 2 O 固体 为黄绿色
衡
⇌
A.A B.B C.C D.D
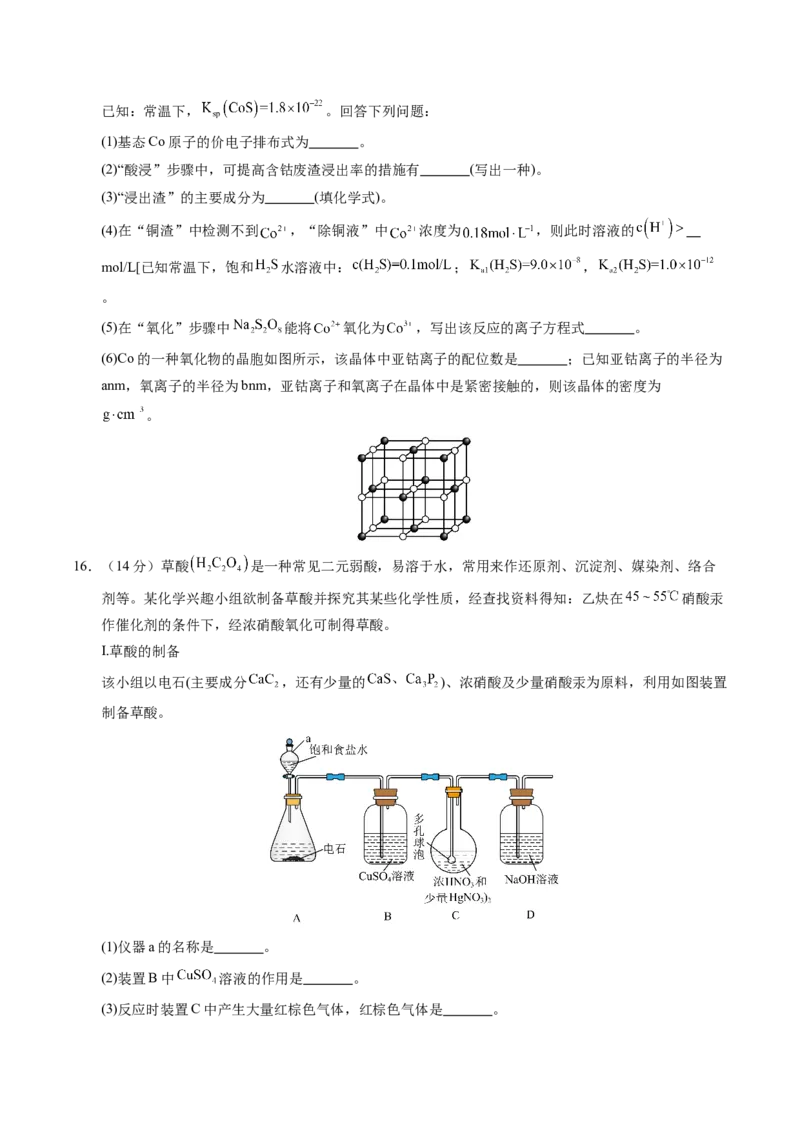
13.铁镁合金是一种新型储氢材料,晶胞类似于 ,结构如图所示,晶胞参数为 ,下列说法错误的
是A.铁原子和镁原子之间的最短距离为
B. 该合金的质量为
C.熔融该合金的过程中需要破坏金属键
D.镁原子填充在铁原子构成的正四面体空隙中
14.常温下,向20.00 mL 0.1 mol·L-1 HA溶液中滴入0.1 mol·L-1 NaOH溶液,溶液中由水电离出的氢离子
浓度的负对数[-lgc (H+)]与所加NaOH溶液体积的关系如图所示。下列说法不正确的是
水
A.HA为弱酸,酸性强于碳酸[K (H CO)=4.3×10-7]
a1 2 3
B.N点表示滴入NaOH溶液20 mL,此时溶液中存在:c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+)
C.P点溶液中由水电离产生的氢离子浓度为1.0×10-7 mol·L-1,溶液呈中性
D.当滴入NaOH溶液10 mL时,c(HA)+2c(H+)=c(A-)+2c(OH-)
二、非选择题:本题共4小题,共58分。
15.(15分)某炼锌废渣含有锌、铅、铜、铁、钴的 价氧化物及锌和铜的单质。从该废渣中提取钴的
一种流程如下。已知:常温下, 。回答下列问题:
(1)基态Co原子的价电子排布式为 。
(2)“酸浸”步骤中,可提高含钴废渣浸出率的措施有 (写出一种)。
(3)“浸出渣”的主要成分为 (填化学式)。
(4)在“铜渣”中检测不到 ,“除铜液”中 浓度为 ,则此时溶液的
mol/L[已知常温下,饱和 水溶液中: ; ,
。
(5)在“氧化”步骤中 能将 氧化为 ,写出该反应的离子方程式 。
(6)Co的一种氧化物的晶胞如图所示,该晶体中亚钴离子的配位数是 ;已知亚钴离子的半径为
anm,氧离子的半径为bnm,亚钴离子和氧离子在晶体中是紧密接触的,则该晶体的密度为
。
16.(14分)草酸 是一种常见二元弱酸,易溶于水,常用来作还原剂、沉淀剂、媒染剂、络合
剂等。某化学兴趣小组欲制备草酸并探究其某些化学性质,经查找资料得知:乙炔在 硝酸汞
作催化剂的条件下,经浓硝酸氧化可制得草酸。
I.草酸的制备
该小组以电石(主要成分 ,还有少量的 )、浓硝酸及少量硝酸汞为原料,利用如图装置
制备草酸。
(1)仪器a的名称是 。
(2)装置B中 溶液的作用是 。
(3)反应时装置C中产生大量红棕色气体,红棕色气体是 。a.NO b. c. d.
(4)装置C中多孔球泡的作用是 。
(5)装置A中主要反应的化学方程式: 。
II.产品中草酸晶体 质量分数的测定
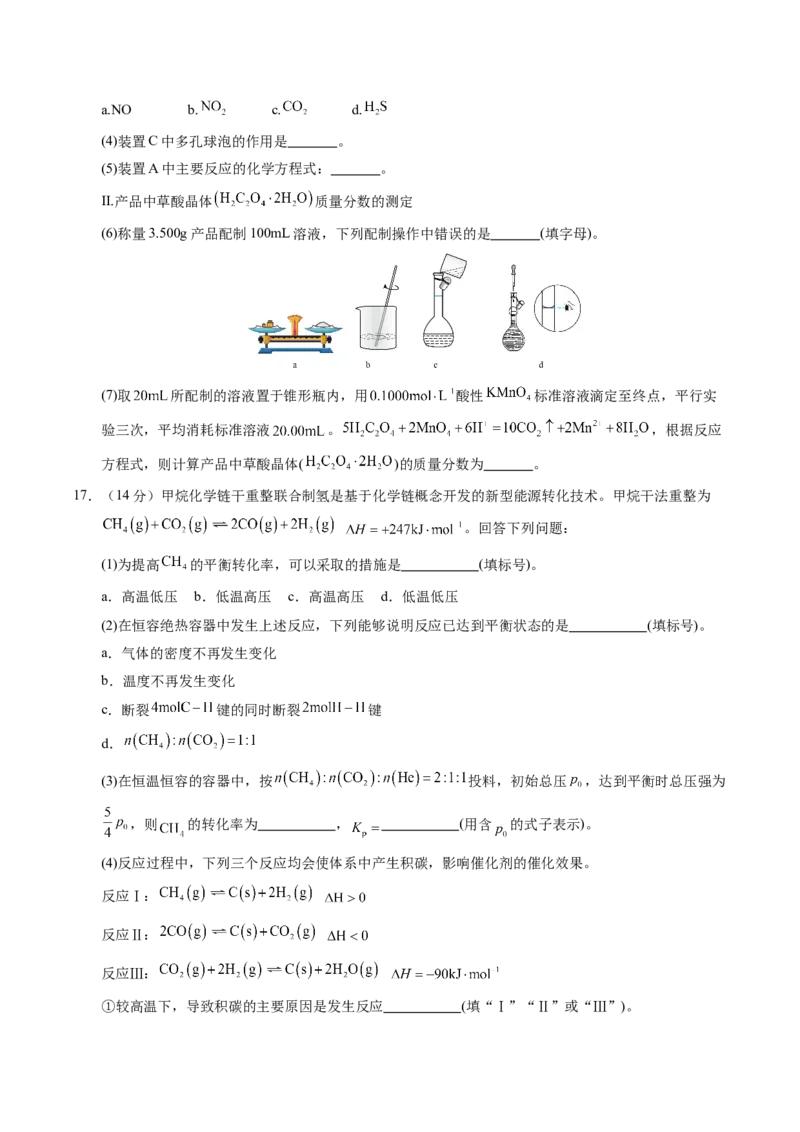
(6)称量3.500g产品配制100mL溶液,下列配制操作中错误的是 (填字母)。
(7)取 所配制的溶液置于锥形瓶内,用 酸性 标准溶液滴定至终点,平行实
验三次,平均消耗标准溶液 。 ,根据反应
方程式,则计算产品中草酸晶体( )的质量分数为 。
17.(14分)甲烷化学链干重整联合制氢是基于化学链概念开发的新型能源转化技术。甲烷干法重整为
。回答下列问题:
(1)为提高 的平衡转化率,可以采取的措施是 (填标号)。
a.高温低压 b.低温高压 c.高温高压 d.低温低压
(2)在恒容绝热容器中发生上述反应,下列能够说明反应已达到平衡状态的是 (填标号)。
a.气体的密度不再发生变化
b.温度不再发生变化
c.断裂 键的同时断裂 键
d.
(3)在恒温恒容的容器中,按 投料,初始总压 ,达到平衡时总压强为
,则 的转化率为 , (用含 的式子表示)。
(4)反应过程中,下列三个反应均会使体系中产生积碳,影响催化剂的催化效果。
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
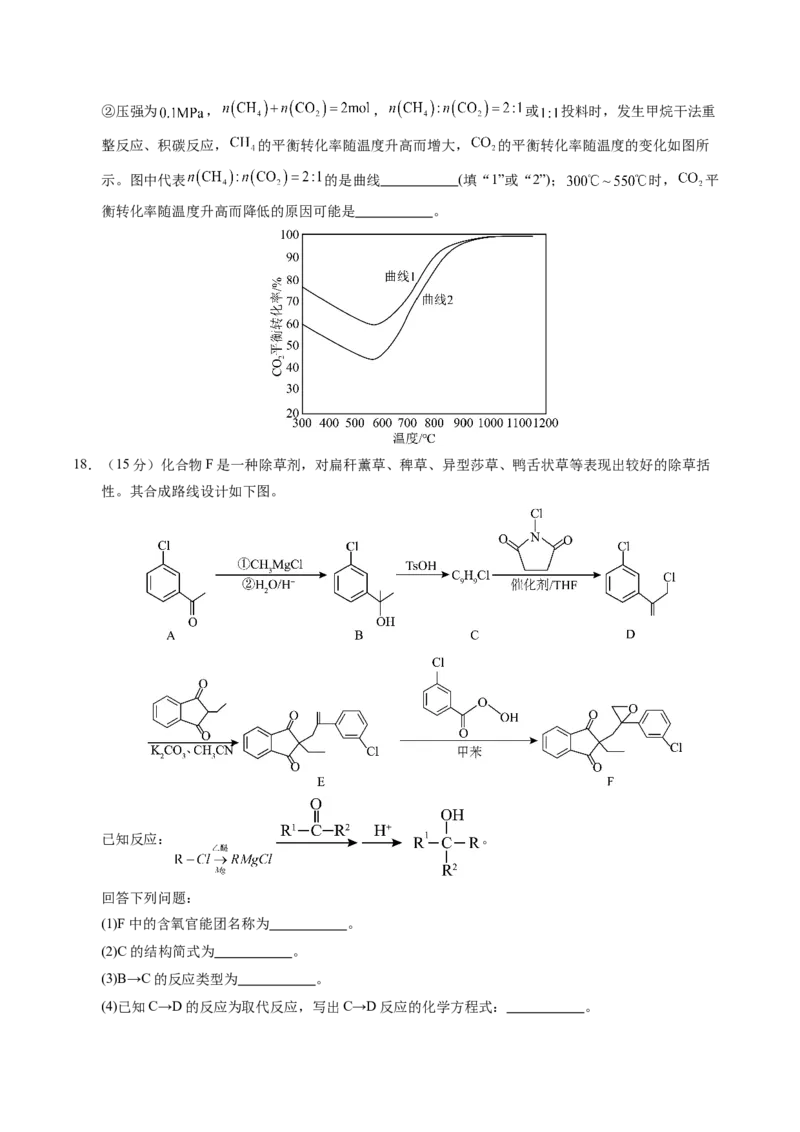
①较高温下,导致积碳的主要原因是发生反应 (填“Ⅰ”“Ⅱ”或“Ⅲ”)。②压强为 , , 或 投料时,发生甲烷干法重
整反应、积碳反应, 的平衡转化率随温度升高而增大, 的平衡转化率随温度的变化如图所
示。图中代表 的是曲线 (填“1”或“2”); 时, 平
衡转化率随温度升高而降低的原因可能是 。
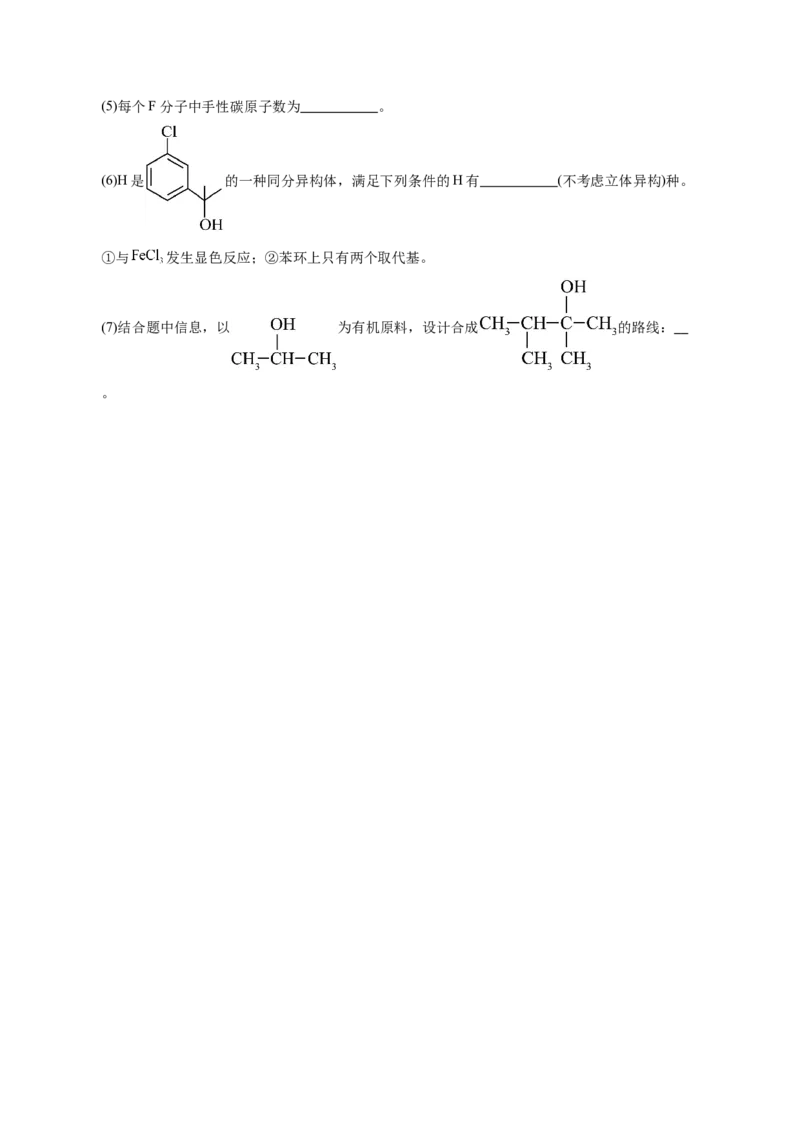
18.(15分)化合物F是一种除草剂,对扁秆薰草、稗草、异型莎草、鸭舌状草等表现出较好的除草括
性。其合成路线设计如下图。
已知反应: 。
回答下列问题:
(1)F中的含氧官能团名称为 。
(2)C的结构简式为 。
(3)B→C的反应类型为 。
(4)已知C→D的反应为取代反应,写出C→D反应的化学方程式: 。(5)每个F分子中手性碳原子数为 。
(6)H是 的一种同分异构体,满足下列条件的H有 (不考虑立体异构)种。
①与 发生显色反应;②苯环上只有两个取代基。
(7)结合题中信息,以 为有机原料,设计合成 的路线:
。