文档内容
4.表格型实验方案的设计及评价
1.(2024·贵州六校联盟联考三)下列实验设计可以达到实验目的的是( )
选项 实验目的 实验设计
向2 mL 0.01 mol·L-1 KI溶液中加入5 mL 0.01 mol·L-1
A 证明Fe3+和I-的反应存在限度 FeCl 溶液,溶液呈棕黄色,再滴加几滴KSCN溶液,溶液
3
变为红色
B 检验待测液中含有Na+ 用玻璃棒蘸取待测液在无色火焰上灼烧观察现象
将5~6滴饱和FeCl 溶液滴加到煮沸的蒸馏水中,继续
3
C 制备Fe(OH) 胶体
3
煮沸至液体呈红褐色为止
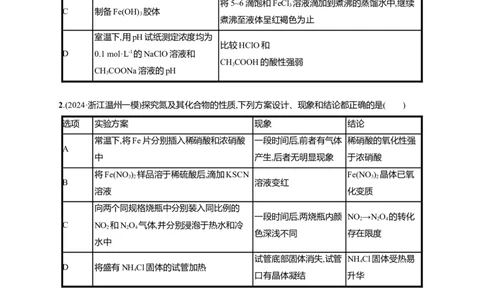
室温下,用pH试纸测定浓度均为
比较HClO和
D 0.1 mol·L-1的NaClO溶液和
CHCOOH的酸性强弱
3
CHCOONa溶液的pH
3
2.(2024·浙江温州一模)探究氮及其化合物的性质,下列方案设计、现象和结论都正确的是( )
选项 实验方案 现象 结论
常温下,将Fe片分别插入稀硝酸和浓硝酸 一段时间后,前者有气体 稀硝酸的氧化性强
A
中 产生,后者无明显现象 于浓硝酸
将Fe(NO ) 样品溶于稀硫酸后,滴加KSCN Fe(NO ) 晶体已氧
3 2 3 2
B 溶液变红
溶液 化变质
向两个同规格烧瓶中分别装入同比例的
一段时间后,两烧瓶内颜 NO →NO 的转化
2 2 4
C NO 和NO 气体,并分别浸泡于热水和冷
2 2 4
色深浅不同 存在限度
水中
试管底部固体消失,试管 NH Cl固体受热易
4
D 将盛有NH Cl固体的试管加热
4
口有晶体凝结 升华
3.(2024·湖南邵阳二模)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
取少量Fe与水蒸气高温反应后的固体产物于试
第一份溶液变红
管中,加足量的稀硫酸溶解,分成两份:第一份滴加 固体产物中铁元素只
A 色,第二份溶液紫
1~2滴KSCN溶液,第二份滴加1~2滴KMnO 溶 有+3价态
4
红色褪去
液
B 向某钾盐中滴加浓盐酸 产生的气体可以 该钾盐一定为KSO
2 3或KHSO 或二者的
3
使品红溶液褪色
混合物
NaSO 使蛋白质变
2 4
C 向蛋白质溶液中加入饱和NaSO 溶液 产生沉淀
2 4
性
在小烧杯中加入约5 g动物脂肪、6 mL 95%的乙
沉淀溶解、溶液
D 醇,再加入6 mL 40%的氢氧化钠溶液,微热一段时 油脂已发生水解
呈绛蓝色
间后取少量溶液,加入新制氢氧化铜
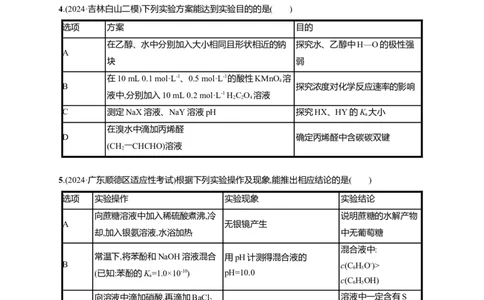
4.(2024·吉林白山二模)下列实验方案能达到实验目的的是( )
选项 方案 目的
在乙醇、水中分别加入大小相同且形状相近的钠 探究水、乙醇中H—O的极性强
A
块 弱
在10 mL 0.1 mol·L-1、0.5 mol·L-1的酸性KMnO 溶
4
B 探究浓度对化学反应速率的影响
液中,分别加入10 mL 0.2 mol·L-1 H C O 溶液
2 2 4
C 测定NaX溶液、NaY溶液pH 探究HX、HY的K 大小
a
在溴水中滴加丙烯醛
D 确定丙烯醛中含碳碳双键
(CH CHCHO)溶液
2
5.(2024·广东顺德区适应性考试)根据下列实验操作及现象,能推出相应结论的是( )
选项 实验操作 实验现象 实验结论
向蔗糖溶液中加入稀硫酸煮沸,冷 说明蔗糖的水解产物
A 无银镜产生
却,加入银氨溶液,水浴加热 中无葡萄糖
混合液中:
常温下,将苯酚和NaOH溶液混合 用pH计测得混合液的
B c(C HO-)>
6 5
(已知:苯酚的K=1.0×10-10) pH=10.0
a
c(C HOH)
6 5
向溶液中滴加硝酸,再滴加BaCl 溶液中一定含有S
2
C 有白色沉淀生成
溶液
O2-
4
将Ag和AgNO 溶液与Cu和
3
Ag电极表面有银白色金属沉
D NaSO 溶液组成双液原电池,连通 金属性:Cu>Ag
2 4
积,Cu电极附近溶液变蓝
装置
6.(2024·山东临沂二模)根据下列实验操作和现象,得出的相应结论正确的是( )
选项 实验操作及现象 结论A 乙醇和浓硫酸共热至170 ℃,产生的气体使溴水褪色 乙烯发生了加成反应
在25 ℃和40 ℃时,测得0.1 mol·L-1 Na SO 溶液的pH分
SO2-
的水解程度随温度升高而增
2 3 3
B
别是9.66和9.37 大
向KCr O 溶液中加入少量AgNO 溶液,只有Ag CrO 沉 K (Ag CrO)<
2 2 7 3 2 4 sp 2 4
C
淀生成 K sp (Ag 2 Cr 2 O 7 )
常温下,分别向无水乙醇和冰醋酸中加入大小相同的金属
D 分子中氢氧键的极性:乙醇<乙酸
钠,前者反应更剧烈
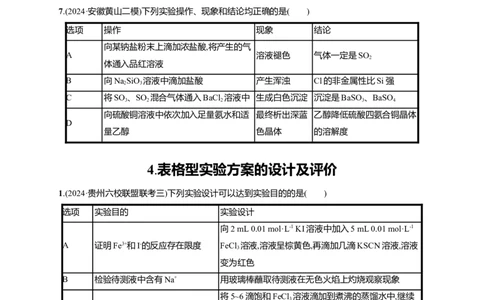
7.(2024·安徽黄山二模)下列实验操作、现象和结论均正确的是( )
选项 操作 现象 结论
向某钠盐粉末上滴加浓盐酸,将产生的气
A 溶液褪色 气体一定是SO
2
体通入品红溶液
B 向NaSiO 溶液中滴加盐酸 产生浑浊 Cl的非金属性比Si强
2 3
C 将SO 、SO 混合气体通入BaCl 溶液中 生成白色沉淀 沉淀是BaSO、BaSO
3 2 2 3 4
向硫酸铜溶液中依次加入足量氨水和适 最终析出深蓝 乙醇降低硫酸四氨合铜晶体
D
量乙醇 色晶体 的溶解度
4.表格型实验方案的设计及评价
1.(2024·贵州六校联盟联考三)下列实验设计可以达到实验目的的是( )
选项 实验目的 实验设计
向2 mL 0.01 mol·L-1 KI溶液中加入5 mL 0.01 mol·L-1
A 证明Fe3+和I-的反应存在限度 FeCl 溶液,溶液呈棕黄色,再滴加几滴KSCN溶液,溶液
3
变为红色
B 检验待测液中含有Na+ 用玻璃棒蘸取待测液在无色火焰上灼烧观察现象
将5~6滴饱和FeCl 溶液滴加到煮沸的蒸馏水中,继续
3
C 制备Fe(OH) 胶体
3
煮沸至液体呈红褐色为止
室温下,用pH试纸测定浓度均为
比较HClO和
D 0.1 mol·L-1的NaClO溶液和
CHCOOH的酸性强弱
3
CHCOONa溶液的pH
3
答案:C解析:向2 mL 0.01 mol·L-1 KI溶液中加入5 mL 0.01 mol·L-1 FeCl 溶液,该反应中FeCl 过量,溶液呈棕
3 3
黄色,再滴加几滴KSCN溶液,溶液变为红色,只能说明溶液中存在Fe3+,不能说明Fe3+和I-的反应存在
限度,A错误;玻璃中含有硅酸钠,因此不能用玻璃棒做焰色试验,应该用铂丝或洁净铁丝,B错误;饱和
氯化铁溶液在加热条件下水解平衡正向移动,当出现红褐色时即可制得氢氧化铁胶体,C正确;次氯酸
钠有强氧化性,不能用pH试纸测定其pH,D错误。
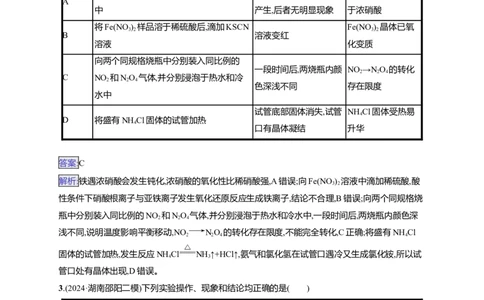
2.(2024·浙江温州一模)探究氮及其化合物的性质,下列方案设计、现象和结论都正确的是( )
选项 实验方案 现象 结论
常温下,将Fe片分别插入稀硝酸和浓硝酸 一段时间后,前者有气体 稀硝酸的氧化性强
A
中 产生,后者无明显现象 于浓硝酸
将Fe(NO ) 样品溶于稀硫酸后,滴加KSCN Fe(NO ) 晶体已氧
3 2 3 2
B 溶液变红
溶液 化变质
向两个同规格烧瓶中分别装入同比例的
一段时间后,两烧瓶内颜 NO →NO 的转化
2 2 4
C NO 和NO 气体,并分别浸泡于热水和冷
2 2 4
色深浅不同 存在限度
水中
试管底部固体消失,试管 NH Cl固体受热易
4
D 将盛有NH Cl固体的试管加热
4
口有晶体凝结 升华
答案:C
解析:铁遇浓硝酸会发生钝化,浓硝酸的氧化性比稀硝酸强,A错误;向Fe(NO ) 溶液中滴加稀硫酸,酸
3 2
性条件下硝酸根离子与亚铁离子发生氧化还原反应生成铁离子,结论不合理,B错误;向两个同规格烧
瓶中分别装入同比例的NO 和NO 气体,并分别浸泡于热水和冷水中,一段时间后,两烧瓶内颜色深
2 2 4
浅不同,说明温度影响平衡移动,NO NO 的转化存在限度,不能完全转化,C正确;将盛有NH Cl
2 2 4 4
固体的试管加热,发生反应NH Cl NH ↑+HCl↑,氨气和氯化氢在试管口遇冷又生成氯化铵,所以试
4 3
管口处有晶体出现,D错误。
3.(2024·湖南邵阳二模)下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
取少量Fe与水蒸气高温反应后的固体产物于试
第一份溶液变红
管中,加足量的稀硫酸溶解,分成两份:第一份滴加 固体产物中铁元素只
A 色,第二份溶液紫
1~2滴KSCN溶液,第二份滴加1~2滴KMnO 溶 有+3价态
4
红色褪去
液
产生的气体可以 该钾盐一定为KSO
B 向某钾盐中滴加浓盐酸 2 3
使品红溶液褪色 或KHSO 或二者的
3混合物
NaSO 使蛋白质变
2 4
C 向蛋白质溶液中加入饱和NaSO 溶液 产生沉淀
2 4
性
在小烧杯中加入约5 g动物脂肪、6 mL 95%的乙
沉淀溶解、溶液
D 醇,再加入6 mL 40%的氢氧化钠溶液,微热一段时 油脂已发生水解
呈绛蓝色
间后取少量溶液,加入新制氢氧化铜
答案:D
解析:取少量Fe与水蒸气高温反应后的固体产物于试管中,加足量的稀硫酸溶解,分成两份:第一份滴
加1~2滴KSCN溶液,第二份滴加1~2滴KMnO 溶液,第一份溶液变红色,说明含有Fe3+,第二份溶液
4
紫红色褪去,说明含有Fe2+,固体产物中铁元素有+2、+3两种价态,A错误;向某钾盐中滴加浓盐酸,产
生的气体可以使品红溶液褪色,放出的气体为二氧化硫或氯气,所以该钾盐可能为KSO 或KHSO 或
2 3 3
二者的混合物,也可能为KClO、KMnO 等强氧化性盐,B错误;向蛋白质溶液中加入饱和NaSO 溶
3 4 2 4
液,产生沉淀,Na SO 使蛋白质溶液盐析,C错误;在小烧杯中加入约5 g动物脂肪、6 mL 95%的乙醇,
2 4
再加入6 mL 40%的氢氧化钠溶液,微热一段时间后取少量溶液,加入新制氢氧化铜,沉淀溶解,溶液呈
绛蓝色,说明有甘油生成,则油脂已发生水解,D正确。
4.(2024·吉林白山二模)下列实验方案能达到实验目的的是( )
选项 方案 目的
在乙醇、水中分别加入大小相同且形状相近的钠 探究水、乙醇中H—O的极性强
A
块 弱
在10 mL 0.1 mol·L-1、0.5 mol·L-1的酸性KMnO 溶
4
B 探究浓度对化学反应速率的影响
液中,分别加入10 mL 0.2 mol·L-1 H C O 溶液
2 2 4
C 测定NaX溶液、NaY溶液pH 探究HX、HY的K 大小
a
在溴水中滴加丙烯醛
D 确定丙烯醛中含碳碳双键
(CH CHCHO)溶液
2
答案:A
解析:A项,若水中产生H 的过程较乙醇中更剧烈,则水中H—O极性比乙醇中的强,能达到目的;B项,
2
酸性KMnO 溶液过量,溶液不褪色,不能判断浓度对反应速率的影响,不能达到目的;C项,未标明钠盐
4
浓度,无法比较两种酸的酸性强弱,不能达到目的;D项,溴水具有强氧化性,能氧化醛基,不能达到目的;
故选A。
5.(2024·广东顺德区适应性考试)根据下列实验操作及现象,能推出相应结论的是( )选项 实验操作 实验现象 实验结论
向蔗糖溶液中加入稀硫酸煮沸,冷 说明蔗糖的水解产物
A 无银镜产生
却,加入银氨溶液,水浴加热 中无葡萄糖
混合液中:
常温下,将苯酚和NaOH溶液混合 用pH计测得混合液的
B c(C HO-)>
6 5
(已知:苯酚的K=1.0×10-10) pH=10.0
a
c(C HOH)
6 5
向溶液中滴加硝酸,再滴加BaCl 溶液中一定含有S
2
C 有白色沉淀生成
溶液
O2-
4
将Ag和AgNO 溶液与Cu和
3
Ag电极表面有银白色金属沉
D NaSO 溶液组成双液原电池,连通 金属性:Cu>Ag
2 4
积,Cu电极附近溶液变蓝
装置
答案:D
解析:银镜反应需要在碱性环境中进行,故需加入碱调节溶液酸碱性后再进行银镜实验,A错误;测得
c(C H O-)c(H+) c(C H O-)×1.0×10-10
混合液的pH=10.0,则K= 6 5 = 6 5 =1.0×10-10,故
a c(C H OH) c(C H OH)
6 5 6 5
c(C HO-)=c(C HOH),B错误;溶液中若含有银离子也会生成氯化银白色沉淀,C错误;该原电池的总反
6 5 6 5
应式:Cu+2Ag+ Cu2++2Ag,铜比银活泼,在形成原电池过程中,铜作负极,发生氧化反应生成铜离子,
铜电极附近溶液逐渐变蓝;银作正极,发生还原反生成银单质,银表面有银白色金属沉积;所以该实验
可以比较铜和银的金属性强弱,D正确。
6.(2024·山东临沂二模)根据下列实验操作和现象,得出的相应结论正确的是( )
选项 实验操作及现象 结论
A 乙醇和浓硫酸共热至170 ℃,产生的气体使溴水褪色 乙烯发生了加成反应
在25 ℃和40 ℃时,测得0.1 mol·L-1 Na SO 溶液的pH分
SO2-
的水解程度随温度升高而增
2 3 3
B
别是9.66和9.37 大
向KCr O 溶液中加入少量AgNO 溶液,只有Ag CrO 沉 K (Ag CrO)<
2 2 7 3 2 4 sp 2 4
C
淀生成 K sp (Ag 2 Cr 2 O 7 )
常温下,分别向无水乙醇和冰醋酸中加入大小相同的金属
D 分子中氢氧键的极性:乙醇<乙酸
钠,前者反应更剧烈
答案:C
解析:乙醇和浓硫酸共热至170 ℃,产生的乙烯气体中混有二氧化硫,二氧化硫也可以使溴水褪色,不
能证明乙烯和Br 发生了加成反应,A错误;升高温度,溶液pH减小,不能说明升高温度促进水解使平
2衡正向移动,B错误;K Cr O
溶液中存在平衡:CrO2-
+H O
2H++2CrO2- ,CrO2- 的浓度小于CrO2-
,
2 2 7 2 7 2 4 4 2 7
加入少量AgNO 溶液,只有Ag CrO 沉淀生成,更加说明Ag CrO 的溶解度小于
3 2 4 2 4
Ag Cr O,K (Ag CrO)乙酸,D错误。
7.(2024·安徽黄山二模)下列实验操作、现象和结论均正确的是( )
选项 操作 现象 结论
向某钠盐粉末上滴加浓盐酸,将产生的气
A 溶液褪色 气体一定是SO
2
体通入品红溶液
B 向NaSiO 溶液中滴加盐酸 产生浑浊 Cl的非金属性比Si强
2 3
C 将SO 、SO 混合气体通入BaCl 溶液中 生成白色沉淀 沉淀是BaSO、BaSO
3 2 2 3 4
向硫酸铜溶液中依次加入足量氨水和适 最终析出深蓝 乙醇降低硫酸四氨合铜晶体
D
量乙醇 色晶体 的溶解度
答案:D
解析:高锰酸钠固体能与浓盐酸反应生成能使品红溶液褪色的氯气,则向某钠盐粉末上滴加浓盐酸,将
产生的气体通入品红溶液,溶液褪色不能说明产生的气体一定是二氧化硫,A错误;元素的非金属性强
弱与最高价氧化物对应水化物的强弱有关,与氢化物的酸性无关,则向硅酸钠溶液中滴加盐酸产生浑
浊只能说明盐酸的酸性强于硅酸,但不能说明氯元素的非金属性强于硅元素,B错误;亚硫酸的酸性弱
于盐酸,由强酸制弱酸的原理可知,二氧化硫不能与氯化钡溶液反应,则将三氧化硫、二氧化硫混合气
体通入氯化钡溶液中,反应生成的白色沉淀中不可能含有亚硫酸钡,C错误;硫酸铜溶液与足量氨水反
应生成硫酸四氨合铜,向硫酸铜溶液中依次加入足量氨水和适量乙醇,最终析出深蓝色晶体是因为乙
醇降低了硫酸四氨合铜晶体的溶解度,D正确。