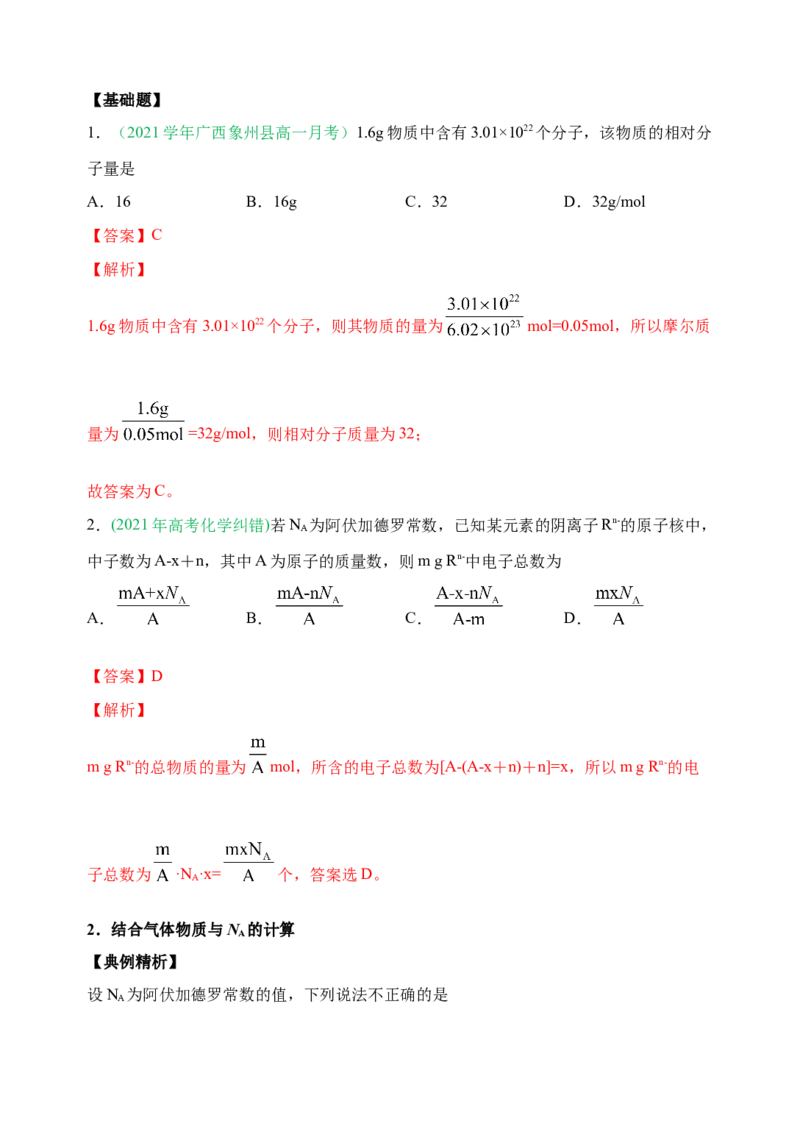文档内容
微专题 02 以物质的量为中心的计算
化学学科中的有关计算是以物质的量为中心进行的,化学计算是高考的必考点,更
是重点。
本专题对“以物质的量为中心的有关计算”进行分类解析,并通过分层训练达成掌
握,提升,灵活运用解题方法和技巧,从而实现较难化学计算题的解题突破。
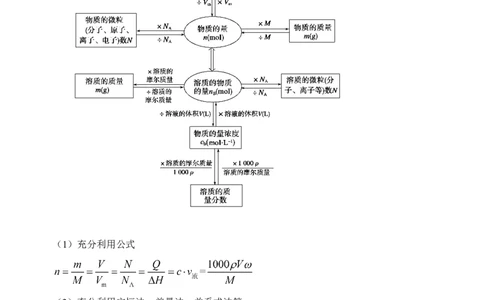
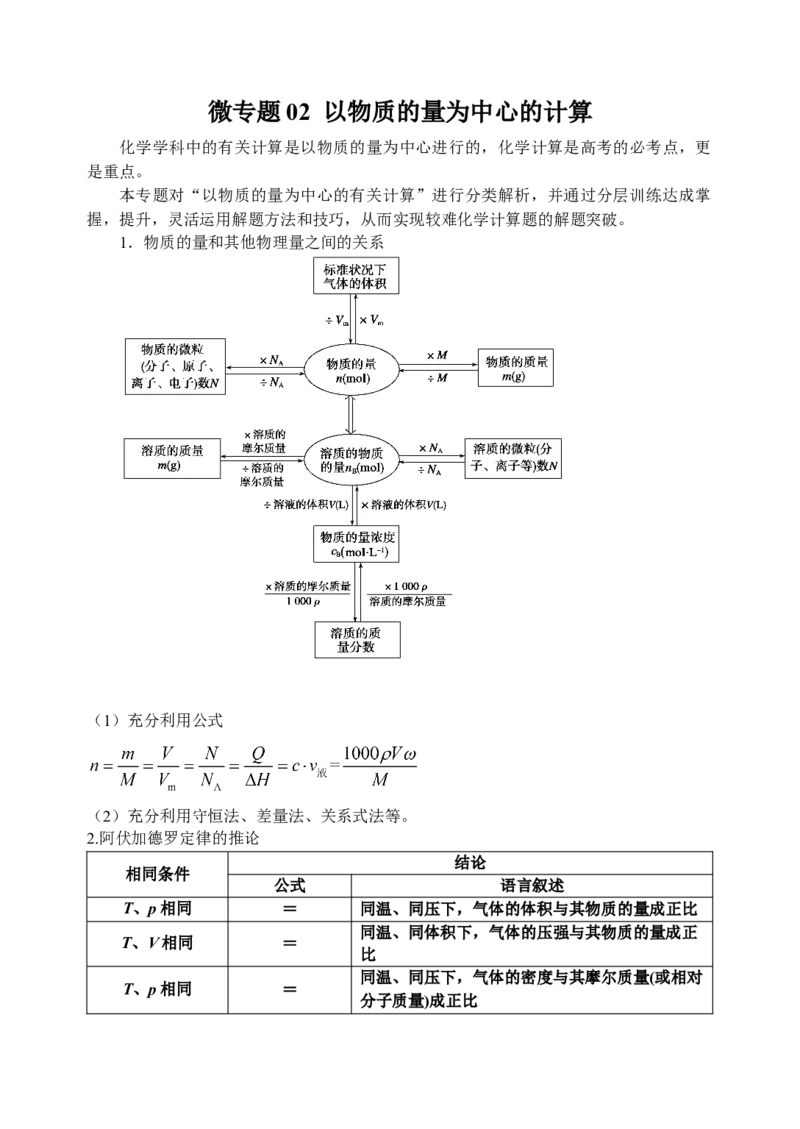
1.物质的量和其他物理量之间的关系
(1)充分利用公式
(2)充分利用守恒法、差量法、关系式法等。
2.阿伏加德罗定律的推论
结论
相同条件
公式 语言叙述
T、p相同 = 同温、同压下,气体的体积与其物质的量成正比
同温、同体积下,气体的压强与其物质的量成正
T、V相同 =
比
同温、同压下,气体的密度与其摩尔质量(或相对
T、p相同 =
分子质量)成正比3.解题要点
(1)对气体来说,在解题时要特别注意气体所处的外界条件,因温度、压强不同,气体
体积不同,注意运用阿伏加德罗定律的推论。当涉及NO2气体时,还要考虑2NO
2
NO 的转化。
2 4
(2)对于混合物中各物质进行分析,既要考虑反应,还要考虑反应进行的程度和过量问
题。
(3)影响因素:V 的数值不是固定不变的,它决定于气体所处的温度和压强。
m
一、与物质的量有关的计算
1.根据 进行相关的计算
【典例精析】
下列叙述不正确的是
A.1molH O的质量为18g/mol
2
B.N 个HSO 分子的质量与HPO 的摩尔质量在数值上相等
A 2 4 3 4
C.3.01×1023个SO 分子的质量为32g
2
D.18gNH 含有电子数为10N
A
【答案】A
【解析】
A.1molH O的质量为18g,故A错误;
2
B.N 个HSO 分子的质量为98g,HPO 的摩尔质量为98g/mol,两者在数值上相等,故
A 2 4 3 4
B正确;
C.3.01×1023个SO 分子的物质的量为 =0.5mol,质量为0.5mol×64g/
2
mol=32g,故C正确;
D.18gNH 的物质的量为1mol,1个NH 中有10个电子,则1mol NH 中含有电子数
为10N ,故D正确;
A
故选A。【基础题】
1.(2021学年广西象州县高一月考)1.6g物质中含有3.01×1022个分子,该物质的相对分
子量是
A.16 B.16g C.32 D.32g/mol
【答案】C
【解析】
1.6g物质中含有3.01×1022个分子,则其物质的量为 mol=0.05mol,所以摩尔质
量为 =32g/mol,则相对分子质量为32;
故答案为C。
2.(2021年高考化学纠错)若N 为阿伏加德罗常数,已知某元素的阴离子Rn-的原子核中,
A
中子数为A-x+n,其中A为原子的质量数,则m g Rn-中电子总数为
A. B. C. D.
【答案】D
【解析】
m g Rn-的总物质的量为 mol,所含的电子总数为[A-(A-x+n)+n]=x,所以m g Rn-的电
子总数为 ·N ·x= 个,答案选D。
A
2.结合气体物质与N 的计算
A
【典例精析】
设N 为阿伏加德罗常数的值,下列说法不正确的是
AA.32gO 含有的电子数为16N
2 A
B.1molCl 与足量NaOH溶液反应,转移的电子数为1N
2 A
C.1L0.1mol·L-1NaSO 溶液中含有的Na+数为0.2N
2 4 A
D.11.2LCH 含有的分子数为0.5N
4 A
【答案】D
【解析】
A.32gO 的物质的量为1mol,电子数为1mol×16×N mol-1=16N ,A正确;
2 A A
B.1molCl 与足量NaOH溶液反应得到1molNaClO和1molNaCl,发生歧化反应,转移电
2
子数为1mol×(1-0)×N mol-1=1N ,B正确;
A A
C.1L0.1mol·L-1NaSO 溶液中含有的Na+数=1L×0.1mol·L-1×2×N mol-1=0.2N ,C正确;
2 4 A A
D.未给标准状况,无法计算,D错误;
答案选D。
【基础题】
1.(2021学年甘南州高一上学期期中考试)设N 表示阿伏加德罗常数的值,请回答下列问
A
题:
(1) O 的摩尔质量为______g/mol,1mol O 中含有_______个O 分子。
2 2 2
(2) 6.02×1023个Na+约含有_______mol Na+,其质量为_______g。
(3) 0.5 mol CH 约含有_______个CH,其标准状况的气体体积_______L。
4 4
(4) 0.2molAl含有_______个铝原子,质量是_______g。
【答案】32 6.02×1023 1 23 3.01×1023 11.2 1.204×1023 5.4
【解析】
(1) 摩尔质量以g/mol为单位数值上等于相对分子质量,则O 的摩尔质量为32g/mol,
2
1mol O 中含有 个O 分子。
2 2
(2) ,6.02×1023个Na+约含有1mol Na+,其质量为 。
(3) 0.5 mol CH 约含有 个CH,其标
4 4
准状况的气体体积 。
(4) 0.2molAl含有 个铝原子,质量
是 。
2.(2021学年桂林市临桂区高二月考)①6gH 分子、②2molNH 分子、③4℃时9mLH O
2 3 2
分子(1g/mL)、④1.505×1023个HSO 分子、⑤标准状况下33.6LO 分子。
2 4 2
(1)其中分子数量最多的是___,分子数由少到多的顺序是___。
(2)质量由小到大的顺序是___。
【答案】① ④<③<⑤<②<① ①<③<④<②<⑤
【解析】
①6gH 分子的分子数为: =1.806×1024,②2molNH 分子的
2 3
分子数为2×6.02×1023=1.204×1024,质量为2mol×17g/mol=34g,③4℃时9mLH O分子
2
(1g/mL)的质量为9mL×1g/mL=9g,分子数为: =3.01×1023,
④1.505×1023个HSO 分子的质量为 =24.5g,⑤标准状况下
2 4
33.6LO 分子的分子数为: =9.03×1023,质量为:
2=48g,据此分析解题:
(1)由分析可知,其中分子数量最多的是①,分子数由少到多的顺序是④<③<⑤<②<
①,故答案为:①;④<③<⑤<②<①;
(2)由分析可知,质量由小到大的顺序是①<③<④<②<⑤,故答案为:①<③<④<
②<⑤。
3.根据 进行相关计算
【典例精析】
根据所学知识填空(N 表示阿伏加德罗常数):
A
(1)0.2 mol Cl 含有_______mol Cl。
2
(2)1.5 mol H O中,氢原子与氧原子个数之比为_______,质量比为_______。
2
(3)1.204×1022个CO 分子,含O的质量为_______。
2
(4)1 mol OH-中含有_______mol 电子。
(5)同温同压下,同体积的N 和SO 分子数之比为_______,物质的量之比为_______,质
2 2
量之比为_______。
【答案】0.4 2:1 1:8 0.64g 10 1:1 1:1 7:16
【解析】
(1)0.2mol Cl 含有Cl的物质的量为:0.2mol×2=0.4mol,故答案为:0.4;
2
(2)1.5mol HO中氢原子与氧原子个数之比为2:1;含有H、O的质量之比=(2×1):
2
(1×16)=1:8,故答案为:2:1;1:8;
(3)1.204×1022个CO 分子的物质的量为: ,含有O的物质的量
2
为:0.02mol×2=0.04mol,含有O的质量为16g/mol×0.04mol=0.64g,故答案为:0.64g;
(4)1个OH-中含有的电子数为8+1+1=10,则1mol OH-中含有电子的物质的量为
1mol×10=10mol,故答案为:10;
(5)同温同压下,同体积的N 和SO 分子数之比为等于物质的量之比,等于体积之比,等
2 2于1:1;质量之比等于摩尔质量之比,等于28:64=7:16,故答案为:1:1;1:1;7:16。
【基础题】
1.(2020学年楚雄高一上学期月考)C、N、O、S、H、Na都是中学化学中常见的元素。
按要求完成下列填空。
(1)2molC HO分子中含___________mol碳原子、___________个氢原子。
2 6
(2)0.5molHSO 分子的质量为___________;0.1N 个Al (SO ) 所含SO 的物质的量为
2 4 A 2 4 3
___________,
(3)等物质的量的NH 和N 两种气体,所含原子数之比为___________,等质量的NH 和
3 2 3
N 物质的量之比为___________。
2
(4)24.8gNa R含Na+0.8mol,则NaR物质的量为___________,摩尔质量为___________。
2 2
(5)现有ag某气体,该气体分子为双原子分子。它的摩尔质量为bg·mol-1.若阿伏加德罗常
数用N 表示,则:
A
①该气体的物质的量为___________mol;
②该气体所含原子总数为___________个。
【答案】4 12N 49g 0.3mol 2:1 28:17 0.4mol 62g/mol
A
【解析】
(1) 1个C HO分子中含有2个C原子、6个氢原子,2molC HO分子中含4mol碳原子、
2 6 2 6
2mol ×6×N =12N 个氢原子。
A A
(2)0.5molHSO 分子的质量为0.5mol×98g/mol=49g;0.1N 个Al (SO ) 含0.3N 个SO ,
2 4 A 2 4 3 A
SO 的物质的量为 mol;
(3)等物质的量的NH 和N 两种气体,所含原子数之比为(n×4×N ):( n×2×N )=2:1;等质量
3 2 A A的NH 和N 物质的量分别是 、 ,物质的量之比为 :
3 2
=28:17。
(4)1个 NaR中含有2个Na+,24.8gNa R含Na+0.8mol,则NaR物质的量为0.4mol,摩
2 2 2
尔质量为 ;
(5)①ag某气体,摩尔质量为bg·mol-1,该气体的物质的量为 ;
②该气体分子为双原子分子,所含原子总数为 个。
2.(2021学年西安交通大学苏州附属中学高一上学期月考)按要求完成下列填空:
(1)0.6molHS与0.3molNH 的质量比______
2 3
(2)标准状况下,aLCO 中含有b个氧原子,则阿伏加德罗常数为_______。
2
(3)某金属氯化物MCl 40.5g,含有0.6molCl-,则金属M的相对原子质量为_______。
2
(4)为测定KSO 溶液的浓度,取25.00mL待测液,向其中加入过量的BaCl 溶液,充分反
2 4 2
应后过滤、洗涤并干燥,得到BaSO 沉淀1.165g。则KSO 的物质的量浓度为_____
4 2 4
(5)人造空气(氧气O 与He的混合气体)可用于减轻某些病痛或供深水潜水员使用,在标准
2
状况下,5.6L“人造空气”的质量是2.4g,其中氧气与氦气的物质的量之比是_____
【答案】4:1 mol-1 64 0.2 mol/L 1:4
【解析】
(1) H S的分子量是34 g/mol ,NH 的摩尔质量是17g/mol,则0.6molHS与0.3molNH 的
2 3 2 3
质量比 =4:1。(2)标准状况下,aLCO 其物质的量是 ,则氧原子物质的量是 ,由公式
2
n= 可得N = = = = mol-1。
A
(3) 某金属氯化物MCl ,含有0.6molCl-,则氯化物MCl物质的量也为0.3mol,则
2
M(MCl)= = =135g/mol,则金属M的相对原子质量=135-71=64。
(4) BaSO 沉淀1.165g,其物质的量为0.005 mol,根据硫酸根离子守恒,可知KSO 的物
4 2 4
质的量为0.005 mol,则c(0.005 mol)= =0.2 mol/L。
(5) 标准状况下,5.6L“人造空气”的物质的量是0.25 mol,混合气体由O 与He组成,设
2
其中氧气物质的量为a,氦气物质的量为b,则由题目条件可列一个二元一次方程组,
,解的a=0.05,b=0.2,则a:b=1:4。
4.结合氧化还原反应知识与N 的相关计算
A
【典例精析】
含2molH SO 的浓硫酸与足量的铜片在加热条件下完全反应,可产生N 个SO 气体分子
2 4 A 2
___
【答案】错
【解析】铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O,随着反应的进行,浓硫酸变成了稀硫酸,稀硫酸与铜不反应,所以
4 2 2
生成气体为SO 分子数小于N ,故判据错误;
2 A
【基础题】
1.50 mL 12 mol·L-1盐酸与足量MnO 共热, 转移的电子数为0.3N ___
2 A
【答案】错
【解析】
随着反应的进行,盐酸的浓度逐渐变小,稀盐酸与二氧化锰不反应,故50 mL 12 mol·L-1
盐酸与足量MnO 共热, 转移的电子数小于0.3N ,故答案为:错。
2 A
2.(2021年高考化学经典小题)0.1 mol Fe 与0.1 mol Cl 充分反应,转移的电子数为0.3
2
N ___
A
【答案】错
【解析】
铁与氯气反应的产物为FeCl ,0.1 mol Fe 与0.1 mol Cl 充分反应,铁过量,氯气完全反应,
3 2
只能按Cl 计算转移的电子数,转移的电子数为0.2N ,故答案为:错。
2 A
3.(2021年高考化学经典小题)NaO 与过量CO 反应时,生成0.1mol O 时,转移的电子
2 2 2 2
数为0.4N ___
A
【答案】错
【解析】
NaO 与过量CO 反应时,NaO 既是氧化剂,又是还原剂,放出的O 由过氧化钠中的氧
2 2 2 2 2 2
而来,当生成0.1 mol O 时,应转移电子数0.1×2N ,故错误。
2 A
4.(2021年高考化学经典小题)0.2 mol Cl 溶于等体积水中,转移电子数为0.2N ___
2 A
【答案】错
【解析】
氯气溶于水,只有一部分氯气与水反应生成盐酸和次氯酸,且该反应是一个可逆反应,
因此转移的电子数比0.2N 小得多,故答案为:错。
A5.结合物质结构基础知识与N 的相关计算
A
【典例精析】
常温常压下,1mol碳烯(:CH )所含的电子数为8N ___
2 A
【答案】对
【解析】
1个碳烯(:CH)所含的电子数为6+2=8,1mol碳烯(:CH)所含的电子数为8N ,故判据
2 2 A
正确。
【基础题】
1.1molC H 中含共价键的数目为30N ___
10 22 A
【答案】错
【解析】
烷烃的通式为C H ,1mol C H 含有共价键的量为(3n+1)mol;所以1molC H 中含共
n 2n+2 n 2n+2 10 22
价键的量为31mol,共价键的数目为31N ,故判据错误。
A
2.(2021年高考化学经典小题)31g白磷分子中,含有的共价单键数目是N 个___
A
【答案】错
【解析】
白磷分子式为P,则31g白磷的物质的量为 ,一个白磷分子含有6
4
个P—P键。所以31g白磷分子中含有 P—P键,故答案为:错。
3.(2021年高考化学经典小题)60 g SiO 晶体中含有硅氧键的数目为2N ___
2 A
【答案】错
【解析】
二氧化硅晶体中,每个硅原子与4个氧原子形成了4个硅氧键,二氧化硅的摩尔质量为
60g/mol,60 g SiO 晶体的质量为1mol,所以1mol SiO 晶体含有4 mol的硅氧键,数目为
2 2
4N ,故判据错误。
A
4.(2021年高考化学经典小题)12 g金刚石中含有化学键的数目为4N ___
A
【答案】错【解析】
金刚石中每一个碳原子有四条C-C共价键,每个碳碳键被2个碳原子共用,即一个碳原
子只形成2个共价键,12 g金刚石中含有1molC,因此12g金刚石中含有化学键的数目为
2N ,故答案为:错。
A
6.以 为中心有关基本粒子的计算
【典例精析】
(1)一个H SO 含_______个H,_______个O,_______个S
2 4
(2)1molH SO 含_______molH,_______molO,_______molS
2 4
(3)1.5molHO含_______molH,_______molO
2
(4)2molNa SO 中含Na+_______mol,含_______molSO
2 4
【答案】2 4 1 2 4 1 3 1.5 4 2
【解析】
(1)由物质组成可知,一个HSO 含2个H,4个O,1个S;
2 4
(2)1molH SO 含H 为1mol×1=1mol,O为1mol×4=4mol,S为1mol×1=1 mol;
2 4
(3)1.5molHO含H为1.5mol×2=3mol,O为1.5mol×1=1.5mol;
2
(4)2molNa SO 中含Na+为2mol×2=4mol,含SO 为2mol×1=2mol;
2 4
【基础题】
1.2molCO 的质量为___g,含分子数约为___N 个,在标准状况下所占的体积约为
2 A
___L,含氧原子的物质的量为___mol。
【答案】88 2 44.8 4
【解析】
2molCO 的质量为 ;含分子数约为 个;在标准
2
状况下所占的体积约为 ;含氧原子的物质的量为
;故答案为:88;2;44.8;4。2.(2021学年莆田市涵江区高二上学期期中)填写下列表格
物质 分子数 质量/g 物质的量/mol 摩尔质量/gmol-1
O _______ 16 ______ ______
2
HCl 3.01×1023 _____ _______ _______
HO _______ _____ 1.5 _______
2
【答案】3.01×1023 0.5 32 18.25 0.5 36.5 9.03×1023 27 18
【解析】
根据O 的分子式,氧气的摩尔质量为16g/mol×2=32g/mol,16g氧气的物质的量为
2
=0.5mol,则含有的分子数目N(O )=n∙N =0.5mol×6.02×1023=3.01×1023;
2 A
HCl的摩尔质量为36.5g/mol,3.01×1023个HCl分子的物质的量=
=0.5mol,其质量m=nM=0.5mol×36.5g/mol=18.25g;
水的摩尔质量为18g/mol,1.5mol水的质量为1.5mol×18g/mol=27g,水分子的数目
N(H O)=n∙N =1.5mol×6.02×1023/mol=9.03×1023。
2 A
7.化学方程式计算中物质的量的运用
【典例精析】
2.4 g镁与100 mL稀盐酸完全反应,反应前后溶液体积的变化忽略不计。
求:(1)产生的气体在标准状况下的体积___________________________。
(2)反应完全后,所得溶液中镁离子的物质的量浓度___________________________。
【答案】2.24L 1mol/L
【解析】
(1)2.4g Mg 的物质的量为 =0.1mol,设产生的氢气在标准状况下的体积为V,则:所以V= ×22.4L=2.24L,
答:生的氢气在标准状况下的体积为2.24L;
(2)溶液中n(Mg2+)=n(Mg)=0.1mol,溶液体积为100mL,故c(Mg2+)= =1mol/L,
答:溶液中镁离子的物质的量浓度为1mol/L。
【基础题】
1.(2021学年钦州市高一上学期期末)现有1.92g铜与足量的稀硝酸反应,回答以下问题。
(1)写出反应的离子方程式______。
(2)计算生成标准状况下气体的体积和被还原硝酸的物质的量______。
【答案】 ;
【解析】
(1)铜和稀硝酸反应,生成硝酸铜、NO和水,反应的化学方程式为:
3Cu+8HNO (稀)=3Cu(NO)+2NO↑+4HO,HNO 和Cu(NO ) 都是可溶于水的强电解质,
3 3 2 2 3 3 2
可以写成离子,离子方程式为:3Cu+8H++2 =3Cu2++2NO↑+4HO。
2
(2)1.92g铜的物质的量为 =0.03mol。根据反应的化学方程式可知,消耗3mol铜
生成2molNO,则消耗0.03molCu生成0.02molNO,标准状况下NO的体积为
0.02mol×22.4L/mol=0.448L;根据反应的化学方程式,当有3molCu参加反应时,消耗
8molHNO,其中只有2molHNO 发生了化合价的变化,即只有2molHNO 被还原,所以
3 3 3
当0.03molCu参加反应时,被还原的硝酸的物质的量为0.02mol。
2.(2021学年武冈市高一下学期开学考试)浓硫酸和铜在加热时反应,生成二氧化硫气体的体积为3.36L(标准状况下)。请回答下列问题:
(1)请写出该反应的化学方程式________;
(2)计算反应中消耗的铜的质量________;
(3)将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是__________。
【答案】Cu+2H SO (浓) CuSO +SO↑+2H O 9.6g 0.3mol/L
2 4 4 2 2
【解析】
(1)浓硫酸和铜在加热时反应,生成二氧化硫,反应的化学方程式:Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O;
4 2 2
(2)根据关系式: ,解得m=9.6g,则消耗铜的质量是9.6g;
(3)根据关系式: ,解得n=0.15mol/L,配制成500mL的溶液,则
该溶液中溶质的物质的量浓度是 。
二、与物质的量浓度有关的计算
1.依据物质的量浓度公式的基本计算
【典例精析】
将12gNaOH固体溶于水配成150mL溶液,其物质的量浓度为
A.0.1mol/L B.0.5mol/L C.2mol/L D.1mol/L
【答案】C
【解析】12gNaOH的物质的量n(NaOH)= =0.3mol,根据
=2mol/L,故选C。
【基础题】
1.将10mol/L的盐酸溶液10mL ,加水稀释至100mL ,再取出10mL ,此时该盐酸溶液
的浓度是( )
A.10mol/L B.5mol/L C.1mol/L D.0.5mol/L
【答案】C
【解析】
根据c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液),10mL10mol/L的盐酸溶液加水稀释到
100mL,所得盐酸溶液物质的量浓度为 =1mol/L,从稀释液中取出
10mL,取出溶液的物质的量浓度仍为1mol/L;
故答案选C。
2.(2021学年莆田高一上学期第二次月考)关于1L1mol·L-1NaSO 溶液,下列说法正确的
2 4
是(N 表示阿伏加德罗常数的值)
A
A.Na+的数目为N
A
B.溶液中Na+质量为23g
C.SO 的物质的量浓度为1mol·L-1
D.SO 物质的量为2mol
【答案】C
【解析】
A.Na+的数目为1L×1mol·L-1×2×N mol-1=2N ,A错误;
A A
B.溶液中Na+质量为1L×1mol·L-1×2×23g/mol=46g,B错误;C.1L1mol·L-1NaSO 溶液含有SO 的物质的量为:1L×1mol·L-1=1mol,故SO 的物质
2 4
的量浓度为 =1mol·L-1,C正确;
D.1L1mol·L-1NaSO 溶液含有SO 的物质的量为:1L×1mol·L-1=1mol,D错误;
2 4
故答案为:C。
2.与溶质成分有关的计算
【典例精析】
下列溶液中氯离子浓度与50 mL 1 mol/L AlCl 溶液中氯离子浓度相等的是
3
A.150 mL 1 mol/L的NaCl溶液 B.150 mL 3 mol/LNHCl溶液
4
C.75 mL 2 mol/L的NH Cl溶液 D.75 mL 1 mol/L CuCl 溶液
4 2
【答案】B
【解析】
A.150 mL 1 mol/L的NaCl溶液中氯离子浓度为1 mol/L×1=1mol/L,与题意不相符,故A
不选;
B.150 mL 3 mol/LNHCl溶液中氯离子浓度为3 mol/L×1=3mol/L,与题意相符,故B选;
4
C.75 mL 2 mol/L的NH Cl溶液中氯离子浓度为2mol/L×1=2mol/L,与题意不相符,故C
4
不选;
D.75 mL 1 mol/L CuCl 溶液中氯离子浓度为1mol/L×2=2mol/L,与题意不相符,故D不
2
选;
故选B。
【基础题】
1.(2020学年南平市浦城县高一上学期第一次月考)下列溶液中Cl- 浓度由小到大的顺序是
①200mL 2mol/L MgCl 溶液 ② 1000mL 2.5mol/L NaCl溶液 ③300mL 5mol/L KCl
2
溶液 ④ 250mL 1mol/L AlCl 溶液。
3
A.③①④② B.④①③② C.②④①③ D.④①②③【答案】A
【解析】
①200mL 2mol/L MgCl 溶液中c(Cl-)=2mol/L×2=4mol/L;
2
②1000mL 2.5mol/L NaCl溶液中c(Cl-)=2.5mol/L;
③300mL 5mol/L KCl溶液中c(Cl-)=5mol/L;
④250mL 1mol/L AlCl 溶液中c(Cl-)=1mol/L×3=3mol/L;
3
综上所述,c(Cl-)由大到小的顺序为③①④②,答案为A。
2.(2021学年江苏省震泽中学高一上学期月考)欲使1L0.5 mol·L-1 NaOH溶液的浓度增大
一倍, 可采取的合理措施是
A.加入20g固体NaOH,搅拌、溶解
B.将溶液加热浓缩至0.5 L
C.加入1L1.5 mol·L-1的NaOH溶液混合均匀
D.加入10 mol·L-1 NaOH溶液0.1L,再稀释至1.5L
【答案】BD
【解析】
A.加入20g固体NaOH,搅拌、溶解,由于溶解后的溶液体积会发生变化,NaOH的物
质的量为1mol,但是溶液的体积不是1L,所以浓度不是1mol/L,A不符合题意;
B.将溶液加热浓缩至0.5L,物质的量不变,溶液体积缩小一半,所以物质的量浓度增大
一倍,B符合题意;
C.加入1L1.5mol/L的NaOH溶液混合均匀,混合液的体积不是2.5L,故所得溶液的浓
度不是1mol/L,C不符合题意;
D.加入10mol/L的NaOH溶液0.1L,再稀释至1.5L,此时溶液中NaOH的浓度c=
=1mol/L,浓度是原来的两倍,D符合题意;
故选BD。
3.溶液配制有关计算
【典例精析】实验中需0.2 mol/L的NaCO 溶液950 mL,配制时应选用的容量瓶的规格和称取
2 3
NaCO·10H O的质量分别是
2 3 2
A.1000 mL,21.2 g B.950 mL,54.34 g
C.1000 mL,57.2 g D.950 mL,20.14 g
【答案】C
【解析】
在实验室中没有规格是950 mL的容量瓶,根据选择仪器的标准是“大而近”的原则,应
该选择使用1000 mL的容量瓶。配制1000 mL的0.2 mol/L的NaCO 溶液,需要溶质的物
2 3
质的量n(Na CO)=0.2 mol/L×1 L=0.2 mol,根据C元素守恒,可知需NaCO·10H O的物
2 3 2 3 2
质的量是0.2 mol,其质量m(Na CO·10H O)=0.2 mol×286 g/mol=57.2 g,故合理选项是
2 3 2
C。
【基础题】
1.(2020学年长沙市第一中学高一上学期期中)下列说法正确的是
A.用浓硫酸配制一定物质的量浓度的稀硫酸时,量取浓硫酸时仰视量筒,会使所配溶液
浓度偏小
B.配制 的 溶液 ,则用托盘天平称量
C.同温同压下 和 所含的原子数之比为5∶6
D.镁原子的摩尔质量等于它的相对原子质量
【答案】C
【解析】
A.仰视时所量取的浓硫酸的体积偏大,所以所配制的溶液浓度偏大,故A错;
B.无480mL的容量瓶,所以应选择500mL的容量瓶,则计算时也按500mL进行计算,
则 ,故B错;
C.同温同压下气体的体积之比等于物质的量之比即,由于甲烷为5原子分子,氧
气为双原子分子,所以原子个数之比 ,故选C;
D.摩尔质量的单位为g/mol,而相对原子质量无单位,所以摩尔质量在以g/mol为单位
时,镁原子的摩尔质量在数值等于它的相对原子质量,故D错;
答案选C。
2.(浙江新东方)实验室欲配制480 mL0.5 mol/L的CuSO 溶液,据此回答下列问题:
4
(1)需称量胆矾CuSO ·5H O___________g。
4 2
(2)从配制好的CuSO 溶液中取出10 mL,将这10 mL的CuSO 溶液稀释至100 mL,稀释
4 4
后CuSO 溶液的浓度变为___________mol/L。
4
【答案】62.5 0.05
【解析】
实验室欲配制480 mL0.5 mol/L的CuSO 溶液,根据容量瓶的规格,应该配制500mL溶
4
液;
需称量胆矾的质量为 ,故答案为
62.5g;
根据稀释前后溶质的物质的量不变,可得 ,
故答案为:0.05mol/L;
4.溶液稀释的有关计算
【典例精析】
取2 mol/L的NaCl溶液10 mL稀释到50 mL,从中取出5 mL,这5 mL溶液中溶质的物质
的量浓度为
A.0.4 mol/L B.0.04 mol/L C.0.2 mol/L D.0.002 mol/L
【答案】A
【解析】溶液在稀释前后溶质的物质的量不变,将2 mol/L的NaCl溶液10 mL稀释到50 mL,稀
释后溶液的物质的量浓度c= 。溶液具有均一性,溶液各处的
浓度相等,因此从稀释后的溶液中取出50 mL溶液,其物质的量浓度为0.4 mol/L,故合
理选项是A。
【基础题】
1.(浙江新东方)将 溶液加水稀释至 ,稀释后 的物
质的量浓度为
A. B. C. D.
【答案】A
【解析】
1 mol·L-1NaSO 溶液中c(Na+)=2mol/L,将溶液稀释10倍后,c(Na+)变为原来的 ,故稀
2 4
释后Na+的物质的量浓度为0.2mol/L,答案选A。
2.(2021学年张家口市张垣联盟高一上学期12月阶段检测)将200 mL 1.5 mol·L-1 Fe (SO )
2 4 3
溶液稀释至1000 mL,稀释后SO 的物质的量浓度是
A.0.015 mol·L-1 B.0.045 mol·L-1 C.0.30 mol·L-1 D.0.90 mol·L-1
【答案】D
【解析】
200 mL 1.5 mol·L-1 Fe (SO ) 溶液稀释至1000 mL,稀释后Fe (SO ) 的浓度是
2 4 3 2 4 3
mol·L-1,根据化学式Fe (SO ),稀释后SO 的物质的量浓
2 4 3度是0.3 mol·L-1×3=0.90 mol·L-1,故选D。
5.溶液混合的有关计算
【典例精析】
已知17mol·L-1氨水的密度为0.92g·cm-3,3mol·L-1氨水的密度为0.98g·cm-3,若将上述两溶
液等质量混合,所得氨水溶液的物质的量浓度为
A.等于10mol·L-1 B.大于10mol·L-1 C.小于10mol·L-1 D.无法判断
【答案】B
【解析】
已知17mol·L-1氨水的密度为0.92g·cm-3,3mol·L-1氨水的密度为0.98g·cm-3,则等质量时密
度大的氨水体积小,设17mol·L-1氨水的体积为V,3mol·L-1氨水的体积为V,则
1 2
,若将上述两溶液等质量混合,则所得氨水溶液的体积 ,可看成是按以下
方式混合的:先各取VmL2种氨水混合得10 mol·L-1的氨水、再加入(V -V ) mL的
2 1 2
17mol·L-1氨水,则混合的结果为大于10mol·L-1,B正确;
答案选B。
【基础题】
1.(2021学年晋城市陵川县高一下学期开学考试)取 100 mL 0.3 mol/L 的硝酸和300 mL
0.25 mol/L的硫酸注入 500 mL的容量瓶中,加水稀释至刻度线,该混合溶液中 H+ 的物
质的量浓度是
A.0.18 mol/L B.0.36 mol/L C.0.2 mol/L D.0.4 mol/L
【答案】B
【解析】
100 mL 0.3 mol/L 的硝酸中硝酸的物质的量为0.1L ×0.3 mol/L=0.03mol,300 mL 0.25 mol/L
的硫酸中硫酸的物质的量为0.3L×0.25 mol/L=0.075mol,则混合酸液中氢离子的物质的量
为0.03mol+0.075mol×2=0.18mol,则500 mL该混合酸液中H+ 的物质的量浓度是=0.36mol/L,答案选B。
2.(2021学年广安市高一11月月考) 的 溶液和 200mL
的 溶液混合后(不考虑混合后溶液 体积的变化),溶液中 的物质
的量浓度为
A.0.3 B.0.4 C.0.5 D.0.46
【答案】C
【解析】
100mL 0.3mol•L-1的KSO 溶液中含有溶质硫酸钾的物质的量为:0.3mol/
2 4
L×0.1L=0.03mol,含有硫酸根离子的物质的量为0.03mol;
200mL 0.2mol•L-1的Fe (SO ) 溶液中含有硫酸铁的物质的量为:0.2mol/L×0.2L=0.04mol,
2 4 3
含有硫酸根离子的物质的量为:0.04mol×3=0.12mol;
混合液中含有硫酸根离子的总物质的量为0.03mol+0.12mol=0.15mol,则混合液中硫酸根
离子的物质的量浓度为 =0.5mol/L,故选C。
【能力题】
1.(2021届辽宁省高三年级5月模拟)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,9.5g羟基(-18OH)中所含中子数为5N
A
B.常温下,密闭容器中2molNO与 充分反应,产物的分子数为2N
A
C.1mol/L的NaClO溶液中含有 的数目为N
A
D.100g46%的乙醇溶液中含有氧原子的数目为N
A
【答案】A
【解析】A.常温常压下,9.5g羟基(-18OH)为0.5mol,其中第个羟基含有9个中子,故所含中子
数为5N ,选项A正确;
A
B.存在 ,为可逆反应,故产物的分子数小于2N ,选项B错误;
A
C.没有给定体积,无法计算 的数目,选项C错误;
D.还含有水分子,氧原子的数目远大于N ,选项D错误。
A
答案选A。
2.(2021届泰安市高三高考全真模拟)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.36g40Ar中含有的质子总数为18N
A
B.0.4gN H 与6gCHOH的混合物中含有的共价键总数为N
2 4 3 A
C.0.1mol·L-1的HS溶液中HS、HS-和S2-的总数为0.1N
2 2 A
D.标准状况下,22.4LH O 催化分解产生的O 的分子数为0.5N
2 2 2 A
【答案】B
【解析】
A. 36g40Ar中含有的质子总数为 =16.2N ,A错误;
A
B. 0.4gN H 与6gCHOH的混合物中含有的共价键总数为
2 4 3
=N ,B正确;
A
C. 未告知溶液的体积,故无法计算出0.1mol·L-1的HS溶液中HS、HS-和S2-的总数,C
2 2
错误;
D. 标准状况HO 是无色液体,故无法计算标准状况下,22.4LH O 催化分解产生的O 的
2 2 2 2 2
分子数,D错误;
故答案为:B。
3.(2021届鹰潭市高考二模)设N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.球碳盐KC 中阴阳离子个数比为1:3
3 60B.标准状况下,46gNO 气体中所含的分子数为
2
C.32g铜与足量硫单质完全反应,转移电子数为N
A
D.22.4L Cl 和CO的混合气体中含有的原子数为2N
2 A
【答案】A
【解析】
A.球碳盐KC 中存在阳离子为K+、阴离子为C ,则阴阳离子个数比为1:3,A说法
3 60
正确;
B.NO 气体中存在2NO ⇌ NO,则标准状况下,46gNO 气体中所含的分子数小于
2 2 2 4 2
N ,B说法错误;
A
C.32g铜与足量硫单质完全反应,Cu的化合价由0价变为+1价,则转移电子数为
0.5N ,C说法错误;
A
D.标况下,22.4L Cl 和CO的混合气体的物质的量为1mol,含有的原子数为2N ,未给
2 A
定气体状态,则原子数不能确定,D说法错误;
答案为A。
4.(2021届大连市高三第二次模拟)设N 表示阿伏加德罗常数的值。下列说法正确的是
A
A.14g聚丙烯中含C—H键总数目为2N
A
B.常温下,pH=13的NaOH溶液中含有的OH-数目为0.1N
A
C.标准状况下:2.24LNO与1.12LO 混合后的气体分子数为0.1N
2 A
D.电解精炼铜时,若阳极质量减少64g,则阴极得到电子的数目为2N
A
【答案】A
【解析】
A.聚丙烯的最简式为CH,14g聚丙烯中含H: ,所有H
2
均与C以单键相连,所以C-H键总数目为2N ,A正确;
A
B.没有提供溶液体积,无法计算OH-数目,B错误;C.两者发生反应2NO+O=2NO,2NO NO,标准状况下2.24LNO与1.12LO 混合
2 2 2 2 4 2
后气体分子的物质的量小于0.1mol,气体分子数应小于0.1N ,C错误;
A
D.电解精炼铜时,阳极溶解的除了Cu还有比Cu活泼的金属,所以若阳极质量减少
64g,则阴极得到电子的数目不为2N ,D错误;
A
故选A。
5.(2021年高考化学押题预测卷)捕获二氧化碳生成甲酸的过程如图所示。下列说法错误
的是(N 为阿伏加德罗常数的值)
A
A.二氧化碳的电子式:
B.在第一步“捕获”过程中CO 的共价键并没有断裂
2
C.100g46%的甲酸水溶液中所含的氢原子数目为2N
A
D.理论上捕获1mol CO 生成甲酸转移的电子数为2N
2 A
【答案】C
【解析】
A.二氧化碳中每个原子均为8电子稳定结构,并且C原子与氧原子以双键连接,故二氧
化碳的电子式为 ,A项正确;
B.由图可知,二氧化碳中的共价键在第一步“捕获”过程中并没有断裂,B项正确;
C.100g46%的甲酸水溶液中,含甲酸的物质的量为 ,故甲
酸中所含的氢原子数目为2N ,但是甲酸水溶液中含有水,水中含有H原子,故
A100g46%的甲酸水溶液中所含的氢原子数目大于2N ,C项错误;
A
D.由化合价变化可知二氧化碳转化为甲酸,碳原子由+4价变为+2价,故捕获1mol CO
2
生成甲酸转移的电子数为2N ,D项正确;
A
答案选C。
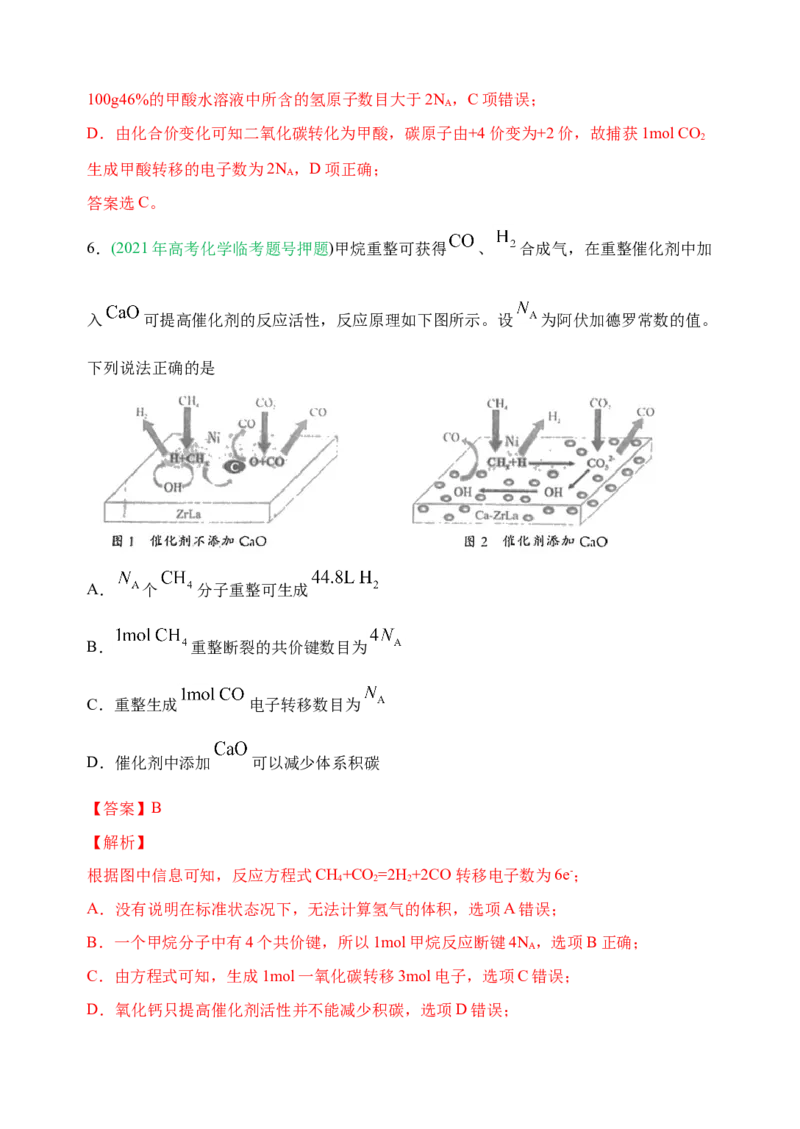
6.(2021年高考化学临考题号押题)甲烷重整可获得 、 合成气,在重整催化剂中加
入 可提高催化剂的反应活性,反应原理如下图所示。设 为阿伏加德罗常数的值。
下列说法正确的是
A. 个 分子重整可生成
B. 重整断裂的共价键数目为
C.重整生成 电子转移数目为
D.催化剂中添加 可以减少体系积碳
【答案】B
【解析】
根据图中信息可知,反应方程式CH+CO =2H +2CO 转移电子数为6e-;
4 2 2
A.没有说明在标准状态况下,无法计算氢气的体积,选项A错误;
B.一个甲烷分子中有4个共价键,所以1mol甲烷反应断键4N ,选项B正确;
A
C.由方程式可知,生成1mol一氧化碳转移3mol电子,选项C错误;
D.氧化钙只提高催化剂活性并不能减少积碳,选项D错误;答案选B。
7.(2021届宁波市高三下学期高考适应性考试(二模))硫粉和 溶液反应可以生成
多硫化钠( ),离子反应为: 、 …
(1)在 溶液中加入 硫粉,只发生 ,反应后溶液中 和
无剩余,则原 _______ 。
(2)在一定体积和浓度的 溶液中加入 硫粉,控制一定条件使硫粉完全反应,反
应后溶液中的阴离子有 、 、 (忽略其他阴离子),且物质的量之比为 。
则反应后溶液中的 _______ 。(写出计算过程)
【答案】0.25 0.1
【解析】
(1) 硫粉的物质的量为 =0.025mol,只发生 ,则
, 0.25 ;
(2) , ,根据 , ,
,
, 。
8.(上海市崇明县高考二模)已知:硝酸铜受热易分解。170℃时,2Cu(NO )
3 22CuO+4NO ↑+O ↑开始分解,至250℃分解完全。(其中2NO NO,2NO
2 2 2 2 4 2
2NO+O 等反应忽略不计)。
2
800℃时,4CuO 2Cu O+O↑ 开始分解,至1000℃以上分解完全。
2 2
(1)取5.64 g无水硝酸铜,加热至1000℃以上,将生成的气体导入足量的NaOH溶液充分
吸收后,还有逸出的气体是____(填分子式),体积(标准状况)为______;将吸收液
加水稀释到100 mL,此溶液中NO -的物质的量浓度为_____________。
3
(2)取5.64 g无水硝酸铜加热至某温度分解后的残留固体中含有1.60 g CuO,则残留固体的
质量可能是_________。实验证明,当温度达到1800℃时,Cu O也会发生分解:2Cu O
2 2
4Cu+O ↑。
2
(3)取8.00 g CuO,加热到1800℃左右,冷却后称得质量为6.88 g,通过计算求出反应后剩
余固体中各成分的物质的量之比________________。
(4)取8.00 g CuO,通入一定量H 并加热,使其部分还原为Cu和Cu O,且其中n(Cu O):
2 2 2
n(Cu)=x。将此混合物溶于足量的稀硫酸中(Cu O+2H+=Cu+Cu2++H O),充分反应后过滤得
2 2
到Cu y g,试求未被还原的CuO的物质的量(用含x、y的代数式表示)。_________
【答案】O 0.168 L 0.6 mol/L 3.48 g或2.32 g n(Cu O):n(Cu)=3:4 n(CuO)=0.1-
2 2
【解析】
(1)5.64g无水硝酸铜物质的量为n[Cu(NO )]= =0.03 mol,无水硝酸铜分解生成
3 2
CuO时,生成的NO 与O 恰好与水完全反应,多余的气体为CuO分解生成的氧气,由
2 2
Cu元素守恒可知n(CuO)= n[Cu(NO )]=0.03 mol,根据方程式中物质关系4CuO~O 可知,
3 2 2n(O )=0.03 mol× =0.0075 mol,所以标准状况下氧气的体积为0.0075 mol×22.4
2
L/mol=0.168 L,由N元素转化关系可知,5.64g无水硝酸铜中含有的NO -等于溶液中含有
3
的NO -,故溶液中n(NO -)=0.03 mol×2=0.06 mol,故稀释后溶液中c(NO -)= =0.6
3 3 3
mol/L;
(2)残留固体可能是CuO和Cu O的混合物,也可能是CuO和Cu(NO ) 的混合物。若为
2 3 2
CuO和Cu O的混合物,则n(CuO)= =0.02 mol,根据Cu元素守恒可得:
2
n(CuO)+2n(Cu O)=0.03 mol,所以n(Cu O)=0.005 mol,故m(Cu O)=144 g/mol×0.005
2 2 2
mol=0.72 g,m(残留固体)=1.60 g+0.72 g=2.32 g;若为CuO和Cu(NO ) 的混合物,则
3 2
n(CuO)=0.02 mol,则n(CuO)+n[Cu(NO )]=0.03 mol,n[Cu(NO )]=0.01 mol,
3 2 3 2
m[Cu(NO )]=0.01 mol×188 g/mol=1.88 g,m(残留固体)=1.60 g+1.88 g=3.48 g;
3 2
(3)取8.00 gCuO,加热到1800℃左右,冷却后称得质量为6.88 g,则生成的氧气的质量为
8 g-6.88 g=1.12 g,8 gCuO中O元素质量为8 g× =1.6g>1.12g,则CuO未完全转化为
Cu,剩余固体中O元素质量为1.6 g-1.12 g=0.48 g,Cu元素质量为6.88 g-0.48 g=6.4 g,剩
余固体中n(Cu):n(O)= : =10:3,故剩余固体为Cu、Cu O, n(Cu O)=n(O)=
2 2
=0.03 mol,n(Cu)= -0.03 mol×2=0.04 mol,故n(Cu O):
2n(Cu)=0.03mol:0.04mol=3:4;
(4)8.00 g CuO的物质的量n(CuO)= =0.1 mol,假设氢气还原生成的Cu的
物质的量为n mol,则Cu O的物质的量分别nx mol,根据Cu O+2H+=Cu+Cu2++H O可知
2 2 2
nx molCu O反应产生Cu物质的量为nx mol,n+nx= ,则n= ,故
2
n(Cu O)=nx= ,根据铜原子守恒可知,未被还原的CuO的物质的量为
2
n(CuO)=0.1-n-2nx=0.1- -2× =0.1- 。
【提升题】
1.(2021学年白城市洮南市高一上学期第三次月考)将mg镁铝合金投入500mL 2mol•L-1的
盐酸中,固体完全溶解,收集到气体5.6L(标准状况下)。向反应所得溶液中加入
4mol•L-1的氢氧化钠溶液,沉淀质量的最大值为13.60g,则m的值为( )
A.5.10 B.8.50 C.9.35 D.11.48
【答案】A
【解析】
由关系式Mg(OH) -Mg-H -2OH-、2Al(OH) -2Al-3H -6OH-可知,n(OH-)=2n(H )=2×
2 2 3 2 2
=0.5mol,则m(OH-)=0.5mol×17g/mol=8.50g,从而得出
m=13.60g-8.50g=5.10g;故选A。
2.(2021学年白城市洮南市高一上学期第三次月考)以天然气为原料经由合成气(CO、H)
2制化学品是目前天然气转化利用的主导技术路线。制备CHOH的反应转化关系如图所示。
3
设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.用1 mol CH 理论上能生产标准状况下CHOH 22.4 L
4 3
B.等物质的量的CHOH和CH,CHOH的质子数比CH 多8N
3 4 3 4 A
C.44 g CO 气体和44 g CH 与CO的混合气体,所含C原子数均为N
2 4 A
D.用CH 制备合成气的反应中,若生成1 mol CO,反应转移电子数为3N
4 A
【答案】D
【解析】
A.CHOH在标况下不是气体,故无法得出标况下的体积是22.4 L的结论,故A错误;
3
B.1mol的CHOH和CH,一个甲醇分子含有18个质子,一个甲烷分子含有10个质子,
3 4
一个甲醇分子比一个甲烷分子多8个质子,1mol的CHOH比CH 多8N 个质子,但等物
3 4 A
质的量没给出具体的物质的量数值,故CHOH的质子数不一定比CH 多8N ,故B错误;
3 4 A
C.44 g CO 气体的物质的量为 ,一氧化碳的相对分子质量为28,
2
甲烷的相对分子质量为16,44 g CH 与CO的混合气体假设全部是CH 气体,物质的量为
4 4
>1mol,44 g CH 与CO的混合气体假设全部是CO气体,物质的量为
4
>1mol,故44 g CH 与CO的混合气体的物质的量大于1mol,所含C原子数
4
大于1mol,故C原子数大于N ,故C错误;
A
D.制备CHOH的反应过程中生成一氧化碳,发生反应:CO(g)+C(s)=2CO(g),生成
3 22mol一氧化碳时,转移2mol电子消耗1mol碳原子,消耗的碳原子来自于甲烷的分解,
CH(g)=C(s)+2H (g) ,甲烷中碳的化合价从-4价升高到0价,生成1mol碳原子转移的电
4 2
子的物质的量为4mol,要生成2mol一氧化碳共需要转移6mol电子,则若生成1 mol
CO,反应转移电子的物质的量为3mol,转移的电子数为3N ;
A
答案选D。
3.(2020届盐城市高三年级第三次(5月)模拟)NH Cl是实验室常用试剂,下列相关说
4
法正确的是
A.反应2NH Cl(s)+Ba(OH) (s)=BaCl (s)+2NH (g)+2HO(s)的△H>0,△S<0
4 2 2 3 2
B.0.1mol·L-1NH Cl溶液从15C升温到25°C时, 的值不变
4
C.反应NH Cl+NaNO =NaCl+N↑+2H O,每生成1molN 转移电子数为6×6.02×1023
4 2 2 2 2
D.常温下,K [Mg(OH) ]=1.8x10-11,K (NH ·H O)=1.8x10-5,NH Cl饱和溶液中加入少量
sp 2 b 3 2 4
Mg(OH) ,振荡,固体逐渐溶解
2
【答案】D
【解析】
A.NH Cl和Ba(OH) 的反应是吸热反应,△H>0,但是反应后气体体积增大,混乱度增
4 2
大,△S>0,A错误;
B.NH +在溶液中会水解,NH ++HO NH ·H O+H+,水解吸热,升高温度,促进
4 4 2 3 2
水解,水解平衡常数 增大,B错误;
C.反应中NH Cl中的N的化合物为-3升高到0,NaNO 中的N的化合价从+3降低到0
4 2
价,都生成N,则每转移3mol电子生成1molN ,即转移的电子数为3×6.02×1023,C错
2 2
误;
D.若Mg(OH) 和NH Cl反应,离子方程式为2NH ++Mg(OH) Mg2++2NH ·H O,
2 4 4 2 3 2
该反应的平衡常数,带
入数据, ,平衡常数较小,为可逆反应。
NH Cl饱和溶液中NH +浓度很大,可以促进反应正向进行,Mg(OH) 会溶解,D正确。
4 4 2
答案选D。
4.(2020学年长沙市长郡中学高一下学期期末)铜镁合金2.14 g完全溶于一定浓度的硝酸,
硝酸被还原成NO 、NO、NO三种气体且标准况下它们体积均为0.224 L。反应后的溶液
2 2
中加入足量氢氧化钠溶液,生成的沉淀经过滤、洗涤、干燥后称量,质量为
A.3.12 g B.4.68 g C.5.08 g D.4.18 g
【答案】D
【解析】
铜镁合金溶于一定浓度的硝酸,反应生成Mg(NO)、Cu(NO )、NO 、NO、NO和
3 2 3 2 2 2
HO,反应后的溶液中加入足量NaOH溶液所得沉淀为Mg(OH) 和Cu(OH) ,沉淀的质量
2 2 2
等于原铜镁合金的质量与OH-的质量之和;而n(NO )=n(NO)=n(N O)=
2 2
=0.01mol;铜镁合金溶于一定浓度的硝酸发生氧化还原反应,反应中铜、镁失去的电子总
物质的量等于HNO 得到的电子总物质的量,HNO 得到电子被还原成NO 、NO、NO,
3 3 2 2
则2n(Mg)+2n(Cu)=0.01mol×[(+5)-(+4)]+ 0.01mol×[(+5)-(+2)]+
0.01mol×2×[(+5)-(+1)]=0.12mol;根据沉淀的组成Mg(OH) 和Cu(OH) ,沉淀中n
2 2
(OH-)=2n(Mg2+)+2n(Cu2+)=2n(Mg)+2n(Cu)=0.12mol,m(OH-)
=0.12mol×17g/mol=2.04g;沉淀的质量为2.14g+2.04g=4.18g,答案选D。
5.(2021学年眉山市彭山区高一4月月考)将一定质量的镁和铝混合物投入200 mL硫酸中,
固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是:
A.镁和铝的总质量为9 g
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L-1
D.生成的氢气在标准状况下的体积为11.2 L
【答案】D
【解析】
A、当V(NaOH溶液)=240mL时,沉淀不再减少,此时全部为Mg(OH) ,
2
n(Mg)=n[Mg(OH) ]=0.15mol,m(Mg)=0.15mol×24g•mol-1=3.6g,
2
n(Al)=n[Al(OH) ]=0.35mol-0.15mol=0.2mol,m(Al)=0.2mol×27g•mol-1=5.4g,所以镁和铝
3
的总质量为9g,A项正确;
B、根据A中分析可知B项正确;
C、从200mL到240mL,NaOH溶解Al(OH) :NaOH+Al(OH) =NaAlO+2H O,则此过程
3 3 2 2
消耗n(NaOH)=n[Al(OH) ]=0.2mol,c(NaOH)=0.2mol÷0.04 L=5mol•L-1,在200mL时溶液
3
中只有硫酸钠,根据硫酸钠的化学式分析,硫酸的物质的量为5mol•L-1×0.2L÷2=0.5 mol,
硫酸的浓度为0.5 mol÷0.2 L =2.5 mol·L-1,C项正确;
D、由Mg+HSO =MgSO +H ↑,2Al+3H SO =2Al(SO )+3H ↑可以计算出生成
2 4 4 2 2 4 2 4 3 2
n(H )=0.45mol,标准状况下V(H )=0.45mol×22.4L•mol-1=10.08L,D项错误;
2 2
答案选D。
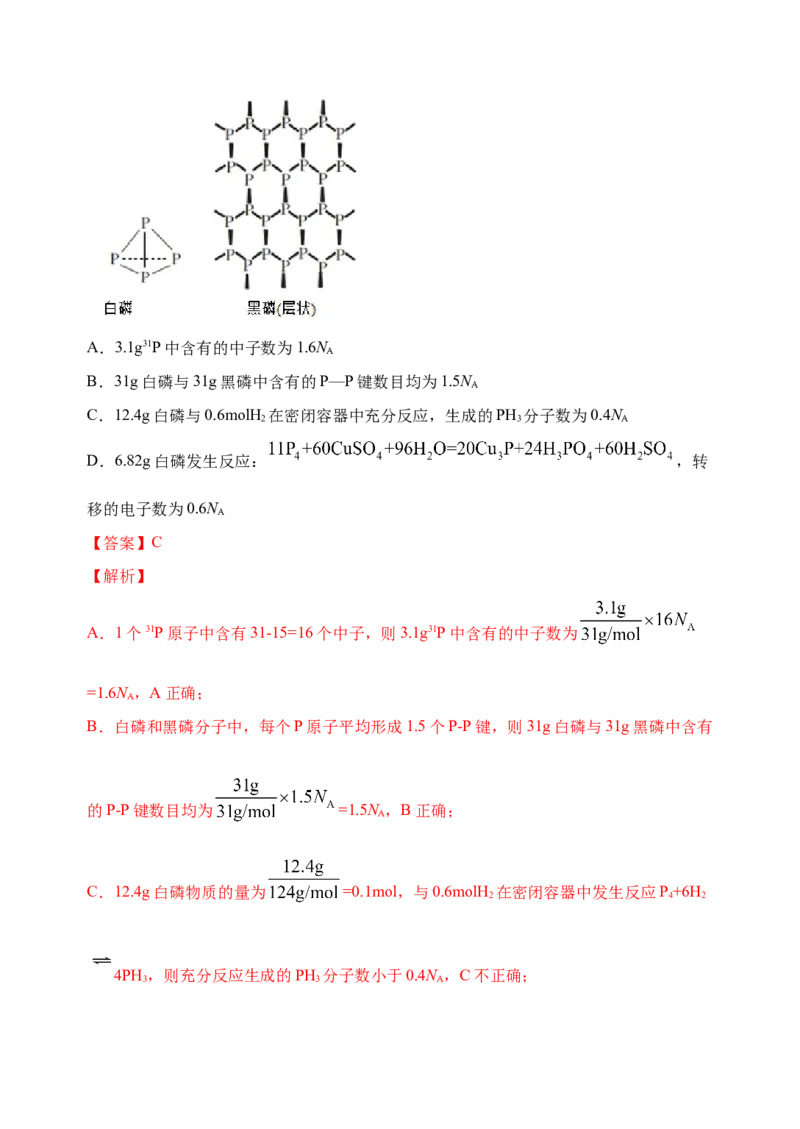
6.(2021年高考化学专练)磷有多种同素异形体,其中白磷和黑磷(每一个层由曲折的磷原
子链组成)的结构如图所示,设N 为阿伏加德罗常数的值。下列说法不正确的是
AA.3.1g31P中含有的中子数为1.6N
A
B.31g白磷与31g黑磷中含有的P—P键数目均为1.5N
A
C.12.4g白磷与0.6molH 在密闭容器中充分反应,生成的PH 分子数为0.4N
2 3 A
D.6.82g白磷发生反应: ,转
移的电子数为0.6N
A
【答案】C
【解析】
A.1个31P原子中含有31-15=16个中子,则3.1g31P中含有的中子数为
=1.6N ,A正确;
A
B.白磷和黑磷分子中,每个P原子平均形成1.5个P-P键,则31g白磷与31g黑磷中含有
的P-P键数目均为 =1.5N ,B正确;
A
C.12.4g白磷物质的量为 =0.1mol,与0.6molH 在密闭容器中发生反应P+6H
2 4 2
4PH ,则充分反应生成的PH 分子数小于0.4N ,C不正确;
3 3 AD.6.82g白磷的物质的量为 =0.055mol,反应
中,电子转移的数目为24×(5-
0)e-=120e-,则0.055molP 参加反应时转移的电子数为 =0.6N ,
4 A
D正确;
故选C。
7.(2018版考前特训)把11.6 g FeO和Fe O 的固体混合物分成等质量的两份。第一份混合
2 3
物用氢气完全还原后生成水的质量为1.80 g;第二份混合物中加入100 mL HI溶液充分反
应,在反应后的溶液中加入硫氰化钾溶液,无现象。试计算:
(1)原混合物中Fe O 的质量为________ g。
2 3
(2)HI溶液的物质的量浓度c(HI)=________。
【答案】 8.00 2.00 mol·L-1
【解析】(1)设每一份中 FeO和Fe O 的物质的量分别是xmol、ymol,则72x+160y=
2 3
11.6/2,x+3y=1.8÷18,解得x=y=0.025,因此原混合物中Fe O 的质量为
2 3
0.025mol×2×160g/mol=8.00g;(2)第二份混合物中加入100 mL HI溶液充分反应,在反
应后的溶液中加入硫氰化钾溶液,无现象,说明全部转化为碘化亚铁、单质碘和水,根
据氧原子守恒可知生成水是0.1mol,所以HI的物质的量是0.2mol,则HI溶液的物质的量
浓度c(HI)=0.2mol÷0.1L=2.00mol/L。
8. (2017届浙江省稽阳联谊学校高三8月联考)取一定质量NH HSO 和MgSO 的固体混
4 4 4
合物溶于水配成200mL溶液,向溶液中加入0.100mol/LBa(OH) 溶液,产生沉淀的质量与
2
所加Ba(OH) 的体积有如图所示关系。
2试计算:
(l)所得混合溶液中c(SO 2-)=_________。
4
(2)原固体混合物中,NH HSO 和MgSO 的物质的量之比为__________。
4 4 4
【答案】 0.200mol/L 1:1
【解析】向溶液中加入0.100mol/LBa(OH) 溶液,首先与氢离子反应,同时产生硫酸钡沉
2
淀,即0~100mL为第一阶段,发生的反应为2NH HSO +Ba(OH) =BaSO↓+
4 4 2 4
(NH )SO +2H O,硫酸钡是0.01mol,所以硫酸氢铵的物质的量是0.02mol;100~300mL
4 2 4 2
为第二阶段,此时加入的氢氧化钡与硫酸镁反应生成硫酸钡和氢氧化镁沉淀,二者形成
的沉淀质量为8.15g-2.33g=5.82g,所以硫酸镁的物质的量是5.82g÷(58+233)g/mol=
0.02mol;第三阶段为最后的100mL氢氧化钡与硫酸铵反应生成2.33g硫酸钡沉淀。则
(l)根据以上分析可知所得混合溶液中c(SO 2-)=0.04mol÷0.2L=0.200mol/L。(2)原固
4
体混合物中,NH HSO 和MgSO 的物质的量之比为0.02mol:0.02mol=1:1。
4 4 4
点睛:明确反应的原理,尤其是反应的先后顺序是解答的关键。注意掌握图像的答题技
巧:①看面:弄清纵、横坐标的含义。②看线:弄清线的变化趋势,每条线都代表着一
定的化学反应过程。③看点:弄清曲线上拐点的含义,如与坐标轴的交点、曲线的交点、
折点、最高点与最低点等。曲线的拐点代表着一个反应过程的结束和开始。