文档内容
2022—2023 学年度上学期 2020 级
第二次月考化学试卷
时间:75分钟 分数:100分 考试时间:2022年9月28日
可能用到的相对原子质量:H 1 C 12 O 16 N 14 S 32 Cl 35.5 Ge 73 Br 80
第I卷(选择题 共45分)
一、选择题(本题包括15小题,每小题3分,共45分,每小题只有一个选项符合题意)
1. 生活中处处有化学,下列叙述不正确的是( )
A. HB铅笔芯的成分为黏土和石墨 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 漂白粉与洁厕灵不可混合使用
2. 2021年诺贝尔化学奖授予利斯特和麦克米伦,以表彰他们在不对称有机催化剂领域的
重要贡献。如在合成R-(+)苦杏仁腈时(结构中—Ph为苯基),D-羟腈酶就是该反应的不
对称有机催化剂,其合成过程如图所示。下列说法错误的是( )
A. 不对称有机催化剂对产物有选择性,从而使合成更加“绿色”
B. HCN的电子式为H+[∶C⋮⋮N∶]-
C. 酶发挥催化功能需要适宜的温度及酸碱性环境条件
D. R-(+)苦杏仁腈和S-(-)苦杏仁腈互为同分异构体
3. 设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A. 水溶液中,0.1molFeI 与0.2 mol Cl 充分反应,转移的电子数为0.3N
2 2 A
B. 常温下,1 L 0.1 mol·L-1乙二酸溶液的pH>1,则含H+的数目大于0.1N
A
C. 1 mol AlCl 晶体中含有的Cl-数目为3N
3 A
D. 100g46%乙醇溶液中含有的O-H键数为N
A
4. 能正确表示下列反应的离子方程式为( )
A. 向NaClO溶液中通入少量SO :2ClO-+SO +HO===2HClO+SO
2 2 2B. NaHCO 的水解:HCO+HO===CO+HO+
3 2 3
C. 向CuSO 溶液中通入HS气体:Cu2++S2-===CuS↓
4 2
D. 将等物质的量浓度的Ba(OH) 和NH HSO 溶液等体积混合:Ba2++2OH-+H++NH+
2 4 4 4
+SO = BaSO↓+H O+NH ·HO
4 2 3 2
5.下列装置或操作能达到实验目的的是( )
A.检验乙炔的 D.除去氯气中
B.进行铝热反应 C.溶液滴加
还原性 的HCl气体
6.下列关于元素周期表和元素周期律的说法中,正确的是( )
A.所含元素种类最多的族是ⅢB
B.元素周期表的p区共包含5列
C.第三周期元素的简单离子半径从左到右逐渐减小
D.卤素单质和它们的氢化物沸点从上到下均依次升高
7. 配位化合物广泛的应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制
备某些配位化合物。如2CoCl +2NH Cl+8NH +HO===2[Co(NH)Cl]Cl +2HO,下
2 4 3 2 2 3 5 2 2
列说法正确的是( )
A.1 mol[Co(NH )Cl]Cl 含有σ键的数目为15N
3 5 2 A
B.含1 mol [Ti(NH )Cl]Cl 的水溶液中加入足量AgNO 溶液,产生2mol白色沉淀
3 5 2 3
C.[Co(NH )Cl]2+中存在配位键、共价键和离子键
3 5
D.氧化剂HO 是非极性分子
2 2
8. 某白色粉末样品,可能含有NaSO 、NaSO 、NaS和NaCO 中一种或几种。取少量
2 4 2 3 2 2 3
样品进行如下实验:
①溶于水,得到无色透明溶液②向①的溶液中滴加过量稀硫酸,溶液变浑浊,有无色气体逸出。离心分离。
③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中可以确定存在的是( )
A. NaCO NaS NaSO B. NaSO NaS
2 3 、 2 、 2 3 2 3、 2
C. NaSO NaCO D. NaSO NaSO NaS
2 4 、 2 3 2 4 、 2 3 、 2
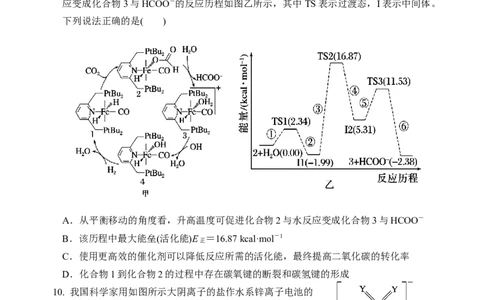
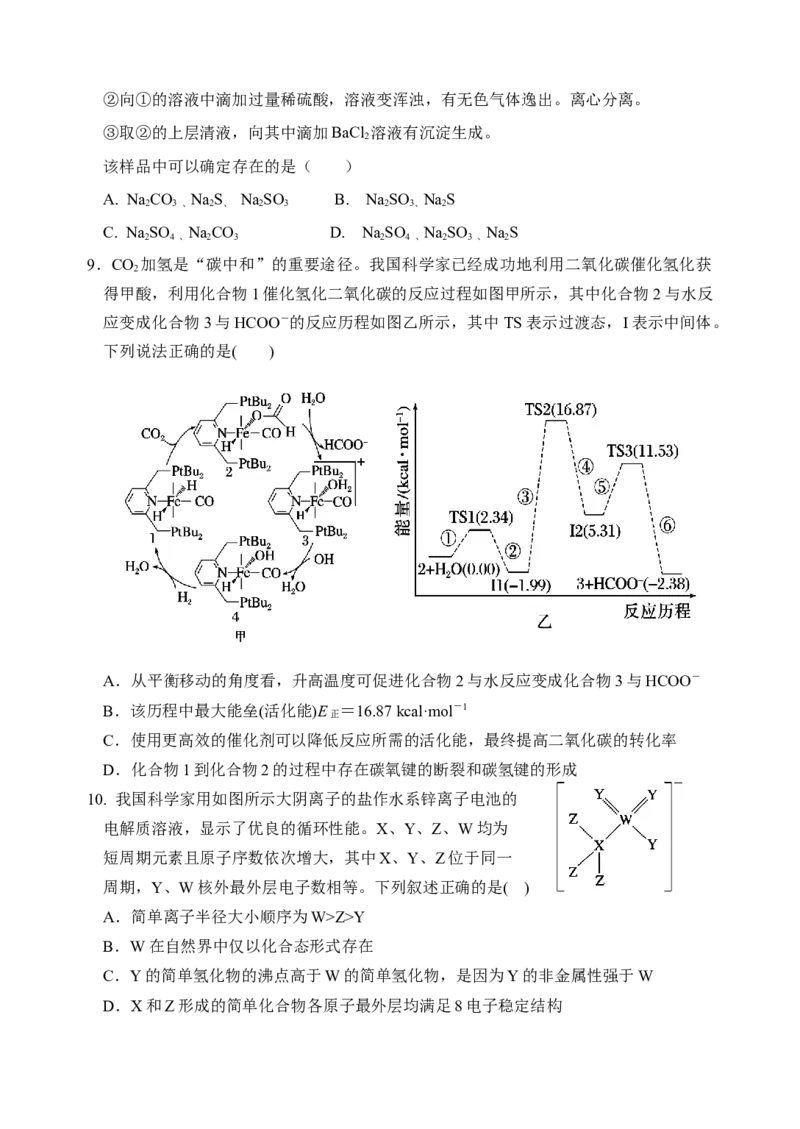
9.CO 加氢是“碳中和”的重要途径。我国科学家已经成功地利用二氧化碳催化氢化获
2
得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反
应变成化合物3与HCOO-的反应历程如图乙所示,其中TS表示过渡态,I表示中间体。
下列说法正确的是( )
A.从平衡移动的角度看,升高温度可促进化合物2与水反应变成化合物3与HCOO-
B.该历程中最大能垒(活化能)E =16.87 kcal·mol-1
正
C.使用更高效的催化剂可以降低反应所需的活化能,最终提高二氧化碳的转化率
D.化合物1到化合物2的过程中存在碳氧键的断裂和碳氢键的形成
10. 我国科学家用如图所示大阴离子的盐作水系锌离子电池的
电解质溶液,显示了优良的循环性能。X、Y、Z、W均为
短周期元素且原子序数依次增大,其中X、Y、Z位于同一
周期,Y、W核外最外层电子数相等。下列叙述正确的是( )
A.简单离子半径大小顺序为W>Z>Y
B.W在自然界中仅以化合态形式存在
C.Y的简单氢化物的沸点高于W的简单氢化物,是因为Y的非金属性强于W
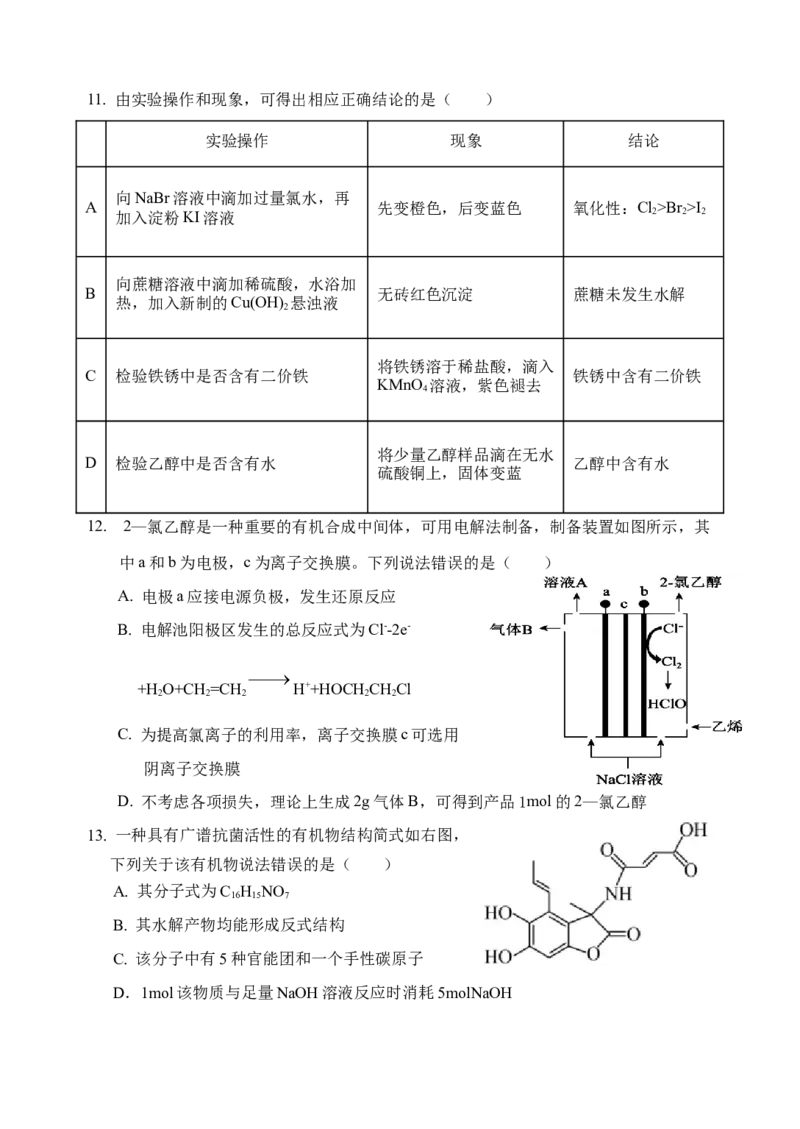
D.X和Z形成的简单化合物各原子最外层均满足8电子稳定结构11. 由实验操作和现象,可得出相应正确结论的是( )
实验操作 现象 结论
向NaBr溶液中滴加过量氯水,再
A 先变橙色,后变蓝色 氧化性:Cl>Br >I
加入淀粉KI溶液 2 2 2
向蔗糖溶液中滴加稀硫酸,水浴加
B 无砖红色沉淀 蔗糖未发生水解
热,加入新制的Cu(OH) 悬浊液
2
将铁锈溶于稀盐酸,滴入
C 检验铁锈中是否含有二价铁 铁锈中含有二价铁
KMnO 溶液,紫色褪去
4
将少量乙醇样品滴在无水
D 检验乙醇中是否含有水 乙醇中含有水
硫酸铜上,固体变蓝
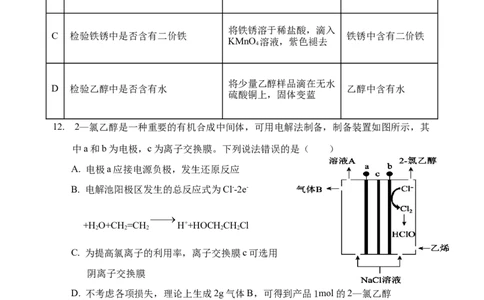
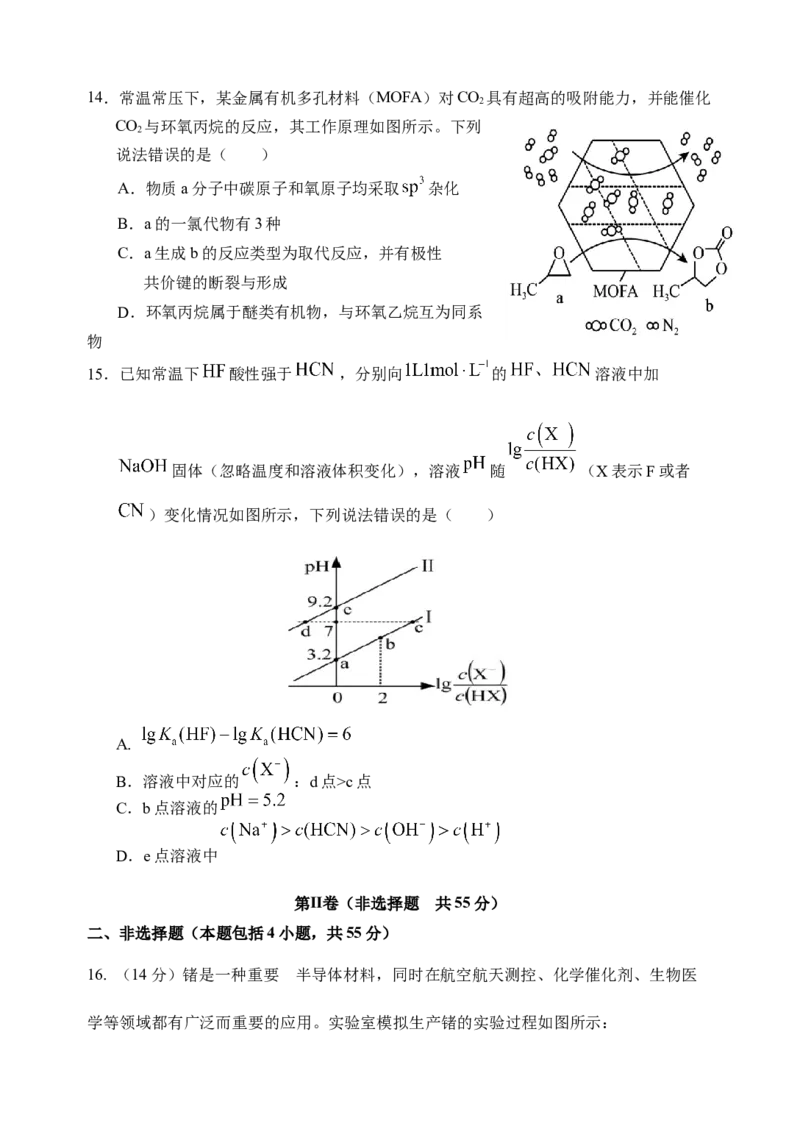
12. 2—氯乙醇是一种重要的有机合成中间体,可用电解法制备,制备装置如图所示,其
中a和b为电极,c为离子交换膜。下列说法错误的是( )
A. 电极a应接电源负极,发生还原反应
B. 电解池阳极区发生的总反应式为Cl--2e-
+H O+CH=CH H++HOCH CHCl
2 2 2 2 2
C. 为提高氯离子的利用率,离子交换膜c可选用
阴离子交换膜
D. 不考虑各项损失,理论上生成2g气体B,可得到产品1mol的2—氯乙醇
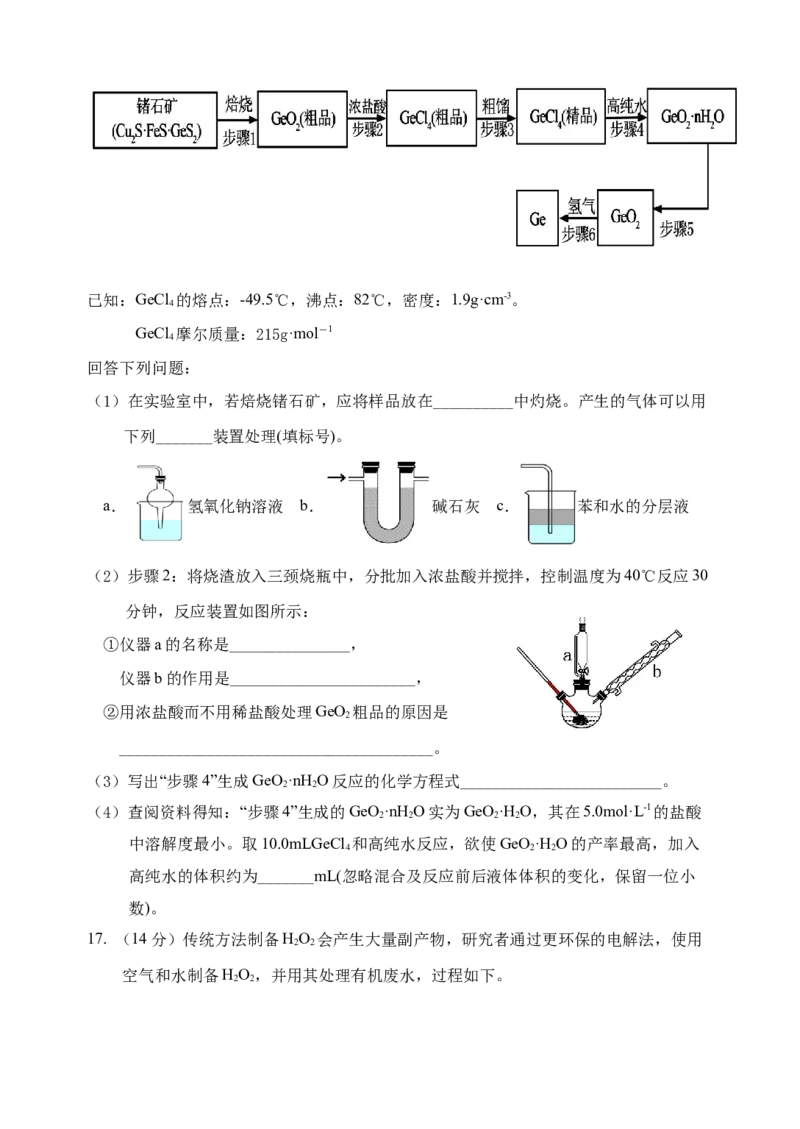
13. 一种具有广谱抗菌活性的有机物结构简式如右图,
下列关于该有机物说法错误的是( )
A. 其分子式为C H NO
16 15 7
B. 其水解产物均能形成反式结构
C. 该分子中有5种官能团和一个手性碳原子
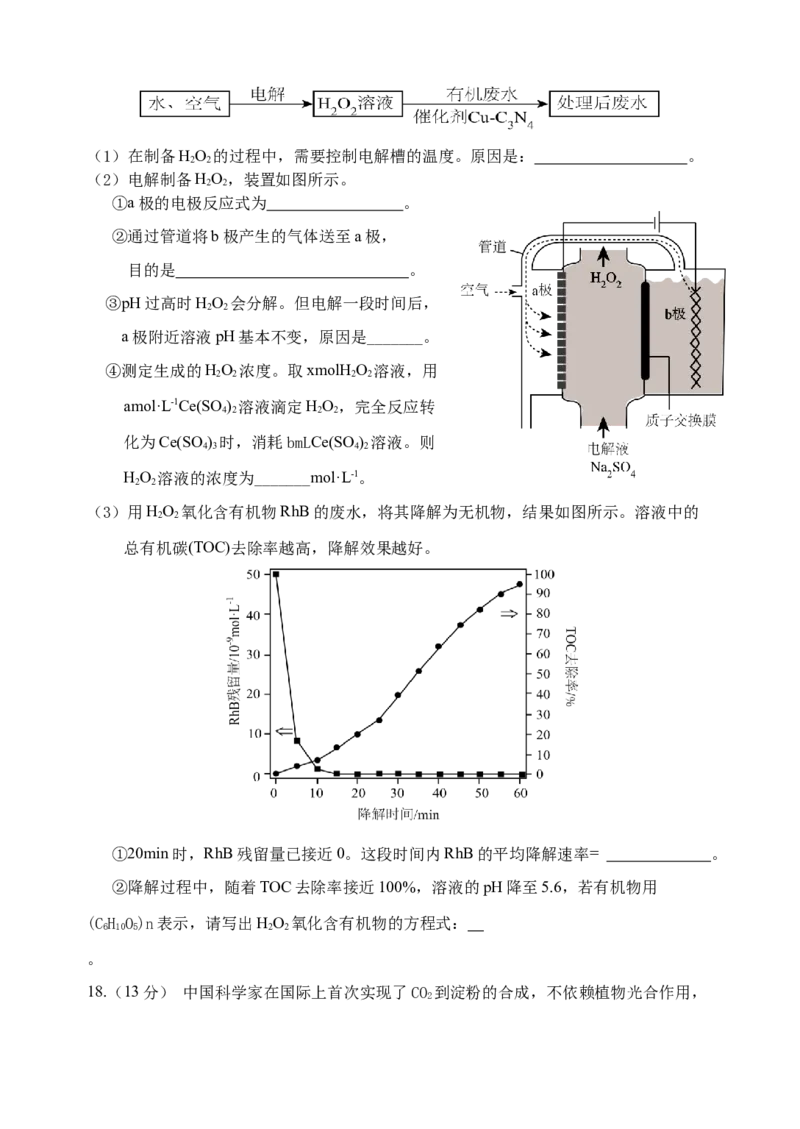
D.1mol该物质与足量NaOH溶液反应时消耗5molNaOH14.常温常压下,某金属有机多孔材料(MOFA)对CO 具有超高的吸附能力,并能催化
2
CO 与环氧丙烷的反应,其工作原理如图所示。下列
2
说法错误的是( )
A.物质a分子中碳原子和氧原子均采取 杂化
B.a的一氯代物有3种
C.a生成b的反应类型为取代反应,并有极性
共价键的断裂与形成
D.环氧丙烷属于醚类有机物,与环氧乙烷互为同系
物
15.已知常温下 酸性强于 ,分别向 的 溶液中加
固体(忽略温度和溶液体积变化),溶液 随 (X表示F或者
)变化情况如图所示,下列说法错误的是( )
A.
B.溶液中对应的 :d点>c点
C.b点溶液的
D.e点溶液中
第II卷(非选择题 共55分)
二、非选择题(本题包括4小题,共55分)
的
16. (14分)锗是一种重要 半导体材料,同时在航空航天测控、化学催化剂、生物医
学等领域都有广泛而重要的应用。实验室模拟生产锗的实验过程如图所示:已知:GeCl 的熔点:-49.5℃,沸点:82℃,密度:1.9g·cm-3。
4
GeCl 摩尔质量:215g·mol-1
4
回答下列问题:
(1)在实验室中,若焙烧锗石矿,应将样品放在__________中灼烧。产生的气体可以用
下列_______装置处理(填标号)。
a. 氢氧化钠溶液 b. 碱石灰 c. 苯和水的分层液
(2)步骤2:将烧渣放入三颈烧瓶中,分批加入浓盐酸并搅拌,控制温度为40℃反应30
分钟,反应装置如图所示:
①仪器a的名称是_______________,
仪器b的作用是_______________________,
②用浓盐酸而不用稀盐酸处理GeO 粗品的原因是
2
_______________________________________。
(3)写出“步骤4”生成GeO ·nH O反应的化学方程式_________________________。
2 2
(4)查阅资料得知:“步骤4”生成的GeO ·nH O实为GeO ·H O,其在5.0mol·L-1的盐酸
2 2 2 2
中溶解度最小。取10.0mLGeCl 和高纯水反应,欲使GeO ·H O的产率最高,加入
4 2 2
高纯水的体积约为_______mL(忽略混合及反应前后液体体积的变化,保留一位小
数)。
17. (14分)传统方法制备HO 会产生大量副产物,研究者通过更环保的电解法,使用
2 2
空气和水制备HO,并用其处理有机废水,过程如下。
2 2(1)在制备HO 的过程中,需要控制电解槽的温度。原因是: 。
2 2
(2)电解制备HO,装置如图所示。
2 2
①a极的电极反应式为 。
②通过管道将b极产生的气体送至a极,
目的是 。
③pH过高时HO 会分解。但电解一段时间后,
2 2
a极附近溶液pH基本不变,原因是_______。
④测定生成的HO 浓度。取xmolHO 溶液,用
2 2 2 2
amol·L-1Ce(SO) 溶液滴定HO,完全反应转
4 2 2 2
化为Ce(SO) 时,消耗bmLCe(SO) 溶液。则
4 3 4 2
HO 溶液的浓度为_______mol·L-1。
2 2
(3)用HO 氧化含有机物RhB的废水,将其降解为无机物,结果如图所示。溶液中的
2 2
总有机碳(TOC)去除率越高,降解效果越好。
①20min时,RhB残留量已接近0。这段时间内RhB的平均降解速率= 。
②降解过程中,随着TOC去除率接近100%,溶液的pH降至5.6,若有机物用
(CH O)n表示,请写出HO 氧化含有机物的方程式:
6 10 5 2 2
。
18.(13分) 中国科学家在国际上首次实现了CO 到淀粉的合成,不依赖植物光合作用,
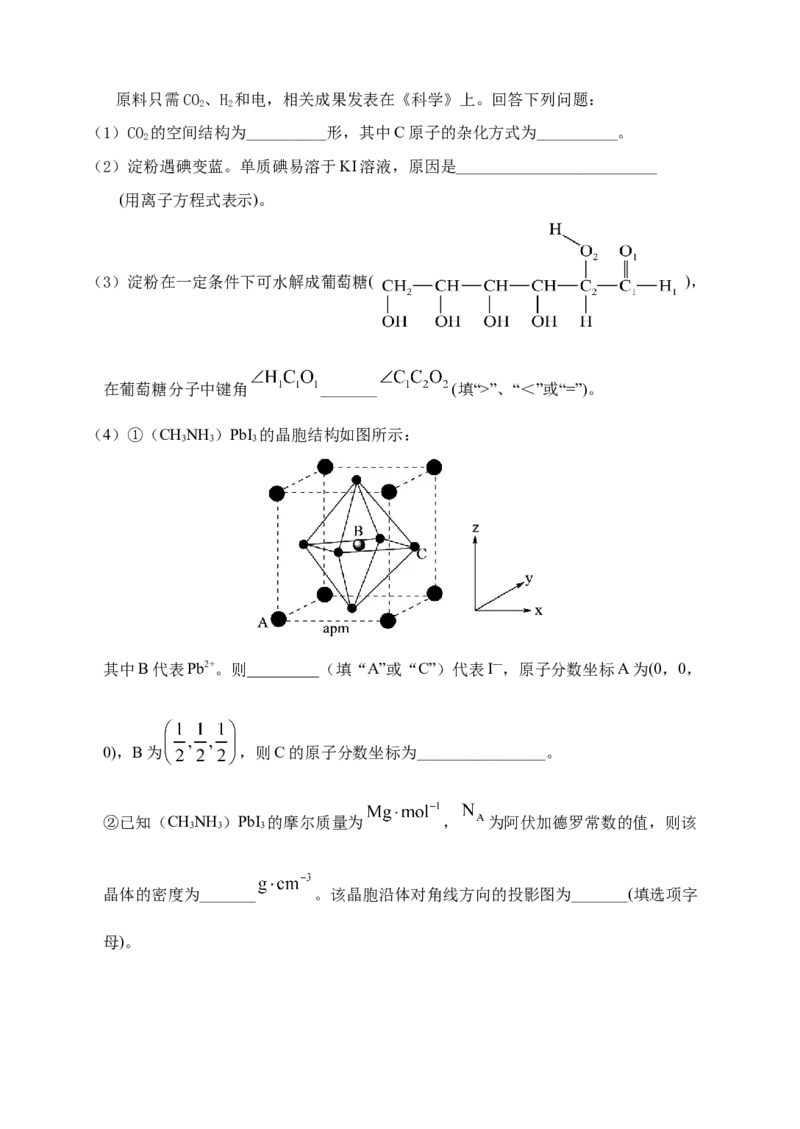
2原料只需CO、H 和电,相关成果发表在《科学》上。回答下列问题:
2 2
(1)CO 的空间结构为__________形,其中C原子的杂化方式为__________。
2
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是_________________________
(用离子方程式表示)。
(3)淀粉在一定条件下可水解成葡萄糖( ),
在葡萄糖分子中键角 _______ (填“>”、“<”或“=”)。
(4)①(CHNH )PbI 的晶胞结构如图所示:
3 3 3
其中B代表Pb2+。则_________(填“A”或“C”)代表I—,原子分数坐标A为(0,0,
0),B为 ,则C的原子分数坐标为________________。
②已知(CHNH )PbI 的摩尔质量为 , 为阿伏加德罗常数的值,则该
3 3 3
晶体的密度为_______ 。该晶胞沿体对角线方向的投影图为_______(填选项字
母)。a. b. c. d
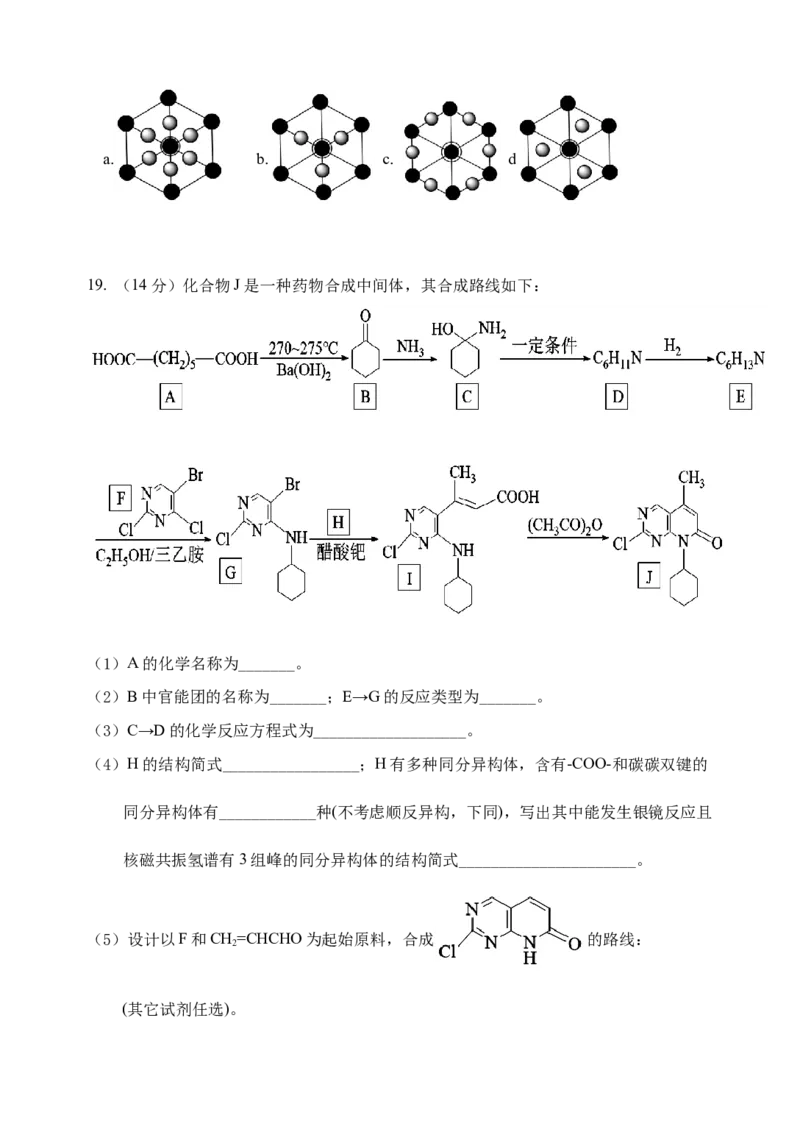
19. (14分)化合物J是一种药物合成中间体,其合成路线如下:
(1)A的化学名称为_______。
(2)B中官能团的名称为_______;E→G的反应类型为_______。
(3)C→D的化学反应方程式为___________________。
(4)H的结构简式_________________;H有多种同分异构体,含有-COO-和碳碳双键的
同分异构体有____________种(不考虑顺反异构,下同),写出其中能发生银镜反应且
核磁共振氢谱有3组峰的同分异构体的结构简式______________________。
(5)设计以F和CH=CHCHO为起始原料,合成 的路线:
2
(其它试剂任选)。下载最新免费模拟卷,到公众号:一枚试卷君