文档内容
第 3 讲 盐类的水解
课 程 标 准 知 识 建 构
1.认识盐类水解的原理,讨论盐溶液呈酸性、中性或碱
性的原因。
2.认识盐类水解的主要因素,了解盐类水解的应用,如
铝盐和铁盐的净水作用。
一、盐类水解及其规律
1.盐类的水解
2.盐类水解的规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
溶液的 溶液
盐的类型 实例 是否水解 水解的离子
酸碱性 的pH
强酸强碱盐 NaCl、KNO 否 中性 pH = 7
3
NH Cl、 NH 、 Cu 2 +
4
强酸弱碱盐 是 酸性 pH < 7
Cu(NO )
3 2
CH COONa、 CH COO - 、
3 3
弱酸强碱盐 是 碱性 pH>7
Na CO CO
2 3
3.盐类水解离子方程式的书写
(1)一般要求
水解记三点,水写分子式,中间用可逆(),后无沉气出。如NH Cl水解的离子方
4
程式为 NH + H O NH ·H O + H + 。
2 3 2
(2)三种类型的盐水解离子方程式的书写
①多元弱酸盐水解:分步进行,以第一步为主,一般只写第一步水解方程式。如Na CO 水解的离子方程式为 CO + H O HCO + OH - 。
2 3 2
②多元弱碱盐水解:水解离子方程式一步写完。
如FeCl 水解的离子方程式为 Fe 3 + + 3H O Fe(OH) + 3H + 。
3 2 3
③阴、阳离子相互促进的水解:水解程度较大,书写时要用“===”、“↑”、“↓”
等。如 Na S 溶液与 AlCl 溶液混合水解的离子方程式为 2Al 3 + + 3S 2 - +
2 3
6H O == =2Al(OH) ↓ + 3H S ↑ 。
2 3 2
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)盐类水解的过程就是盐和水发生反应的过程( )
(2)溶液呈中性的盐一定是强酸、强碱生成的盐( )
(3)某盐溶液呈酸性,该盐一定发生了水解反应( )
(4)常温下,pH=10的CH COONa溶液与pH=4的NH Cl溶液,水的电离程度相
3 4
同( )
(5)常温下,pH=11的CH COONa溶液与pH=3的CH COOH溶液,水的电离程
3 3
度相同( )
(6)NaHCO 、NaHSO 都能促进水的电离( )
3 4
(7)向NaAlO 溶液中滴加NaHCO 溶液,水解相互促进有沉淀和气体生成( )
2 3
(8)FeCl 溶液与NaHCO 溶液混合:Fe3++3HCO===Fe(OH) ↓+3CO ↑( )
3 3 3 2
答案 (1)√ (2)× (3)× (4)√ (5)× (6)× (7)× (8)√
二、盐类水解的影响因素及应用
1.影响盐类水解平衡的因素
(1)内因:盐类本身的性质,形成盐的酸或碱越弱,其盐就越易水解。
(2)外因
水解产生离子
因素 水解平衡 水解程度
的浓度
温度 升高 右移 增大 增大
增大 右移 减小 增大
浓度
减小(稀释) 右移 增大 减小
酸 弱碱阳离子的水解程度减小
外加酸碱
碱 弱酸根离子的水解程度减小
(3)以NH+H ONH ·H O+H+为例,填写下表。
2 3 2
平衡移动 c(H+) c(NH)
升高温度 右移 增大 减小加水稀释 右移 减小 减小
通入少量HCl 左移 增大 增大
加入少量NaOH固体 右移 减小 减小
加入固体NH Cl 右移 增大 增大
4
2.盐类水解的应用
应用 举例
FeCl 溶 液 显 酸 性 , 原 因 是 Fe 3 + +
3
判断溶液的酸碱性
3H O Fe(OH) + 3H +
2 3
等物质的量浓度的NaX、NaY、NaZ三种盐溶液
判断酸性强弱
的pH分别为8、9、10,则酸性: HX > HY > HZ
配制CuSO 溶液时,加入少量H SO ,防止Cu2+
4 2 4
水解;配制 FeCl 溶液,加入少量盐酸;贮存
3
配制或贮存易水解的盐溶液
Na CO 溶液、Na SiO 溶液不能用带磨口玻璃塞
2 3 2 3
的试剂瓶
胶体的 制取 Fe(OH) 胶体的离子方程式: Fe 3 + +
3
制取 3H O ===== Fe(OH) ( 胶体 ) + 3H +
2 3
成分为NaHCO 与Al (SO ) ,发生反应为 Al 3 + +
3 2 4 3
泡沫灭火器原理
3HCO == =Al(OH) ↓ + 3CO ↑
3 2
明 矾 可 作 净 水 剂 , 原 理 为 Al 3 + +
作净水剂
3H O Al(OH) ( 胶体 ) + 3H +
2 3
化肥的
铵态氮肥与草木灰不得混用
使用
除锈剂 NH Cl与ZnCl 溶液可作焊接时的除锈剂
4 2
如:Na CO 溶液中离子浓度由大到小的顺序为
2 3
比较溶液中离子浓度的大小
c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)
盐水解生成挥发性酸,蒸干灼烧后一般得氧化
物。如AlCl →Al O
3 2 3
盐水解生成难挥发性酸,蒸干后得原物质。如
判断盐溶液蒸干时的产物 CuSO →CuSO
4 4
考虑盐受热时是否分解。如KMnO →K MnO 和
4 2 4
MnO
2
还 原 性 盐 溶 液 蒸 干 时 会 被 O 氧 化 。 如
2Na SO →Na SO
2 3 2 4
弱酸的铵盐溶液蒸干后无固体剩余。如
NH HCO 、(NH ) CO
4 3 4 2 3
3.熟记下列因相互促进水解不能大量共存的离子组合
(1)Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-。
(2)Fe3+与HCO、CO、AlO、SiO、ClO-。
(3)NH与SiO、AlO。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)加热0.1 mol·L-1 Na CO 溶液,CO的水解程度和溶液的pH均增大( )
2 3
(2)氯化铵溶液加水稀释时,的值减小( )
(3)在CH COONa溶液中加入适量CH COOH,可使c(Na+)=c(CH COO-)( )
3 3 3
(4)水解平衡右移,盐离子的水解程度可能增大,也可能减小( )
(5)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强( )
(6)天然弱碱性水呈碱性的原因是其中含有较多的Fe3+、Cu2+等离子( )
(7)生活中用电解食盐水的方法制取消毒液,运用了盐类的水解原理( )
答案 (1)√ (2)√ (3)√ (4)√ (5)× (6)× (7)×
三、水解常数(K )
h
1.数学表达式
用HA表示酸,用MOH表示碱,MA表示由它们生成的盐,在MA溶液中,若M
+、A-均能水解,A-+H OHA+OH-,则 A-的水解常数为 K =;M++
2 h
H OMOH+H+,则M+的水解常数为K =。
2 h
2.水解常数与电离常数的关系
若NaA为强碱弱酸盐,A-+H OHA+OH-,K ===;若MCl为强酸弱碱盐
2 h
同理可得K =。
h
3.意义
水解常数可以表示盐的水解程度的大小,K 越大,盐类水解程度越大。
h
4.外界影响因素
水解常数是只是温度的函数,K 随温度的升高而增大。
h
5.水解常数的应用
(1)计算盐溶液中的c(H+)或c(OH-)
如 A- +H O HA + OH-
2
起始 c 0 0平衡 c-c(OH-) c(OH-) c(OH-))
K =≈,c(OH-)=;
h
同理,对于M++H OMOH+H+,c(H+)=。
2
(2)判断水解程度和电离程度大小,判断盐溶液的酸碱性。
①单一溶液。
a.一定浓度的NaHCO 溶液,K =4.4×10-7,K =5.6×10-11,K ==≈2.27×10
3 a1 a2 h
-8>K ,HCO的水解程度大于电离程度,溶液呈碱性,c(OH-)>c(H+),c(H CO )
a2 2 3
>c(CO)。
b.一定浓度的NaHSO 溶液,K =1.54×10-2,K =1.2×10-7,K ==≈6.5×10-
3 a1 a2 h
13<K ,HSO的水解程度小于电离程度,溶液呈酸性,c(H+)>c(OH-),c(SO)>
a2
c(H SO )。
2 3
c . 一 定 浓 度 的 CH COONH 溶 液 , 由 于 K (CH COOH) = 1.75×10 -
3 4 a 3
5≈K (NH ·H O)=1.71×10-5,则CH COO-与NH的水解常数近似相等,二者水
b 3 2 3
解程度相同,CH COONH 溶液呈中性,c(CH COO-)=c(NH)。
3 4 3
②混合溶液。
a.对于等物质的量浓度的CH COOH、CH COONa混合溶液,K (CH COOH)=
3 3 a 3
1.75×10-5,K (CH COO-)===5.7×10-10<K (CH COOH),CH COO-的水解
h 3 a 3 3
程度小于CH COOH的电离程度,溶液显酸性,c(H+)>c(OH-),c(CH COO-)>
3 3
c(Na+)>c(CH COOH)。b.对于物质的量浓度相等的HCN和NaCN混合溶液,
3
K (HCN)=4.9×10-10,K ===2.0×10-5>K (HCN),CN-水解程度大于HCN电
a h a
离程度,溶液呈碱性,c(OH-)>c(H+),c(HCN)>c(Na+)>c(CN-)。
【诊断3】 25 ℃时,H SO HSO+H+的电离常数K =1×10-2 mol·L-1,则该温
2 3 a
度下NaHSO 水解反应的平衡常数K =________ mol·L-1,若向NaHSO 溶液中
3 h 3
加入少量的I ,则溶液中将________(填“增大”“减小”或“不变”)。
2
答案 1×10-12 增大
解析 K =
a
K =====1×10-12 mol·L-1。
h
HSO+H OH SO +OH-,当加少量I 时,发生I +HSO+H O===2I-+3H++
2 2 3 2 2 2
SO,H+增多导致c(OH-)减小,所以=增大。
考点一 盐类水解实质的分析和理解应用
【典例1】 (2020·河南省洛阳高三模拟)常温下,浓度均为0.1 mol·L-1的下列四种盐溶液,其pH测定如表所示:
序号 ① ② ③ ④
溶液 CH COONa NaHCO Na CO NaClO
3 3 2 3
pH 8.8 9.7 11.6 10.3
下列说法正确的是( )
A.四种溶液中,水的电离程度:③>②>④>①
B.Na CO 和NaHCO 溶液中,粒子种类相同
2 3 3
C.将等浓度的CH COOH和HClO溶液比较,pH小的是HClO
3
D.Na CO 溶液中,c(Na+)=c(CO)+c(HCO)+c(H CO )
2 3 2 3
答案 B
解析 这几种盐都是强碱弱酸盐,弱酸根离子发生水解反应使溶液显碱性,当盐
的浓度相同时,酸的酸性越弱,酸根离子水解的程度越大,水的电离程度越大,溶
液的碱性越强。根据表格数据可知,四种溶液中水的电离程度:①<②<④<③,A
错误;在Na CO 和NaHCO 溶液中,存在的粒子有Na+、HCO、CO、H CO 、H O、
2 3 3 2 3 2
H+、OH-,粒子种类相同,B正确;根据盐的水解程度大小可知,等浓度的
CH COOH和HClO溶液的酸性:CH COOH>HClO,所以pH小的是CH COOH,
3 3 3
C错误;在Na CO 溶液中,Na+与C原子数目比为2∶1,可得c(Na+)=2c(CO)+
2 3
2c(HCO)+2c(H CO ),D错误。
2 3
【对点练1】 (盐类水解的实质和规律)相同温度、相同浓度下的八种溶液,其pH
由小到大的顺序如图所示,图中①②③④⑤代表的物质可能分别为( )
A.NH Cl (NH ) SO CH COONa NaHCO NaOH
4 4 2 4 3 3
B.(NH ) SO NH Cl CH COONa NaHCO NaOH
4 2 4 4 3 3
C.(NH ) SO NH Cl NaOH CH COONa NaHCO
4 2 4 4 3 3
D.CH COOH NH Cl (NH ) SO NaHCO NaOH
3 4 4 2 4 3
答案 B
解析 酸性从强到弱的顺序为电离呈酸性>水解呈酸性>中性>水解呈碱性>电
离呈碱性。
【对点练2】 (盐类水解反应离子方程式)写出符合要求的离子方程式:
(1)AlCl 溶液呈酸性__________________________________________________。
3
(2)Na CO 溶液呈碱性________________________________________________。
2 3
(3)NaHS溶液呈碱性的原因____________________________________________。(4)NH Cl溶于D O中_________________________________________________。
4 2
(5)对于易溶于水的正盐M R 溶液,若pH>7,其原因是____________________
n m
___________________________________________________________________;
(用离子方程式说明,下同);
若pH<7,其原因是__________________________________________________。
答案 (1)Al3++3H OAl(OH) +3H+
2 3
(2)CO+H OHCO+OH-
2
HCO+H OH CO +OH-
2 2 3
(3) HS-+H OH S+OH-
2 2
(4)NH+D ONH ·HDO+D+
2 3
(5)Rn-+H OHR(n-1)-+OH-
2
Mm++mH OM(OH) +mH+
2 m
【对点练3】 (水解实质的拓展延伸)广义的水解观认为:无论是盐的水解还是非盐
的水解,其最终结果是反应中各物质和水分别离解成两部分,然后两两重新组合
成新的物质。根据上述观点,下列说法不正确的是( )
A.BaO 的水解产物是Ba(OH) 和H O
2 2 2 2
B.PCl 的水解产物是HClO和H PO
3 3 4
C.Al C 的水解产物是Al(OH) 和CH
4 3 3 4
D.CH COCl的水解产物是CH COOH和HCl
3 3
答案 B
解析 BaO 的水解产物是Ba(OH) 和H O ,符合水解原理,故A项正确;PCl 的
2 2 2 2 3
水解产物应是H PO 和HCl,不符合水解原理,故B项错误;Al C 水解得到氢氧
3 3 4 3
化铝和甲烷,符合水解原理,故C项正确;CH COCl的水解产物是两种酸,为
3
CH COOH和HCl,符合水解原理,故D项正确。
3
考点二 盐类水解平衡的移动和应用
【典例2】 (2020·河南开封市一模)某同学探究溶液的酸碱性对FeCl 水解平衡的
3
影响,实验方案如下:配制50 mL 0.001 mol·L-1 FeCl 溶液、50 mL对照组溶液X,
3
向两种溶液中分别滴加1滴1 mol·L-1 HCl溶液、1滴1 mol·L-1 NaOH溶液,测得
溶液pH随时间变化的曲线如下图所示。下列说法不正确的是( )
A.依据M点对应的pH,说明Fe3+发生了水解反应
B.对照组溶液X的组成可能是0.003 mol·L-1 KCl溶液
C.依据曲线c和d说明Fe3+水解平衡发生了移动
D.通过仪器检测体系浑浊度的变化,可表征水解平衡移动的方向
答案 B
解析 FeCl 溶液的pH小于7,溶液显酸性,原因是Fe3+在溶液中发生了水解,A
3
正确;图中对照组溶液 X加碱后溶液的pH的变化程度比加酸后的 pH的变化程
度大,若对照组溶液X是0.003 mol·L-1 KCl溶液,则加酸和加碱后溶液的pH的
变化应呈现轴对称的关系,B错误;在FeCl 溶液中加碱、加酸后,溶液的pH的变
3
化均比对照组溶液X的变化小,因为加酸或加碱均引起了Fe3+水解平衡的移动,
故溶液的pH的变化比较缓和,C正确;FeCl 水解生成氢氧化铁,故溶液的浑浊程
3
度变大,则表明水解被促进,否则被抑制,D正确。
利用平衡移动原理解释问题的思维模板
(1)解答此类题的思维过程
①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件
③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系
(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)
【对点练4】 (盐类水解的影响因素)已知NaHSO 溶液常温时显酸性,溶液中存在
3
以下平衡:
HSO+H OH SO +OH- ①
2 2 3
HSOH++SO ②向0.1 mol·L-1的NaHSO 溶液中分别加入以下物质,下列有关说法正确的是(
3
)
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO)增大
B.加入少量Na SO 固体,则c(H+)+c(Na+)=c(HSO)+c(OH-)+c(SO)
2 3
C.加入少量NaOH溶液,、的值均增大
D.加入氨水至中性,则2c(Na+)=c(SO)>c(H+)=c(OH-)
答案 C
解析 NaHSO 溶液显酸性,则HSO的电离程度>HSO的水解程度,加入钠后平
3
衡①左移、平衡②右移,c(HSO)减小,A项错误;根据电荷守恒可知,应为c(H+)+
c(Na+)=c(HSO)+c(OH-)+2c(SO),B项错误;加入少量NaOH,平衡②右移,、的
值均增大,C 项正确;溶液中存在物料守恒,即 c(Na+)=c(SO)+c(HSO)+
c(H SO ),c(Na+)>c(SO),c(H+)=c(OH-),D项错误。
2 3
【对点练5】 (盐类水解的应用)下列有关盐类水解的事实或应用、解释的说法不正
确的是( )
选项 事实或应用 解释
纯碱与油污直接发生反
A 用热的纯碱溶液去除油污
应,生成易溶于水的物质
Al (SO ) 与 NaHCO 溶液
2 4 3 3
B 泡沫灭火器灭火
反应产生CO 气体
2
施肥时,草木灰(主要成分
K CO 与 NH Cl 反应生成
2 3 4
C K CO )与NH Cl不能混合
2 3 4
NH ,降低肥效
3
使用
明矾[KAl(SO ) ·12H O]作 明矾溶于水生成 Al(OH)
4 2 2 3
D
净水剂 胶体
答案 A
【对点练6】 (盐类水解平衡的实验探究)已知:
[FeCl (H O) ]-为黄色,溶液中存在可逆反应:Fe3++4Cl-+2H O[FeCl (H O) ]
4 2 2 2 4 2 2
-,下列实验所得结论不正确的是( )
① ② ③ ④加入 NaCl 后,溶
加热前溶液为浅黄 加热前溶液接近无 加热前溶液为黄
液立即变为黄色,
色,加热后颜色变 色,加热后溶液颜 色,加热后溶液颜
加热后溶液颜色变
深 色无明显变化 色变深
深
注:加热为微热,忽略体积变化。
A.实验①中,Fe (SO ) 溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)
2 4 3 3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,加热,可逆反应:Fe3++4Cl-+2H O[FeCl (H O) ]-正向移动
2 4 2 2
D.实验④,可证明升高温度,颜色变深一定是因为Fe3+水解平衡正向移动
答案 D
解析 加热促进水解,铁离子水解生成氢氧化铁,则实验①中,Fe (SO ) 溶液显
2 4 3
浅黄色原因是 Fe3+水解产生了少量 Fe(OH) ,故 A 项正确;由 Fe3++
3
3H OFe(OH) +3H+可知,酸化后加热溶液颜色无明显变化,氢离子抑制水解
2 3
则实验②中酸化对Fe3+水解的影响程度大于温度的影响,故B项正确;加入NaCl
后,溶液立即变为黄色,发生Fe3++4Cl-+2H O[FeCl (H O) ]-,[FeCl (H O) ]
2 4 2 2 4 2 2
-为黄色,加热时平衡正向移动,溶液颜色变深,故C项正确;实验④中存在Fe3+
+4Cl-+2H O[FeCl (H O) ]-,升高温度平衡正向移动,溶液颜色变深,不能
2 4 2 2
证明对Fe3+水解平衡的影响,故D项错误。
考点三 水解常数(K )的意义和应用
h
【典例3】 磷酸是三元弱酸,常温下三级电离常数分别是K =7.1×10-3,K =
a1 a2
6.2×10-8,K =4.5×10-13,回答下列问题:
a3
(1)常温下同浓度①Na PO 、②Na HPO 、③NaH PO 的pH由小到大的顺序是
3 4 2 4 2 4
________(填序号)。
(2)常温下,NaH PO 的水溶液pH________(填“>”“<”或“=”)7。
2 4
(3)常温下,Na HPO 的水溶液呈________(填“酸”“碱”或“中”)性,用K 与
2 4 a
K 的相对大小,说明判断理由:_______________________________________
h
___________________________________________________________________。
答案 (1)③<②<① (2)< (3)碱 Na HPO 的水解常数K ===≈1.61×10
2 4 h
-7,K >K ,即HPO的水解程度大于其电离程度,因而Na HPO 溶液显碱性
h a3 2 4
解析 (1)K 越大,K 越小,所以①Na PO 、②Na HPO 、③NaH PO 的水解程度
a h 3 4 2 4 2 4
依次减小,pH依次减小。
(2)NaH PO 的水解常数
2 4K ===≈1.4×10-12,K >K ,即H PO的电离程度大于其水解程度,因而pH<
h a2 h 2
7。
(3)Na HPO 的水解常数
2 4
K ===≈1.6×10-7,K <K ,即H PO的水解程度大于其电离程度,因而pH>
h a3 h 2
7。
K 与K (或K )、K 的关系
h a b W
(1)一元弱酸盐:K ·K =K
a h W
(2)一元弱碱盐:K ·K =K
b h W
(3)多元弱酸盐,如Na A溶液:K =
m h
Na HA溶液K =
m-1 h
依次类推……
【对点练7】 (水解常数的计算)(2020·安徽省太和第一中学月考)已知:25 ℃ 时,
K (NH ·H O)=1.8×10-5。该温度下,用0.100 mol·L-1的氨水滴定10.00 mL 0.100
b 3 2
mol·L-1的一元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中lg 的关系
如图所示。下列说法不正确的是( )
A.HA为强酸
B.a<10
C.25 ℃时,NH的水解常数为×10-9
D.当滴入20 mL氨水时, 溶液中存在c(NH)>c(A-)>c(NH ·H O)>c(OH-)>c(H+)
3 2
答案 B
解析 根据图像,0.1 mol/L 的一元酸 HA溶液中 lg=12,则=1012,结合 c(H
+)×c(OH-)=10-14解得c(H+)=0.1 mol/L,则HA为强酸,A正确;若a=10,则
二者恰好完全反应生成NH A,该铵盐水解,溶液显酸性,lg>0,结合图像可知,
4
当lg=0时,a>10,B不正确;25 ℃时,NH的水解常数===×10-9,C正确;当
滴入氨水的体积V=20 mL时得到等物质的量浓度的NH A和氨水的混合液,由
4
于NH ·H O的电离常数大于NH的水解常数,则NH ·H O的电离程度大于NH
3 2 3 2的 水 解 程 度 , 所 以 c(NH)>c(A - ) 、 c(OH - )>c(H + ) , 则 c(NH)>c(A
-)>c(NH ·H O)>c(OH-)>c(H+),D正确。
3 2
【对点练8】 (水解常数的应用)根据已知条件填空:
(1)已知25 ℃时,NH ·H O的电离平衡常数K =1.8×10-5,该温度下1 mol·L-1
3 2 b
的NH Cl溶液中c(H+)=________mol·L-1。(已知≈2.36)
4
(2)已知某温度时,Na CO 溶液的水解常数K =2×10-4 mol·L-1,则当溶液中
2 3 h
c(HCO)∶c(CO)=2∶1时,试求该溶液的pH=________。
答案 (1)2.36×10-5 (2)10
解析 (1)K ==
h
c(H+)≈c(NH ·H O),而c(NH)≈1 mol·L-1。
3 2
所以c(H+)== mol·L-1≈2.36×10-5 mol·L-1。
(2)K ==2×10-4,
h
又c(HCO)∶c(CO)=2∶1,则c(OH-)=10-4 mol·L-1,结合K =1.0×10-14,可得
W
c(H+)=10-10 mol·L-1。
【对点练9】 (判断溶液的酸碱性)已知常温下CN-的水解常数K =1.61×10-5。
h
(1)常温下,含等物质的量浓度的HCN与NaCN的混合溶液显________(填“酸”
“碱”或“中”)性,c(CN-)________(填“>”“<”或“=”)c(HCN)。该溶液中各
离子浓度由大到小的顺序为________。
(2)常温下,若将c mol·L-1盐酸与0.62 mol·L-1 KCN溶液等体积混合后恰好得到
中性溶液,则c=________(小数点后保留4位数字)。
答案 (1)碱 < c(Na+)>c(CN-)>c(OH-)>c(H+)
(2)0.616 2 mol·L-1
解析 (1)K (CN-)=1.61×10-5,由此可求出K (HCN)≈6.2×10-10,故CN-的水
h a
解能力强于HCN的电离能力,由于NaCN与HCN的物质的量相等,故水解产生
的c(OH-)大于电离生成的c(H+),混合溶液显碱性,且c(CN-)c(CH COO-)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CH COO-)+c(CH COOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CH COOH)+c(H+)=c(NH ·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)c(CH COO-),A项正确;当滴入氨水10 mL时,
3 3
加入的氨水的体积、浓度和初始醋酸溶液的体积、浓度均相等,由物料守恒可知,
c(NH)+c(NH ·H O)=c(CH COO-)+c(CH COOH),B项正确;当滴入氨水20 mL
3 2 3 3
时,溶液中溶质为 CH COONH 和 NH Cl,根据电荷守恒式 c(NH)+c(H+)=
3 4 4
c(CH COO-)+c(Cl-)+c(OH-),物料守恒式c(NH)+c(NH ·H O)=c(CH COO-)
3 3 2 3
+c(CH COOH)+c(Cl-),可得c(CH COOH)+c(H+)=c(NH ·H O)+c(OH-),C项
3 3 3 2
正确;恰好反应时,生成等物质的量的氯化铵和醋酸铵,此时溶液呈酸性,若溶液
呈中性,则氨水滴入量大于20 mL,c(NH)>c(Cl-),D项错误。
3.(双选)(2020·江苏化学,14)室温下,将两种浓度均为0.10 mol·L-1的溶液等体
积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓
度关系正确的是( )
A.NaHCO -Na CO 混合溶液(pH=10.30):c(Na+)>c(HCO)>c(CO)>c(OH-)
3 2 3
B.氨水-NH Cl混合溶液(pH=9.25):c(NH)+c(H+)=c(NH ·H O)+c(OH-)
4 3 2
C . CH COOH - CH COONa 混 合 溶 液 (pH = 4.76) : c(Na
3 3
+)>c(CH COOH)>c(CH COO-)>c(H+)
3 3
D.H C O -NaHC O 混合溶液(pH=1.68,H C O 为二元弱酸):c(H+)+c(H C O )
2 2 4 2 4 2 2 4 2 2 4
=c(Na+)+c(C O)+c(OH-)
2
答案 AD
解析 浓度均为0.10 mol·L-1的NaHCO -Na CO 的混合溶液中,CO的水解程
3 2 3
度大于HCO的水解程度,HCO的水解程度大于其电离程度,所以溶液中 c(Na+)>c(HCO)>c(CO)>c(OH-),A项正确;浓度均为0.10 mol·L-1的氨水-NH Cl混
4
合溶液的 pH=9.25,说明 NH ·H O的电离程度大于 NH的水解程度,溶液中
3 2
c(NH ·H O)c(NH ·H O)+c(OH-),B 项错误;浓度均为 0.10 mol·L-1的
3 2
CH COOH-CH COONa混合溶液的pH=4.76,说明CH COOH的电离程度大于
3 3 3
CH COO-的水解程度,则溶液中c(CH COO-)>c(Na+)>c(CH COOH)>c(H+),C
3 3 3
项错误;浓度均为0.10 mol·L-1的H C O -NaHC O 混合溶液的pH=1.68,根据
2 2 4 2 4
电荷守恒有c(Na+)+c(H+)=c(OH-)+c(HC O)+2c(C O),根据物料守恒有2c(Na
2 2
+)=c(C O)+c(H C O )+c(HC O),联立上述两式得c(H+)+c(H C O )=c(Na+)+
2 2 2 4 2 2 2 4
c(C O)+c(OH-),D项正确。
2
4.(2020·天津学业水平等级考试,7)常温下,下列有关电解质溶液的说法错误的
是( )
A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则K (HCOOH)>K (HF)
a a
B.相同浓度的CH COOH和CH COONa两溶液等体积混合后pH约为4.7,则溶
3 3
液中c(CH COO-)>c(Na+)>c(H+)>c(OH-)
3
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D.在1 mol·L-1 Na S溶液中,c(S2-)+c(HS-)+c(H S)=1 mol·L-1
2 2
答案 A
解析 酸根离子的水解能力越强,对应酸的酸性越弱,HF的酸性比HCOOH强,
A项错误;等浓度的CH COOH和CH COONa混合溶液呈酸性,说明CH COOH
3 3 3
的电离程度大于 CH COO-的水解程度,则离子浓度关系:c(CH COO-)>c(Na
3 3
+)>c(H+)>c(OH-),B项正确;FeS溶于稀硫酸,而CuS不溶于稀硫酸,说明FeS的
溶解度大于CuS,K (FeS)>K (CuS),C项正确;根据物料守恒可知,c(S2-)+c(HS
sp sp
-)+c(H S)=1 mol·L-1,D项正确。
2
5.(2019·北京理综,12)实验测得0.5 mol·L-1 CH COONa溶液、0.5 mol·L-1 CuSO
3 4
溶液以及H O的pH随温度变化的曲线如图所示。下列说法正确的是( )
2A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CH COONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结
4 W
果
D.随温度升高,CH COONa溶液和CuSO 溶液的pH均降低,是因为CH COO-、
3 4 3
Cu2+水解平衡移动方向不同
答案 C
解析 任何温度时,纯水中H+浓度与OH-浓度始终相等,A项错误;随温度升高,
CH COONa水解程度增大,溶液中c(OH-)增大,且温度升高,水的电离程度增大,
3
c(OH-)也增大,B项错误;温度升高,水的电离程度增大,c(H+)增大,又CuSO 水
4
解使溶液显酸性,温度升高,水解平衡正向移动,故c(H+)增大,C项正确;温度升
高,能使电离平衡和水解平衡均向正反应方向移动,而CH COONa溶液随温度升
3
高pH降低的原因是水的电离程度增大得多,而 CuSO 溶液随温度升高pH降低
4
的原因是Cu2+水解程度增大得多,D项错误。
6.(2019·上海选考)常温下0.1 mol·L-1 ①CH COOH、②NaOH、③CH COONa,下
3 3
列叙述正确的是( )
A.①中c(CH COOH)>c(CH COO-)>c(H+)>c(OH-)
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则c(Na+)>c(CH COO-)>c(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合后水的电离程度小
答案 B
解析 A项,0.1 mol·L-1 CH COOH发生部分电离产生CH COO-和H+,水发生
3 3
微弱电离产生H+和OH-,故①中c(CH COOH)>c(H+)>c(CH COO-)>c(OH-),错
3 3
误;B项,①②等体积混合后恰好反应生成CH COONa,且c(CH COONa)=0.05
3 3
mol·L-1,由于①②混合后c(CH COONa)小于③,则混合液中CH COO-的水解程
3 3度比③大,故混合液中c(CH COO-)小于③中c(CH COO-),正确;C项,①③等体
3 3
积混合后为等物质的量的CH COOH和CH COONa的混合溶液,溶液显酸性说
3 3
明 CH COOH 的电离程度大于 CH COO-的水解程度,则 c(CH COO-)>c(Na
3 3 3
+)>c(H+),错误;D项,①②等体积混合后恰好生成CH COONa,CH COO-水解
3 3
促进水的电离,①③等体积混合后,由于CH COOH电离程度大于CH COO-的
3 3
水解程度,水的电离被抑制,故①②等体积混合后的水的电离程度比①③等体积
混合后水的电离程度大,错误。
一、选择题(每小题只有一个选项符合题意)
1.下列事实与盐类水解无关的是( )
A.MgCO 可以除去MgCl 酸性溶液中的Fe3+
3 2
B.氯化铁溶液常用作铜印刷电路板的腐蚀剂
C.常用热的纯碱溶液除去油污
D.长期施用硫酸铵易使土壤酸化
答案 B
解析 MgCO 调节pH,使Fe3+的水解平衡正向移动,使Fe3+沉淀完全,转化成
3
Fe(OH) ,MgCO 难溶于水,不引入新杂质,A项与盐类水解有关;氯化铁具有强
3 3
氧化性,可与铜发生氧化还原反应,可用于腐蚀铜印刷电路板,B项与盐类水解无
关;Na CO 的水解是吸热反应,故升高温度,溶液碱性增强,去油污能力增强,C
2 3
项和盐类的水解有关;铵态氮肥中铵根离子水解显酸性,长期施用硫酸铵易使土
壤酸化,D项与盐类水解有关。
2.对滴有酚酞溶液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.Na CO 溶液加热
2 3
C.氨水中加入少量NH Cl固体
4
D.小苏打溶液中加入少量NaCl固体
答案 B
3.向三份 0.1 mol·L-1 CH COONa 溶液中分别加入少量 NH NO 、Na CO 、
3 4 3 2 3
CH COONa固体(忽略溶液体积变化),则CH COO-浓度的变化依次为( )
3 3
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
答案 C解析 CH COONa是强碱弱酸盐,其水溶液显碱性,NH NO 是强酸弱碱盐,其水
3 4 3
溶液显酸性,所以向CH COONa溶液中加NH NO 固体会促进CH COO-的水解
3 4 3 3
导致 CH COO-浓度减小;Na CO 是强碱弱酸盐,其水溶液呈碱性,所以向
3 2 3
CH COONa溶液中加入Na CO 固体,会抑制CH COO-的水解,导致CH COO-
3 2 3 3 3
浓度增大,向CH COONa溶液中加入CH COONa固体,会导致CH COO-浓度增
3 3 3
大。
4.下列有关盐类水解的事实或应用、解释的说法不正确的是( )
选项 事实或应用 解释
纯碱与油污直接发生反
A 用热的纯碱溶液去除油污
应,生成易溶于水的物质
Al (SO ) 与 NaHCO 溶液
2 4 3 3
B 泡沫灭火器灭火
反应产生CO 气体
2
施肥时,草木灰(主要成分
K CO 与 NH Cl 反应生成
2 3 4
C K CO )与 NH Cl 不能混合
2 3 4
NH ,降低肥效
3
使用
明矾[KAl(SO ) ·12H O]作 明矾溶于水生成 Al(OH)
4 2 2 3
D
净水剂 胶体
答案 A
解析 用热的纯碱溶液去除油污,其原因是Na CO 水解使溶液显碱性,油脂在碱
2 3
性溶液中发生水解生成高级脂肪酸盐和甘油,并非纯碱与油污直接发生反应,A
项错误;泡沫灭火器灭火的反应原理是利用Al (SO ) 与NaHCO 溶液发生相互促
2 4 3 3
进的水解反应:Al3++3HCO===Al(OH) ↓+3CO ↑,生成CO 气体,B项正确;
3 2 2
K CO 是弱酸强碱盐,NH Cl是强酸弱碱盐,混合使用时,二者发生相互促进的水
2 3 4
解反应生成NH ,降低肥效,C项正确;明矾溶于水电离产生的Al3+发生水解反应,
3
生成Al(OH) 胶体,Al(OH) 胶体能吸附水中悬浮的杂质,从而起到净水作用,D
3 3
项正确。
5.25 ℃时,实验测得0.10 mol·L-1的NaHB溶液的pH=9.1。下列说法中正确的
是( )
A.NaHB的电离方程式为:NaHB===Na++H++B2-
B.HB-在水溶液中只存在HB-的水解平衡
C.HB-的水解程度大于电离程度
D.溶液中水电离出的c(H+)为10-9.1 mol·L-1答案 C
解析 HB-在水中不完全电离,A错误;HB-在水中水解程度大于电离程度,B错
误,C正确;HB-以水解为主,促进水的电离,D错误。
6.常温下,0.2 mol·L-1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶
液中部分微粒组分及浓度如图所示,下列说法正确的是( )
A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A-)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH-,Z表示H+
答案 C
解析 0.2 mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合,恰好生成
0.1 mol·L-1 NaA溶液,由题图中A-浓度小于0.1 mol·L-1,可知A-发生了水解,
故HA为弱酸,A项错误;NaA为强碱弱酸盐,水解使溶液显碱性,溶液pH>7.0,
B项错误;A-发生水解生成HA:A-+H OHA+OH-,同时还存在水的电离,
2
故溶液中除Na+、水分子外,各粒子的浓度大小关系为c(A-)>c(OH-)>c(HA)>
c(H+),故X为OH-,Y为HA,Z为H+,D项错误;根据物料守恒有:c(Na+)=c(A
-)+c(HA),C项正确。
7.25 ℃时浓度都是1 mol·L-1的四种正盐溶液:AX、BX、AY、BY;AX的溶液pH
=7且溶液中c(X-)=1 mol·L-1,BX的溶液pH=4,BY的溶液pH=6。下列说法
正确的是( )
A.电离常数K(BOH)小于K(HY)
B.AY溶液的pH小于BY溶液的pH
C.稀释相同倍数,溶液pH变化BX等于BY
D.将浓度均为1 mol·L-1的HX和HY溶液分别稀释10倍后,HX溶液的pH大
于HY
答案 A
解析 A项,根据BY溶液的pH=6,B+比Y-更易水解,则BOH比HY更难电离,
因此电离常数K(BOH)小于K(HY),正确;B项,根据AX、BX、BY溶液的pH可知,AX为强酸强碱盐,BX为强酸弱碱盐,BY为弱酸弱碱盐,则AY为弱酸强碱
盐,溶液的pH>7,故AY溶液的pH大于BY溶液的pH,错误;C项,稀释相同倍
数,BX、BY溶液的pH均增大,且BX溶液的pH变化大于BY溶液,错误;D项,
HX为强酸,HY为弱酸,浓度相同时,稀释10倍后,HY的电离程度增大,但仍不
可能全部电离,故HX溶液的酸性强,pH小,错误。
8.已知常温下,HCOOH比NH ·H O电离常数大。向10 mL 0.1 mol·L-1 HCOOH
3 2
中滴加同浓度的氨水,有关叙述正确的是( )
A.滴加过程中水的电离程度始终增大
B.当加入10 mL NH ·H O时,c(NH)>c(HCOO-)
3 2
C.当两者恰好中和时,溶液pH=7
D.滴加过程中n(HCOOH)与n(HCOO-)之和保持不变
答案 D
解析 A项,甲酸能够抑制水的电离,滴加氨水过程中,水的电离程度增大,氨水
过量时,抑制水的电离,所以滴加过程中水的电离程度先增大,恰好中和后再减
小,错误;B项,当加入10 mL NH ·H O时,恰好生成甲酸铵,HCOO-水解程度不
3 2
如NH水解程度大,溶液显酸性,c(NH)K (A2-),等物质的量浓度
a2 a2 a2 h
NaHA、Na A等体积混合,HA-的电离程度大于A2-的水解程度,所以c(HA-)<
2
c(A2-),故pH>3,D项错误。
12.(2020·广东广州、深圳学调联盟高三调研)已知:p[]=-lg[]。室温下,向0.10
mol/L HX溶液中滴加0.10 mol/LNaOH溶液,溶液pH随p[]变化关系如图所示。
下列说法正确的是( )
A.溶液中水的电离程度:a>b>c
B.c点溶液中:c(Na+)=10c(HX)
C.室温下NaX的水解常数为10-4.75
D.图中b点坐标为(0,4.75)
答案 D
解析 根据图示可知,a、b、c均为酸性溶液,则溶质为HX和NaX,pH<7的溶液
中,HX的电离程度大于X-的水解程度,可只考虑H+对水的电离的抑制,溶液
pH越大氢离子浓度越小,水的电离程度越大,则溶液中水的电离程度:a”“<”或“=”)。
(5)25 ℃时,测得 HCN 和 NaCN 的混合溶液的 pH=11,则约为________。向
NaCN溶液中通入少量CO ,则发生反应的离子方程式为__________________
2
______________________________________________________。
答案 (1)②>①>④>③ 1.0×10-13 mol·L-1
(2)c(Na+)>c(CN-)>c(OH-)>c(H+)
(3)2.5×10-8
(4)< (5)0.02 CN-+CO +H O===HCN+HCO
2 2
解析 (1)相同浓度的4种溶液中,NaCN溶液水解显碱性,NaOH溶液为强碱溶
液,CH COONa 溶液水解显碱性,NaHCO 溶液水解显碱性,因为酸性:
3 3
CH COOH>H CO >HCN>HCO,越弱越水解,因此溶液的碱性:②>①>④>
3 2 3
③,4种溶液pH由大到小的顺序是②>①>④>③;0.1 mol·L-l的NaOH pH=
13,由水电离的H+浓度为1.0×10-13 mol·L-1。(2)NaCN溶液中CN-水解,溶液显
碱性,离子浓度大小关系为 c(Na+)>c(CN-)>c(OH-)>c(H+)。(3)K ====
h
2.5×10-8。(4)等体积等浓度的CH COONa溶液和NaHCO 溶液,NaHCO 水解程
3 3 3
度大于CH COONa,溶液的碱性强于CH COONa,滴加盐酸至呈中性,则消耗盐
3 3
酸的体积③<④。(5)由HCN的电离常数K =可知,==≈0.02,H CO 的一级电
a 2 3
离常数大于HCN,二级电离常数小于HCN,故H CO 的酸性强于HCN,HCO的
2 3
酸性弱于HCN,故向NaCN溶液中通入少量CO ,反应生成HCN与NaHCO ,该
2 3
反应的离子方程式为CN-+CO +H O===HCN+HCO。
2 2
15.NH Al(SO ) 是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH HSO
4 4 2 4 4
在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其理由是___________________________________
4 4 2
_____________________________________________________________________
(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1 NH Al(SO ) 中c(NH)________(填“等于”“大于”
4 4 2或“小于”)0.1 mol·L-1 NH HSO 中c(NH)。
4 4
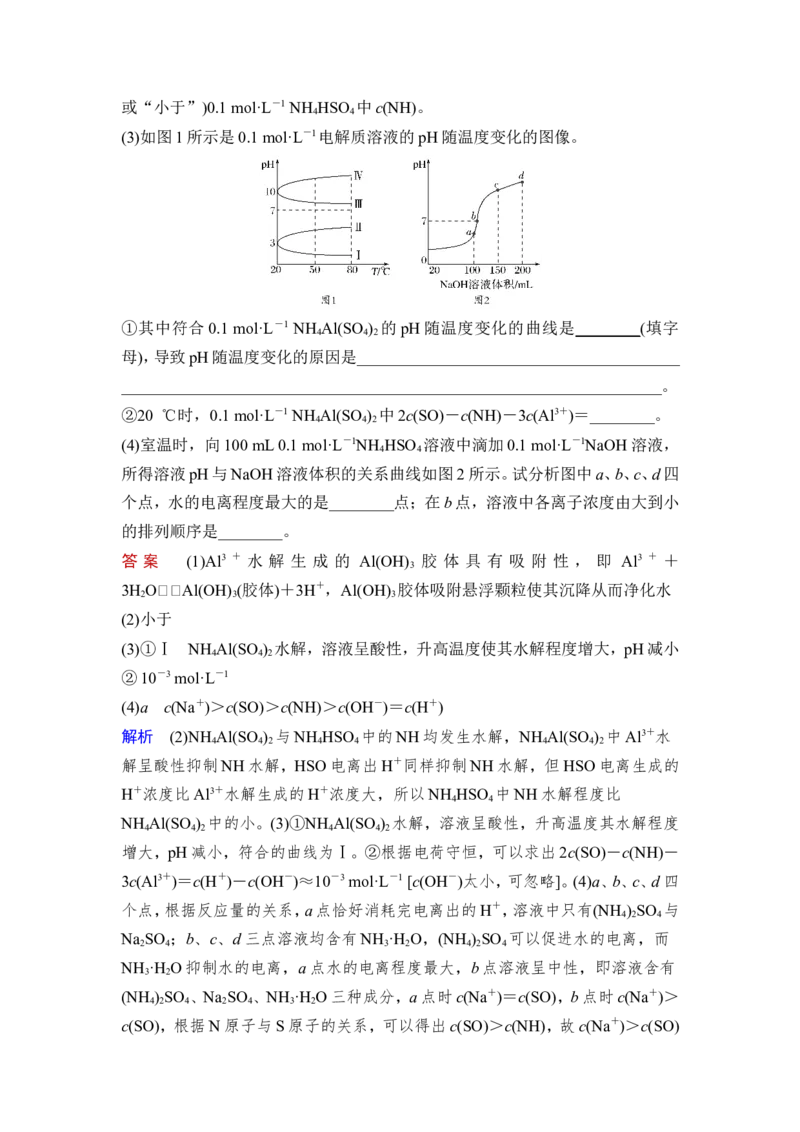
(3)如图1所示是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1 NH Al(SO ) 的pH随温度变化的曲线是________(填字
4 4 2
母),导致pH随温度变化的原因是________________________________________
___________________________________________________________________。
②20 ℃时,0.1 mol·L-1 NH Al(SO ) 中2c(SO)-c(NH)-3c(Al3+)=________。
4 4 2
(4)室温时,向100 mL 0.1 mol·L-1NH HSO 溶液中滴加0.1 mol·L-1NaOH溶液,
4 4
所得溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四
个点,水的电离程度最大的是________点;在b点,溶液中各离子浓度由大到小
的排列顺序是________。
答 案 (1)Al3 + 水 解 生 成 的 Al(OH) 胶 体 具 有 吸 附 性 , 即 Al3 + +
3
3H OAl(OH) (胶体)+3H+,Al(OH) 胶体吸附悬浮颗粒使其沉降从而净化水
2 3 3
(2)小于
(3)①Ⅰ NH Al(SO ) 水解,溶液呈酸性,升高温度使其水解程度增大,pH减小
4 4 2
②10-3 mol·L-1
(4)a c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)
解析 (2)NH Al(SO ) 与NH HSO 中的NH均发生水解,NH Al(SO ) 中Al3+水
4 4 2 4 4 4 4 2
解呈酸性抑制NH水解,HSO电离出H+同样抑制NH水解,但HSO电离生成的
H+浓度比Al3+水解生成的H+浓度大,所以NH HSO 中NH水解程度比
4 4
NH Al(SO ) 中的小。(3)①NH Al(SO ) 水解,溶液呈酸性,升高温度其水解程度
4 4 2 4 4 2
增大,pH减小,符合的曲线为Ⅰ。②根据电荷守恒,可以求出2c(SO)-c(NH)-
3c(Al3+)=c(H+)-c(OH-)≈10-3 mol·L-1 [c(OH-)太小,可忽略]。(4)a、b、c、d四
个点,根据反应量的关系,a点恰好消耗完电离出的H+,溶液中只有(NH ) SO 与
4 2 4
Na SO ;b、c、d三点溶液均含有NH ·H O,(NH ) SO 可以促进水的电离,而
2 4 3 2 4 2 4
NH ·H O抑制水的电离,a点水的电离程度最大,b点溶液呈中性,即溶液含有
3 2
(NH ) SO 、Na SO 、NH ·H O三种成分,a点时c(Na+)=c(SO),b点时c(Na+)>
4 2 4 2 4 3 2
c(SO),根据N原子与S原子的关系,可以得出c(SO)>c(NH),故c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)。
微专题30 电解质溶液中“粒子”浓度关系
(一)熟悉两大理论,构建思维基点
(1)电离平衡→建立电离过程是微弱的意识
弱电解质(弱酸、弱碱、水)的电离是微弱的,且水的电离能力远远小于弱酸和弱碱
的电离能力。如在稀醋酸溶液中:CH COOHCH COO-+H+,H OOH-+H
3 3 2
+,粒子浓度由大到小的顺序:c(CH COOH)>c(H+)>c(CH COO-)>c(OH-)。
3 3
(2)水解平衡→建立水解过程是微弱的意识
弱酸根离子或弱碱阳离子的水解是微弱的,但水的电离程度远远小于盐的水解程
度。如稀的CH COONa溶液中:CH COONa===CH COO-+Na+,CH COO-+
3 3 3 3
H OCH COOH+OH-,H OH++OH-,粒子浓度由大到小的顺序:c(Na+)
2 3 2
>c(CH COO-)>c(OH-)>c(CH COOH)>c(H+)。
3 3
(二)把握三大守恒,明确定量关系
1.物料守恒(原子守恒)
在电解质溶液中,由于某些离子能够水解,粒子种类增多,但这些粒子所含某些
原子的总数始终不变,符合原子守恒。如NaHCO 溶液中,因HCO水解:HCO+
3
H OH CO +OH-以及HCO电离:HCOH++CO,C元素的存在形式有3
2 2 3
种,即HCO、H CO 、CO,由n(Na+)∶n(C原子)=1∶1,得c(Na+)=c(HCO)+
2 3
c(CO)+c(H CO )。
2 3
2.电荷守恒
在电解质溶液中,阳离子的电荷总数与阴离子的电荷总数相等,即溶液呈电中性
如NaHCO 溶液中有Na+、H+、HCO、CO、OH-,存在如下关系:c(Na+)+c(H+)=
3
c(HCO)+2c(CO)+c(OH-)(因CO带2个单位负电荷,所以其所带电荷数为其离
子数的2倍)。
3.质子守恒
电解质溶液中分子或离子得到或失去质子(H+)的物质的量相等。例如:
(1)在Na CO 溶液中:
2 3
质子守恒:c(OH-)=c(H+)+c(HCO)+2c(H CO )。
2 3(2)在NaHCO 溶液中:
3
质子守恒:c(H+)+c(H CO )=c(OH-)+c(CO)。
2 3
另外,质子守恒式可以由电荷守恒式和物料守恒式推导得出。以KHS溶液为例,
电荷守恒式为c(K+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)①,物料守恒式为c(K+)
=c(HS-)+c(S2-)+c(H S)②,由①-②消去没有参与变化的K+得质子守恒式
2
c(H+)+c(H S)=c(OH-)+c(S2-)。
2
(三)明晰三大类型,掌握解题流程
溶液中粒子浓度大小比较三大类型
类型一 单一溶液中各粒子浓度的比较
(1)多元弱酸溶液:多元弱酸分步电离,电离程度逐级减弱,如H PO 溶液中:c(H
3 4
+)>c(H PO)>c(HPO)>c(PO)。
2
(2)多元弱酸的正盐溶液:多元弱酸的酸根离子分步水解,水解程度逐级减弱。如
在Na CO 溶液中:c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H CO )。
2 3 2 3
类型二 混合溶液中各粒子浓度的比较
混合溶液要综合分析电离、水解等因素。如在0.1 mol·L-1 NH Cl溶液和0.1 mol·L
4
-1的氨水混合溶液中,NH ·H O的电离程度强于NH的水解程度,溶液呈碱性,各
3 2
离子浓度大小顺序为c(NH)>c(Cl-)>c(OH-)>c(H+)。
类型三 不同溶液中同一粒子浓度的比较
不同溶液要看溶液中其他离子对该离子的影响。
如在相同物质的量浓度的下列溶液中:①NH Cl;②CH COONH ;③NH HSO ,
4 3 4 4 4
c(NH)由大到小的顺序为③>①>②。
(四)分类精析
1.单一溶液中离子浓度的关系
【典例1】 0.1 mol·L-1的Na CO 溶液中各离子浓度的关系
2 3
(1)大小关系:______________________________________________________。
(2)物料守恒:______________________________________________________。
(3)电荷守恒:______________________________________________________。
(4)质子守恒:______________________________________________________。
答案 (1)c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)(2)c(Na+)=2[c(CO)+c(HCO)+c(H CO )]
2 3
(3)c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)
(4)c(OH-)=c(H+)+c(HCO)+2c(H CO )
2 3
解析 Na CO ===2Na++CO(完全电离),
2 3
CO+H OHCO+OH-(主要),
2
HCO+H OH CO +OH-(次要),
2 2 3
H OH++OH-(极微弱)。
2
【典例2】 0.1 mol·L-1的NaHCO 溶液中各离子浓度的关系
3
(1)大小关系:______________________________________________________。
(2)物料守恒:______________________________________________________。
(3)电荷守恒:_____________________________________________________。
(4)质子守恒:______________________________________________________。
答案 (1)c(Na+)>c(HCO)>c(OH-)>c(H+)>c(CO)
(2)c(Na+)=c(HCO)+c(CO)+c(H CO )
2 3
(3)c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-)
(4)c(OH-)=c(H CO )+c(H+)-c(CO)
2 3
解析 NaHCO ===Na++HCO(完全电离),
3
HCO+H OH CO +OH-(主要),
2 2 3
HCOH++CO(次要),
H OH++OH-(极微弱)。
2
规避等量关系中的2个易失分点
①电荷守恒式中不只是各离子浓度的简单相加。如2c(CO)的化学计量数2代表
一个CO带2个负电荷,不可漏掉。
②物料守恒式中,离子浓度系数不能漏写或颠倒。如Na S溶液中的物料守恒式中
2
“2”表示c(Na+)是溶液中各种含硫原子离子总浓度的2倍。
2.混合溶液中离子浓度的关系
【典例3】 浓度均为0.1 mol·L-1的NH Cl和氨水的混合溶液中粒子浓度关系
4
(1)电荷守恒:______________________________________________________。
(2)物料守恒:______________________________________________________。
(3)质子守恒:______________________________________________________。(4)大小关系:______________________________________________________。
答案 (1)c(NH)+c(H+)=c(Cl-)+c(OH-)
(2)c(NH)+c(NH ·H O)=2c(Cl-)
3 2
(3)c(NH)+2c(H+)=c(NH ·H O)+2c(OH-)
3 2
(4)c(NH)>c(Cl-)>c(NH ·H O)>c(OH-)>c(H+)
3 2
解析 NH Cl===NH+Cl-(完全电离),
4
NH ·H ONH+OH-(主要,混合液呈碱性),
3 2
NH+H ONH ·H O+H+(次要),
2 3 2
H OH++OH-(极微弱)。
2
【典例4】 浓度均为0.1 mol·L-1的CH COONa和CH COOH的混合溶液中粒子
3 3
浓度关系
(1)电荷守恒:______________________________________________________。
(2)物料守恒:______________________________________________________。
(3)质子守恒:______________________________________________________。
(4)大小关系:_____________________________________________________。
答案 (1)c(Na+)+c(H+)=c(CH COO-)+c(OH-)
3
(2)c(CH COO-)+c(CH COOH)=2c(Na+)
3 3
(3)c(CH COOH)+2c(H+)=c(CH COO-)+2c(OH-)
3 3
(4)c(CH COO-)>c(Na+)>c(CH COOH)>c(H+)>c(OH-)
3 3
解析 CH COONa===CH COO-+Na+(完全电离),
3 3
CH COOHCH COO-+H+(主要,混合液呈酸性),
3 3
CH COO-+H OCH COOH+OH-(次要),
3 2 3
H OH++OH-(极微弱)。
2
【典例5】 浓度均为0.1 mol·L-1的Na CO 和NaHCO 的混合溶液中离子浓度关
2 3 3
系
(1)电荷守恒:______________________________________________________。
(2)物料守恒:_____________________________________________________。
(3)质子守恒:______________________________________________________。
(4)大小关系:______________________________________________________。
答案 (1)c(Na+)+c(H+)=c(OH-)+c(HCO)+2c(CO)
(2)2c(Na+)=3[c(CO)+c(HCO)+c(H CO )]
2 3
(3)2c(OH-)+c(CO)=2c(H+)+c(HCO)+3c(H CO )
2 3(4)c(Na+)>c(HCO)>c(CO)>c(OH-)>c(H+)
解析 Na CO ===2Na++CO(完全电离),
2 3
NaHCO ===Na++HCO(完全电离),
3
CO+H OHCO+OH-(主要,CO的水解程度大于HCO的水解程度),
2
HCO+H OH CO +OH-(次要),
2 2 3
HCOH++CO(微弱),
H OH++OH-(极微弱)。
2
3.不同溶液中同一离子浓度大小的比较
[解题流程]
【典例6】 25 ℃时,相同物质的量浓度的下列溶液中:
①NH Cl、②CH COONH 、③NH HSO 、④(NH ) SO 、⑤(NH ) Fe(SO ) ,c(NH)由
4 3 4 4 4 4 2 4 4 2 4 2
大到小的顺序为________。
答案 ⑤>④>③>①>②
解析 分析流程为
分组――→
1.室温下,下列溶液中粒子浓度关系正确的是( )
A.Na S溶液:c(Na+)>c(HS-)>c(OH-)>c(H S)
2 2
B.Na C O 溶液:c(OH-)=c(H+)+c(HC O)+2c(H C O )
2 2 4 2 2 2 4
C.Na CO 溶液:c(Na+)+c(H+)=2c(CO)+c(OH-)
2 3
D.CH COONa 和 CaCl 混合溶液:c(Na+)+c(Ca2+)=c(CH COO-)+
3 2 3
c(CH COOH)+2c(Cl-)
3
答案 B
解析 A项,由于S2-+H OHS-+OH-、HS-+H OH S+OH-、H OH
2 2 2 2++OH-,故粒子浓度关系应为c(Na+)>c(OH-)>c(HS-)>c(H S),错误;B项,符
2
合电解质溶液中质子守恒关系,正确;C项,根据电荷守恒有c(Na+)+c(H+)=
c(HCO)+2c(CO)+c(OH-),错误;D项,根据物料守恒,离子浓度的关系应为
c(Na+)+c(Ca2+)=c(CH COO-)+c(CH COOH)+c(Cl-),错误。
3 3
2.(2020·河北唐山市高三期末)已知氢硫酸(H S) 的电离平衡常数为: K (H S)=
2 a1 2
9.1×10-8, K (H S)=1.1×10 -12。H S溶液中c(总)=c(H S)+c(HS-)+c(S2-)。室
a2 2 2 2
温下向25.00 mL 0.100 0 mol·L-1 H S 溶液中逐滴滴入NaOH溶液。下列说法正确
2
的是( )
A.随着NaOH溶液滴入,溶液中水的电离程度不断增大
B.c(Na+)=c(总)的溶液: c(Na +)>c(S2-)>c(H S)>c(H+)
2
C.pH=7的溶液: c(Na+)>c(S2-)>c(HS-)>c(OH-)=c(H+)
D.c(H+)=9.1×10-8 mol·L-1时: c(H S)+2c(S2-)+c(OH-)=c(Na +)+c(H+)
2
答案 D
解析 A.H S是二元弱酸,在溶液中抑制水的电离,向25.00 mL 0.100 0 mol·L-1
2
H S溶液中逐滴滴入NaOH溶液,H S与NaOH反应生成NaHS、Na S时,由于
2 2 2
NaHS、Na S水解,促进水的电离,溶液中水的电离程度不断增大,当H S完全反
2 2
应,再滴入NaOH溶液,溶液中过量的NaOH抑制水的电离,水的电离程度会减
小,故A错误;B.c(Na+)=c(总)的溶液为NaHS溶液,NaHS的水解常数K ==>
h
K =1.1×10 -12,溶液中NaHS的水解程度大于电离程度,NaHS溶液呈碱性, 溶
a2
液中c(H S)>c(S2-),故B错误;C.因NaHS溶液呈碱性,pH=7的溶液为H S与
2 2
NaHS的混合溶液,则溶液中c(HS-)>c(S2-),故C错误;D.由K ==9.1×10-8
a1
可知c(H+)=9.1×10-8 mol·L-1时,溶液中c(H S)=c(HS-),由电荷守恒c(HS-)
2
+2c(S2-)+c(OH-)=c(Na +)+c(H+)可得c(H S)+2c(S2-)+c(OH-)=c(Na +)+
2
c(H+),故D正确。
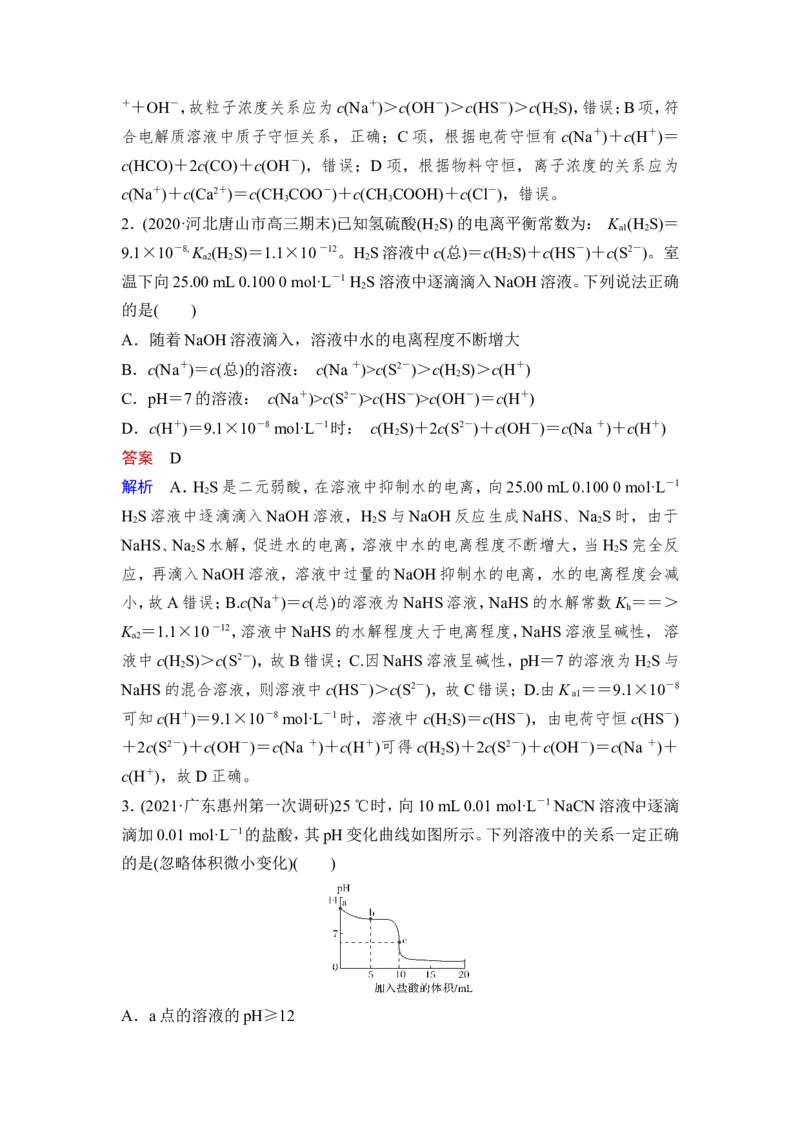
3.(2021·广东惠州第一次调研)25 ℃时,向10 mL 0.01 mol·L-1 NaCN溶液中逐滴
滴加0.01 mol·L-1的盐酸,其pH变化曲线如图所示。下列溶液中的关系一定正确
的是(忽略体积微小变化)( )
A.a点的溶液的pH≥12B.b点的溶液:c(CN-)>c(HCN)
C.c点的溶液:c(CN-)+c(HCN)+c(Cl-)=0.01 mol·L-1
D.pH=7的溶液:c(Na+)+c(H+)=c(Cl-)+c(CN-)
答案 C
解析 NaCN溶液的pH>7,说明NaCN是强碱弱酸盐,CN-在水溶液中部分水
解,若NaCN完全水解,则溶液的pH等于12,而CN-不能完全水解,故a点溶液
pH小于12,A项错误;b点加入了5 mL盐酸,溶液中的溶质为等物质的量的
NaCN、NaCl、HCN,此时溶液显碱性,说明NaCN的水解程度大于HCN的电离程
度,c(CN-)<c(HCN),B项错误;c点加入10 mL盐酸,溶液中的溶质为NaCl、
HCN,根据物料守恒知溶液中 c(CN-)+c(HCN)+c(Cl-)=(10×10-3 L×0.01
mol·L-1+10×10-3 L×0.01 mol·L-1)÷(20×10-3 L)=0.01 mol·L-1,C项正确;pH
=7时c(OH-)=c(H+),根据电荷守恒:c(CN-)+c(OH-)+c(Cl-)=c(Na+)+c(H
+),可得c(CN-)+c(Cl-)=c(Na+),D项错误。
4.有4种混合溶液,分别由等体积0.1 mol·L-1的两种溶液混合而成:①NH Cl与
4
CH COONa ② NH Cl 与 HCl ③ NH Cl 与 NaCl ④ NH Cl 与 NH ·H O(混合
3 4 4 4 3 2
液呈碱性)下列各项排序正确的是( )
A.pH:②<①<③<④
B.c(NH):①<③<②<④
C.溶液中c(H+):①<③<②<④
D.c(NH ·H O):①<③<④<②
3 2
答案 B
解析 ①中NH Cl水解呈酸性与水解呈碱性的CH COONa混合,水解相互促进,
4 3
但溶液接近中性;②中NH Cl水解呈酸性被 HCl 抑制,但溶液呈酸性;③中
4
NH Cl与NaCl混合,为单水解呈酸性;④NH Cl与相应的碱NH ·H O(混合液呈
4 4 3 2
碱性)混合,则说明电离程度大于水解程度。所以由分析可知pH:②<③<①<④,
A错误;c(NH):①<③<②<④,B正确;溶液中c(H+):④ <①<③<②,C错
误;c(NH ·H O):②<③<①<④,D错误,故选B。
3 2
5.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数
据如下表:
起始浓度/(mol·L-1)
实验编号 反应后溶液的pH
c(HA) c(KOH)
① 0.1 0.1 9② x 0.2 7
下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol·L-1
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
答案 B
解析 实验①反应后溶液的pH=9,即溶液显碱性,说明HA为弱酸,二者等浓度
等体积混合恰好反应生成KA,A-水解,A项正确;实验①反应后的溶液中,由电
荷守恒式c(H+)+c(K+)=c(A-)+c(OH-)知,c(K+)-c(A-)=c(OH-)-c(H+),B
项错误;因为HA为弱酸,如果与等体积等浓度的KOH溶液混合,溶液显碱性,
若溶液显中性,则在两溶液体积相等的条件下,HA溶液的浓度应大于0.2 mol·L-
1,所以实验②反应后的溶液中,c(A-)+c(HA)>0.1 mol·L-1,C项正确;实验②反
应后溶液显中性,根据电荷守恒式c(H+)+c(K+)=c(A-)+c(OH-),且c(H+)=
c(OH-),则c(K+)=c(A-),即c(K+)=c(A-)>c(H+)=c(OH-),D项正确。
6.(双选)(2019·江苏化学)室温下,反应HCO+H OH CO +OH-的平衡常数
2 2 3
K=2.2×10-8。将NH HCO 溶液和氨水按一定比例混合,可用于浸取废渣中的
4 3
ZnO。若溶液
混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确
的是( )
A.0.2 mol·L-1氨水:c(NH ·H O)>c(NH)>c(OH-)>c(H+)
3 2
B.0.2 mol·L-1 NH HCO 溶液(pH>7):c(NH)>c(HCO)>c(H CO )>c(NH ·H O)
4 3 2 3 3 2
C.0.2 mol·L-1 氨水和 0.2 mol·L-1 NH HCO 溶液等体积混合:c(NH)+
4 3
c(NH ·H O)=c(H CO )+c(HCO)+c(CO)
3 2 2 3
D.0.6 mol·L-1氨水和 0.2 mol·L-1 NH HCO 溶液等体积混合:c(NH ·H O)+
4 3 3 2
c(CO)+c(OH-)=0.3 mol·L-1+c(H CO )+c(H+)
2 3
答案 BD
解析 A项,氨水中存在 NH ·H ONH+OH-,H OH++OH-,氨水中
3 2 2
NH ·H O部分电离,所以主要以NH ·H O分子形式存在,两个电离方程式均电离
3 2 3 2
出OH-,所以c(OH-)>c(NH),错误;B项,NH HCO 溶液显碱性,说明HCO的
4 3
水解程度大于NH的水解程度,所以c(NH)>c(HCO)>c(H CO )>c(NH ·H O),
2 3 3 2
正确;C项,由物料守恒可知,n(N)∶n(C)=2∶1,则有c(NH)+c(NH ·H O)=
3 22[c(H CO )+c(HCO)+c(CO)],错误;D项,由物料守恒可知,n(N)∶n(C)=4∶1,
2 3
则有 c(NH)+c(NH ·H O)=4[c(H CO )+c(HCO)+c(CO)]①,电荷守恒式为
3 2 2 3
c(NH)+c(H+)=c(HCO)+2c(CO)+c(OH-)②,结合①②消去 c(NH),得:
c(NH ·H O)+c(OH-)=c(H+)+4c(H CO )+3c(HCO)+2c(CO)③,0.2 mol·L-1
3 2 2 3
NH HCO 溶液与0.6 mol·L-1氨水等体积混合后,c(NH HCO )=0.1 mol·L-1,由
4 3 4 3
碳元素守恒可知,c(H CO )+c(HCO)+c(CO)=0.1 mol·L-1④,将③等式两边各加
2 3
一个c(CO),则有c(NH ·H O)+c(OH-)+c(CO)=c(H+)+c(H CO )+3c(H CO )+
3 2 2 3 2 3
3c(HCO)+3c(CO)⑤,将④代入⑤中得,c(NH ·H O)+c(OH-)+c(CO)=c(H+)+
3 2
c(H CO )+0.3 mol·L-1,正确。
2 3
微专题31 中和滴定过程中的“粒子”浓度关系
抓住滴定曲线中的“五点”,破解溶液中的“粒子”浓度关系
酸、碱中和反应过程中,溶液中的离子浓度随酸、碱的加入会发生变化,可借助滴
定图像,抓住反应的关键点,破解离子浓度大小比较。
以用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 HA溶液为例,其
滴定曲线如图。
关键点 离子浓度关系
O点时为HA的单一溶液,0.100 0 mol·L-1 HA的pH>
点O
1,说明是弱酸,c(HA)>c(H+)>c(A-)>c(OH-)
溶液中含有等物质的量HA和NaA,此时溶液pH<7,说
点① 明 HA 电离程度大于 A-水解程度,c(A-)>c(Na+)>
c(HA)>c(H+)>c(OH-)
此时溶液pH=7,溶液呈中性,酸没有完全被反应,c(A-)
点②
=c(Na+)>c(HA)>c(H+)=c(OH-)
此时两者恰好反应生成NaA,为强碱弱酸盐,c(Na+)>
点③
c(A-)>c(OH-)>c(H+)
此时NaOH过量或者远远过量,溶液显碱性,可能出现
点③之后 c(Na+)>c(A-)>c(OH-)>c(H+),也可能出现c(Na+)>
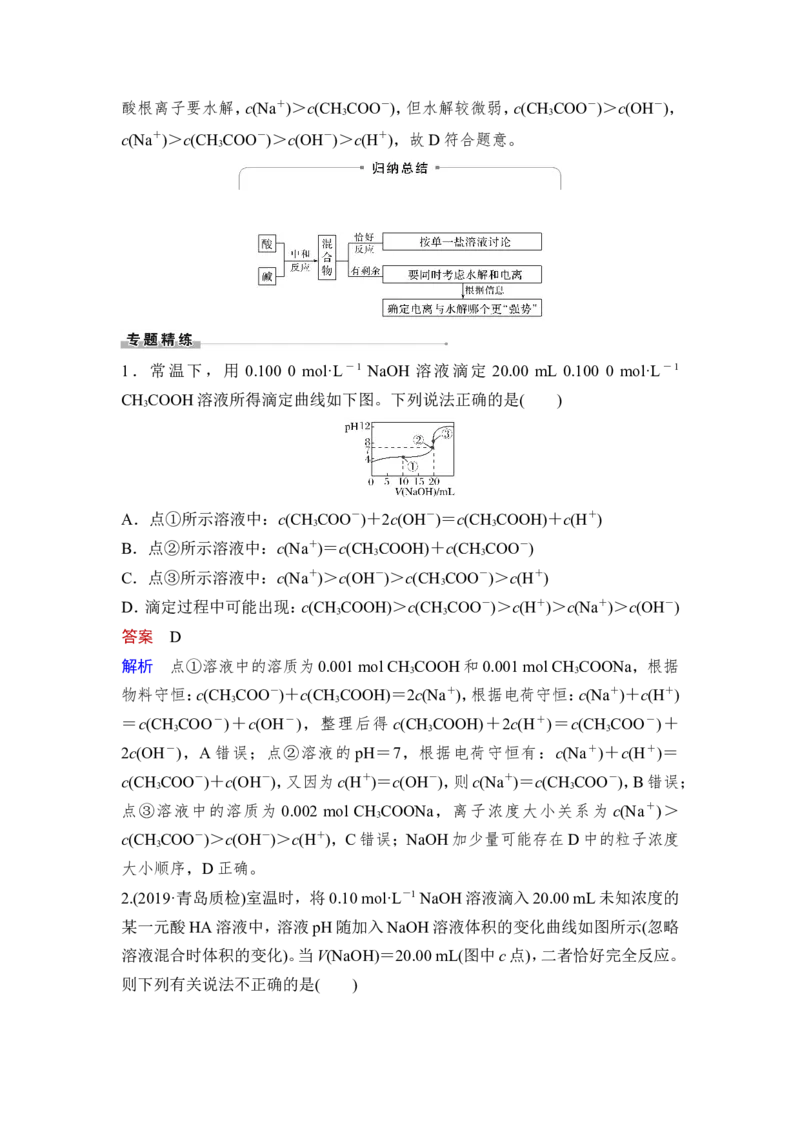
c(OH-)>c(A-)>c(H+)【典例】 (双选)(2021·1月湖南普高校招生适应性考试,14)常温下,向20.00 mL
0.100 0 mol·L-1的CH COOH溶液中滴加0.100 0 mol-1的NaOH溶液,溶液中,lg
3
随pH的变化关系如图所示(取lg 5=0.7)。
INCLUDEPICTURE "G:\\2021课件\\X8.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\X8.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\X8.TIF" \* MERGEFORMATINET
下列说法正确的是( )
A.常温下,CH COOH的电离常数为10-4.76
3
B.当溶液的pH=7时,消耗NaOH溶液20.00 mL
C.溶液中水的电离程度大小:a>b>c
D.c点溶液中:c(Na+)>c(CH COO-)>c(OH-)>c(H+)
3
答案 AD
解析 常温下,CH COOH 的电离常数 K =,b 点 pH=4.76 时,lg=0,
3 a
c(CH COOH)=c(CH COO-),CH COOH的电离常数等于c(H+)=10-4.76,故A符
3 3 3
合题意;向20.00 mL 0.100 0 mol·L-1的CH COOH溶液中滴加0.100 0 mol·L-1的
3
NaOH溶液20 mL,溶质为CH COONa,为弱酸强碱盐,水解显碱性,此时溶液的
3
pH>7,故B不符合题意;酸碱抑制水的电离,弱酸强碱盐水解显碱性,促进水的
电离,a点为CH COOH,K ===10-9.24,CH COONa存在水解平衡,K = ,pH
3 h 3 h
=8.73时,c(OH-)==10-5.27,lg=3.97,=10-3.97,K ==10-3.97×10-5.27=10-9.24
h
=K ,c点为CH COONa溶液,b点为CH COOH和CH COONa的混合溶液,溶
h 3 3 3
液中水的电离程度大小:c>b>a,故C不符合题意;CH COONa溶液中,由于醋
3酸根离子要水解,c(Na+)>c(CH COO-),但水解较微弱,c(CH COO-)>c(OH-),
3 3
c(Na+)>c(CH COO-)>c(OH-)>c(H+),故D符合题意。
3
1.常温下,用 0.100 0 mol·L-1 NaOH 溶液滴定 20.00 mL 0.100 0 mol·L-1
CH COOH溶液所得滴定曲线如下图。下列说法正确的是( )
3
A.点①所示溶液中:c(CH COO-)+2c(OH-)=c(CH COOH)+c(H+)
3 3
B.点②所示溶液中:c(Na+)=c(CH COOH)+c(CH COO-)
3 3
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH COO-)>c(H+)
3
D.滴定过程中可能出现:c(CH COOH)>c(CH COO-)>c(H+)>c(Na+)>c(OH-)
3 3
答案 D
解析 点①溶液中的溶质为0.001 mol CH COOH和0.001 mol CH COONa,根据
3 3
物料守恒:c(CH COO-)+c(CH COOH)=2c(Na+),根据电荷守恒:c(Na+)+c(H+)
3 3
=c(CH COO-)+c(OH-),整理后得 c(CH COOH)+2c(H+)=c(CH COO-)+
3 3 3
2c(OH-),A 错误;点②溶液的 pH=7,根据电荷守恒有:c(Na+)+c(H+)=
c(CH COO-)+c(OH-),又因为c(H+)=c(OH-),则c(Na+)=c(CH COO-),B错误;
3 3
点③溶液中的溶质为 0.002 mol CH COONa,离子浓度大小关系为 c(Na+)>
3
c(CH COO-)>c(OH-)>c(H+),C错误;NaOH加少量可能存在D中的粒子浓度
3
大小顺序,D正确。
2.(2019·青岛质检)室温时,将0.10 mol·L-1 NaOH溶液滴入20.00 mL未知浓度的
某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图所示(忽略
溶液混合时体积的变化)。当V(NaOH)=20.00 mL(图中c点),二者恰好完全反应。
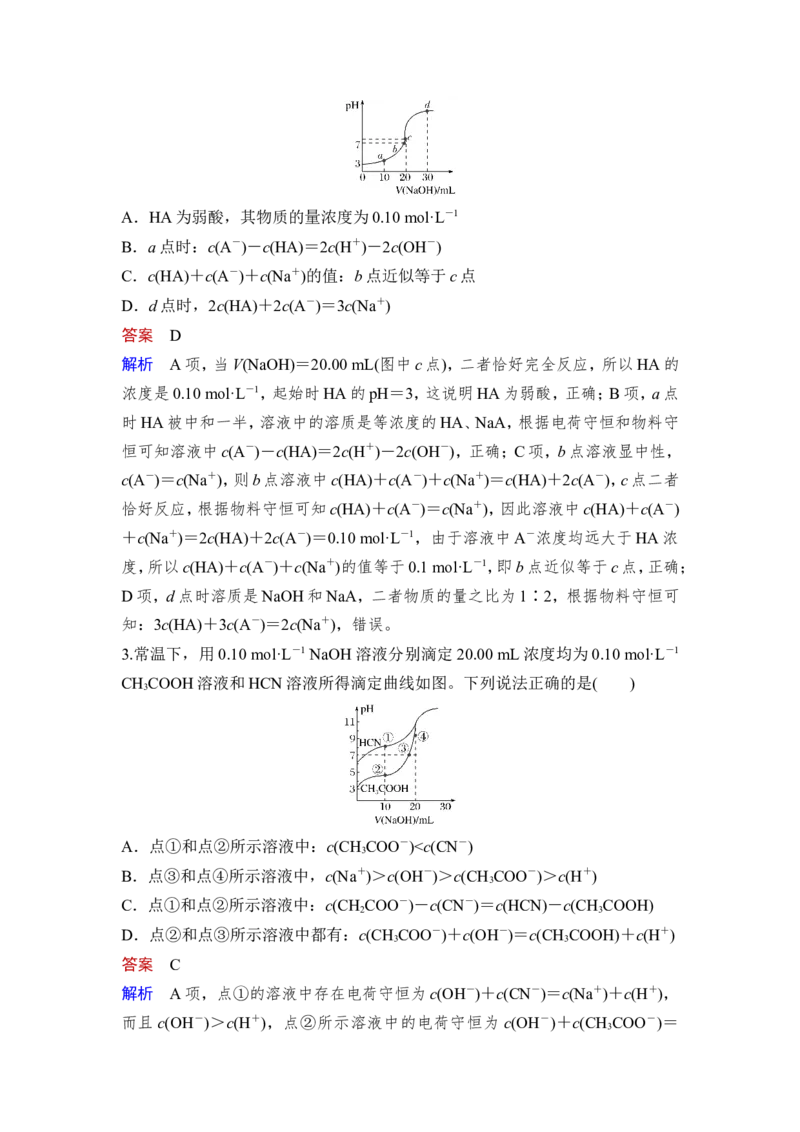
则下列有关说法不正确的是( )A.HA为弱酸,其物质的量浓度为0.10 mol·L-1
B.a点时:c(A-)-c(HA)=2c(H+)-2c(OH-)
C.c(HA)+c(A-)+c(Na+)的值:b点近似等于c点
D.d点时,2c(HA)+2c(A-)=3c(Na+)
答案 D
解析 A项,当V(NaOH)=20.00 mL(图中c点),二者恰好完全反应,所以HA的
浓度是0.10 mol·L-1,起始时HA的pH=3,这说明HA为弱酸,正确;B项,a点
时HA被中和一半,溶液中的溶质是等浓度的HA、NaA,根据电荷守恒和物料守
恒可知溶液中c(A-)-c(HA)=2c(H+)-2c(OH-),正确;C项,b点溶液显中性,
c(A-)=c(Na+),则b点溶液中c(HA)+c(A-)+c(Na+)=c(HA)+2c(A-),c点二者
恰好反应,根据物料守恒可知c(HA)+c(A-)=c(Na+),因此溶液中c(HA)+c(A-)
+c(Na+)=2c(HA)+2c(A-)=0.10 mol·L-1,由于溶液中A-浓度均远大于HA浓
度,所以c(HA)+c(A-)+c(Na+)的值等于0.1 mol·L-1,即b点近似等于c点,正确;
D项,d点时溶质是NaOH和NaA,二者物质的量之比为1∶2,根据物料守恒可
知:3c(HA)+3c(A-)=2c(Na+),错误。
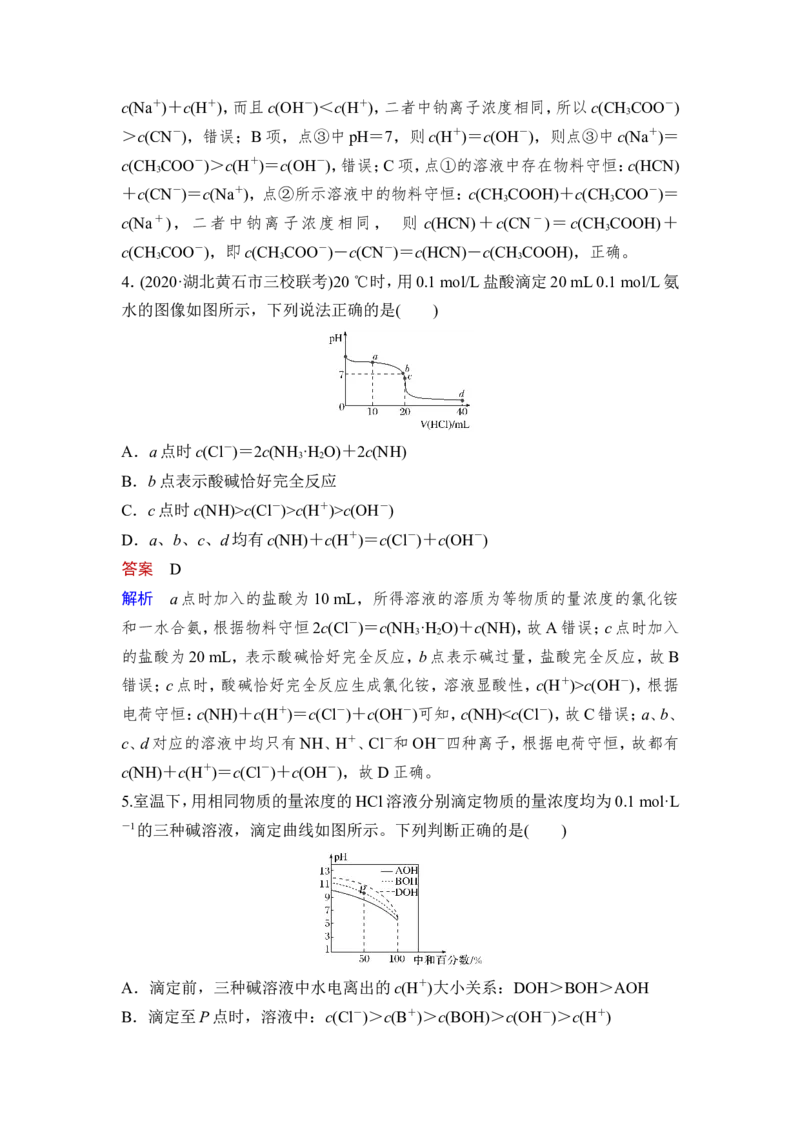
3.常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L-1
CH COOH溶液和HCN溶液所得滴定曲线如图。下列说法正确的是( )
3
A.点①和点②所示溶液中:c(CH COO-)c(Cl-)>c(H+)>c(OH-)
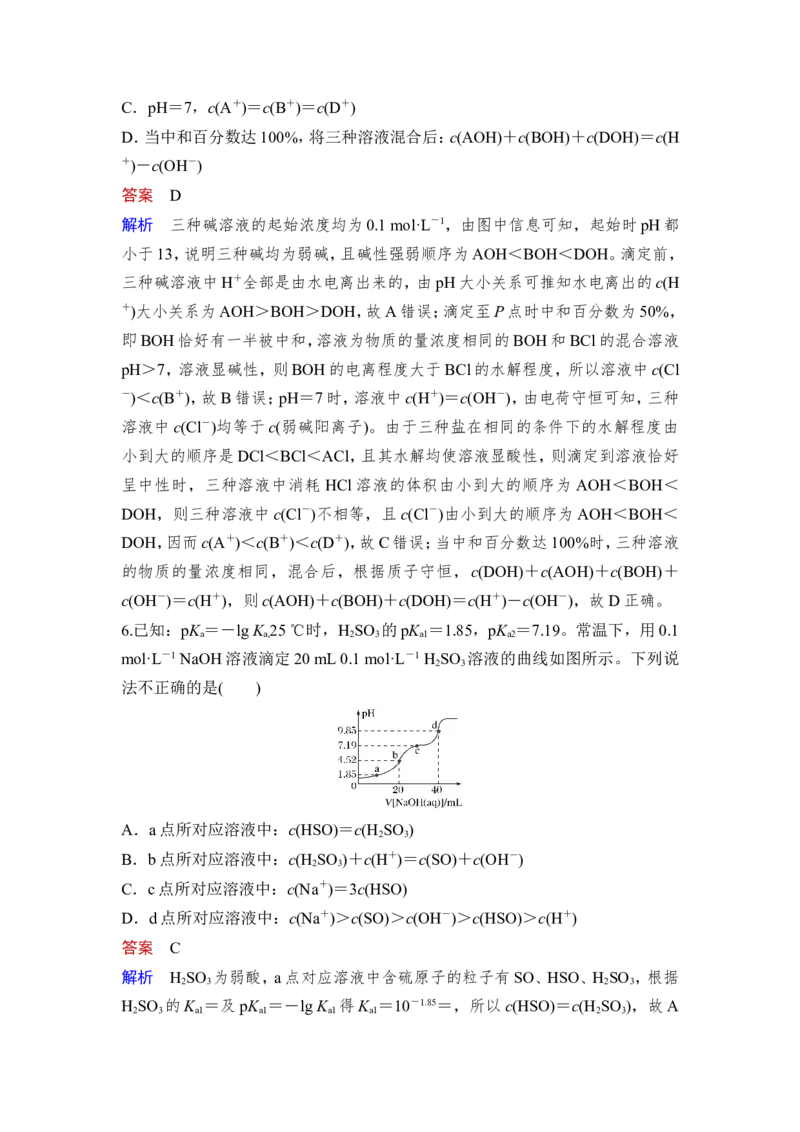
D.a、b、c、d均有c(NH)+c(H+)=c(Cl-)+c(OH-)
答案 D
解析 a点时加入的盐酸为10 mL,所得溶液的溶质为等物质的量浓度的氯化铵
和一水合氨,根据物料守恒2c(Cl-)=c(NH ·H O)+c(NH),故A错误;c点时加入
3 2
的盐酸为20 mL,表示酸碱恰好完全反应,b点表示碱过量,盐酸完全反应,故B
错误;c点时,酸碱恰好完全反应生成氯化铵,溶液显酸性,c(H+)>c(OH-),根据
电荷守恒:c(NH)+c(H+)=c(Cl-)+c(OH-)可知,c(NH)7,A错误;根据c(HA)=c(A-)
时,溶液显酸性,可知A-水解程度小于HA电离程度,继续加入氢氧化钠,HA浓
度减小,达到中性时,c(A-)>c(HA),B错误;NaOH溶液滴定HA溶液时,滴定突
跃pH在6.0到8.0之间,用酚酞做指示剂,C正确;25 ℃时,根据c(H B-)=
2
c(H B)时,pH在2.0~3.0之间,H B-离子的水解常数K==c(OH-),数量级为10
3 2
-12,D错误。
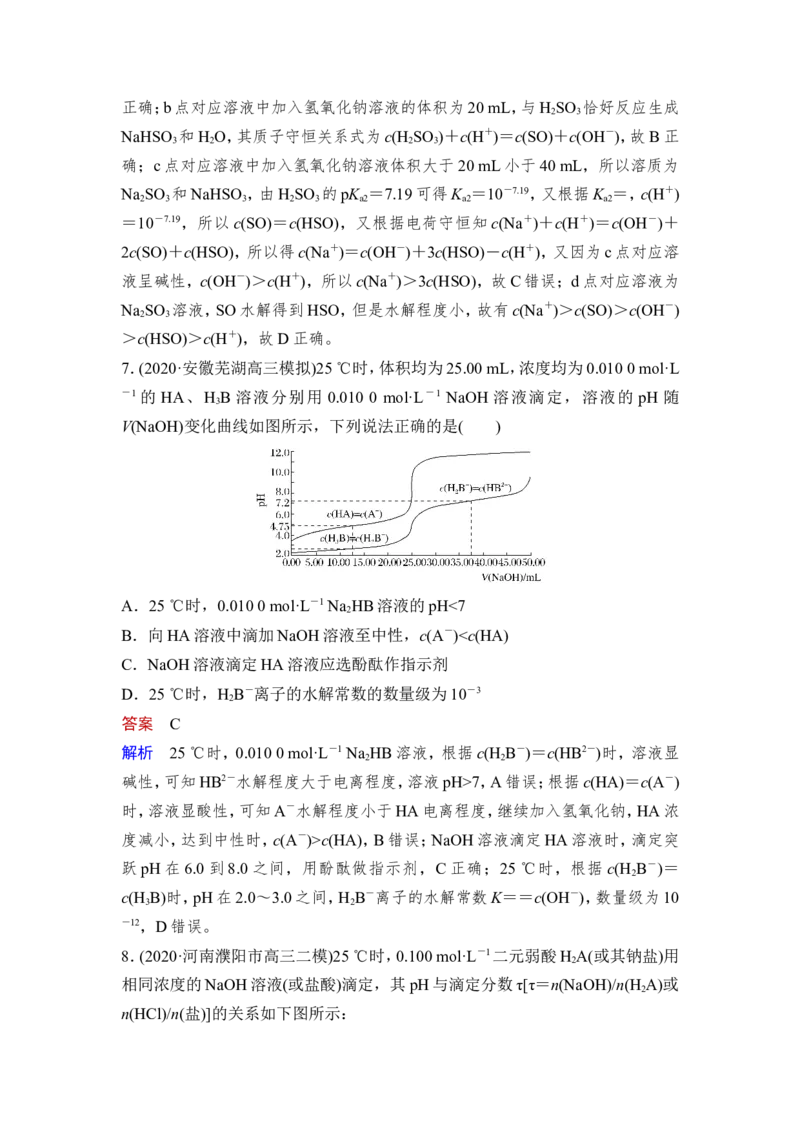
8.(2020·河南濮阳市高三二模)25 ℃时,0.100 mol·L-1二元弱酸H A(或其钠盐)用
2
相同浓度的NaOH溶液(或盐酸)滴定,其pH与滴定分数τ[τ=n(NaOH)/n(H A)或
2
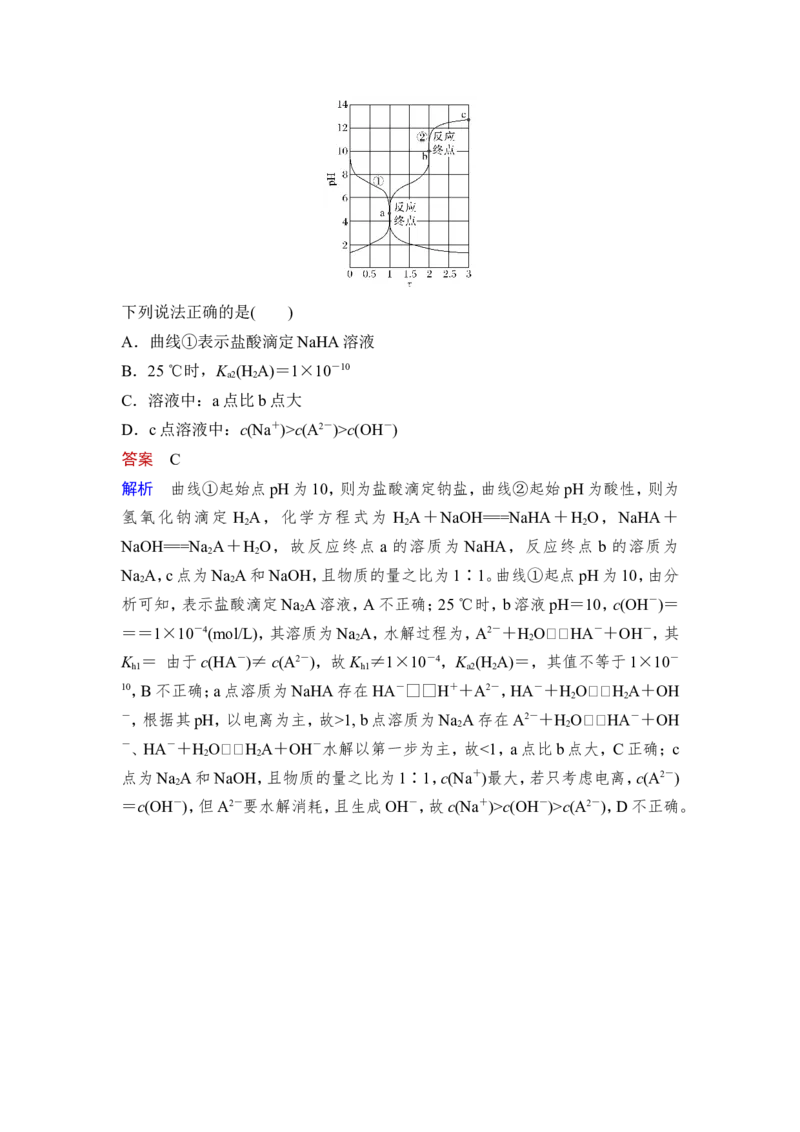
n(HCl)/n(盐)]的关系如下图所示:下列说法正确的是( )
A.曲线①表示盐酸滴定NaHA溶液
B.25 ℃时,K (H A)=1×10-10
a2 2
C.溶液中:a点比b点大
D.c点溶液中:c(Na+)>c(A2-)>c(OH-)
答案 C
解析 曲线①起始点pH为10,则为盐酸滴定钠盐,曲线②起始pH为酸性,则为
氢氧化钠滴定 H A,化学方程式为 H A+NaOH===NaHA+H O,NaHA+
2 2 2
NaOH===Na A+H O,故反应终点 a 的溶质为 NaHA,反应终点 b 的溶质为
2 2
Na A,c点为Na A和NaOH,且物质的量之比为1∶1。曲线①起点pH为10,由分
2 2
析可知,表示盐酸滴定Na A溶液,A不正确;25 ℃时,b溶液pH=10,c(OH-)=
2
==1×10-4(mol/L),其溶质为Na A,水解过程为,A2-+H OHA-+OH-,其
2 2
K = 由于c(HA-)≠ c(A2-),故K ≠1×10-4,K (H A)=,其值不等于1×10-
h1 h1 a2 2
10,B不正确;a点溶质为NaHA存在HA-H++A2-,HA-+H OH A+OH
2 2
-,根据其pH,以电离为主,故>1, b点溶质为Na A存在A2-+H OHA-+OH
2 2
-、HA-+H OH A+OH-水解以第一步为主,故<1,a点比b点大,C正确;c
2 2
点为Na A和NaOH,且物质的量之比为1∶1,c(Na+)最大,若只考虑电离,c(A2-)
2
=c(OH-),但A2-要水解消耗,且生成OH-,故c(Na+)>c(OH-)>c(A2-),D不正确。