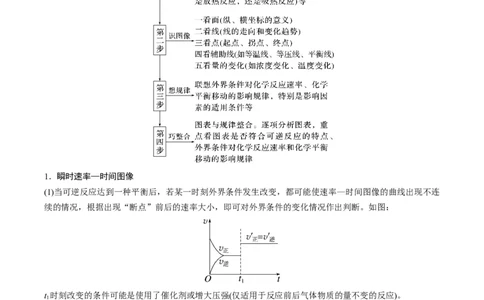
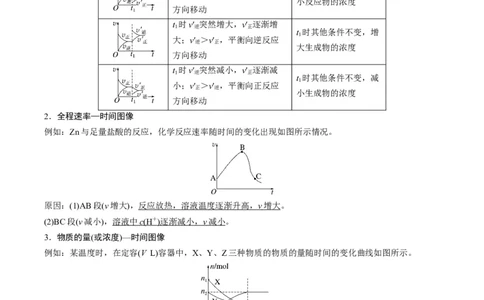
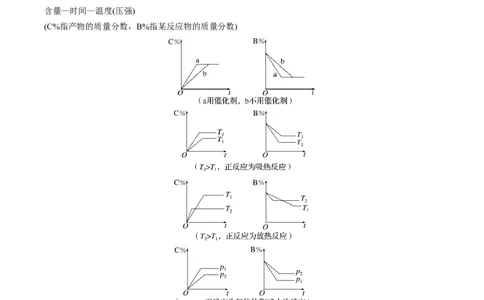
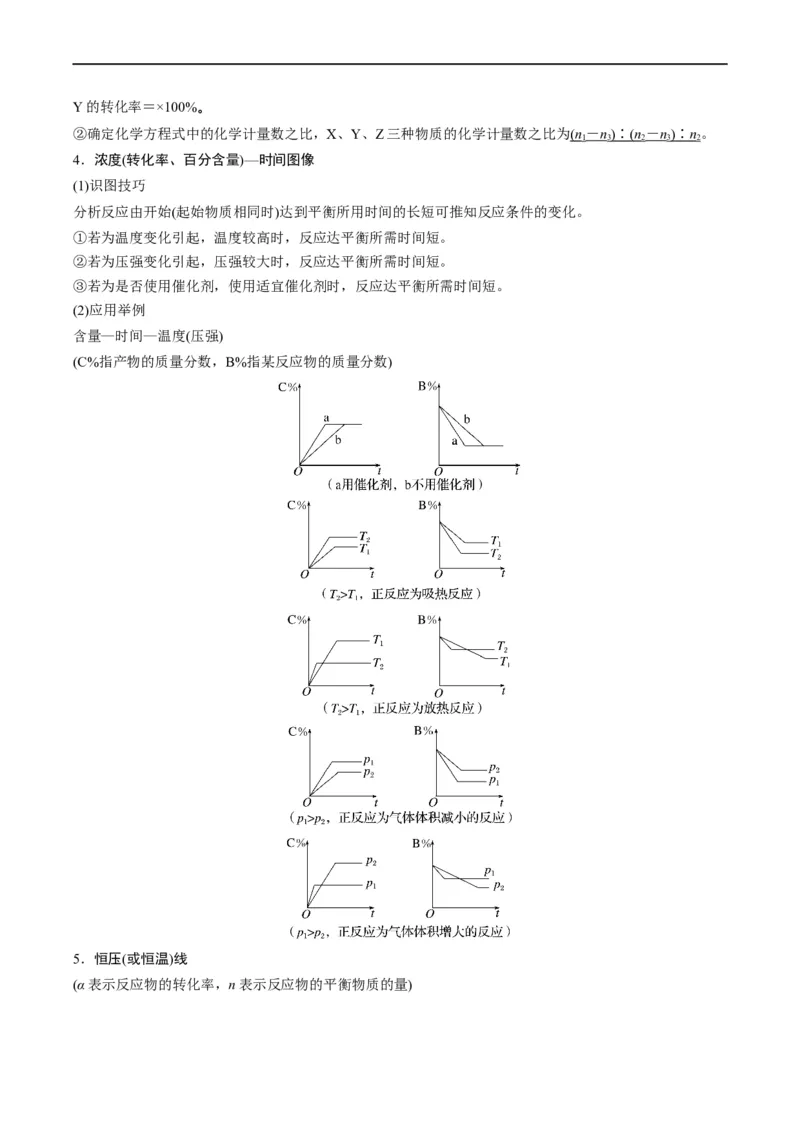
文档内容
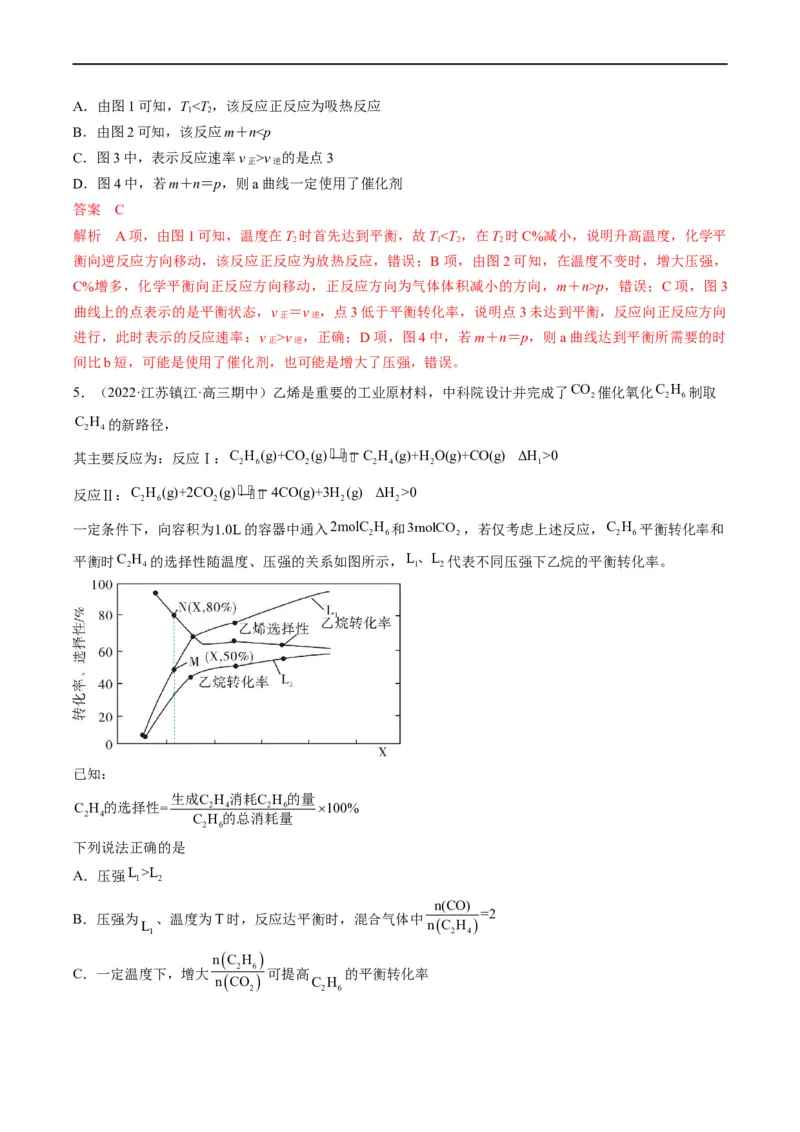
T ,温度升高,平衡逆向移动,而纵坐标所示的 2 2 1 数值越小,则纵坐标不可能代表NO的百分含量,B错误; C.由丙图信息可知,P 时的反应速率更大,故压强P
K(I) C.t ~t 时反应向正反应方向移动 2 3 D.平衡时A的体积分数φ:φ(II)>φ(I) 【答案】D 【解析】 A.若t 时升温,瞬间正反应速率增大,与图像不符,由正反应速率逐渐增大,可知t 时改变的条件:向 2 2 容器中加入C,故A错误; B.温度不变,则平衡常数不变,即K:K(II)=K(I),故B错误; C.t ~t 正反应速率逐渐增大,t 时加入物质C,逆反应速率大于正反应速率,平衡逆向移动,反应向逆 2 3 2 反应方向移动,故C错误; D.起始充入1molA和3molB,投料比为1:3,达平衡后加入物质C,相当于按1:2的投料比投入A和B, 则加入C后相当于总体系中A和B的投料比大于1:3,平衡状态II相当于平衡状态I再充入A所达到的平 衡,则平衡时A的体积分数φ:φ(II)>φ(I),故D正确; 故选:D。 10.(2022·广东深圳·一模)在容积为VL的恒温密闭容器中模拟工业合成氨。充入N 和H 的总物质的量 2 2 为1mol,容器内各组分的物质的量分数与反应时间t的关系如图所示。下列说法不正确的是 A.a表示N 物质的量分数的变化情况物质的量分数 2 0.2 B.0~tmin,v(H )= mol·L-1·min-1 1 2 Vt 1 C.tmin时,NH 的分解速率小于其生成速率 2 3D.tmin时改变的条件可能为减小容器容积 3 【答案】B 【解析】由题中图示可知,开始时N 和H 各占50%,总物质的量是1mol,则N 和H 各为0.5mol,由 2 2 2 2 N(g) 3H g 2NH g 2 2 3 起始物质的量mol 0.5 0.5 0 可得,某时刻总物质的量为n(总)=(0.5- 变化物质的量mol x 3x 2x 某时刻物质的量mol 0.5x 0.53x 2x x)mol+(0.5-3x)mol+2xmol=(1-2x)mol,某时刻N 的物质的量分数为 2 1 0.5xmol 12xmol 100% 2 100%=50%,所以,N 2 的物质的量分数一直保持不变,是50%,则a 12xmol 12xmol 代表N 的物质的量分数,随反应进行减小的是c代表H 的物质的量分数,b代表NH 的物质的量分数;据 2 2 3 此解答。 A.由上述分析可知,N 的物质的量分数一直保持不变,是50%,则a代表N 的物质的量分数,故A正确; 2 2 B.由上述分析可知,a代表N 的物质的量分数,c代表H 的物质的量分数,b代表NH 的物质的量分数, 2 2 3 0.53xmol 2xmol t 时H、NH 的物质的量分数相等,即 ,解之x=0.1mol,则0~tmin,v(H )= 1 2 3 12xmol 12xmol 1 2 3xmol VL 0.3 mol·L-1·min-1,故B错误; t min Vt 1 1 C.由上述分析可知,b代表NH 的物质的量分数,t 时刻及以后,NH 的物质的量分数增大,说明反应向 3 2 3 右进行,则NH 的分解速率小于其生成速率,故C正确; 3 D.由N(g)+3H(g) 2NH (g)可知,t 时刻,减小容积,压强增大,平衡正向移动,NH 的物质的量分 2 2 3 3 3 数增大,H 的物质的量分数减小,故D正确; 2 答案为B。 11.某温度时,在体积为2 L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图 甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在t、t 2 4 时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是( ) A.此温度下,该反应的化学方程式为2A(g)+E(g)2B(g)+F(g) B.若平衡状态①和②对应的温度相同,则①和②对应的平衡常数K一定相同C.t 时刻改变的条件是增大压强 2 D.t 时刻改变的条件是降低温度 4 答案 C 解析 由图甲分析可知,各物质发生变化的物质的量等于化学方程式的化学计量数之比,此温度下该反应 的化学方程式为2A(g)+E(g) 2B(g)+F(g),故A正确;平衡常数K只与温度有关,平衡状态①和② 的温度相同,故K相等,故B正确;该反应前后气体的体积不变,若改变压强,平衡不会发生移动,故t 2 时刻不可能是增大压强,故C错误;根据方程式知,反应前后气体体积不变,故不可能是压强的变化,t 4 时刻速率减小,且变化的点不连续,因此是降低温度的结果,故D正确。 12.(2022·江苏南通·高三期中)一碘甲烷(CHI)热裂解可制取乙烯等低碳烯烃化工原料。一碘甲烷(CHI) 3 3 热裂解时主要反应有: 反应Ⅰ 2CH 3 I(g) C 2 H 4 (g)+2HI(g) ΔH >0 1 反应Ⅱ 3C 2 H 4 (g) 2C 3 H 6 (g) ΔH <0 2 反应Ⅲ 2C 2 H 4 (g) C 4 H 8 (g) ΔH <0 3 向容积为1L的密闭容器中起始投入1molCH I(g),反应温度对平衡体系中乙烯、丙烯和丁烯占所有气体物 3 质的量分数的影响如图所示。已知715K时,CHI的转化率为80%。 3 下列说法正确的是 A.曲线a表示反应温度对平衡体系中乙烯物质的量分数的影响 B.由图像可知,温度越高,催化剂的活性越强 C.715K时,C H(g)的平衡物质的量浓度为0.1mol/L 4 8 D.400K时使用活性更强的催化剂,可以提高曲线a、b对应物质的物质的量分数 【答案】AC 【分析】反应Ⅰ为吸热反应,反应Ⅱ、Ⅲ均为放热反应,温度升高Ⅰ正向移动,Ⅱ、Ⅲ逆向移动都会导致 乙烯含量增加,故a为乙烯含量曲线、b为丙烯含量曲线; 【详解】A.由分析可知,曲线a表示反应温度对平衡体系中乙烯物质的量分数的影响,A正确; B.催化剂需要一定的活性温度,不是温度越高越好,且图像也不能体现温度越高催化剂的活性越强,B错误; C.已知715K时,CHI的转化率为80%;此时丁烯、丙烯物质的量分数均为8%; 3 2CH 3 I(g) C 2 H 4 (g)+2HI(g) 起始(mol) 1 转化(mol) 0.8 0.4 0.8 平衡(mol) 0.2 3C 2 H 4 (g) 2C 3 H 6 (g) 起始(mol) 转化(mol) 1.5a a 平衡(mol) 2C 2 H 4 (g) C 4 H 8 (g) 起始(mol) 转化(mol) 2a a 平衡(mol) a 则平衡时总的物质的量为(1.4-1.5a)mol, 100%=8%,a=0.1mol,则715K时,C H(g)的平衡物质 1.4-1.5a 4 8 的量浓度为0.1mol÷1L=0.1mol/L,C正确; D.400K时使用活性更强的催化剂,可以加快反应速率,但是不能改变平衡移动,不能提高曲线a、b对 应物质的物质的量分数,D错误; 故选AC。 催化剂 13.甲烷催化氧化为合成气的主反应为:2CH (g)O (g) 2CO(g)4H (g) ΔH0。 转化率、 4 2 2 CH 4 nH n(CO) 2 选择性 和 选择性 随温度变化如图所示。下列说法不正确的是 H 2 nH 2 +nH 2 O CO n(CO)+nCO 2 A.800℃时,副反应①CH 2O CO 2H O进行程度很小 4 2 2 2 B.对比图中H 和CO的选择性,推测可能存在副反应②CH H O CO3H 2 4 2 2 C.CH 转化率随温度升高而增大,可以用勒夏特列原理解释 4 D.增大压强使容器容积减小,可使单位体积内活化分子数增多,化学反应速率增大【答案】C 【详解】A.结合图示信息,800℃时,CH 转化率、H 选择性和CO选择性接近1,主要发生甲烷催化氧 4 2 化为合成气的主反应,副反应①CH 2O CO 2H O进行程度很小,A正确; 4 2 2 2 B.对比图中H 和CO的选择性,H 选择性变化较为平缓,CO选择性变化较大,推测可能存在副反应② 2 2 CH H O CO3H ,B正确; 4 2 2 C.主反应为放热反应,根据勒夏特列原理,升高温度,反应逆向进行,CH 转化率应减小,不可以用勒 4 夏特列原理解释,C错误; D.增大压强使容器容积减小,反应物浓度增大,可使单位体积内活化分子数增多,化学反应速率增大, D正确; 故选C。 14.常温下,向10.0mL浓度均为0.1molL1的AlCl 和FeCl 混合溶液中加入NaOH固体,溶液中金属元 3 3 素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b点溶液pH分别为 3,0、4.3。 已知: ①K sp AlOH 3 K sp FeOH 3 c AlOH ② ,298K下,K 4 1.11033 Al3aq4OHaq AlOH aq 稳 c Al3 c4 OH 4 下列叙述正确的是 A.曲线Ⅱ代表Fe3 B.常温下,K sp FeOH 3 1.01038 C.b点溶液中铝元素主要以 AlOH 形式存在 4 D.AlOH OH AlOH 的平衡常数K为1.1105 3 4 【答案】B 【详解】A.根据a点、b点对应的pH,计算溶度积K c3 OH c M3 ,分别为 sp1014 3 1014 3 Kspa 1105 1.01038、Kspb 1105 1.01034.1,根据信息①可知,前者为 103 104.3 FeOH 的溶度积,后者为AlOH 溶度积。溶解度小,优先沉淀,故曲线Ⅰ代表Fe3,曲线Ⅱ代表Al3, 3 3 A项错误; B.K sp FeOH 3 1.01038 ,B项正确: C.b点恰好两种金属离子完全沉淀,金属元素主要存在形式为FeOH 和AlOH ,C项错误; 3 3 D.K K sp AlOH 3 K 稳 1.01034.11.11033 1.1101.1 ,D项错误; 故答案为:B。