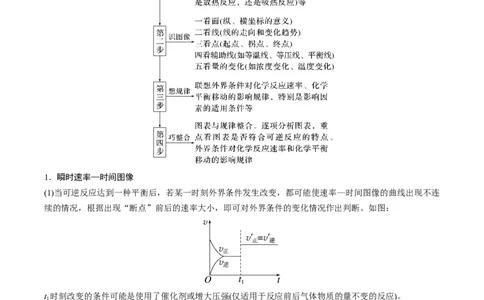
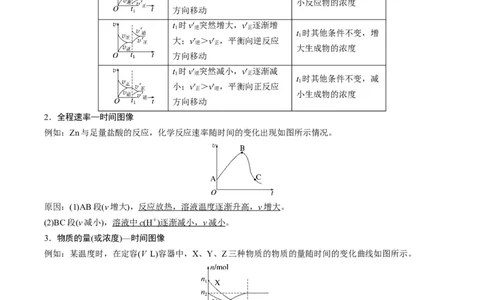
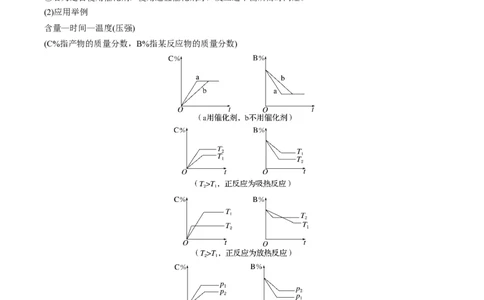
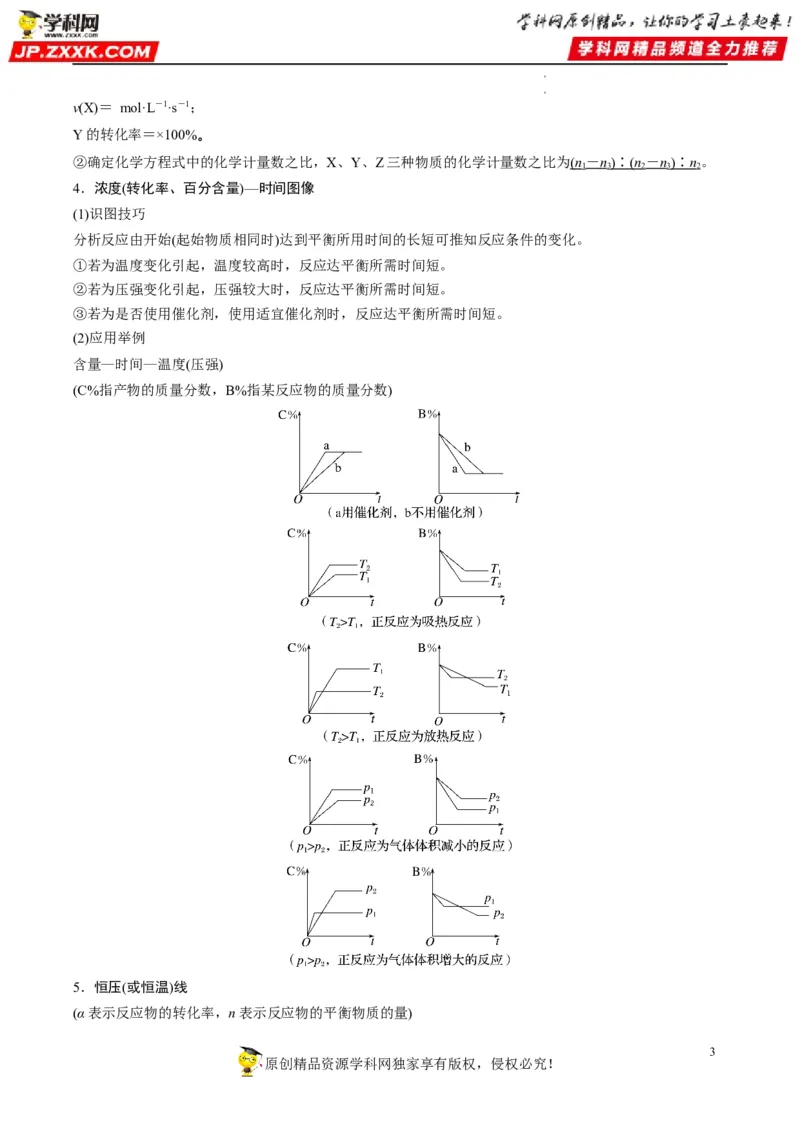
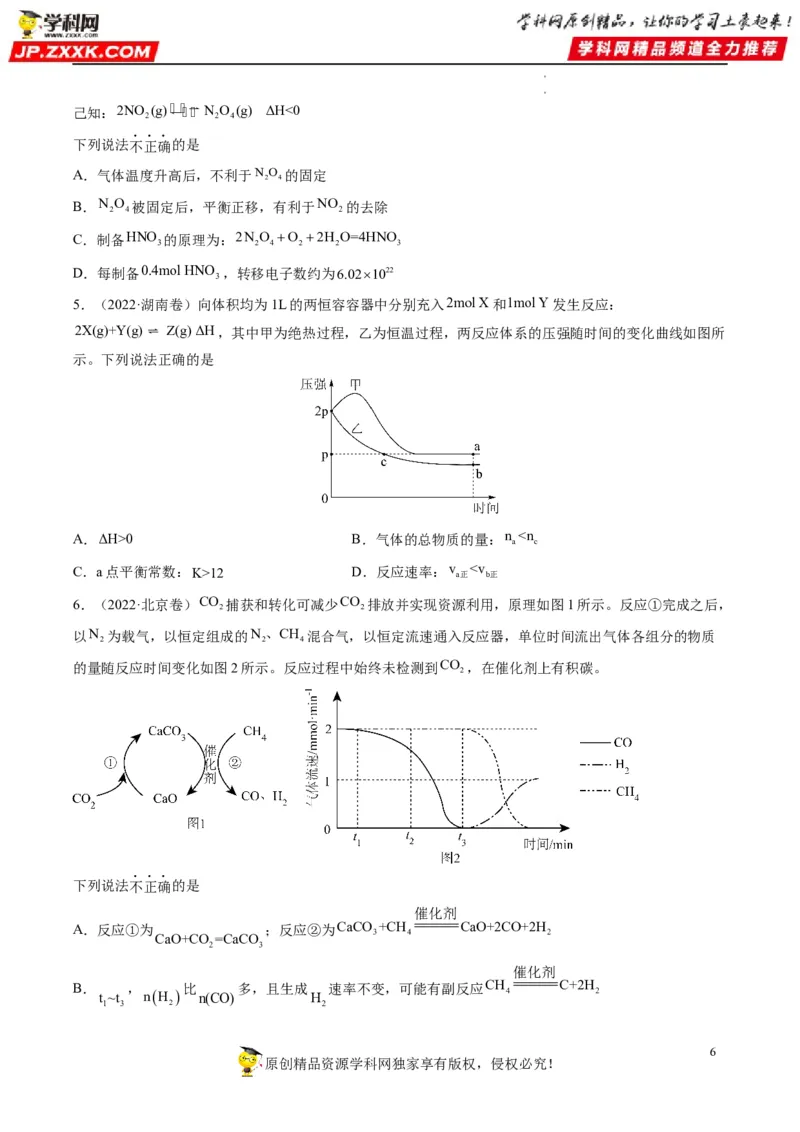
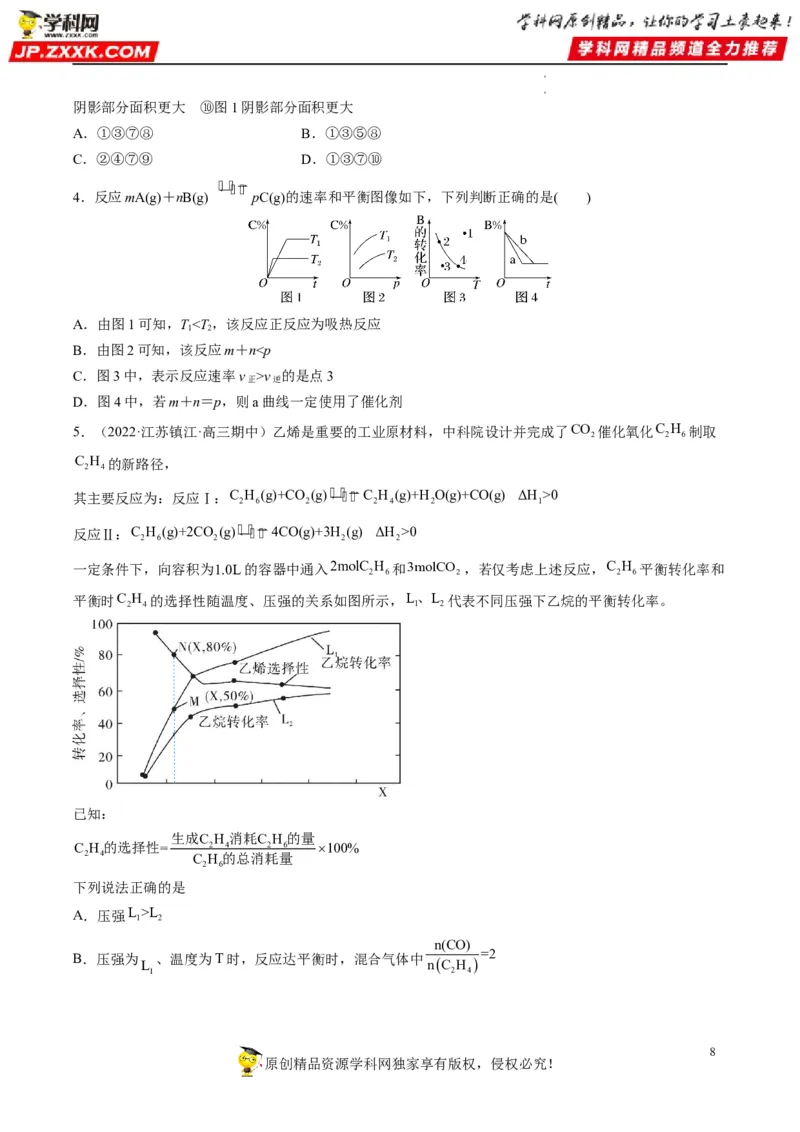
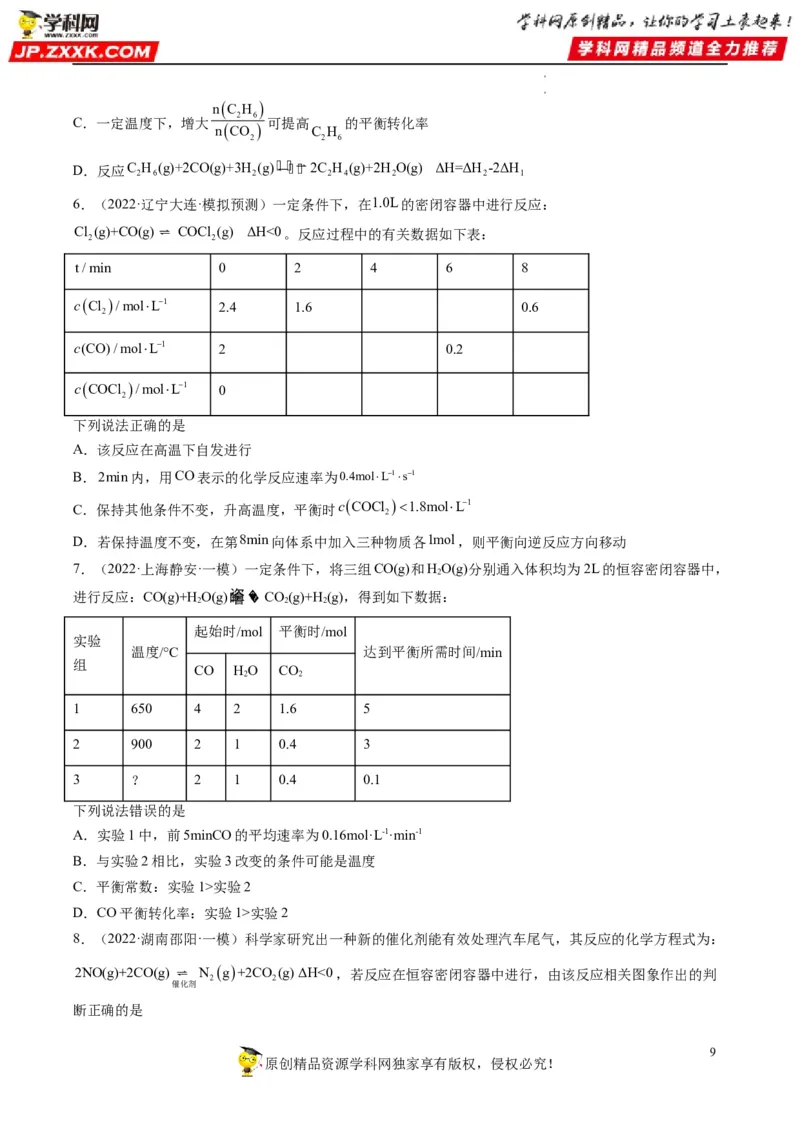
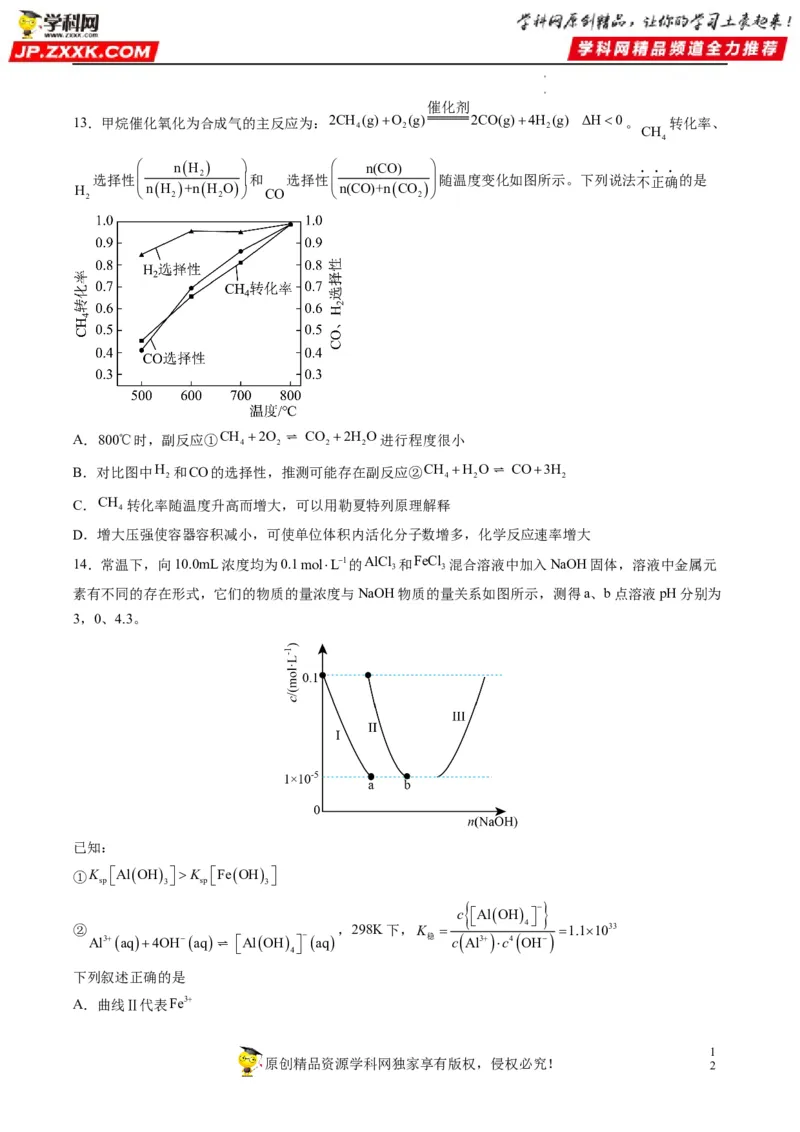
文档内容
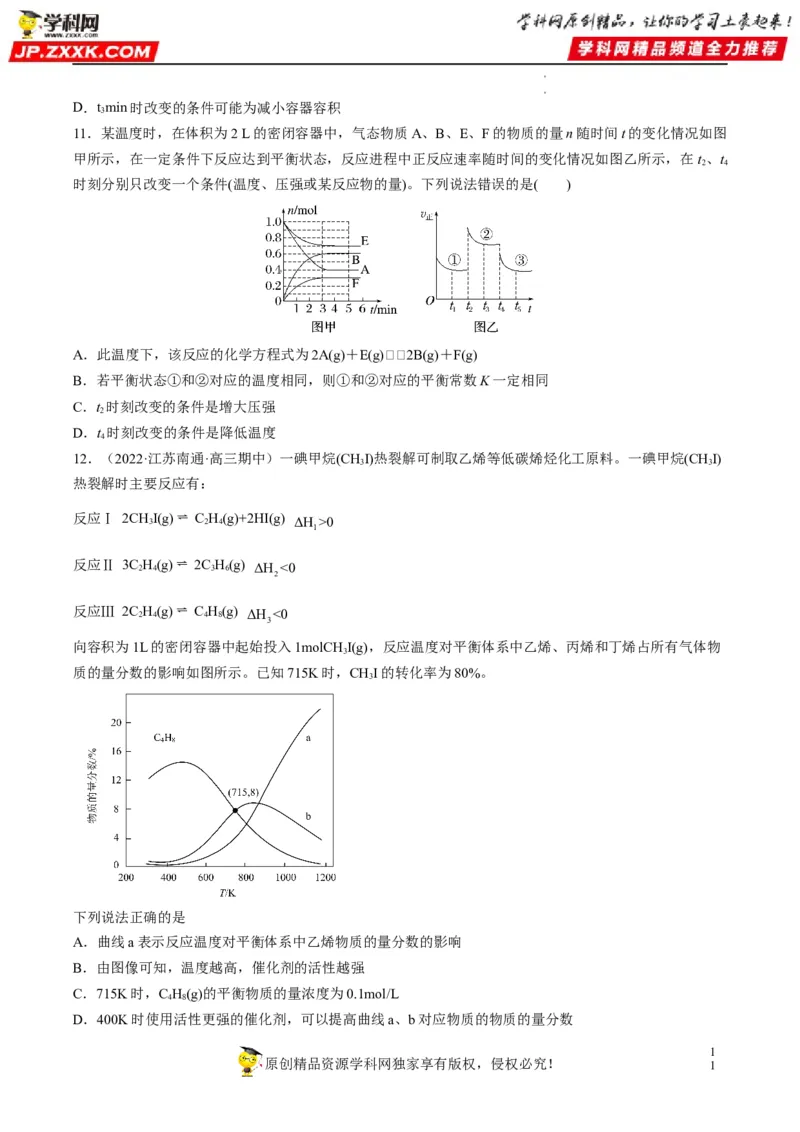
K(I) C.t ~t 时反应向正反应方向移动 2 3 D.平衡时A的体积分数φ:φ(II)>φ(I) 10.(2022·广东深圳·一模)在容积为VL的恒温密闭容器中模拟工业合成氨。充入N 和H 的总物质的量 2 2 为1mol,容器内各组分的物质的量分数与反应时间t的关系如图所示。下列说法不正确的是 A.a表示N 物质的量分数的变化情况物质的量分数 2 0.2 B.0~tmin,v(H )= mol·L-1·min-1 1 2 Vt 1 C.tmin时,NH 的分解速率小于其生成速率 2 3 1 原创精品资源学科网独家享有版权,侵权必究! 0 学学科科网网((北北京京))股股份份有有限公司D.tmin时改变的条件可能为减小容器容积 3 11.某温度时,在体积为2 L的密闭容器中,气态物质A、B、E、F的物质的量n随时间t的变化情况如图 甲所示,在一定条件下反应达到平衡状态,反应进程中正反应速率随时间的变化情况如图乙所示,在t、t 2 4 时刻分别只改变一个条件(温度、压强或某反应物的量)。下列说法错误的是( ) A.此温度下,该反应的化学方程式为2A(g)+E(g)2B(g)+F(g) B.若平衡状态①和②对应的温度相同,则①和②对应的平衡常数K一定相同 C.t 时刻改变的条件是增大压强 2 D.t 时刻改变的条件是降低温度 4 12.(2022·江苏南通·高三期中)一碘甲烷(CHI)热裂解可制取乙烯等低碳烯烃化工原料。一碘甲烷(CHI) 3 3 热裂解时主要反应有: 反应Ⅰ 2CH 3 I(g) C 2 H 4 (g)+2HI(g) ΔH >0 1 反应Ⅱ 3C 2 H 4 (g) 2C 3 H 6 (g) ΔH <0 2 反应Ⅲ 2C 2 H 4 (g) C 4 H 8 (g) ΔH <0 3 向容积为1L的密闭容器中起始投入1molCH I(g),反应温度对平衡体系中乙烯、丙烯和丁烯占所有气体物 3 质的量分数的影响如图所示。已知715K时,CHI的转化率为80%。 3 下列说法正确的是 A.曲线a表示反应温度对平衡体系中乙烯物质的量分数的影响 B.由图像可知,温度越高,催化剂的活性越强 C.715K时,C H(g)的平衡物质的量浓度为0.1mol/L 4 8 D.400K时使用活性更强的催化剂,可以提高曲线a、b对应物质的物质的量分数 1 原创精品资源学科网独家享有版权,侵权必究! 1 学学科科网网((北北京京))股股份份有有限公司催化剂 13.甲烷催化氧化为合成气的主反应为:2CH (g)O (g) 2CO(g)4H (g) ΔH0。 转化率、 4 2 2 CH 4 nH n(CO) 2 选择性 和 选择性 随温度变化如图所示。下列说法不正确的是 H 2 nH 2 +nH 2 O CO n(CO)+nCO 2 A.800℃时,副反应①CH 2O CO 2H O进行程度很小 4 2 2 2 B.对比图中H 和CO的选择性,推测可能存在副反应②CH H O CO3H 2 4 2 2 C.CH 转化率随温度升高而增大,可以用勒夏特列原理解释 4 D.增大压强使容器容积减小,可使单位体积内活化分子数增多,化学反应速率增大 14.常温下,向10.0mL浓度均为0.1molL1的AlCl 和FeCl 混合溶液中加入NaOH固体,溶液中金属元 3 3 素有不同的存在形式,它们的物质的量浓度与NaOH物质的量关系如图所示,测得a、b点溶液pH分别为 3,0、4.3。 已知: ①K sp AlOH 3 K sp FeOH 3 c AlOH ② ,298K下,K 4 1.11033 Al3aq4OHaq AlOH aq 稳 c Al3 c4 OH 4 下列叙述正确的是 A.曲线Ⅱ代表Fe3 1 原创精品资源学科网独家享有版权,侵权必究! 2 学学科科网网((北北京京))股股份份有有限公司B.常温下,K sp FeOH 3 1.01038 C.b点溶液中铝元素主要以 AlOH 形式存在 4 D.AlOH OH AlOH 的平衡常数K为1.1105 3 4 1 原创精品资源学科网独家享有版权,侵权必究! 3 学学科科网网((北北京京))股股份份有有限公司1 原创精品资源学科网独家享有版权,侵权必究! 4 学学科科网网((北北京京))股股份份有有限公司