文档内容
高考解密10 常见金属及其重要化合物
A 组 基础练
1.(2022·浙江舟山·舟山中学校考模拟预测)下列物质的转化在给定条件下能实现的是
A.HSO (稀) SO NH HSO (NH )SO
2 4 2 4 3 4 2 3
B.NH NO NO HNO
3 2 3
C.Fe FeCl Fe(OH) Fe(OH)
2 2 3
D.Al NaAlO AlCl 溶液 无水AlCl
2 3 3
2.(2022·浙江宁波·镇海中学校考模拟预测)根据下列实验操作和现象,不能得到相应结论的是
选项 实验操作和现象 结论
往装有铁钉的试管中加入 饱和氯化钠和1滴 铁钉周围出现蓝色沉淀,说明
A
有 生成
溶液
向 的 溶液中滴加5滴
B 证明 和 的反应有限度
溶液,再滴入 溶液,溶液显红色
向矿物油和地沟油中分别加入烧碱溶液,加热,
C 油层变少的是地沟油
冷却后观察,一个油层变少,一个油层不变
D 向酸性高锰酸钾溶液中通入 ,溶液褪色 有漂白性
A.A B.B C.C D.D
3.(2022·浙江杭州·杭州高级中学校考模拟预测)下列说法正确的是
A.常温下铁与浓硫酸不发生化学反应
B.铜粉与硫粉加热反应可生成硫化铜
C.石油裂解、煤的干馏和气化都是化学变化
D.石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体
4.(2023·浙江杭州·学军中学校考模拟预测)下列说法不正确的是
A.熟石膏与水混合成糊状后能很快凝固,常用于制作模型和医疗石膏绷带
B.碳酸钠是一种大宗化学品,可用作食用碱或工业用碱C.大兴机场航站楼顶部镶嵌八百块玻璃,玻璃属于新型无机非金属材料
D.NaO、活性炭都可用于防毒呼吸面具,但两者的应用原理不同
2 2
5.(2023·北京朝阳·北京八十中校考模拟预测)下列能说明金属性Mg>Al的是
①表面积相同的金属与盐酸反应的剧烈程度Mg>Al
②Mg(OH) 不溶于NaOH,Al(OH) 溶于NaOH
2 3
③等浓度的Mg(NO) 和Al(NO ) 溶液的pH前者大
3 2 3 3
④电负性Mg<Al
⑤第一电离能Mg>Al
A.①②③ B.①②④ C.②③④ D.②④⑤
6.(2023·湖南岳阳·统考一模)下列物质应用错误的是
A.石膏可用于调节水泥的硬化速率 B.掺杂了 的聚乙炔具有导电性
C.硫酸铜用作无水酒精的检水剂 D.氧化钙用作食品抗氧化剂
7.(2023·广东·华南师大附中校联考模拟预测)下表中,陈述Ⅰ、Ⅱ均正确及两者间具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 具有较强的还原性 用于除去废水中的
B 溶液呈酸性 溶液可用于腐蚀铜电路板
C 着火不能用 灭火 会与 反应生成
D 铁比铜活泼 铜板上的铁钉在潮湿空气中更容易生锈
A.A B.B C.C D.D
8.(2022·浙江舟山·统考二模)由铜粉、铁粉、无水硫酸铜粉末组成的混合物22.4g,等分为两份。第一
份投入有足量水的甲烧杯后充分搅拌,最终剩下8.00g 固体;第二份置于乙烧杯中,加入足量的91.5g稀
硫酸,搅拌并充分反应后,杯中留有2.50g红色固体和100g浅绿色溶液(溶液中只含有一种溶质FeSO )。
4
求:
(1)原22.4g混合物中CuSO 的质量___________
4
(2)乙烧杯溶液中FeSO 的质量分数___________。
4
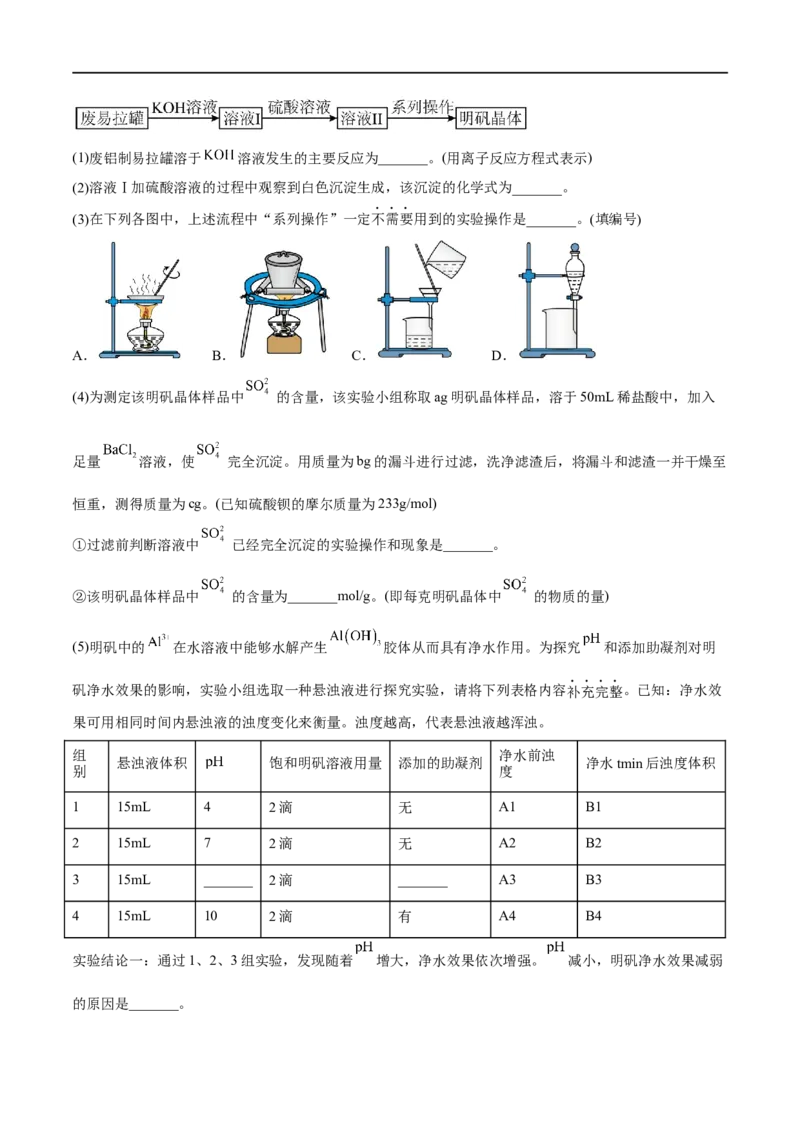
9.(2023·广东·华南师大附中校联考模拟预测)明矾( )在工业上用作印染媒染剂和净水
剂,医药上用作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾并测定其组成,探究明矾净
水的影响因素。(1)废铝制易拉罐溶于 溶液发生的主要反应为_______。(用离子反应方程式表示)
(2)溶液Ⅰ加硫酸溶液的过程中观察到白色沉淀生成,该沉淀的化学式为_______。
(3)在下列各图中,上述流程中“系列操作”一定不需要用到的实验操作是_______。(填编号)
A. B. C. D.
(4)为测定该明矾晶体样品中 的含量,该实验小组称取ag明矾晶体样品,溶于50mL稀盐酸中,加入
足量 溶液,使 完全沉淀。用质量为bg的漏斗进行过滤,洗净滤渣后,将漏斗和滤渣一并干燥至
恒重,测得质量为cg。(已知硫酸钡的摩尔质量为233g/mol)
①过滤前判断溶液中 已经完全沉淀的实验操作和现象是_______。
②该明矾晶体样品中 的含量为_______mol/g。(即每克明矾晶体中 的物质的量)
(5)明矾中的 在水溶液中能够水解产生 胶体从而具有净水作用。为探究 和添加助凝剂对明
矾净水效果的影响,实验小组选取一种悬浊液进行探究实验,请将下列表格内容补充完整。已知:净水效
果可用相同时间内悬浊液的浊度变化来衡量。浊度越高,代表悬浊液越浑浊。
组 净水前浊
悬浊液体积 饱和明矾溶液用量 添加的助凝剂 净水tmin后浊度体积
别 度
1 15mL 4 2滴 无 A1 B1
2 15mL 7 2滴 无 A2 B2
3 15mL _______ 2滴 _______ A3 B3
4 15mL 10 2滴 有 A4 B4
实验结论一:通过1、2、3组实验,发现随着 增大,净水效果依次增强。 减小,明矾净水效果减弱
的原因是_______。实验结论二:添加助凝剂 能够显著提高净水效果。该实验结论成立的判断依据是_______。(用表中
数据表示)
10.(2022·上海徐汇·统考二模)不锈钢具有良好的耐腐蚀性和耐磨性,铬(Cr)是不锈钢的重要成分。完成
下列填空:
I.
(1)通过 可以得到较纯的铬, 的熔点比 _______。(选填“高”或
“低”),某工厂用 含 的铬铁矿粉 制备 ,最终得到产品bkg,产率为
_______。(用含a和b的代数式表示)
II.元素 在溶液中主要以(蓝紫色)、 (绿色)、 (橙红色)、 (黄色)等形式存在, 为
难溶于水的灰蓝色固体。
(2) 与 的化学性质相似,在 溶液中逐滴加入 溶液直至过量,可观察到的现象是
_______。
III. 和 在溶液中可以相互转化。室温下,初始浓度为 溶液中 随
的变化如图所示。
(3)用离子方程式表示 溶液中的转化平衡_______。
(4)写出该反应平衡常数的表达式K=_______。(5)由图可知,溶液酸性增强, 的平衡转化率_______。(选填“增大”、“减小”或“不变”)
(6)升高温度,溶液中 的平衡转化率减小,则该反应是_____反应。(选填“吸热”或“放热”)
B 组 提升练
1.(2022·重庆·模拟预测)废旧锌锰电池处理后的废料[含MnO 、MnOOH、Zn(OH) 、 Fe等]制备Zn和
2 2
MnO 的一种工艺流程如下:
2
已知:Mn的金属活动性强于Fe,Mn2+在pH大于5.5时易被氧化。
下列说法不正确的是
A.“还原焙烧”时Mn元素被还原
B.“酸浸” 过程中适当加热,主要目的是加快浸取速率
C.“净化”时MnCO 的作用是调节溶液的pH,使Fe3+形成Fe(OH) 沉淀而除去
3 3
D.“电解”时阳极反应式为Mn2+-2e-+4OH-=MnO+2HO
2 2
2.(2023·浙江金华·浙江省东阳中学校考模拟预测)下列物质不能通过化合反应一步合成的是
A. B. C. D.
3.(2022·湖南·湘潭一中校联考模拟预测)《本草备要》记载了化合物 具有治喉痹、咳逆、
敛疮毒等功效。W、X、Y、Z是元素周期表中前四周期元素,其中X、Z、W为短周期元素,原子序数依
次增加,Y、X最外层电子数相同且质子数均为奇数,W、Z位于同一主族,Z的成对电子数与未成对电子
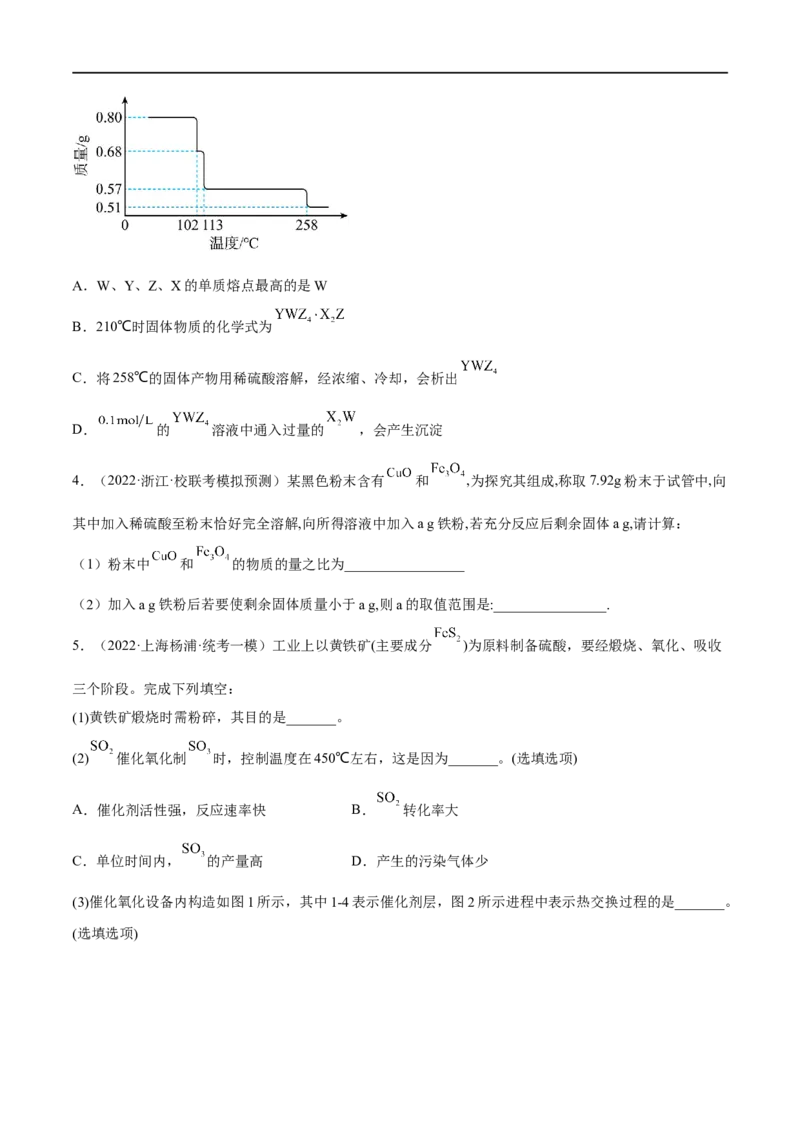
数之比为3∶1, 和生命活动密切相关。 热重曲线如图所示。下列说法正确的是。A.W、Y、Z、X的单质熔点最高的是W
B.210℃时固体物质的化学式为
C.将258℃的固体产物用稀硫酸溶解,经浓缩、冷却,会析出
D. 的 溶液中通入过量的 ,会产生沉淀
4.(2022·浙江·校联考模拟预测)某黑色粉末含有 和 ,为探究其组成,称取7.92g粉末于试管中,向
其中加入稀硫酸至粉末恰好完全溶解,向所得溶液中加入a g铁粉,若充分反应后剩余固体a g,请计算:
(1)粉末中 和 的物质的量之比为_________________
(2)加入a g铁粉后若要使剩余固体质量小于a g,则a的取值范围是:________________.
5.(2022·上海杨浦·统考一模)工业上以黄铁矿(主要成分 )为原料制备硫酸,要经煅烧、氧化、吸收
三个阶段。完成下列填空:
(1)黄铁矿煅烧时需粉碎,其目的是_______。
(2) 催化氧化制 时,控制温度在450℃左右,这是因为_______。(选填选项)
A.催化剂活性强,反应速率快 B. 转化率大
C.单位时间内, 的产量高 D.产生的污染气体少
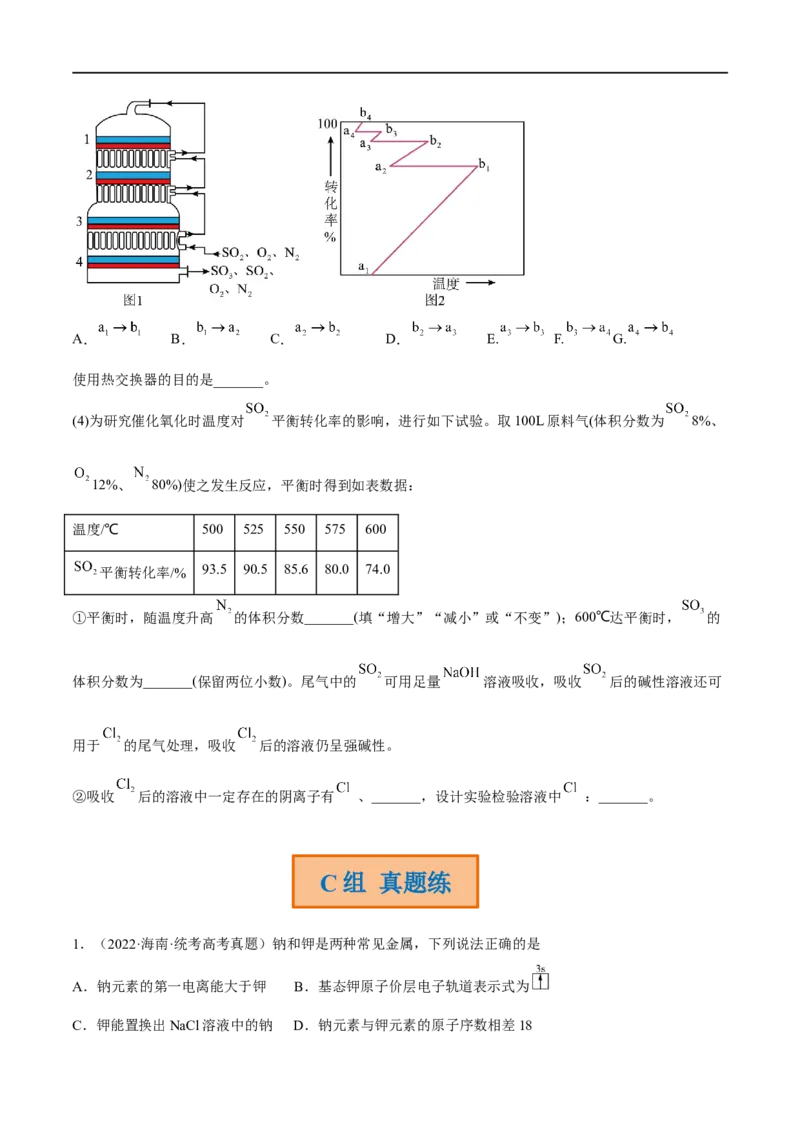
(3)催化氧化设备内构造如图1所示,其中1-4表示催化剂层,图2所示进程中表示热交换过程的是_______。
(选填选项)A. B. C. D. E. F. G.
使用热交换器的目的是_______。
(4)为研究催化氧化时温度对 平衡转化率的影响,进行如下试验。取100L原料气(体积分数为 8%、
12%、 80%)使之发生反应,平衡时得到如表数据:
温度/℃ 500 525 550 575 600
平衡转化率/% 93.5 90.5 85.6 80.0 74.0
①平衡时,随温度升高 的体积分数_______(填“增大”“减小”或“不变”);600℃达平衡时, 的
体积分数为_______(保留两位小数)。尾气中的 可用足量 溶液吸收,吸收 后的碱性溶液还可
用于 的尾气处理,吸收 后的溶液仍呈强碱性。
②吸收 后的溶液中一定存在的阴离子有 、_______,设计实验检验溶液中 :_______。
C 组 真题练
1.(2022·海南·统考高考真题)钠和钾是两种常见金属,下列说法正确的是
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差182.(2022·山东·高考真题)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂
质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
3.(2022·山东·高考真题)实验室制备 过程为:①高温下在熔融强碱性介质中用 氧化
制备 ;②水溶后冷却,调溶液 至弱碱性, 歧化生成 和 ;③减压
过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得 。下列说法正确的是
A.①中用瓷坩埚作反应器
B.①中用 作强碱性介质
C.②中 只体现氧化性
D. 转化为 的理论转化率约为66.7%
4.(2022·山东·高考真题)某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。
下列物质组合不符合要求的是气体 液体 固体粉末
A 饱和 溶液
B 溶液
C
溶液
D
A.A B.B C.C D.D
5.(2022·浙江·统考高考真题)尖晶石矿的主要成分为 (含 杂质)。已知:
。该反应难以发生,但采用“加炭氯化法”可以
制备 和 ,同时还可得到副产物 ( 沸点为 , 在 升华):
。下列说法不正确的是
A.制备时要保持无水环境
B.输送气态产物的管道温度要保持在 以上
C.氯化时加炭,既增大了反应的趋势,又为氯化提供了能量
D.为避免产生大量 ,反应过程中需保持炭过量
6.(2021·江苏·高考真题)下列有关物质的性质与用途不具有对应关系的是
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于净水
7.(2021·浙江·统考高考真题)铝硅酸盐型分子筛中有许多笼状空穴和通道(如图),其骨架的基本结构单
元是硅氧四面体和铝氧四面体,化学组成可表示为M[(AlO )·(SiO)]·zHO(M代表金属离子)。
a 2 x 2 y 2
下列推测不正确的是
A.常采用水玻璃、偏铝酸钠在强酸溶液中反应后结晶制得分子筛
B.若a=x/2,则M为二价阳离子
C.调节y/x(硅铝比)的值,可以改变分子筛骨架的热稳定性
D.分子筛中的笼状空穴和通道,可用于筛分分子
8.(2022·海南·统考高考真题)胆矾( )是一种重要化工原料,某研究小组以生锈的铜屑为原
料[主要成分是Cu,含有少量的油污、CuO、 、 ]制备胆矾。流程如下。
回答问题:
(1)步骤①的目的是_______。
(2)步骤②中,若仅用浓 溶解固体B,将生成_______(填化学式)污染环境。
(3)步骤②中,在 存在下Cu溶于稀 ,反应的化学方程式为_______。
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是_______。
(5)实验证明,滤液D能将 氧化为 。
ⅰ.甲同学认为不可能是步骤②中过量 将 氧化为 ,理由是_______。ⅱ.乙同学通过实验证实,只能是 将 氧化为 ,写出乙同学的实验方案及结果_______(不要求写具体
操作过程)。
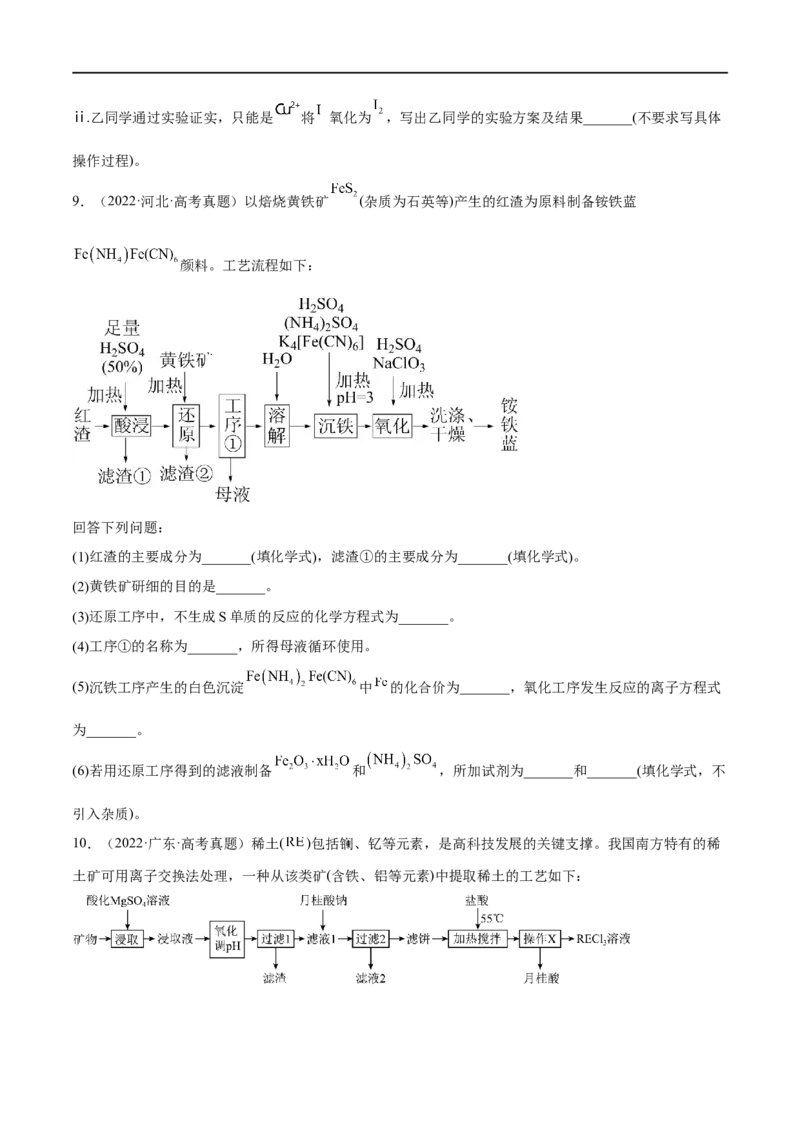
9.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
颜料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不
引入杂质)。
10.(2022·广东·高考真题)稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀
土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提
高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位有效数
字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为_______。