文档内容
第二章 分子结构
即刻题库 www.jike.vip
1 、 单选题
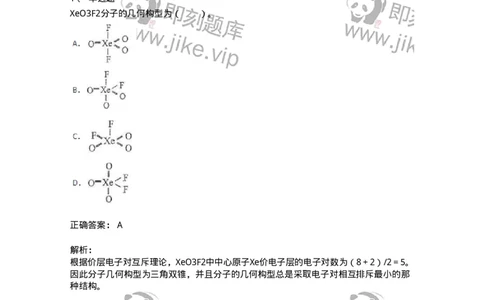
XeO3F2分子的几何构型为( )。
正确答案: A
解析:
根据价层电子对互斥理论,XeO3F2中中心原子Xe价电子层的电子对数为(8+2)/2=5。
因此分子几何构型为三角双锥,并且分子的几何构型总是采取电子对相互排斥最小的那
种结构。
2 、 单选题
按价键理论,下列分子中的中心原子在成键时必须拆开电子对的是( )。
A : NCl3
B : H2O
C : BCl3
D : SO2
正确答案: C解析:
3 、 单选题
下列分子或离子中,键角最小的是( )。
A : NH3
B : PCl4+
C : BF3
D : H2O
正确答案: D
解析:
A项:NH3中由于存在一对孤对电子对成键电子对的排斥作用,使氨分子中的N-H共价
单键之间的键角为107°18’;B项:PCl4+是正四面体型,键角为109°28’;C项:BF3
中B没有孤对电子,形成平面三角形的结构,键角为120°;D项:H2O的键角为104.5°。
4 、 单选题
下列分子为直线构型的为( )。
A : PbCl2
B : OF2
C : HCN
D : H2S
正确答案: C
解析:
OF2、H2S原子之间均为不等性 杂化,HCN原子间 杂化,呈直线型。
5 、 单选题
下列属于极性分子的是( )。
A : BCl3B : PH3
C : NH+4
D : BeCl2
正确答案: B
解析:
6 、 单选题
下列化合物中,键角大小排列顺序正确的是( )。
正确答案: B
解析:
7 、 单选题
气态CCl4的空间构型是( )。
A : 正四面体
B : 八面体
C : 平面三角形
D : 平面四方型
正确答案: A
解析:CCl4采取sp3等性杂化,空间构型为正四面体形。
8 、 单选题
气态SO3分子的几何构型是( )。
A : 直线形
B : 平面三角形
C : 弯曲形
D : 三角锥形
正确答案: B
解析:
SO3采取sp2杂化,几何构型为平面三角形。
9 、 单选题
下列分子中,中心原子不是采用sp^3d杂化轨道成键的是( )。
A : XeF2
B : ClF3
C : SF4
D : IF5
正确答案: D
解析:
10 、 单选题
下列各组化合物分子中,键角大小顺序正确的是( )。
A : HgCl2>BF3=PH3>CH4
B : CH4>PH3=BF3>HgCl2
C : HgCl2>BF3>CH4>PH3
D : PH3>CH4>HgCl2>BF3
正确答案: C
解析:
HgCl2是直线形,键角为180°;BF3是平面三角形,键角为120°;CH4为正四面体,键角
为109°28′;NH3是三棱锥形,键角为107°。由于P的电负性较N小,PH3中的成键电子云比NH3中的更偏向于H,同时P-H键长比N-H键长大,这样导致PH3中成键电子对之
间的斥力减小,孤对电子对成键电子的斥力使H-P-H键角更小,即PH3的键角小
于107°。故HgCl2>BF3>CH4>PH3。
11 、 单选题
某元素基态原子的电子构型为 ,它在周期表中的位置是( )。
A : S区,ⅡA
B : S区,VA
C : d区,ⅡB
D : d区,ⅦB
A : 等性sp3杂化
B : 等性sp2杂化
C : 非等性sp3杂化
D : sp杂化
正确答案: D
解析:
AB两项,基态原子的4s轨道全满,3d轨道半满,说明一定为副族元素。再由核外电子数
推得该原子处于ⅦB族,Mn原子。
12 、 单选题
下列说法正确的是( )。
A : 中心原子采取sp^3杂化的分子几何构型都是正四面体
B : AB4型分子都是非极性分子
C : 极性分子之间只存在取向力
D : 所有正面体分子都是非极性分子
正确答案: D
解析:
A项:中心原子采取sp^3杂化的分子几何构型都是四面体,不一定为正四面体;B
项:AB4型分子若为sp^3杂化,则为非极性分子;C项,极性分子之间不仅存在取向力,
还存在色散力,诱导力等;D项:正面体分子中正负电荷中心重合,不存在永久分子偶
极矩,因而为非极性分子。
13 、 单选题
下列物质中,存在分子内氢键的是( )。
A : HNO3B : C2H4
C : HI
D : NH3
正确答案: A
解析:
HNO3存在分子内氢键,NH3存在分子间氢键。
14 、 单选题
在石墨晶体中碳原子层与碳原子层之间的作用力为( )。
A : 配位键
B : 共价键
C : 双键
D : 范德华力
正确答案: D
解析:
石墨晶体层内C原子间采用共价键结合,层与层之间采用较弱的范德华力结合,层与层
之间可以滑动。
15 、 单选题
根据价层电子对互斥理论,下列各对物质中分子几何构型明显不同的是( )。
A : CH4和NH4^+
B : PH3和NCl3
C : H2O和H2S
D : CCl4和SF4
正确答案: D
解析:
D项中心原子C有4个价电子,Cl原子各提供1个电子,所以P原子的价层电子对数(4+4)
/2=4,构型为正四面体;中心原子S有6个价电子,F原子各提供1个电子,所以P原子的
价层电子对数(6+4)/2=5,其构型为三角双锥。
16 、 单选题正确答案: A
解析:
17 、 单选题
下列离子的电子构型可以用[Ar]3d^6表示的是( )。
A : Mn^2+
B : Fe^3+
C : 0^3+
D : Cr^3+
正确答案: C
解析:
18 、 单选题
d轨道与d轨道相互重叠可形成的化学键类型为( )。
A : 只能形成σ键
B : 可形成σ、π键
C : 只能形成π键
D : 可形成σ、π、δ键
正确答案: D
解析:
d轨道含有5个轨道,既可以“肩并肩”的方式成键,也可以“头碰头”的方式成键,由
两个相同或不同的原子的价电子沿着轨道对称轴方向相互重叠所形成δ键。
19 、 单选题按分子轨道理论,O2分子中最高能量的电子所处的分子轨道是( )。
A : π2p
B : π2p^*
C : σ2p
D : σ2p^*
正确答案: B
解析:
20 、 单选题
N2、O2、F2分子的键强度为N2>O2>F2。该顺序的最佳解释为( )。
A : 分子量增加的顺序为N2<O2<F2
B : 电负性增加的顺序为N<O<F
C : 气态原子的摩尔生成焓的增大顺序为N(g)>O(g)>F(g)
D : 成键轨道的电子数的增大顺序为N2>O2>F2
正确答案: C
解析:
气态原子的摩尔生成焓即是生成1mol的气态原子所需要的能量,若所需能量越大,则键
强越大。
21 、 单选题
下列各物种中,键角大小的顺序正确的是( )。
正确答案: B
解析:根据价层电子对互斥理论可以推测出三种分子或离子的分子结构,NO2+为直线型,其
他两种为平面三角型。
22 、 单选题
下列分子中哪一个具有最小的键角( )。
A : PH3
B : AsH3
C : NH3
D : H2O
正确答案: B
解析:
P、As、N、O与H成键都会有孤对电子的存在,其对键角的大小都有影响,而As的半径
最大,其与H成键后最容易受到电子对的影响而偏离电子对,使其键角最小。
23 、 单选题
中心原子以等性 杂化轨道成键的化合物为( )。
正确答案: D
解析: