文档内容
★ 保密·启用前
★
吉林地区普通中学2024-2025学年度高中毕业年级第三次调研测试
化 学 试 题
说明:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上,贴好条形码。
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案标号涂
黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。答非选择题时,用0.5
毫米的黑色签字笔将答案写在答题卡上。字体工整,笔迹清楚。
3.请按题号顺序在答题卡相应区域作答,超出区域所写答案无效;在试卷上、草
纸上答题无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Fe 56
一、选择题:本题共15小题,每题3分,共45分,在每小题给出的四个选项中,只有一
项符合题目要求。
1.近年我国“硬核化学”科技成果收获丰硕,对提升新质生产力功不可没。下列说法正确
的是
A.我国自主建造的航母使用高性能富锌底漆是采用牺牲阳极法防腐蚀
B.通过破坏共价键实施CO 海底液化封存,可助力“碳达峰”、“碳中和”
2
C.北斗卫星的“星载铷钟”中使用的铷单质遇水会缓慢反应放出氢气
D.利用CO 合成高级脂肪酸甘油酯,实现无机小分子向有机高分子的转化
2
2.下列化学用语或表述错误的是
A. 的结构示意图为:
B. 的最外层电子排布图为:
C.用电子式表示 的形成:
D. 的系统命名:2-甲基苯酚
3.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.18 g重水(DO)中含有的质子数为10 N
2 A
B.12g NaHSO 中含有0.2 N 个阳离子
4 A
C.标准状况下,22.4 L HCl气体中H+数目为N
A
D.0.20 mol苯甲酸完全燃烧,生成CO 的数目为1.4 N
2 A
高三化学试题 第 1 页 (共 10 页)4.苦杏仁酸具有促进新陈代谢、补充营养和去角质等作用,可用如下方法制备。
下列说法错误的是
A.①②分别为加成反应、水解反应
B. 上述过程中涉及到的有机物中有手性化合物
C.苦杏仁酸的聚合产物 可作为高吸水性材料
D.1mol 最多可与5mol H 发生反应
2
5.下列有关物质性质与用途正确,且具有对应关系的是
A. 浓硫酸有脱水性,可用作干燥剂
B.NH 显碱性,可用作制冷剂
3
C.碳酸钠受热分解产生气体,可用作食品膨松剂
D. SiO 传导光的能力非常强,可用于制光导纤维
2
6.下列实验的现象及相应的结论都正确的是
实验 现象 结论
向装有经硫酸处理的CrO (橘
3 固体逐渐由橘红色变
A 红色)的硅胶导管中吹入乙醇蒸 乙醇具有还原性
为浅绿色( )
气
将铁锈溶于浓盐酸,滴入
B 溶液紫色褪去 铁锈中含有二价铁
溶液
在纯净物X柱面上滴一滴熔化
C 的石蜡,用一根红热的铁针刺中 石蜡熔化呈椭圆形 说明物质X为非晶体
凝固的石蜡
向10 mL 0.2 mol·L-1 ZnSO 溶 相同温度下,溶度积
4 先产生白色沉淀,然后
D 液中加入 10 mL 0.4 mol·L-1 常 数 : K (CuS) <
沉淀变黑 sp
Na S溶液,再滴加CuSO 溶液 K (ZnS)
2 4 sp
7.部分含铁微粒所带的电荷数与其中铁元素化合价的关系如图所示,下列推断合理的是
高三化学试题 第 2 页 (共 10 页)A.若A为单质,则常温下浓硝酸可将A溶解
B.若B不溶于水,则B一定为FeO
2 3
C.若C为金属阳离子,则可用K[Fe(CN) ]溶液检验,
3 6
可由FeO 与过量氢碘酸反应生成
2 3
D.Fe3+与氧化剂在酸性条件下反应可生成FeO,
FeO能对饮用水进行消毒、净化
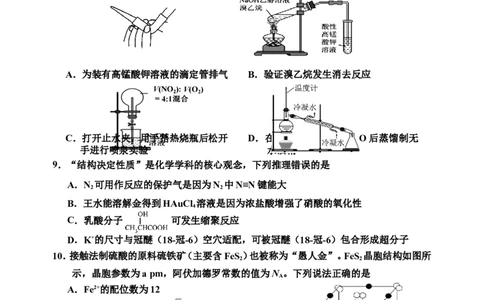
8.下列实验装置正确且能达到实验目的的是
A.为装有高锰酸钾溶液的滴定管排气 B.验证溴乙烷发生消去反应
C.打开止水夹,用手捂热烧瓶后松开 D.在含水酒精中加入CaO后蒸馏制无
手进行喷泉实验 水酒精
9.“结构决定性质”是化学学科的核心观念,下列推理错误的是
A.N 可用作反应的保护气是因为N 中N≡N键能大
2 2
B.王水能溶解金得到HAuCl 溶液是因为浓盐酸增强了硝酸的氧化性
4
C.乳酸分子 可发生缩聚反应
D.K+的尺寸与冠醚(18-冠-6)空穴适配,可被冠醚(18-冠-6)包合形成超分子
10.接触法制硫酸的原料硫铁矿(主要含FeS )也被称为“愚人金”。FeS 晶胞结构如图所
2 2
示,晶胞参数为a pm,阿伏加德罗常数的值为N 。下列说法正确的是
A
A.Fe2+的配位数为12
B.Fe2+间的最短距离为 a pm
C.S位于Fe2+所形成的正四面体空隙
D.FeS 晶胞密度为
2
11.汽车尾气是导致空气质量问题的重要原因,利用反应2CO(g)+2NO(g) 2CO (g)+
2
N(g)可有效降低汽车尾气污染物的排放。一定条件下该反应历程如图所示(TS代表过
2
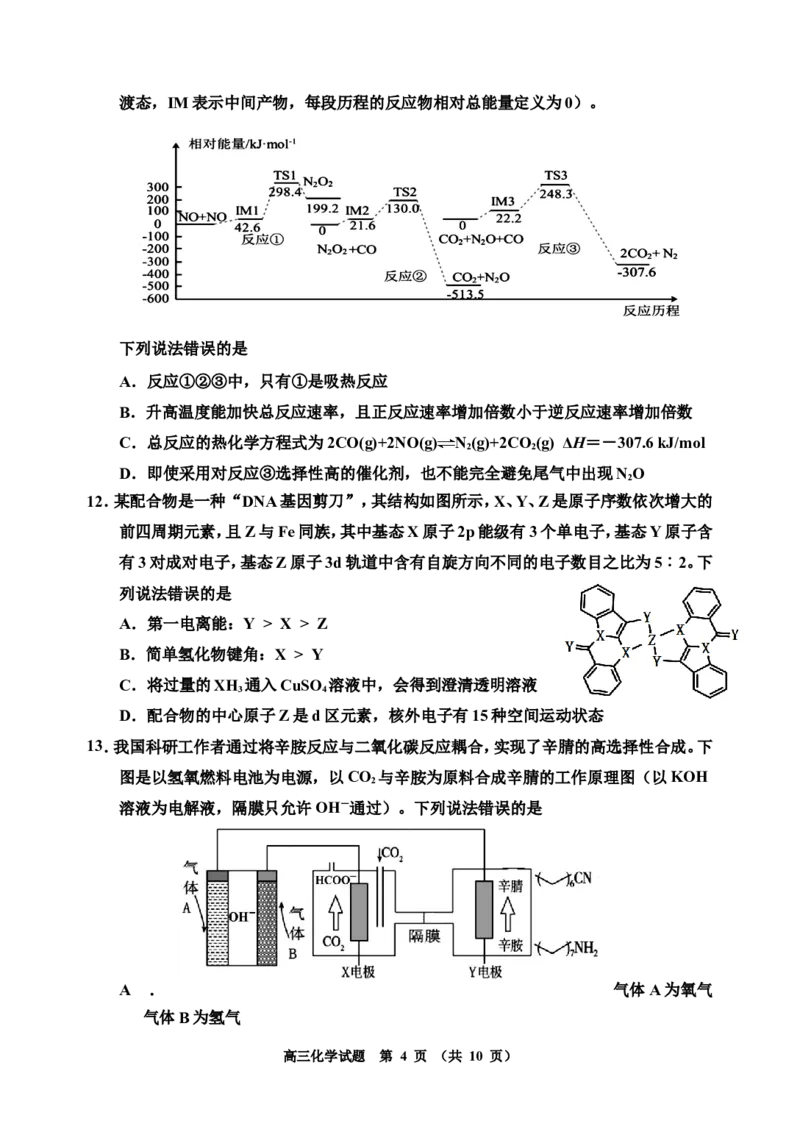
高三化学试题 第 3 页 (共 10 页)渡态,IM表示中间产物,每段历程的反应物相对总能量定义为0)。
下列说法错误的是
A.反应①②③中,只有①是吸热反应
B.升高温度能加快总反应速率,且正反应速率增加倍数小于逆反应速率增加倍数
C.总反应的热化学方程式为2CO(g)+2NO(g) N(g)+2CO (g) ΔH=-307.6 kJ/mol
2 2
D.即使采用对反应③选择性高的催化剂,也不能完全避免尾气中出现NO
2
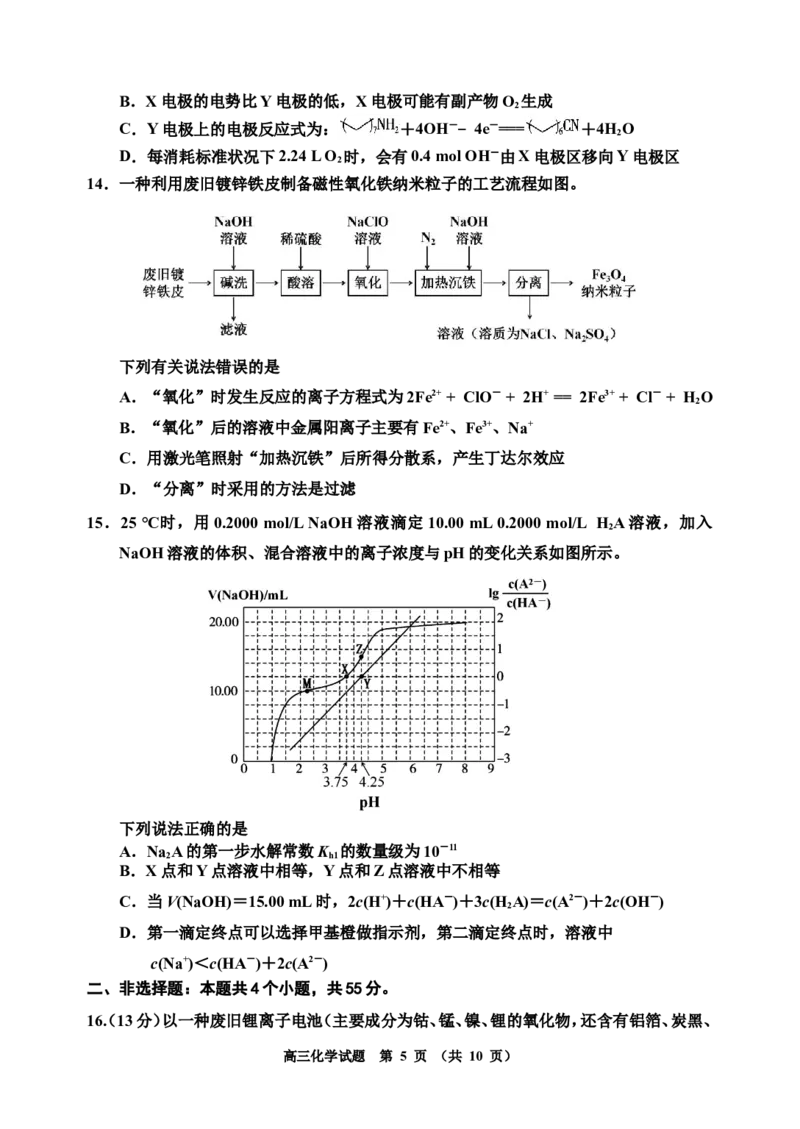
12.某配合物是一种“DNA基因剪刀”,其结构如图所示,X、Y、Z是原子序数依次增大的
前四周期元素,且Z与Fe同族,其中基态X原子2p能级有3个单电子,基态Y原子含
有3对成对电子,基态Z原子3d轨道中含有自旋方向不同的电子数目之比为5︰2。下
列说法错误的是
A.第一电离能:Y > X > Z
B.简单氢化物键角:X > Y
C.将过量的XH 通入CuSO 溶液中,会得到澄清透明溶液
3 4
D.配合物的中心原子Z是d区元素,核外电子有15种空间运动状态
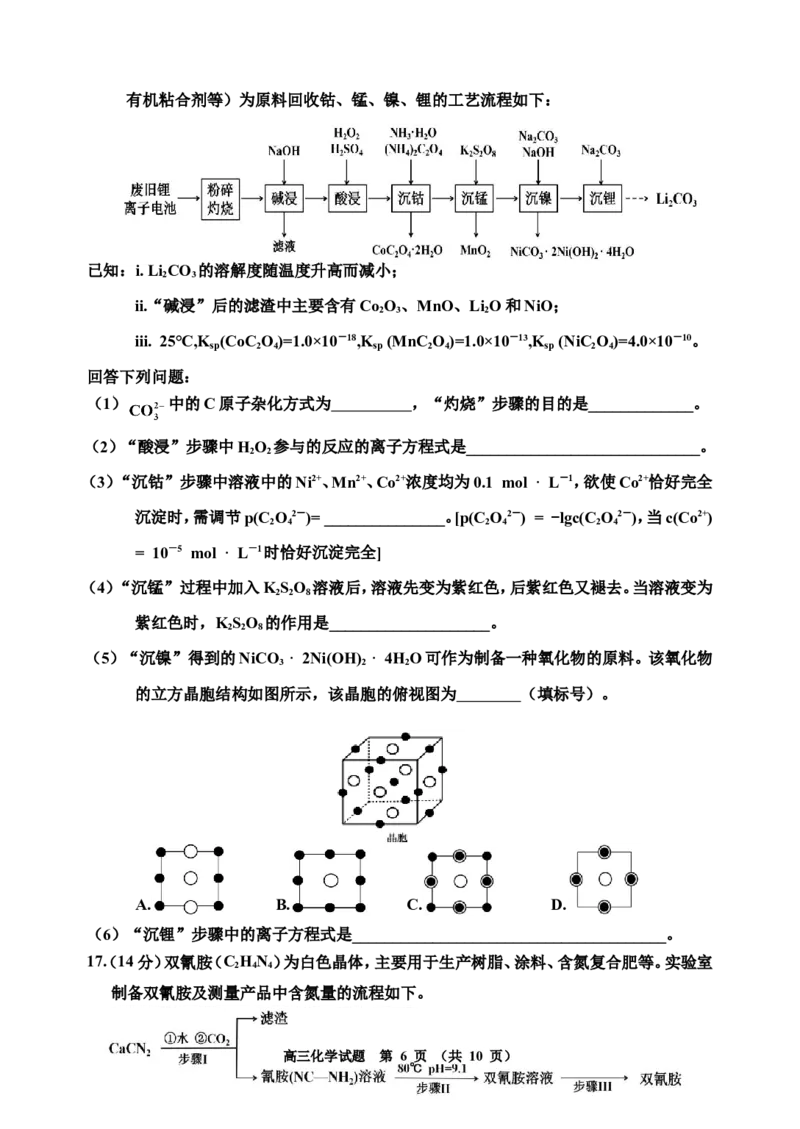
13.我国科研工作者通过将辛胺反应与二氧化碳反应耦合,实现了辛腈的高选择性合成。下
图是以氢氧燃料电池为电源,以CO 与辛胺为原料合成辛腈的工作原理图(以KOH
2
溶液为电解液,隔膜只允许OH-通过)。下列说法错误的是
A . 气体A为氧气
气体B为氢气
高三化学试题 第 4 页 (共 10 页)B.X电极的电势比Y电极的低,X电极可能有副产物O 生成
2
C.Y电极上的电极反应式为: +4OH-- 4e-=== +4HO
2
D.每消耗标准状况下2.24 L O 时,会有0.4 mol OH-由X电极区移向Y电极区
2
14.一种利用废旧镀锌铁皮制备磁性氧化铁纳米粒子的工艺流程如图。
下列有关说法错误的是
A.“氧化”时发生反应的离子方程式为2Fe2+ + ClO- + 2H+ == 2Fe3+ + Cl- + HO
2
B.“氧化”后的溶液中金属阳离子主要有Fe2+、Fe3+、Na+
C.用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
D.“分离”时采用的方法是过滤
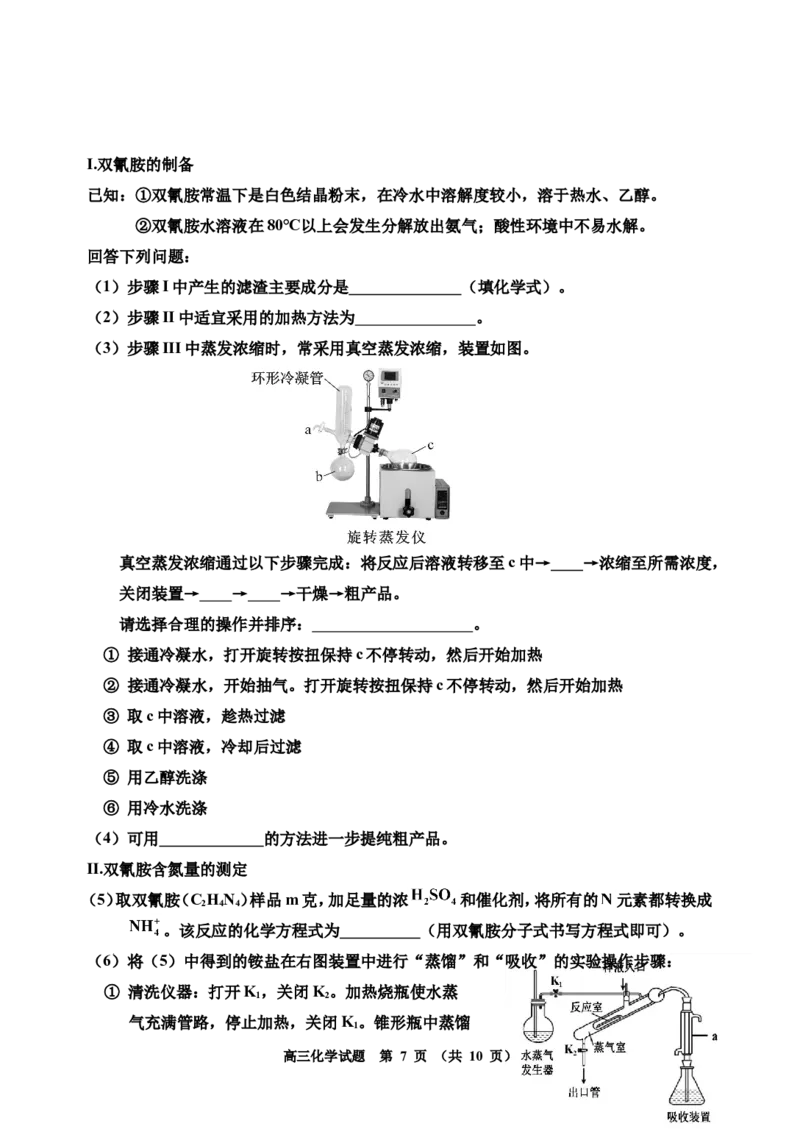
15.25 ℃时,用0.2000 mol/L NaOH溶液滴定10.00 mL 0.2000 mol/L HA溶液,加入
2
NaOH溶液的体积、混合溶液中的离子浓度与pH的变化关系如图所示。
下列说法正确的是
A.Na A的第一步水解常数K 的数量级为10-11
2 h1
B.X点和Y点溶液中相等,Y点和Z点溶液中不相等
C.当V(NaOH)=15.00 mL时,2c(H+)+c(HA-)+3c(H A)=c(A2-)+2c(OH-)
2
D.第一滴定终点可以选择甲基橙做指示剂,第二滴定终点时,溶液中
c(Na+)<c(HA-)+2c(A2-)
二、非选择题:本题共4个小题,共55分。
16(. 13分)以一种废旧锂离子电池(主要成分为钴、锰、镍、锂的氧化物,还含有铝箔、炭黑、
高三化学试题 第 5 页 (共 10 页)有机粘合剂等)为原料回收钴、锰、镍、锂的工艺流程如下:
已知:i. Li CO 的溶解度随温度升高而减小;
2 3
ii.“碱浸”后的滤渣中主要含有Co O、MnO、LiO和NiO;
2 3 2
iii. 25℃,K (CoC O)=1.0×10-18,K (MnC O)=1.0×10-13,K (NiC O)=4.0×10-10。
sp 2 4 sp 2 4 sp 2 4
回答下列问题:
(1) 中的C原子杂化方式为 ,“灼烧”步骤的目的是_____________。
(2)“酸浸”步骤中HO 参与的反应的离子方程式是_____________________________。
2 2
(3)“沉钴”步骤中溶液中的Ni2+、Mn2+、Co2+浓度均为0.1 mol · L-1,欲使Co2+恰好完全
沉淀时,需调节p(C O2-)= _______________。[p(C O2-) = -lgc(C O2-),当c(Co2+)
2 4 2 4 2 4
= 10-5 mol · L-1时恰好沉淀完全]
(4)“沉锰”过程中加入KSO 溶液后,溶液先变为紫红色,后紫红色又褪去。当溶液变为
2 2 8
紫红色时,KSO 的作用是____________________。
2 2 8
(5)“沉镍”得到的NiCO · 2Ni(OH) · 4HO可作为制备一种氧化物的原料。该氧化物
3 2 2
的立方晶胞结构如图所示,该晶胞的俯视图为 (填标号)。
A. B. C. D.
(6)“沉锂”步骤中的离子方程式是_______________________________________。
17(. 14分)双氰胺(CHN)为白色晶体,主要用于生产树脂、涂料、含氮复合肥等。实验室
2 4 4
制备双氰胺及测量产品中含氮量的流程如下。
高三化学试题 第 6 页 (共 10 页)Ⅰ.双氰胺的制备
已知:①双氰胺常温下是白色结晶粉末,在冷水中溶解度较小,溶于热水、乙醇。
②双氰胺水溶液在80℃以上会发生分解放出氨气;酸性环境中不易水解。
回答下列问题:
(1)步骤I中产生的滤渣主要成分是 (填化学式)。
(2)步骤II中适宜采用的加热方法为 。
(3)步骤III中蒸发浓缩时,常采用真空蒸发浓缩,装置如图。
真空蒸发浓缩通过以下步骤完成:将反应后溶液转移至c中→ →浓缩至所需浓度,
关闭装置→ → →干燥→粗产品。
请选择合理的操作并排序: 。
① 接通冷凝水,打开旋转按扭保持c不停转动,然后开始加热
② 接通冷凝水,开始抽气。打开旋转按扭保持c不停转动,然后开始加热
③ 取c中溶液,趁热过滤
④ 取c中溶液,冷却后过滤
⑤ 用乙醇洗涤
⑥ 用冷水洗涤
(4)可用 的方法进一步提纯粗产品。
Ⅱ.双氰胺含氮量的测定
(5)取双氰胺(CHN)样品m克,加足量的浓 和催化剂,将所有的 元素都转换成
2 4 4
。该反应的化学方程式为 (用双氰胺分子式书写方程式即可)。
(6)将(5)中得到的铵盐在右图装置中进行“蒸馏”和“吸收”的实验操作步骤:
① 清洗仪器:打开K,关闭K。加热烧瓶使水蒸
1 2
气充满管路,停止加热,关闭K。锥形瓶中蒸馏
1
高三化学试题 第 7 页 (共 10 页)水倒吸进入反应室,原因是 。
打开K 放掉洗涤水,重复操作2~3次。
2
② 向锥形瓶中加入硼酸溶液及指示剂。
铵盐由样液入口注入反应室,并注入一定量的氢氧化钠溶液,用蒸馏水冲洗后,封闭
样液入口,开始蒸馏,使产生的气体进入吸收装置。反应装置使用了双层玻璃,其作
用是 。
18.(14分)氢气在化学工业中应用广泛,回答下列问题:
(1)将CH 和CO 两种气体转化为合成气(H 和CO),可以实现能量综合利用,对环境保护
4 2 2
具有十分重要的意义。甲烷及二氧化碳重整涉及以下反应:
I.
Ⅱ.
Ⅲ.
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1 mol该物
质的焓变。对于稳定相态单质,其 为零。根据下表数据,计算反应Ⅱ的焓变
___________。
物质 CH CO CO HO(g)
4 2 2
( )
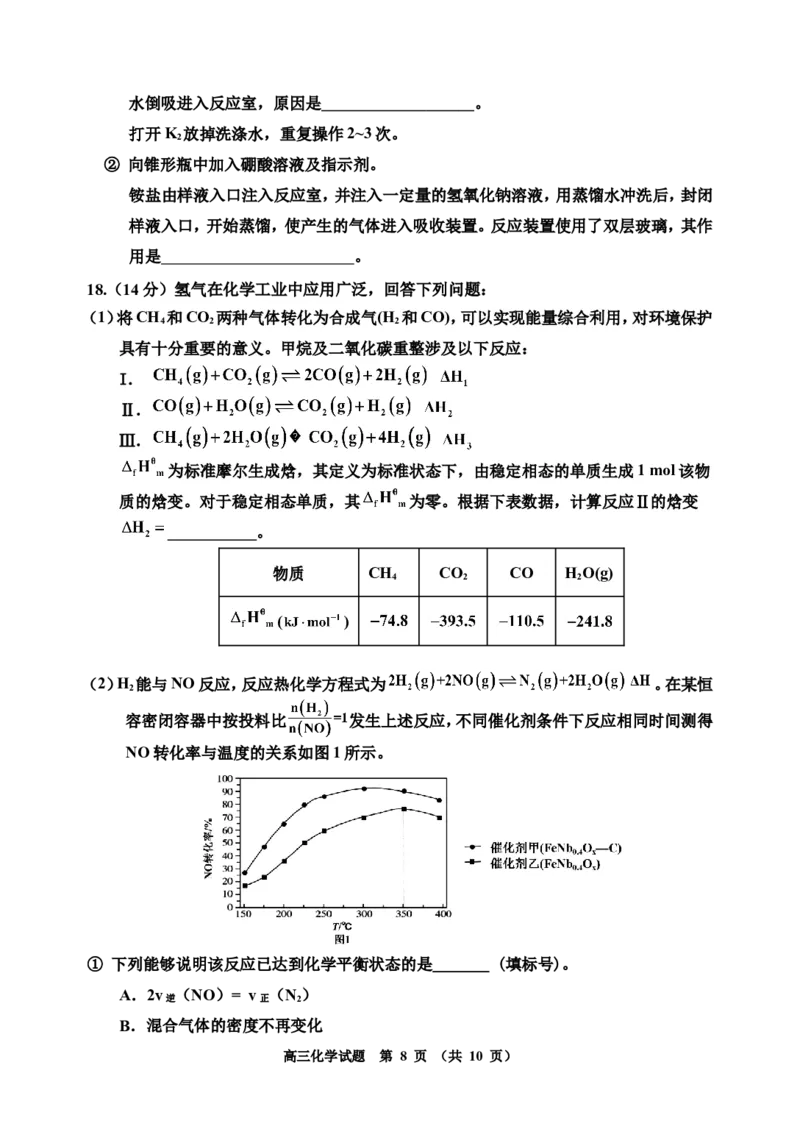
(2)H 能与NO反应,反应热化学方程式为 。在某恒
2
容密闭容器中按投料比 发生上述反应,不同催化剂条件下反应相同时间测得
NO转化率与温度的关系如图1所示。
① 下列能够说明该反应已达到化学平衡状态的是_______ (填标号)。
A.2v (NO)= v (N)
逆 正 2
B.混合气体的密度不再变化
高三化学试题 第 8 页 (共 10 页)C.容器内总压强不再变化
D.混合气体的平均相对分子质量不再变化
② 使用催化剂乙时,NO转化率随温度升高先增大后减小,当温度高于350℃后NO转化
率减小的可能原因是_______。
③ 研究表明该反应v = kcm(H )c2(NO),其中k为速率常数,与温度、活化能有关。T ℃的
2 1
初始速率为v,当H 转化率为50%时,反应速率为 ,由此可知m=_______。设此时反
0 2
应的活化能为E ′,不同温度T 、T 条件下对应的速率常数分别为k、k,存在关系:
a 1 2 1 2
(R为常数)。据此推测:活化能越大,改变温度,速率常数受到的影
响_______ (填“越大”或“越小” )。
(3)La A BCoO (A、B均为过渡元素)是一种高效催化剂,利用表面氧缺位来催化化学
0.8 0.2 3+x
反应。用H 还原NO的机理如下:
2
第一阶段:Co4(+ 不稳定)+H →低价态的金属离子(还原前后催化剂中金属原子的个数
2
不变)
第二阶段:I.NO(g)+□→NO(a) Ⅱ.2NO(a)→2N(a)+O (g)
2
Ⅲ.2N(a)→N (g)+2□ Ⅳ.2NO(a)→N (g)+2O(a)
2 2
V.2O(a)→O (g)+2□
2
注:□表示催化剂表面的氧缺位,g表示气态,a表示吸附态
第一阶段用氢气还原Co4+得到低价态的金属离子越多,第二阶段反应的速率越快,原
因是_______。
(4)工业上常利用反应N
2
(g)+3H
2
(g)⇌2NH
3
(g) △H<0合成氨气,在30MPa、不同物质的量
分数(75%的H 和25%的N;67.5%的H、22.5%的
2 2 2
N 和10%的惰性气体)条件下进行实验,测得平衡时,
2
NH 体积分数与温度的关系如图2。
3
① 物质的量分数为75%的H 和25%的N 对应的曲
2 2
线
是_______(填“a”或“b”)。
② M 点,该反应的压强平衡常数 K =____(MPa) -
p
2(用 平衡分压代替平衡浓度,分压=总压×物质的
量分数)。
19(. 14分)抗体偶联药物DXD有较高的生物活性,目前用于肿瘤的治疗中。下图是其中一
高三化学试题 第 9 页 (共 10 页)种关键中间体J的合成路线:
请回答下列问题:
(1)化合物B中含氧官能团的名称为__________________。
(2)I→J的反应类型是__________________。
(3)D转化为E时另一中性有机生成物为__________________(填结构简式)。
(4)化合物H→I的合成过程中,经历了硝化、还原和取代三步反应,其中取代反应的化学
方程式为_______________________________________________________。
(5)化合物C的同分异构体中满足下列条件的有_________种。
① 只有苯环1种环状结构
② 在核磁共振氢谱上有3组吸收峰
③ 氟原子与苯环直接相连
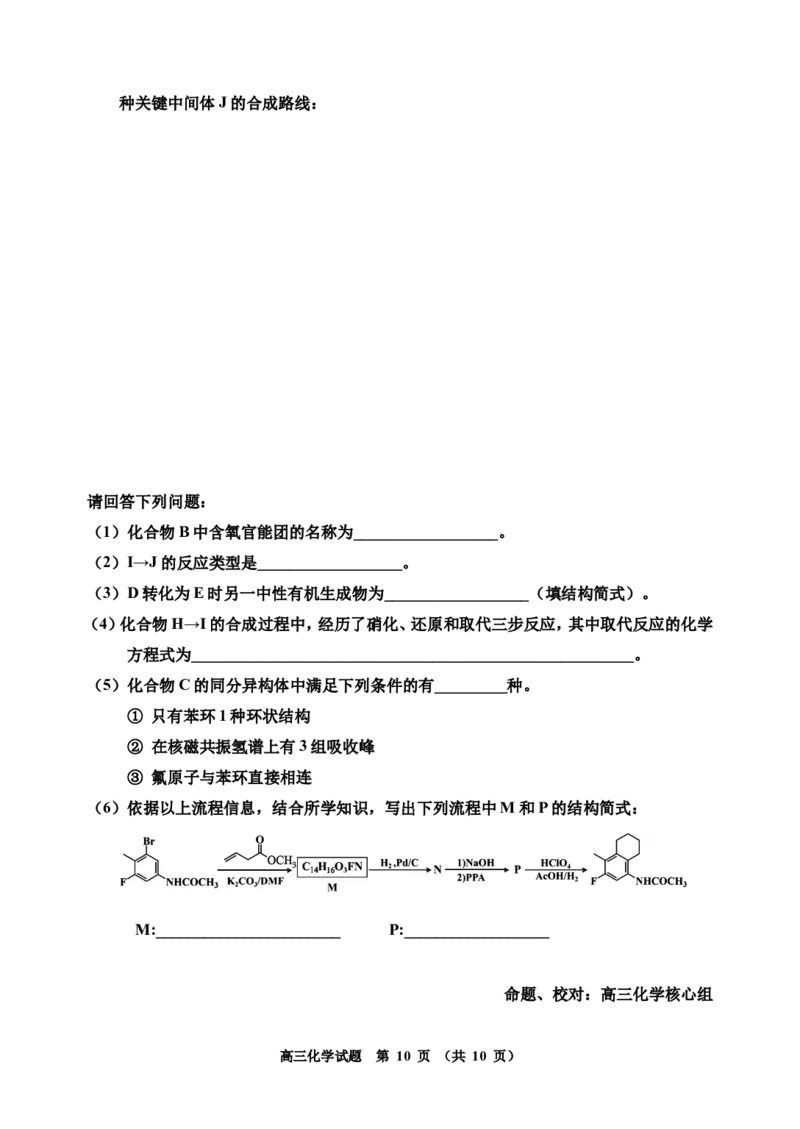
(6)依据以上流程信息,结合所学知识,写出下列流程中M和P的结构简式:
M:_______________________ P:__________________
命题、校对:高三化学核心组
高三化学试题 第 10 页 (共 10 页)