文档内容
高三化学
考生请注意:
1. 本试卷共8页,满分100分,考试时间75分钟.考试结束后,交回答题
纸;
2. 答题前,请务必将自己的姓名、考生号用0.5毫米黑色中性笔或碳素笔
在答题纸上进行书写;
3. 作答选择题,必须用2B铅笔将答题纸上的对应题目的答题标号涂黑涂
满;如需改动,请用橡皮擦干净后,再更正其它的答案.未在答题纸上
作答的、在答题纸规定区域以外答题的一律无效;
4. 如有作图需要,请使用2B铅笔作图,并加黑加粗,描写清楚.
可能用 到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Cl 35.5 Cr 52
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与生产、生活等密切相关。下列说法错
.
误
.
的是
A.漂白粉和漂粉精既可作漂白棉、麻的漂白剂,也可用作游泳池等场所的消毒剂
B.向煤中加入适量生石灰,燃烧时使硫元素转移到煤渣中,可减少二氧化硫的排放
C.陶瓷的烧制、石油的分馏、煤的干馏过程中,均涉及化学变化
D.颁奖礼服内胆里添加的导热系数高的柔性石墨烯发热材料属于新型无机非金属材料
2.下列图示过程中,由太阳能直接转化为化学能的是
A. B. C. D.
3.下列反应中,属于放热反应的是
A.Ba(OH) ·8H O与NH Cl混合搅拌
2 2 4
B.高温煅烧石灰石
C.铝与盐酸反应
D.碳与水蒸气高温下反应
4.实验探究有助于提高学习效果。某同学用如图所示装置研究原电池原理,下列说法错
.
误
.
的是
第 1 页 共 8 页
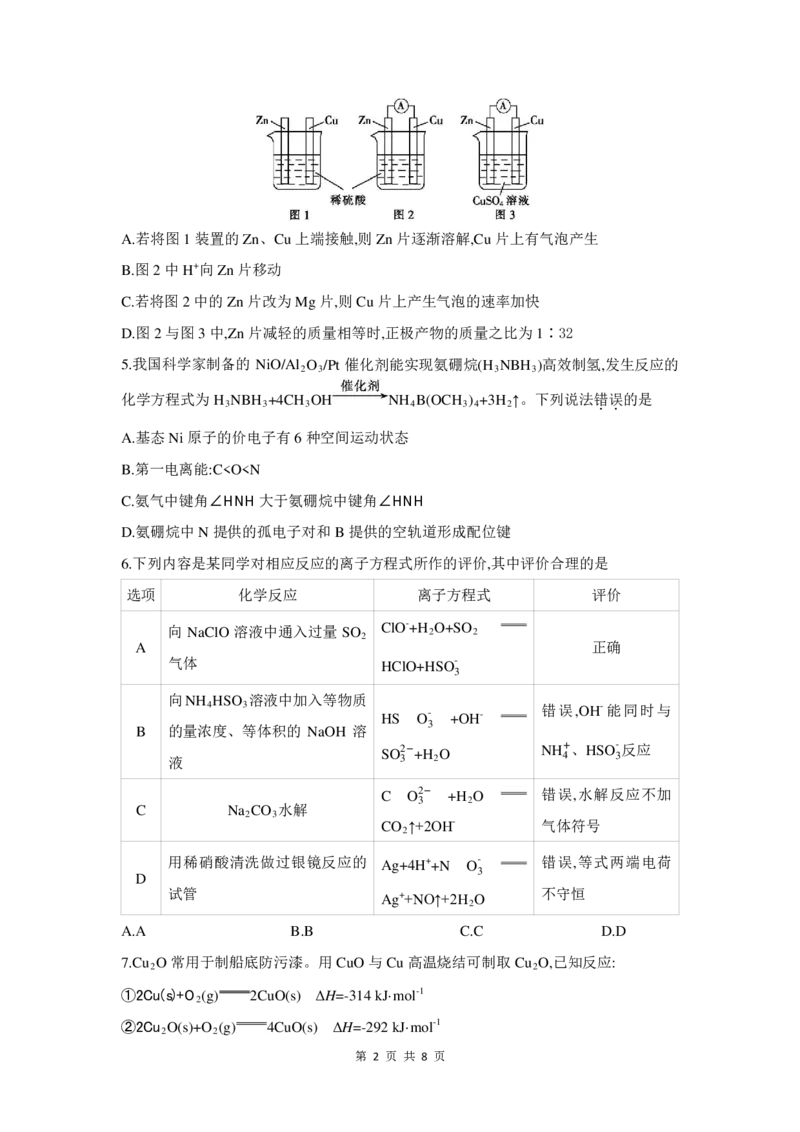
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}A.若将图1装置的Zn、Cu上端接触,则Zn片逐渐溶解,Cu片上有气泡产生
B.图2中H+向Zn片移动
C.若将图2中的Zn片改为Mg片,则Cu片上产生气泡的速率加快
D.图2与图3中,Zn片减轻的质量相等时,正极产物的质量之比为1∶32
5.我国科学家制备的 NiO/Al O /Pt 催化剂能实现氨硼烷(H NBH )高效制氢,发生反应的
2 3 3 3
化学方程式为H 3 NBH 3 +4CH 3 OH NH 4 B(OCH 3 ) 4 +3H 2 ↑。下列说法错 . 误 . 的是
A.基态Ni原子的价电子有6种空间运动状态
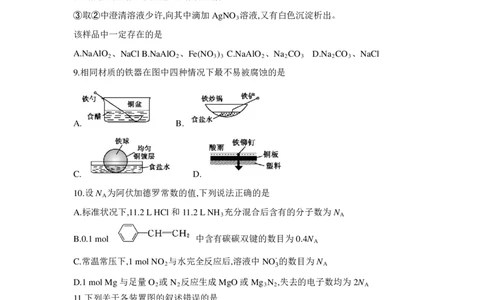
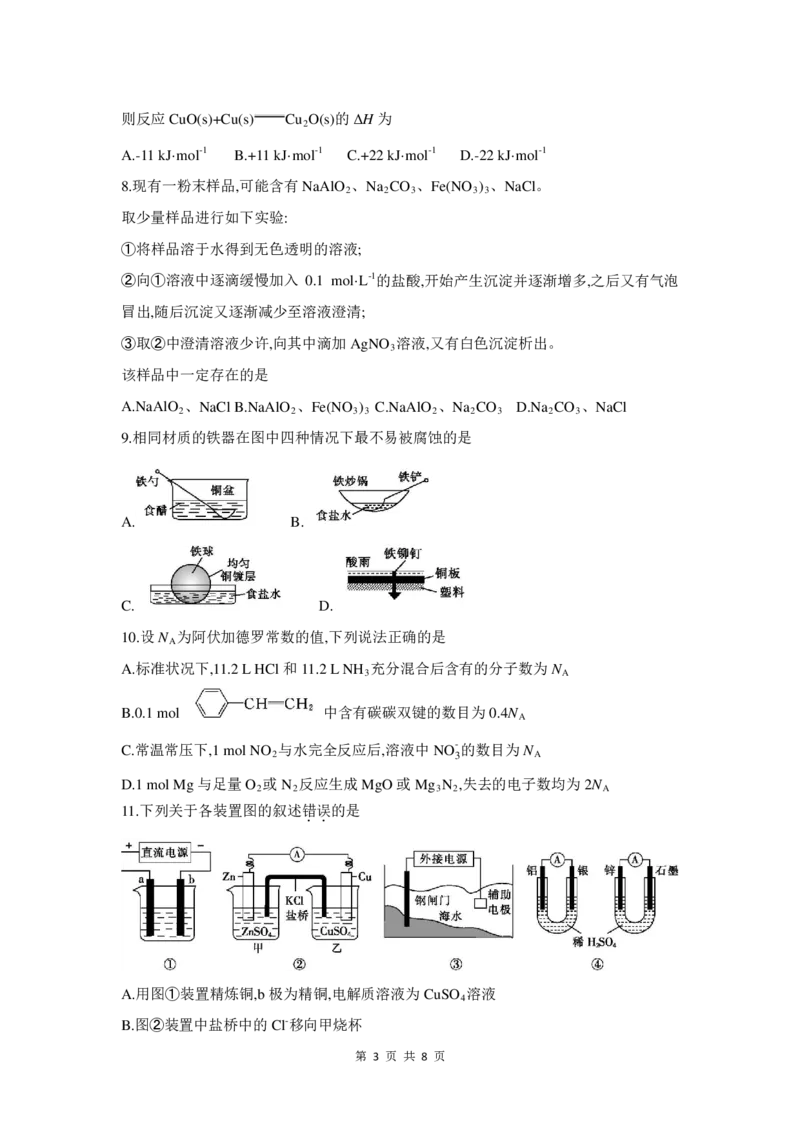
B.第一电离能:CW>Z>Y>X B.第一电离能:W>R
C.X、W、R能形成离子晶体 D.最高价含氧酸的酸性:Y>Z
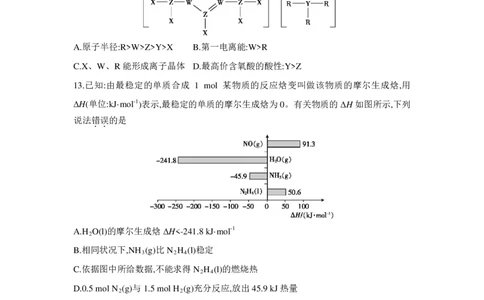
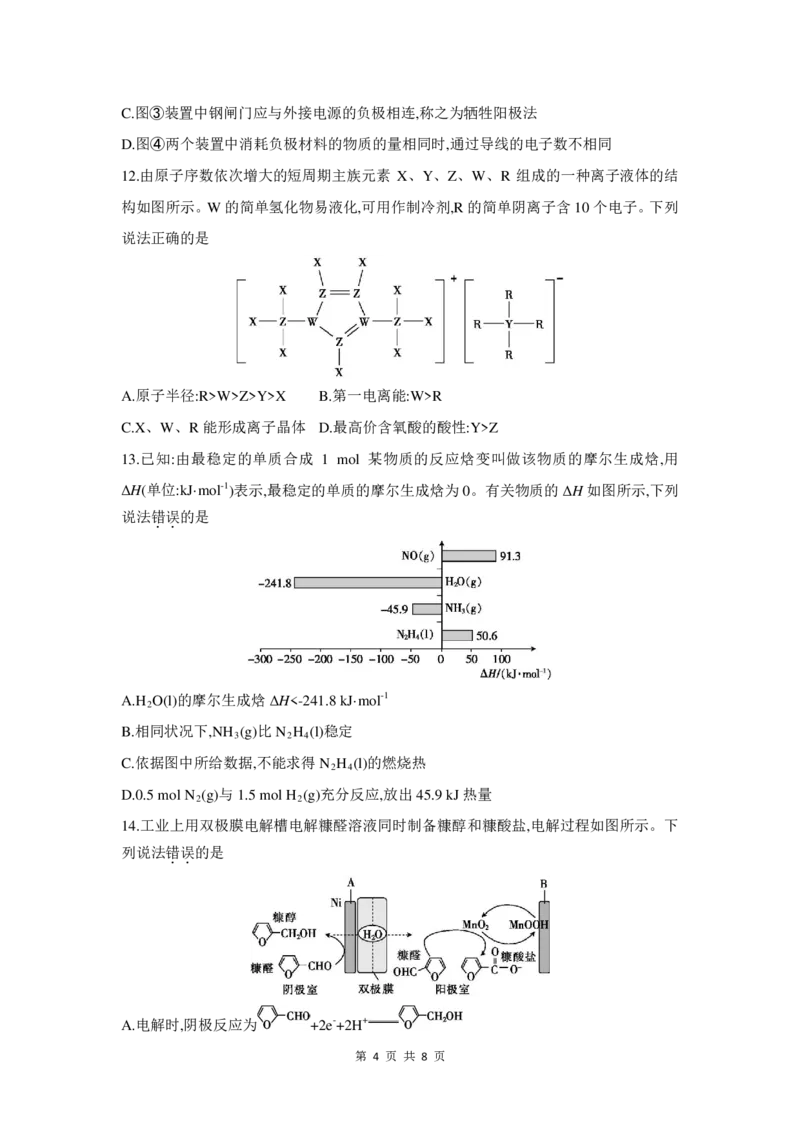
13.已知:由最稳定的单质合成 1 mol 某物质的反应焓变叫做该物质的摩尔生成焓,用
ΔH(单位:kJ·mol-1)表示,最稳定的单质的摩尔生成焓为0。有关物质的ΔH如图所示,下列
说法错
.
误
.
的是
A.H O(l)的摩尔生成焓ΔH<-241.8 kJ·mol-1
2
B.相同状况下,NH (g)比N H (l)稳定
3 2 4
C.依据图中所给数据,不能求得N H (l)的燃烧热
2 4
D.0.5 mol N (g)与1.5 mol H (g)充分反应,放出45.9 kJ热量
2 2
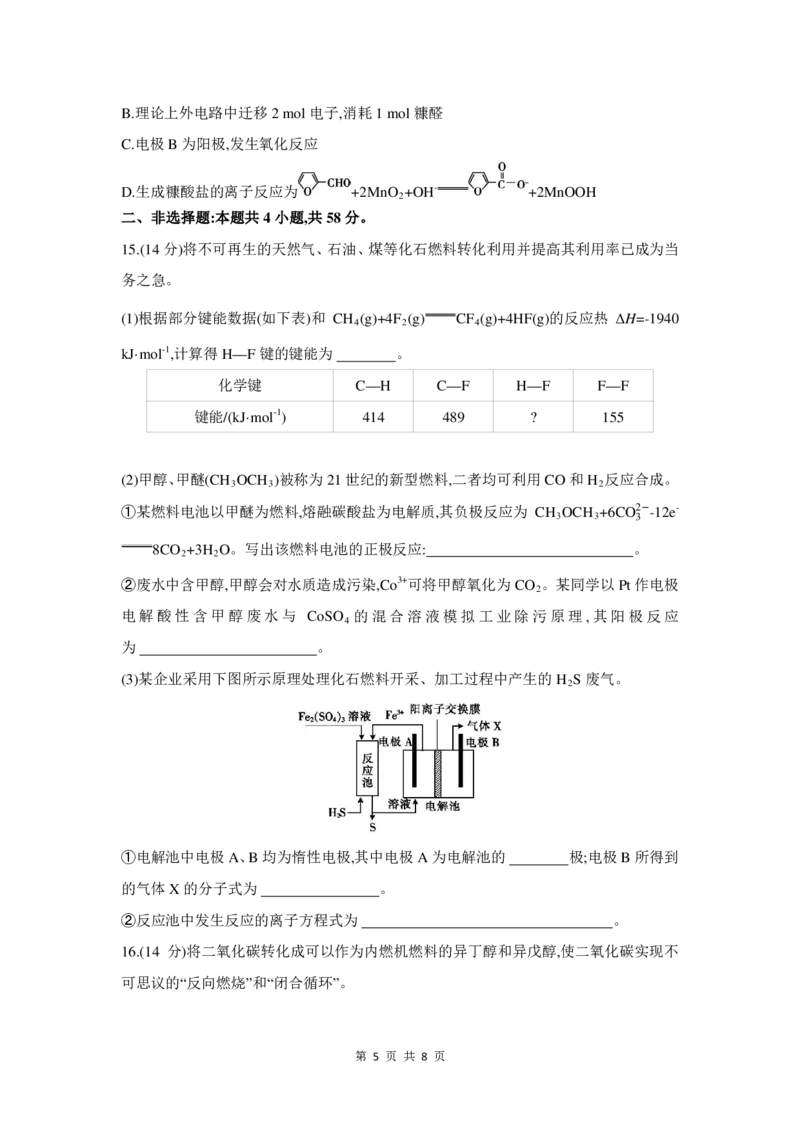
14.工业上用双极膜电解槽电解糠醛溶液同时制备糠醇和糠酸盐,电解过程如图所示。下
列说法错
.
误
.
的是
A.电解时,阴极反应为 +2e-+2H+
第 4 页 共 8 页
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}B.理论上外电路中迁移2 mol电子,消耗1 mol糠醛
C.电极B为阳极,发生氧化反应
D.生成糠酸盐的离子反应为 +2MnO +OH- +2MnOOH
2
二、非选择题:本题共4小题,共58分。
15.(14分)将不可再生的天然气、石油、煤等化石燃料转化利用并提高其利用率已成为当
务之急。
(1)根据部分键能数据(如下表)和 CH (g)+4F (g) CF (g)+4HF(g)的反应热 ΔH=-1940
4 2 4
kJ·mol-1,计算得H—F键的键能为 。
化学键 C—H C—F H—F F—F
键能/(kJ·mol-1) 414 489 ? 155
(2)甲醇、甲醚(CH OCH )被称为21世纪的新型燃料,二者均可利用CO和H 反应合成。
3 3 2
①某燃料电池以甲醚为燃料,熔融碳酸盐为电解质,其负极反应为 CH OCH +6CO2 -12e-
3 3 3
−
8CO +3H O。写出该燃料电池的正极反应: 。
2 2
②废水中含甲醇,甲醇会对水质造成污染,Co3+可将甲醇氧化为CO 。某同学以Pt作电极
2
电解酸性含甲醇废水与 CoSO 的混合溶液模拟工业除污原理,其阳极反应
4
为 。
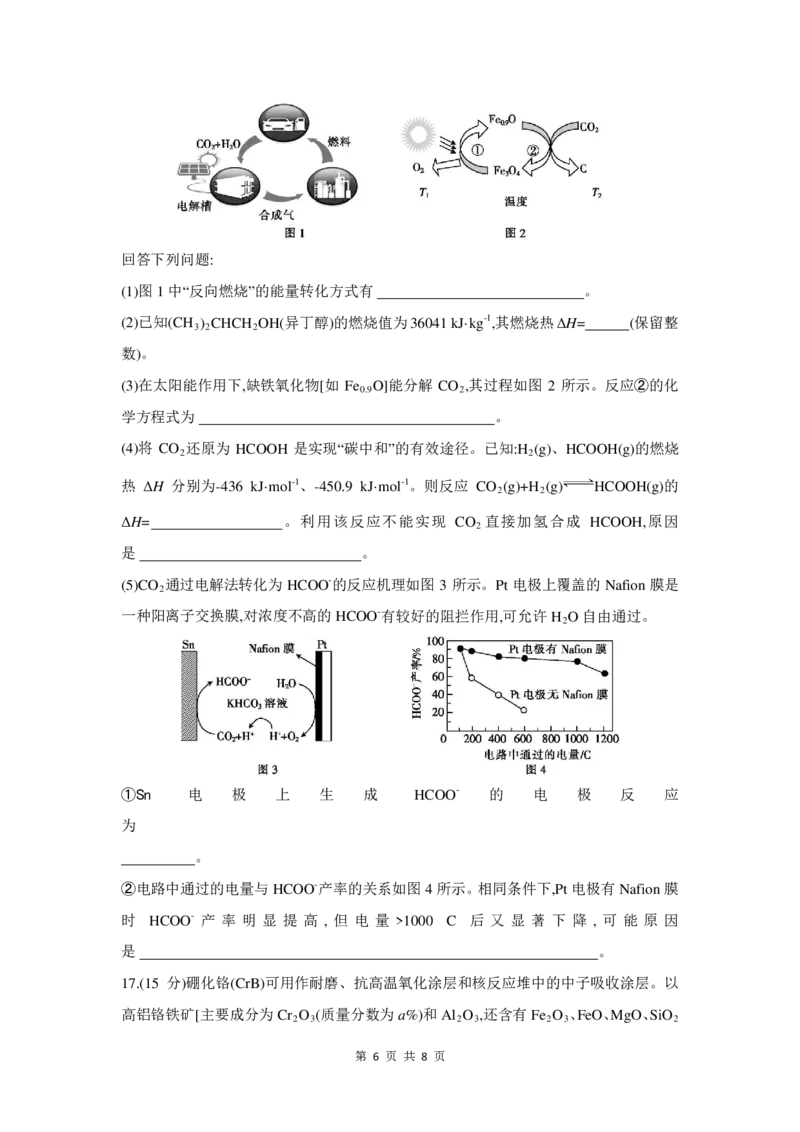
(3)某企业采用下图所示原理处理化石燃料开采、加工过程中产生的H S废气。
2
①电解池中电极A、B均为惰性电极,其中电极A为电解池的 极;电极B所得到
的气体X的分子式为 。
②反应池中发生反应的离子方程式为 。
16.(14 分)将二氧化碳转化成可以作为内燃机燃料的异丁醇和异戊醇,使二氧化碳实现不
可思议的“反向燃烧”和“闭合循环”。
第 5 页 共 8 页
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}回答下列问题:
(1)图1中“反向燃烧”的能量转化方式有 。
(2)已知(CH ) CHCH OH(异丁醇)的燃烧值为36041 kJ·kg-1,其燃烧热ΔH= (保留整
3 2 2
数)。
(3)在太阳能作用下,缺铁氧化物[如 Fe O]能分解 CO ,其过程如图 2 所示。反应②的化
0.9 2
学方程式为 。
(4)将 CO 还原为 HCOOH 是实现“碳中和”的有效途径。已知:H (g)、HCOOH(g)的燃烧
2 2
热 ΔH 分别为-436 kJ·mol-1、-450.9 kJ·mol-1。则反应 CO (g)+H (g) HCOOH(g)的
2 2
ΔH= 。利用该反应不能实现 CO 直接加氢合成 HCOOH,原因
2
是 。
(5)CO 通过电解法转化为 HCOO-的反应机理如图 3 所示。Pt 电极上覆盖的 Nafion 膜是
2
一种阳离子交换膜,对浓度不高的HCOO-有较好的阻拦作用,可允许H O自由通过。
2
①Sn 电 极 上 生 成 HCOO- 的 电 极 反 应
为
。
②电路中通过的电量与HCOO-产率的关系如图4所示。相同条件下,Pt电极有Nafion膜
时 HCOO- 产 率 明 显 提 高, 但 电 量>1000 C 后 又 显 著 下 降 , 可 能 原 因
是 。
17.(15 分)硼化铬(CrB)可用作耐磨、抗高温氧化涂层和核反应堆中的中子吸收涂层。以
高铝铬铁矿[主要成分为Cr O (质量分数为a%)和Al O ,还含有Fe O 、FeO、MgO、SiO
2 3 2 3 2 3 2
第 6 页 共 8 页
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}等]为原料制备硼化铬和铝的工艺流程如图所示。
金属离子 Fe3+ Mg2+ Cr3+ Fe2+ Al3+
开始沉淀的pH 2.3 10.4 4.9 7.5 3.4
沉淀完全的pH 4.1 12.4 6.8 9.7 4.7
回答下列问题:
(1)“氧化”的目的是将溶液中的Fe2+转化为Fe3+,试剂X可选用H O 或Cl ,写出X为H O
2 2 2 2 2
时的离子方程式: 。
(2)试剂Y是 ,操作1的名称是 。
(3)向溶液M中通入过量CO ,发生反应的离子方程式为 。
2
(4)第 2 次加氨水“调节 pH”的范围是 ;加稀盐酸中和前,需要洗涤沉淀,
证明沉淀洗涤干净的操作是 。
(5)硼化铬是由金属镁、硼、氯化铬在 650 ℃时反应制得的,写出该反应的化学方程
式: 。
(6)硼化铬晶胞结构如图所示,已知晶胞边长为a pm,阿伏加德罗常数的值为N ,硼化铬晶
A
体的密度是 g·cm-3。
18.(15 分)反应 CO(g)+H O(g) CO (g)+H (g)常应用于制备合成氨工业原料气。缺点
2 2 2
是能耗较大,副产物增加了温室气体的排放量。以下是一种利用电化学原理合成原料气
并充分利用副产物的联合制备设想。
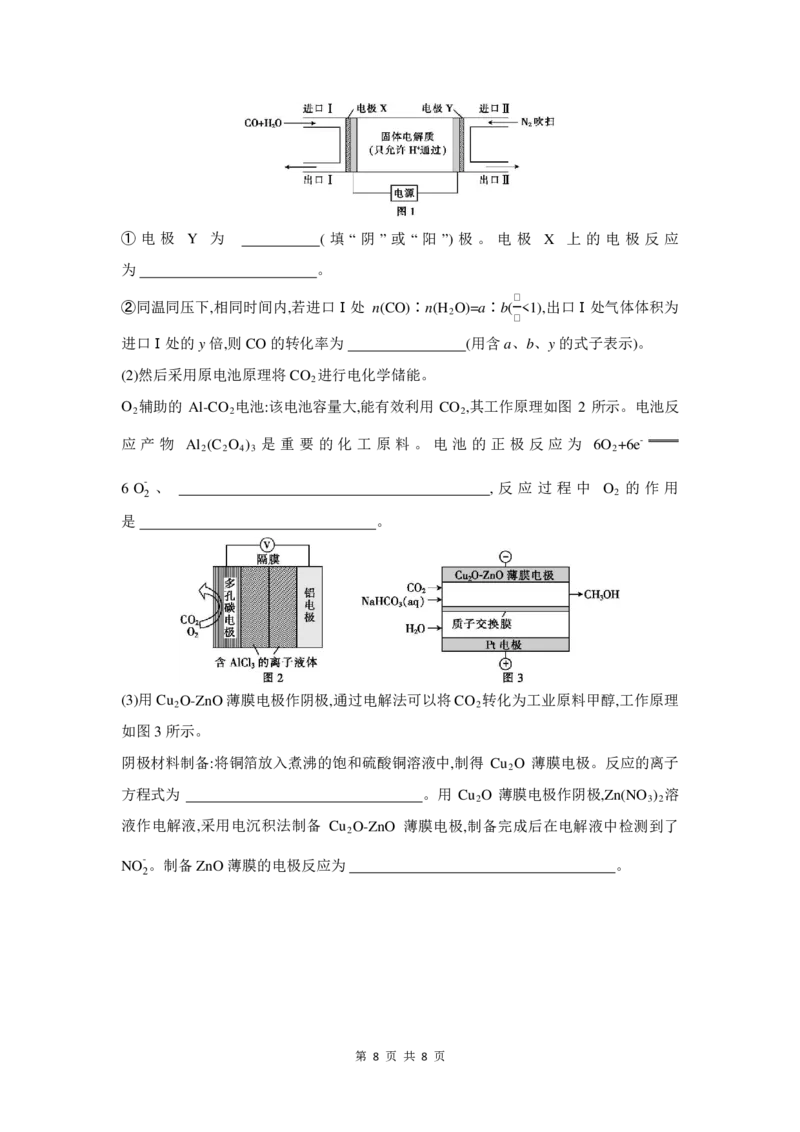
(1)首先采用电解的方法合成氨工业原料气,反应装置如图1所示。
第 7 页 共 8 页
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}① 电 极 Y 为 ( 填 “ 阴 ” 或 “ 阳 ”) 极 。 电 极 X 上 的 电 极 反 应
为 。
�
②同温同压下,相同时间内,若进口Ⅰ处 n(CO)∶n(H O)=a∶b( <1),出口Ⅰ处气体体积为
2
�
进口Ⅰ处的y倍,则CO的转化率为 (用含a、b、y的式子表示)。
(2)然后采用原电池原理将CO 进行电化学储能。
2
O 辅助的 Al-CO 电池:该电池容量大,能有效利用 CO ,其工作原理如图 2 所示。电池反
2 2 2
应 产 物 Al (C O ) 是 重 要 的 化 工 原 料 。 电 池 的 正 极 反 应 为 6O +6e-
2 2 4 3 2
6 O - 、 , 反 应 过 程 中 O 的 作 用
2 2
是 。
(3)用Cu O-ZnO薄膜电极作阴极,通过电解法可以将CO 转化为工业原料甲醇,工作原理
2 2
如图3所示。
阴极材料制备:将铜箔放入煮沸的饱和硫酸铜溶液中,制得 Cu O 薄膜电极。反应的离子
2
方程式为 。用 Cu O 薄膜电极作阴极,Zn(NO ) 溶
2 3 2
液作电解液,采用电沉积法制备 Cu O-ZnO 薄膜电极,制备完成后在电解液中检测到了
2
NO -。制备ZnO薄膜的电极反应为 。
2
第 8 页 共 8 页
{#{QQABDQWo4wgYkMZACS6aQUWQCAiYsJOTLKgGhVCSqAZCAQFIBCA=}#}