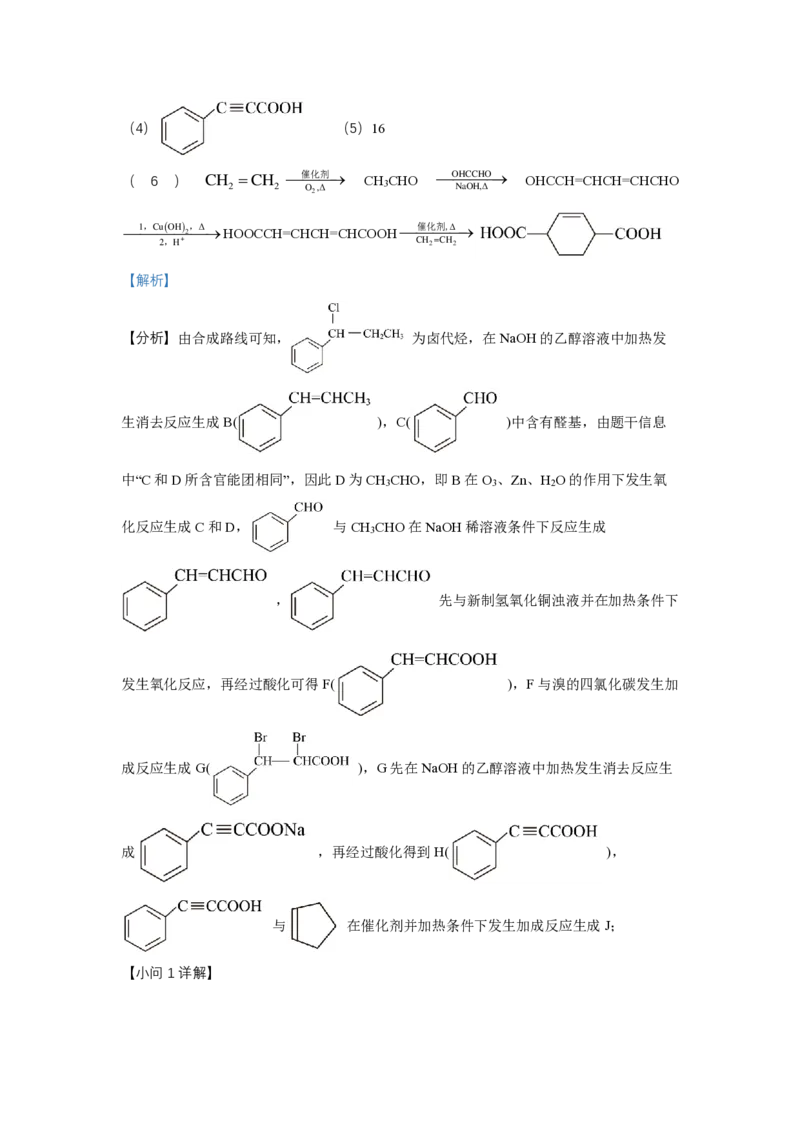
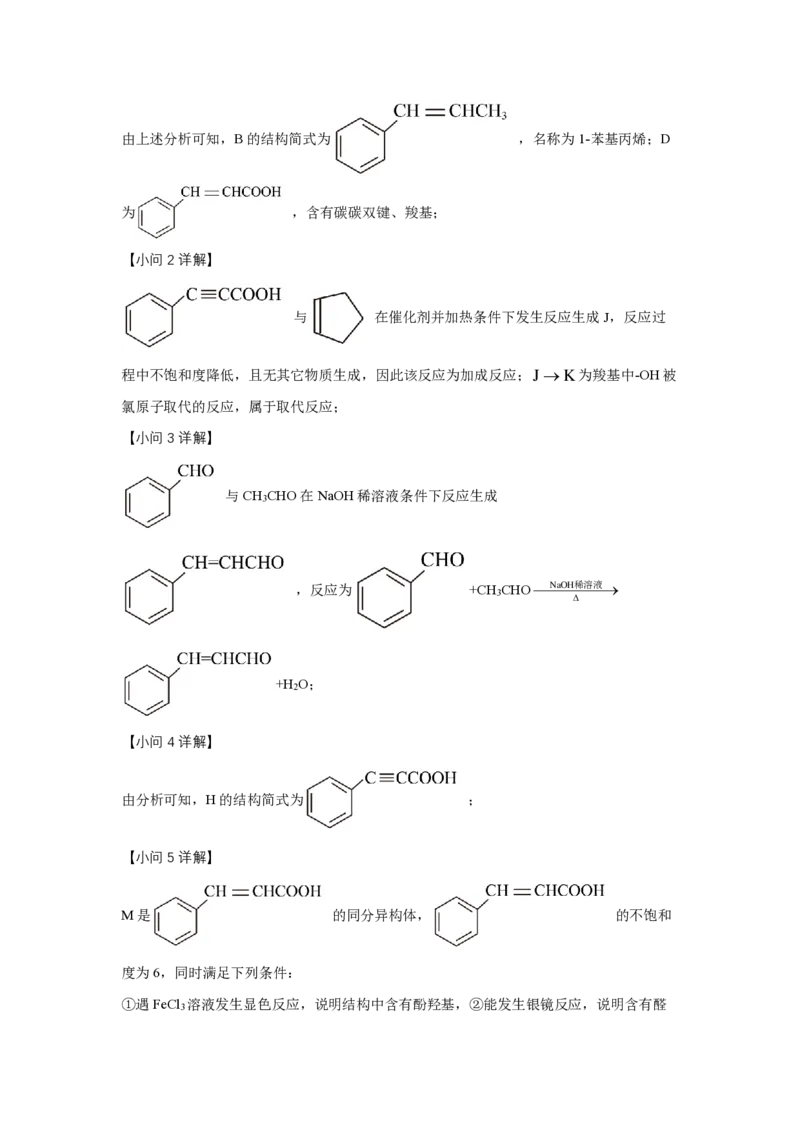
文档内容
衡阳市八中 2024 届高三暑假检测答案
1.B【解析】油脂不是高分子。
2.D【解析】淀粉的分子式为 ( C
6
H
1 0
O
5
)
n
,A错误.铍原子最外层电子在 s 轨道上,电子
云轮廓图为球形,B错误.基态 F e 2 + 的价电子排布式为 3 d 6 ,故对应的价电子排布图应在
3 d 轨道上排6个电子,C错误.
3.B 【解析】 A g N O
3
溶液中滴加过量氨水,最终生成 A g ( N H
3
)
2
+ ,A错误.用过
量氨水吸收 S O
2
,由于氨水过量,得到 N H +4 和 S O 23 − ,无法得到 H S O −3 ,C错误. H
2
S
为弱酸,离子方程式中不可拆写为 S 2 − ,D错误.
4.D 【解析】 H
2
O 分子稳定性与共价键强弱有关,与分子间氢键无关,A错
误. N H
2
O H 的水溶液显碱性与 N H
3
类似,NH OH+H O NH OH+ +OH−,
2 2 3
并非自身电离出 O H − ,B错误. N H
2
O H 与 N H +4 中 N 均为 s p 3 杂化,中心 N 原子价层电
子对数为4, N H +4 中H−N−H键角为10928,但 N H
2
O H
题 1 2 3 4 5 6 7 8 9 10 11 12 13 14
号
答 B D B D D D B C A D B B C A
案
中存在孤电子对,
H−N−H键角小于10928,C错误,D正确.
5.D【解析】反应①②③均断裂化学键吸收热量,ΔH 0,A项正确;催化剂具有一定的
选择性,使用恰当的催化剂,可调控反应进行的程度甚至停止,B项正确;根据A的稳定性
大于B,物质越稳定所含能量越低,所以得到等质量的A和B时,生成B消耗的能量更多,
C项正确;日光直射可能会爆炸,D项错误。
6. D【解析】A.进行实验前必须进行的操作检验装置的气密性,一旦漏气实验失败,故A
正确;B.氧气和硫化氢反应生成硫,H中出现浅黄色浑浊,可证明O非金属性强于S,故
B正确;C.Cu(NH ) 2+ 中存在N-H极性共价键和配位键,NH 中N原子价层电子对
3 4 3
1
数为3+ (5−31) =4,N原子的杂化类型为sp3杂化,故C正确;D.装置B与D中比
2
较,D中形成原电池后可以加快反应速率,则若硫酸浓度及锌片大小表面积等均相同,则
B中产生氢气速率小于D中速率,故D错误;
7.【答案】B
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}【解析】
【详解】A.与苯环直接相连的原子共面,醛基中原子共面,故A中所有原子可能共平
面,A正确
B.A发生氧化反应使高锰酸钾溶液褪色,和溴水发生取代反应使其褪色;B发生氧化反应
使高锰酸钾溶液褪色,和溴水发生加成应、氧化反应使其褪色;C发生氧化反应使高锰酸
钾溶液褪色,和溴水发生加成应、取代反应、氧化反应使其褪色;反应原理不相同,B错
误;
C.B含有醛基、醚键、碳碳双键,C含有醛基、酚羟基、碳碳双键;官能团数目相同,C
正确;
D.有机物A的同分异构体中含有苯环且能发生银镜反应的还有醛基羟基处于邻、间位,
以及甲酸苯酚酯三种(不包含A),D正确;
8. 【答案】C
【解析】
【分析】X、Y、Z、W为核电荷数依次增大的前20号主族元素,且位于不同的周期,则它
们分别为第一、二、三和四周期,而W可形成一价阳离子,为K元素,根据结构图,可推
出X、Y、Z分别是H、O、P元素。
【详解】A.该化合物含有K元素,焰色反应是紫色,A错误;
B.非金属性O>N>P,故PH 的热稳定性比H O的要差,B错误;
3 2
C.O元素与其它三种元素可形成:H O、H O ;K O 、KO ;P O 、P O 至少两种二元
2 2 2 2 2 2 2 5 4 10
化合物,C正确;
D.KH PO 溶液中,H PO -既能电离也能水解,H PO - HPO 2-+H+,H PO -+H O
2 4 2 4 2 4 4 2 4 2
H PO +OH-,溶液显酸性,电离程度大于水解程度,故c(HPO 2-)>c(H PO ),故D错误。
3 4 4 3 4
故选C。
9. 【答案】A
【解析】
【详解】A.二氧化硫、硫化钠、碳酸钠反应生成Na S O 同时生成二氧化碳,反应为
2 2 3
4 S O
2
+ 2 S 2 − + C O 23 − = 3 S
2
O 23 − + C O
2
,A正确;
B.硫代硫酸钠和稀盐酸反应生成硫单质沉淀、二氧化硫和氯化钠,取少量样品溶于水,
先加入过量稀盐酸,再滴加BaCl 溶液,有沉淀生成,不能证明样品含有硫酸钠,B错
2
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}误;
C.探究温度对硫代硫酸钠与硫酸反应速率的影响,应该首先加热至反应要求温度,然后
再将两种反应溶液混合,反应的离子方程式为S O2-+2H+=S↓+SO ↑+H O,C错误;
2 3 2 2
D.少量氯气和过量硫代硫酸钠反应生成硫酸根离子、氯离子、硫单质、二氧化硫气体,
反应为 6 S
2
O 23 - + 4 C l
2
= 2 S O 24 - + 8 C l - + 5 S + 5 S O
2
,D错误;
故选A。
10. 【答案】D
【解析】
【详解】A.基态碳原子核外电子排布为1s22s22p2,核外存在2对自旋相反的电子,A错
误
B. C S
2
分子中C价层电子对数为 2 +
4 - 2
2
2
= 2 ,则中心原子为sp杂化,B错误;
C.一定条件下 C O 能与金属 F e 形成 F e ( C O )
5
,该化合物的熔点为253K,沸点为
3 7 6 K ,其晶体熔沸点较低,类型属于分子晶体,C错误;
D.SiC的晶体结构与晶体硅相似,为共价晶体,则 S i C 晶体中微粒间存在的作用力是共
价键,D正确;
故选D。
11. 【答案】B
【解析】
【详解】A.由题干可知,H T为二元弱酸,在水溶液中的电离方程式为:
2
H
2
T H + + H T - 、HT- H++T2-,A错误;
10−14
B.常温下,HT-的水解常数为K = =1.110−11 K =4.310−6,则
h K 2
1
0.01mol/L NaHT水溶液中电离大于水解,溶液显酸性,往0.01mol/L NaHT水溶液中
继续加水稀释,溶液中氢离子浓度减小,溶液的 p H 逐渐增大,B正确;
C. 0 .0 1 m o l / L N a
2
T 水溶液中由质子守恒可知:
c ( OH−) =c ( H+) +c ( HT−) +2c(H T) ,C错误;
2
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}D.由题干提供电离常数可知, H
2
C
2
O
4
与过量的 N a
2
T 水溶液反应生成草酸根离子和
H T - ,离子方程式:H C O +2T2− =C O2- +2HT−,D错误;
2 2 4 2 4
故选B。
12. 【答案】B
【解析】
【分析】由图可知,放电时,镁失去电子发生氧化反应生成镁离子,故Mg电极为负极,则
FeS为正极;
【详解】A.由分析可知, M g 电极为负极,A正确;
B.镁、FeS均会和硫酸反应,故不能加硫酸,B错误;
C.充电时,FeS为阳极,铁发生氧化反应生成FeS,阳极电极反应式为
F e + L i
2
S − 2 e − = F e S + 2 L i + ,C正确;
D.充电时,阳极电极反应式为 F e + L i
2
S − 2 e − = F e S + 2 L i + ,阴极反应为
M g 2 + + 2 e − = M g ,则每转移 1 m o l 电子,生成1mol锂离子、消耗0.5mol镁离子,电解质
溶液质量减少12g-7g= 5 g ,D正确;
故选B。
13. 【答案】C
【解析】
详解】A.Ⅰ、CH (g)+H O(g)=CO(g)+3H (g) ΔH=+206.2kJmol−1,Ⅱ、
4 2 2
C H
4
( g ) + 2 H
2
O ( g ) = C O
2
( g ) + 4 H
2
( g ) Δ H = + 1 6 5 k J m o l − 1 ,根据盖斯定律,由Ⅰ2-
Ⅱ得到 C H
4
( g ) + C O
2
( g ) = 2 C O ( g ) + 2 H
2
( g ) Δ H = + 2 4 7 .4 k J m o l − 1 ,选项A正确;
B.过程Ⅱ的反应第一步是CO+CO +H +Fe O +CaO→H O+Fe+CaCO ,第二步反应:
2 2 3 4 2 3
Fe+CaCO +稀有气体→稀有气体+Fe+CaCO +CO,两步反应实现了含碳物质与含氢物质的
3 3
分离,选项B正确;
C.过程Ⅱ中Fe O、CaO为催化剂,改变反应速率不能改变反应的
3 4
H
【
,选项C不正
确;
D.根据流程中物质的参与和生成情况,结合反应过程中有催化剂和中间产物,总反应可
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}表示为 C H
4
+ 3 C O
2
= 4 C O + 2 H
2
O ,选项D正确;
答案选C。
14. 【答案】A
【解析】
【分析】海绵铜加入硫酸和硝酸铵溶解得到的溶液主要是硫酸铜,硫酸铵等,加入亚硫酸
铵还原硫酸铜、在氯化铵环境中发生反应生成氯化亚铜沉淀、硫酸铵和硫酸,过滤得到氯
化亚铜沉淀、用稀硫酸洗涤,最终得到氯化亚铜;
【详解】A.空气中氧气具有氧化性,酸性条件下也能将铜氧化为铜离子,故“溶解”时,
通入空气可以减少大气污染,A正确;
B. “还原”时,铜离子、亚硫酸根离子、氯离子反应生成氯化亚铜沉淀、硫酸根离子,反
应的离子方程式为: 2 C u 2 + + S O 23 − + H
2
O + 2 C l - = 2 C u C l + S O 24 − + 2 H + ,B错误;
C. “过滤”时,玻璃棒搅拌液体有可能捣破滤纸,故过滤时不可以搅拌,C错误;
D.氯化亚铜微溶于水,不溶于稀酸,可溶于Cl-浓度较大的体系,在潮湿空气中易水解氧
化,则 “酸洗”时不能用盐酸、不能用硝酸(防止被氧化),最适宜选用的是稀硫酸,还可
循环利用,D错误;
故选A。
15. 【答案】(1)分水器中液体不分层
(2)趁热过滤,洗涤,干燥
(3)CCl 密度比水大,会在分水器的下层,水在上层
4
(4)96% (5) ①. S O 23 - + 2 H + = H
2
O + S O
2
a ②. 淀粉溶液 ③. 0.1344
【解析】
【分析】通过蒸馏得到无水醋酸铅,再利用滴定法测定其溶液中含有的亚硫酸盐的含量。
【小问1详解】
互不相溶的水和甲苯在加热过程中形成共沸物进入分水器,水的密度比甲苯大,在分水器
的下层,甲苯在.上层,打开分水器下部的活塞可将水从下部接收,当分水器中液体不分层
时,则脱水完成,可以停止加热;
【小问2详解】
停止加热,烧瓶底部由大量白色醋酸铅粉末状固体析出,进一步得到醋酸铅的操作为:趁
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}热过滤,洗涤,干燥;
【小问3详解】
用CCl 不行, 因为CCl 密度比水大,会在分水器的下层,水在上层,导致液体超过分水
4 4
器支管口后水又重新流入二颈瓶中,达不到脱水的目的;答案为CCl 密度比水大,会在分
4
水器的下层,水在上层;
【小问4详解】
根据反应可得关系式:
( C H
3
C O
3
O
3
7
) P
7 9
. 9 g
b 3 H
2
O ~ ( C H
3
C
3
O
2
x g
5
O ) P b
列比例式可得出,x=32. 5,故醋酸铅的产率=
3
3
1
2
. 2
. 5
g
g
?
100%=96%;
【小问5详解】
a.辣椒粉样品酸化时发生的离子方程式为 S O 23 - + 2 H + = H
2
O + S O
2
;
b.滴定的原理为SO +I +2H+=H SO +2HI,选用淀粉做指示剂,当滴入最后半滴,锥形瓶的
2 2 2 4
溶液中出现蓝色,且半分钏不褪色,即达到滴定终点,操作中选择的指示剂为淀粉溶液;
c.根据滴定原理消耗2.10mL0.01mol/L的I 溶液,则辣椒粉中残留亚硫酸盐的含量为
2
0.012.1010−364
=0.1334
1010−3
g / k g 。
16.【答案】(1)NH (氨水或液氨)
3
(2)6NH +H SiF +2H O=6NH F+SiO ,
3 2 6 2 4 2
(3)5AsF +10HF +6H++2MnO−=2Mn2++5 A F +8H O
3 4 S 5 2
(4)当HF浓度大于5.0mol/L时,HF与F-形成氢键,形成 H F −2 ,促进了HF的电离;
4M
(5) ①. 8 ②.
g/cm3
N a3
A
【解析】
【分析】该题涉及到两个工艺流程过程,在第一个中.以氟硅酸(H SiF )制备氟化钙,在第二
2 6
个中用氟化钙与浓硫酸反应可以制取HF,同时本题还考查了晶胞的相关计算以及价层电子
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}对互斥理论。
【小问1详解】
从工艺流程分析在化学预处理NH 和H SiF 反应制得NH F,利用制得的NH F和石灰石
3 2 6 4 4
反应制得HF和NH ,因此可以循环利用的物质是NH (氨水或液氨);
3 3
【小问2详解】
据I的工艺流程分析,通过化学预处理中NH 和H SiF 反应制得NH F,因此聚四氟乙烯
3 2 6 4
反应釜中发生反应的化学方程式为:6NH +H SiF +2H O=6NH F+SiO ;
3 2 6 2 4 2
【小问3详解】
精制HF过程中,用高锰酸钾溶液进行化学预处理,将AsF 氧化,氧化得到的物质AsF ,
3 5
其化学处理的离子方程式为:5AsF +10HF +6H++2
3
M n O −4 =2Mn2++5 A F +8H O;
S 5 2
【小问4详解】
当HF浓度大于5.0mol/L时,溶液的酸性变强,可能的原因是:当HF浓度大于5.0mol/L
时,会发生自偶电离,HF与F-形成氢键,形成HF−,促进了HF的电离;
2
【小问5详解】
根据氟化钙的晶胞所示,每个钙离子周围最近的F-为8个,因此钙离子的配位数为8;根
m
据均摊法可以算出一个晶胞含有4个CaF ,当晶胞参数为acm,则该晶体的密度= =
2
V
N
4 M
A
a 3
g / c m 3
17. 【答案】(1)平面三角形
(2) ①. acd ②. 0.005 ③. 1.85×10-6Pa-1 ④. 移走0.25molCO ⑤. 不变
(3) ①. 阴 ②. CO +H O+2e-=CO+2OH-
2 2
【解析】
【小问1详解】
COCl 的中心原子价层电子对数为
2
1
2
( 4 − 2 1 − 1 2 ) + 3 = 3 ,则其 VSEPR模型为平面三
角形,答案:平面三角形;
【小问2详解】
①a.根据“变量不变”的思想,在恒温恒容条件下,随着反应的进行,气体物质的量减小,
压强不断减小,容器内压强不再改变 ,反应达平衡,a正确;
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}b. v ( C O ) = v ( C O C l
2
) ,无法判断正逆反应速率是否相等,无法判断反应是否达平衡,b
正确;
c.气体颜色不再改变,说明c(Cl )不再改变,反应达平衡,c正确;
2
d.容器内气体的平均摩尔质量 M =
m
n
,,在恒温恒容条件下,随着反应的进行,气体物
质的量减小,气体的平均摩尔质量增大,当容器内气体的平均摩尔质量不再改变,反应达
平衡,d正确;
答案为acd。
②用 CO 表示的该反应在 0~6 min 内的化学反应速率 v ( C O ) =
( 0 .1 2 - 0
6
.0
m
9 )
i n
m o l L
= 0 .0 0 5
m o l L − 1 m i n − 1 ,答案:0.005;
③由信息可知,达到平衡后,气体CO:0.09mol∙L-1×5L=0.45mol,COCl :0.03 mol∙L-
2
1×5L=0.15mol,Cl :0.45mol-0.15mol=0.3mol,容器的总压为:
2
p ( 总 ) = 6 .3 1 0 5 P a
0 . 4 5
0
+
.6
0
+
. 1
0
5
.4
+
5
0 . 3
= 5 .4 1 0 5 P a ,各物质分压分别为
p ( C O C l
2
) = 5 .4 1 0 5 P a
0
0
.1 5
.9
= 9 1 0 4 P a , p ( C O ) = 2 . 7 1 0 5 P a ,
p ( C l
2
) = 1 .8 1 0 5 P a ,
K p =
p (
p
C
(
O
C O
)
C
p
l
(
2
C
)
l
2
)
=
2 .7 1 0
9
5
P
1
a
0
4
1
P
.8
a
1 0 5 P a
= 1 . 8 5 1 0 − 6 P a − 1 ,第8分钟,在改变条件
的瞬间,c(CO)浓度减小,而c(COCl )不变,平衡向左移动,故改变的条件是移走0.25
2
molCO,温度没变,K不变。答案分别为:1.85×10-6Pa-1,移走0.25 molCO,不变;
【小问3详解】
电极 2 与电源 负极相连,为阴极,其电极反应式 CO +H O+2e-=CO+2OH-,答案:
2 2
CO +H O+2e-=CO+2OH-。
2 2
18. 【答案】(1) ①. 1-苯基丙烯 ②. 碳碳双键、羧基
(2) 取代反应
(3) +CH CHO
3
⎯ N⎯ a O H⎯ 稀Δ 溶⎯ 液 ⎯→
的
+H O
2
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}(4) (5)16
( 6 ) C H
2
= C H
2
⎯ 催⎯O 化
2
剂⎯,Δ → CH CHO
3
⎯ O H C C ⎯ ⎯
N a O H
H O⎯
,Δ
→ OHCCH=CHCH=CHCHO
⎯ , 1⎯ C u⎯2 (O
,
H⎯H ) ,⎯ 2
+
Δ → HOOCCH=CHCH=CHCOOH ⎯ 催⎯C
H
化
2
剂⎯=
C
, ⎯
H 2
→
【解析】
【分析】由合成路线可知, 为卤代烃,在NaOH的乙醇溶液中加热发
生消去反应生成B( ),C( )中含有醛基,由题干信息
中“C和D所含官能团相同”,因此D为CH CHO,即B在O 、Zn、H O的作用下发生氧
3 3 2
化反应生成C和D, 与CH CHO在NaOH稀溶液条件下反应生成
3
, 先与新制氢氧化铜浊液并在加热条件下
发生氧化反应,再经过酸化可得F( ),F与溴的四氯化碳发生加
成反应生成G( ),G先在NaOH的乙醇溶液中加热发生消去反应生
成 ,再经过酸化得到H( ),
与 在催化剂并加热条件下发生加成反应生成J;
【小问1详解】
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}由上述分析可知,B的结构简式为 ,名称为1-苯基丙烯;D
为 ,含有碳碳双键、羧基;
【小问2详解】
与 在催化剂并加热条件下发生反应生成J,反应过
程中不饱和度降低,且无其它物质生成,因此该反应为加成反应; J → K 为羧基中-OH被
氯原子取代的反应,属于取代反应;
【小问3详解】
与CH CHO在NaOH稀溶液条件下反应生成
3
,反应为 +CH CHO
3
⎯ N⎯ a O H⎯ 稀Δ 溶⎯ 液 ⎯→
+H O;
2
【小问4详解】
由分析可知,H的结构简式为 ;
【小问5详解】
M是 的同分异构体, 的不饱和
度为6,同时满足下列条件:
①遇FeCl 溶液发生显色反应,说明结构中含有酚羟基,②能发生银镜反应,说明含有醛
3
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}基,③除苯环外不含其他环,由不饱和度可知,该结构中还含有1个碳碳双键,若苯环上
有3个取代基,−CH=CH 、—CHO、—OH,有10种结构;若苯环上有2个取代基,则分
2
别为—OH、−CH=CHCHO或—OH、−C(CHO)=CH ,共有6种结构,符合条件的结构有
2
16种;
【小问6详解】
乙烯首先催化氧化为乙醛,和 O H C C H O 生成 OHCCH=CHCH=CHCHO,然后和新制氢氧
化铜发生反应后酸化得到 HOOCCH=CHCH=CHCOOH,再和乙烯发生加成反应生成
,故流程为:
C H
2
= C H
2
⎯催⎯化⎯剂→ ⎯O⎯HC⎯CHO⎯→
O 2 ,Δ CH 3 CHO NaOH,Δ
OHCCH=CHCH=CHCHO
⎯ , 1⎯ C u⎯2 (O
,
H⎯H ) ,⎯ 2
+
Δ →
HOOCCH=CHCH=CHCOOH
⎯ 催⎯C
H
化
2
剂⎯=
C
, ⎯
H 2
→
。
{#{QQABZYYEggCAAAAAARhCEQEiCkMQkBGAAKgOhEAIMAAByQFABAA=}#}