文档内容
第二章 烃
第二节 烯烃 炔烃
第2课时 炔烃
一、单选题
1.(2019·上海浦东新区·高二学业考试)关于乙炔的说法中,错误的是
A.属于不饱和烃 B.是直线型分子
C.能发生加聚反应 D.密度比空气大
【答案】D
【解析】
【详解】
A.乙炔分子中含有碳碳叁键,是不饱和烃,故A正确;
B.乙炔分子中碳原子是sp杂化,其分子构型为直线型,故B正确;
C.乙炔能发生加聚反应,生成聚乙炔,结构简式为 ,故C正确;
D.乙炔分子的相对分子质量是26,密度比空气小,故D错误;
故答案为D。
2.(2021·上海浦东新区·高三一模)下列有关实验设计合理的是
A B C D
验证浓硫酸稀释放
验证氧化性:Cl>Br 纸层析法分离Cu2+与Fe3+ 实验室制乙炔
热 2 2
A.A B.B C.C D.D
【答案】B
【详解】
A.验证浓硫酸稀释放热时,应将浓硫酸滴入水中,A不正确;
B.氯水滴入NaBr溶液中,发生反应Cl+2NaBr=2NaCl+Br ,从而得出氧化性Cl>Br ,B正确;
2 2 2 2C.纸层析法分离Cu2+与Fe3+时,滤纸条上的试液点滴应位于展开剂液面的上方,C不正确;
D.电石遇水易转化为粉末,从塑料板小孔漏到试管底部,起不到控制反应随时发生、随时停止的作用,
D不正确;
故选B。
3.(2020·沙坪坝区·重庆八中高二期中)下列关于实验室制取乙烯和乙炔的装置说法正确的是(夹持仪器
未画出)
A.①装置完全正确
B.①装置中浓硫酸的作用是作催化剂和吸水剂
C.②装置制备乙炔的反应方程式为:CaC +2H O→Ca(OH) +C H↑
2 2 2 2 2
D.②装置中酸性KMnO 溶液褪色,说明乙炔具有还原性
4
【答案】C
【详解】
A.装置①为实验室制乙烯装置,需将反应液迅速升温到170℃,故温度计应插入液面以下,A错误;
B.在乙醇消去制乙烯中,浓硫酸起催化剂和脱水剂作用,B错误;
C.电石CaC 和水反应方程式为:CaC +2H O→Ca(OH) +C H↑,C正确;
2 2 2 2 2 2
D.电石中常含有CaS等杂质,CaS与水反应生成HS气体也能使酸性KMnO 溶液褪色,即此时KMnO
2 4 4
溶液褪色不一定是因为C H,D错误;正确操作应该将气体先通过盛有FeCl 溶液或CuSO 溶液的洗气装
2 2 3 4
置,再通入KMnO 溶液;
4
故答案选C。
4.(2019·上海市复兴高级中学高二期末)下列分子中所有原子在同一平面上的是( )
A.CHCHCHCH B.CHCH=CHCH
3 2 2 3 3 3
C.CHC≡CCH D.CH=CHC≡CH
3 3 2
【答案】D
【详解】A.CHCHCHCH 中含有-CH,呈四面体结构,则所有原子不可能都处于同一平面,故A不符合题意;
3 2 2 3 3
B.CHCH=CHCH 含有-CH,呈四面体结构,则所有原子不可能都处于同一平面,故B不符合题意;
3 3 3
C.CHC≡CCH 含有-CH,呈四面体结构,则所有原子不可能都处于同一平面,故C不符合题意;
3 3 3
D.乙烯是平面结构,乙炔是直线型分子,CH=CHC≡CH中所有的原子处于同一平面,故D符合题意;
2
答案为D。
5.(2014·湖南岳阳市·高二期末)下列关于有机物结构的叙述正确的是( )
A.CH=CH 与 均含有碳碳双键,两者互为同系物
2 2
B.H-C≡C-H分子中所有原子一定处在同一条直线上
C. -Cl与 CH-CH 均属于平面形分子
2 2
D.烯烃、炔烃中都可能存在顺反异构
【答案】B
【详解】
A.结构相似,类别相同,在分子组成上相差一个或多个“-CH-”原子团的有机物互称同系物,CH=CH
2 2 2
与 结构不相似,两者不互为同系物,故A错误;
B.H-C≡C-H为乙炔分子的结构简式,乙炔为直线形分子,所有原子一定处在同一条直线上,故B正确;
C.苯为平面结构, —Cl可看做苯上的一个氢原子被氯原子取代的产物,与苯的结构相似,为平面形
分子;聚乙烯 CH—CH 中所有的碳原子均以单键相连,类似与甲烷的空间构型,不是平面形分子,故
2 2
C错误;
D.烯烃中碳碳双键上同一碳上可能连接不同的基团可能存在顺反异构,炔烃中不可能形成顺反异构,故
D错误;
答案选B。
6.(2011·重庆万州区·高二期中)下列说法中正确的是
A.乙炔有特殊难闻的气味
B.乙烯和乙炔都能使溴水褪色,但与乙炔反应时消耗的溴要比等物质的量的乙烯反应消耗的多
C.乙炔可用电石与水反应而制得,故实验室最好选用启普发生器为气体的发生装置D.乙炔含碳量比乙烯含碳量高,等物质的量的乙炔和乙烯燃烧时,乙炔所耗氧气多
【答案】B
【解析】
【分析】
A.乙炔是无色无味的气体,因含有硫化氢、磷化氢而导致有特殊气味;
B. 1mol碳碳双键消耗1mol溴,1mol碳碳叁键消耗2mol溴;
C.电石与水剧烈反应,放出大量的热;
D.1mol乙烯完全燃烧消耗氧气3mol,1mol乙炔完全燃烧消耗氧气2.5mol。
【详解】
A.电石(主要成分碳化钙)中含有磷化钙、硫化钙等杂质,遇到水后,生成硫化氢、磷化氢等有特殊气味
的气体,而乙炔是无色无味的气体,因混有磷化氢、硫化氢等气体才有特殊难闻的气味,A错误;
B.乙烯含有碳碳双键、乙炔含有碳碳三键,1mol碳碳双键消耗1mol溴,1mol碳碳叁键消耗2mol溴,因此
乙炔反应时消耗的溴要比等物质的量的乙烯反应消耗的多,B正确;
C.电石与水剧烈反应,放出大量的热,不能用启普发生器制备乙炔气体,C错误;
D.1mol乙烯完全燃烧消耗氧气3mol,1mol乙炔完全燃烧消耗氧气2.5mol,乙炔所耗氧气少,D错误;
综上所述,本题正确选项B。
7.(2020·广西南宁市·南宁三中高二期中)下图是制备和研究乙炔性质的实验装置图,下列有关说法错误
的是
A.用蒸馏水替代a中饱和食盐水可使产生的乙炔更为纯净
B.c中溶液的作用是除去HS、PH
2 3
C.d、e中溶液褪色的原理不同
D.f处产生明亮、伴有浓烟的火焰
【答案】A
【详解】
A.装置b中饱和食盐水与电石反应生成氢氧化钙和乙炔气体,若用蒸馏水代替饱和食盐水会使反应速率加
快,反应不容易控制,会有大量泡沫随乙炔气体逸出,故A错误;B.电石中混有硫化钙和磷化钙,与水反应生成的乙炔气体中混有的硫化氢和磷化氢,装置c中硫酸铜溶液
能除去乙炔气体中混有的硫化氢和磷化氢,防止对后续实验的影响,故B正确;
C.装置d中溴水与乙炔发生加成反应生成的1,1,2,2-四溴乙烷,使溴水褪色,装置e中乙炔与酸性高
锰酸钾溶液发生氧化反应,使酸性高锰酸钾溶液褪色,溶液褪色的反应原理不同,故C正确;
D.乙炔的含碳量高,在f处燃烧时会产生明亮、伴有浓烟的火焰,故D正确;
故选A。
8.(2020·上海市奉贤区奉城高级中学高二期末)下列关于乙炔的化学性质说法不正确的是( )
A.乙炔与氢气加成的产物是不一定是乙烯 B.乙炔与氯化氢反应的产物可能是氯乙烯
C.乙炔与氯化氢反应的产物也可能是氯乙烷D.乙炔也能发生聚合反应
【答案】C
【详解】
A.乙炔分子中有碳碳三键,和少量氢气发生加成反应可以生成乙烯,若和足量的氢气发生加成反应,可
以生成乙烷,故A正确;
B.乙炔和氯化氢发生加成反应,若控制一定条件,只断开碳碳三键中的一个键,可以生成氯乙烯,故B
正确;
C.乙炔和氯化氢发生不完全加成,生成氯乙烯,完全加成,生成的可能是1,1-二氯乙烷,也可能是1,2-二
氯乙烷,不能生成氯乙烷,故C错误;
D.乙炔含有碳碳三键,也能发生加聚反应生成聚乙炔,故D正确 ;
故选C。
9.(2017·上海市奉贤区奉城高级中学高二期末)除去乙烷中混有的少量乙炔,正确的方法是
A.将混合气体通入澄清石灰水 B.将混合气体通入碱石灰
C.将混合气体通入浓硫酸 D.将混合气体通入溴水
【答案】D
【分析】
除去乙烷中混有的少量乙炔,需要加入与乙炔反应但和乙烷不反应的物质,符合除杂的原则,由此分析。
【详解】
A.将含有乙烷和乙炔的混合气体通入澄清的石灰水,乙炔与澄清的石灰水不反应,不能除去乙炔,故A
不符合题意;
B.碱石灰中含有氢氧化钠和氧化钙,将含有乙烷和乙炔的混合气体通入碱石灰,乙炔与碱石灰不反应,
不能除去乙炔,故B不符合题意;
C.将含有乙烷和乙炔的混合气体通入浓硫酸,乙炔与浓硫酸不反应,不能除去乙炔,故C不符合题意;D.将含有乙烷和乙炔的混合气体通入溴水,乙烷和溴不反应,乙炔与溴单质发生加成反应,生成的1,
1,2,2-四溴乙烷是液体,留在溴水中,可以除去乙烷中的乙炔,故D符合题意;
答案选D。
10.(2021·北京西城区·高三期末)用下图所示装置及药品进行实验,能达到对应实验目的的是
图1 图2 图3 图4
A.图1:实验室制氨气 B.图2:检验乙炔具有还原性
C.图3:用乙醇萃取碘水中的I D.图4:用海水制取蒸馏水
2
【答案】D
【详解】
A. 氯化铵受热分解生成氨气和氯化氢,离开加热部位,气体温度降低后又会化合生成氯化铵固体,故实
验室不能用分解氯化铵制氨气,故A错误;
B. 用电石制取的乙炔中常含有HS气体,HS也具有还原性,能将高锰酸钾还原,使其褪色,干扰乙炔的
2 2
检验,因此应先除去HS,再检验乙炔具有还原性,故B错误;
2
C. 乙醇与水互溶,故不能用乙醇萃取碘水中的I,故C错误;
2
D. 可以用蒸馏的方法,用海水制取蒸馏水,故D错误;
故选D。
11.(2019·上海市第二工业大学附属龚路中学高二期中)有关乙炔性质、用途的叙述中,错误的是
A.乙炔在氧气中燃烧温度可高达3000℃ ,所以氧炔焰可以用来切割、焊接金属
B.乙炔可以制得聚氯乙烯塑料,所以聚氯乙烯的单体是乙炔
C.乙炔能使溴水褪色
D.乙炔也能使酸性KMnO 溶液褪色
4
【答案】B
【详解】
A.利用乙炔在氧气中燃烧温度可高达3000℃,常用氧炔焰来切割、焊接金属,故A正确;
B.乙炔与HCl发生加成反应生成氯乙烯,再由氯乙烯加聚制得聚氯乙烯塑料,则聚氯乙烯的单体是氯乙烯,故B错误;
C.乙炔分子结构中含有碳碳叁键,能使溴水褪色,故C正确;
D.乙炔分子结构中含有碳碳叁键,能使酸性KMnO 溶液褪色,故C正确;
4
故答案为B。
12.(2020·昭通市绥江县教育局高二期末)既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔的方法
是( )
A.通入足量的酸性高锰酸钾溶液 B.与足量的溴水反应
C.点燃 D.在一定条件下与氢气加成
【答案】B
【解析】
【详解】
A.乙炔和酸性高锰酸钾发生氧化还原反应生成二氧化碳气体,会引入新杂质,不能用高锰酸钾溶液除去
乙烷中含有的乙炔,故A错误;
B.通入足量的溴水中,乙炔与溴水发生加成反应,溴水褪色,既可以用来鉴别乙烷和乙炔,又可以用来
除去乙烷中混有的乙炔,故B正确;
C.乙烷和乙炔都可燃烧,不能用点燃的方法除杂,故C错误;
D.在一定条件下通入氢气不能鉴别乙烷和乙炔,能引入新的杂质,也不能除去乙烷中含有的乙炔,故D
错误;
答案选B。
13.(2020·赣榆智贤中学高二月考)分子式为C H 的烃有多种结构,下列叙述中能说明其结构是
4 6
的事实是
A.所有碳原子在同一直线上 B.能使酸性高锰酸钾溶液褪色
C.与Br 加成可以得到2种产物 D.1 mol该烃最多能与2 molBr 发生加成反应
2 2
【答案】A
【详解】
A.根据H-C≡C-H中所有原子在同一直线上,所有碳原子在同一直线上,说明两个甲基取代乙炔中两
个氢原子,因此其结构是 ,故A符合题意;
B.碳碳双键能使酸性高锰酸钾溶液褪色,可能含有两个碳碳双键HC=CHCH=CH,故B不符合题意;
2 2C.HC=CHCH=CH 与Br 加成可以得到2种产物,因此不能说明是其结构是 ,故
2 2 2
C不符合题意;
D.1 mol H C=CHCH=CH 最多能与2 molBr 发生加成反应,因此不能说明其结构是
2 2 2
,故D不符合题意。
综上所述,答案为A。
14.(2019·大安市第六中学校高二期末)某气态烃0.5 mol能与1 molHCl完全加成,加成后的产物分子
上的氢原子又可被2 molCl 完全取代。则此气态烃可能是( )
2
A.HC≡C-CH B.CH=CH C.HC≡CH D.CH=C(CH )
3 2 2 2 3 2
【答案】C
【分析】
气态烃0.5mol能与1molHCl加成,说明烃中含有1个C≡C键或2个C=C键,加成后产物分子上的氢原子
又可被2molCl 完全取代,说明0.5mol氯代烃中含有2molH原子,则原0.5mol烃中含有1molH原子,即
2
1mol烃含有含有2molH,并含有1个C≡C键或2个C=C键,以此解答该题。
【详解】
气态烃0.5mol能与1molHCl加成,说明烃中含有1个C≡C键或2个C=C键,加成后产物分子上的氢原子
又可被2molCl 完全取代,说明0.5mol氯代烃中含有2molH原子,则原先0.5mol烃中含有1molH原子,即
2
1mol烃含有含有2molH,并含有1个C≡C键或2个C=C键,符合要求的只有HC≡CH,故选C。
15.(2020·兴安县第三中学高二期中)下列有关乙炔性质的叙述中,既不同于乙烯又不同于乙烷的是
A.能燃烧生成CO 和HO
2 2
B.能发生加成反应
C.能与KMnO 发生氧化反应
4
D.能与HCl反应生成氯乙烯
【答案】D
【详解】
A.乙烯、乙烷、乙炔燃烧都生成CO 和HO,故A不符合题意;
2 2
B.乙烯、乙炔都能够发生加成反应,如:都能够使溴水褪色,故B不符合题意;
C.乙烯、乙炔都被酸性的高锰酸钾氧化,使高锰酸钾溶液褪色,故C不符合题意;
D.乙烯能与HCl反应生成氯乙烷,乙炔能与HCl反应生成氯乙烯,乙烷能与HCl不反应,所以乙炔性质
既不同于乙烯又不同于乙烷,故D符合题意;答案选D。
16.(2020·苏州新草桥中学高一月考)含有一个叁键的炔烃,与氢气加成后的产物如图所示,则该烃的结
构简式可能有( )
A.1种 B.2种 C.3种 D.4种
【答案】B
【详解】
根据炔烃与氢气加成反应的原理,推知该烷烃分子中相邻的碳原子上均带2个氢原子的碳原子间时对应炔
存在 的位置,有如图 所示的3个位置可以还原 ,其中1、2
两位置相同,故该炔烃共有2种,综上所述B符合题意,故选B。
答案选B。
二、填空题
17.(2020·湖南长沙市·雅礼中学高三月考)化学兴趣实验“一触即发”,它的实验原理是:将乙炔通入
到新制银氨溶液中,立即反应生成白色的乙炔银( )沉淀,继续通入乙炔至反应完全后过滤,洗涤滤
渣;将滤渣分成绿豆大小,在阴凉处风干,将风干后的乙炔银放在厚书本中,稍用力合书本即发生爆炸;
放在地面轻轻用鞋底摩擦即发生爆炸,微热也会发生爆炸;乙炔银主要用作引爆剂。
(1)实验室制取乙炔气体所用电石主要成分的电子式是___________,不能用启普发生器制取乙炔气体的原
因主要有:生成的 为糊状物、会堵塞导管,另一个主要原因是___________;为防止堵塞,制备
时需要控制反应速率,可以采用哪些措施___________(写出一点即可)。乙炔气体中常含有硫化氢,除去硫
化氢的离子方程式是___________。
(2)生成乙炔银( )沉淀的化学方程式是___________。
(3)将乙炔银投入到 溶液中,产生气体同时有黑色沉淀产生,该反应的离子方程式是___________。
(4)下列有关乙炔银的说法正确的是___________(填字母代号)。
A.应储存在郊外专业仓库内,仓库内要求阴凉通风B.必须与氧化剂、可燃物分开存放,切忌混储混运
C.发生泄漏时,无关人员应从顺风方向撤离
D.发生泄漏时,应防止泄漏物进入地表水、地下水和下水道
【答案】 反应剧烈且放出大量热量,可能会使启普发生器炸裂 饱和食盐水替
代水或通过分液漏斗逐滴加水 (或 )
ABD
【详解】
(1)实验室制取乙炔气体所用电石和水反应,电石的主要成分是CaC ,其电子式是 ;
2
不能用启普发生器制取乙炔气体的原因主要有:生成的 为糊状物、会堵塞导管,另一个主要原
因是反应剧烈且放出大量热量,可能会使启普发生器炸裂;为防止堵塞,制备时需要控制反应速率,可以
采用饱和食盐水替代水或通过分液漏斗逐滴加水;乙炔气体中常含有硫化氢,除去硫化氢可通过硫酸铜溶
液生成难溶的CuS(或硫化氢是酸性气体,用碱液吸收),离子方程式是 (或
);
(2) 将乙炔通入到新制银氨溶液中,立即反应生成白色的乙炔银( )沉淀,则生成乙炔银( )沉
淀的化学方程式是 ;
(3)将乙炔银投入到 溶液中,产生气体同时有黑色沉淀产生,该反应的离子方程式是
;
(4) A.根据题意,乙炔银极不稳定,摩擦或微热均会发生爆炸,应储存在郊外专业仓库内,仓库内要求阴
凉通风,故A正确;
B.乙炔银具有较强的还原性,因此必须与氧化剂、可燃物分开存放,避免发生氧化还原反应引起爆炸,故B正确;
C.乙炔银发生泄漏时,会生成易燃气体乙炔,应选择逆风方向,避免过多伤害,故C错误;
D.乙炔银不稳定,会与水反应生成有毒气体,且Ag+属于重金属离子,也有毒,会使水资源受到污染,
故应防止泄漏物进入水中,妥善保存,故D正确;
答案选ABD。
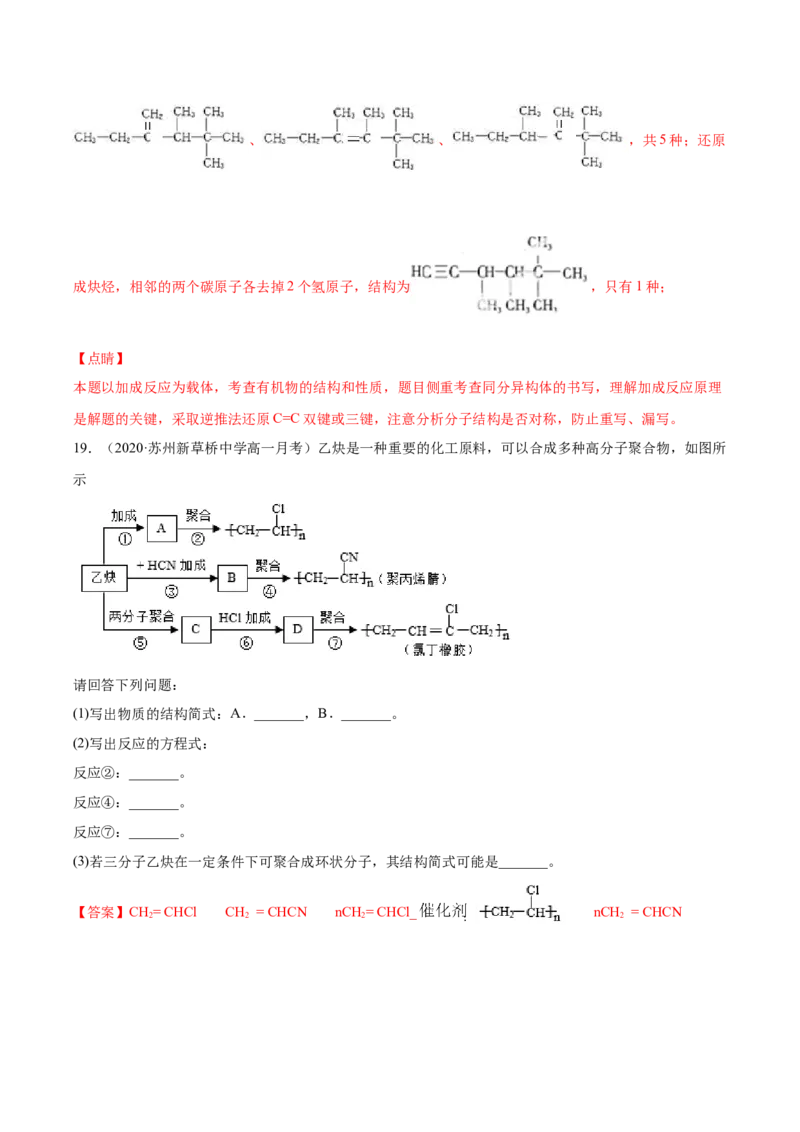
18.(2016·上海市控江中学高二期中)(1)有机物 用系统命名法命名_________
(2)若 是某单烯烃与氢气加成后的产物,则该烯烃可能有___________种结构;
若是某炔烃与氢气加成后的产物,则此炔烃可能有___________种结构。
【答案】2,2,3,4-四甲基己烷 5 1
【分析】
(1) 根据烷烃系统命名法的原则命名;
(2) 的碳链结构为 ,5号碳原子上没有H原子,与相连接
C原子不能形成碳碳双键,对应炔烃存在C≡C三键的位置,能形成三键位置有:1和2之间;
【详解】
(1)根据烷烃系统命名法的原则, 的名称是2,2,3,4-四甲基己烷;
(2) 是由单烯烃与氢气加成后的产物,还原成单烯烃时相邻的两个碳原子各去
掉一个氢原子,结构有 、 、、 、 ,共5种;还原
成炔烃,相邻的两个碳原子各去掉2个氢原子,结构为 ,只有1种;
【点睛】
本题以加成反应为载体,考查有机物的结构和性质,题目侧重考查同分异构体的书写,理解加成反应原理
是解题的关键,采取逆推法还原C=C双键或三键,注意分析分子结构是否对称,防止重写、漏写。
19.(2020·苏州新草桥中学高一月考)乙炔是一种重要的化工原料,可以合成多种高分子聚合物,如图所
示
请回答下列问题:
(1)写出物质的结构简式:A._______,B._______。
(2)写出反应的方程式:
反应②:_______。
反应④:_______。
反应⑦:_______。
(3)若三分子乙炔在一定条件下可聚合成环状分子,其结构简式可能是_______。
【答案】CH= CHCl CH = CHCN nCH= CHCl_ nCH = CHCN
2 2 2 2nCH= CCl- CH=CH 。
2 2
【分析】
乙炔与氯化氢发生加成反应生成A为CH= CHCl, A发生加聚反应得聚氯乙烯。乙炔与HCN发生加成反
2
应生成B为CH = CHCN, B发生加聚反应生成聚丙烯腈。2分子乙炔聚合得C为CH C- CH =CH ,C
2 2
与氯化氢发生加成反应得到D为CH= CCl- CH=CH ,D发生加聚反应生成氯丁橡胶。以此分析解答。
2 2
【详解】
(1)由上述分析可以知道,A为A为CH= CHCl,B为CH = CHCN,故答案是: CH= CHCl;CH =
2 2 2 2
CHCN。
(2) 反应②是CH= CHCl的聚合反应,生成聚氯乙烯,其反应的方程式:nCH= CHCl_
2 2
,故答案:nCH= CHCl_ ;
2
反应④是CH = CHCN的聚合反应,生成聚丙烯腈,其反应的方程式:nCH = CHCN
2 2
,故答案:nCH = CHCN ;
2
反应⑦是CH= CCl- CH=CH 发生加聚反应生成氯丁橡胶,反应方程式为:nCH= CCl- CH=CH
2 2 2 2
,故答案:nCH= CCl- CH=CH ;
2 2
(3)若三分子乙炔在一定条件下可聚合成环状分子为苯环,其结构简式是 ,故答案: 。
20.(2020·赣州市赣县第三中学高二月考)在75℃左右,用HgSO 作催化剂,乙炔可水化为乙醛,但
4
HgSO 遇到某些特定物质常会发生催化剂中毒而失去催化作用,HS就是其中一种。现用乙炔水化法,只
4 2
用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图:请回答以下问题:
(1)实验开始时,仪器A中盛放电石,B中应装入__________,其作用是_________。
(2)仪器D中盛放水,其作用是________________。
(3)蒸馏烧瓶F中应加入HgO和另外两种试剂,若将三者分别直接加入,请按加入的先后顺序写出包括
HgO在内的各试剂名称_____,将HgO加入F中的操作方法是__________。
(4)装置图中,加热F的方式叫________,所选用温度计G的量程表示正确的是_____(填代号)。
A.0℃~50℃B.0℃~100℃C.0℃~200℃D.0℃~360℃
【答案】NaOH溶液或者CuSO 溶液 除去HS、PH 这些杂质气体,防止催化剂中毒 冷却并吸收生
4 2 3
成的乙醛蒸气 氧化汞、水、浓硫酸 取一纸槽,加适量的HgO药品,然后将蒸馏烧瓶平放后,将纸
槽慢慢送入烧瓶内,慢慢竖立纸槽让药品滑入即可 水浴加热 B
【分析】
由图可以知道仪器的名称,A中碳化钙与分液漏斗中的水(或饱和食盐水)制备乙炔,B中NaOH溶液可除
去杂质HS,防止制备乙醛时催化剂中毒,F中先加固体后加液体,液体先加密度小的后加密度大的,C中
2
水浴加热75℃,乙炔与水在HgSO 做催化剂下反应生成CHCHO,D中水可吸收乙醛,以此来解答。
4 3
【详解】
(1)电石与饱和食盐水反应生成乙炔气体中含有少量杂质HS、AsH 、PH 等,因此为防止制备乙醛时催化
2 3 3
剂中毒,B中盛放的试剂为NaOH溶液或CuSO 溶液,其目的是为了除去由A装置导出的气流中混有的
4
HS、AsH 、PH 这些杂质气体,防止催化剂中毒;
2 3 3
(2)乙醛易溶于水,且沸点低,仪器D中盛放水,其作用是冷却并吸收乙醛蒸气;
(3)根据试剂加入顺序:先加固体氧化汞,接着加水,再加密度大的浓硫酸;将HgO加入F中的操作方法
是:将蒸馏烧瓶横置,用药匙或纸槽将粉末送至底部、再慢慢竖立、让药品滑入即可;
(4) 已知反应温度为75℃左右,故需控制75℃:把反应物放在蒸馏烧瓶内,蒸馏烧瓶放入盛有烧杯的水中
进行加热,使反应物受热均匀,易于控制温度,因此装置图中,加热F的方式叫水浴加热;由于水的沸点
为100℃,反应所需温度75℃左右,因此所选用温度计G的量程为0℃~100℃,B正确。
【点睛】本题以乙醛的制备为载体,考查了气体的提纯、水浴加热、温度计的选用以及试剂的取用等,熟练掌握基
本操作和仪器的使用是关键。