文档内容
第三章 晶体结构与性质
第四节 配合物与超分子
培优第一阶——基础过关练
1.下列关于超分子的叙述中正确的是
A.超分子就是高分子 B.超分子都是无限伸展的
C.形成超分子的微粒都是分子 D.超分子具有分子识别和自组装的特征
【答案】D
【详解】A.超分子通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组
织的聚集体,有的是高分子,有的不是,故A错误;
B.超分子这种分子聚集体有的是无限伸展的,有的的是有限的,故B错误;
C.形成超分子的微粒也包括离子,故C错误;
D.超分子的特征是分子识别和自组装,故D正确。
答案选D。
2.(2022·新疆·乌苏市第一中学高二阶段练习)下列各种说法中错误的是
A.形成配位键的条件是一方有空轨道,一方有孤电子对
B.共价键的形成条件是成键原子必须有未成对电子
C.配位化合物中的配体可以是分子也可以是阴离子
D.配位键是一种特殊的共价键
【答案】B
【详解】A.微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是能够接受孤
电子对的空轨道的原子或离子,故A正确;
B.形成共价键的成键原子不一定有未成对电子,如配位键中就是一方提供电子对,双方共用,故B错误;
C.配位化合物中,配体可以是HO、NH 、CO等含有孤电子对的分子,也可以是F-、Cl-、CN-等含有孤
2 3
电子对的阴离子,故C正确;
D.配位键又称配位共价键,是一方提供孤电子对,一方提供空轨道形成的,是一种特殊的共价键,故D
正确;
答案选B。
3.(2022·浙江·高二期末)下列说法不正确的是
A.超分子是由两种或两种以上的分子通过化学键作用形成的分子聚集体
B.过渡金属配合物远比主族金属配合物多
C.石墨中电子不能从一个平面跳跃到另一个平面
D.晶体具有自范性,某些物理性质会表现出各向异性
【答案】A
【详解】A.超分子是由两种或两种以上的分子通过分子间作用力形成的分子聚集体,A错误;
B.由于许多过渡元素金属李对多种配体具有很强的结合力,能形成种类繁多的配合物,所以过渡金属配合物远比主族金属的配合物多,B正确;
C.石墨中的电子在碳原子评上中运动,不能从一个平面跳跃到另一个平面上,C正确;
D.晶体有自范性,在光学性质或导电性或热膨胀系数或机械强度等方面表现为各向异性,D正确;
故选A。
4.(2022·福建省建瓯市芝华中学高二阶段练习)下列配合物的水溶液中加入硝酸银不能生成沉淀的是
A. B.
C. D.
【答案】B
【详解】A.由化学式可知,配合物[Co(NH )Cl]Cl的内界为[Co(NH )Cl]+、外界为氯离子,则配合物的
3 4 2 3 4 2
水溶液中加入硝酸银能生成氯化银沉淀,故A不符合题意;
B.由化学式可知,配合物[Co(NH )Cl]中氯离子与三价钴离子形成配位键,不易电离,则配合物的水溶液
3 3 3
中加入硝酸银不能生成氯化银沉淀,故B符合题意;
C.由化学式可知,配合物[Co(NH )]Cl 中内界为[Co(NH )]3+、外界为氯离子,则配合物的水溶液中加入
3 6 3 3 6
硝酸银能生成氯化银沉淀,故C不符合题意;
D.由化学式可知,配合物[Co(NH )Cl]Cl 中内界为[Co(NH )Cl]2+、外界为氯离子,则配合物的水溶液中
3 4 2 3 4
加入硝酸银能生成氯化银沉淀,故D不符合题意;
故选B。
5.(2022·四川·雅安中学高二阶段练习)配合物 可用于离子检验,下列说法不正确的是
A.此配合物中存在离子键、配位键、极性键、非极性键
B.配体为CN-,与N、CO互为等电子体
2
C.1mol配合物中 键数目为
D.该配合物为离子化合物,易电离,1mol该配合物电离得到阴、阳离子的数目共
【答案】A
【详解】A. 此配合物中存在离子键、配位键、极性键,没有非极性键,A错误;
B.原子个数相等且价电子数也相等的分子或离子即为等电子体,CN-、N、CO都是两个原子,且价电子
2
数都是10个,即为等电子体,故B正确;
C.1mol配合物每个C-N中一个 σ 键,共有6个;每个Fe-CN中一个 σ 键,共有6个,一共就是12个,
C正确;
D. 1mol该配合物电离得到3mol钠离子和1mol[Fe(CN) ]-,阴、阳离子的数目共 4NA,D正确;
6
故选A。
6.利用超分子可分离 和 。将 、 混合物加入一种空腔大小适配 的杯酚中进行分离的流程如
图所示。下列说法错误的是
A.该流程体现了超分子具有“分子识别”的特征
B.杯酚分子中存在大 键
C.杯酚与 形成氢键
D. 与金刚石晶体类型不同
【答案】C
【详解】A.利用杯酚分离 和 体现了超分子具有“分子识别”的特征,A项正确;
B.杯酚分子中含有苯环结构,存在大 键,B项正确;
C.杯酚与 形成的不是氢键,C项错误;
D.金刚石是共价晶体, 为分子晶体,二者晶体类型不同,D项正确;
故选D。
7.(2022·山东省沂南第一中学高二阶段练习)许多过渡金属离子对多种配体有很强结合力,能形成种类
繁多的配合物。下列说法错误的是
A.CuSO 溶液呈蓝色,是由于存在配离子[Cu(H O) ]2+
4 2 4
B.配合物[PtCl (NH )]为平面结构,存在顺反异构体
2 3 2
C.配合物[Ti(OH) (H O) ]2+中Ti4+的配位数是4
4 2 2
D.向配合物[TiCl(H O) ]Cl ·H O溶液中加入足量AgNO 溶液,只有 的Cl-被沉淀
2 5 2 2 3
【答案】C
【详解】A.CuSO 溶液中的铜离子以水合离子的形式存在,即溶液呈蓝色是因为溶液中存在
4
[Cu(H O) ]2+,A正确;
2 4
B.配合物[PtCl (NH )]为平面结构,有 、 两种结构,所以存在顺反异构体,B正确;
2 3 2
C.配合物[Ti(OH) (H O) ]2+中Ti4+的配体是OH-、HO,配位数是6,C错误;
4 2 2 2
D.内界的氯不能电离,外界的氯能电离,向配合物[TiCl(H O) ]Cl ·H O的溶液中加入足量AgNO 溶液,
2 5 2 2 3
只有 的Cl-生成氯化银沉淀,D正确;
故答案选C。8.(2022·湖北·浠水县实验高级中学高二阶段练习)某超分子的结构如图所示,下列有关超分子的描述不
正确的是
A.超分子就是高分子
B.超分子的特征是分子识别和分子自组装
C.图示中的超分子是两个不同的分子通过氢键形成的分子聚集体
D.图示中的超分子中的N原子采取sp2、sp3两种杂化方式
【答案】A
【详解】A.超分子通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组
织的聚集体,超分子不同于高分子,A错误;
B.超分子的特征是分子识别和分子自组装,例如细胞和细胞器的双分子膜具有自组装性质,生物体的细
胞即是由各种生物分子自组装而成,B正确;
C.超分子通常是指由两种或两种以上分子依靠分子间相互作用结合在一起,组成复杂的、有组织的聚集
体,图示中的超分子是两个不同的分子通过氢键形成的分子聚集体,C正确;
D.图示中的超分子中的N原子有双键、单键,则采取sp2、sp3杂化,D正确;
故选A。
9.(2022·重庆市二0三中学校高二阶段练习)配合物[Cu(NH )](OH) 的中心离子、配体、中心离子的电
3 4 2
荷数和配位数分别为
A.Cu2+、OH-、2+、2 B.Cu+、NH 、1+、4
3
C.Cu2+、NH 、2+、4 D.Cu2+、NH 、2+、2
3 3
【答案】C
【详解】配合物[Cu(NH )](OH) 的中心离子是Cu2+,4个氨分子和Cu2+形成配位键,配体是NH ,中心离
3 4 2 3
子的电荷数为+2,配位数为4,故选C。
10.(2022·四川省内江市第六中学高二期中)某化合物的化学式为CoCl ·4NH ,1mol此化合物中加入足
3 3
量的AgNO 溶液,能生成1mol的白色沉淀,以强碱处理并加热没有NH 放出,则此化合物的说法正确的
3 3
是
A.该化合物的配体数为4 B.Co3+只与NH 分子形成配位键
3
C.该化合物可以写成[Co(NH )Cl]Cl D.该化合物可能显平面正方形结构
3 4 2
【答案】C【分析】实验式为CoCl ·4NH 的物质,1molA中加入足量的AgNO 溶液中能生成1mol白色沉淀,说明A
3 3 3
中含有1个Cl-,以强碱处理并没有NH 放出,说明不存在游离的氨分子,则该物质的配位化学式为
3
[Co(NH )Cl]Cl,据此答题。
3 4 2
【详解】A.配合物中中心原子的电荷数为3,配位数为6,A错误;
B.由分析可知,Cl-与NH 分子均与Co3+形成配位键,B错误;
3
C.由分析可知,此配合物可写成[Co(NH )Cl] Cl,C正确;
3 4 2
D.该配合物应是八面体结构,Co与6个配题成键,D错误;
故选C。
11.(2022·重庆市清华中学校高二阶段练习)已知某紫色配合物的组成为CoCl ·5NH ·H O,其水溶液显
3 3 2
弱酸性,加入强碱并加热至沸腾有NH 放出,同时产生Co O 沉淀;向一定量该配合物溶液中加过量
3 2 3
AgNO 溶液,有AgCl沉淀生成,待沉淀完全后过滤,再加过量AgNO 溶液于滤液中,无明显变化,但加
3 3
热至沸腾又有AgCl沉淀生成,且第二次沉淀量为第一次沉淀量的二分之一,则该配合物的化学式最可能
为
A.[CoCl (NH )]Cl·NH ·H O B.[Co(NH )(H O)]Cl
2 3 4 3 2 3 5 2 3
C.[CoCl (NH )(H O)]Cl·2NH D.[CoCl(NH )]Cl ·H O
2 3 3 2 3 3 5 2 2
【答案】D
【详解】CoCl ·5NH ·H O水溶液加过量AgNO 溶液,有AgCl沉淀生成,说明外界离子有氯离子,过滤后
3 3 2 3
再加过量AgNO 溶液于滤液中,无明显变化,但加热至沸腾又有AgCl沉淀生成,说明配体中含有氯离子,
3
且第二次沉淀量为第一次沉淀量的二分之一,说明外界离子中的氯离子与配体中的氯离子的个数比为
2:1,则该配合物的化学式最可能为[CoCl(NH )]Cl ·H O,
3 5 2 2
答案选D。
培优第二阶——拓展培优练
12.(2022·四川省绵阳江油中学高二阶段练习)已知 在溶液中与 或 等可形成配位数为4的配
离子。某同学通过实验研究铜盐溶液颜色的变化。下列说法不正确的是
A.溶液②中形成了 , 中有12molσ键
B.由④可知, 与 可能会结合产生黄色物质
C.由②③④推测,溶液中存在:D.若取少量④中溶液进行稀释,溶液依然为绿色
【答案】D
【详解】A.实验①②可知,无水CuSO 是白色的,加入水后CuSO 溶液呈蓝色,这说明②中溶液呈蓝色
4 4
是Cu2+与水分子作用的结果;1mol 中含有4mol水中的8molσ键和4mol配位键,共12molσ
键,故A正确;
B.向③中溶液加入NaCl固体后,底部的NaCl固体表面变为黄色,说明Cu2+与Cl-可能会结合产生黄色物
质,故B正确;
C.③中蓝色溶液加入足量NaCl固体后固体表面为黄色,振荡后溶液呈绿色可以是黄色和蓝色的混合呈现
的颜色,说明CuCl 水溶液中存在平衡: ,[CuCl ]2-可能为黄色,
2 4
故C正确;
D.③中溶液为蓝色,④中溶液为绿色,说明Cl−的浓度对铜盐溶液的颜色产生影响,CuCl 的稀溶液为蓝
2
色,浓溶液为绿色,故D错误;
故选D。
13.(2021·北京朝阳·高二期末)实验:①将少量白色 固体溶于水,得到蓝色溶液;将少量
固体溶于水,得到无色溶液;
②向蓝色溶液滴加氨水,首先形成难溶物,继续添加氨水并振荡试管,难溶物溶解,得到深蓝色透明溶液;
③向深蓝色透明溶液加入乙醇,析出深蓝色晶体。
下列分析不正确的是
A.①中蓝色溶液中呈蓝色的物质是 离子
B.②中形成难溶物的反应为
C.②中难溶物溶解的反应为
D.③中加入乙醇后析出的深蓝色晶体是
【答案】D
【详解】A.将少量白色 固体溶于水,得到蓝色溶液,铜离子与水分子结合形成蓝色的
离子,A正确;
B.向蓝色溶液滴加氨水,形成难溶物,铜离子与一水合氨反应生成氢氧化铜沉淀,离子方程式为:
,B正确;
C.氢氧化铜沉淀溶于氨水,反应生成蓝色的四氨合铜离子,离子方程式为:
,C正确;
D.向深蓝色透明溶液加入乙醇, 的溶解度减低,析出深蓝色晶体,D错误;
故选D。14.(2022·北京顺义·高二期末)Fe3+的配位化合物较稳定且应用广泛。Fe3+可与HO、SCN-、F-等配体形
2
成使溶液呈浅紫色的[Fe(H O) ]3+、红色的[Fe(SCN) ]3-、无色的[FeF ]3-配离子。某同学按如下步骤完成实验:
2 6 6 6
已知:向Co2+的溶液中加入KSCN溶液生成蓝色的[Co(SCN) ]2-配离子;Co2+不能与F-形成配离子。下列说
4
法不正确的是
A.Fe第四电离能(I)大于其第三电离能(I)
4 3
B.Ⅰ中溶液呈黄色可能是由Fe3+水解产物的颜色造成
C.可用NaF和KSCN溶液检验FeCl 溶液中是否含有Co2+
3
D.[Fe(H O) ]3+中H-O-H的键角与HO分子中H-O-H的键角相等
2 6 2
【答案】D
【详解】A.Fe3+的价电子排布式为3d5,3d轨道处于半满状态,电子的能量低,失电子困难,所以Fe的第
四电离能(I)大于其第三电离能(I),A正确;
4 3
B.Ⅰ中Fe(NO ) 溶于水后,Fe3+发生部分水解生成Fe(OH) 等,使溶液呈黄色,B正确;
3 3 3
C.先往溶液中加入足量的NaF溶液,再加入KSCN溶液,若溶液呈蓝色,则表明含有Co2+,否则不含
Co2+,C正确;
D.[Fe(H O) ]3+中HO分子内O原子最外层只存在一对孤对电子,对H-O-H中O-H键的排斥作用减小,所
2 6 2
以键角比HO分子中H-O-H的键角大,D不正确;
2
故选D。
15.(2022·山东济宁·高二期末)冠醚是一类皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属
离子。18-冠-6可以通过图示方法制备。
下列说法错误的是
A.18-冠-6分子中C、O都采用sp3杂化
B.18-冠-6可以适配任意碱金属离子
C.冠醚的空穴结构对离子有选择作用,在有机反应中可作催化剂
D.制取方法中(1)为取代反应,(2)为加成反应
【答案】B
【详解】A.18-冠-6分子中,C、O的价层电子对数都为4,所以都采用sp3杂化,A正确;B.题干信息显示:“不同大小的空穴适配不同大小的碱金属离子”,所以18-冠-6只能适配相应大小的碱
金属离子,B错误;
C.由题干信息可知,冠醚的空穴结构对离子有选择作用,与金属离子形成的配离子,在有机反应中可作
催化剂,C正确;
D.制取方法(1)中,生成18-冠-6的同时,还有HCl生成,为取代反应,(2)中,只有18-冠-6一种物质生成,
为加成反应,D正确;
故选B。
16.(2022·福建三明·高二期末)英国牛津大学的研究人员发现一种基于铝的配位化合物,它能将苯环转
换成链状化合物,反应如下:
其中 为邻苯二甲酸异戊酯。下列说法正确的是
A. 有 和 两种结构
B.X、Y均属于鳌合物,配位原子只有N、O
C.Y中Al的化合价为
D.Z中处于同一平面的碳原子最多8个
【答案】D
【详解】A.(CH)SnCl 以Sn为中心形成四面体结构,因此(CH)SnCl 没有同分异构体,A错误
3 2 2 3 2 2
B.X和Y中的N和O与Al形成鳌合环,但Y中除N和O之外,Cl也是配位原子,B错误;
C.Y中Al的配位数为5,为+3价的Al3+,C错误;
D.Z( )中1-6号C在同一平面内,由于以Sn为中心形成四面体,
因此7、8和9、10中只能各有一个可以在该平面内,因此最多8个C在一个平面内,D正确;
故选D。
17.(2022·四川省内江市第六中学高二期中)在碱性溶液中,Cu2+可与缩二脲形成紫色配离子,其结构如图。下列说法错误的是
A.该配离子中非金属元素的电负性大小顺序为O>N>C>H
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中能与水分子形成氢键的原子只有N和O
【答案】D
【详解】A.根据同周期主族元素的电负性由左到右逐渐增大,同主族元素的电负性由上到下逐渐减小,
所以该配离子中的非金属元素的电负性大小顺序为 ,A项正确;
B.根据配离子的结构可知,铜离子形成4个共价键,B项正确;
C.根据铜离子的电子排布式可知,基态铜原子的价电子排布式为 ,C项正确;
D.N原子和O原子可与水分子中的H原子形成氢键,水分子中的O原子也可与配离子中的H原子形成氢
键,D项错误;
故选D。
18.(2022·四川省内江市第六中学高二期中)含有多个配位原子的配体与同一中心离子(或原子)通过螯合
配位成环而形成的配合物为螯合物。一种原子序数为48的Cd2+配合物的结构如图所示,则下列说法正确的
是
A.该螯合物中N的杂化方式有2 种
B.1mol该配合物中通过螯合作用形成的配位键有6mol
C.Cd属于d区元素
D.Cd的价电子排布式为4d85s2
【答案】B
【详解】A.该整合物中无论是硝基中的N原子,还是 中的N原子,还是六元环中的N原子,N均为
杂化,即N只有1种杂化方式,A错误;
B.该整合物中 与5个N原子、2个O原子形成化学键,其中与1个O原子形成的为共价键,另外的
均为配位键,故1mol该配合物中通过整合作用形成6mol配位键,B正确;C.原子序数为48的Cd属于ds区元素,C错误;
D.Cd的价电子排布式为4d105s2,D错误;
故选B。
19.(2021·四川省南充市嘉陵第一中学高二阶段练习)将过量的氨水加到硫酸铜溶液中,溶液最终变成深
蓝色。
(1)Cu的价电子轨道表达式为____;在周期表中,Cu元素属于___________区。
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程
式:___________。
(3)向深蓝色溶液继续加入___________,析出深蓝色的晶体[Cu(NH )]SO ·H O。[Cu(NH )]SO ·H O中,
3 4 4 2 3 4 4 2
1mol[Cu(NH)] 2+含有σ键的数目为___________。
3 4
(4)___________(填“HO”或“NH ”)与Cu2+形成的配位键更稳定。
2 3
(5)SO 的VSEPR模型名称为___________,HO+空间构型为___________。
3
(6)硫酸铜溶液中滴入氨基乙酸钠(H NCH COONa)即可得到配合物A,其结构如下图所示。
2 2
该结构中,除共价键外还存在配位键,请在图中用“→”表示出配位键___________。
【答案】(1) ds
(2)Cu(OH) +4NH=[Cu(NH)]2++ 2OH-
2 3 3 4
(3) 乙醇 16N
A
(4)NH
3
(5) (正)四面体形 三角锥形
(6)
【解析】(1)
Cu的原子序数为29,其价电子排布式为3d104s1,轨道表达式为: ,属于ds区元素。
(2)
将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀为氢氧化铜,继续滴加氨水,沉淀溶解,氢氧化铜中的铜
离子和氨气形成了配离子,相应的离子方程式为:Cu(OH) +4NH=[Cu(NH)]2++ 2OH-。
2 3 3 4(3)
向深蓝色溶液继续加入乙醇,[Cu(NH )]SO ·H O溶解度降低,析出深蓝色的晶体,[Cu(NH )]2+的每个NH
3 4 4 2 3 4 3
中存在3个N-Hσ键,铜离子和氮原子之间存在的配位键为σ键,每个[Cu(NH )]2+中存在16个σ键,则
3 4
1mol[Cu(NH)] 2+含有16molσ键,数目为16N 。
3 4 A
(4)
配位原子电负性越小,越易给出孤对电子,生成的配合物越稳定,N的电负性比O小,因此NH 与Cu2+形
3
成的配位键更稳定。
(5)
SO 的中心原子价电子对数为4+ =4,采取sp3杂化,VSEPR模型为正四面体形,HO+的中心原子
3
价电子对数为3+ =4,采取sp3杂化,有1对孤对电子,空间构型为三角锥形。
(6)
配合物A中铜离子提供空轨道,HNCH COO-中氮原子提供孤对电子,因此配位键可表示为:
2 2
。
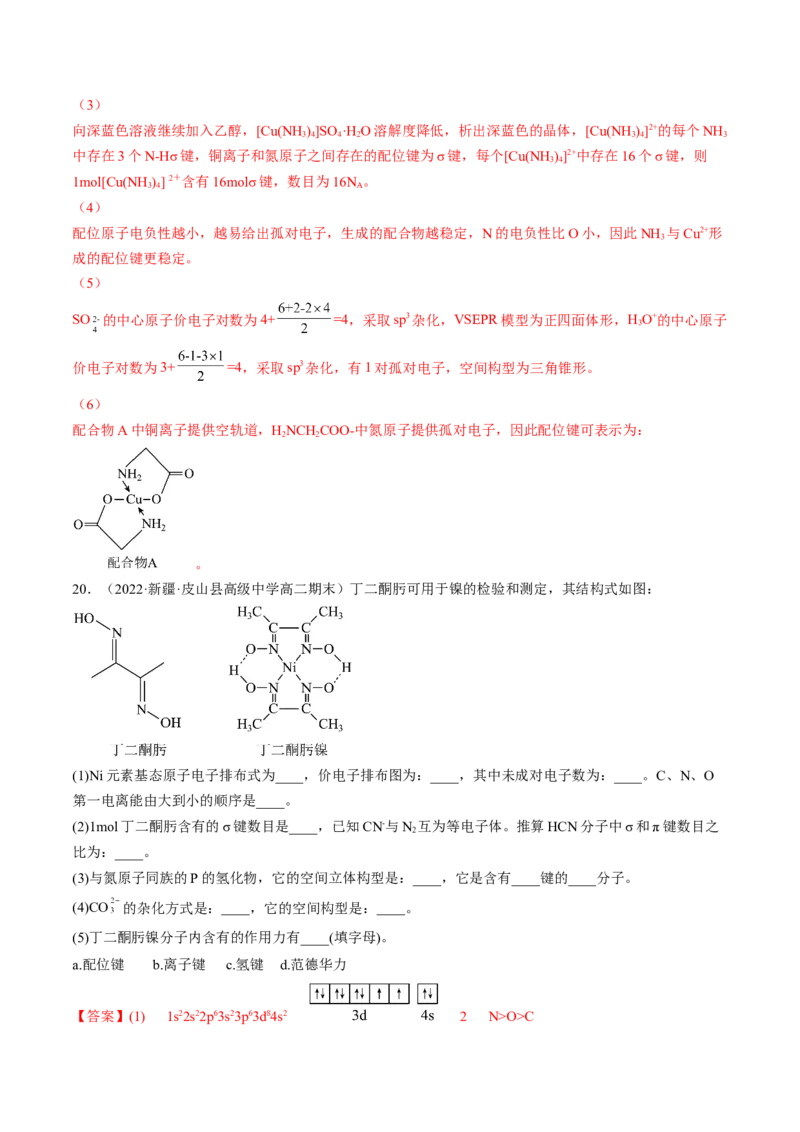
20.(2022·新疆·皮山县高级中学高二期末)丁二酮肟可用于镍的检验和测定,其结构式如图:
(1)Ni元素基态原子电子排布式为____,价电子排布图为:____,其中未成对电子数为:____。C、N、O
第一电离能由大到小的顺序是____。
(2)1mol丁二酮肟含有的σ键数目是____,已知CN-与N 互为等电子体。推算HCN分子中σ和π键数目之
2
比为:____。
(3)与氮原子同族的P的氢化物,它的空间立体构型是:____,它是含有____键的____分子。
(4)CO 的杂化方式是:____,它的空间构型是:____。
(5)丁二酮肟镍分子内含有的作用力有____(填字母)。
a.配位键 b.离子键 c.氢键 d.范德华力
【答案】(1) 1s22s22p63s23p63d84s2 2 N>O>C(2) 15N 1:1
A
(3) 三角锥形 极性 极性
(4) sp2杂化 平面三角形
(5)ac
【解析】(1)
Ni元素为28号元素,基态原子电子排布式为1s22s22p63s23p63d84s2,价电子排布图为:
,其中未成对电子数为:2。同一周期随着原子序数变大,第一电离能变大,N的2p
轨道为半充满稳定状态,第一电离能大于同周期相邻元素,故C、N、O的第一电离能大小:N>O>C;
(2)
单键均为σ键,双键中含有1个σ键1个π键,由结构简式可知,1mol丁二酮肟含有的σ键数目是15N ,
A
1个N 中含有1个σ键2个π键,已知CN-与N 互为等电子体,则1分子HCN分子中σ和π键数目分别为
2 2
2、2,两者之比为1:1;
(3)
与氮原子同族的P的氢化物为PH ,中心P原子价层电子对数为3+ =4,P原子采用sp3杂化,空间立
3
体构型是:三角锥形,它是含有P-H极性键的极性分子。
(4)
CO 中心C原子价层电子对数为3+ =3,C原子采用sp2杂化,空间立体构型是:平面三角形;
(5)
由结构简式可知,丁二酮肟镍分子内含有的作用力有氢键,镍和氮原子间存在配位键,C=N、O-N、C-C、
C-H间存在共价键;故选ac。
21.(2022·江苏苏州·高二期中)铜及其化合物在工农业生产中有广泛的应用。
Ⅰ.金属铜的原子堆积模型如图-1所示,
(1)该晶胞中每个Cu原子周围最近距离的Cu原子数目为_______。
Ⅱ. 能与 、 、 、 等形成配位数为4的配合物。
(2)向 溶液中加入过量NaOH溶液可生成 。 中除了配位键外,还存在的化学键类型有_______(填字母)。
A.离子键 B.金属键 C.极性共价键 D.非极性共价键
(3)将CuO投入 、 的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约为9.5,CuO转
化为 溶液。
①CuO被浸取的离子方程式为_______。
② 结构中,若用两个 分子代替两个 分子,可以得到两种不同结构的化合物,由此
推测 的空间构型为_______。
(4) 可以与乙二胺( )形成配离子,如题图-2所示:
③H、O、N三种元素的电负性从大到小的顺序为_______。
④乙二胺分子中N原子成键时采取的杂化类型是_______。乙二胺和三甲胺 均属于胺,但乙二
胺比三甲胺的沸点高很多,原因是_______。
Ⅲ.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,
(5)下列物质中,属于顺磁性物质的是_______(填标号)。
A. B. C.
【答案】(1)12
(2)AC
(3) 正方形
(4) O>N>H sp3 乙二胺可以形成分子间氢键
(5)BC
【详解】(1)金属铜的原子堆积模型位面心立方最密堆积,该晶胞中每个Cu原子周围最近距离的Cu原
子数目为12;
(2)根据信息可知 能与 形成配位键, 中除了配位键外,Na+与 之间
存在离子键, 之间存在极性共价键,故 还存在的化学键类型有离子键、极性共价键,
故答案为:AC;
(3)①将CuO投入 、 生成 ,CuO被浸取的离子方程式为;
② 结构中,若用两个 分子代替两个 分子,如果 是正四面体结构,两
个 分子代替两个 分子,得到 只有一种结构; 可以得到两种不
同结构的化合物,由此推测 的空间构型为正方形结构;
(4)③同周期元素从左到右电负性依次增大,故电负性为O>N>H;
④乙二胺分子中N原子与H和C形成3个 键,有一对个电子对,价层电子对为4,采取sp3杂化;乙二胺
分子间可以形成氢键,三甲胺 不能形成氢键,只有分子间作用力,所以乙二胺沸点高;
(5)具有未成对电子的物质具有顺磁性,Cu+价电子排布为3d10,Cu2+价电子排布为3d9,+2价的铜离子形
成的物质具有顺磁性,故答案为BC;
22.(2022·北京东城·高二期末)实验小组研究硫酸四氨合铜(II)([Cu(NH )]SO ·H O)晶体的制备。
3 4 4 2
[实验一]制备[Cu(NH )]SO 溶液
3 4 4
甲:向2 mol/L CuSO 溶液中滴加NaOH溶液,产生蓝色沉淀,再向所得浊液(标记为浊液a)中加入过量
4
6mol/L氨水,沉淀不溶解。
乙:向2mol/LCuSO 溶液中滴加6mol/L氨水,产生蓝色沉淀,再向浊液中继续滴加过量6mol/L氨水,沉
4
淀溶解,得到深蓝色溶液。
(1)画出四氨合铜配离子中的配位键:_______。
(2)甲中,生成蓝色沉淀的离子方程式是_______。
(3)研究甲、乙中现象不同的原因。
[提出猜测]
i.Na+可能影响[Cu(NH )]2+的生成。
3 4
ii. 促进了[Cu(NH )]2+的生成。
3 4
[进行实验]
①将浊液a过滤,洗涤沉淀,把所得固体分成两份。
②向其中一份加入过量6 mol/L氨水,观察到_______ , 说明猜测i不成立。
③向另一份加入过量6 mol/L氨水,再滴入几滴_______(填试剂),沉淀溶解,得到深蓝色溶液,说明猜测
ii成立。
[实验反思]
④从平衡移动的角度,结合化学用语解释为什么 能促进[Cu(NH )]2+的生成:_______。
3 4
[实验二]制备硫酸四氨合铜晶体
资料:
i.[Cu(NH )]SO ·H O受热易分解;
3 4 4 2
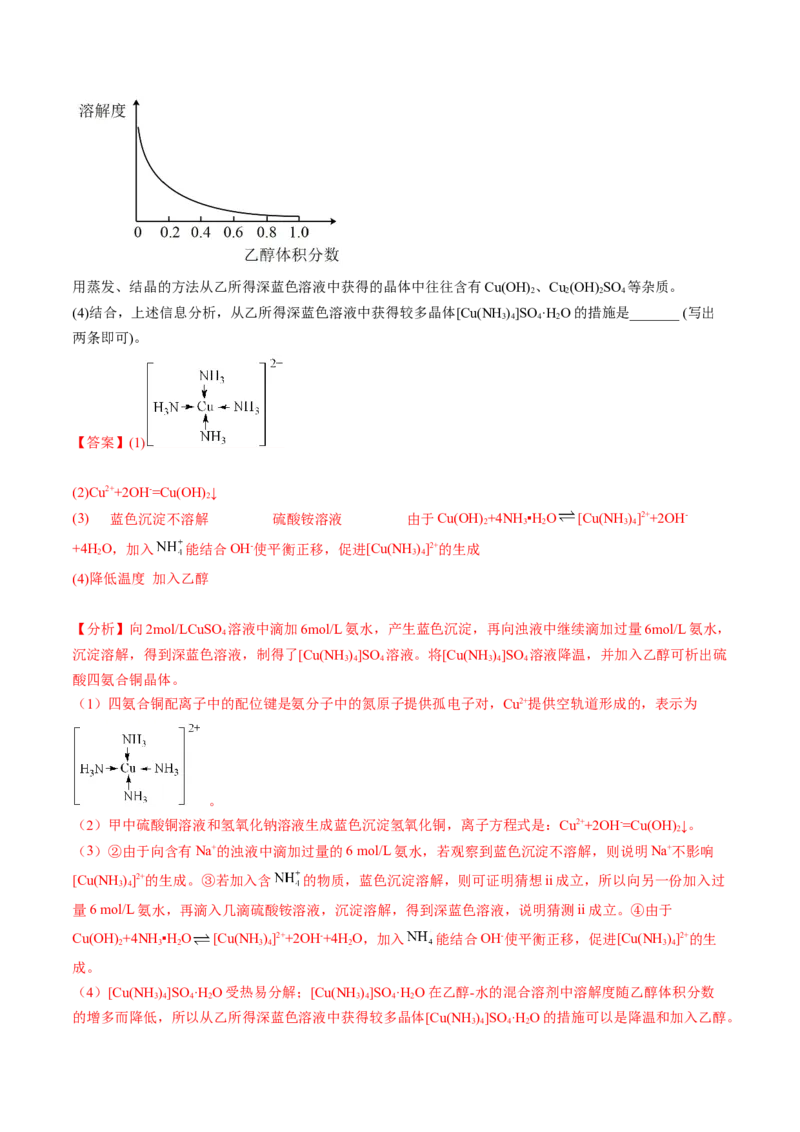
ii. [Cu(NH )]SO ·H O在乙醇-水的混合溶剂中溶解度随乙醇体积分数的变化如下图所示。
3 4 4 2用蒸发、结晶的方法从乙所得深蓝色溶液中获得的晶体中往往含有Cu(OH) 、Cu (OH) SO 等杂质。
2 2 2 4
(4)结合,上述信息分析,从乙所得深蓝色溶液中获得较多晶体[Cu(NH )]SO ·H O的措施是_______ (写出
3 4 4 2
两条即可)。
【答案】(1)
(2)Cu2++2OH-=Cu(OH) ↓
2
(3) 蓝色沉淀不溶解 硫酸铵溶液 由于Cu(OH) +4NH▪H O [Cu(NH )]2++2OH-
2 3 2 3 4
+4H O,加入 能结合OH-使平衡正移,促进[Cu(NH )]2+的生成
2 3 4
(4)降低温度 加入乙醇
【分析】向2mol/LCuSO 溶液中滴加6mol/L氨水,产生蓝色沉淀,再向浊液中继续滴加过量6mol/L氨水,
4
沉淀溶解,得到深蓝色溶液,制得了[Cu(NH )]SO 溶液。将[Cu(NH )]SO 溶液降温,并加入乙醇可析出硫
3 4 4 3 4 4
酸四氨合铜晶体。
(1)四氨合铜配离子中的配位键是氨分子中的氮原子提供孤电子对,Cu2+提供空轨道形成的,表示为
。
(2)甲中硫酸铜溶液和氢氧化钠溶液生成蓝色沉淀氢氧化铜,离子方程式是:Cu2++2OH-=Cu(OH) ↓。
2
(3)②由于向含有Na+的浊液中滴加过量的6 mol/L氨水,若观察到蓝色沉淀不溶解,则说明Na+不影响
[Cu(NH )]2+的生成。③若加入含 的物质,蓝色沉淀溶解,则可证明猜想ii成立,所以向另一份加入过
3 4
量6 mol/L氨水,再滴入几滴硫酸铵溶液,沉淀溶解,得到深蓝色溶液,说明猜测ii成立。④由于
Cu(OH) +4NH▪H O [Cu(NH )]2++2OH-+4H O,加入 能结合OH-使平衡正移,促进[Cu(NH )]2+的生
2 3 2 3 4 2 3 4
成。
(4)[Cu(NH )]SO ·H O受热易分解;[Cu(NH )]SO ·H O在乙醇-水的混合溶剂中溶解度随乙醇体积分数
3 4 4 2 3 4 4 2
的增多而降低,所以从乙所得深蓝色溶液中获得较多晶体[Cu(NH )]SO ·H O的措施可以是降温和加入乙醇。
3 4 4 2