文档内容
长沙市一中 2024 届高考适应性演练(二)
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D B D B B B B C B D A C C D
1.D【解析】A.臭氧具有强氧化性,可用于自来水消毒,A正确;B.碳纤维材料属于
新型无机非金属材料,B正确;C.钛合金是以钛为基础加入其它元素形成的合金材料,属
于金属材料,C正确;D.纳米铁粉主要是通过其还原性,将Cu2+、Ag+、Hg2+还原为相应的金
属单质将其除去,D错误;综上所述答案为D。
2.B【解析】A.碳原子半径大于氧原子半径,A错误;B.N,N-二甲基甲酰胺的结构
简式: ,B正确;C.球棍模型不能表示出孤对电子,图示为VSEPR模型,C错
误;D.CaO 中含过氧键,该电子式错误,D错误;故选B。
2
3.D【解析】A.连接4个不同原子或原子团的碳原子为手性碳原子,甘草素中含有1
个手性碳原子( ),故A不正确;B.甘草素分子结构中不含酯基,含酮
基、醚键及羟基,故B不正确;C.甘草素含有酚羟基,能与饱和溴水发生取代反应,但无
碳碳双键,不能发生加成反应,故C不正确;D.1mol甘草素含有2mol酚羟基,最多能与
2molNaOH反应,故D正确;答案选D。
4.B【解析】A.单质碘和四氯化碳都是非极性分子,根据相似相溶的原理,I 易溶于
2
CCl ,A正确;B.分子间氢键可以增大其熔沸点,则对羟基苯甲酸存在分子间氢键,是其
4
沸点比邻羟基苯甲酸的高的主要原因,B错误;C.银离子可以和氨气形成配合物离子,导
致氯化银可以溶解在氨水中,C正确;D.氯化钠在熔融状态产生了自由移动的Na和Cl,
从而可以导电,D正确;故选B。
5.B【解析】A.标准状况下,己烷为液态,无法计算其物质的量,故A错误;B.单
键由1个σ键形成,双键由1个σ键和1个π键形成,1分子 中含有11个σ键,
则0.1mol该物质中含有的σ键数目为1.1N,故B正确;C.1molNaO 参加反应转移1 mol
A 2 2
电子,3.9gNaO 物质的量为0.05mol,与足量水反应,转移电子数为0.05N,故C错误;D.没
2 2 A
有明确体积,无法计算其物质的量,故D错误;故选:B。
6.B【解析】A.由图可知,过渡态能量的大小顺序为①>②>③,故A正确;B.(CH)COCH
3 3 2 5
与HBr在一定条件下可以逆向转化为(CH)CBr,即为(CH)CBr和CHOH转化为(CH)COCH
3 3 3 3 2 5 3 3 2 5
的逆过程,该过程需要先转化为(CH)C+Br-和CHOH,(CH)C+Br-和CHOH再转化为(CH)CBr
3 3 2 5 3 3 2 5 3 3
和CHOH,但(CH)C+Br-和CHOH同时也能转化为(CH)C=CH,故B错误;C.氯元素的电负
2 5 3 3 2 5 3 2 2
性大于溴元素,则叔丁基氯的能量低于叔丁基溴,(CH)C+Cl-的能量高于(CH)C+Br-,所以若
3 3 3 3
将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E的值增大,故C正确;D.由图可知,
4 3
化学(一中)答案 (第 1 页,共 7 页)
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}(CH)CBr的乙醇溶液生成(CH)C=CH 过程放出能量相较于生成(CH)COCH 低,加入氢氧化
3 3 3 2 2 3 3 2 5
钠能与HBr反应使得平衡正向移动,适当升温会使平衡逆向移动,放热越小的反应逆向移动
程度更小,因此可以得到较多的(CH)C=CH,故D正确;故选B。
3 2 2
7.B【分析】菱镁矿煅烧后得到轻烧粉,MgCO 转化为MgO,加入氯化铵溶液浸取,浸
3
出的废渣有SiO、Fe(OH)、Al(OH),同时产生氨气,则此时浸出液中主要含有Mg2+,加入
2 3 3
氨水得到Mg(OH) 沉淀,煅烧得到高纯镁砂。
2
【解析】A.高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根水解产生的氢
离子反应,促进铵根的水解,所以得到氯化镁、氨气和水,化学方程式为
MgO+2NHCl=MgCl+2NH↑+HO,故A正确;B.一水合氨受热易分解,沉镁时在较高温度下进
4 2 3 2
行会造成一水合氨大量分解,挥发出氨气,降低利用率,故B错误;C.浸出过程产生的氨
气可以回收制备氨水,沉镁时氯化镁与氨水反应生成的氯化铵又可以利用到浸出过程中,故
C正确;D.Fe(OH)、Al(OH) 的K 远小于Mg(OH) 的K,所以当pH达到一定值时Fe3+、Al3+
3 3 sp 2 sp
产生沉淀,而Mg2+不沉淀,从而将其分离,故D正确;故答案为B。
8.C【解析】A.钠的燃烧反应在坩埚中进行,A错误;B.用装置②制备溴苯,但验证
有HBr产生过程中挥发的溴是干扰,B错误;C.氯化镁晶体在蒸干过程中镁离子易水解生
成挥发性酸需在氯化氢氛围下进行,故可以用装置③制备无水MgCl,C正确;D.铁片上镀
2
铜,铁应连接电源的负极作阴极受保护,D错误;故选C。
9.B【解析】A.BHET中含C、H、O三种元素,其电负性为:OCH,A项正确;
B.PET中含有成单键的碳原子,所有原子不可能处于同一平面,B项错误;C.
中碳原子和氧原子的杂化方式均为sp3,C项正确;PET、BHET中均含有酯基和苯环,均
能发生水解反应和加成反应,D项正确;故选B。
10.D【解析】A.溴易溶于CCl,不能用萃取、分液法分离Br 和CCl 混合物,分离
4 2 4
Br 和CCl 的混合物需要蒸馏, A错误;B.检验淀粉是否水解,需检测反应液中是否生成
2 4
葡萄糖,应在碱性环境下进行,而淀粉的稀硫酸溶液呈酸性,不能直接完成银镜反应、应先
用氢氧化钠溶液中和反应液后再进行银镜反应实验,B错误;C.澄清石灰水与碳酸钠、碳
酸氢钠均反应产生白色沉淀碳酸钙,不能鉴别,C错误;D.KMnO 溶液和0.1000molL1草
4
酸溶液能发生氧化还原反应,利用氧化还原滴定原理,可以用KMnO 溶液滴定
4
0.1000molL1草酸溶液,KMnO 溶液具有腐蚀性用酸式滴定管盛放、高锰酸钾本身有色,
4
不需要其它指示剂,故仪器与试剂均是正确的,D正确,答案选D。
11.A【分析】某有机化合物由原子序数依次增大的短周期主族元素W、X、Y、Z组成,
Y、Z同主族且Z的原子序数是Y的2倍,Y为O元素、Z为S元素,有机物含C,则X为C,
W为H,碎片离子为CHOS+。
7 7
【解析】A.电负性:O>S>C>H,A正确;B.C的氢化物有多种,C数越多沸点越高,
B错误;C.二氧化碳分子中碳原子的价层电子对数为2、孤对电子对数为0,则分子的空间
结构为直线形;二氧化硫分子中硫原子的价层电子对数都为2、孤对电子对数都为1,分子
的空间结构为V形;CS 分子中,以C为中心,价层电子对数为2、孤对电子对数为0,则分
2
子的空间结构为直线形,C错误;D.过氧化氢溶液与氢硫酸溶液反应生成硫沉淀和水,则
过氧化氢溶液与氢硫酸溶液混合有明显实验现象,D错误;故选A。
12.C【解析】A.观察给出的晶胞可知,镁原子位于硅原子所构成的正四面体空隙中,
空隙填充率为100%,A错误;B.与硅原子等距且最近的镁原子数为8,故晶体中硅原子配
化学(一中)答案 (第 2 页,共 7 页)
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}2
位数为8,B错误;C.最近的硅原子之间的距离为晶胞面对角线的一半,其距离为 rnm,
2
476
C正确;D.该晶体的化学式为MgSi,该晶胞包含4个MgSi,该晶胞的质量为 g,晶
2 2 N
A
476 304
胞的体积为(r×10-7)3cm3,故晶体的密度为 g/cm3 g/cm3 ,D错误;
N (r10-7)3 N (r10-7)3
A A
故答案为:C。
13.C【分析】收集废热时,KNi[Fe(CN)]的一极为阳极,电极反应为KNi[Fe(CN)]-e-=
2 6 2 6
KNi[Fe(CN)]+K+,AgCl-极为阴极,电极反应为AgCl+e-=Ag+Cl-。低温工作时,Ag电极为负
6
极,电极反应为Ag-e-+Cl-=AgCl,KNi[Fe(CN)]电极为正极,电极反应为KNi[Fe(CN)]+e-+K+=
6 6
KNi[Fe(CN)]。
2 6
【解析】A.收集废热时,阴极电极反应为AgCl+e-=Ag+Cl-,AgCl转化为Ag和Cl-,阴
极上附着的 AgCl 减少,A 正确;B.收集废热时,阳极电极反应式为 KNi[Fe(CN)]-e-=
2 6
KNi[Fe(CN)]+K+,B正确;C.低温工作时,Ag电极为负极,电解质溶液中的阳离子向正极
6
移动,K+通过多孔隔膜移向KNi[Fe(CN)]电极,C错误;D.低温工作时,负极上Ag-e-+Cl-=AgCl,
6
Ag电极增重7.1g,说明有0.2molCl-参与反应,则理论上外电路中转移电子为0.2mol,D
正确;故答案选C。
14.D【解析】A.a~b段:Cu(OH) (s) Cu2(aq) 2OH(aq),随pH升高,c(OH-)
2
增大,平衡逆向移动,上层清液的含量减小,选项A正确;B.b~c段:
Cu(OH)
2
4NH
3
H
2
O
CuNH
3
4
2 2OH4H
2
O,随着c(OH-)增大,NH+
4
与OH-结合
生成NH·HO,c(NH·HO)增大,发生上述反应,使上层清液中铜元素的含量增大,选项B
3 2 3 2
正确;C.c-d段:随pH升高,使Cu(OH)
2
4NH
3
H
2
O
CuNH
3
4
2 2OH4H
2
O平
衡逆向移动,再次出现Cu(OH) 沉淀,选项C正确;D.d点以后,随pH升高,可能发生
2
Cu(OH)
2
2OH
CuNH
3
4
2 ,则上层清液中铜元素含量可能上升,选项D错误;答
案选D。
二、非选择题(本题共4小题,共58分)
15.(14分)
(1)长颈漏斗(1分) 防止倒吸(1分)
(2)SO +H O +Ba2+=BaSO +2H+(2分)
2 2 2 4
(3)冷凝作用(1分) 偏小(1分)
(4)取最后一次洗涤液少许于试管中,滴加稀HNO 酸化的AgNO 溶液,若无白色沉
3 3
淀产生,证明沉淀已洗涤干净(2分)
用浓HNO 代替H O ,反应过程中会产生有毒的氮氧化物,污染空气(2分)
3 2 2
(5)硫氰化钾溶液(1分) 红色(1分)
600~700°C
4FeS +25O = 6Fe O +16SO (2分)
3 4 2 2 3 2
【分析】利用氧气将管式炉中的样品在高温下煅烧反应,生成的气体通过足量的氯化钡和双
氧水反应,所得固体的量进行分析,确定反应的产生,再通过管式炉中固体的变化判断固体
产物;
【解析】
(1)根据仪器的构造可知,仪器N的名称是长颈漏斗,其作用是防止倒吸;
(2)管式炉中产生的气体能使品红溶液褪色,产生的气体是SO ,三颈烧瓶中发生反应的
2
离子方程式为SO +H O +Ba2+=BaSO +2H+;
2 2 2 4
化学(一中)答案 (第 3 页,共 7 页)
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}(3)长玻璃管M除了导气外还有冷凝作用,若没有长玻璃管,通入三颈烧瓶中的SO 温度
2
过高,可能来不及与H O 和BaCl 反应就排出去,造成测定的y值偏小;
2 2 2
(4)检验沉淀已洗涤干净的方法是:取最后一次洗涤液少许于试管中,滴加稀HNO 酸化
3
的AgNO 溶液,若无白色沉淀产生,证明沉淀已洗涤干净,用浓HNO 代替H O ,反应过
3 3 2 2
程中会产生有毒的氮氧化物,污染空气;
(5)充分反应后,取管式炉中固体溶于足量的稀硫酸中,取少量反应后的溶液,加入KSCN
(硫氰化钾)溶液,溶液变红色证明含有Fe3+,加入K [Fe(CN) ]溶液没有明显变化,证
3 6
明无Fe2+,则管式炉中固体颜色是红色(生成Fe O ),S~SO ~BaSO ,试样中n(Fe):n
2 3 2 4
2.96g-1.28g 9.32g
(S)= : 3:4(1.28g是S元素质量),化学式为Fe S ,管式炉中发
3 4
56g/mol 233g/mol
600~700°C
生反应的化学方程式为4FeS +25O = 6Fe O +16SO 。
3 4 2 2 3 2
16.(14分)
(1)两性氧化物 In(OH) OH=InO2H O
3 2 2
(2)增大 减小
(3)2In3H O 6CH COOH2CH COO In6H O
2 2 3 3 3 2
(4)2In33Zn3Zn22In 2:1
【分析】ITO靶材废料(主要由In O 、SnO 组成)用H SO 处理,In O 与硫酸反应产生In (SO )
2 3 2 2 4 2 3 2 4 3
进入溶液,而SnO 有少量反应产生Sn(SO ) 进入溶液,大部分仍以固体形式存在,过滤后
2 4 2
除去固体SnO ,向滤液中加入Zn粉,发生反应Sn4++2Zn=Sn+2Zn2+,将反应产生的Sn过
2
滤除去,向滤液中加入Zn粉,发生置换反应:3Zn+2In3+=3Zn2++2In,由于Zn过量,所以
过滤,除去滤液,得到的滤渣中含有Zn、In,向滤渣中加入双氧水和醋酸进行酸溶,经一
系列处理后得到醋酸铟;
【解析】
(1)已知In O 和Cs O可反应生成偏铟酸铯(CsInO ),也可以与CrO 反应生成InCrO ,即
2 3 2 2 2 3 3
既能与酸反应生成盐和水,也能与碱反应生成盐和水,据此判断In O 属于两性氧化物;
2 3
In(OH) 与NaOH反应生成NaInO 和水,反应的离子方程式为:
3 2
In(OH) OH=InO2H O;
3 2 2
(2)由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而增大,温度越高,
硫酸浓度对铟的浸出率影响减小,故答案为:增大;减小;
(3)酸溶时无气泡产生,则酸溶时铟在双氧水、醋酸的作用下反应生成醋酸铟和水,发生
反应的化学方程式为;2In3H O 6CH COOH2CH COO In6H O ;
2 2 3 3 3 2
1 1
(4)在Oa段发生反应:Sn4++2Zn=Sn+2Zn2+,n(Sn4+)= n(Zn)= ×0.02mol=0.01mol,在
2 2
2 2
ab段发生反应:3Zn+2In3+=3Zn2++2In;n(In3+)= n(Zn)= ×(0.08-0.02)mol=0.04mol,溶液
3 3
的体积相同,所以离子浓度比等于它们的物质的量的比,故c(In3+):c(Sn4+)=0.04:0.01=4:
化学(一中)答案 (第 4 页,共 7 页)
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}1;则c[In SO ]:c[SnSO ]=2:1。
2 4 3 4 2
17.(15分)
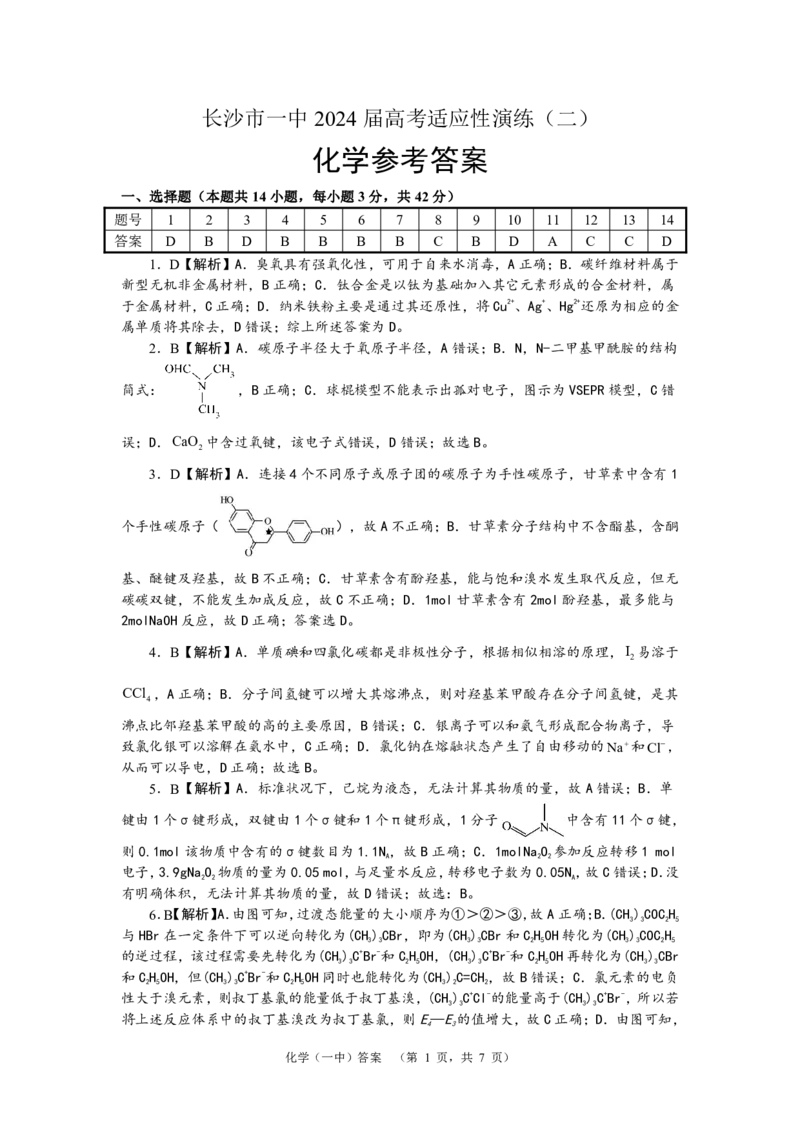
(1)1074.8
(2)CaO与生成物CO 反应,生成物浓度减小,平衡正向移动,氢气的体积分数
2
增大
(3) 0.5
(4)30.0
(5)( )
【解析】
(2)其他条件不变,在体系中投入一定量CaO,CaO与生成物CO 反应生成CaCO ,
2 3
生成物浓度减小,平衡正向移动,氢气的体积分数增大。
(3)由反应可知,反应前后总压不变,所以平衡时总压为p ,H O的分压为p - ×3= ,
0 2 0
A点的坐标为(t, );由图可知,平衡时CO 、H 、CO、H O的平衡分压分别为
2 2 2
,平衡常数K = =0.5。
p
(4)已知 Arrhenius 经验公式为 Rln k=- +C,根据图像可得①63.0=-3.0E +C,
a
②33.0=-4.0E +C,联立方程解得E =30.0,则反应的活化能为30.0kJ·mol-1;使用高效催
a a
化剂,活化能降低。
(5)由a和b的坐标可得c的坐标为( ),由均摊法可知,La为4× +4× +2× +2× =2,
Ni原子位于内部和面心:12× +4=10,N(La)∶N(Ni)=2∶10=1∶5,故化学式为LaNi 。
5
化学(一中)答案 (第 5 页,共 7 页)
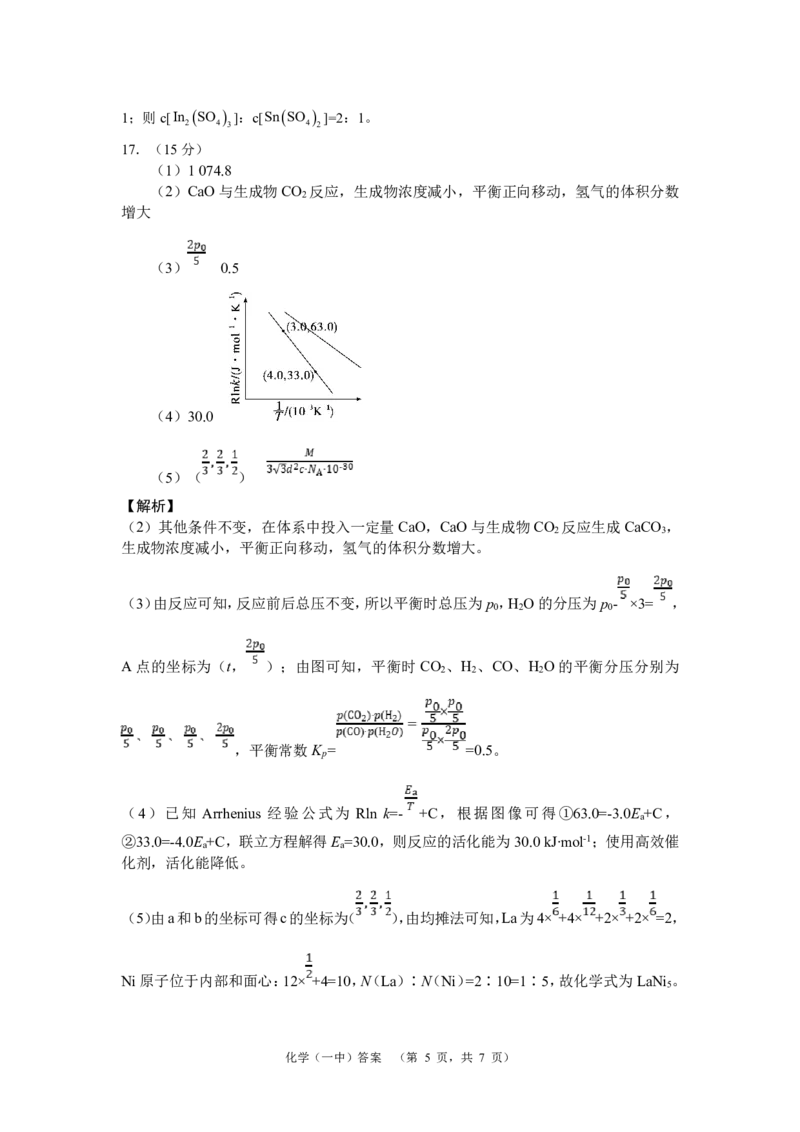
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}X射线衍射测定两晶面间距为dpm,设底面边长为a,则 a=3d,可得a=2 d,底面
积为2 d×3d=6 d2,则晶体的密度为ρ= g·cm-3= g·cm-3。
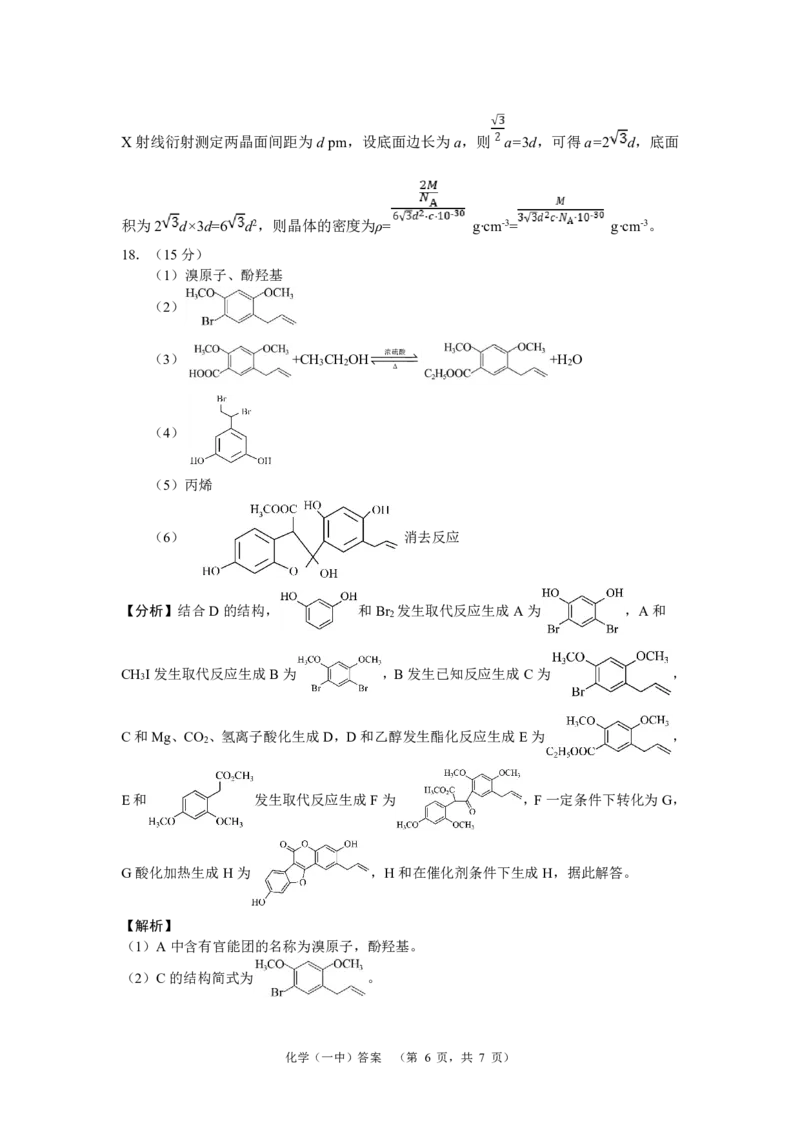
18.(15分)
(1)溴原子、酚羟基
(2)
(3) +CH 3 CH 2 OH 浓硫 酸 +H 2 O
Δ
(4)
(5)丙烯
(6) 消去反应
【分析】结合D的结构, 和Br 发生取代反应生成A为 ,A和
2
CH I发生取代反应生成B为 ,B发生已知反应生成C为 ,
3
C和Mg、CO 、氢离子酸化生成D,D和乙醇发生酯化反应生成E为 ,
2
E和 发生取代反应生成F为 ,F一定条件下转化为G,
G酸化加热生成H为 ,H和在催化剂条件下生成H,据此解答。
【解析】
(1)A中含有官能团的名称为溴原子,酚羟基。
(2)C的结构简式为 。
化学(一中)答案 (第 6 页,共 7 页)
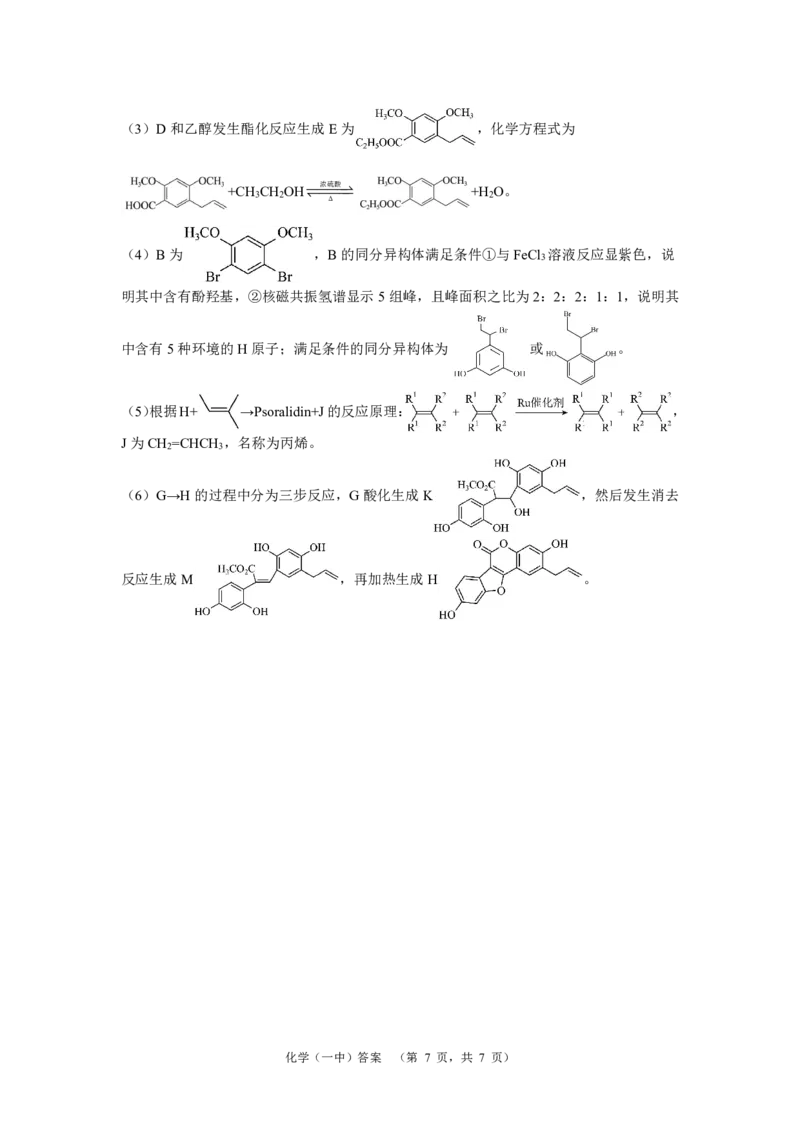
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}(3)D和乙醇发生酯化反应生成E为 ,化学方程式为
+CH 3 CH 2 OH 浓硫 酸 +H 2 O。
Δ
(4)B为 ,B的同分异构体满足条件①与FeCl 溶液反应显紫色,说
3
明其中含有酚羟基,②核磁共振氢谱显示5组峰,且峰面积之比为2:2:2:1:1,说明其
中含有5种环境的H原子;满足条件的同分异构体为 或 。
(5)根据H+ →Psoralidin+J的反应原理: ,
J为CH =CHCH ,名称为丙烯。
2 3
(6)G→H的过程中分为三步反应,G酸化生成K ,然后发生消去
反应生成M ,再加热生成H 。
化学(一中)答案 (第 7 页,共 7 页)
{#{QQABYYiAogCAAoBAARhCEQEACgMQkBGACAoGAAAAoAAASBFABCA=}#}