文档内容
人教版(2019)必修第二册第七章第二节 乙烯与有机高分子材
料课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
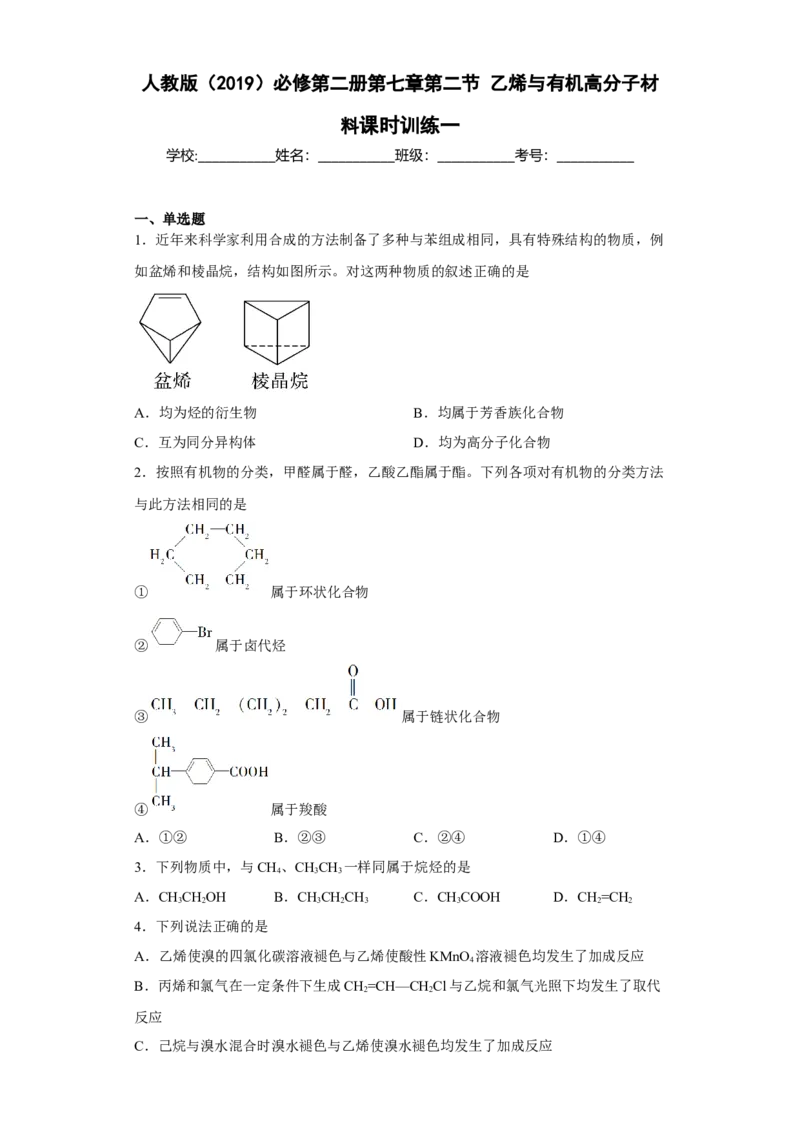
1.近年来科学家利用合成的方法制备了多种与苯组成相同,具有特殊结构的物质,例
如盆烯和棱晶烷,结构如图所示。对这两种物质的叙述正确的是
A.均为烃的衍生物 B.均属于芳香族化合物
C.互为同分异构体 D.均为高分子化合物
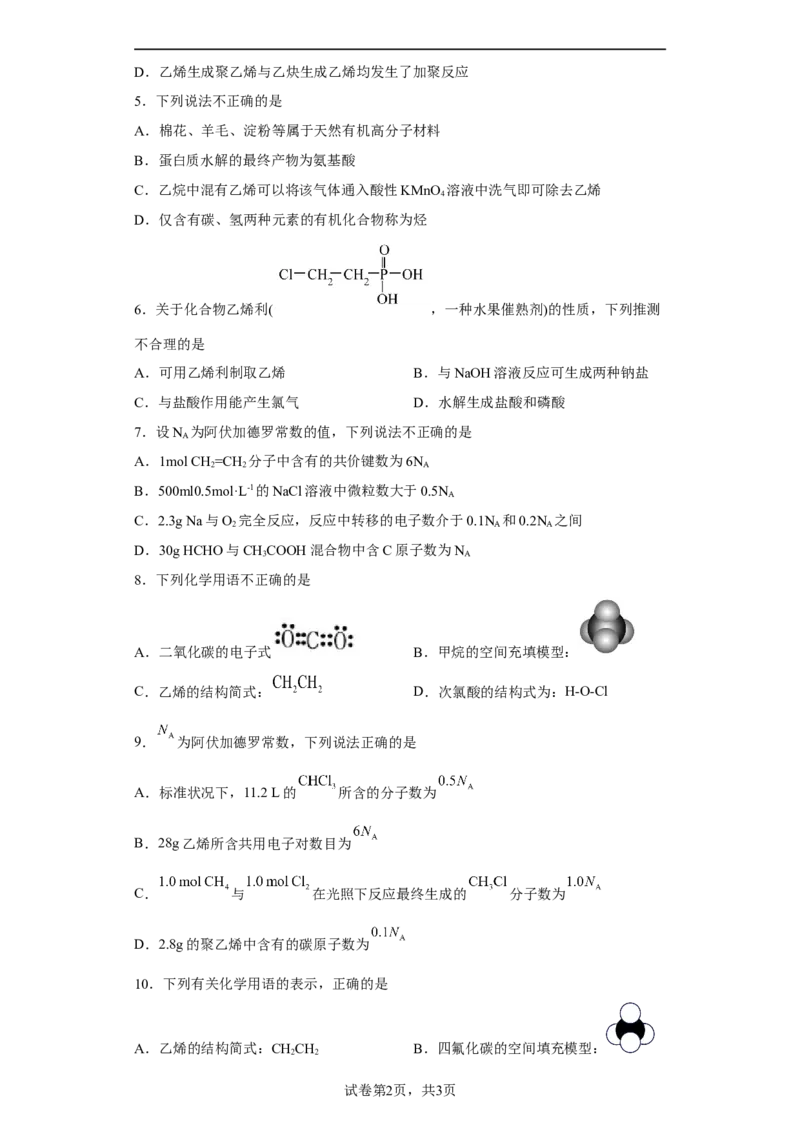
2.按照有机物的分类,甲醛属于醛,乙酸乙酯属于酯。下列各项对有机物的分类方法
与此方法相同的是
① 属于环状化合物
② 属于卤代烃
③ 属于链状化合物
④ 属于羧酸
A.①② B.②③ C.②④ D.①④
3.下列物质中,与CH、CHCH 一样同属于烷烃的是
4 3 3
A.CHCHOH B.CHCHCH C.CHCOOH D.CH=CH
3 2 3 2 3 3 2 2
4.下列说法正确的是
A.乙烯使溴的四氯化碳溶液褪色与乙烯使酸性KMnO 溶液褪色均发生了加成反应
4
B.丙烯和氯气在一定条件下生成CH=CH—CHCl与乙烷和氯气光照下均发生了取代
2 2
反应
C.己烷与溴水混合时溴水褪色与乙烯使溴水褪色均发生了加成反应D.乙烯生成聚乙烯与乙炔生成乙烯均发生了加聚反应
5.下列说法不正确的是
A.棉花、羊毛、淀粉等属于天然有机高分子材料
B.蛋白质水解的最终产物为氨基酸
C.乙烷中混有乙烯可以将该气体通入酸性KMnO 溶液中洗气即可除去乙烯
4
D.仅含有碳、氢两种元素的有机化合物称为烃
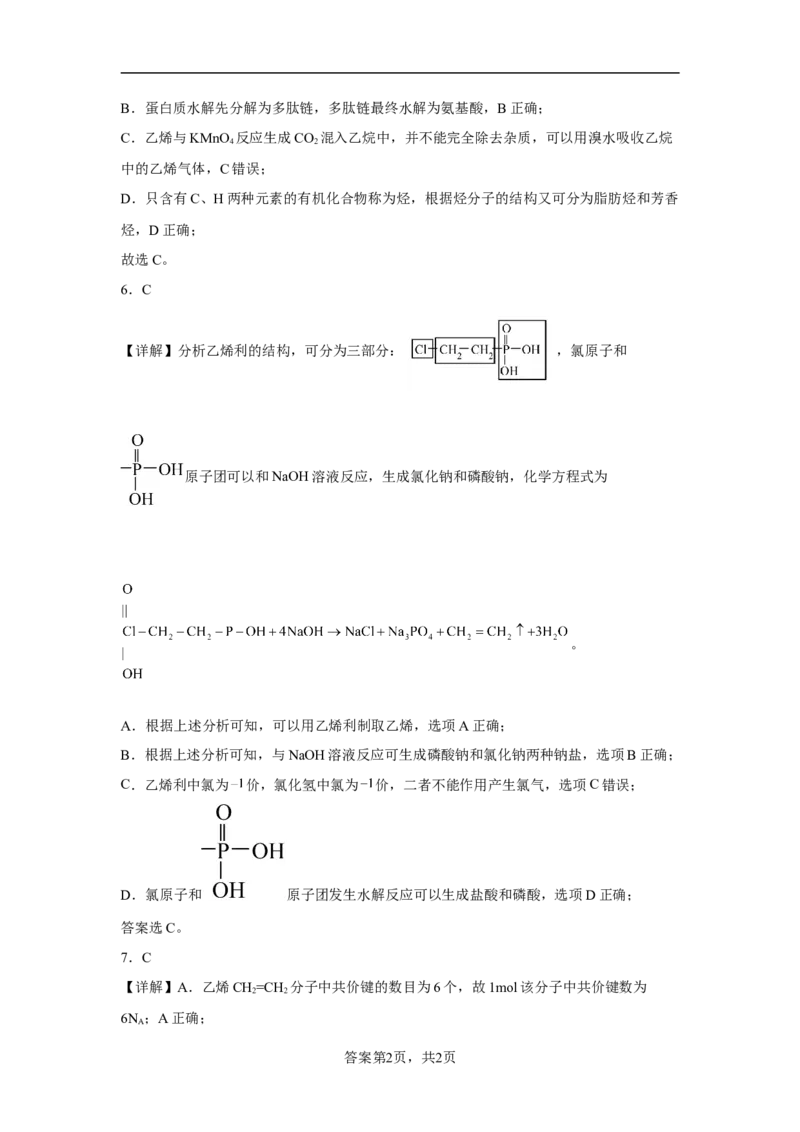
6.关于化合物乙烯利( ,一种水果催熟剂)的性质,下列推测
不合理的是
A.可用乙烯利制取乙烯 B.与NaOH溶液反应可生成两种钠盐
C.与盐酸作用能产生氯气 D.水解生成盐酸和磷酸
7.设N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.1mol CH=CH 分子中含有的共价键数为6N
2 2 A
B.500ml0.5mol·L-1的NaCl溶液中微粒数大于0.5N
A
C.2.3g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N 之间
2 A A
D.30g HCHO与CHCOOH混合物中含C原子数为N
3 A
8.下列化学用语不正确的是
A.二氧化碳的电子式 B.甲烷的空间充填模型:
C.乙烯的结构简式: D.次氯酸的结构式为:H-O-Cl
9. 为阿伏加德罗常数,下列说法正确的是
A.标准状况下,11.2 L的 所含的分子数为
B.28g乙烯所含共用电子对数目为
C. 与 在光照下反应最终生成的 分子数为
D.2.8g的聚乙烯中含有的碳原子数为
10.下列有关化学用语的表示,正确的是
A.乙烯的结构简式:CHCH B.四氟化碳的空间填充模型:
2 2
试卷第2页,共3页C.聚丙烯的结构简式: D.羟基的电子式:
11.以 表示阿伏加德罗常数的值。下列叙述中正确的是
A.常温常压下,11.2L的甲烷气体含有分子数为0.5
B.14g乙烯和环丙烷的混合物中总原子数为3
C.0.2mol/L的氢氧化钠溶液中含钠离子数为0.2
D.5.6g铁与足量的稀硫酸反应失去电子数为0.3
12.乙烯可作水果催熟剂。下列有关乙烯的说法正确的是
A.常温常压下为无色液体 B.易溶于水
C.能使酸性KMnO 溶液褪色 D.分子中C、H元素的质量之比为1∶2
4
13.下列除去物质中混有少量杂质的方法正确的是
选
物质 杂质 方法
项
A NaCO(s) NaHCO (s) 将固体混合物加热至恒重
2 3 3
B NaO(s) NaOH(s) 通入足量的CO 气体
2 2 2
C CO(g) HCl(g) 通过盛有足量的饱和NaCO 溶液的洗气瓶
2 2 3
D CH(g) C H(g) 依次通过盛有酸性KMnO 溶液、浓硫酸的洗气瓶
4 2 4 4
A.A B.B C.C D.D
14.下列方法中不能用来鉴别乙烯和乙烷的
A.在空气中燃烧 B.分别通入酸性高锰酸钾溶液中
C.分别通入溴水中 D.把燃烧后的产物分别通入澄清的石灰
水中
二、多选题
15.除去下列物质中所含少量杂质(括号内为杂质),所选试剂和方法均正确的是A.溴苯(Br)溶液:加 溶液,分液
2
B.甲烷(C H):酸性 溶液,洗气
2 4
C.乙醛(HCOOH):新制 ,蒸馏
D.氯化亚铁溶液(FeCl ),铁粉,过滤
3
三、填空题
16.乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。
请回答下列问题。
(1)乙烯的电子式为_____。
(2)鉴别甲烷和乙烯的试剂是_____(填字母)。
A.稀硫酸 B.溴的四氯化碳溶液C.水 D.酸性高锰酸钾
溶液
(3)下列物质中,一定条件下,可以通过乙烯加成反应得到的是_____(填字母)。
A.CHCH B.CHCHCl C.CHCHOH D.CHCHBr
3 3 3 2 3 2 3 2
(4)乙烯使溴的四氯化碳溶液褪色的化学方程式为_____,反应类型是_____。
17.乙烯的产量是衡量一个国家石油化工发展水平的标志,它的分子结构模型如图所
示。乙烯也是一种常用的果实催熟剂。鲜花在切下之后,很容易枯萎,这是由于植物
的茎叶被损伤后释放出乙烯的缘故。
(1)请写出乙烯的结构式:_______。
(2)工业上可用乙烯与水反应来生产工业酒精,该反应的化学方程式为_______(不要求
写反应条件),该有机反应的类型是_______反应。
(3)甲烷和乙烯都是无色气体,请写出一种能够鉴别两者的试剂:_______。
(4)乙烯在适宜的温度、压强和有催化剂存在的条件下,能生成高分子化合物
_______(填名称),该反应的类型是_______。
18.回答下列问题:
(1)2022年3月13日,永恒的“微火”在万众瞩目中缓缓熄灭,为北京冬奥画上圆满的
句号。北京作为双奥之城为世界奉献了一届简约、精彩、卓越的冬奥盛会。
①“微火”不微,照亮世界。奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材
料制成,能经受住1200℃的高温。“飞扬”火炬外壳属于____(填“金属材料”“有机
试卷第4页,共3页高分子材料”“复合材料”之一)。
②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切
割,它由聚乙烯(化学式为 )、聚氨基甲酸酯等化学纤维复合而成。在聚
乙烯中,碳元素和氢元素的质量比为_____(填最简整数比)。
③“氢”车上阵,助力绿色冬奥。氢氧燃料电池就像冬奥大巴车的“心脏”,在这种
电池中,氢气和氧气通过化学反应生成水。下列有关说法中,不合理的是____(填选项
序号之一)。
A.H 和O 发生了氧化还原反应
2 2
B.该种电池的应用有利于环保
C.该电池的使用过程中,电能转化为化学能
(2)我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。其生
产过程中有下列反应:
NaCl+NH +CO +H O=NaHCO +NHC1
3 2 2 3 4
2NaHCO NaCO+CO ↑+H O
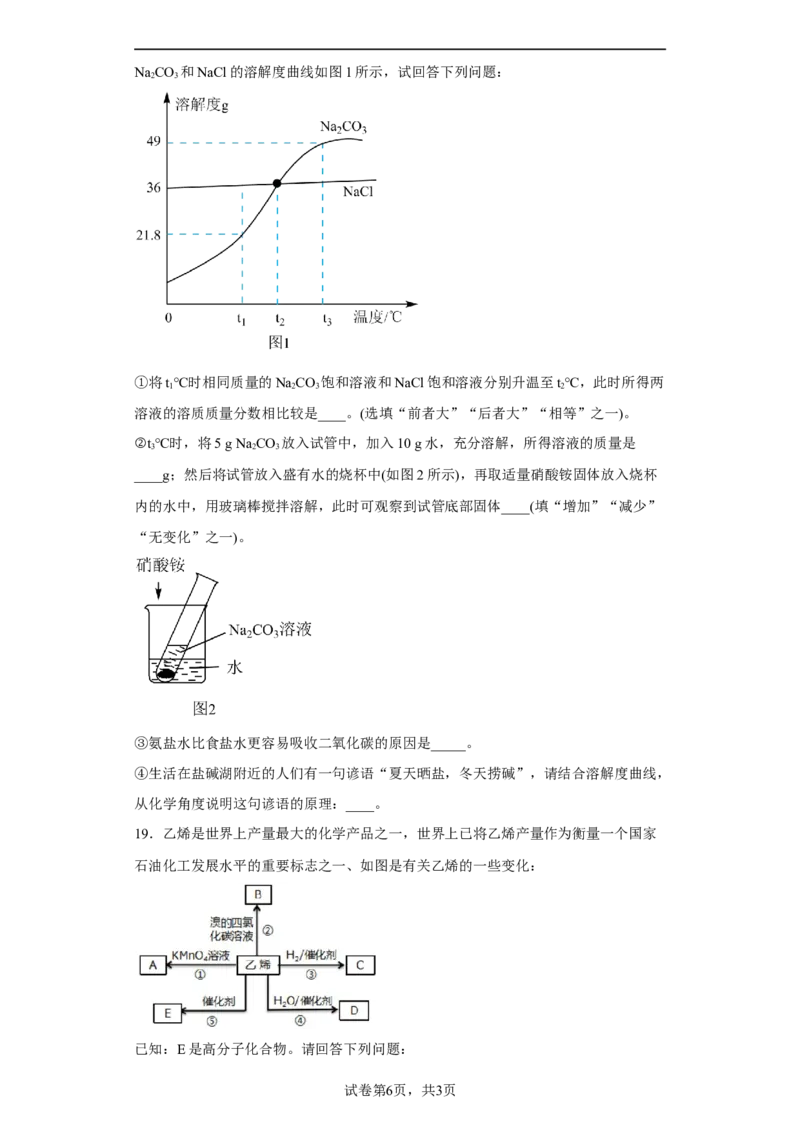
3 2 3 2 2NaCO 和NaCl的溶解度曲线如图1所示,试回答下列问题:
2 3
①将t℃时相同质量的NaCO 饱和溶液和NaCl饱和溶液分别升温至t℃,此时所得两
1 2 3 2
溶液的溶质质量分数相比较是____。(选填“前者大”“后者大”“相等”之一)。
②t ℃时,将5 g Na CO 放入试管中,加入10 g水,充分溶解,所得溶液的质量是
3 2 3
____g;然后将试管放入盛有水的烧杯中(如图2所示),再取适量硝酸铵固体放入烧杯
内的水中,用玻璃棒搅拌溶解,此时可观察到试管底部固体____(填“增加”“减少”
“无变化”之一)。
③氨盐水比食盐水更容易吸收二氧化碳的原因是_____。
④生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,
从化学角度说明这句谚语的原理:____。
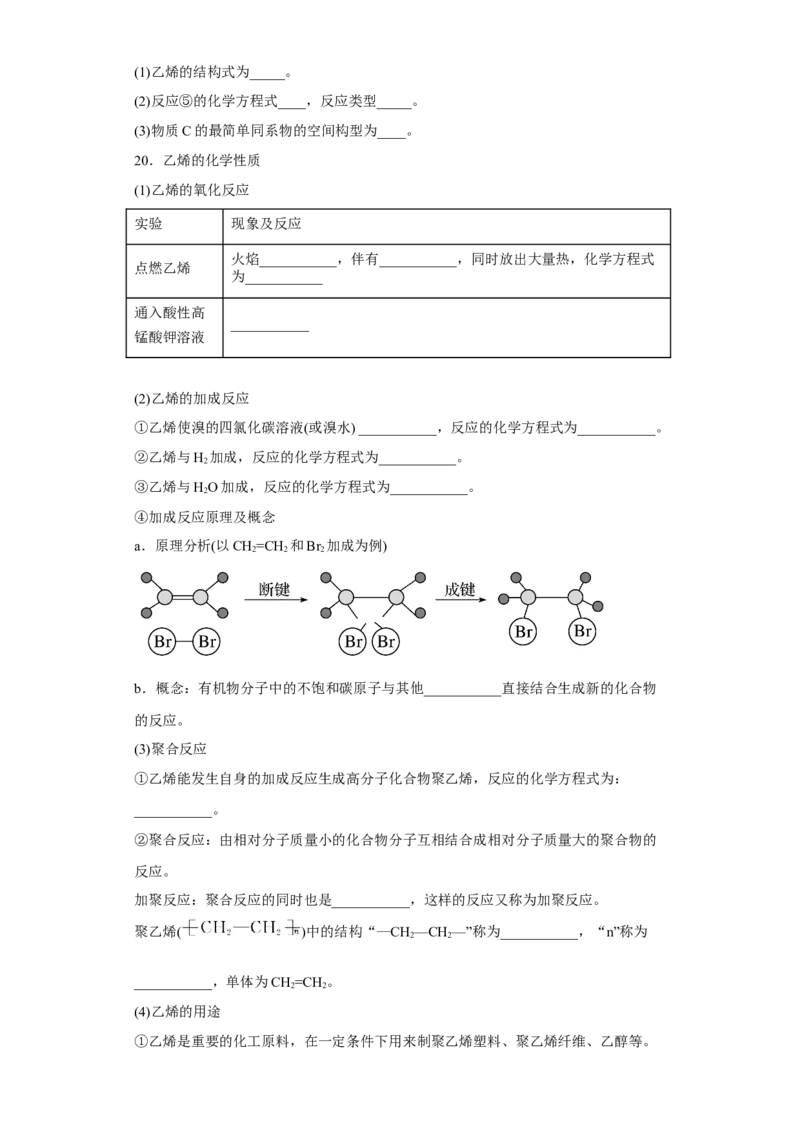
19.乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家
石油化工发展水平的重要标志之一、如图是有关乙烯的一些变化:
已知:E是高分子化合物。请回答下列问题:
试卷第6页,共3页(1)乙烯的结构式为_____。
(2)反应⑤的化学方程式____,反应类型_____。
(3)物质C的最简单同系物的空间构型为____。
20.乙烯的化学性质
(1)乙烯的氧化反应
实验 现象及反应
火焰___________,伴有___________,同时放出大量热,化学方程式
点燃乙烯
为___________
通入酸性高
___________
锰酸钾溶液
(2)乙烯的加成反应
①乙烯使溴的四氯化碳溶液(或溴水) ___________,反应的化学方程式为___________。
②乙烯与H 加成,反应的化学方程式为___________。
2
③乙烯与HO加成,反应的化学方程式为___________。
2
④加成反应原理及概念
a.原理分析(以CH=CH 和Br 加成为例)
2 2 2
b.概念:有机物分子中的不饱和碳原子与其他___________直接结合生成新的化合物
的反应。
(3)聚合反应
①乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为:
___________。
②聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的
反应。
加聚反应:聚合反应的同时也是___________,这样的反应又称为加聚反应。
聚乙烯( )中的结构“—CH—CH—”称为___________,“n”称为
2 2
___________,单体为CH=CH 。
2 2
(4)乙烯的用途
①乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。乙烯的产量可以用来衡量一个国家的石油化工发展水平。
②在农业生产中用作___________。
四、实验题
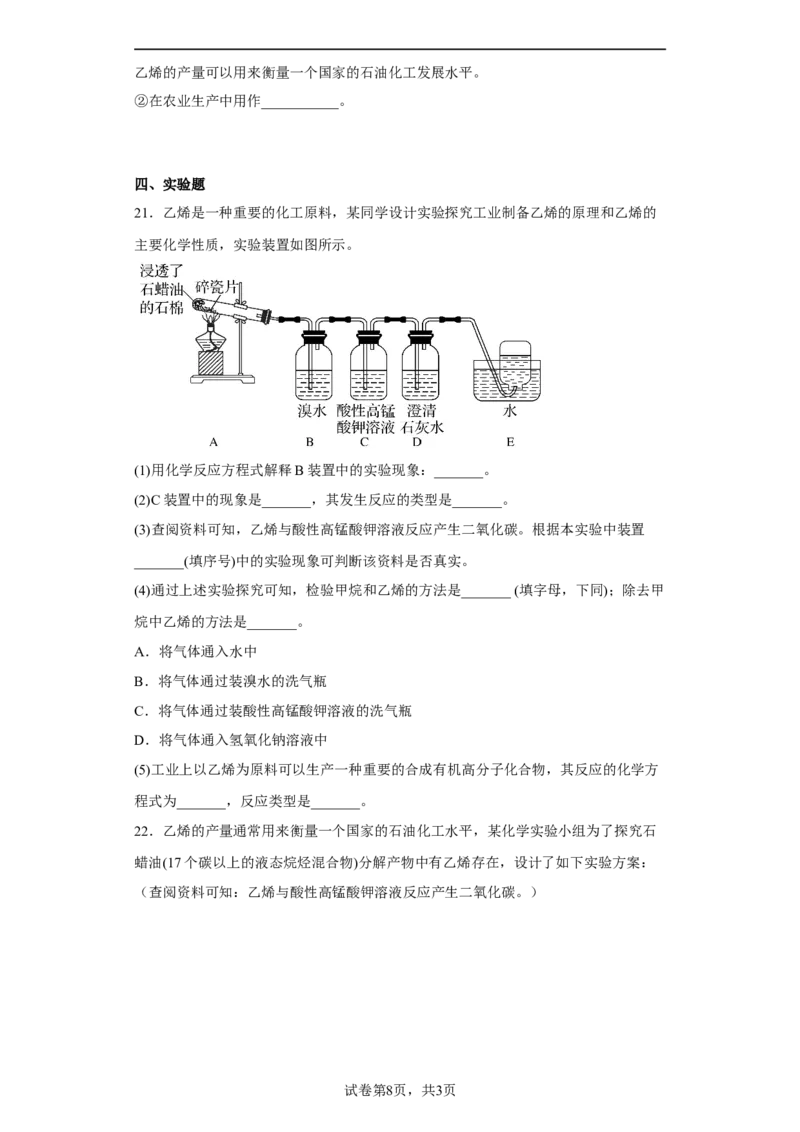
21.乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的
主要化学性质,实验装置如图所示。
(1)用化学反应方程式解释B装置中的实验现象:_______。
(2)C装置中的现象是_______,其发生反应的类型是_______。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置
_______(填序号)中的实验现象可判断该资料是否真实。
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是_______ (填字母,下同);除去甲
烷中乙烯的方法是_______。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
(5)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方
程式为_______,反应类型是_______。
22.乙烯的产量通常用来衡量一个国家的石油化工水平,某化学实验小组为了探究石
蜡油(17个碳以上的液态烷烃混合物)分解产物中有乙烯存在,设计了如下实验方案:
(查阅资料可知:乙烯与酸性高锰酸钾溶液反应产生二氧化碳。)
试卷第8页,共3页(1)乙烯的结构式是___。
(2)B中实验现象:___。
(3)C中发生反应的化学方程式:__,反应类型:___。
(4)通过上述实验探究可知,除去乙烷中混有的乙烯,可以选择的试剂是___。
A.水 B.溴水
C.氢氧化钠溶液 D.酸性高锰酸钾溶液
(5)关于乙烯,下列说法中不正确的是___。
A.聚乙烯塑料可以用做食品包装袋
B.乙烯在一定条件下可以和水反应制乙醇
C.乙烯分子中所有原子不共面
D.乙烯是一种植物生长调节剂,可以延长果实和花朵的成熟期参考答案:
1.C
【详解】A.盆烯和棱晶烷只含C、H两种元素,均为烃,故A错误;
B.盆烯和棱晶烷不含苯环,不是芳香族化合物,故B错误;
C.盆烯和棱晶烷分子式都是C H,但结构不同,互为同分异构体,故C正确;
6 6
D.盆烯和棱晶烷相对分子质量小,不是高分子化合物,故D错误;
选C。
2.C
【详解】甲醛属于醛,乙酸乙酯属于酯,均是按照有机物中所含官能团进行分类
①是根据碳骨架进行的分类,分成链状化合物和环状化合物,①不符合题意;
②因为含有-Br,因此此有机物属于卤代烃,②符合题意;
③根据碳骨架进行分类,③不符合题意;
④含有羧基,属于羧酸,按照官能团进行分类,④符合题意;
综上,②④符合题意,答案选C。
3.B
【详解】A.CHCHOH的名称是乙醇,它属于醇类,不属于烷烃,A不符合题意;
3 2
B.CHCHCH 的名称是丙烷,与甲烷、乙烷一样,都属于烷烃,B符合题意;
3 2 3
C.CHCOOH的名称是乙酸,属于羧酸类,不属于烷烃类,C不符合题意;
3
D.CH=CH 的名称为乙烯,属于烯烃类,不属于烷烃类,D不符合题意;
2 2
故选B。
4.B
【详解】A.乙烯使溴的四氯化碳溶液褪色发生了加成反应,乙烯使酸性KMnO 溶液褪色
4
是KMnO 被还原了,A错误;
4
B.丙烯和氯气在一定条件下生成CH=CH—CHCl,是丙烯中的甲基上的氢原子被Cl原子
2 2
取代,乙烷和氯气光照下发生取代反应生成CHCHCl,二者均是取代反应,B正确;
3 2
C.己烷与溴水混合时溴水褪色是由于溴单质从水中转移到己烷,该过程是萃取,乙烯使
溴水褪色发生了加成反应,生成1,2-二溴乙烷,C错误;
D.乙烯生成聚乙烯是发生加聚反应,乙炔生成乙烯是乙炔与氢气发生加成反应,D错误;
故选B。
5.C
【详解】A.棉花为纤维素,与淀粉均为多糖,属于天然高分子化合物,羊毛为蛋白质,
也属于天然高分子化合物,A正确;B.蛋白质水解先分解为多肽链,多肽链最终水解为氨基酸,B正确;
C.乙烯与KMnO 反应生成CO 混入乙烷中,并不能完全除去杂质,可以用溴水吸收乙烷
4 2
中的乙烯气体,C错误;
D.只含有C、H两种元素的有机化合物称为烃,根据烃分子的结构又可分为脂肪烃和芳香
烃,D正确;
故选C。
6.C
【详解】分析乙烯利的结构,可分为三部分: ,氯原子和
原子团可以和NaOH溶液反应,生成氯化钠和磷酸钠,化学方程式为
。
A.根据上述分析可知,可以用乙烯利制取乙烯,选项A正确;
B.根据上述分析可知,与NaOH溶液反应可生成磷酸钠和氯化钠两种钠盐,选项B正确;
C.乙烯利中氯为 价,氯化氢中氯为 价,二者不能作用产生氯气,选项C错误;
D.氯原子和 原子团发生水解反应可以生成盐酸和磷酸,选项D正确;
答案选C。
7.C
【详解】A.乙烯CH=CH 分子中共价键的数目为6个,故1mol该分子中共价键数为
2 2
6N ;A正确;
A
答案第2页,共2页B.500ml0.5mol·L-1的NaCl的物质的量为n=cV=0.25mol,含钠离子和氯离子,则离子微粒
数为0.5N ,但溶液中还有氢离子和氢氧根离子,则溶液中微粒数大于0.5N ,B正确;
A A
C.2.3g Na的物质的量为 ,Na转化为Na+,则转移电子数为
0.1N ,C错误;
A
D.HCHO与CHCOOH的最简式都是CHO,30g混合物的物质的量为
3 2
,含 原子数为N ,D正确;
A
故选C。
8.C
【详解】A.二氧化碳分子碳、氧原子均达到8电子稳定结构,电子式 ,A
正确;
B.甲烷是正四面体形结构,其空间填充模型为: ,B正确;
C.乙烯含有碳碳双键,结构简式为:CH=CH ,C错误;
2 2
D.次氯酸分子中中心原子为氧原子,结构式为:H-O-Cl ,D正确;
答案选C。
9.B
【详解】A.标准状况下,CHCl 呈液态,不能用气体摩尔体积进行计算,A项错误;
3
B.乙烯的结构式为 ,1个乙烯分子中含有6对共用电子,则28 g 乙烯(物质的
量为1 mol)所含共用电子对数目为6N ,B项正确;
A
C.CH 与Cl 反应为可逆反应,且甲烷与氯气反应生成一氯甲烷、二氯甲烷、三氯甲烷、
4 2
四氯化碳等氯代物,所以1.0 mol CH 与1.0 mol Cl 在光照下反应最终生成的CHCl分子数
4 2 3
小于1.0N ,C项错误;
A
D.聚乙烯的链节为 ,2.8g的聚乙烯中含有的碳原子的物质的量为,即2.8g的聚乙烯中含有的碳原子数为0.2N ,D项错误;
A
故选B。
10.B
【详解】A.乙烯的分子式为C H,分子内的碳碳双键不能省略,则结构简式为:
2 4
CH=CH ,A不正确;
2 2
B.四氟化碳的空间填充模型与甲烷相似,都呈正四面体,且C原子半径比Cl原子半径小,
则四氟化碳的空间填充模型为: ,B正确;
C.丙烯CH=CH-CH 加聚生成聚丙烯,其结构简式为: ,C不正确;
2 3
D.羟基的化学式为∙OH,其电子式为 ,D不正确;
故选B。
11.B
【详解】A.不是标准状况,无法计算,A错误;
B.乙烯和丙烯的最简式均为CH,所以14g乙烯和丙烯的混合物可以看作是14gCH,
2 2
14gCH 为1mol,原子总数为3N ,B正确;
2 A
C.无体积,所以无法计算,C错误;
D.铁与硫酸反应失去2个电子,所以5.6g铁失去电子数为0.2 N ,D错误;
A
故答案为:B。
12.C
【详解】A. 乙烯常温常压下为无色气体,故A错误;
B. 乙烯是有机物,难溶于水,故B错误
C. 乙烯含有碳碳双键,能被酸性KMnO 溶液氧化,则能使酸性KMnO 溶液褪色,故C
4 4
正确;
D. 乙烯的分子式为C H,故分子中C、H元素的物质的量之比为1∶2,, 质量之比不是
2 4
1∶2,故D错误;
答案第4页,共2页故选C。
13.A
【详解】A. 加热至恒重后NaHCO 转化为NaCO,达到除杂目的,故A正确;
3 2 3
B. 通入CO 气体后,NaO 和NaOH都会反应,故B错误;
2 2 2
C. CO 可以和NaCO 反应,故C错误;
2 2 3
D. C H(g)与酸性KMnO 溶液反应生成CO,又引入新杂质故D错误;
2 4 4 2
故答案为A。
14.D
【分析】乙烯中含有碳碳双键,可以发生加成、氧化反应;
【详解】A.在空气中燃烧,有黑烟生成的是乙烯,可以鉴别两种气体,不符合题意,A
项错误;
B.使酸性高锰酸钾溶液褪色的是乙烯,可以鉴别两种气体,不符合题意,B项错误;
C.使溴水褪色的是乙烯,可以鉴别两种气体,不符合题意,C项错误;
D.二者燃烧后的产物均有二氧化碳,分别通入澄清的石灰水中均有白色沉淀生成,无法
鉴别两种气体,D项正确;
答案选D。
15.AD
【详解】A.溴苯(Br)溶液:加 溶液, 与 反应生成可溶于水的钠盐溶液,
2
再用分液方法分离,A正确;
B.酸性 溶液将 氧化,生成 ,在甲烷气体中引入新的杂质,B错误;
C.乙醛和 都能与新制 反应,不能用新制 反应除去乙醛中的
,C错误;
D.氯化亚铁溶液(FeCl ),加入铁粉,发生反应: ,过滤除去多余的铁
3
粉,D正确;
故选A D。
16.(1)
(2)BD
(3)ACD(4) CH=CH +Br →CHBrCHBr 加成反应
2 2 2 2 2
【详解】(1)乙烯的分子式为C H,含有碳碳双键,乙烯的电子式为 ;
2 4
(2)乙烯能与溴的四氯化碳发生加成反应,使溴的四氯化碳褪色,乙烯能被高锰酸钾氧化
而使高锰酸钾溶液褪色,甲烷不能,故可以用溴的四氯化碳和酸性高锰酸钾鉴别甲烷和乙
烯;
(3)乙烯能和 发生加成反应生成 ,乙烯能与 发生加成反应生成
,能与 发生加成反应生成 ,故选ACD;
(4)乙烯与溴的四氯化碳发生加成反应而使溶液褪色,化学方程式为:
,反应类型为:加成反应。
17.(1)
(2) CH=CH +H O C HOH 加成
2 2 2 2 5
(3)溴水(或酸性 溶液、溴的 溶液等其他合理答案)
(4) 聚乙烯 加聚反应
【解析】(1)
乙烯化学式为C H,分子中含有碳碳双键,结构式: ;
2 4
(2)
乙烯与水发生加成反应生成乙醇,CH=CH +H O C HOH;反应为加成反应;
2 2 2 2 5
(3)
甲烷不含碳碳双键;,乙烯含有碳碳双键能和溴发生加成反应,使溴水褪色(也能被酸性
高锰酸钾氧化而使高锰酸钾溶液褪色);故可以选择溴水(或酸性 溶液、溴的
答案第6页,共2页溶液等其他合理答案);
(4)
乙烯含有碳碳双键乙烯在适宜的温度、压强和有催化剂存在的条件下,能发生加聚反应生
成高分子化合物聚乙烯: ,该反应的类型是加聚反应。
18.(1) 复合材料 6:1 C
(2) 后者大 14.9 增加 氨盐水显碱性,更容易吸收酸性气体二氧化
碳 氯化钠的溶解度受温度的影响不大,碳酸钠的溶解度受温度的影响较大,温度
越高溶解度越大。夏天温度升高。水分蒸发,所以碳酸钠不易析出而氯化钠容易析出;冬
天温度降低,碳酸钠溶解度减小,所以从溶液中析出
【解析】(1)
一奥运火炬“飞扬”的外壳是由聚硅氮烷树脂和碳纤维材料制成,聚硅氮烷树脂是有机合
成材料,碳纤维材料是无机非金属材料,因此该材料属于复合材料;
②科技“战衣”,助力中国速度。短道速滑“战衣”所用面料能承受碰撞中冰刀的切割,
它由聚乙烯(化学式为 )、聚氨基甲酸酯等化学纤维复合而成。在聚乙烯中,
C、H原子个数比=2:4=1:2,则碳元素和氢元素的质量比为m(C):m(H)=12:2=6:1;
③A.H 和O 发生反应产生HO,反应过程中元素化合价发生了变化,因此该反应属于氧
2 2 2
化还原反应,A正确;
B.该种电池由于反应产物是HO,无污染,HO又是制取燃料H 的原料,因此该电池的
2 2 2
反应的应用有利于环保,B正确;
C.该电池的使用过程中,化学能转化为电能,C错误;
故合理选项是C;
(2)
①t℃时氯化钠的溶解度大于碳酸钠,因此饱和溶液中氯化钠质量分数大于碳酸钠,将相同
1
质量的NaCO 饱和溶液和NaCl饱和溶液均升温至t℃,都变成不饱和溶液,但是质量分
2 3 2
数都不变,此时,NaCO 溶液的溶质质量分数小于NaCl溶液的溶质质量分数,即质量分
2 3
数后者大;
②根据图示可知在t℃时,NaCO 的溶解度为49 g,因此将5 gNa CO 加入10 g水中,能
3 2 3 2 3溶解的NaCO 的质量为4.9 g,因此形成的溶液的质量为14.9 g;硝酸铵溶于水吸收热量,
2 3
温度降低,碳酸钠的溶解度减小,因此饱和溶液中析出晶体,可观察到试管底部固体增加;
③氨盐水比食盐水更容易吸收二氧化碳的原因是:氨盐水显碱性,更容易吸收酸性气体二
氧化碳;
④“夏天晒盐,冬天捞碱”这句谚语的原理是:氯化钠的溶解度受温度的影响不大,碳酸
钠的溶解度受温度的影响较大,温度越高溶解度越大。夏天温度升高,水分蒸发,所以碳
酸钠不易析出,而氯化钠容易析出;冬天温度降低,碳酸钠溶解度减小,所以从溶液中析
出。
19.(1)
(2) nCH=CH 加聚反应
2 2
(3)正四面体
【解析】(1)
乙烯的结构式为 ;
(2)
反应⑤为乙烯在催化剂作用下反应生成高分子化合物E,故该反应为加聚反应,E为聚乙
烯,该反应的化学方程式为nCH=CH ;
2 2
(3)
乙烯与氢气在催化剂的作用下发生加成反应得到物质C,C为乙烷,乙烷的最简单同系物
为甲烷,其空间构型为正四面体。
20.(1) 明亮 黑烟 C H+3O 2CO+2HO 紫色高锰酸钾溶
2 4 2 2 2
液褪色
(2) 褪色 CH=CH +Br CH=CH +H
2 2 2 2 2 2
CHCH CH=CH +HO CHCHOH 原子或原子团
3 3 2 2 2 3 2
答案第8页,共2页(3) nCH=CH 加成反应 链节 聚
2 2
合度
(4)植物生产调节剂
【解析】略
21.(1)CH =CH +Br →CHBr—CHBr
2 2 2 2 2
(2) 酸性高锰酸钾溶液褪色 氧化还原反应
(3)D
(4) BC B
(5) nCH=CH 加聚反应
2 2
【分析】石蜡油裂化生成C H,根据实验装置图可知,A中产生的乙烯与B中的溴水发生
2 4
加成反应,使溴水褪色;在C中乙烯被高锰酸钾溶液氧化生成二氧化碳,溶液褪色,生成
的二气氧化碳在D中与澄清石灰水反应,石灰水变浑浊,装置最后多余的乙烯可以用排水
法收集,据此分析解答。
(1)
乙烯含有碳碳双键,能够与溴发生加成反应生成无色CHBr-CH Br,故B中溴水褪色,化
2 2
学反应方程式为:CH=CH +Br →CHBr-CH Br。
2 2 2 2 2
(2)
乙烯含有碳碳双键,能够被酸性高锰酸钾溶液氧化,故C装置中的现象是高锰酸钾溶液褪
色,反应类型为氧化还原反应。
(3)
乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应,生成碳酸钙
沉淀,D中装有澄清的石灰水,可根据D中的澄清石灰水变浑浊判断该资料是否真实。
(4)
A.甲烷、乙烯不溶于水,且常温下都不与水反应,不能用于除杂和鉴别;
B.乙烯含有碳碳双键,能与溴水发生加成反应生成1,2-二溴乙烷液体,使溴水褪色,甲烷
与溴水不反应,可用溴水除去甲烷中混有的乙烯,并且可用于鉴别甲烷、乙烯;
C.甲烷与酸性高锰酸钾溶液不反应,但是乙烯能够被酸性高锰酸钾溶液氧化生成二氧化
碳气体,高锰酸钾溶液褪色,可用于鉴别甲烷、乙烯,有新的杂质生成,不能用于除杂;D.甲烷、乙烯都不溶于氢氧化钠溶液,不能用来除杂和鉴别;
综上,检验甲烷和乙烯的方法是BC,除去甲烷中乙烯的方法是B。
(5)
乙烯发生加聚反应生成高分子材料聚乙烯,反应的化学方程式为nCH=CH
2 2
。
22. 酸性KMnO 溶液褪色 CH=CH +
4 2 2
Br →BrCH—CHBr 加成反应 B CD
2 2 2
【分析】装置A中给碎瓷片加强热,石蜡油蒸汽通过炽热的碎瓷片表面,分解产生乙烯等
物质,乙烯含有碳碳双键可以被酸性高锰酸钾,使装置B中的酸性高锰酸钾溶液褪色,乙
烯可以可以溴发生加成反应,使装置C中溴的四氯化碳溶液褪色。
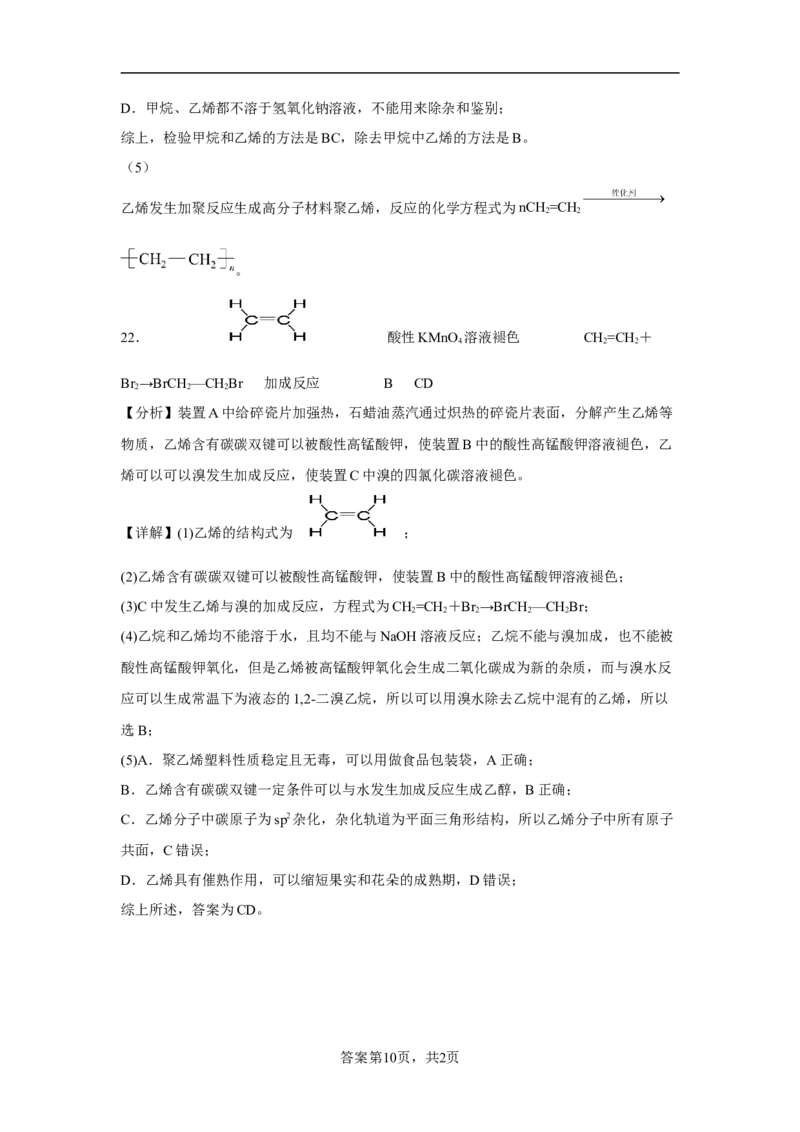
【详解】(1)乙烯的结构式为 ;
(2)乙烯含有碳碳双键可以被酸性高锰酸钾,使装置B中的酸性高锰酸钾溶液褪色;
(3)C中发生乙烯与溴的加成反应,方程式为CH=CH +Br →BrCH—CHBr;
2 2 2 2 2
(4)乙烷和乙烯均不能溶于水,且均不能与NaOH溶液反应;乙烷不能与溴加成,也不能被
酸性高锰酸钾氧化,但是乙烯被高锰酸钾氧化会生成二氧化碳成为新的杂质,而与溴水反
应可以生成常温下为液态的1,2-二溴乙烷,所以可以用溴水除去乙烷中混有的乙烯,所以
选B;
(5)A.聚乙烯塑料性质稳定且无毒,可以用做食品包装袋,A正确;
B.乙烯含有碳碳双键一定条件可以与水发生加成反应生成乙醇,B正确;
C.乙烯分子中碳原子为sp2杂化,杂化轨道为平面三角形结构,所以乙烯分子中所有原子
共面,C错误;
D.乙烯具有催熟作用,可以缩短果实和花朵的成熟期,D错误;
综上所述,答案为CD。
答案第10页,共2页