文档内容
高中化学人教版(2019)选择性必修1 第三章第三节 盐类的水解
一、单选题(共10题;共20分)
1.下列属于水解的离子方程式且书写正确的是( )
A. HCO -+HO HO++CO2- B. Fe3++3HO Fe(OH) ↓
3 2 3 3 2 3
+3H+
C. SO 2-+2HO HSO +2OH- D. CHCOO-+HO
3 2 2 3 3 2
CHCOOH+OH-
3
2.下列物质的水溶液因水解呈酸性的是( )
A. HCl B. NaHCO C. FeCl D. NaHSO。
3 3 4
3.下列说法正确的是( )
A. 中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同
B. 在醋酸钠溶液中再加入少量水,水解平衡正向移动
C. 用冰醋酸、蒸馏水和容量瓶可以配制pH=1的醋酸溶液
D. 室温下pH=12的Ba(OH) 溶液与pH=2的盐酸恰好中和,消耗二者体积比为1:2
2
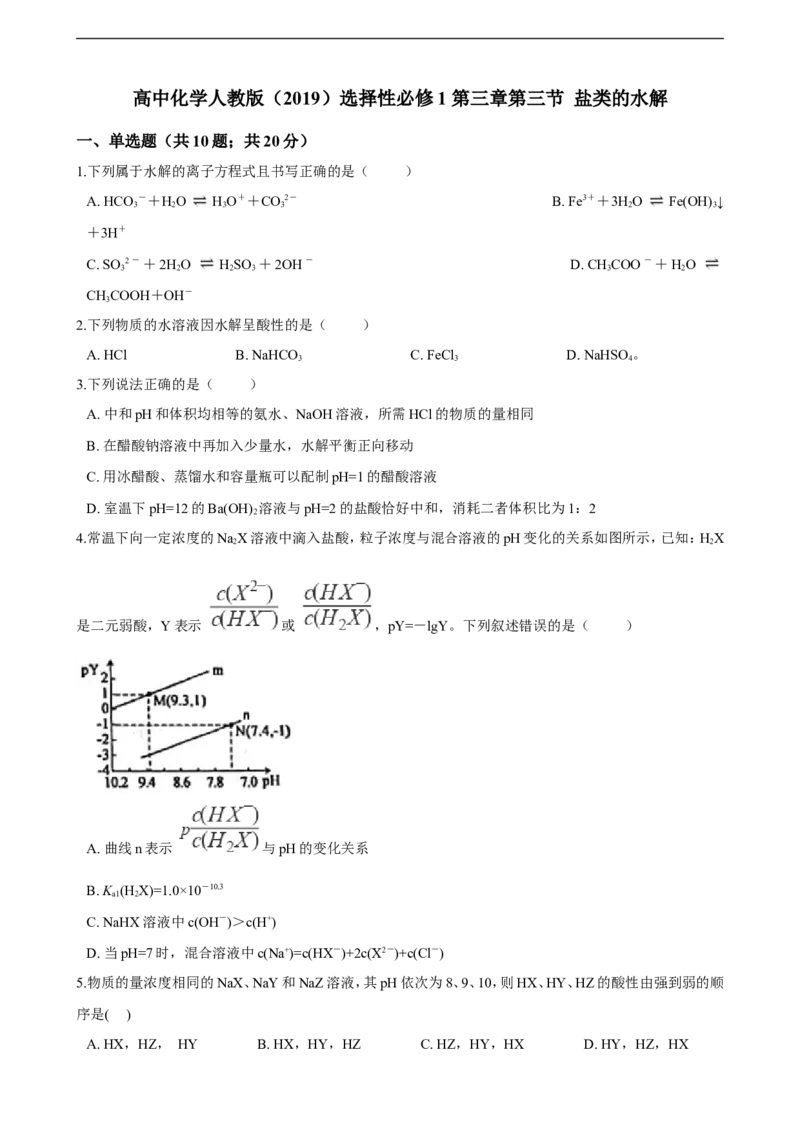
4.常温下向一定浓度的NaX溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示,已知:HX
2 2
是二元弱酸,Y表示 或 ,pY=-lgY。下列叙述错误的是( )
A. 曲线n表示 与pH的变化关系
B. K (H X)=1.0×10-10.3
a1 2
C. NaHX溶液中c(OH-)>c(H+)
D. 当pH=7时,混合溶液中c(Na+)=c(HX-)+2c(X2-)+c(Cl-)
21世纪教育网版权所有
5.物质的量浓度相同的NaX、NaY和NaZ溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺
序是( )
21·世纪*教育网
A. HX,HZ, HY B. HX,HY,HZ C. HZ,HY,HX D. HY,HZ,HX6.室温下,有两种溶液:①0.01mol•L﹣1 NH•H O 溶液、②0.01mol•L﹣1 NHCl 溶液,下列操作可以使两种溶
3 2 4
液中 c(NH +)都增大的是( )
4 www-2-1-cnjy-com
A. 通入少量 HCl 气体 B. 加入少量 NaOH 固体 C. 加
入少量 HO D. 适当升高温度
2
7.草酸(HC O )是二元弱酸,NaHC O 溶液呈酸性。常温下,向10mL 0.01mol/L NaHC O 溶液中滴加
2 2 4 2 4 2 4
0.01mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系错误的是( )
A. V(NaOH)=0时,c(H+)>1×10﹣7mol/L
B. V(NaOH)<10mL时,可能存在c(Na+)=2c(C O2﹣)+c(HC O﹣)
2 4 2 4
C. V(NaOH)=10mL时,溶液的pH为9,则 10﹣9=10﹣5﹣2c(HC O)﹣c(HC O﹣)
2 2 4 2 4
D. V(NaOH)>10mL时,可能存在c(OH﹣)>c(Na+)>c(C O2﹣)
2 4 【来源:21cnj*y.co*m】
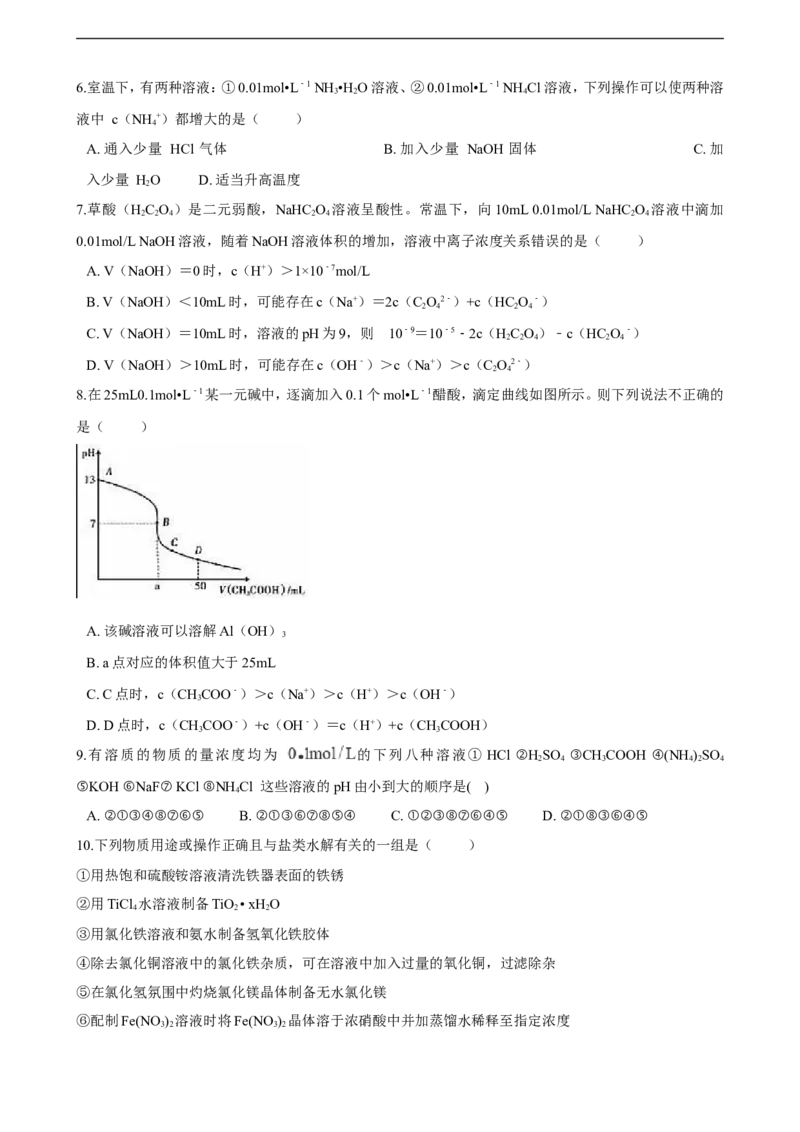
8.在25mL0.1mol•L﹣1某一元碱中,逐滴加入0.1个mol•L﹣1醋酸,滴定曲线如图所示。则下列说法不正确的
是( )
21*cnjy*com
A. 该碱溶液可以溶解Al(OH)
3
B. a点对应的体积值大于25mL
C. C点时,c(CHCOO﹣)>c(Na+)>c(H+)>c(OH﹣)
3
D. D点时,c(CHCOO﹣)+c(OH﹣)=c(H+)+c(CHCOOH)
3 3
9.有溶质的物质的量浓度均为 的下列八种溶液① HCl ②H SO ③CH COOH ④(NH )SO
2 4 3 4 2 4
⑤KOH ⑥NaF⑦ KCl ⑧NH Cl 这些溶液的pH由小到大的顺序是( )
4
A. ②①③④⑧⑦⑥⑤ B. ②①③⑥⑦⑧⑤④ C. ①②③⑧⑦⑥④⑤ D. ②①⑧③⑥④⑤
10.下列物质用途或操作正确且与盐类水解有关的一组是( )
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用TiCl 水溶液制备TiO • xHO
4 2 2
③用氯化铁溶液和氨水制备氢氧化铁胶体
④除去氯化铜溶液中的氯化铁杂质,可在溶液中加入过量的氧化铜,过滤除杂
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制Fe(NO ) 溶液时将Fe(NO ) 晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
3 2 3 2⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火
A. ①③⑥⑦⑧ B. ③④⑤⑦⑧ C. ①②④⑤⑧ D. ②③④⑤⑥
二、综合题(共5题;共23分)
11.溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)NaCO 溶液显碱性的原因,用离子反应方程式表示________;CuSO 溶液呈酸性的原因,用离子反应方
2 3 4
程式表示:________。
21教育网
(2)25 ℃时,pH为9的CHCOONa溶液中c(OH-)=________。
3
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c( )=c(Cl-),则
溶液显________(填“酸”“碱”或“中”)性。用含a的代数式表示NH ·H O的电离常数K=________。
3 2 b
12.醋酸、盐酸和碳酸钠是生活中常见的物质。
(1)碳酸钠水溶液显碱性的原因是(用离子方程式表示)________。
(2)25 ℃时,浓度均为 0.1 mol·L-1 的盐酸和醋酸溶液,下列说法正确是________。
a.两溶液的 pH 相同
b.两溶液的导电能力相同
c.两溶液中由水电离出的 c(OH-)相同
d.中和等物质的量的NaOH,消耗两溶液的体积相同
(3)25 ℃时, pH 均等于 4 的醋酸溶液和氯化铵溶液,醋酸溶液中水电离出的H+浓度与氯化铵溶液中水电
离出的H+浓度之比是________。
21教育名师原创作品
(4)醋酸溶液中存在电离平衡:CHCOOH CHCOO-+H- , 下列叙述错误的是________。
3 3
a. CHCOOH 溶液中离子浓度关系满足:c(H+)=c(OH-)+c(CHCOO-)
3 3
b. 0.1 mol·L-1的CHCOOH溶液加水稀释,溶液中 c(OHˉ)减小
3
c. CHCOOH 溶液中加入少量 CHCOONa 固体,平衡逆向移动
3 3
d. 常温下,pH=2 的 CHCOOH 溶液与 pH=12 的 NaOH 溶液等体积混合后溶液的 pH>7
3
e.室温下 pH=3 的醋酸溶液加水稀释,溶液中 不变
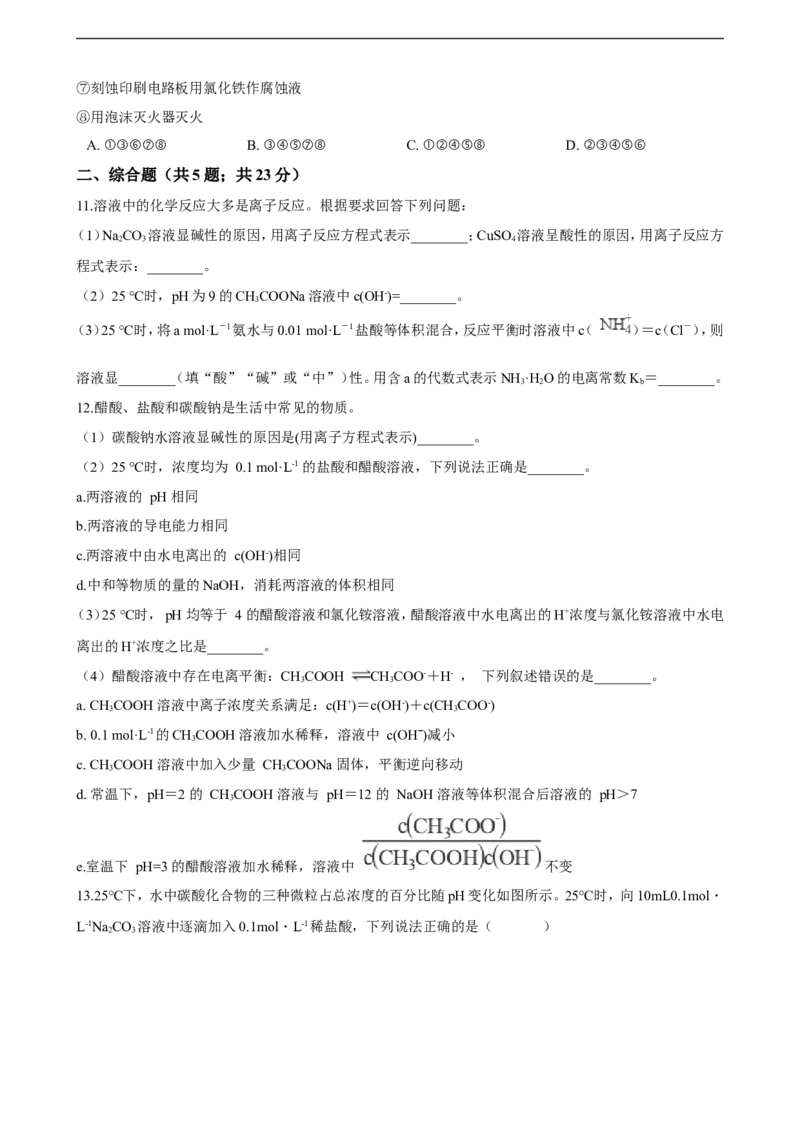
13.25℃下,水中碳酸化合物的三种微粒占总浓度的百分比随pH变化如图所示。25℃时,向10mL0.1mol・
L-1NaCO 溶液中逐滴加入0.1mol・L-1稀盐酸,下列说法正确的是( )
2 3A. 0.1mol・L-1NaCO 溶液中:c(Na+)+c(H+)=c(CO 2-)+c(HCO-)+c(OH-)
2 3 3 3
B. 溶液pH=8.3时,c(Na+)=c(Cl-)
C. 溶液pH=7时,加入盐酸体枳大于10mL
D. 溶液pH=6时的导电能力强于pH=11时的导电能力
14.
(1)25 ℃时,将体积V、pH=a的某一元强碱与体积为V、pH=b的某二元强酸混合。
a b
①若所得溶液的pH=11,且a=13,b=2,则V∶V=________。
a b
②为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg 。25 ℃时,
若溶液呈中性,则AG=________,溶液的pH与AG的换算公式为AG=________。
(2)常温下,浓度均为0.1mol•L-1的下列五种钠盐溶液的pH如下表:
溶质CHCOONaNaHCO NaCO NaClONaCN
3 3 2 3
pH 8.8 9.7 11.6 10.3 11.1
①上述盐溶液中的阴离子,结合H+能力最强的是________。
②根据表中数据,浓度均为0.01 mol•L-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是________
(填编号)。
www.21-cn-jy.com
A.HCN B.HClO C.CHCOOH D.HCO
3 2 3
(3)已知常温下,K [Fe(OH) ]=4.0×10-38 , 在FeCl 溶液中加入NaHCO 溶液产生沉淀和气体,反应的离子
sp 3 3 3
方程式为:________;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为________mol/L。
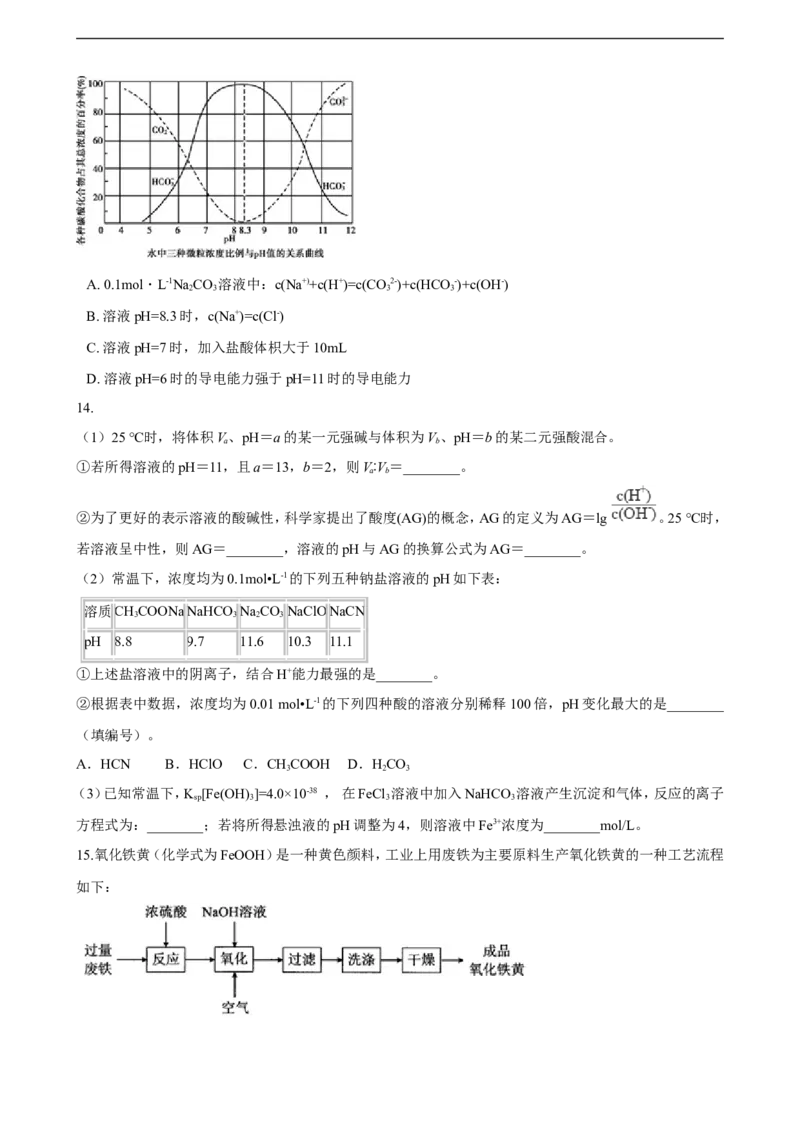
15.氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上用废铁为主要原料生产氧化铁黄的一种工艺流程
如下:
【出处:21教育名师】(1)氧化铁黄中铁元素的化合价为________,废铁在反应前常用热的纯碱溶液清洗表面油污,其原理是
________ (写离子方程式)。
21·cn·jy·com
(2)氧化过程生成氧化铁黄的化学方程式是________。
(3)上述流程中,检验“洗涤”是否完全的方法是________。
(4)氧化时应控制pH的合理范围是3.5-4.0,pH过小导致氧化铁黄产率较低的可能原因是________。答案解析部分
一、单选题
1. D
解析:A.HCO -水解生成HCO 和OH- , 该离子方程式不符合客观事实,A不符合题意;
3 2 3
B.Fe3+水解生成Fe(OH) 胶体,不生成Fe(OH) 沉淀,该离子方程式不符合客观事实,B不符合题意;
3 3
C.SO 2-的水解分步进行,水解产生HSO- , HSO -进一步水解产生HSO , 该离子方程式不符合客观
3 3 3 2 3
事实,C不符合题意;
21cnjy.com
D.CHCOO-水解产生CHCOOH和OH- , 该离子方程式正确,D符合题意;
3 3
故答案为:
此题是对水解离子方程式书写的考查,结合水解原理进行分析即可。
2. C
解析:A. HCl因电离呈酸性,A不符合题意;
B. NaHCO 是强碱弱酸盐,因水解程度大于电离程度呈碱性,B不符合题意;
3
C. FeCl 是强酸弱碱盐,因水解呈酸性,C符合题意;
3
D. NaHSO 因电离呈酸性,D不符合题意;
4
故答案为:C。
强酸弱碱盐,水解呈酸性
3. B
解析:A.一水合氨为弱电解质,pH相等时氨水浓度较大,分别中和 pH 相等、体积相等的两溶液,氨水消耗
盐酸的物质的量较多,故A不符合题意;
21*cnjy*com
B.在醋酸钠溶液中再加入少量水,醋酸钠溶液的浓度减小,水解程度增大,水解平衡正向移动,故B符合题
意;
【版权所有:21教育】
C.醋酸为弱酸,难以配制pH=1的溶液,且缺少量取(滴定管或移液管)或称取(分析天平)醋酸的仪器,故C
不符合题意;
D.室温下,pH=12的Ba(OH) 溶液中c(H+)=10-12mol/L,c(OH-)= =0.01mol/L,pH=2的盐酸两溶液中
2
c(H+)=10-2mol/L=0.01mol/L,二者OH-和H+浓度相同,恰好中和的体积之比应为 1:1,故D不符合题意;
故答案为:B。
A、要电离等量的氢氧根,氨水的量要比氢氧化钠多,故中和消耗的盐酸多
C、由于醋酸是弱酸,不能准确配制pH=1的醋酸D、消耗的体积之比为1:1
4. B
解析:A.根据分析可知,n表示pH与p 的变化关系,A选项不符合题意;
B.M点pH=9.3,c(H+)=10-9.3mol/L,p =-lg =1,则 =0.1,所以K (HX)= ×c
a2 2
(H+)=10-9.3×0.1=1.0×10-10.3 , N点pH=7.4,c(H+)=10-7.4mol/L,p =-lg =-1,则 =10,所
以K (H X)= ×c(H+)=10-7.4×10=1.0×10-6.4 , B选项符合题意;
a1 2
C.根据B可知HX﹣的电离平衡常数为1.0×10﹣10.3;曲线n表示pH与p 的变化关系,n点pH=7.4,p
=-lg =-1, =10,所以HX-的水解平衡常数K = =
h
=1.0×10-7.6>1.0×10-10.3 , 说明HX-的水解程度大于其电离程度,则NaHX溶液溶液呈碱性,c(H+)<c(OH-),
C选项不符合题意;
2-1-c-n-j-y
D.当溶液呈中性时,c(H+)=c(OH-),根据电荷守恒可知:c(Na+)=c(HX-)+2c(X2-)+c(Cl-),D选项不符合题意;
故答案为:B。
HX为二元弱酸,以第一步电离为主,则K (HX)>K (HX),则pH相同时 < ,pY=-
2 a1 2 a2 2
lgY,则p >p ,则m、n分别表示pH与p 、p 的变化关系,据此结合选项分析
解答。
2·1·c·n·j·y
5. B
解析:物质的量浓度相同的NaX、NaY和NaZ溶液,其pH依次为8、9、10,说明NaX、NaY和NaZ均为强碱
弱酸盐,根据盐类的水解是越弱越水解,根据其pH逐渐增大,所以盐的水解能力逐渐增强,则HX、HY、HZ的酸性越来越弱,由强到弱的顺序是HX>HY>HZ,B符合题意。
故答案为:B
盐类的水解是:有弱才水解,无弱不水解;越弱越水解,弱弱都水解;谁强显谁性,等弱显中性。强酸强碱盐
显中性,弱酸强碱盐显碱性,强酸弱碱盐显酸性,弱酸弱碱慢确定。
6. A
解析:两者的电离和水解如下:NH •H O NH ++OH-,NH ++H O NH •H O +H+
3 2 4 4 2 3 2
A. ①向0.01mol/LNH •H O溶液中通入少量HCl气体,氢氧根离子浓度减小,平衡右移,c(NH +)增大;②
3 2 4
向0.01mol/LNH Cl溶液中通入少量HCl气体,氢离子浓度增大,平衡左移,c(NH +)增大,A符合题意;
4 4
B.①向0.01mol/LNH •H O溶液中加入少量NaOH固体,氢氧根离子浓度增大,平衡左移,c(NH +)减小;②
3 2 4
向0.01mol/LNH Cl溶液中加入少量NaOH固体,氢离子浓度减小,平衡右移,c(NH +)减小,B不符合题意;
4 4
C.①向0.01mol/LNH •H O溶液中加入少量HO,NH •H O浓度降低,c(NH +)减小;②向0.01mol/LNH Cl
3 2 2 3 2 4 4
溶液中加入少量HO,NH Cl浓度减小,c(NH +)减小,C不符合题意;
2 4 4
D.①升高温度,促进NH •H O电离,平衡右移,c(NH +)增大;②升高温度,促进NH +水解,平衡右移,
3 2 4 4
c(NH +)减小,D不符合题意。
4
故答案为:A
A. 通入少量HCl气体,消耗氢氧根离子,平衡右移,c(NH +)增大;②通入少量HCl气体,氢离子浓度增大,
4
平衡左移,c(NH +)增大;
4
B.①少量NaOH固体,氢氧根离子浓度增大,平衡左移,c(NH +)减小;②加入少量NaOH固体,氢离子浓度
4
减小,平衡右移,c(NH +)减小;
4
C.加入水导致溶液浓度减小,各离子浓度均减小;
D.升高温度,会促进水解和电离。
7. D
解析:常温下,向 NaHC O 溶液中滴加 NaOH溶液,发生反应:NaHC O+NaOH= Na C O+H O;
2 4 2 4 2 2 4 2
A.V(NaOH) = 0时,溶液为NaHC O , NaHC O 溶液呈酸性,A不符合题意;
2 4 2 4
B.V(NaOH) < 10 mL时,溶质为NaHC O、NaC O , 可能存在c(Na+) =2 c(C O2-)+2 c(HC O-),B
2 4 2 2 4 2 4 2 4
不符合题意;
C.V(NaOH)> 10 mL时,溶质为NaC O、NaOH,溶液显碱性,在常温下,溶液c(H+)<1 × 10-7mol/L,C
2 2 4
不符合题意;
D.V(NaOH)> 10 mL时,溶质为NaC O、NaOH,c(Na+)> c(C O2-)>c(HC O-),D符合题意。
2 2 4 2 4 2 4
故答案为:D
A.溶质只有NaHC O , NaHC O 溶液呈酸性;
2 4 2 4B.V(NaOH) < 10 mL时,NaHC O 不能完全反应;
2 4
C.V(NaOH)> 10 mL时,NaOH过量,溶液显碱性;
D.V(NaOH)> 10 mL时,NaOH过量,溶液为碱性,钠离子来自于氢氧化钠,肯定要大于OH-。
8. D
解析:A.起始时0.1mol•L﹣1一元碱的PH=13,溶液中c(OH﹣)=0.1mol/L,说明一元碱为强碱,A(l OH)为
3
两性氢氧化物,能与强碱反应,故A不符合题意;
B.25mL0.1mol•L﹣1一元强碱和25mL0.1mol•L﹣1醋酸恰好反应时,溶液呈碱性,a点溶液呈中性,则酸过量,
所以醋酸的体积大于25ml,故B不符合题意;
C.C点溶液中c(H+)>c(OH﹣),电荷关系为c(CHCOO﹣)+c(OH﹣)=c(H+)+c(Na+),所以离子浓度大小
3
关系为c(CHCOO﹣)>c(Na+)>c(H+)>c(OH﹣),故C不符合题意;
3
D.D点为等量CHCOOH和CHCOONa的混合溶液,物料关系为c(CHCOO﹣)+c(CHCOOH)=2c
3 3 3 3
(Na+),电荷关系为c(CHCOO﹣)+c(OH﹣)=c(H+)+c(Na+),消去c(Na+)有c(CHCOO﹣)+2c(OH﹣)=2c
3 3
(H+)+c(CHCOOH),故D符合题意;
3
故答案为:D。
0.1mol/l某一元碱的pH=13,说明属于强碱,强碱溶液中滴加醋酸,生成的是强碱弱酸盐,结合盐类水解和
电荷守恒与物料守恒判断离子浓度大小关系即可。
9. A
解析:A.先将物质分类:pH最值大的应该是碱溶液KOH,pH小的是酸溶液HCl 、HSO 、CHCOOH,其中
2 4 3
最小的是HSO , 盐溶液中考虑(NH )SO 和NH Cl水解溶液呈酸性,NaF溶液呈碱性,故pH由小到大的
2 4 4 2 4 4
顺序HSO c(Cl-),B不符合题意;
C. 当加入盐酸体积为10mL时,碳酸钠与盐酸恰好反应生成碳酸氢钠和氯化钠,溶液显碱性,pH>7,若使溶
液pH=7,溶液中加入盐酸体枳大于10mL,C符合题意
D. 溶液中离子浓度越大,导电能力越强;离子所带电荷数越高,导电能力越强,根据图像可知,溶液pH=11
时的导电能力强于pH=6时的导电能力,D不符合题意;
故答案为:C。
A.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
B.溶液的pH=8.3,溶液中的溶质恰好为碳酸氢钠和氯化钠,根据物料守恒判断;
C.当加入10mL盐酸时,NaCO 恰好与盐酸完全反应生成碳酸氢钠和氯化钠,据此判断;
2 3
D.根据导电能力与离子浓度成正比判断。
14. (1)1∶ 9;0;-2pH+14
(2)CO2-;C
3
(3)Fe3++3HCO-=Fe(OH)↓+3CO ↑;4.0×10-8
3 3 2
解析:(1)①25 ℃时,K =10-14 , pH=a的某一元强碱,a=13,浓度为0.1mol/L,pH=b的某二元强酸,b=
w
2,浓度为0.01mol/L,所得溶液的pH=11,c(OH-)=0.001mol/L,则0.1mol/L×V-0.01mol/L×V=0.001mol/L×
a b
(V+V),化简求解V∶V=1∶9;②25 ℃时,若溶液呈中性,c(H+)=c(OH-),AG=lg1=0;AG=lg =lgc
a b a b
(H+)-lgc(OH-)=2lgc(H+)-lgK =-2pH+14;(2)①上述5种盐均为强碱弱酸盐,溶液显碱性,弱酸根离子越
w
弱,结合氢离子能力越强,碱性越强,根据表中数据,CO2-结合H+能力最强;②酸性越强,电离出的氢离子浓
3
度越大,加水稀释相同倍数时,pH变化越大,根据表中数据,CHCOOH酸性最强,答案为C;(3)FeCl 溶液
3 3
与NaHCO 溶液混合生成氢氧化铁沉淀和二氧化碳气体,反应的离子方程式为 Fe3++3HCO-=Fe(OH)
3 3
↓+3CO ↑;若将所得悬浊液的pH调整为4,溶液中c(H+)=10-4mol/L,则c(OH-)=K /c(H+)=10-10mol/L,
3 2 w
K [Fe(OH) ]=c(Fe3+)×c3(OH-)=4.0×10-38 , 则c(Fe3+)=4.0×10-38/10-30=4.0×10-8mol/L。
sp 3
(1)①酸碱中和反应后溶液显碱性时,利用c(OH-)=[n(OH-)-n(H+)]/(V+V)计算;②利用K =c(H+)×c
a b w
(OH-)进行计算;(2)①利用盐的水解规律,越弱越水解解释;②酸性越强,电离出的氢离子浓度越大,加水稀释相同倍数时,pH变化越大;(3)利用K 计算。
sp
15. (1)+3;CO2-+H O HCO -+OH-
3 2 3
(2)4FeSO +O +8NaOH= FeOOH↓+4Na SO +2H O
4 2 2 4 2
(3)取最后一次洗涤液,加入少量氯化钡溶液,后加入适量稀盐酸,如未观察到白色沉淀,即可证明洗干净
(4)pH过低导致氧化铁黄部分溶于酸
解析:(1)FeOOH中O元素为-2价,H元素为+1价,由化合价代数和为零可知Fe元素为+3价;废铁表面有
防锈的油脂,碳酸钠在溶液中水解使溶液呈碱性,加热溶液碱性增强,油脂会在碳酸钠溶液中发生水解反应,
达到清洗表面油污的目的,碳酸钠在溶液中水解的离子方程式为CO2-+H O HCO -+OH- , 故答案为:
3 2 3
+3;CO2-+H O HCO -+OH-;
3 2 3
( 2)氧化过程为向硫酸亚铁溶液中加入氢氧化钠溶液,并通入空气,发生氧化还原反应生成氧化铁黄,反应
的化学方程式为 4FeSO +O +8NaOH=FeOOH↓+4Na SO +2H O,故答案为:4FeSO +O +8NaOH=
4 2 2 4 2 4 2
FeOOH↓+4Na SO +2H O;
2 4 2
(3)由氧化过程的化学方程式可知,氧化铁黄表面附有可溶的硫酸钠,检查洗涤是否完全的标准是洗涤液
中不含有硫酸根离子,则检验洗涤是否完全的方法是,取少量最后一次的洗涤液于试管中,向其中滴加盐酸
酸化的氯化钡溶液,若不产生沉淀,则表明已洗涤干净,否则未洗涤干净,故答案为:取最后一次洗涤液,加
入少量氯化钡溶液,后加入适量稀盐酸,如未观察到白色沉淀,即可证明洗干净;
( 4)氧化时应控制pH的合理范围是保证产率最高,此时的pH范围为:3.5~4.0,若pH过小,氧化铁黄会溶
解于酸导致产率降低,故答案为:pH过低导致氧化铁黄部分溶于酸。
( 1)结合化合物物中化合价代数和为0计算铁元素的化合价;纯碱溶液中存在CO2-的水解,使得溶液显碱
3
性,可去除油污;
(2)根据流程确定反应物和生成物,结合原子个数守恒书写反应的化学方程式;
(3)洗涤过程中是为了除去可溶性的NaSO , 可结合SO 2-的检验分析;
2 4 4
(4)若pH过低,会导致FeOOH溶解;