文档内容
第1 页 共2 页
化学(一)参考答案
1~5 ABBAD 6~10 BCABD 11~14 CADC
1.A。解析:碳纳米管材料是一种纯净物,胶体既要有分散质又要有分散剂,所以A 不正确。
2.B。解析:苏打是Na2CO3,碱性较强,不能用于治疗胃酸过多,小苏打用于治疗胃酸过多。
3.B。解析:焰色试验、粗盐潮解、蒸发浓缩均是物理变化。
4.A。解析:原子半径:Mg>Si;Al 既能与酸反应,又能与强碱反应;Mn 是第四周期的元素。
5.D。解析:Pb2+→PbO2,铅元素化合价升高,被氧化,需要氧化剂。
6.B。解析:酸性溶液中,CH3COO
-不能大量共存;Cl
-与MnO
-
4 不能大量共存;HCO
-
3 与OH
-不能大量共存。
7.C。解析:NaCl 的电子式为
;Na
+的结构示意图为
;37Cl2 与35Cl2 均是单质。
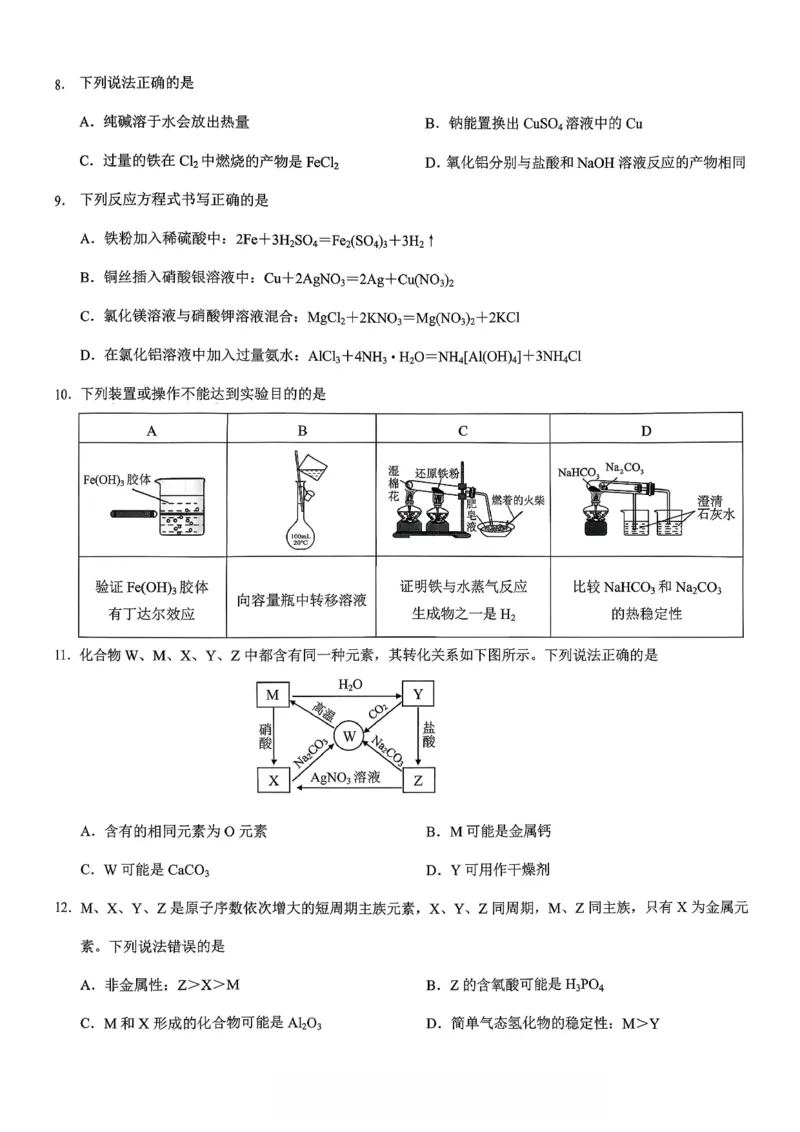
8.A。解析:钠放入CuSO4 溶液中,钠先与水反应;铁在Cl2 中燃烧,不管铁是否过量,产物都是FeCl3;氧化
铝与盐酸和NaOH 溶液反应的产物分别是AlCl3 和Na[Al(OH)4]。
9.B。解析:铁粉加入稀硫酸应生成FeSO4;氯化镁溶液与硝酸钾溶液不发生反应;氯化铝溶液中加入过量氨水
发生反应:AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl。
10.D。解析:D 选项,Na2CO3 与NaHCO3 的位置应交换。
11.C。解析:W、M、X、Y、Z 分别为CaCO3、CaO、Ca(NO3)2、Ca(OH)2、CaCl2。
12.A。解析:X、Y、Z 是第三周期元素,X 可能是Na、Mg、Al,A 选项,非金属性:M>Z>X。
13.D。解析:NaOH 没有漂白性;在溶液中通入Cl2 后加入KSCN 溶液变红,可能原溶液中含有Fe3+;Al(OH)3
不与氨水反应,但能与强碱反应。
14.C.解析:根据电荷守恒n(Fe3+) ×3+0.2×1=2×0.2×2+3×0.2×1,解得n(Fe3+)=0.4mol。
15.(14 分,除标注外每空2 分)
(1)Mg(1 分) S(1 分) Cl(1 分) CO2(1 分)
(2)F2>Cl2>S
(3)NH4NO3 HClO4
(4)Li2CO3+2H
+=2Li
++CO2↑+H2O
(5)
第2 页 共2 页
16.(15 分,除标注外每空2 分)
(1)+6(1 分) 第三周期ⅦA 族
(2)Cl2+2OH
-=Cl
-+ClO
-+H2O NaClO
取少量溶液于试管中,先滴入稀硝酸,再滴入AgNO3 溶液,有白色沉淀生成,则溶液中有Cl
-
(3)氧化性 4、10、4、3、8 33.6
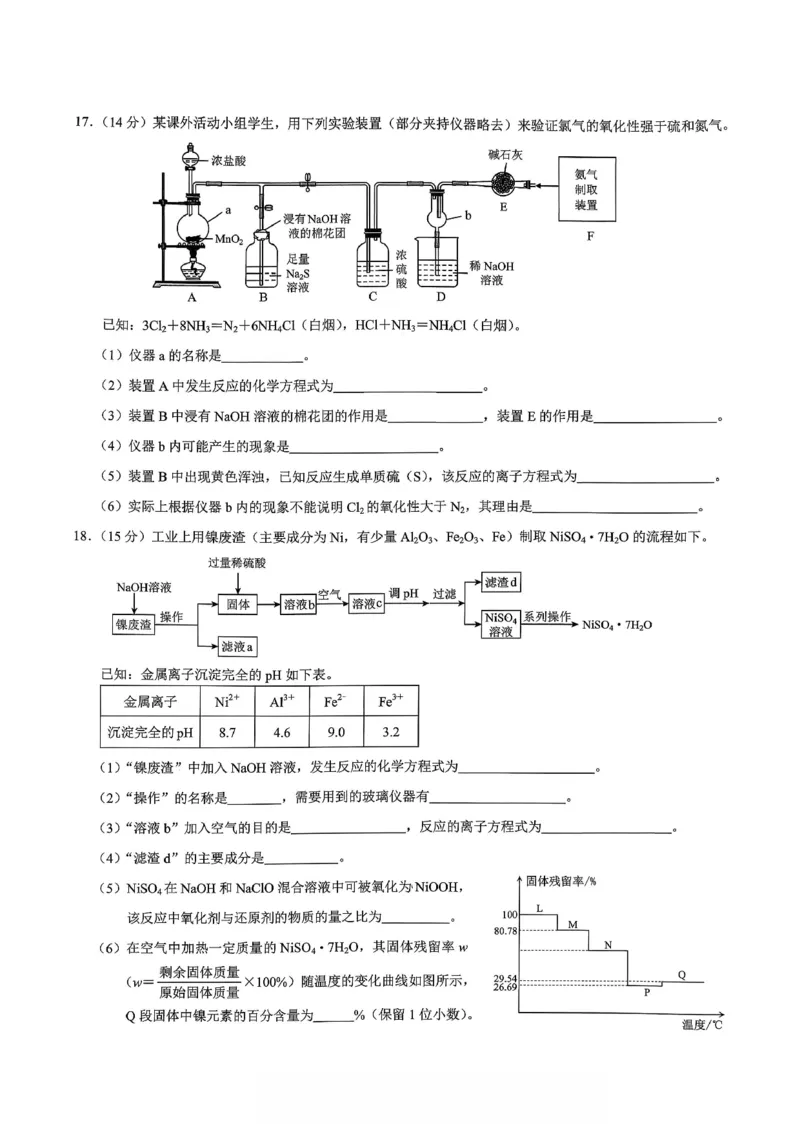
17.(14 分,每空2 分)
(1)圆底烧瓶
(2)MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
(3)吸收Cl2,防止污染空气 干燥NH3
(4)产生大量白烟
(5)S2-+Cl2=S↓+2Cl
-
(6)在装置C 前没有连接盛饱和食盐水的洗气瓶,进入装置D 的气体中有HCl,与NH3 反应也会产生白烟
18.(15 分,除标注外每空2 分)
(1)Al2O3+2NaOH+3H2O=2Na[Al(OH)4]
(2)过滤(1 分) 烧杯、玻璃棒、漏斗
(3)将Fe2+氧化成Fe3+ 4Fe2++O2+4H
+=4Fe3++2H2O
(4)Fe(OH)3
(5)1∶2
(6)71.1